2024年中考科学重点题型突破练习--推断题(框架类)(含解析)
文档属性
| 名称 | 2024年中考科学重点题型突破练习--推断题(框架类)(含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 373.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-04-30 00:00:00 | ||
图片预览


文档简介
2024年中考科学重点题型突破练习--推断题(框架类)
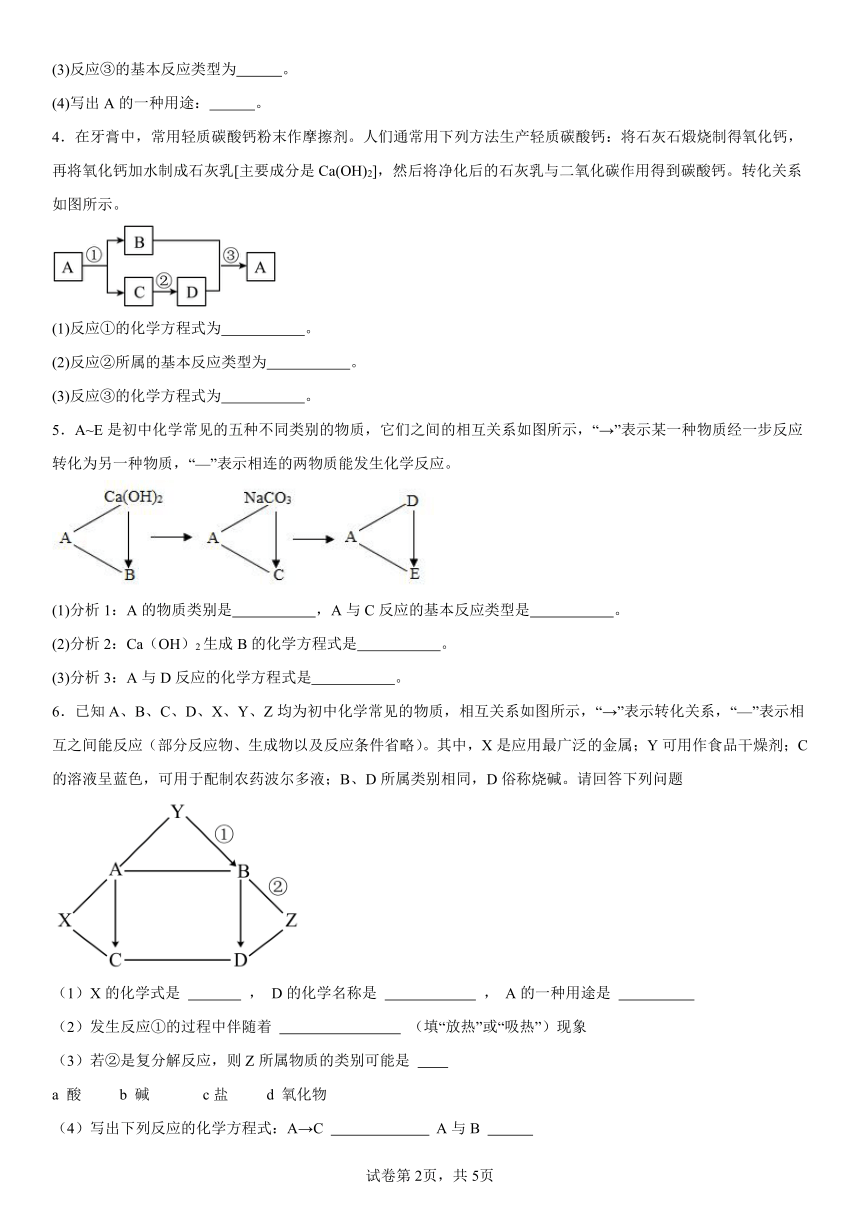
1.如图所示,A一F是初中化学常见的物质,A、D为两种黑色粉末,D与E反应后的生成物可用于配制波尔多液,C、E、F均含有三种元素,且分别为酸碱盐中的一种,E、F两种溶液反应有明显的实验现象。用两圆间的短线“-”表示两种物质以发生化学反应,箭头“→”表示一种物质能转化为另一种物质。请回答下列问题:(以上反应均在初中范围内)
(1)请写出下列物质的化学式:C ;F 。
(2)写出D和E发生反应的化学方程式 。
(3)写出A转化为B反应的实验现象 。
2.甲、乙、丙是中学化学的常见物质,已知甲为单质,乙、丙的组成元素完全相同,它们的转化关系如图所示(“→”表示反应可一步实现,部分物质和反应条件已略去)。
(1)若它们都含有形成化合物种类最多的元素,乙可以用于灭火。则甲为 ;乙和丙的性质有很大不同,从微观角度解释其原因是 。
(2)若它们都含有地壳中含量居第二位的金属元素,甲与氯气化合生成乙,且乙中金属元素显+3价。则乙的化学式为 ;甲转化为丙的化学方程式为: 。
3.已知A~I均为初中化学常见的物质,其中组成A、C两种气体的元素相同,且C是常见的温室气体,B是铁锈的主要成分,F是盐酸盐,它们之间的转化关系如图所示(反应条件已略去)。
回答下列问题:
(1)C的化学式为 。
(2)反应②的化学方程式为 。
(3)反应③的基本反应类型为 。
(4)写出A的一种用途: 。
4.在牙膏中,常用轻质碳酸钙粉末作摩擦剂。人们通常用下列方法生产轻质碳酸钙:将石灰石煅烧制得氧化钙,再将氧化钙加水制成石灰乳[主要成分是Ca(OH)2],然后将净化后的石灰乳与二氧化碳作用得到碳酸钙。转化关系如图所示。
(1)反应①的化学方程式为 。
(2)反应②所属的基本反应类型为 。
(3)反应③的化学方程式为 。
5.A~E是初中化学常见的五种不同类别的物质,它们之间的相互关系如图所示,“→”表示某一种物质经一步反应转化为另一种物质,“—”表示相连的两物质能发生化学反应。
(1)分析1:A的物质类别是 ,A与C反应的基本反应类型是 。
(2)分析2:Ca(OH)2生成B的化学方程式是 。
(3)分析3:A与D反应的化学方程式是 。
6.已知A、B、C、D、X、Y、Z均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“—”表示相互之间能反应(部分反应物、生成物以及反应条件省略)。其中,X是应用最广泛的金属;Y可用作食品干燥剂;C的溶液呈蓝色,可用于配制农药波尔多液;B、D所属类别相同,D俗称烧碱。请回答下列问题
(1)X的化学式是 , D的化学名称是 , A的一种用途是
(2)发生反应①的过程中伴随着 (填“放热”或“吸热”)现象
(3)若②是复分解反应,则Z所属物质的类别可能是
a 酸 b 碱 c盐 d 氧化物
(4)写出下列反应的化学方程式:A→C A与B
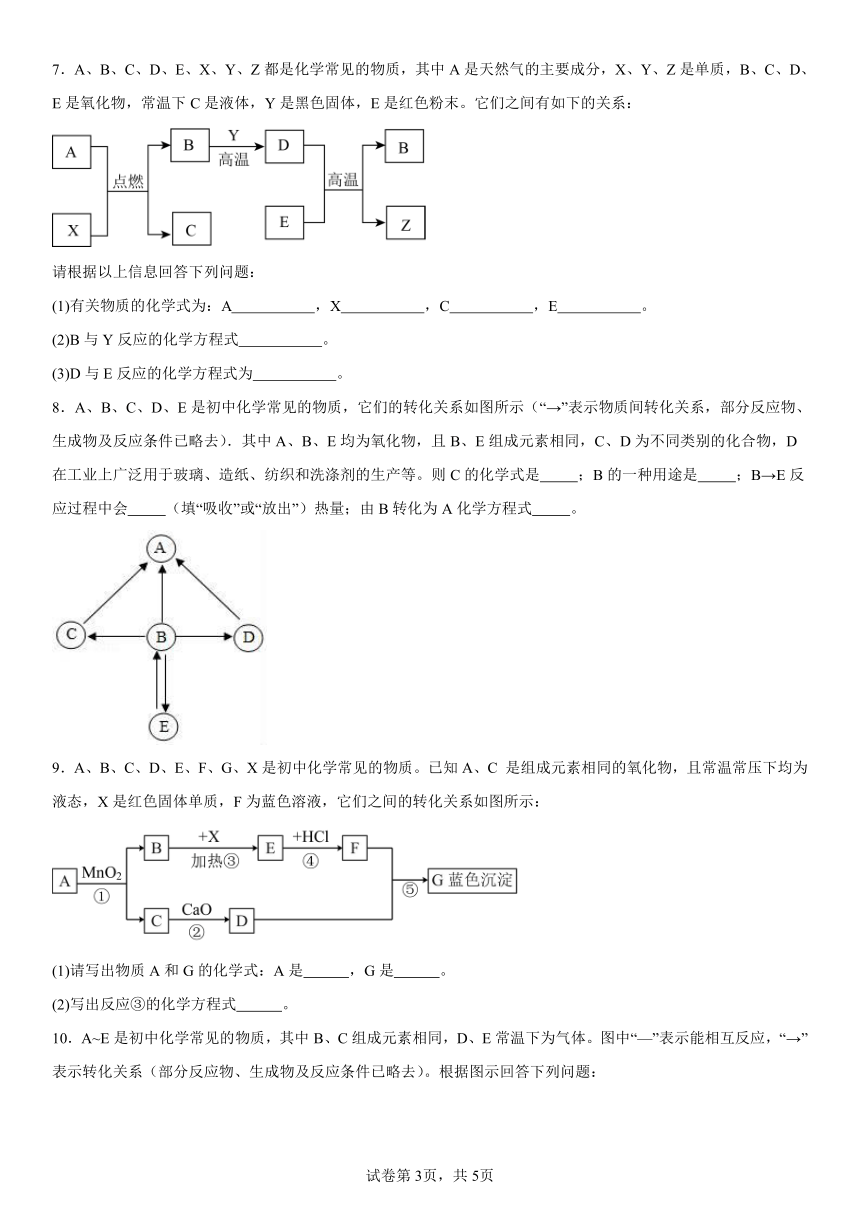
7.A、B、C、D、E、X、Y、Z都是化学常见的物质,其中A是天然气的主要成分,X、Y、Z是单质,B、C、D、E是氧化物,常温下C是液体,Y是黑色固体,E是红色粉末。它们之间有如下的关系:
请根据以上信息回答下列问题:
(1)有关物质的化学式为:A ,X ,C ,E 。
(2)B与Y反应的化学方程式 。
(3)D与E反应的化学方程式为 。
8.A、B、C、D、E是初中化学常见的物质,它们的转化关系如图所示(“→”表示物质间转化关系,部分反应物、生成物及反应条件已略去).其中A、B、E均为氧化物,且B、E组成元素相同,C、D为不同类别的化合物,D在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等。则C的化学式是 ;B的一种用途是 ;B→E反应过程中会 (填“吸收”或“放出”)热量;由B转化为A化学方程式 。
9.A、B、C、D、E、F、G、X是初中化学常见的物质。已知A、C 是组成元素相同的氧化物,且常温常压下均为液态,X是红色固体单质,F为蓝色溶液,它们之间的转化关系如图所示:
(1)请写出物质A和G的化学式:A是 ,G是 。
(2)写出反应③的化学方程式 。
10.A~E是初中化学常见的物质,其中B、C组成元素相同,D、E常温下为气体。图中“—”表示能相互反应,“→”表示转化关系(部分反应物、生成物及反应条件已略去)。根据图示回答下列问题:
(1)D的化学式是 。
(2)写出图示中C→E的反应方程式: 。
11.A、B、C、D、E是九年级化学中常见的五种物质。已知C是人体胃液中可以帮助消化的物质,D是大理石的主要成分,其相互反应及转化关系如图所示,“一”表示相连的两物质之间能发生反应,“→”表示一种物质能转化为另一种物,部分反应条件、反应物、生成物已略去。
(1)写出下列反应的化学方程式。
B与E的反应: 该反应是 (填“吸热”或“放热”)反应。B转化为A的反应: 。
(2)写出E物质的一种用途 。
12.已知A、B、C、D分别是氧化铁、稀盐酸、氢氧化钠溶液、硫酸铜溶液是四种物质中的一种,它们以及Fe之间相互反应情况如图所示,“—”连接的两物质能反应。已知B+Fe→无色气体,Cu(OH)2是沉淀。请回答下列问题:
(1)B、D物质中的溶质分别是 、 (填化学式);
(2)写出B和C反应的化学方程式 ;
(3)写出A和D反应的化学方程式 。
13.A、B、 C、D是初中化学常见的四种不同类别的化合物,其中有一种物质中含有人体中含量最多的金属元素,C和D反应时能生成厨房中常用的一种调味品的主要成分。它们之间的反应和转化关系如图所示(“一”表示两物质能发生化学反应,“→”表示一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。回答下列问题。
(1) B物质的名称 。
(2)写出A和D反应的化学方程式 。
(3)写出A和C的化学方程式 。
(4)写出A物质的一种用途 。
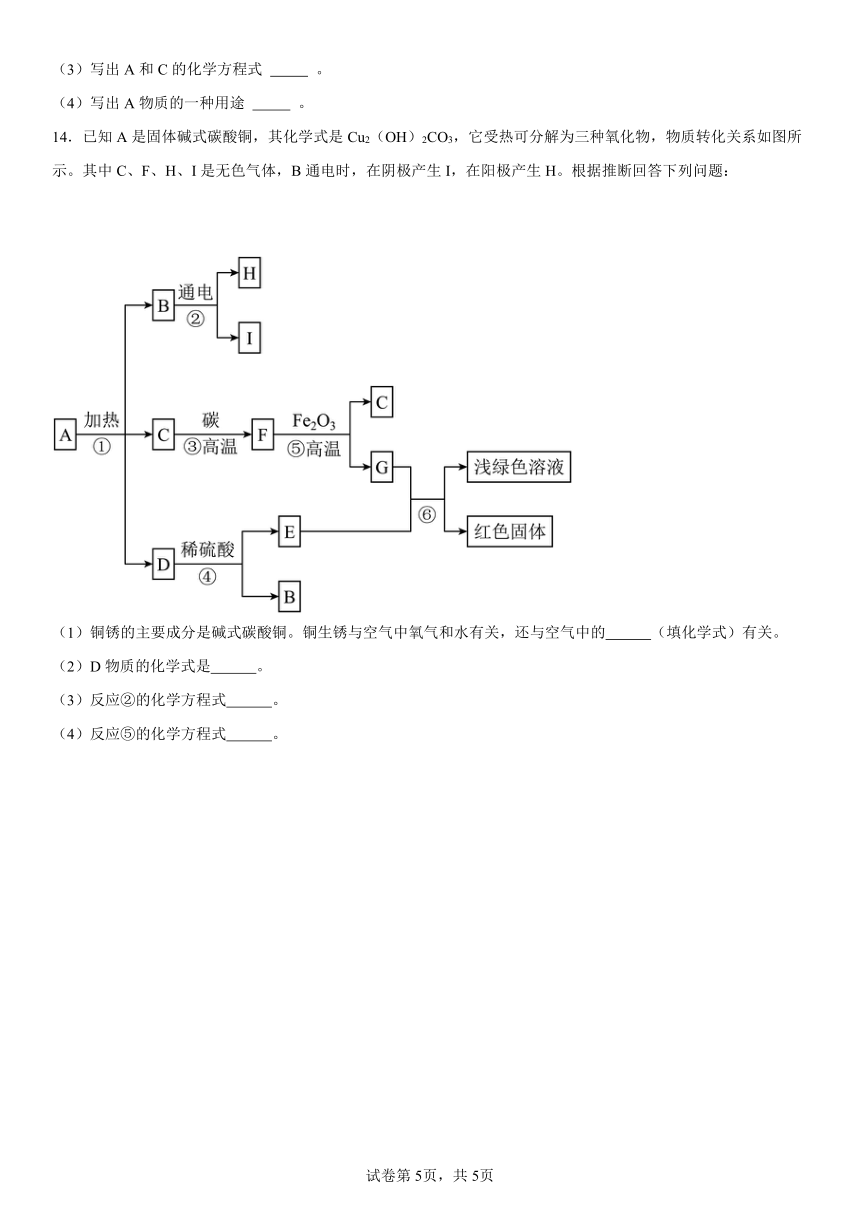
14.已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,它受热可分解为三种氧化物,物质转化关系如图所示。其中C、F、H、I是无色气体,B通电时,在阴极产生I,在阳极产生H。根据推断回答下列问题:
(1)铜锈的主要成分是碱式碳酸铜。铜生锈与空气中氧气和水有关,还与空气中的 (填化学式)有关。
(2)D物质的化学式是 。
(3)反应②的化学方程式 。
(4)反应⑤的化学方程式 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.(1) Cu(NO3)2 Ba(OH)2
(2)
(3)黑色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色
【分析】D为黑色粉末,D与E反应后的生成物可用于配制波尔多液,则D为氧化铜,E为硫酸;A为黑色粉末,能够反应生成B,B能够与D(氧化铜)相互转化,则A为铁,B为铜;C含有三种元素,能够与A(铁)反应,能够与B(铜)相互转化,能够与D(氧化铜)反应生成,则C为硝酸铜;C、E、F均含有三种元素,且分别为酸碱盐中的一种,F能够与E(硫酸)反应,还能够与C(硝酸铜)反应,且E、F两种溶液反应有明显的实验现象,则F为氢氧化钡等。
【详解】(1)由分析可知,C为硝酸铜,其化学式为Cu(NO3)2,故填Cu(NO3)2;
F为氢氧化钡,其化学式为Ba(OH)2,故填Ba(OH)2。
(2)由分析可知,D为氧化铜,E为硫酸,则D和E发生的反应是氧化铜与硫酸反应生成硫酸铜和水,故反应的化学方程式写为:CuO+H2SO4=CuSO4+H2O。
(3)由分析可知,A为铁,B为铜,则A转化为B的反应可以说铁与硫酸铜反应生成硫酸亚铁和铜,观察到的实验现象是黑色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色,故填黑色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色。
2.(1) 碳/C 它们的分子构成不同
(2) FeCl3 Fe+2HC1=FeCl2+H2↑(合理即可)
【详解】(1)形成化合物种类最多的元素为碳元素,甲为单质,乙、丙的组成元素完全相同,且乙可以灭火,则说明甲为碳单质,乙为二氧化碳,丙为一氧化碳。一氧化碳和二氧化碳虽然组成元素相同,但由于它们的分子构成不同,则它们的性质不同。
(2)地壳中含量居第二位的金属元素为铁元素,甲为单质,则甲为铁单质,甲能与氯气化合生成乙,且乙中铁元素显+3价,则乙为FeCl3,又由于乙、丙的组成元素完全相同,则丙为FeCl2,则甲转化为丙的反应为铁转化为FeCl2,铁能与盐酸反应生成氯化亚铁和氢气,或铁能与氯化铜反应生成铜和氯化亚铁,则反应的化学方程式为或。
3.(1)CO2
(2)Fe2O3+6HCl=2FeCl3+3H2O
(3)分解反应
(4)作燃料(合理即可)
【分析】A、C两种气体的组成元素相同,推测是二氧化碳和一氧化碳,且C是常见的温室气体,C是二氧化碳,A是一氧化碳;B是铁锈的主要成分,B是氧化铁;氧化铁和一氧化碳反应会生成铁和二氧化碳,D是铁;F是盐酸盐,说明E是盐酸,与氧化铁反应生成氯化铁和水,谁可以分解产生氢气和氧气,氧气能转化为氧化铁和二氧化碳,说明H是氧气,I是氢气;
综上分析:A是一氧化碳,B是氧化铁,C是二氧化碳,D是铁,E是稀盐酸,F是氯化铁,G是水,H是氧气,I是氢气。
【详解】(1)C是二氧化碳,故填:CO2;
(2)反应②是氧化铁和稀盐酸反应生成氯化铁和水,故填:Fe2O3+6HCl=2FeCl3+3H2O;
(3)反应③是水分解产生氢气和氧气,属于分解反应,故填:分解反应;
(4)A是一氧化碳,可以冶炼金属或作燃料,故填:作燃料(合理即可)。
4.(1)
(2)化合反应
(3)
【分析】根据题意结合框图可知,A是碳酸钙,C是氧化钙,D是氢氧化钙,B是二氧化碳。将答案代入框图,经检验正确无误。
【详解】(1)A是碳酸钙,B是二氧化碳,C是氧化钙。碳酸钙高温分解生成氧化钙和二氧化碳,所以反应①的化学方程式为。
故填:。
(2)C是氧化钙,D是氢氧化钙。C生成D,即氧化钙与水反应生成氢氧化钙。该反应符合化合反应多变一的特征,所以反应②所属的基本反应类型为化合反应。
故填:化合反应。
(3)D是氢氧化钙,B是二氧化碳。反应③是B和D反应生成A,即二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,化学方程式。故填:。
5.(1) 酸 复分解反应
(2)(合理即可)
(3)(合理即可)
【分析】A~E是初中化学常见的五种不同类别的物质,氢氧化钙转化成的B会与A反应,所以A是酸,可以是HCl,B是碱,可以是NaOH;Na2CO3转化成的C会与HCl反应,所以C是盐,可以是CaCO3;D会转化成E,HCl会与D、E反应,所以D是金属氧化物,E是金属单质,D可以是Fe2O3,E可以是Fe,然后将推出的物质验证即可。
【详解】(1)由分析可知,A的物质类别是酸;C是盐,A与C反应是酸和盐相互交换成分反应生成新酸和新盐,属于复分解反应;
(2)B是碱,可通过碱和盐反应生成新碱和新盐获得B,故Ca(OH)2生成B化学方程式可以是,合理即可;
(3)由分析可知,A是酸,D是金属氧化物,可以是盐酸和氧化铁反应生成氯化铁和水,反应的化学方程式是,合理即可。
6. Fe 氢氧化钠 除锈 放热 ac H2SO4+CuO=CuSO4+H2O H2SO4+Ca(OH)2=CaSO4+2H2O
【分析】根据A、B、C、D、X、Y、Z均为初中化学常见的物质,X是应用最广泛的金属,所以X是铁,Y可用作食品干燥剂,所以Y是氧化钙,C的溶液呈蓝色,可用于配制农药波尔多液,所以C是硫酸铜,D俗称烧碱,所以D是氢氧化钠,铁会与A反应,A会转化成硫酸铜,所以A是硫酸,氧化钙会转化成B,B、D所属物质类别相同,所以B是氢氧化钙,Z会与氢氧化钙、氢氧化钠反应,所以Z可能是盐酸或硝酸等酸类物质,也可能是氯化镁、氯化铜等盐类物质,还可以是二氧化碳等非金属氧化物,将推出的物质进行验证合理。
【详解】(1)根据推导,X是Fe,D是NaOH,俗称烧碱,A为硫酸,可用于除锈;
(2)反应①是氧化钙和水反应生成氢氧化钙,属于放热反应;
(3)若②是复分解反应,则反应②可以是盐酸等酸和氢氧化钙反应生成盐和水,则Z是酸,也可以是氯化镁、氯化铜等盐和氢氧化钙反应生成氢氧化物沉淀和相应的盐,则Z是盐,但Z不可以是非金属氧化物,因为非金属氧化物和碱的反应不属于复分解反应,故选ac;
(4)A→C的反应是稀硫酸和氧化铜反应生成硫酸铜和水,化学方程式为:H2SO4+CuO=CuSO4+H2O,也可以是硫酸和氢氧化铜反应,合理即可;A与B是硫酸和氢氧化钙反应生成硫酸钙和水,化学方程式为:H2SO4+Ca(OH)2=CaSO4+2H2O。
7.(1) CH4 O2 H2O Fe2O3
(2)
(3)
【分析】A、B、C、D、E、X、Y、Z都是化学常见的物质,其中A是天然气的主要成分,则A为甲烷,甲烷和单质X点燃会生成氧化物B、C,根据常温下C是液体,甲烷和氧气点燃生成二氧化碳和水,所以X是氧气,C是水,B是二氧化碳,二氧化碳和黑色的固体单质Y反应生成气体D,二氧化碳和碳高温下反应生成一氧化碳,所以D是一氧化碳,Y就是木炭,一氧化碳和红棕色粉末E(氧化物)在高温的条件下生成Z(单质)和二氧化碳,一氧化碳高温下还原氧化铁生成铁和二氧化碳,所以E是氧化铁,Z是铁,代入验证,推论合理。
【详解】(1)A为甲烷,化学式为CH4;X为氧气,化学式为O2;C为水,化学式为H2O;E为氧化铁,化学式为Fe2O3;
(2)B与Y反应即为二氧化碳和碳高温下反应生成一氧化碳,化学方程式为:;
(3)D与E反应即为一氧化碳和氧化铁高温下反应生成铁和二氧化碳,化学方程式为:。
8. H2CO3 灭火 吸收 Ca(OH)2+CO2═CaCO3↓+H2O
【分析】A、B、C、D、E是初中化学常见的物质,A、B、E均为氧化物,且B、E组成元素相同,B、E能相互转化,二氧化碳与碳在高温条件下生成一氧化碳,一氧化碳在氧气中燃烧生成二氧化碳, B、E可能是二氧化碳、一氧化碳中的一种,C、D为不同类别的化合物,D在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等, D是碳酸钠,B会转化成碳酸钠,氢氧化钠与二氧化碳反应生成碳酸钠和水,B是二氧化碳,E是一氧化碳;碳酸钠会转化成氧化物A,二氧化碳能转化为A,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水A可能是水,二氧化碳也会转化成C,二氧化碳与水化合生成碳酸,C可能是碳酸,经过验证,推导正确。
【详解】根据以上分析可知:
(1)C是碳酸,化学式是H2CO3,B是二氧化碳,可用作灭火;
(2)B→E是二氧化碳与碳在高温的条件下生成一氧化碳,反应过程中会吸收热量;
(3)B→A的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O。
【点睛】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
9.(1) H2O2 Cu(OH)2
(2)
【分析】已知A、C 是组成元素相同的氧化物,且常温常压下均为液态,A能在二氧化锰的作用下转化为B和C,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,因此A是过氧化氢,B是氧气,C是水;氧化钙和水生成氢氧化钙,因此D是氢氧化钙;X是红色固体单质,F为蓝色溶液,铜和氧气在加热的条件下生成氧化铜,因此X是铜,E是氧化铜;氧化铜和硫酸反应生成硫酸铜和水,因此F是硫酸铜;硫酸铜和氢氧化钙反应生成氢氧化铜蓝色沉淀和硫酸钙,因此G是氢氧化铜,代入验证,符合题意。
【详解】(1)由分析可知,A为过氧化氢,化学式为:H2O2;G为氢氧化铜,化学式为:Cu(OH)2;
(2)反应③为铜与氧气在加热的条件下反应生成氧化铜,该反应的化学方程式为:。
10. H2
【分析】A~E是初中化学常见的物质,其中B、C组成元素相同,D、E常温下为气体,C能转化为B、E,B、E能相互转化,所以B是水,C是过氧化氢,E是氧气,B能与D相互转化,D能与E反应,可推出D是氢气,A能转化为B、D,可推出A是酸,代入验证,推理正确。
【详解】由分析可知(1)D是氢气,化学式是H2;
(2)C→E是过氧化氢在二氧化锰催化作用下生成水和氧气,反应的化学方程式为:。
11. 放热 2H2O2H2↑+O2↑ 做食品干燥剂
【分析】A、B、C、D、E是九年级化学中常见的五种物质,已知C是人体胃液中可以帮助消化的物质,所以C是盐酸,D是大理石的主要成分,所以D是碳酸钙,B通电会生成A,所以B是水,水会与E反应,E能与C(HCl)反应,所以E是氧化钙,盐酸也会转化成A,所以A是氢气,经过验证,推导正确。
【详解】由分析可知:
(1) B与E的反应是氧化钙和水反应生成氢氧化钙,反应的化学方程为,此反应放出热量;B转化为A的反应是水在通电的条件下生成氢气和氧气,化学方程式为:2H2O2H2↑+O2↑;
(2) E是氧化钙,可以做食品干燥剂等。
12. HCl CuSO4
【详解】A、B、C、D分别是氧化铁、稀盐酸、氢氧化钠溶液、硫酸铜溶液是四种物质中的一种,B+Fe→无色气体,则B是盐酸,氧化铁和氢氧化钠可以与盐酸发生反应,盐酸和硫酸铜可以与铁发生反应,故D是硫酸铜,A可以与硫酸铜和稀盐酸发生反应,又Cu(OH)2是沉淀,故A是氢氧化钠,C是氧化铁,综上A是氢氧化钠、B是稀盐酸、C是氧化铁、D是硫酸铜。
(1)B、D物质中的溶质分别是HCl、CuSO4;
(2)B和C反应,即稀盐酸与氧化铁反应生成氯化铁和水,化学方程式是;
(3)A和D反应,即氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式是。
13. 二氧化碳 改良酸性土壤(合理即可)
【分析】A、B、C、D是初中化学常见的四种不同类别的化合物,其中有一种物质中含有人体中含量最多的金属元素,则该元素为钙;C和D反应时能生成厨房中常用的一种调味品的主要成分,该调味品为氯化钠,则C、D为碳酸钠与稀盐酸,B与D可以相互转化,二氧化碳能与碳酸钠相互转化,所以B为二氧化碳,C为稀盐酸,D为碳酸钠,则A中含有钙元素,又A、B、 C、D是初中化学常见的四种不同类别的化合物,所以A为氢氧化钙。
【详解】(1)由分析可知,B为二氧化碳,故填二氧化碳。
(2)由分析可知,A为氢氧化钙,D为碳酸钠,氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故反应的化学方程式写为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。
(3)由分析可知,A为氢氧化钙,C为盐酸,氢氧化钙与盐酸反应生成氯化钙和水,故反应的化学方程式写为:Ca(OH)2+2HCl=CaCl2+2H2O。
(4)A为氢氧化钙,氢氧化钙可用于改良酸性土壤,配制波尔多液等,故填改良酸性土壤(合理即可)。
14. CO2 CuO
【详解】已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,可以将A视为Cu(OH)2+CuCO3,所以其受热会产生CuO、H2O、和CO2,B通电可以生成两种无色气体H和I,所以B为H2O,在阴极产生I,在阳极产生H,则I为H2,H为O2,C为无色气体,则C为CO2,所以D是CuO,CO2与碳高温下生产无色气体F:CO,然后CO高温还原Fe2O3生成CO2和Fe,则G为Fe,D:CuO与稀硫酸反应B:H2O和E:CuSO4,综上,A:Cu2(OH)2CO3、B:H2O、C:CO2、D:CuO、E:CuSO4、F: CO、G:Fe、H:O2、I: H2;
(1)、铜锈的主要成分是碱式碳酸铜,含有碳酸根,所以铜生锈还与空气中的CO2有关;
(2)、已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,可以将A视为Cu(OH)2+CuCO3,所以其受热会产生CuO、H2O、和CO2,而H2O、和CO2都不与稀硫酸反应,所以D为CuO;
(3)、反应②就是水被电解生成氢气和氧气,其化学方程式为: ;
(4)、反应⑤即一氧化碳高温下还原氧化铁生产二氧化碳和铁单质,其化学反应方程式为: 。
答案第1页,共2页
答案第1页,共2页
1.如图所示,A一F是初中化学常见的物质,A、D为两种黑色粉末,D与E反应后的生成物可用于配制波尔多液,C、E、F均含有三种元素,且分别为酸碱盐中的一种,E、F两种溶液反应有明显的实验现象。用两圆间的短线“-”表示两种物质以发生化学反应,箭头“→”表示一种物质能转化为另一种物质。请回答下列问题:(以上反应均在初中范围内)
(1)请写出下列物质的化学式:C ;F 。
(2)写出D和E发生反应的化学方程式 。
(3)写出A转化为B反应的实验现象 。
2.甲、乙、丙是中学化学的常见物质,已知甲为单质,乙、丙的组成元素完全相同,它们的转化关系如图所示(“→”表示反应可一步实现,部分物质和反应条件已略去)。
(1)若它们都含有形成化合物种类最多的元素,乙可以用于灭火。则甲为 ;乙和丙的性质有很大不同,从微观角度解释其原因是 。
(2)若它们都含有地壳中含量居第二位的金属元素,甲与氯气化合生成乙,且乙中金属元素显+3价。则乙的化学式为 ;甲转化为丙的化学方程式为: 。
3.已知A~I均为初中化学常见的物质,其中组成A、C两种气体的元素相同,且C是常见的温室气体,B是铁锈的主要成分,F是盐酸盐,它们之间的转化关系如图所示(反应条件已略去)。
回答下列问题:
(1)C的化学式为 。
(2)反应②的化学方程式为 。
(3)反应③的基本反应类型为 。
(4)写出A的一种用途: 。
4.在牙膏中,常用轻质碳酸钙粉末作摩擦剂。人们通常用下列方法生产轻质碳酸钙:将石灰石煅烧制得氧化钙,再将氧化钙加水制成石灰乳[主要成分是Ca(OH)2],然后将净化后的石灰乳与二氧化碳作用得到碳酸钙。转化关系如图所示。
(1)反应①的化学方程式为 。
(2)反应②所属的基本反应类型为 。
(3)反应③的化学方程式为 。
5.A~E是初中化学常见的五种不同类别的物质,它们之间的相互关系如图所示,“→”表示某一种物质经一步反应转化为另一种物质,“—”表示相连的两物质能发生化学反应。
(1)分析1:A的物质类别是 ,A与C反应的基本反应类型是 。
(2)分析2:Ca(OH)2生成B的化学方程式是 。
(3)分析3:A与D反应的化学方程式是 。
6.已知A、B、C、D、X、Y、Z均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“—”表示相互之间能反应(部分反应物、生成物以及反应条件省略)。其中,X是应用最广泛的金属;Y可用作食品干燥剂;C的溶液呈蓝色,可用于配制农药波尔多液;B、D所属类别相同,D俗称烧碱。请回答下列问题
(1)X的化学式是 , D的化学名称是 , A的一种用途是
(2)发生反应①的过程中伴随着 (填“放热”或“吸热”)现象
(3)若②是复分解反应,则Z所属物质的类别可能是
a 酸 b 碱 c盐 d 氧化物
(4)写出下列反应的化学方程式:A→C A与B
7.A、B、C、D、E、X、Y、Z都是化学常见的物质,其中A是天然气的主要成分,X、Y、Z是单质,B、C、D、E是氧化物,常温下C是液体,Y是黑色固体,E是红色粉末。它们之间有如下的关系:
请根据以上信息回答下列问题:
(1)有关物质的化学式为:A ,X ,C ,E 。
(2)B与Y反应的化学方程式 。
(3)D与E反应的化学方程式为 。
8.A、B、C、D、E是初中化学常见的物质,它们的转化关系如图所示(“→”表示物质间转化关系,部分反应物、生成物及反应条件已略去).其中A、B、E均为氧化物,且B、E组成元素相同,C、D为不同类别的化合物,D在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等。则C的化学式是 ;B的一种用途是 ;B→E反应过程中会 (填“吸收”或“放出”)热量;由B转化为A化学方程式 。
9.A、B、C、D、E、F、G、X是初中化学常见的物质。已知A、C 是组成元素相同的氧化物,且常温常压下均为液态,X是红色固体单质,F为蓝色溶液,它们之间的转化关系如图所示:
(1)请写出物质A和G的化学式:A是 ,G是 。
(2)写出反应③的化学方程式 。
10.A~E是初中化学常见的物质,其中B、C组成元素相同,D、E常温下为气体。图中“—”表示能相互反应,“→”表示转化关系(部分反应物、生成物及反应条件已略去)。根据图示回答下列问题:
(1)D的化学式是 。
(2)写出图示中C→E的反应方程式: 。
11.A、B、C、D、E是九年级化学中常见的五种物质。已知C是人体胃液中可以帮助消化的物质,D是大理石的主要成分,其相互反应及转化关系如图所示,“一”表示相连的两物质之间能发生反应,“→”表示一种物质能转化为另一种物,部分反应条件、反应物、生成物已略去。
(1)写出下列反应的化学方程式。
B与E的反应: 该反应是 (填“吸热”或“放热”)反应。B转化为A的反应: 。
(2)写出E物质的一种用途 。
12.已知A、B、C、D分别是氧化铁、稀盐酸、氢氧化钠溶液、硫酸铜溶液是四种物质中的一种,它们以及Fe之间相互反应情况如图所示,“—”连接的两物质能反应。已知B+Fe→无色气体,Cu(OH)2是沉淀。请回答下列问题:
(1)B、D物质中的溶质分别是 、 (填化学式);
(2)写出B和C反应的化学方程式 ;
(3)写出A和D反应的化学方程式 。
13.A、B、 C、D是初中化学常见的四种不同类别的化合物,其中有一种物质中含有人体中含量最多的金属元素,C和D反应时能生成厨房中常用的一种调味品的主要成分。它们之间的反应和转化关系如图所示(“一”表示两物质能发生化学反应,“→”表示一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。回答下列问题。
(1) B物质的名称 。
(2)写出A和D反应的化学方程式 。
(3)写出A和C的化学方程式 。
(4)写出A物质的一种用途 。
14.已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,它受热可分解为三种氧化物,物质转化关系如图所示。其中C、F、H、I是无色气体,B通电时,在阴极产生I,在阳极产生H。根据推断回答下列问题:
(1)铜锈的主要成分是碱式碳酸铜。铜生锈与空气中氧气和水有关,还与空气中的 (填化学式)有关。
(2)D物质的化学式是 。
(3)反应②的化学方程式 。
(4)反应⑤的化学方程式 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.(1) Cu(NO3)2 Ba(OH)2
(2)
(3)黑色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色
【分析】D为黑色粉末,D与E反应后的生成物可用于配制波尔多液,则D为氧化铜,E为硫酸;A为黑色粉末,能够反应生成B,B能够与D(氧化铜)相互转化,则A为铁,B为铜;C含有三种元素,能够与A(铁)反应,能够与B(铜)相互转化,能够与D(氧化铜)反应生成,则C为硝酸铜;C、E、F均含有三种元素,且分别为酸碱盐中的一种,F能够与E(硫酸)反应,还能够与C(硝酸铜)反应,且E、F两种溶液反应有明显的实验现象,则F为氢氧化钡等。
【详解】(1)由分析可知,C为硝酸铜,其化学式为Cu(NO3)2,故填Cu(NO3)2;
F为氢氧化钡,其化学式为Ba(OH)2,故填Ba(OH)2。
(2)由分析可知,D为氧化铜,E为硫酸,则D和E发生的反应是氧化铜与硫酸反应生成硫酸铜和水,故反应的化学方程式写为:CuO+H2SO4=CuSO4+H2O。
(3)由分析可知,A为铁,B为铜,则A转化为B的反应可以说铁与硫酸铜反应生成硫酸亚铁和铜,观察到的实验现象是黑色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色,故填黑色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色。
2.(1) 碳/C 它们的分子构成不同
(2) FeCl3 Fe+2HC1=FeCl2+H2↑(合理即可)
【详解】(1)形成化合物种类最多的元素为碳元素,甲为单质,乙、丙的组成元素完全相同,且乙可以灭火,则说明甲为碳单质,乙为二氧化碳,丙为一氧化碳。一氧化碳和二氧化碳虽然组成元素相同,但由于它们的分子构成不同,则它们的性质不同。
(2)地壳中含量居第二位的金属元素为铁元素,甲为单质,则甲为铁单质,甲能与氯气化合生成乙,且乙中铁元素显+3价,则乙为FeCl3,又由于乙、丙的组成元素完全相同,则丙为FeCl2,则甲转化为丙的反应为铁转化为FeCl2,铁能与盐酸反应生成氯化亚铁和氢气,或铁能与氯化铜反应生成铜和氯化亚铁,则反应的化学方程式为或。
3.(1)CO2
(2)Fe2O3+6HCl=2FeCl3+3H2O
(3)分解反应
(4)作燃料(合理即可)
【分析】A、C两种气体的组成元素相同,推测是二氧化碳和一氧化碳,且C是常见的温室气体,C是二氧化碳,A是一氧化碳;B是铁锈的主要成分,B是氧化铁;氧化铁和一氧化碳反应会生成铁和二氧化碳,D是铁;F是盐酸盐,说明E是盐酸,与氧化铁反应生成氯化铁和水,谁可以分解产生氢气和氧气,氧气能转化为氧化铁和二氧化碳,说明H是氧气,I是氢气;
综上分析:A是一氧化碳,B是氧化铁,C是二氧化碳,D是铁,E是稀盐酸,F是氯化铁,G是水,H是氧气,I是氢气。
【详解】(1)C是二氧化碳,故填:CO2;
(2)反应②是氧化铁和稀盐酸反应生成氯化铁和水,故填:Fe2O3+6HCl=2FeCl3+3H2O;
(3)反应③是水分解产生氢气和氧气,属于分解反应,故填:分解反应;
(4)A是一氧化碳,可以冶炼金属或作燃料,故填:作燃料(合理即可)。
4.(1)
(2)化合反应
(3)
【分析】根据题意结合框图可知,A是碳酸钙,C是氧化钙,D是氢氧化钙,B是二氧化碳。将答案代入框图,经检验正确无误。
【详解】(1)A是碳酸钙,B是二氧化碳,C是氧化钙。碳酸钙高温分解生成氧化钙和二氧化碳,所以反应①的化学方程式为。
故填:。
(2)C是氧化钙,D是氢氧化钙。C生成D,即氧化钙与水反应生成氢氧化钙。该反应符合化合反应多变一的特征,所以反应②所属的基本反应类型为化合反应。
故填:化合反应。
(3)D是氢氧化钙,B是二氧化碳。反应③是B和D反应生成A,即二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,化学方程式。故填:。
5.(1) 酸 复分解反应
(2)(合理即可)
(3)(合理即可)
【分析】A~E是初中化学常见的五种不同类别的物质,氢氧化钙转化成的B会与A反应,所以A是酸,可以是HCl,B是碱,可以是NaOH;Na2CO3转化成的C会与HCl反应,所以C是盐,可以是CaCO3;D会转化成E,HCl会与D、E反应,所以D是金属氧化物,E是金属单质,D可以是Fe2O3,E可以是Fe,然后将推出的物质验证即可。
【详解】(1)由分析可知,A的物质类别是酸;C是盐,A与C反应是酸和盐相互交换成分反应生成新酸和新盐,属于复分解反应;
(2)B是碱,可通过碱和盐反应生成新碱和新盐获得B,故Ca(OH)2生成B化学方程式可以是,合理即可;
(3)由分析可知,A是酸,D是金属氧化物,可以是盐酸和氧化铁反应生成氯化铁和水,反应的化学方程式是,合理即可。
6. Fe 氢氧化钠 除锈 放热 ac H2SO4+CuO=CuSO4+H2O H2SO4+Ca(OH)2=CaSO4+2H2O
【分析】根据A、B、C、D、X、Y、Z均为初中化学常见的物质,X是应用最广泛的金属,所以X是铁,Y可用作食品干燥剂,所以Y是氧化钙,C的溶液呈蓝色,可用于配制农药波尔多液,所以C是硫酸铜,D俗称烧碱,所以D是氢氧化钠,铁会与A反应,A会转化成硫酸铜,所以A是硫酸,氧化钙会转化成B,B、D所属物质类别相同,所以B是氢氧化钙,Z会与氢氧化钙、氢氧化钠反应,所以Z可能是盐酸或硝酸等酸类物质,也可能是氯化镁、氯化铜等盐类物质,还可以是二氧化碳等非金属氧化物,将推出的物质进行验证合理。
【详解】(1)根据推导,X是Fe,D是NaOH,俗称烧碱,A为硫酸,可用于除锈;
(2)反应①是氧化钙和水反应生成氢氧化钙,属于放热反应;
(3)若②是复分解反应,则反应②可以是盐酸等酸和氢氧化钙反应生成盐和水,则Z是酸,也可以是氯化镁、氯化铜等盐和氢氧化钙反应生成氢氧化物沉淀和相应的盐,则Z是盐,但Z不可以是非金属氧化物,因为非金属氧化物和碱的反应不属于复分解反应,故选ac;
(4)A→C的反应是稀硫酸和氧化铜反应生成硫酸铜和水,化学方程式为:H2SO4+CuO=CuSO4+H2O,也可以是硫酸和氢氧化铜反应,合理即可;A与B是硫酸和氢氧化钙反应生成硫酸钙和水,化学方程式为:H2SO4+Ca(OH)2=CaSO4+2H2O。
7.(1) CH4 O2 H2O Fe2O3
(2)
(3)
【分析】A、B、C、D、E、X、Y、Z都是化学常见的物质,其中A是天然气的主要成分,则A为甲烷,甲烷和单质X点燃会生成氧化物B、C,根据常温下C是液体,甲烷和氧气点燃生成二氧化碳和水,所以X是氧气,C是水,B是二氧化碳,二氧化碳和黑色的固体单质Y反应生成气体D,二氧化碳和碳高温下反应生成一氧化碳,所以D是一氧化碳,Y就是木炭,一氧化碳和红棕色粉末E(氧化物)在高温的条件下生成Z(单质)和二氧化碳,一氧化碳高温下还原氧化铁生成铁和二氧化碳,所以E是氧化铁,Z是铁,代入验证,推论合理。
【详解】(1)A为甲烷,化学式为CH4;X为氧气,化学式为O2;C为水,化学式为H2O;E为氧化铁,化学式为Fe2O3;
(2)B与Y反应即为二氧化碳和碳高温下反应生成一氧化碳,化学方程式为:;
(3)D与E反应即为一氧化碳和氧化铁高温下反应生成铁和二氧化碳,化学方程式为:。
8. H2CO3 灭火 吸收 Ca(OH)2+CO2═CaCO3↓+H2O
【分析】A、B、C、D、E是初中化学常见的物质,A、B、E均为氧化物,且B、E组成元素相同,B、E能相互转化,二氧化碳与碳在高温条件下生成一氧化碳,一氧化碳在氧气中燃烧生成二氧化碳, B、E可能是二氧化碳、一氧化碳中的一种,C、D为不同类别的化合物,D在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等, D是碳酸钠,B会转化成碳酸钠,氢氧化钠与二氧化碳反应生成碳酸钠和水,B是二氧化碳,E是一氧化碳;碳酸钠会转化成氧化物A,二氧化碳能转化为A,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水A可能是水,二氧化碳也会转化成C,二氧化碳与水化合生成碳酸,C可能是碳酸,经过验证,推导正确。
【详解】根据以上分析可知:
(1)C是碳酸,化学式是H2CO3,B是二氧化碳,可用作灭火;
(2)B→E是二氧化碳与碳在高温的条件下生成一氧化碳,反应过程中会吸收热量;
(3)B→A的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O。
【点睛】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
9.(1) H2O2 Cu(OH)2
(2)
【分析】已知A、C 是组成元素相同的氧化物,且常温常压下均为液态,A能在二氧化锰的作用下转化为B和C,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,因此A是过氧化氢,B是氧气,C是水;氧化钙和水生成氢氧化钙,因此D是氢氧化钙;X是红色固体单质,F为蓝色溶液,铜和氧气在加热的条件下生成氧化铜,因此X是铜,E是氧化铜;氧化铜和硫酸反应生成硫酸铜和水,因此F是硫酸铜;硫酸铜和氢氧化钙反应生成氢氧化铜蓝色沉淀和硫酸钙,因此G是氢氧化铜,代入验证,符合题意。
【详解】(1)由分析可知,A为过氧化氢,化学式为:H2O2;G为氢氧化铜,化学式为:Cu(OH)2;
(2)反应③为铜与氧气在加热的条件下反应生成氧化铜,该反应的化学方程式为:。
10. H2
【分析】A~E是初中化学常见的物质,其中B、C组成元素相同,D、E常温下为气体,C能转化为B、E,B、E能相互转化,所以B是水,C是过氧化氢,E是氧气,B能与D相互转化,D能与E反应,可推出D是氢气,A能转化为B、D,可推出A是酸,代入验证,推理正确。
【详解】由分析可知(1)D是氢气,化学式是H2;
(2)C→E是过氧化氢在二氧化锰催化作用下生成水和氧气,反应的化学方程式为:。
11. 放热 2H2O2H2↑+O2↑ 做食品干燥剂
【分析】A、B、C、D、E是九年级化学中常见的五种物质,已知C是人体胃液中可以帮助消化的物质,所以C是盐酸,D是大理石的主要成分,所以D是碳酸钙,B通电会生成A,所以B是水,水会与E反应,E能与C(HCl)反应,所以E是氧化钙,盐酸也会转化成A,所以A是氢气,经过验证,推导正确。
【详解】由分析可知:
(1) B与E的反应是氧化钙和水反应生成氢氧化钙,反应的化学方程为,此反应放出热量;B转化为A的反应是水在通电的条件下生成氢气和氧气,化学方程式为:2H2O2H2↑+O2↑;
(2) E是氧化钙,可以做食品干燥剂等。
12. HCl CuSO4
【详解】A、B、C、D分别是氧化铁、稀盐酸、氢氧化钠溶液、硫酸铜溶液是四种物质中的一种,B+Fe→无色气体,则B是盐酸,氧化铁和氢氧化钠可以与盐酸发生反应,盐酸和硫酸铜可以与铁发生反应,故D是硫酸铜,A可以与硫酸铜和稀盐酸发生反应,又Cu(OH)2是沉淀,故A是氢氧化钠,C是氧化铁,综上A是氢氧化钠、B是稀盐酸、C是氧化铁、D是硫酸铜。
(1)B、D物质中的溶质分别是HCl、CuSO4;
(2)B和C反应,即稀盐酸与氧化铁反应生成氯化铁和水,化学方程式是;
(3)A和D反应,即氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式是。
13. 二氧化碳 改良酸性土壤(合理即可)
【分析】A、B、C、D是初中化学常见的四种不同类别的化合物,其中有一种物质中含有人体中含量最多的金属元素,则该元素为钙;C和D反应时能生成厨房中常用的一种调味品的主要成分,该调味品为氯化钠,则C、D为碳酸钠与稀盐酸,B与D可以相互转化,二氧化碳能与碳酸钠相互转化,所以B为二氧化碳,C为稀盐酸,D为碳酸钠,则A中含有钙元素,又A、B、 C、D是初中化学常见的四种不同类别的化合物,所以A为氢氧化钙。
【详解】(1)由分析可知,B为二氧化碳,故填二氧化碳。
(2)由分析可知,A为氢氧化钙,D为碳酸钠,氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故反应的化学方程式写为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。
(3)由分析可知,A为氢氧化钙,C为盐酸,氢氧化钙与盐酸反应生成氯化钙和水,故反应的化学方程式写为:Ca(OH)2+2HCl=CaCl2+2H2O。
(4)A为氢氧化钙,氢氧化钙可用于改良酸性土壤,配制波尔多液等,故填改良酸性土壤(合理即可)。
14. CO2 CuO
【详解】已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,可以将A视为Cu(OH)2+CuCO3,所以其受热会产生CuO、H2O、和CO2,B通电可以生成两种无色气体H和I,所以B为H2O,在阴极产生I,在阳极产生H,则I为H2,H为O2,C为无色气体,则C为CO2,所以D是CuO,CO2与碳高温下生产无色气体F:CO,然后CO高温还原Fe2O3生成CO2和Fe,则G为Fe,D:CuO与稀硫酸反应B:H2O和E:CuSO4,综上,A:Cu2(OH)2CO3、B:H2O、C:CO2、D:CuO、E:CuSO4、F: CO、G:Fe、H:O2、I: H2;
(1)、铜锈的主要成分是碱式碳酸铜,含有碳酸根,所以铜生锈还与空气中的CO2有关;
(2)、已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,可以将A视为Cu(OH)2+CuCO3,所以其受热会产生CuO、H2O、和CO2,而H2O、和CO2都不与稀硫酸反应,所以D为CuO;
(3)、反应②就是水被电解生成氢气和氧气,其化学方程式为: ;
(4)、反应⑤即一氧化碳高温下还原氧化铁生产二氧化碳和铁单质,其化学反应方程式为: 。
答案第1页,共2页
答案第1页,共2页
