人教版九年级下册第九单元课题3《溶液的浓度》ppt课件(23张)
文档属性
| 名称 | 人教版九年级下册第九单元课题3《溶液的浓度》ppt课件(23张) |

|
|
| 格式 | zip | ||
| 文件大小 | 370.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-11-12 00:00:00 | ||
图片预览




文档简介
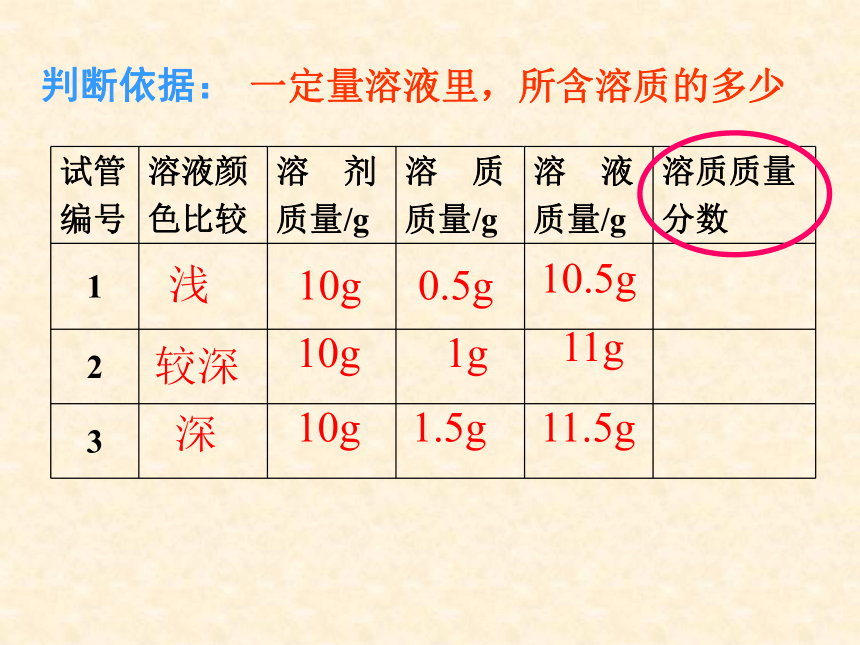
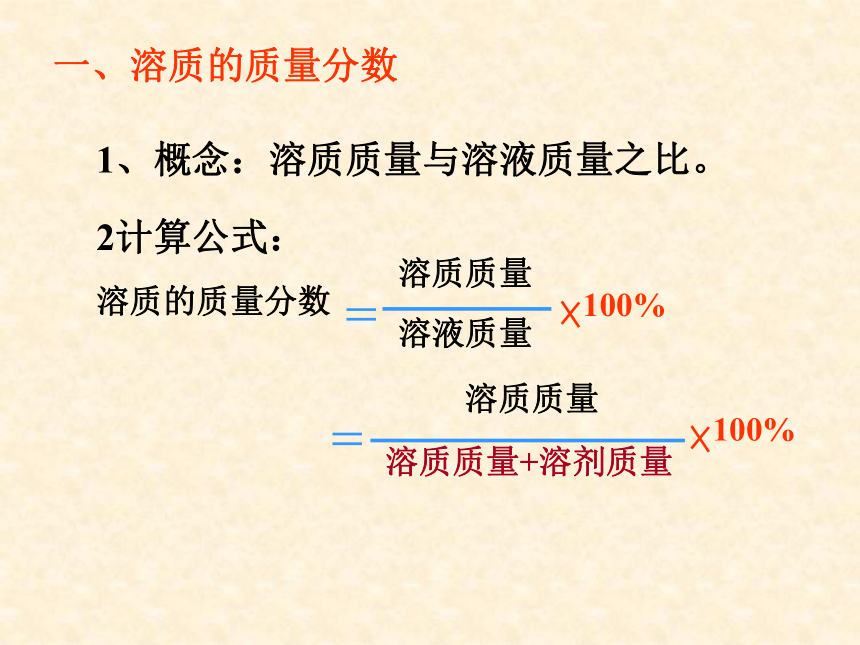
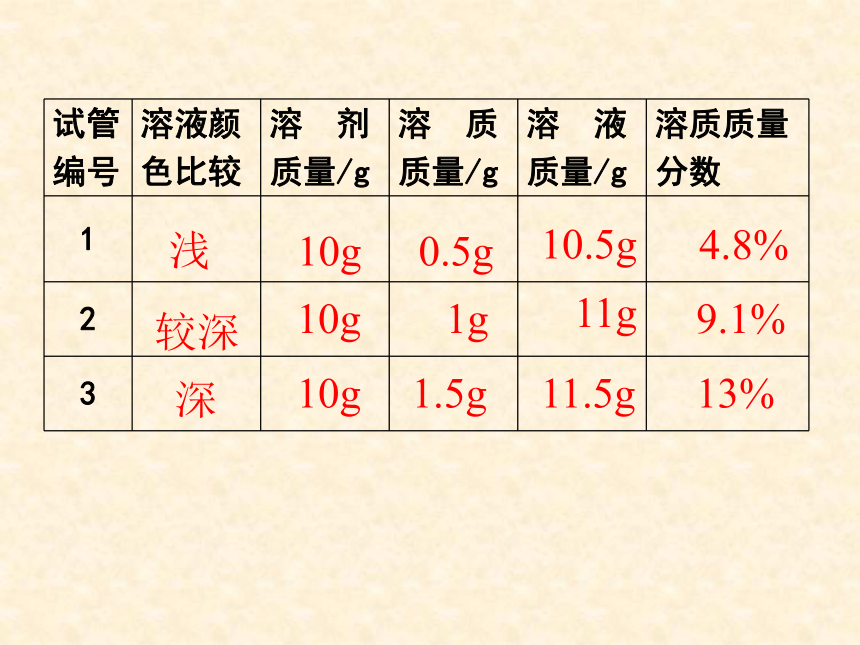
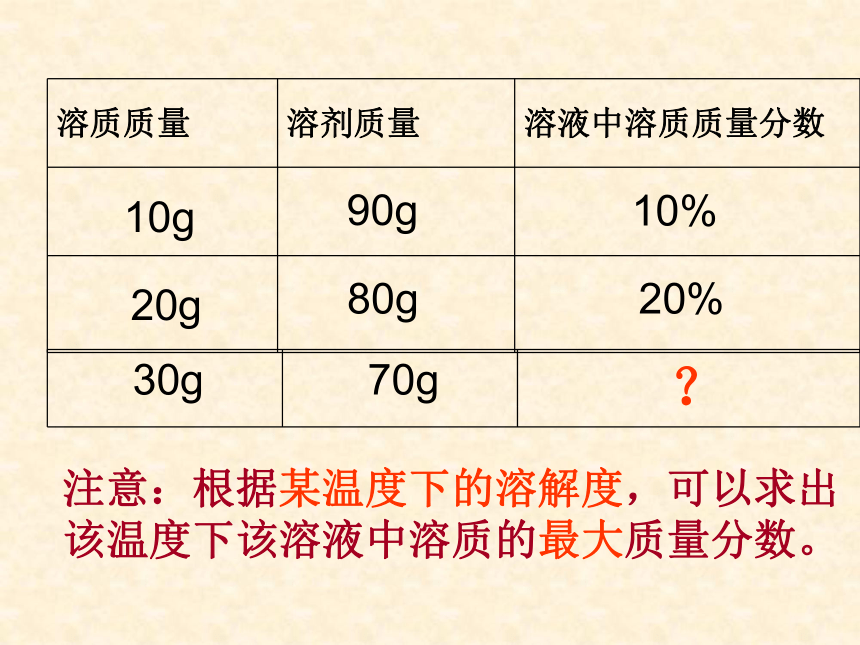
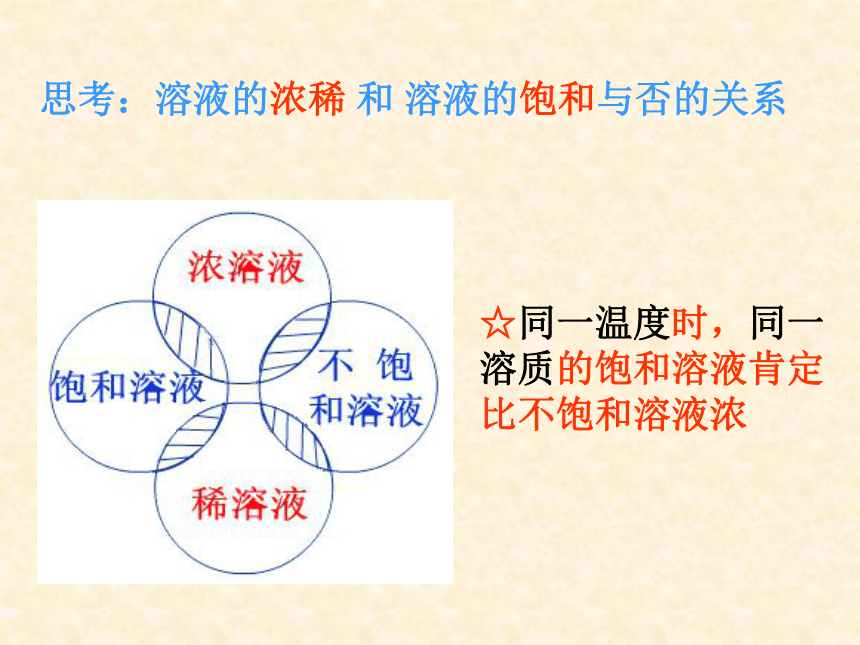
课件23张PPT。复 习1、什么叫饱和溶液?2、KNO3不饱和溶液怎样变成饱和溶液?3、Ca(OH)2饱和溶液怎样变成不饱和溶液?实验9-5颜色:淡蓝 蓝色 深蓝浅较深深10g10g10g0.5g1g1.5g10.5g11g11.5g判断依据:一定量溶液里,所含溶质的多少一、溶质的质量分数1、概念:溶质质量与溶液质量之比。2计算公式:浅较深深10g10g10g0.5g1g1.5g10.5g11g11.5g4.8%9.1%13%10g20g90g80g10%20%注意:根据某温度下的溶解度,可以求出该温度下该溶液中溶质的最大质量分数。思考:溶液的浓稀 和 溶液的饱和与否的关系☆同一温度时,同一溶质的饱和溶液肯定比不饱和溶液浓 例1在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150Kg这种溶液,需要氯化钠和水的质量各是多少?解: 练习 配制500mL质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),需要氢氧化钠和水各多少克?解:需氢氧化钠的质量=体积×密度×质量分数
=500 ×1.1 ×10%=55g
需水的质量=溶液质量-溶质质量
=500 ×1.1-55g=495g
答:需氢氧化钠55g,水495g。溶质的质量分数(第2课时)讨论: 在温度不变的条件下,如何使原有溶液 的溶质质量分数增大或减小?溶液稀释的方法:加溶剂,加入更稀的溶液溶液变浓的方法:加入溶质,加入更浓的该溶 液,蒸发溶剂(稀释前后,溶质的质量不变) 要把50g质量分数为98%的浓硫酸稀释为质
量分数为20%的硫酸溶液,需要多少克水?解:设需要水的质量为x。50g× 98%=(50g+X) × 20% X=195g 答:需要水的质量为195g。 某工厂化验室配制5000g20%的盐酸,需要38%的
盐酸(密度为1.19g/mL)的盐酸多少毫升?解:设需盐酸的体积为X
X×1.19g/cm3 ×38%=5000 g×20%
X=2211.4ml
溶 液 的 配 制 例1:配制50g质量分数为6%的食盐水 计算:需食盐:50 g× 6% = 3 g
需水: 50 g– 3 g= 47 g称量:用天平称量 3.0 g食盐 用量筒量取47mL水 溶解:烧杯、玻璃棒 装瓶:试剂瓶1.计算
2.称 托盘天平、药匙 取用药品,托盘天平使用
量 量筒,胶头滴管 读数时 注意事项
3.溶解 烧杯,玻璃棒
4. 装瓶 试剂瓶配制溶液的归纳配制步骤 所用仪器 注意事项练习:下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,请找出其中的错误,并说明理由。
溶质质量分数在化学方程式中应用1. 50g盐酸与锌完全反应,得到0.2g氢
气,求盐酸的溶质的质量分数?
2. 盐酸溶液100g,与13g含杂质5%的锌完全
反应,这种盐酸的溶质质量分数是多少? 取大理石12.5g,加入盛有100g稀盐酸的烧杯中,两者恰好完全反应(假设其他杂质不与盐酸反应,也不溶解)。烧杯内物质质量变为108.1g。
(1)生成CO2气体 质量
(2)12.5g大理石含CaCO3的质量 ,大理石CaCO3的质量分数为____
(3)100g稀盐酸中的溶质是 ,其质量是_____g
(4)完全反应后烧杯内还有_______g不溶杂质。烧杯内生成的溶液是______,其中溶质是_________,溶剂是__________。3、配制溶质质量分数一定的溶液⑴计算 ⑵称量 ⑶溶解 ⑷装瓶药匙 天平 烧杯 量筒 滴管 玻璃棒 饱和溶液的
溶质质量分数= 溶解度100g+溶解度 溶质的质量分数36% 是指: 100g溶液中含有36g溶质。
溶质T0C时溶解度36g是指: 在T0C 时,100g水最多溶解该溶质36g。溶质质量分数与溶解度的比较 例1、已知20℃时食盐的溶解度为36g,求20℃时食盐饱和溶液的溶质质量分数。 解:20℃时食盐饱和溶液的溶质质量分数为=26.5%36g100g+36g答:略 2、200C时,NaCl的溶解度是36克。现有50克水放入20克NaCl,求:所得溶液的溶质质量分数 分析:溶解度即为“溶解的限度”,50克水若溶不下20克NaCl,则溶液中NaCl的质量分数即为饱和溶液的浓度 36 /(100+36)。解:x = 18g < 20g则:溶质在溶液中的质量分数为:×100% ≈ 26.5% 100g36g=50gx18g50g+18g或36g100g+36g
=500 ×1.1 ×10%=55g
需水的质量=溶液质量-溶质质量
=500 ×1.1-55g=495g
答:需氢氧化钠55g,水495g。溶质的质量分数(第2课时)讨论: 在温度不变的条件下,如何使原有溶液 的溶质质量分数增大或减小?溶液稀释的方法:加溶剂,加入更稀的溶液溶液变浓的方法:加入溶质,加入更浓的该溶 液,蒸发溶剂(稀释前后,溶质的质量不变) 要把50g质量分数为98%的浓硫酸稀释为质
量分数为20%的硫酸溶液,需要多少克水?解:设需要水的质量为x。50g× 98%=(50g+X) × 20% X=195g 答:需要水的质量为195g。 某工厂化验室配制5000g20%的盐酸,需要38%的
盐酸(密度为1.19g/mL)的盐酸多少毫升?解:设需盐酸的体积为X
X×1.19g/cm3 ×38%=5000 g×20%
X=2211.4ml
溶 液 的 配 制 例1:配制50g质量分数为6%的食盐水 计算:需食盐:50 g× 6% = 3 g
需水: 50 g– 3 g= 47 g称量:用天平称量 3.0 g食盐 用量筒量取47mL水 溶解:烧杯、玻璃棒 装瓶:试剂瓶1.计算
2.称 托盘天平、药匙 取用药品,托盘天平使用
量 量筒,胶头滴管 读数时 注意事项
3.溶解 烧杯,玻璃棒
4. 装瓶 试剂瓶配制溶液的归纳配制步骤 所用仪器 注意事项练习:下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,请找出其中的错误,并说明理由。
溶质质量分数在化学方程式中应用1. 50g盐酸与锌完全反应,得到0.2g氢
气,求盐酸的溶质的质量分数?
2. 盐酸溶液100g,与13g含杂质5%的锌完全
反应,这种盐酸的溶质质量分数是多少? 取大理石12.5g,加入盛有100g稀盐酸的烧杯中,两者恰好完全反应(假设其他杂质不与盐酸反应,也不溶解)。烧杯内物质质量变为108.1g。
(1)生成CO2气体 质量
(2)12.5g大理石含CaCO3的质量 ,大理石CaCO3的质量分数为____
(3)100g稀盐酸中的溶质是 ,其质量是_____g
(4)完全反应后烧杯内还有_______g不溶杂质。烧杯内生成的溶液是______,其中溶质是_________,溶剂是__________。3、配制溶质质量分数一定的溶液⑴计算 ⑵称量 ⑶溶解 ⑷装瓶药匙 天平 烧杯 量筒 滴管 玻璃棒 饱和溶液的
溶质质量分数= 溶解度100g+溶解度 溶质的质量分数36% 是指: 100g溶液中含有36g溶质。
溶质T0C时溶解度36g是指: 在T0C 时,100g水最多溶解该溶质36g。溶质质量分数与溶解度的比较 例1、已知20℃时食盐的溶解度为36g,求20℃时食盐饱和溶液的溶质质量分数。 解:20℃时食盐饱和溶液的溶质质量分数为=26.5%36g100g+36g答:略 2、200C时,NaCl的溶解度是36克。现有50克水放入20克NaCl,求:所得溶液的溶质质量分数 分析:溶解度即为“溶解的限度”,50克水若溶不下20克NaCl,则溶液中NaCl的质量分数即为饱和溶液的浓度 36 /(100+36)。解:x = 18g < 20g则:溶质在溶液中的质量分数为:×100% ≈ 26.5% 100g36g=50gx18g50g+18g或36g100g+36g
同课章节目录
