2024年中考科学重点题型突破---推断题(含解析)
文档属性
| 名称 | 2024年中考科学重点题型突破---推断题(含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 561.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-04-30 00:00:00 | ||
图片预览

文档简介
2024年中考科学重点题型突破---推断题
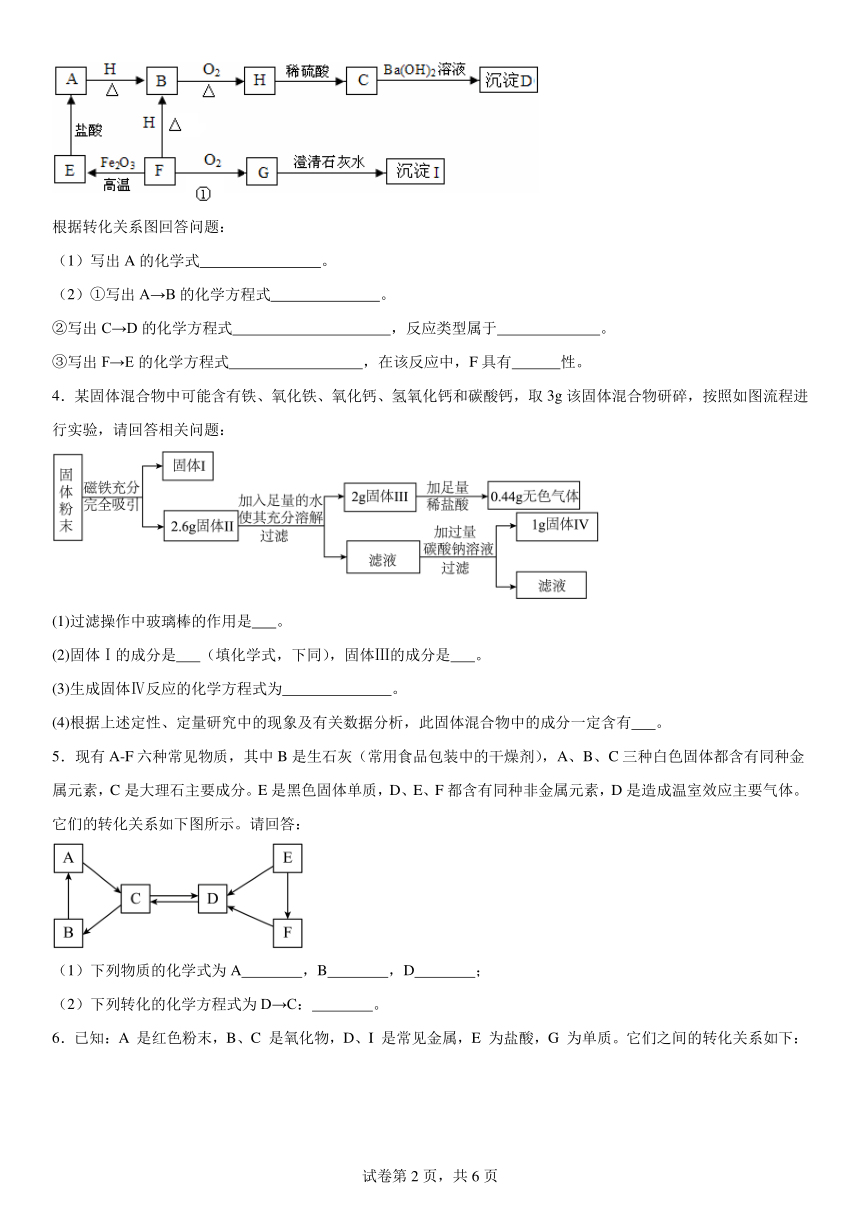
1.如图所示,A~F是初中化学常见的物质,A和B可发生中和反应,B为人体胃液中的一种物质,D为厨房中经常使用的一种调味品,但人体摄入过多可能引发高血压,F可供给呼吸,X为一种蓝绿色溶液。请根据图示回答下列问题:
(1)A的俗名为
(2)E的化学式为
(3)反应②的化学方程式为 ,其基本反应类型
(4)反应②中分别与电源正极、负极相连的玻璃管内产生的气体体积比为
(5)反应③的化学方程式为
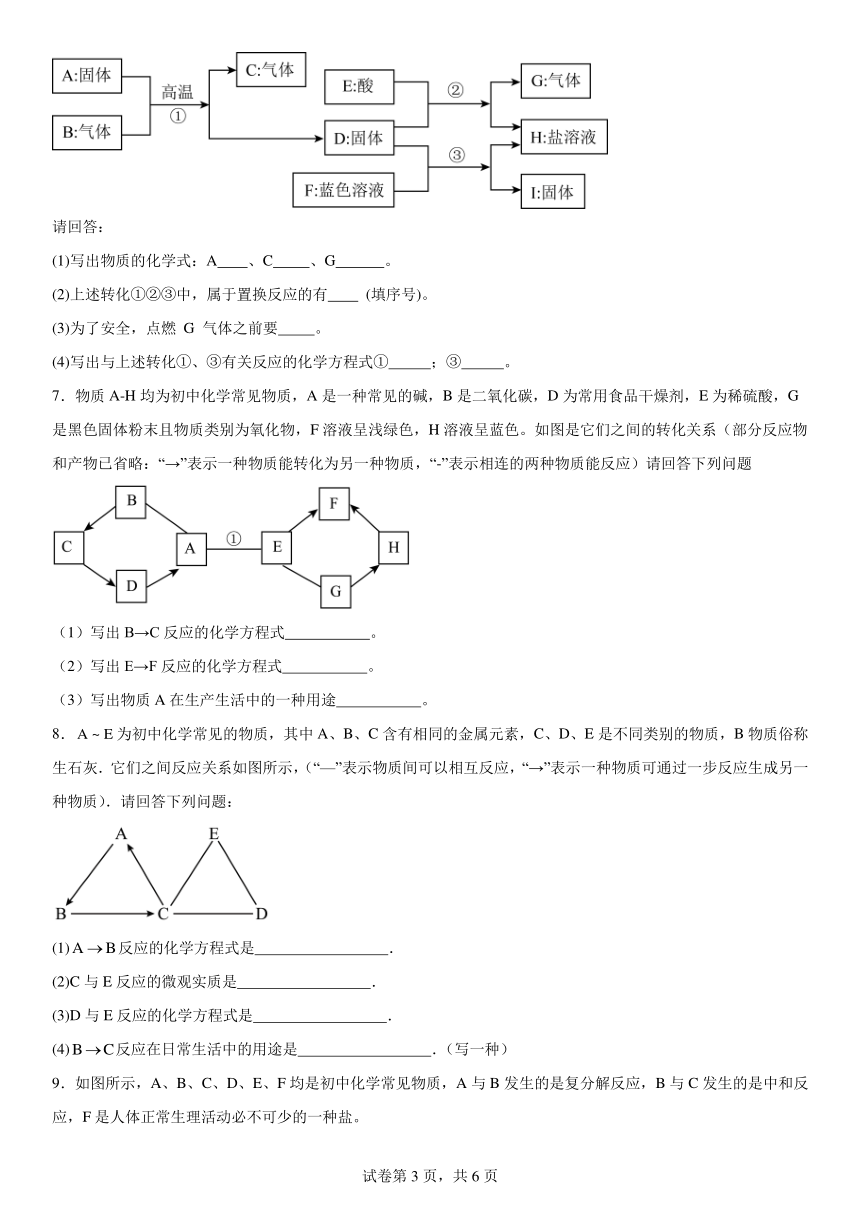
2.有一包固体粉末,可能含氯化钠、碳酸氢钠、硫酸钠、氢氧化铜、氢氧化钡中的一种或几种,某兴趣小组为探究其成分做了下列实验:
根据该实验过程及出现的现象回答:
(1)反应生成气体A的化学方程式为 。
(2)步骤②中滴加硝酸铜溶液没变化,说明B中没有 离子。
(3)生成白色滤渣C反应的化学方程式为 。
(4)原固体中一定含有的物质是 ,一定没有 。
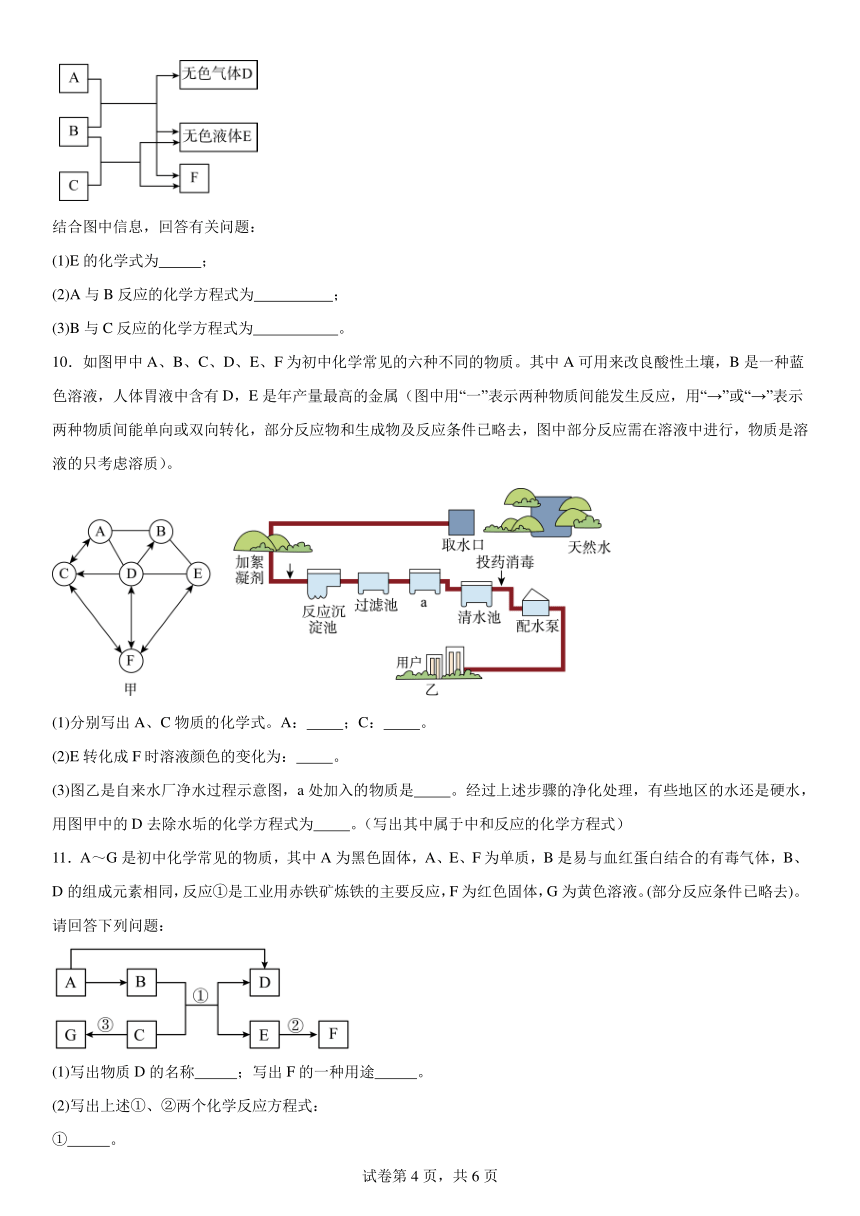
3.A、B、C、D、E、F、G、H、I都是初中化学常见的物质。其中B为紫红色固体,E、H均为黑色固体,F是一种无色气体。它们之间有下图转化关系(所发生的反应均恰好完全,部分生成物已省去)。
根据转化关系图回答问题:
(1)写出A的化学式 。
(2)①写出A→B的化学方程式 。
②写出C→D的化学方程式 ,反应类型属于 。
③写出F→E的化学方程式 ,在该反应中,F具有 性。
4.某固体混合物中可能含有铁、氧化铁、氧化钙、氢氧化钙和碳酸钙,取3g该固体混合物研碎,按照如图流程进行实验,请回答相关问题:
(1)过滤操作中玻璃棒的作用是 。
(2)固体Ⅰ的成分是 (填化学式,下同),固体Ⅲ的成分是 。
(3)生成固体Ⅳ反应的化学方程式为 。
(4)根据上述定性、定量研究中的现象及有关数据分析,此固体混合物中的成分一定含有 。
5.现有A-F六种常见物质,其中B是生石灰(常用食品包装中的干燥剂),A、B、C三种白色固体都含有同种金属元素,C是大理石主要成分。E是黑色固体单质,D、E、F都含有同种非金属元素,D是造成温室效应主要气体。它们的转化关系如下图所示。请回答:
(1)下列物质的化学式为A ,B ,D ;
(2)下列转化的化学方程式为D→C: 。
6.已知:A 是红色粉末,B、C 是氧化物,D、I 是常见金属,E 为盐酸,G 为单质。它们之间的转化关系如下:
请回答:
(1)写出物质的化学式:A 、C 、G 。
(2)上述转化①②③中,属于置换反应的有 (填序号)。
(3)为了安全,点燃 G 气体之前要 。
(4)写出与上述转化①、③有关反应的化学方程式① ;③ 。
7.物质A-H均为初中化学常见物质,A是一种常见的碱,B是二氧化碳,D为常用食品干燥剂,E为稀硫酸,G是黑色固体粉末且物质类别为氧化物,F溶液呈浅绿色,H溶液呈蓝色。如图是它们之间的转化关系(部分反应物和产物已省略:“→”表示一种物质能转化为另一种物质,“-”表示相连的两种物质能反应)请回答下列问题
(1)写出B→C反应的化学方程式 。
(2)写出E→F反应的化学方程式 。
(3)写出物质A在生产生活中的一种用途 。
8.为初中化学常见的物质,其中A、B、C含有相同的金属元素,C、D、E是不同类别的物质,B物质俗称生石灰.它们之间反应关系如图所示,(“—”表示物质间可以相互反应,“→”表示一种物质可通过一步反应生成另一种物质).请回答下列问题:
(1)反应的化学方程式是 .
(2)C与E反应的微观实质是 .
(3)D与E反应的化学方程式是 .
(4)反应在日常生活中的用途是 .(写一种)
9.如图所示,A、B、C、D、E、F均是初中化学常见物质,A与B发生的是复分解反应,B与C发生的是中和反应,F是人体正常生理活动必不可少的一种盐。
结合图中信息,回答有关问题:
(1)E的化学式为 ;
(2)A与B反应的化学方程式为 ;
(3)B与C反应的化学方程式为 。
10.如图甲中A、B、C、D、E、F为初中化学常见的六种不同的物质。其中A可用来改良酸性土壤,B是一种蓝色溶液,人体胃液中含有D,E是年产量最高的金属(图中用“一”表示两种物质间能发生反应,用“→”或“→”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。
(1)分别写出A、C物质的化学式。A: ;C: 。
(2)E转化成F时溶液颜色的变化为: 。
(3)图乙是自来水厂净水过程示意图,a处加入的物质是 。经过上述步骤的净化处理,有些地区的水还是硬水,用图甲中的D去除水垢的化学方程式为 。(写出其中属于中和反应的化学方程式)
11.A~G是初中化学常见的物质,其中A为黑色固体,A、E、F为单质,B是易与血红蛋白结合的有毒气体,B、D的组成元素相同,反应①是工业用赤铁矿炼铁的主要反应,F为红色固体,G为黄色溶液。(部分反应条件已略去)。请回答下列问题:
(1)写出物质D的名称 ;写出F的一种用途 。
(2)写出上述①、②两个化学反应方程式:
① 。
② 。
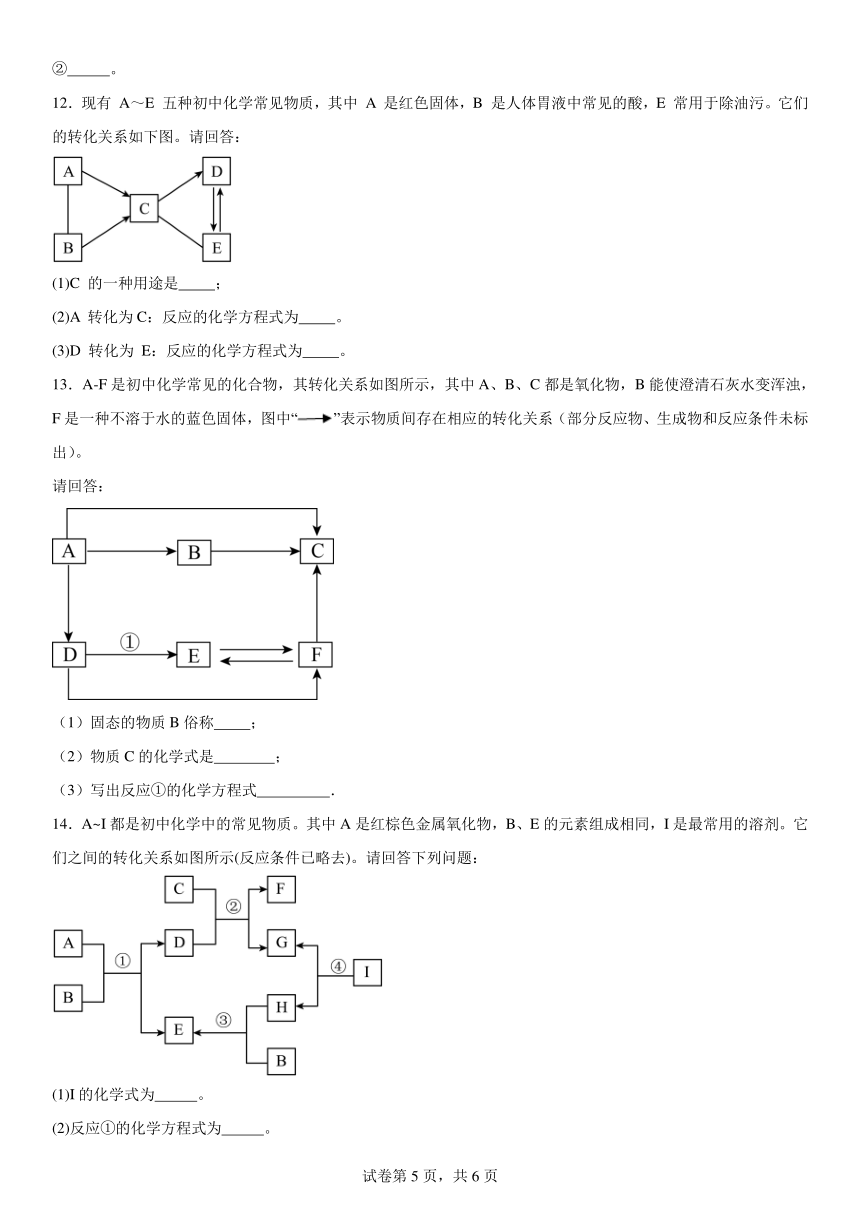
12.现有 A~E 五种初中化学常见物质,其中 A 是红色固体,B 是人体胃液中常见的酸,E 常用于除油污。它们的转化关系如下图。请回答:
(1)C 的一种用途是 ;
(2)A 转化为C:反应的化学方程式为 。
(3)D 转化为 E:反应的化学方程式为 。
13.A-F是初中化学常见的化合物,其转化关系如图所示,其中A、B、C都是氧化物,B能使澄清石灰水变浑浊,F是一种不溶于水的蓝色固体,图中“”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出)。
请回答:
(1)固态的物质B俗称 ;
(2)物质C的化学式是 ;
(3)写出反应①的化学方程式 .
14.A~I都是初中化学中的常见物质。其中A是红棕色金属氧化物,B、E的元素组成相同,I是最常用的溶剂。它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为 。
(2)反应①的化学方程式为 。
(3)反应②的基本反应类型为 。
(4)H的一种用途是 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1. 火碱、烧碱、苛性钠 H2 2H2O2H2↑+O2↑ 分解反应 1:2 2H2+O22H2O
【详解】A和B可发生中和反应,B为人体胃液中的一种物质,故B是稀盐酸,D为厨房中经常使用的一种调味品,但人体摄入过多可能引发高血压,故D是氯化钠,F可供给呼吸,故F是氧气,A和B发生中和反应,生成C,C可以在通电的条件下反应生成氧气和E,故E是氢气,A是氢氧化钠,故A是氢氧化钠,B是稀盐酸,C是水,D是氯化钠,E是氢气,F是氧气,经推断,合理。
(1)A的俗称是火碱、烧碱、苛性钠。
(2)E物质是氢气,化学式为:H2.
(3). 反应②是电解水,水在通电的条件下反应生成氢气和氧气,反应的方程式为:2H2O2H2↑+O2↑。该反应是分解反应。
(4)反应②是电解水,电解水中分别与电源正极、负极相连的玻璃管内产生的气体分别是氧气和氢气,体积比为1:2
(5)反应③是氢气和氧气在点燃的条件下反应生成水,反应的方程式为:2H2+O22H2O。
2. 氢氧根(OH -) 碳酸氢钠和氢氧化钡 硫酸钠和氢氧化铜
【详解】(1)由图可知,固体样品滴加稀盐酸产生气体A,而在样品可能组成中只有碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳,故填写:;
(2)由图可知,无色溶液B中滴加硝酸铜,无现象(无气体、沉淀、溶液颜色变化),而铜离子和氢氧根离子结合,会生成蓝色沉淀氢氧化铜,因此,说明B中没有氢氧根(OH -),故填写:氢氧根(OH -);
(3)由图可知,滴加硝酸铜溶液后的溶液又滴加了过量的硫酸镁溶液,过滤得到了白色滤渣C,由(2)可知,滴加硝酸铜溶液后的溶液中无氢氧根离子,因此,白色沉淀是硫酸根离子与阳离子结合产生的,由题干可知,能与硫酸根离子产生沉淀的阳离子是钡离子,由于步骤①中加入了稀盐酸,因此,没加硫酸镁溶液前的溶液中有氯离子,生成白色滤渣C的反应是氯化钡与硫酸镁生产成硫酸钡和氯化镁,故填写: ;
(4)由(1)和(3)可知,原固体中一定含有的物质是碳酸氢钠和氢氧化钡,故填写:碳酸氢钠和氢氧化钡;
由图可知,固体样品滴加稀盐酸产生气体和无色溶液,说明原固体中没有氢氧化铜和硫酸钠,因为氢氧化铜与盐酸反应生成氯化铜,氯化铜溶液显蓝色,而硫酸钠与氯化钡不能共存,能产生硫酸钡沉淀,故填写:硫酸钠和氢氧化铜。
【点睛】该题为流程图型的推断题,解题关键是将图中每一步实验,都得出结论,从最熟悉的结论入手,推出原物质中的成分,进而解答问题。
3. H2 复分解反应 还原
【分析】A、B、C、D、E、F、G、H、I都是初中化学常见的物质。其中B为紫红色固体,可推出B为铜,F是一种无色气体,F能与氧气反应生成G,G能与澄清石灰水反应生成沉淀I,可推出F为一氧化碳,G为二氧化碳,I为碳酸钙,F能与氧化铁在高温下反应生成E,E为黑色固体,可推出E为铁,E能与盐酸转化为A,A能与H在加热的条件下反应生成B,可推出A为氢气,H为氧化铜,H能与稀硫酸反应生成C,C能与氢氧化钡反应生成沉淀D,可推出C为硫酸铜,D为硫酸钡或氢氧化铜,代入验证,符合题意。
【详解】(1)由分析可知,A为氢气,化学式为:H2;
(2)①A为氢气,B为单质铜,故A→B的反应为氢气和氧化铜在加热的条件下反应生成铜和二氧化碳
②C→D的反应为硫酸铜与氢氧化钡反应生成氢氧化铜和硫酸钡,该反应的化学方程式为:;
该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;
③F→E的反应为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:;
在该反应中,一氧化碳得到氧,具有还原性。
4.(1)引流
(2) Fe CaCO3、Fe2O3
(3)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(4)Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【分析】固体混合物中可能含有铁、氧化铁、氧化钙、氢氧化钙和碳酸钙,磁铁充分完全吸引后得到固体Ⅰ和2.6g固体Ⅱ,固体Ⅱ充分溶解过滤后得到2g固体Ⅲ和滤液,铁、氧化铁和碳酸钙均不溶于水,氧化钙与水反应生成氢氧化钙,氢氧化钙微溶于水,则固体Ⅰ为3g-2.6g=0.4g铁;2g固体Ⅲ与足量稀盐酸反应生成0.44g无色气体,根据质量守恒定律可知,该气体为二氧化碳且固体Ⅲ中含有碳酸钙,设碳酸钙的质量为x,
= 解得x=1g
2g固体Ⅲ中含有1g碳酸钙和2g-1g=1g氧化铁;2.6g-2g=0.6g固体溶解后得到的滤液为氢氧化钙溶液,滤液中的氢氧化钙与过量碳酸钠溶液反应生成的1g固体Ⅳ为碳酸钙,设滤液中氢氧化钙的质量为y,
= 解得y=0.74g
设固体混合物中氧化钙和氢氧化钙的质量分别为m、n,
综上所述,有m+n=0.6g、m+n=0.74g,解得m≈0.44g、n≈0.16g,说明固体混合物中也含有氧化钙和氢氧化钙。
【详解】(1)过滤时,玻璃棒用于向漏斗中添加液体时引流。
(2)分析可知,固体Ⅰ的成分为0.4g铁(Fe),固体Ⅲ的成分为1g碳酸钙(CaCO3)和1g氧化铁(Fe2O3)。
(3)氢氧化钙与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。
(4)分析可知,该固体混合物中一定含有铁(Fe)、氧化铁(Fe2O3)、氧化钙(CaO)、氢氧化钙[Ca(OH)2]和碳酸钙(CaCO3)。
5. Ca(OH)2 CaO CO2
【分析】B是生石灰(常用食品包装中的干燥剂),氧化钙;A、B、C三种白色固体都含有同种金属元素钙元素,C是大理石主要成分,C为碳酸钙;观察ABC转化为钙三角转化关系,氧化钙和水反应生成氢氧化钙,则A为氢氧化钙;D是造成温室效应主要气体,为二氧化碳;E是黑色固体单质,D、E、F都含有同种非金属元素,观察DEF转化为碳三角转化,E为碳、F为一氧化碳;代入检验推理正确;
【详解】(1)化学式为A:Ca(OH)2,B:CaO,D:CO2;
(2)D→C反应为二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水:。
6.(1)
(2)②③/③②
(3)检验纯度
(4)
【分析】A是红色粉末,B是气态氧化物,且A与B在高温条件下反应生成气体C与固体D,则A为氧化铁,B为一氧化碳,C为二氧化碳,D为铁;E为胃酸的主要成分,则E为稀盐酸;D(铁)与E(稀盐酸)反应生成G(气体)与H(盐),则G为氢气,H为氯化亚铁;F为蓝色溶液,且能与D(铁)反应生成H(氯化亚铁)和I,则F为氯化铜,I为铜。
【详解】(1)由分析可知,A为氧化铁,C为二氧化碳,G为氢气,故填、、;
(2)反应①为一氧化碳高温还原氧化铁,不符合置换反应“一种单质置换另一种单质”特点,故①不是置换反应;
②反应为稀盐酸和铁生成氢气和氯化亚铁,方程式为 ,符合置换反应特点,属于置换反应;
③反应为铁和氯化铜反应生成氯化亚铁和铜的反应,方程式为,符合置换反应特点,属于置换反应,故填②③;
(3)G为氢气,氢气在纯度不足时燃烧容易引发爆炸,故点燃氢气之前需要检验纯度,故填检验纯度;
(4)反应①为一氧化碳高温还原氧化铁,方程式为;
反应③为铁和氯化铜反应生成氯化亚铁和铜的反应,方程式为。
7. 改良酸性土壤(等合理即可)
【分析】A-H均为初中化学常见物质,A是一种常见的碱,D为常用食品干燥剂,且D 可转化为A,可推出D为氧化钙,A为氢氧化钙,B是二氧化碳,且B可转化为C,C可转化为氧化钙,可推出C为碳酸钙,E为稀硫酸, F溶液呈浅绿色,且稀硫酸可转化为F,可推出F为硫酸亚铁,G是黑色固体粉末且物质类别为氧化物,G能与稀硫酸反应,且G能转化为H,H溶液呈蓝色,可推出G为氧化铜,H为硫酸铜。
【详解】(1)B是二氧化碳,C为碳酸钙,二氧化碳可与氢氧化钙反应生成碳酸钙和水,该反应的化学方程式为:;
(2)E为稀硫酸,F为硫酸亚铁,稀硫酸可与铁反应生成硫酸亚铁和氢气,该反应的化学方程式为:;
(3)A为氢氧化钙,A在生活中可以改良酸性土壤、配制农药波尔多液等。
8.(1)
(2)氢离子与氢氧根离子结合生成水分子
(3)
(4)用作食品干燥剂
【分析】
B物质俗称生石灰,则B为氧化钙;A能生成B,推测A为碳酸钙,即碳酸钙高温生成B氧化钙和二氧化碳;B能生成C,氧化钙和水反应生成C氢氧化钙;C能生成A,即氢氧化钙和二氧化碳反应生成碳酸钙和水;C和D能相互反应,推测D为碳酸钠,即碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氯化钠;D和E、C和E能相互反应,推测E为盐酸;带入验证符合题意。
【详解】(1)根据分析,A能生成B,推测A为碳酸钙,A→B反应即碳酸钙高温生成氧化钙和二氧化碳,反应的化学方程式为;故填:;
(2)由分析知,C为氢氧化钙,E为盐酸, C与E反应为氢氧化钙和盐酸反应生成氯化钙和水,反应的微观实质是氢离子与氢氧根离子结合生成水分子;故填:氢离子与氢氧根离子结合生成水分子;
(3)由分析知,D为碳酸钠,E为盐酸,D与E反应为碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式是;故填:;
(4)由分析知B为氢氧化钙,C为碳酸钙,B→C反应为氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,在日常生活中的用途是用作食品干燥剂或自热米饭的发热包或干燥剂;故填:用作食品干燥剂。
9.(1)
(2)
(3)
【分析】
F是人体正常生理活动必不可少的一种盐,F就是氯化钠,B与C发生的是中和反应,所以B和C就是盐酸和氢氧化钠,无色液体E就是水,A与B发生的是复分解反应,且会生成氯化钠、水和无色气体D,所以B就是盐酸,C就是氢氧化钠,A就应该是碳酸钠,代入验证,推理正确。
【详解】(1)由分析可知,E就是水,化学式为:;
(2)A与B是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:;
(3)B与C是盐酸和氢氧化钠反应生成氯化钠和水,反应的化学方程式为:。
10.(1)
(2)溶液由无色变为浅绿色
(3) 活性炭
【分析】图甲中A、B、C、D、E、F为初中化学常见的六种不同的物质。其中A可用来改良酸性土壤,可推出A为氢氧化钙,人体胃液中含有D,可推出D为盐酸,E是年产量最高的金属,可推出E为铁,B是一种蓝色溶液,D能转化为B,可推出B为氯化铜,D能转化为C,A能与C相互转化,可推出C为水,C、D、E均能与F相互转化,可推出F为氢气,代入验证,符合题意。
【详解】(1)由分析可知,A为氢氧化钙,化学式为:Ca(OH)2;C为水,化学式为:H2O;
(2)E转化成F的反应为铁和稀盐酸反应生成氯化亚铁和氢气,溶液颜色的变化为:溶液由无色变为浅绿色;
(3)a处是吸附,加入的物质是活性炭,活性炭结构疏松多孔,具有吸附性,可以吸附水中的色素和异味;
水垢的主要成分是碳酸钙和氢氧化镁,碳酸钙能与稀盐酸反应生成氯化钙、二氧化碳和水,氢氧化镁能与稀盐酸反应生成氯化镁和水,故可用稀盐酸除去水垢,氢氧化镁和稀盐酸的反应属于中和反应,该反应的化学方程式为:。
11. 二氧化碳 作导线 Fe2O3+3CO2Fe+3CO2 Fe+CuSO4=FeSO4+Cu(这里用CuCl2或Cu(NO3)2均可)
【分析】B是易与血红蛋白结合的有毒气体,则B为一氧化碳;B、D的组成元素相同,则D为二氧化碳;A为黑色固体,且为单质,还能够反应生成B(一氧化碳)和D(二氧化碳),则A为碳;反应①是工业用赤铁矿炼铁的主要反应,则C为氧化铁,E为铁;F为红色固体,能够由E(铁)反应生成,则F为铜;G为黄色溶液,能够由C(氧化铁)反应生成,则G是一种铁盐溶液。
【详解】(1)由分析可知,D为二氧化碳,故填二氧化碳;
由分析可知,F是铜,铜具有良好的导电性,可作导线,故填作导线。
(2)①反应①氧化铁与一氧化碳在高温的条件下反应生成铁和二氧化碳,故反应的化学方程式写为:Fe2O3+3CO2Fe+3CO2。
②反应②是铁与铜盐溶液反应生成亚铁盐和铜,如铁与硫酸铜反应生成硫酸亚铁和铜,故反应的化学方程式写为:Fe+CuSO4=FeSO4+Cu。
12.(1)灭火等
(2)等
(3)
【分析】B 是人体胃液中常见的酸,则B是盐酸,A 是红色固体,且能与B盐酸反应,则A是氧化铁,E 常用于除油污,则E是氢氧化钠,A和B都能反应生成C,且C能与E氢氧化钠反应,则C可能是二氧化碳,D可能为碳酸钠,综合整体,C二氧化碳,D碳酸钠,符合题意。
【详解】(1)依据分析可知,C为二氧化碳,其用途有做气体肥料,灭火等。
(2)A是氧化铁,碳或一氧化碳都可还原生成二氧化碳,其反应的化学方程式为:或
(3)D是碳酸钠,与氢氧化钙反应可生成E氢氧化钠,其反应的化学方程式为:
13. 干冰 H2O CuSO4+BaCl2=BaSO4↓+CuCl2
【详解】A-F是初中化学常见的化合物,A、B、C都是氧化物,B能使澄清石灰水变浑浊,故B是二氧化碳,F是一种不溶于水的蓝色固体,故F是氢氧化铜,氢氧化铜会转化成C,故C是水, A会转化成二氧化碳、水,故A可能为氧化铜,氧化铜转化成的D可以直接转化成氢氧化铜,E和氢氧化铜可以相互转化,故E是氯化铜,D是硫酸铜,代入验证,推导正确;
(1)由分析可知:B是二氧化碳,固态的二氧化碳俗称干冰;
(2)由分析可知:C是水,故化学式为:H2O;
(3)由分析可知:反应①是硫酸铜转化为氯化铜,反应①可能为硫酸铜溶液和氯化钡溶液反应生成硫酸钡沉淀和氯化铜,故反应的化学方程式为:CuSO4+BaCl2=BaSO4↓+CuCl2。
【点睛】考查物质的推断,根据框图和题目信息进行分析,推导出各物质,并代入验证是否正确。
14.(1)H2O
(2)3CO+Fe2O32Fe+3CO2
(3)置换反应
(4)医疗急救
【分析】A~I都是初中化学中的常见物质。其中A是红棕色金属氧化物,故A为氧化铁,B、E的元素组成相同,I是最常用的溶剂,故I为水,A与B反应可生成D和E,一氧化碳和氧化铁高温下反应生成二氧化碳和铁,故B为一氧化碳,E为二氧化碳,D为铁,C和D(铁)反应可生成F和G,I(水)可转化为G和H,H和B(一氧化碳)可生成E(二氧化碳),水通电分解生成氢气和氧气,一氧化碳和氧气点燃生成二氧化碳,故H为氧气,G为氢气,铁和稀盐酸或稀硫酸反应生成氯化亚铁或硫酸亚铁和氢气,故C为稀盐酸或稀硫酸,F为氯化亚铁或硫酸亚铁,代入验证,推论合理。
【详解】(1)I为水,化学式为H2O;
(2)反应①为一氧化和氧化铁高温下反应生成铁和二氧化碳,化学方程式为:;
(3)反应②为铁和稀盐酸或稀硫酸反应生成氯化亚铁或硫酸亚铁和氢气,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应;
(4)H为氧气,氧气可以供给呼吸,可用于医疗急救。
答案第1页,共2页
答案第1页,共2页
1.如图所示,A~F是初中化学常见的物质,A和B可发生中和反应,B为人体胃液中的一种物质,D为厨房中经常使用的一种调味品,但人体摄入过多可能引发高血压,F可供给呼吸,X为一种蓝绿色溶液。请根据图示回答下列问题:
(1)A的俗名为
(2)E的化学式为
(3)反应②的化学方程式为 ,其基本反应类型
(4)反应②中分别与电源正极、负极相连的玻璃管内产生的气体体积比为
(5)反应③的化学方程式为
2.有一包固体粉末,可能含氯化钠、碳酸氢钠、硫酸钠、氢氧化铜、氢氧化钡中的一种或几种,某兴趣小组为探究其成分做了下列实验:
根据该实验过程及出现的现象回答:
(1)反应生成气体A的化学方程式为 。
(2)步骤②中滴加硝酸铜溶液没变化,说明B中没有 离子。
(3)生成白色滤渣C反应的化学方程式为 。
(4)原固体中一定含有的物质是 ,一定没有 。
3.A、B、C、D、E、F、G、H、I都是初中化学常见的物质。其中B为紫红色固体,E、H均为黑色固体,F是一种无色气体。它们之间有下图转化关系(所发生的反应均恰好完全,部分生成物已省去)。
根据转化关系图回答问题:
(1)写出A的化学式 。
(2)①写出A→B的化学方程式 。
②写出C→D的化学方程式 ,反应类型属于 。
③写出F→E的化学方程式 ,在该反应中,F具有 性。
4.某固体混合物中可能含有铁、氧化铁、氧化钙、氢氧化钙和碳酸钙,取3g该固体混合物研碎,按照如图流程进行实验,请回答相关问题:
(1)过滤操作中玻璃棒的作用是 。
(2)固体Ⅰ的成分是 (填化学式,下同),固体Ⅲ的成分是 。
(3)生成固体Ⅳ反应的化学方程式为 。
(4)根据上述定性、定量研究中的现象及有关数据分析,此固体混合物中的成分一定含有 。
5.现有A-F六种常见物质,其中B是生石灰(常用食品包装中的干燥剂),A、B、C三种白色固体都含有同种金属元素,C是大理石主要成分。E是黑色固体单质,D、E、F都含有同种非金属元素,D是造成温室效应主要气体。它们的转化关系如下图所示。请回答:
(1)下列物质的化学式为A ,B ,D ;
(2)下列转化的化学方程式为D→C: 。
6.已知:A 是红色粉末,B、C 是氧化物,D、I 是常见金属,E 为盐酸,G 为单质。它们之间的转化关系如下:
请回答:
(1)写出物质的化学式:A 、C 、G 。
(2)上述转化①②③中,属于置换反应的有 (填序号)。
(3)为了安全,点燃 G 气体之前要 。
(4)写出与上述转化①、③有关反应的化学方程式① ;③ 。
7.物质A-H均为初中化学常见物质,A是一种常见的碱,B是二氧化碳,D为常用食品干燥剂,E为稀硫酸,G是黑色固体粉末且物质类别为氧化物,F溶液呈浅绿色,H溶液呈蓝色。如图是它们之间的转化关系(部分反应物和产物已省略:“→”表示一种物质能转化为另一种物质,“-”表示相连的两种物质能反应)请回答下列问题
(1)写出B→C反应的化学方程式 。
(2)写出E→F反应的化学方程式 。
(3)写出物质A在生产生活中的一种用途 。
8.为初中化学常见的物质,其中A、B、C含有相同的金属元素,C、D、E是不同类别的物质,B物质俗称生石灰.它们之间反应关系如图所示,(“—”表示物质间可以相互反应,“→”表示一种物质可通过一步反应生成另一种物质).请回答下列问题:
(1)反应的化学方程式是 .
(2)C与E反应的微观实质是 .
(3)D与E反应的化学方程式是 .
(4)反应在日常生活中的用途是 .(写一种)
9.如图所示,A、B、C、D、E、F均是初中化学常见物质,A与B发生的是复分解反应,B与C发生的是中和反应,F是人体正常生理活动必不可少的一种盐。
结合图中信息,回答有关问题:
(1)E的化学式为 ;
(2)A与B反应的化学方程式为 ;
(3)B与C反应的化学方程式为 。
10.如图甲中A、B、C、D、E、F为初中化学常见的六种不同的物质。其中A可用来改良酸性土壤,B是一种蓝色溶液,人体胃液中含有D,E是年产量最高的金属(图中用“一”表示两种物质间能发生反应,用“→”或“→”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。
(1)分别写出A、C物质的化学式。A: ;C: 。
(2)E转化成F时溶液颜色的变化为: 。
(3)图乙是自来水厂净水过程示意图,a处加入的物质是 。经过上述步骤的净化处理,有些地区的水还是硬水,用图甲中的D去除水垢的化学方程式为 。(写出其中属于中和反应的化学方程式)
11.A~G是初中化学常见的物质,其中A为黑色固体,A、E、F为单质,B是易与血红蛋白结合的有毒气体,B、D的组成元素相同,反应①是工业用赤铁矿炼铁的主要反应,F为红色固体,G为黄色溶液。(部分反应条件已略去)。请回答下列问题:
(1)写出物质D的名称 ;写出F的一种用途 。
(2)写出上述①、②两个化学反应方程式:
① 。
② 。
12.现有 A~E 五种初中化学常见物质,其中 A 是红色固体,B 是人体胃液中常见的酸,E 常用于除油污。它们的转化关系如下图。请回答:
(1)C 的一种用途是 ;
(2)A 转化为C:反应的化学方程式为 。
(3)D 转化为 E:反应的化学方程式为 。
13.A-F是初中化学常见的化合物,其转化关系如图所示,其中A、B、C都是氧化物,B能使澄清石灰水变浑浊,F是一种不溶于水的蓝色固体,图中“”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出)。
请回答:
(1)固态的物质B俗称 ;
(2)物质C的化学式是 ;
(3)写出反应①的化学方程式 .
14.A~I都是初中化学中的常见物质。其中A是红棕色金属氧化物,B、E的元素组成相同,I是最常用的溶剂。它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为 。
(2)反应①的化学方程式为 。
(3)反应②的基本反应类型为 。
(4)H的一种用途是 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1. 火碱、烧碱、苛性钠 H2 2H2O2H2↑+O2↑ 分解反应 1:2 2H2+O22H2O
【详解】A和B可发生中和反应,B为人体胃液中的一种物质,故B是稀盐酸,D为厨房中经常使用的一种调味品,但人体摄入过多可能引发高血压,故D是氯化钠,F可供给呼吸,故F是氧气,A和B发生中和反应,生成C,C可以在通电的条件下反应生成氧气和E,故E是氢气,A是氢氧化钠,故A是氢氧化钠,B是稀盐酸,C是水,D是氯化钠,E是氢气,F是氧气,经推断,合理。
(1)A的俗称是火碱、烧碱、苛性钠。
(2)E物质是氢气,化学式为:H2.
(3). 反应②是电解水,水在通电的条件下反应生成氢气和氧气,反应的方程式为:2H2O2H2↑+O2↑。该反应是分解反应。
(4)反应②是电解水,电解水中分别与电源正极、负极相连的玻璃管内产生的气体分别是氧气和氢气,体积比为1:2
(5)反应③是氢气和氧气在点燃的条件下反应生成水,反应的方程式为:2H2+O22H2O。
2. 氢氧根(OH -) 碳酸氢钠和氢氧化钡 硫酸钠和氢氧化铜
【详解】(1)由图可知,固体样品滴加稀盐酸产生气体A,而在样品可能组成中只有碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳,故填写:;
(2)由图可知,无色溶液B中滴加硝酸铜,无现象(无气体、沉淀、溶液颜色变化),而铜离子和氢氧根离子结合,会生成蓝色沉淀氢氧化铜,因此,说明B中没有氢氧根(OH -),故填写:氢氧根(OH -);
(3)由图可知,滴加硝酸铜溶液后的溶液又滴加了过量的硫酸镁溶液,过滤得到了白色滤渣C,由(2)可知,滴加硝酸铜溶液后的溶液中无氢氧根离子,因此,白色沉淀是硫酸根离子与阳离子结合产生的,由题干可知,能与硫酸根离子产生沉淀的阳离子是钡离子,由于步骤①中加入了稀盐酸,因此,没加硫酸镁溶液前的溶液中有氯离子,生成白色滤渣C的反应是氯化钡与硫酸镁生产成硫酸钡和氯化镁,故填写: ;
(4)由(1)和(3)可知,原固体中一定含有的物质是碳酸氢钠和氢氧化钡,故填写:碳酸氢钠和氢氧化钡;
由图可知,固体样品滴加稀盐酸产生气体和无色溶液,说明原固体中没有氢氧化铜和硫酸钠,因为氢氧化铜与盐酸反应生成氯化铜,氯化铜溶液显蓝色,而硫酸钠与氯化钡不能共存,能产生硫酸钡沉淀,故填写:硫酸钠和氢氧化铜。
【点睛】该题为流程图型的推断题,解题关键是将图中每一步实验,都得出结论,从最熟悉的结论入手,推出原物质中的成分,进而解答问题。
3. H2 复分解反应 还原
【分析】A、B、C、D、E、F、G、H、I都是初中化学常见的物质。其中B为紫红色固体,可推出B为铜,F是一种无色气体,F能与氧气反应生成G,G能与澄清石灰水反应生成沉淀I,可推出F为一氧化碳,G为二氧化碳,I为碳酸钙,F能与氧化铁在高温下反应生成E,E为黑色固体,可推出E为铁,E能与盐酸转化为A,A能与H在加热的条件下反应生成B,可推出A为氢气,H为氧化铜,H能与稀硫酸反应生成C,C能与氢氧化钡反应生成沉淀D,可推出C为硫酸铜,D为硫酸钡或氢氧化铜,代入验证,符合题意。
【详解】(1)由分析可知,A为氢气,化学式为:H2;
(2)①A为氢气,B为单质铜,故A→B的反应为氢气和氧化铜在加热的条件下反应生成铜和二氧化碳
②C→D的反应为硫酸铜与氢氧化钡反应生成氢氧化铜和硫酸钡,该反应的化学方程式为:;
该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;
③F→E的反应为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:;
在该反应中,一氧化碳得到氧,具有还原性。
4.(1)引流
(2) Fe CaCO3、Fe2O3
(3)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(4)Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【分析】固体混合物中可能含有铁、氧化铁、氧化钙、氢氧化钙和碳酸钙,磁铁充分完全吸引后得到固体Ⅰ和2.6g固体Ⅱ,固体Ⅱ充分溶解过滤后得到2g固体Ⅲ和滤液,铁、氧化铁和碳酸钙均不溶于水,氧化钙与水反应生成氢氧化钙,氢氧化钙微溶于水,则固体Ⅰ为3g-2.6g=0.4g铁;2g固体Ⅲ与足量稀盐酸反应生成0.44g无色气体,根据质量守恒定律可知,该气体为二氧化碳且固体Ⅲ中含有碳酸钙,设碳酸钙的质量为x,
= 解得x=1g
2g固体Ⅲ中含有1g碳酸钙和2g-1g=1g氧化铁;2.6g-2g=0.6g固体溶解后得到的滤液为氢氧化钙溶液,滤液中的氢氧化钙与过量碳酸钠溶液反应生成的1g固体Ⅳ为碳酸钙,设滤液中氢氧化钙的质量为y,
= 解得y=0.74g
设固体混合物中氧化钙和氢氧化钙的质量分别为m、n,
综上所述,有m+n=0.6g、m+n=0.74g,解得m≈0.44g、n≈0.16g,说明固体混合物中也含有氧化钙和氢氧化钙。
【详解】(1)过滤时,玻璃棒用于向漏斗中添加液体时引流。
(2)分析可知,固体Ⅰ的成分为0.4g铁(Fe),固体Ⅲ的成分为1g碳酸钙(CaCO3)和1g氧化铁(Fe2O3)。
(3)氢氧化钙与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。
(4)分析可知,该固体混合物中一定含有铁(Fe)、氧化铁(Fe2O3)、氧化钙(CaO)、氢氧化钙[Ca(OH)2]和碳酸钙(CaCO3)。
5. Ca(OH)2 CaO CO2
【分析】B是生石灰(常用食品包装中的干燥剂),氧化钙;A、B、C三种白色固体都含有同种金属元素钙元素,C是大理石主要成分,C为碳酸钙;观察ABC转化为钙三角转化关系,氧化钙和水反应生成氢氧化钙,则A为氢氧化钙;D是造成温室效应主要气体,为二氧化碳;E是黑色固体单质,D、E、F都含有同种非金属元素,观察DEF转化为碳三角转化,E为碳、F为一氧化碳;代入检验推理正确;
【详解】(1)化学式为A:Ca(OH)2,B:CaO,D:CO2;
(2)D→C反应为二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水:。
6.(1)
(2)②③/③②
(3)检验纯度
(4)
【分析】A是红色粉末,B是气态氧化物,且A与B在高温条件下反应生成气体C与固体D,则A为氧化铁,B为一氧化碳,C为二氧化碳,D为铁;E为胃酸的主要成分,则E为稀盐酸;D(铁)与E(稀盐酸)反应生成G(气体)与H(盐),则G为氢气,H为氯化亚铁;F为蓝色溶液,且能与D(铁)反应生成H(氯化亚铁)和I,则F为氯化铜,I为铜。
【详解】(1)由分析可知,A为氧化铁,C为二氧化碳,G为氢气,故填、、;
(2)反应①为一氧化碳高温还原氧化铁,不符合置换反应“一种单质置换另一种单质”特点,故①不是置换反应;
②反应为稀盐酸和铁生成氢气和氯化亚铁,方程式为 ,符合置换反应特点,属于置换反应;
③反应为铁和氯化铜反应生成氯化亚铁和铜的反应,方程式为,符合置换反应特点,属于置换反应,故填②③;
(3)G为氢气,氢气在纯度不足时燃烧容易引发爆炸,故点燃氢气之前需要检验纯度,故填检验纯度;
(4)反应①为一氧化碳高温还原氧化铁,方程式为;
反应③为铁和氯化铜反应生成氯化亚铁和铜的反应,方程式为。
7. 改良酸性土壤(等合理即可)
【分析】A-H均为初中化学常见物质,A是一种常见的碱,D为常用食品干燥剂,且D 可转化为A,可推出D为氧化钙,A为氢氧化钙,B是二氧化碳,且B可转化为C,C可转化为氧化钙,可推出C为碳酸钙,E为稀硫酸, F溶液呈浅绿色,且稀硫酸可转化为F,可推出F为硫酸亚铁,G是黑色固体粉末且物质类别为氧化物,G能与稀硫酸反应,且G能转化为H,H溶液呈蓝色,可推出G为氧化铜,H为硫酸铜。
【详解】(1)B是二氧化碳,C为碳酸钙,二氧化碳可与氢氧化钙反应生成碳酸钙和水,该反应的化学方程式为:;
(2)E为稀硫酸,F为硫酸亚铁,稀硫酸可与铁反应生成硫酸亚铁和氢气,该反应的化学方程式为:;
(3)A为氢氧化钙,A在生活中可以改良酸性土壤、配制农药波尔多液等。
8.(1)
(2)氢离子与氢氧根离子结合生成水分子
(3)
(4)用作食品干燥剂
【分析】
B物质俗称生石灰,则B为氧化钙;A能生成B,推测A为碳酸钙,即碳酸钙高温生成B氧化钙和二氧化碳;B能生成C,氧化钙和水反应生成C氢氧化钙;C能生成A,即氢氧化钙和二氧化碳反应生成碳酸钙和水;C和D能相互反应,推测D为碳酸钠,即碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氯化钠;D和E、C和E能相互反应,推测E为盐酸;带入验证符合题意。
【详解】(1)根据分析,A能生成B,推测A为碳酸钙,A→B反应即碳酸钙高温生成氧化钙和二氧化碳,反应的化学方程式为;故填:;
(2)由分析知,C为氢氧化钙,E为盐酸, C与E反应为氢氧化钙和盐酸反应生成氯化钙和水,反应的微观实质是氢离子与氢氧根离子结合生成水分子;故填:氢离子与氢氧根离子结合生成水分子;
(3)由分析知,D为碳酸钠,E为盐酸,D与E反应为碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式是;故填:;
(4)由分析知B为氢氧化钙,C为碳酸钙,B→C反应为氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,在日常生活中的用途是用作食品干燥剂或自热米饭的发热包或干燥剂;故填:用作食品干燥剂。
9.(1)
(2)
(3)
【分析】
F是人体正常生理活动必不可少的一种盐,F就是氯化钠,B与C发生的是中和反应,所以B和C就是盐酸和氢氧化钠,无色液体E就是水,A与B发生的是复分解反应,且会生成氯化钠、水和无色气体D,所以B就是盐酸,C就是氢氧化钠,A就应该是碳酸钠,代入验证,推理正确。
【详解】(1)由分析可知,E就是水,化学式为:;
(2)A与B是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:;
(3)B与C是盐酸和氢氧化钠反应生成氯化钠和水,反应的化学方程式为:。
10.(1)
(2)溶液由无色变为浅绿色
(3) 活性炭
【分析】图甲中A、B、C、D、E、F为初中化学常见的六种不同的物质。其中A可用来改良酸性土壤,可推出A为氢氧化钙,人体胃液中含有D,可推出D为盐酸,E是年产量最高的金属,可推出E为铁,B是一种蓝色溶液,D能转化为B,可推出B为氯化铜,D能转化为C,A能与C相互转化,可推出C为水,C、D、E均能与F相互转化,可推出F为氢气,代入验证,符合题意。
【详解】(1)由分析可知,A为氢氧化钙,化学式为:Ca(OH)2;C为水,化学式为:H2O;
(2)E转化成F的反应为铁和稀盐酸反应生成氯化亚铁和氢气,溶液颜色的变化为:溶液由无色变为浅绿色;
(3)a处是吸附,加入的物质是活性炭,活性炭结构疏松多孔,具有吸附性,可以吸附水中的色素和异味;
水垢的主要成分是碳酸钙和氢氧化镁,碳酸钙能与稀盐酸反应生成氯化钙、二氧化碳和水,氢氧化镁能与稀盐酸反应生成氯化镁和水,故可用稀盐酸除去水垢,氢氧化镁和稀盐酸的反应属于中和反应,该反应的化学方程式为:。
11. 二氧化碳 作导线 Fe2O3+3CO2Fe+3CO2 Fe+CuSO4=FeSO4+Cu(这里用CuCl2或Cu(NO3)2均可)
【分析】B是易与血红蛋白结合的有毒气体,则B为一氧化碳;B、D的组成元素相同,则D为二氧化碳;A为黑色固体,且为单质,还能够反应生成B(一氧化碳)和D(二氧化碳),则A为碳;反应①是工业用赤铁矿炼铁的主要反应,则C为氧化铁,E为铁;F为红色固体,能够由E(铁)反应生成,则F为铜;G为黄色溶液,能够由C(氧化铁)反应生成,则G是一种铁盐溶液。
【详解】(1)由分析可知,D为二氧化碳,故填二氧化碳;
由分析可知,F是铜,铜具有良好的导电性,可作导线,故填作导线。
(2)①反应①氧化铁与一氧化碳在高温的条件下反应生成铁和二氧化碳,故反应的化学方程式写为:Fe2O3+3CO2Fe+3CO2。
②反应②是铁与铜盐溶液反应生成亚铁盐和铜,如铁与硫酸铜反应生成硫酸亚铁和铜,故反应的化学方程式写为:Fe+CuSO4=FeSO4+Cu。
12.(1)灭火等
(2)等
(3)
【分析】B 是人体胃液中常见的酸,则B是盐酸,A 是红色固体,且能与B盐酸反应,则A是氧化铁,E 常用于除油污,则E是氢氧化钠,A和B都能反应生成C,且C能与E氢氧化钠反应,则C可能是二氧化碳,D可能为碳酸钠,综合整体,C二氧化碳,D碳酸钠,符合题意。
【详解】(1)依据分析可知,C为二氧化碳,其用途有做气体肥料,灭火等。
(2)A是氧化铁,碳或一氧化碳都可还原生成二氧化碳,其反应的化学方程式为:或
(3)D是碳酸钠,与氢氧化钙反应可生成E氢氧化钠,其反应的化学方程式为:
13. 干冰 H2O CuSO4+BaCl2=BaSO4↓+CuCl2
【详解】A-F是初中化学常见的化合物,A、B、C都是氧化物,B能使澄清石灰水变浑浊,故B是二氧化碳,F是一种不溶于水的蓝色固体,故F是氢氧化铜,氢氧化铜会转化成C,故C是水, A会转化成二氧化碳、水,故A可能为氧化铜,氧化铜转化成的D可以直接转化成氢氧化铜,E和氢氧化铜可以相互转化,故E是氯化铜,D是硫酸铜,代入验证,推导正确;
(1)由分析可知:B是二氧化碳,固态的二氧化碳俗称干冰;
(2)由分析可知:C是水,故化学式为:H2O;
(3)由分析可知:反应①是硫酸铜转化为氯化铜,反应①可能为硫酸铜溶液和氯化钡溶液反应生成硫酸钡沉淀和氯化铜,故反应的化学方程式为:CuSO4+BaCl2=BaSO4↓+CuCl2。
【点睛】考查物质的推断,根据框图和题目信息进行分析,推导出各物质,并代入验证是否正确。
14.(1)H2O
(2)3CO+Fe2O32Fe+3CO2
(3)置换反应
(4)医疗急救
【分析】A~I都是初中化学中的常见物质。其中A是红棕色金属氧化物,故A为氧化铁,B、E的元素组成相同,I是最常用的溶剂,故I为水,A与B反应可生成D和E,一氧化碳和氧化铁高温下反应生成二氧化碳和铁,故B为一氧化碳,E为二氧化碳,D为铁,C和D(铁)反应可生成F和G,I(水)可转化为G和H,H和B(一氧化碳)可生成E(二氧化碳),水通电分解生成氢气和氧气,一氧化碳和氧气点燃生成二氧化碳,故H为氧气,G为氢气,铁和稀盐酸或稀硫酸反应生成氯化亚铁或硫酸亚铁和氢气,故C为稀盐酸或稀硫酸,F为氯化亚铁或硫酸亚铁,代入验证,推论合理。
【详解】(1)I为水,化学式为H2O;
(2)反应①为一氧化和氧化铁高温下反应生成铁和二氧化碳,化学方程式为:;
(3)反应②为铁和稀盐酸或稀硫酸反应生成氯化亚铁或硫酸亚铁和氢气,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应;
(4)H为氧气,氧气可以供给呼吸,可用于医疗急救。
答案第1页,共2页
答案第1页,共2页
