2024年中考科学重点专题复习-推断题(框架类)(含解析)
文档属性
| 名称 | 2024年中考科学重点专题复习-推断题(框架类)(含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 382.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-04-30 00:00:00 | ||
图片预览




文档简介
2024年中考科学重点专题复习-推断题(框架类)
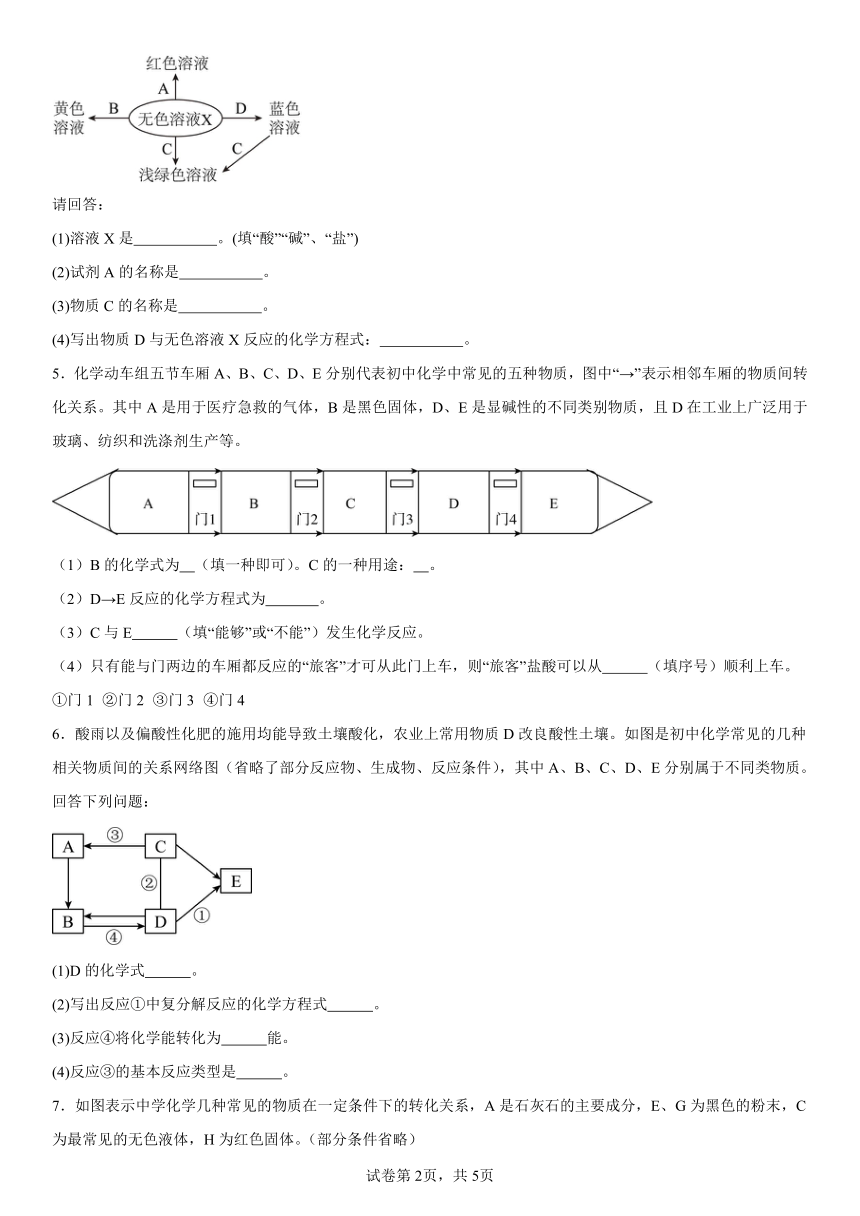
1.A~E均为初中化学常见的物质,它们之间的关系如图所示(部分物质已经略去),已知A是目前世界上年产量最高的金属;B是胃酸的主要成分;C中金属元素的质量分数为40%,其水溶液呈蓝色,常用来配制农药波尔多液;D属于碱;E属于盐。按要求回答下列问题:
(1)写出C的化学式为 。
(2)A与B反应的化学方程式为 ;E转化为D的化学方程式为 。
(3)农业生产上不能用铁制容器配制波尔多液的原因 (用化学方程式表示)。
2.图中A~F是初中化学中常见的物质,其中A、B、C、D、F为五种不同类别的物质,A可由生石灰与水反应制得,B是胃液中帮助消化的成分,E是无色气体,F是红棕色固体。图中“﹣”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
(1)写出化学式:B ,E 。
(2)写出F→ C化学方程式: 。
(3)写出足量的B与F发生反应的现象为 。
3.如图,甲、乙、丙分别是硫酸、氢氧化钙、氯化镁、碳酸钠四种物质中的某一种,“—”表示相连物质的溶液之间能发生化学反应,请回答下列问题:
(1)已知丙物质是一种盐,丙的化学式为 ,反应①的化学方程式为
(2)写出反应④中的现象 (只答一点)
4.如图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”。其中B是铁锈的主要成分,B、C、D分属于不同类别的物质,蓝色溶液可用于配制农药波尔多液。
请回答:
(1)溶液X是 。(填“酸”“碱”、“盐”)
(2)试剂A的名称是 。
(3)物质C的名称是 。
(4)写出物质D与无色溶液X反应的化学方程式: 。
5.化学动车组五节车厢A、B、C、D、E分别代表初中化学中常见的五种物质,图中“→”表示相邻车厢的物质间转化关系。其中A是用于医疗急救的气体,B是黑色固体,D、E是显碱性的不同类别物质,且D在工业上广泛用于玻璃、纺织和洗涤剂生产等。
(1)B的化学式为 (填一种即可)。C的一种用途: 。
(2)D→E反应的化学方程式为 。
(3)C与E (填“能够”或“不能”)发生化学反应。
(4)只有能与门两边的车厢都反应的“旅客”才可从此门上车,则“旅客”盐酸可以从 (填序号)顺利上车。
①门1 ②门2 ③门3 ④门4
6.酸雨以及偏酸性化肥的施用均能导致土壤酸化,农业上常用物质D改良酸性土壤。如图是初中化学常见的几种相关物质间的关系网络图(省略了部分反应物、生成物、反应条件),其中A、B、C、D、E分别属于不同类物质。回答下列问题:
(1)D的化学式 。
(2)写出反应①中复分解反应的化学方程式 。
(3)反应④将化学能转化为 能。
(4)反应③的基本反应类型是 。
7.如图表示中学化学几种常见的物质在一定条件下的转化关系,A是石灰石的主要成分,E、G为黑色的粉末,C为最常见的无色液体,H为红色固体。(部分条件省略)
(1)写出下列物质的化学式:B 。
(2)D物质和CO2反应的化学方程式为 。
(3)B+C→D的化学方程式为 。
(4)F和G反应的实验现象为 。
8.A~G都是初中化学常见的物质,它们的部分反应及转化关系如图所示。其中A为目前世界年产量最高的金属,A、B、C、D物质类别不同,其中C和D中不含相同的元素,E、F的组成元素相同。图中“→”表示转化关系,“-”表示相互反应关系(部分物质和反应条件未标出)。请完成下列问题:
(1)写出B的化学式 。
(2)A和D反应的基本类型是 ,C和D的反应化学方程式 。
(3)写出C和E反应的化学方程式 。
(4)写出F→E反应的化学方程式 ,该反应伴随的能量变化是 。(填“放热”或“吸热)
(5)请你从微观的视角说明A与B反应的实质 。
9.A~E为初中化学五种不同类别的常见物质。已知C含有两种元素,E为世界年产量最高的金属,B的俗称是火碱或烧碱,D为红棕色固体。“—”表示相连的物质能相互反应,“→”表示一种物质转化为另一种物质,请回答下列问题:
(1)物质E是 (填化学式)
(2)写出B物质的一点用途 。
(3)写出下列反应的化学方程式:C+E: D→E: 。
10.A、B、C、D、E、F、G、H、I都是初中化学常见的物质,其中B为紫红色固体单质,H是氧化物E、H均为黑色固体,F是一种无色气体,它们之间有如图转化关系(所发生的反应均恰好完全,部分生成物省去),根据转化关系图回答问题:
(1)A (写物质名称);
(2)①写出F→G (填“一定”或 “不一定”)是放热反应;
②写出C→D反应观察到的现象是 。
③写出H→C的化学方程式 。
11.A~H是初中化学常见的物质,其中A是大理石的主要成分,H为红褐色沉淀,E→C的反应是工业炼铁的常用反应,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.
(1)写出下列物质的化学式:A ,G ,H .
(2)化学反应常伴有能量变化,物质B与水反应时会 (“吸收”或“放出”)热量.
(3)写出D→F的化学方程式: .
(4)写出E→C的化学方程式: .
12.有一包不纯的NaOH粉末,可能含有Na2SO4、NaCl、CuCl2、NH4Cl、Na2CO3、MgCl2中的一种或几种,为分析含有的杂质,现进行如下实验。
(1)取样溶于水,无固体残留,得无色溶液X。则此粉末中一定不含 。
(2)取溶液X适量,微热,无氨味。则此粉末中一定不含 。
(3)另取溶液X适量,滴加BaCl2溶液,有白色沉淀,再加λ足量稀HNO3,沉淀全部溶解,则此粉末中一定含有 。
(4)为进一步探究该粉末的成分,可另取溶液X适量,滴加过量M溶液,再滴加N溶液,观察现象。M、N可能分别为 (选填序号)。
a.硝酸钡、硝酸银 b.稀硝酸、硝酸银 c.氯化钡、硝酸银
13.已知 A—F 均为初中化学常 的物质。其中 E 为鸡蛋壳的主要成分,F 由两种元素组成,且 A, B,F 为三种不同类别的物质。请根据如图所示的转化关系(图中反应条件,部分反应物和 成物均已略去), 回答相关问题:
(1)写出下列物质的化学式:E ;
(2)写出 C 与 F 反应的化学 程式: 。
14.木炭、氢气、一氧化碳具有相似的化学性质,如都能燃烧,都能将某些金属从它们的氧化物中还原出来。现有A、B、C 、D、E五种常见的物质,常温下A、E是气态单质,C是液体,D是一种紫红色金属单质,它们之间的转化关系如图所示,反应条件均已略去。
(1)E的化学式是 。
(2)反应A+B→C+D的化学方程式是 。
(3)用А的单质作燃料用很多有优点,请列举一条 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1. CuSO4
【分析】A是目前世界上年产量最高的金属,A是铁;B是胃酸的主要成分,B是盐酸;C中金属元素的质量分数为40%,其水溶液呈蓝色,常用来配制农药波尔多液,C是CuSO4。D属于碱,D可以是氢氧化钠,E属于盐,且能与盐酸反应、与氢氧化钠相互转化,则E是碳酸钠。将推出的各种物质代入转化关系中进行验证,推断正确。
【详解】(1)C是硫酸铜,化学式为CuSO4。
(2)A与B反应的化学方程式为:;E转化为D的化学方程式为:。
(3)农业生产上不能用铁制容器配制波尔多液的原因是铁制容器能与硫酸铜溶液反应,铁制容器会被腐蚀,反应的化学方程式为:
【点睛】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
2. HCl CO2 红棕色固体逐渐减少至消失,溶液由无色变黄色
【分析】由题意可知,A可由生石灰和水反应制得,则A为氢氧化钙;B是胃液中帮助消化的成分。则B为盐酸;由于F是红色固体,能与盐酸反应,能转化为无色的气体,则F为氧化铁;氧化铁能与一氧化碳在高温条件先下反应生成了铁和二氧化碳,则E为二氧化碳,C为铁;氢氧化钙能与二氧化碳等反应转化为碳酸钙,碳酸钙能与盐酸反应等转化为二氧化碳,代入题中验证,符合题意。
【详解】由分析可知(1)B的化学式是HCl,E的化学式是CO2;
(2)氧化铁能与一氧化碳在高温条件下反应生成了衣蛾和二氧化碳,F→C的化学方程式是:;
(3)F是氧化铁,B是稀盐酸,两者反应的现象为红棕色固体逐渐减少至消失,溶液由无色变黄色。
【点睛】本题为框图型物质推断题,完成此类题目,关键是根据题干提供的信息结合框图,找准解题突破口,直接得出物质的化学式,然后顺推或逆推或从两边向中间推得出其他物质的化学式。
3. Na2CO3 Ca(OH)2+CO2=CaCO3↓+H2O 产生大量气泡
【分析】二氧化碳能与四种物质中的氢氧化钙反应生成碳酸钙沉淀和水,所以甲为氢氧化钙;锌能与四种物质中的硫酸反应生成硫酸锌和氢气,所以乙为硫酸;硫酸与氢氧化钙均能与另外两种物质中的碳酸钠反应,所以丙为碳酸钠。
【详解】(1)由分析可知,丙为碳酸钠,其化学式为Na2CO3,故填Na2CO3;
反应①是二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故反应的化学方程式写为:Ca(OH)2+CO2=CaCO3↓+H2O。
(2)反应④是锌与硫酸反应生成硫酸锌和氢气,观察到的现象是产生大量气泡,故填产生大量气泡。
4.(1)酸
(2)石蕊溶液
(3)铁
(4)
【分析】黄色溶液为含有Fe3+的溶液,且B为铁锈的主要成分氧化铁,说明X溶液为酸溶液,蓝色溶液可用于配制农药波尔多液,其为硫酸铜溶液,所以X溶液为稀硫酸 ; 浅绿色溶液为含有Fe2+的溶液, 由于B、C、E为不同类物质,B氧化铁属于氧化物,所以C为单质铁,D属于碱类,为氢氧化铜;酸性溶液能使紫色的石蕊溶液变红,故A为石蕊溶液。
【详解】(1)X溶液为稀硫酸,故填:酸。
(2)试剂A的名称为石蕊溶液。
(3)物质C的名称为铁。
(4)D物质为氢氧化铜,与硫酸反应生成硫酸铜和水,反应方程式为:。
5. CuO(或Fe3O4) 绿色植物的光合作用(或灭火等合理答案) 能 ④
【分析】化学动车组五节车厢A、B、C、D、E分别代表初中化学中常见的五种物质,其中A是用于医疗急救的气体,可推出A为氧气,B是黑色固体,且氧气能转化为B,可推出B为氧化铜,B能转化为C,C能转化为D,D、E是显碱性的不同类别物质,且D在工业上广泛用于玻璃、纺织和洗涤剂生产等,可推出D为碳酸钠,则C为二氧化碳,E为氢氧化钠,代入验证,符合题意。
【详解】(1)由分析可知,B是氧化铜,化学式为:CuO;
C为二氧化碳,二氧化碳不燃烧、也不支持燃烧,可用于灭火;二氧化碳是光合作用的原料,可用于绿色植物光合作用;
(2)D→E反应为碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,该反应的化学方程式为:;
(3)由分析可知,C是二氧化碳。E是氢氧化钠,二氧化碳能与氢氧化钠反应生成碳酸钠和水;
(4)盐酸与氧气不反应;盐酸与氧化铜反应生成氯化铜和水;盐酸与二氧化碳不反应;盐酸与碳酸钠反应生成氯化钠、二氧化碳和水;盐酸能与氢氧化钠反应生成氯化钠和水,故“旅客”盐酸可以从门4顺利上车。
故填:④。
6.(1)Ca(OH)2
(2)Ca(OH)2+H2CO3=CaCO3↓+2H2O
(3)热
(4)置换反应
【分析】农业上常用物质D改良酸性土壤,可知D是Ca(OH)2,又中A、B、C、D、E分别属于不同类别的物质,且B可以与氢氧化钙相互转化,B可以为水,水与氧化钙生成氢氧化钙,氢氧化钙与盐酸中和生成氯化钙和水,C可以与D反应生成E且C、D、E属于不同类别的物质,C可以是碳酸,碳酸与氢氧化钙反应生成E碳酸钙,C可以生成A,A可以生成B水,碳酸与活泼金属反应生成单质氢气,氢气点燃生成水,A可以是氢气,代入验证,符合题意。
【详解】(1)根据分析可知:A为H2;B为H2O;C为H2CO3;D为:Ca(OH)2;E为:CaCO3,所以D的化学式为Ca(OH)2;
(2)反应①是D生成E,即Ca(OH)2和H2CO3或Na2CO3等物质反应可以生成CaCO3,所以①中复分解反应的化学方程式是Ca(OH)2+H2CO3=CaCO3↓+2H2O等;
(3)反应④是将H2O转化为Ca(OH)2,放出大量的热,所以反应④是将化学能转化为热能;
(4)反应③是C碳酸转化为A氢气,所以反应③的反应可能是金属和酸反应,所以反应③的基本反应类型是置换反应。
7.(1)CaO
(2)Ca(OH)2+CO2=CaCO3↓+H2O
(3)CaO+H2O=Ca(OH)2
(4)黑色固体变成红色
【分析】A是石灰石的主要成分,A在高温条件下分解生成二氧化碳和B,则A是碳酸钙,B是氧化钙;C为最常见的无色液体,氧化钙和C反应生成D,则C是水,D是氢氧化钙;二氧化碳和E反应生成F,F和G反应生成二氧化碳和H,E、G为黑色的粉末,H为红色固体,则E是碳,F是一氧化碳,G是氧化铜,H是铜,代入验证,推断正确。
【详解】(1)由分析可知,B是氧化钙,其化学式为CaO。
(2)D物质是氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,该反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O。
(3)B+C→D的反应为氧化钙和水反应生成氢氧化钙,该反应的化学方程式为CaO+H2O=Ca(OH)2。
(4)F和G的反应为一氧化碳和氧化铜在加热的条件下反应生成铜和二氧化碳,该反应的实验现象为黑色固体变成红色。
【点睛】本题属于物质的推断题,首先根据题眼信息推出部分物质,再结合框图转化关系推出剩余物质,最后代入验证,若推断正确,则进行分析解答。
8.(1)AgNO3
(2) 置换反应
(3)(合理即可)
(4) 吸热
(5)
【分析】A~G都是初中化学常见的物质,其中A为目前世界年产量最高的金属,可推出A为铁,A、B、C、D物质类别不同,其中C和D中不含相同的元素,C能转化为A,D能与A、C反应,可推出C为氧化铁,D为盐酸,A能与B反应,B能与D反应,可推出B为硝酸银,E、F的组成元素相同,E能与F相互转化,E能与C反应,D能转化为F,可推出E为一氧化碳,F为二氧化碳,G能转化为E,G能与F反应,可推出G为碳,代入验证,符合题意。
【详解】(1)由分析可知,B为硝酸银,化学式为:AgNO3;
(2)A和D的反应为铁和稀盐酸反应生成氯化亚铁和氢气,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;
C和D的反应为氧化铁和稀盐酸反应生成氯化铁和水,该反应的化学方程式为:;
(3)C和E的反应为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:;
(4)F→E反应为二氧化碳和碳在高温下反应生成一氧化碳,该反应的化学方程式为:;
该反应伴随的能量变化是吸热;
(5)A与B的反应为铁和硝酸银反应生成硝酸亚铁和银,反应实质是。
9.(1)Fe
(2)作干燥剂
(3) Fe+2HCl=FeCl2+H2↑
【分析】E为世界年产量最高的金属,则E为铁;B的俗称是火碱或烧碱,则B为氢氧化钠;D为红棕色固体,且能够反应生成E(铁),则D为氧化铁;A~E为初中化学五种不同类别的常见物质,C与B(氢氧化钠)、D(氧化铁)、E(铁)都能发生反应,则C为酸,可以是稀盐酸;A能够与B(氢氧化钠)、E(铁)反应,还能够由C(稀盐酸)反应生成,则A为氯化铜。
【详解】(1)由分析可知,E为铁,其化学式为Fe,故填Fe。
(2)由分析可知,B为氢氧化钠,氢氧化钠固体具有潮解的性质,可用作干燥剂,故填作干燥剂。
(3)由分析可知,C为稀盐酸,E为铁,则C与E发生的反应是铁与稀盐酸反应生成氯化亚铁和氢气,故反应的化学方程式写为:Fe+2HCl=FeCl2+H2↑;
D为氧化铁,E为铁,则D→E的反应可以是氧化铁与一氧化碳在高温的条件下反应生成铁和二氧化碳
10.(1)H2
(2) 不一定 生成蓝色沉淀
【分析】A、B、C、D、E、F、G、H、I都是初中化学常见的物质,其中B为紫红色固体单质,可推出B为铜,B能与氧气在加热的条件下反应生成H,H为氧化物,可推出H为氧化铜,F是一种无色气体,F能与氧化铁在高温下反应生成E,E能与盐酸反应生成A,可推出F为一氧化碳,E为铁,A为氢气,H能与稀硫酸反应生成C,可推出C为硫酸铜,硫酸铜能与氢氧化钠反应生成D,D可能是氢氧化铜;F能与氧气在点燃的条件下反应生成G,可推出G为二氧化碳,G能与澄清石灰水反应生成I,I可能是碳酸钙,代入验证,符合题意。
【详解】(1)由分析可知,A为氢气,化学式为:H2;
(2)①F→G可以为一氧化碳燃烧生成二氧化碳,该反应是放热反应,也可以是一氧化碳和氧化铜在加热的条件下反应生成铜和二氧化碳,属于吸热反应,故不一定是放热反应;
②C→D反应为硫酸铜和氢氧化钠反应生成氢氧化铜和硫酸钠,现象为:有蓝色沉淀生成;
③H→C的反应为氧化铜和稀硫酸反应生成硫酸铜和水,该反应的化学方程式为:。
11.(1) CaCO3 Fe2(SO4)3 Fe(OH)3
(2)放出
(3)
【分析】A在高温条件下发生分解反应,可判断为碳酸钙;生成物B能与水反应生成的D会继续与碳酸钠反应,故可判断B应为CaO,D自然为氢氧化钙;C为二氧化碳;H为红褐色沉淀,可判断为氢氧化铁,E→C的反应是工业炼铁的常用反应,故可判断E为氧化铁,G自然为硫酸铁,F为氢氧化钠。
【详解】(1)A为碳酸钙,化学式为:CaCO3;G为硫酸铁,化学式为:Fe2(SO4)3;H为红褐色沉淀,为氢氧化铁,化学式为:Fe(OH)3;
(2)化学反应常伴有能量变化,物质B氧化钙与水反应时会放出热量;
(3)D为氢氧化钙,F为氢氧化钠,故D→F的化学方程式: ;
12.(1)CuCl2、MgCl2
(2)NH4Cl
(3)
(4)b
【详解】(1)取样溶于水,无固体残留,得无色溶液X,则此粉末中一定不含CuCl2、MgCl2;因为氯化铜与氢氧化钠反应生成的氢氧化铜是蓝色沉淀,氯化镁与氢氧化钠反应生成的氢氧化镁是白色沉淀;
(2)取溶液X适量,微热,无氨味,则此粉末中一定不含NH4Cl,因为氯化铵与氢氧化钠反应生成的氨水受热会分解生成氨气;
(3)另取溶液X适量,滴加BaCl2溶液,有白色沉淀,再加入足量稀HNO3,沉淀全部溶解,测此粉末中一定不含,一定含;因为碳酸钠与氯化钡反应生成的碳酸钡沉淀能溶于硝酸,而硫酸钠与氯化钡反应生成的硫酸钡不溶于硝酸
(4)由于有碳酸钡生成,说明有碳酸钠存在,由于固体全部溶解,所以不能含有氯化镁,因此可知现在粉末中有氢氧化钠、碳酸钠,不含有氯化铜、氯化铵、氯化镁,剩余氯化钠,需要验证是否存在,氯化钠可以利用硝酸银验证,观察白色沉淀,而碳酸钠和氢氧化钠会影响实验,所以先去除,可以选择硝酸,因此先加硝酸后加入硝酸银,验证氯化钠是否存在;
故填:b。
13.
【分析】E为鸡蛋壳的主要成分,故E是碳酸钙;F由两种元素组成,能和碳酸钙反应,故F是盐酸;碳酸钙和D互相转化,盐酸也可以生成D,故D是二氧化碳;A和二氧化碳互相转化,则A可以是一氧化碳,一氧化碳燃烧或者与金属氧化物反应会生成二氧化碳,二氧化碳和碳高温下化合会生成一氧化碳,一氧化碳属于氧化物;B可以生成一氧化碳、二氧化碳,故B可以是碳或者氧气,碳或者氧气都属于单质,碳在氧气中充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳;若B是碳,C可以是铁等排在氢之前的金属,如碳和铁的氧化物高温下生成铁和二氧化碳,铁可以和盐酸反应生成氯化亚铁和氢气;若B是氧气,则C可以是某些金属氧化物,如氧化铜,氧化铜和盐酸反应生成氯化铜和水;代入验证即可;
【详解】(1)E为碳酸钙,化学式为;
(2)C 与 F 反应,可以是铁与稀盐酸反应生成氯化亚铁和氢气,反应的化学 程式为:。
14. O2 无污染/燃烧值高/资源广泛(合理即可)
【分析】D是一种紫红色金属单质,故D为铜,常温下A、E是气态单质,C是液体,可推测A为氢气,E为氧气,C为水,铜与氧气反应生成氧化铜,故B为氧化铜,氢气和氧化铜反应生成铜和水,代入框图,推测正确。
【详解】(1)根据分析,E为氧气,化学式为O2。
(2)反应A+B→C+D是氢气和氧化铜反应生成铜和水
(3)用氢气作为燃料的优点很多,氢气燃烧产物是水,不污染环境;氢气的燃烧值高;工业上制取氢气是通过电解水得到的,而地球上水资源丰富,可以从水中提取氢气,说明资源广泛。
答案第1页,共2页
答案第1页,共2页
1.A~E均为初中化学常见的物质,它们之间的关系如图所示(部分物质已经略去),已知A是目前世界上年产量最高的金属;B是胃酸的主要成分;C中金属元素的质量分数为40%,其水溶液呈蓝色,常用来配制农药波尔多液;D属于碱;E属于盐。按要求回答下列问题:
(1)写出C的化学式为 。
(2)A与B反应的化学方程式为 ;E转化为D的化学方程式为 。
(3)农业生产上不能用铁制容器配制波尔多液的原因 (用化学方程式表示)。
2.图中A~F是初中化学中常见的物质,其中A、B、C、D、F为五种不同类别的物质,A可由生石灰与水反应制得,B是胃液中帮助消化的成分,E是无色气体,F是红棕色固体。图中“﹣”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
(1)写出化学式:B ,E 。
(2)写出F→ C化学方程式: 。
(3)写出足量的B与F发生反应的现象为 。
3.如图,甲、乙、丙分别是硫酸、氢氧化钙、氯化镁、碳酸钠四种物质中的某一种,“—”表示相连物质的溶液之间能发生化学反应,请回答下列问题:
(1)已知丙物质是一种盐,丙的化学式为 ,反应①的化学方程式为
(2)写出反应④中的现象 (只答一点)
4.如图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”。其中B是铁锈的主要成分,B、C、D分属于不同类别的物质,蓝色溶液可用于配制农药波尔多液。
请回答:
(1)溶液X是 。(填“酸”“碱”、“盐”)
(2)试剂A的名称是 。
(3)物质C的名称是 。
(4)写出物质D与无色溶液X反应的化学方程式: 。
5.化学动车组五节车厢A、B、C、D、E分别代表初中化学中常见的五种物质,图中“→”表示相邻车厢的物质间转化关系。其中A是用于医疗急救的气体,B是黑色固体,D、E是显碱性的不同类别物质,且D在工业上广泛用于玻璃、纺织和洗涤剂生产等。
(1)B的化学式为 (填一种即可)。C的一种用途: 。
(2)D→E反应的化学方程式为 。
(3)C与E (填“能够”或“不能”)发生化学反应。
(4)只有能与门两边的车厢都反应的“旅客”才可从此门上车,则“旅客”盐酸可以从 (填序号)顺利上车。
①门1 ②门2 ③门3 ④门4
6.酸雨以及偏酸性化肥的施用均能导致土壤酸化,农业上常用物质D改良酸性土壤。如图是初中化学常见的几种相关物质间的关系网络图(省略了部分反应物、生成物、反应条件),其中A、B、C、D、E分别属于不同类物质。回答下列问题:
(1)D的化学式 。
(2)写出反应①中复分解反应的化学方程式 。
(3)反应④将化学能转化为 能。
(4)反应③的基本反应类型是 。
7.如图表示中学化学几种常见的物质在一定条件下的转化关系,A是石灰石的主要成分,E、G为黑色的粉末,C为最常见的无色液体,H为红色固体。(部分条件省略)
(1)写出下列物质的化学式:B 。
(2)D物质和CO2反应的化学方程式为 。
(3)B+C→D的化学方程式为 。
(4)F和G反应的实验现象为 。
8.A~G都是初中化学常见的物质,它们的部分反应及转化关系如图所示。其中A为目前世界年产量最高的金属,A、B、C、D物质类别不同,其中C和D中不含相同的元素,E、F的组成元素相同。图中“→”表示转化关系,“-”表示相互反应关系(部分物质和反应条件未标出)。请完成下列问题:
(1)写出B的化学式 。
(2)A和D反应的基本类型是 ,C和D的反应化学方程式 。
(3)写出C和E反应的化学方程式 。
(4)写出F→E反应的化学方程式 ,该反应伴随的能量变化是 。(填“放热”或“吸热)
(5)请你从微观的视角说明A与B反应的实质 。
9.A~E为初中化学五种不同类别的常见物质。已知C含有两种元素,E为世界年产量最高的金属,B的俗称是火碱或烧碱,D为红棕色固体。“—”表示相连的物质能相互反应,“→”表示一种物质转化为另一种物质,请回答下列问题:
(1)物质E是 (填化学式)
(2)写出B物质的一点用途 。
(3)写出下列反应的化学方程式:C+E: D→E: 。
10.A、B、C、D、E、F、G、H、I都是初中化学常见的物质,其中B为紫红色固体单质,H是氧化物E、H均为黑色固体,F是一种无色气体,它们之间有如图转化关系(所发生的反应均恰好完全,部分生成物省去),根据转化关系图回答问题:
(1)A (写物质名称);
(2)①写出F→G (填“一定”或 “不一定”)是放热反应;
②写出C→D反应观察到的现象是 。
③写出H→C的化学方程式 。
11.A~H是初中化学常见的物质,其中A是大理石的主要成分,H为红褐色沉淀,E→C的反应是工业炼铁的常用反应,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.
(1)写出下列物质的化学式:A ,G ,H .
(2)化学反应常伴有能量变化,物质B与水反应时会 (“吸收”或“放出”)热量.
(3)写出D→F的化学方程式: .
(4)写出E→C的化学方程式: .
12.有一包不纯的NaOH粉末,可能含有Na2SO4、NaCl、CuCl2、NH4Cl、Na2CO3、MgCl2中的一种或几种,为分析含有的杂质,现进行如下实验。
(1)取样溶于水,无固体残留,得无色溶液X。则此粉末中一定不含 。
(2)取溶液X适量,微热,无氨味。则此粉末中一定不含 。
(3)另取溶液X适量,滴加BaCl2溶液,有白色沉淀,再加λ足量稀HNO3,沉淀全部溶解,则此粉末中一定含有 。
(4)为进一步探究该粉末的成分,可另取溶液X适量,滴加过量M溶液,再滴加N溶液,观察现象。M、N可能分别为 (选填序号)。
a.硝酸钡、硝酸银 b.稀硝酸、硝酸银 c.氯化钡、硝酸银
13.已知 A—F 均为初中化学常 的物质。其中 E 为鸡蛋壳的主要成分,F 由两种元素组成,且 A, B,F 为三种不同类别的物质。请根据如图所示的转化关系(图中反应条件,部分反应物和 成物均已略去), 回答相关问题:
(1)写出下列物质的化学式:E ;
(2)写出 C 与 F 反应的化学 程式: 。
14.木炭、氢气、一氧化碳具有相似的化学性质,如都能燃烧,都能将某些金属从它们的氧化物中还原出来。现有A、B、C 、D、E五种常见的物质,常温下A、E是气态单质,C是液体,D是一种紫红色金属单质,它们之间的转化关系如图所示,反应条件均已略去。
(1)E的化学式是 。
(2)反应A+B→C+D的化学方程式是 。
(3)用А的单质作燃料用很多有优点,请列举一条 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1. CuSO4
【分析】A是目前世界上年产量最高的金属,A是铁;B是胃酸的主要成分,B是盐酸;C中金属元素的质量分数为40%,其水溶液呈蓝色,常用来配制农药波尔多液,C是CuSO4。D属于碱,D可以是氢氧化钠,E属于盐,且能与盐酸反应、与氢氧化钠相互转化,则E是碳酸钠。将推出的各种物质代入转化关系中进行验证,推断正确。
【详解】(1)C是硫酸铜,化学式为CuSO4。
(2)A与B反应的化学方程式为:;E转化为D的化学方程式为:。
(3)农业生产上不能用铁制容器配制波尔多液的原因是铁制容器能与硫酸铜溶液反应,铁制容器会被腐蚀,反应的化学方程式为:
【点睛】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
2. HCl CO2 红棕色固体逐渐减少至消失,溶液由无色变黄色
【分析】由题意可知,A可由生石灰和水反应制得,则A为氢氧化钙;B是胃液中帮助消化的成分。则B为盐酸;由于F是红色固体,能与盐酸反应,能转化为无色的气体,则F为氧化铁;氧化铁能与一氧化碳在高温条件先下反应生成了铁和二氧化碳,则E为二氧化碳,C为铁;氢氧化钙能与二氧化碳等反应转化为碳酸钙,碳酸钙能与盐酸反应等转化为二氧化碳,代入题中验证,符合题意。
【详解】由分析可知(1)B的化学式是HCl,E的化学式是CO2;
(2)氧化铁能与一氧化碳在高温条件下反应生成了衣蛾和二氧化碳,F→C的化学方程式是:;
(3)F是氧化铁,B是稀盐酸,两者反应的现象为红棕色固体逐渐减少至消失,溶液由无色变黄色。
【点睛】本题为框图型物质推断题,完成此类题目,关键是根据题干提供的信息结合框图,找准解题突破口,直接得出物质的化学式,然后顺推或逆推或从两边向中间推得出其他物质的化学式。
3. Na2CO3 Ca(OH)2+CO2=CaCO3↓+H2O 产生大量气泡
【分析】二氧化碳能与四种物质中的氢氧化钙反应生成碳酸钙沉淀和水,所以甲为氢氧化钙;锌能与四种物质中的硫酸反应生成硫酸锌和氢气,所以乙为硫酸;硫酸与氢氧化钙均能与另外两种物质中的碳酸钠反应,所以丙为碳酸钠。
【详解】(1)由分析可知,丙为碳酸钠,其化学式为Na2CO3,故填Na2CO3;
反应①是二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故反应的化学方程式写为:Ca(OH)2+CO2=CaCO3↓+H2O。
(2)反应④是锌与硫酸反应生成硫酸锌和氢气,观察到的现象是产生大量气泡,故填产生大量气泡。
4.(1)酸
(2)石蕊溶液
(3)铁
(4)
【分析】黄色溶液为含有Fe3+的溶液,且B为铁锈的主要成分氧化铁,说明X溶液为酸溶液,蓝色溶液可用于配制农药波尔多液,其为硫酸铜溶液,所以X溶液为稀硫酸 ; 浅绿色溶液为含有Fe2+的溶液, 由于B、C、E为不同类物质,B氧化铁属于氧化物,所以C为单质铁,D属于碱类,为氢氧化铜;酸性溶液能使紫色的石蕊溶液变红,故A为石蕊溶液。
【详解】(1)X溶液为稀硫酸,故填:酸。
(2)试剂A的名称为石蕊溶液。
(3)物质C的名称为铁。
(4)D物质为氢氧化铜,与硫酸反应生成硫酸铜和水,反应方程式为:。
5. CuO(或Fe3O4) 绿色植物的光合作用(或灭火等合理答案) 能 ④
【分析】化学动车组五节车厢A、B、C、D、E分别代表初中化学中常见的五种物质,其中A是用于医疗急救的气体,可推出A为氧气,B是黑色固体,且氧气能转化为B,可推出B为氧化铜,B能转化为C,C能转化为D,D、E是显碱性的不同类别物质,且D在工业上广泛用于玻璃、纺织和洗涤剂生产等,可推出D为碳酸钠,则C为二氧化碳,E为氢氧化钠,代入验证,符合题意。
【详解】(1)由分析可知,B是氧化铜,化学式为:CuO;
C为二氧化碳,二氧化碳不燃烧、也不支持燃烧,可用于灭火;二氧化碳是光合作用的原料,可用于绿色植物光合作用;
(2)D→E反应为碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,该反应的化学方程式为:;
(3)由分析可知,C是二氧化碳。E是氢氧化钠,二氧化碳能与氢氧化钠反应生成碳酸钠和水;
(4)盐酸与氧气不反应;盐酸与氧化铜反应生成氯化铜和水;盐酸与二氧化碳不反应;盐酸与碳酸钠反应生成氯化钠、二氧化碳和水;盐酸能与氢氧化钠反应生成氯化钠和水,故“旅客”盐酸可以从门4顺利上车。
故填:④。
6.(1)Ca(OH)2
(2)Ca(OH)2+H2CO3=CaCO3↓+2H2O
(3)热
(4)置换反应
【分析】农业上常用物质D改良酸性土壤,可知D是Ca(OH)2,又中A、B、C、D、E分别属于不同类别的物质,且B可以与氢氧化钙相互转化,B可以为水,水与氧化钙生成氢氧化钙,氢氧化钙与盐酸中和生成氯化钙和水,C可以与D反应生成E且C、D、E属于不同类别的物质,C可以是碳酸,碳酸与氢氧化钙反应生成E碳酸钙,C可以生成A,A可以生成B水,碳酸与活泼金属反应生成单质氢气,氢气点燃生成水,A可以是氢气,代入验证,符合题意。
【详解】(1)根据分析可知:A为H2;B为H2O;C为H2CO3;D为:Ca(OH)2;E为:CaCO3,所以D的化学式为Ca(OH)2;
(2)反应①是D生成E,即Ca(OH)2和H2CO3或Na2CO3等物质反应可以生成CaCO3,所以①中复分解反应的化学方程式是Ca(OH)2+H2CO3=CaCO3↓+2H2O等;
(3)反应④是将H2O转化为Ca(OH)2,放出大量的热,所以反应④是将化学能转化为热能;
(4)反应③是C碳酸转化为A氢气,所以反应③的反应可能是金属和酸反应,所以反应③的基本反应类型是置换反应。
7.(1)CaO
(2)Ca(OH)2+CO2=CaCO3↓+H2O
(3)CaO+H2O=Ca(OH)2
(4)黑色固体变成红色
【分析】A是石灰石的主要成分,A在高温条件下分解生成二氧化碳和B,则A是碳酸钙,B是氧化钙;C为最常见的无色液体,氧化钙和C反应生成D,则C是水,D是氢氧化钙;二氧化碳和E反应生成F,F和G反应生成二氧化碳和H,E、G为黑色的粉末,H为红色固体,则E是碳,F是一氧化碳,G是氧化铜,H是铜,代入验证,推断正确。
【详解】(1)由分析可知,B是氧化钙,其化学式为CaO。
(2)D物质是氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,该反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O。
(3)B+C→D的反应为氧化钙和水反应生成氢氧化钙,该反应的化学方程式为CaO+H2O=Ca(OH)2。
(4)F和G的反应为一氧化碳和氧化铜在加热的条件下反应生成铜和二氧化碳,该反应的实验现象为黑色固体变成红色。
【点睛】本题属于物质的推断题,首先根据题眼信息推出部分物质,再结合框图转化关系推出剩余物质,最后代入验证,若推断正确,则进行分析解答。
8.(1)AgNO3
(2) 置换反应
(3)(合理即可)
(4) 吸热
(5)
【分析】A~G都是初中化学常见的物质,其中A为目前世界年产量最高的金属,可推出A为铁,A、B、C、D物质类别不同,其中C和D中不含相同的元素,C能转化为A,D能与A、C反应,可推出C为氧化铁,D为盐酸,A能与B反应,B能与D反应,可推出B为硝酸银,E、F的组成元素相同,E能与F相互转化,E能与C反应,D能转化为F,可推出E为一氧化碳,F为二氧化碳,G能转化为E,G能与F反应,可推出G为碳,代入验证,符合题意。
【详解】(1)由分析可知,B为硝酸银,化学式为:AgNO3;
(2)A和D的反应为铁和稀盐酸反应生成氯化亚铁和氢气,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;
C和D的反应为氧化铁和稀盐酸反应生成氯化铁和水,该反应的化学方程式为:;
(3)C和E的反应为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:;
(4)F→E反应为二氧化碳和碳在高温下反应生成一氧化碳,该反应的化学方程式为:;
该反应伴随的能量变化是吸热;
(5)A与B的反应为铁和硝酸银反应生成硝酸亚铁和银,反应实质是。
9.(1)Fe
(2)作干燥剂
(3) Fe+2HCl=FeCl2+H2↑
【分析】E为世界年产量最高的金属,则E为铁;B的俗称是火碱或烧碱,则B为氢氧化钠;D为红棕色固体,且能够反应生成E(铁),则D为氧化铁;A~E为初中化学五种不同类别的常见物质,C与B(氢氧化钠)、D(氧化铁)、E(铁)都能发生反应,则C为酸,可以是稀盐酸;A能够与B(氢氧化钠)、E(铁)反应,还能够由C(稀盐酸)反应生成,则A为氯化铜。
【详解】(1)由分析可知,E为铁,其化学式为Fe,故填Fe。
(2)由分析可知,B为氢氧化钠,氢氧化钠固体具有潮解的性质,可用作干燥剂,故填作干燥剂。
(3)由分析可知,C为稀盐酸,E为铁,则C与E发生的反应是铁与稀盐酸反应生成氯化亚铁和氢气,故反应的化学方程式写为:Fe+2HCl=FeCl2+H2↑;
D为氧化铁,E为铁,则D→E的反应可以是氧化铁与一氧化碳在高温的条件下反应生成铁和二氧化碳
10.(1)H2
(2) 不一定 生成蓝色沉淀
【分析】A、B、C、D、E、F、G、H、I都是初中化学常见的物质,其中B为紫红色固体单质,可推出B为铜,B能与氧气在加热的条件下反应生成H,H为氧化物,可推出H为氧化铜,F是一种无色气体,F能与氧化铁在高温下反应生成E,E能与盐酸反应生成A,可推出F为一氧化碳,E为铁,A为氢气,H能与稀硫酸反应生成C,可推出C为硫酸铜,硫酸铜能与氢氧化钠反应生成D,D可能是氢氧化铜;F能与氧气在点燃的条件下反应生成G,可推出G为二氧化碳,G能与澄清石灰水反应生成I,I可能是碳酸钙,代入验证,符合题意。
【详解】(1)由分析可知,A为氢气,化学式为:H2;
(2)①F→G可以为一氧化碳燃烧生成二氧化碳,该反应是放热反应,也可以是一氧化碳和氧化铜在加热的条件下反应生成铜和二氧化碳,属于吸热反应,故不一定是放热反应;
②C→D反应为硫酸铜和氢氧化钠反应生成氢氧化铜和硫酸钠,现象为:有蓝色沉淀生成;
③H→C的反应为氧化铜和稀硫酸反应生成硫酸铜和水,该反应的化学方程式为:。
11.(1) CaCO3 Fe2(SO4)3 Fe(OH)3
(2)放出
(3)
【分析】A在高温条件下发生分解反应,可判断为碳酸钙;生成物B能与水反应生成的D会继续与碳酸钠反应,故可判断B应为CaO,D自然为氢氧化钙;C为二氧化碳;H为红褐色沉淀,可判断为氢氧化铁,E→C的反应是工业炼铁的常用反应,故可判断E为氧化铁,G自然为硫酸铁,F为氢氧化钠。
【详解】(1)A为碳酸钙,化学式为:CaCO3;G为硫酸铁,化学式为:Fe2(SO4)3;H为红褐色沉淀,为氢氧化铁,化学式为:Fe(OH)3;
(2)化学反应常伴有能量变化,物质B氧化钙与水反应时会放出热量;
(3)D为氢氧化钙,F为氢氧化钠,故D→F的化学方程式: ;
12.(1)CuCl2、MgCl2
(2)NH4Cl
(3)
(4)b
【详解】(1)取样溶于水,无固体残留,得无色溶液X,则此粉末中一定不含CuCl2、MgCl2;因为氯化铜与氢氧化钠反应生成的氢氧化铜是蓝色沉淀,氯化镁与氢氧化钠反应生成的氢氧化镁是白色沉淀;
(2)取溶液X适量,微热,无氨味,则此粉末中一定不含NH4Cl,因为氯化铵与氢氧化钠反应生成的氨水受热会分解生成氨气;
(3)另取溶液X适量,滴加BaCl2溶液,有白色沉淀,再加入足量稀HNO3,沉淀全部溶解,测此粉末中一定不含,一定含;因为碳酸钠与氯化钡反应生成的碳酸钡沉淀能溶于硝酸,而硫酸钠与氯化钡反应生成的硫酸钡不溶于硝酸
(4)由于有碳酸钡生成,说明有碳酸钠存在,由于固体全部溶解,所以不能含有氯化镁,因此可知现在粉末中有氢氧化钠、碳酸钠,不含有氯化铜、氯化铵、氯化镁,剩余氯化钠,需要验证是否存在,氯化钠可以利用硝酸银验证,观察白色沉淀,而碳酸钠和氢氧化钠会影响实验,所以先去除,可以选择硝酸,因此先加硝酸后加入硝酸银,验证氯化钠是否存在;
故填:b。
13.
【分析】E为鸡蛋壳的主要成分,故E是碳酸钙;F由两种元素组成,能和碳酸钙反应,故F是盐酸;碳酸钙和D互相转化,盐酸也可以生成D,故D是二氧化碳;A和二氧化碳互相转化,则A可以是一氧化碳,一氧化碳燃烧或者与金属氧化物反应会生成二氧化碳,二氧化碳和碳高温下化合会生成一氧化碳,一氧化碳属于氧化物;B可以生成一氧化碳、二氧化碳,故B可以是碳或者氧气,碳或者氧气都属于单质,碳在氧气中充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳;若B是碳,C可以是铁等排在氢之前的金属,如碳和铁的氧化物高温下生成铁和二氧化碳,铁可以和盐酸反应生成氯化亚铁和氢气;若B是氧气,则C可以是某些金属氧化物,如氧化铜,氧化铜和盐酸反应生成氯化铜和水;代入验证即可;
【详解】(1)E为碳酸钙,化学式为;
(2)C 与 F 反应,可以是铁与稀盐酸反应生成氯化亚铁和氢气,反应的化学 程式为:。
14. O2 无污染/燃烧值高/资源广泛(合理即可)
【分析】D是一种紫红色金属单质,故D为铜,常温下A、E是气态单质,C是液体,可推测A为氢气,E为氧气,C为水,铜与氧气反应生成氧化铜,故B为氧化铜,氢气和氧化铜反应生成铜和水,代入框图,推测正确。
【详解】(1)根据分析,E为氧气,化学式为O2。
(2)反应A+B→C+D是氢气和氧化铜反应生成铜和水
(3)用氢气作为燃料的优点很多,氢气燃烧产物是水,不污染环境;氢气的燃烧值高;工业上制取氢气是通过电解水得到的,而地球上水资源丰富,可以从水中提取氢气,说明资源广泛。
答案第1页,共2页
答案第1页,共2页
