沪教版化学九年级全册(全国版)第一章《开启化学之门》教案
文档属性
| 名称 | 沪教版化学九年级全册(全国版)第一章《开启化学之门》教案 |

|
|
| 格式 | zip | ||
| 文件大小 | 187.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-11-15 00:00:00 | ||
图片预览



文档简介
第一章 开启化学之门
第1节 化学给我们带来什么
1.1化学给我们带来什么第1课时
教学目标:
1、认识学习、研究化学的意义;
2、认识碳酸氢铵的性质
3、知道碳酸氢铵受热后减少的原因及贮存的注意事项。
教学重点:
1、通过碳酸氢铵受热分解实验知道化学能帮助我们正确认识物质。
教学难点
1. 从碳酸氢铵受热分解实验总结出碳酸氢铵存贮注意事项;
2.让学生初步认识到性质、用途及保存等方面的关系
教学过程:
【情景创设】投影
提出下列问题:怎样才能使天空 ( http: / / www.21cnjy.com )变蓝?河水变得清澈?物质变得更丰富?生活变得更美好?……你的美好愿望正在通过化学家的智慧和辛勤劳动逐渐实现。
【明确学习目标】
一、回顾、预习与交流
【交流预习内容】
1、学习和研究化学可以帮助我们正确地 ,合理地 ,
高效地 。
2、思考下列说法是否正确:
点石成金 ( ) 水能变成油 ( )
发功使铝变成金( ) 抽烟有利于头脑清醒( )
用铁锅比铝锅炒菜对人体好( ) 化肥使用越多越好 ( )
农药不能用 ( ) 煤气燃烧时火越红越好( )
在牛奶中添加三聚氰胺有利于儿童身体健康 ( )
【新知导学】:
【思考与交流】
二、合作、研讨与点拨
(一)化学帮助我们正确认识物质
1、正确认识碳酸氢铵
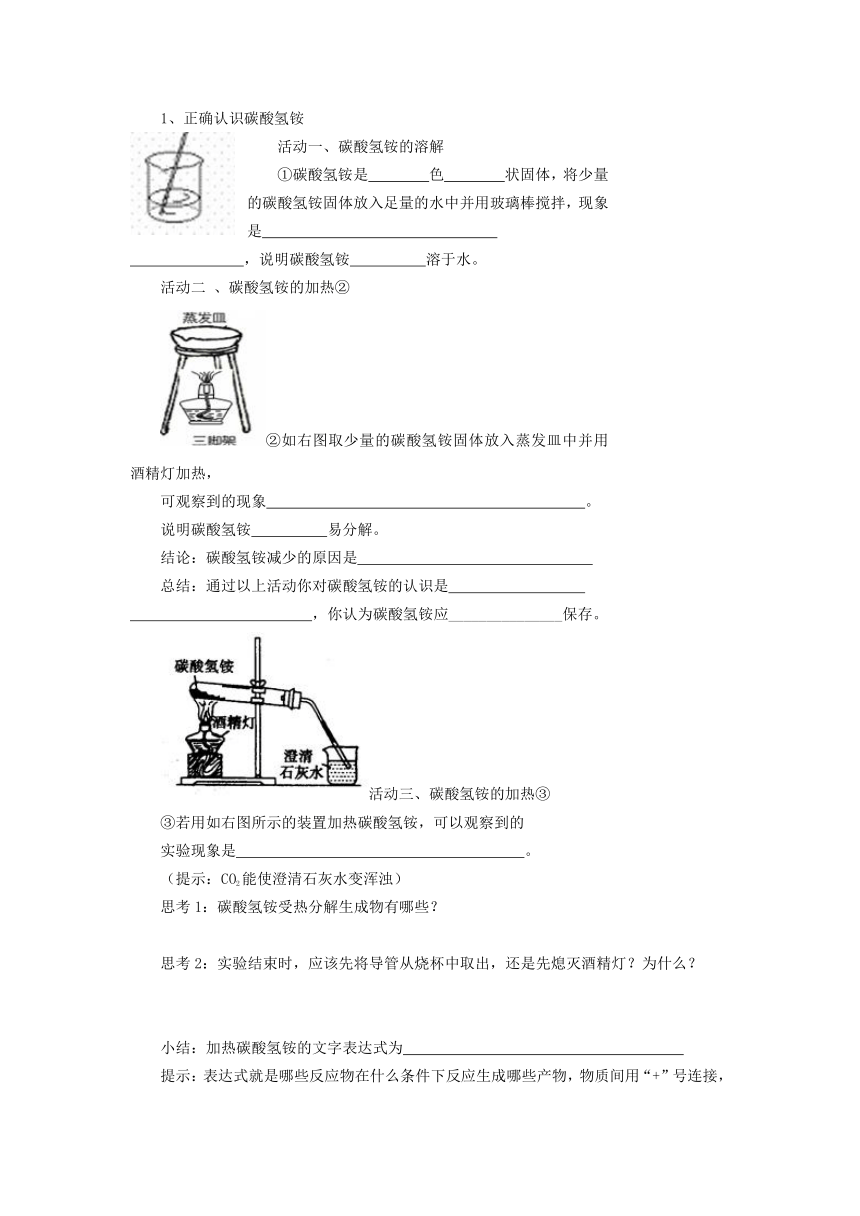
活动一、碳酸氢铵的溶解
①碳酸氢铵是 色 状固体,将少量的碳酸氢铵固体放入足量的水中并用玻璃棒搅拌,现象是
,说明碳酸氢铵 溶于水。
活动二 、碳酸氢铵的加热②
( http: / / www.21cnjy.com )②如右图取少量的碳酸氢铵固体放入蒸发皿中并用酒精灯加热,
可观察到的现象 。
说明碳酸氢铵 易分解。
结论:碳酸氢铵减少的原因是
总结:通过以上活动你对碳酸氢铵的认识是
,你认为碳酸氢铵应_______________保存。
( http: / / www.21cnjy.com )活动三、碳酸氢铵的加热③
③若用如右图所示的装置加热碳酸氢铵,可以观察到的
实验现象是 。
(提示:CO2能使澄清石灰水变浑浊)
思考1:碳酸氢铵受热分解生成物有哪些?
思考2:实验结束时,应该先将导管从烧杯中取出,还是先熄灭酒精灯?为什么?
小结:加热碳酸氢铵的文字表达式为
提示:表达式就是哪些反应物在什么条件下反应 ( http: / / www.21cnjy.com )生成哪些产物,物质间用“+”号连接,读作“和”;反应和生成物间用“=”号或“→”,读作“生成”,并在上面写上反应条件。
三、总结、反思与提升
1、日常生活中,物质的保存也有学问。请你仿照下例说出物质贮存的一些注意事项。
例:受热易分解的物质应放在阴凉的地方
___________________ ;
。
2、符号表达式:
加热碳酸氢铵的符号表达式:
(提示:将文字表达式中的物质的中文名改成对应的物质的化学式(化学符号)就成了符号表达式)
四、自检、反馈与巩固
【课堂作业】
【作业布置】家庭作业课后训练
五、【板书设计】
六、【教学反思】
1.1化学给我们带来什么第2课时
教学目标
1、了解氮气的性质和用途
2、了解延长材料使用,减少资源消耗的措施,特别是铁资源的保护;
3、了解化学促进科学技术的发展。
教学重点
1、了解延长材料使用,减少资源消耗的措施,特别是铁资源的保护;
2、了解化学促进科学技术的发展。
教学难点
1. 铁生锈实验总结出铁生锈的条件
2.铁资源的保护
教学过程:
【情景创设】投影
【明确学习目标】、
一、回顾、预习与交流
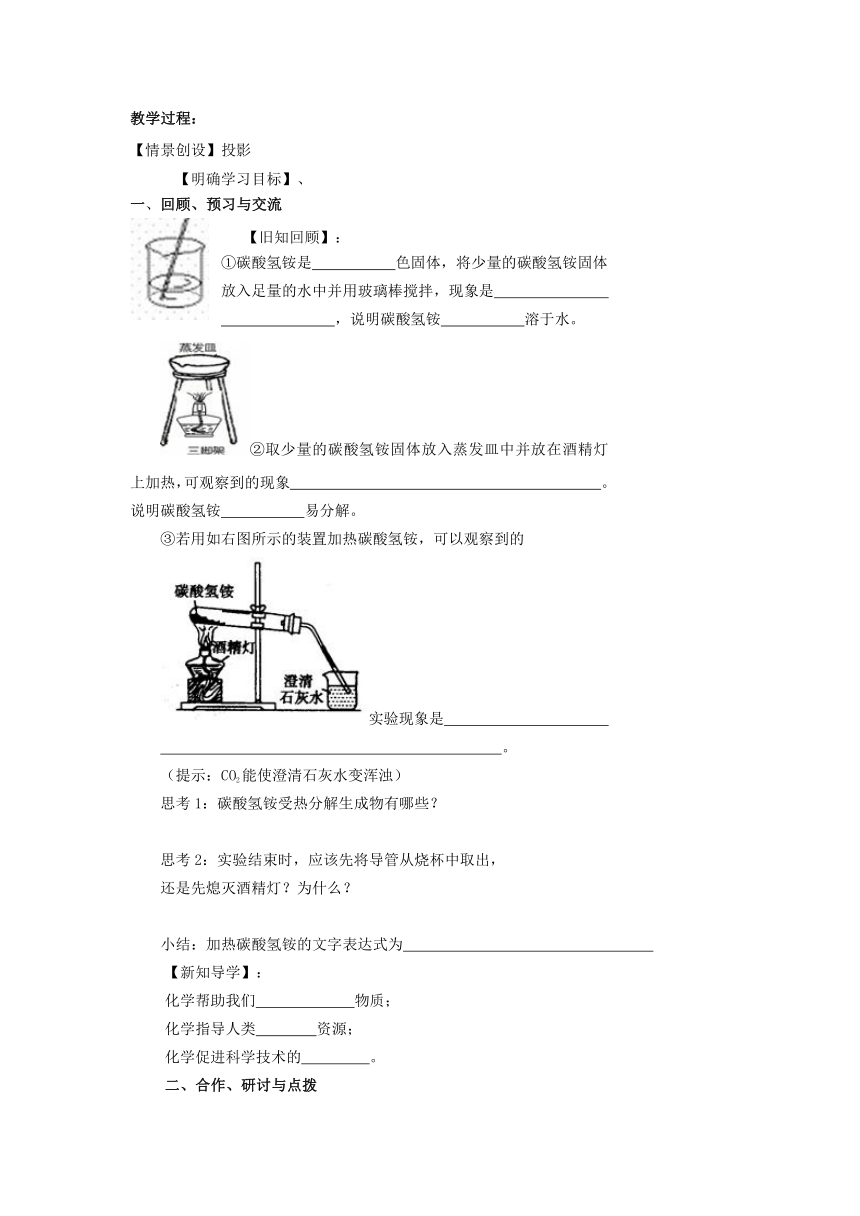
【旧知回顾】:
①碳酸氢铵是 色固体,将少量的碳酸氢铵固体放入足量的水中并用玻璃棒搅拌,现象是
,说明碳酸氢铵 溶于水。
( http: / / www.21cnjy.com )②取少量的碳酸氢铵固体放入蒸发皿中并放在酒精灯上加热,可观察到的现象 。说明碳酸氢铵 易分解。
③若用如右图所示的装置加热碳酸氢铵,可以观察到的
( http: / / www.21cnjy.com )实验现象是
。
(提示:CO2能使澄清石灰水变浑浊)
思考1:碳酸氢铵受热分解生成物有哪些?
思考2:实验结束时,应该先将导管从烧杯中取出,
还是先熄灭酒精灯?为什么?
小结:加热碳酸氢铵的文字表达式为
【新知导学】:
化学帮助我们 物质;
化学指导人类 资源;
化学促进科学技术的 。
二、合作、研讨与点拨
(二)化学指导人类合理利用资源
1.空气中的氮气资源
活动一、阅读教材第4页理解氮气的性质与用途
空气中的氮气很 ,在常温下很 (难或易)与其他物质发生反应
( http: / / www.21cnjy.com )氮气用途有 、 、 、
2.延长材料使用时间,减少资源消耗。
活动二、铁生锈条件的探究实验
阅读教材P5,观察实验,完成下列填空:
据估计,世界上每年都有将近总产量 钢铁锈蚀,造成巨大
经济损失。
探究铁生锈的条件,叙述图中实验现象
,
解释发生此现象的原因是
。
结论:铁在 作用下易生锈,铁与_________ 溶液接触后更易生锈。
拓展:(1)上述实验为什么用红墨水?你还能设计出其他原理相同的实验吗?
(2)应该如何防止铁生锈?
(三)化学促进科学技术的发展
活动三、阅读教材P第6~7页,小组合作交流完成下列问题:
1.人类社会文明和进步离不开化学
历史学家有时以一种新材料出现划分时代:
如 时代、 时代、 时代、 时代。
在古代,我国的化学工艺就已有相当的成就例如, 的制造; 冶炼与应用 发明, 烧制都是举世闻名的。我国在 代会制青铜器
2.化学的发展促进社会生产的发展
化学为工业的发展提供了更多的 ,为农业生产提供了 ,为人类战胜疾病提供了 。
三、总结、反思与提升
1、铁生锈的条件是什么?日常生活中使用哪些措施可以防止钢铁生锈?
2、食品包装袋中充有氮气,其原理是什么?有的充的是二氧化碳,你有办法鉴别
出到底充的是哪种气体吗?
四、自检、反馈与巩固
【当堂检测】
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
第2节 化学研究些什么
1.2 化学研究些什么第1课时
教学目标
1、了解化学研究的内容;
2、知道物理变化、化学变化的概念
3、正确判断日常生活中常见的典型的变化所属类型
教学重点
物理变化、化学变化的本质区别,并依此判断变化类型
教学难点
物理变化和化学变化的判断。
教学过程:
【情景创设】步入化学的殿堂,展现在你面 ( http: / / www.21cnjy.com )前的是一幅幅与物质有关的美丽画卷。它将告诉你化学研究的内容:各种各样的物质是怎样构成的,会发生哪些变化,是用什么方法来合成的?学习化学,你对自然界和社会的发展会有更多更新的认识;学了化学,你会发现化学其实就在你身边。【明确学习目标】
【交流预习内容】
一、回顾、预习与交流
【旧知回顾】:
回忆前面所学内容,回答下列问题:
1.碳酸氢铵加热后变成了什么?此变化过程中伴随哪些现象?写出反应的文字表达式?
2.教材P5铁生锈的实验中铁变成了什么?此变化过程中伴随的现象有哪些?铁生锈的条件是什么?如何防止铁制品生锈?
【新知导学】:
1、化学是一门以实验为基础,研究物质的 与 、
与 、 与 等基础自然科学。
2、研究的对象是 ,研究的工具是: ,研究内容是:
二、合作、研讨与点拨
一、化学研究物质的变化
活动一、1.蜡烛燃烧实验
阅读教材P9“活动与探究”,观察实验现象,完成课本中的表格
思考:
(1)火焰上压白瓷板观察出现现象,分析原因是什么?
(2)吹灭火焰后出现的白烟是什么?请设计简单实验证明自己的猜想。
(3)“蜡炬成灰泪始干”中的“灰”中含有哪些物质?
2.物理变化
的变化属于物理变化,
例如 、 都属于物理变化。
3.化学变化 的变化属于化学变化,
例如 、 都属于化学变化。
4.化学变化常伴随的现象
在化学变化中,常伴随一些现象如
等等,这些现象有助于我们判断物质是否发生了化学变化。
但有上述现象的反应不一定是化学变化。请举例说明?
5.物理变化和化学变化的本质区别是 。
例题:下列变化属于物理变化的是 ,
属于化学变化的是 。(填序号)
A.汽油挥发; B.木材做成课桌; C.食物腐败;
D.钢铁生锈; E.樟脑丸逐渐消失; F.烧制陶器;
G.汽油去油污; H.植物的光合作用; L.灯泡通电后发光发热
6.物理变化与化学变化的联系是 。
三、总结、反思与提升
1. 怎样区分物理变化与化学变化?两者之间有什么联系?
3.发光发热的变化一定是化学变化吗?举例说明。
4.爆炸一定都是化学变化吗?例如,轮胎爆炸属于 变化,
火药爆炸属于___________变化。
四、自检、反馈与巩固
【课堂作业】
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.2 化学研究些什么第2课时
教学目标
1.能正确判断物理性质和化学性质。
2.学会描写物质性质的方法;
3.能正确判断物理性质与化学性质
教学重点
物理变化与化学变化的根本区别,性质与变化的判断方法。
教学难点
性质和变化的判断(关键词)
教学过程:
【情景创设】人类对物质组成的认识经历了漫长的历史时期,比如空气看不见,也摸不
着,甚至都不知道它的存在,物质组成是化学研究的内容之一
【明确学习目标】
一、回顾、预习与交流
【旧知回顾】:
判断变化类型的根本依据是什么?还可由哪些经验上的方法进行判断?
2.某固体物质受热后变化为该物质的气态,这种变化属于 ( )
A.一定是物理变化
B.一定是化学变化
C.可能是物理变化,也可能是化学变化
D.既不是物理变化,也不是化学变化
3、蜡烛燃烧过程发生了什么变化?您判断的依据分别是什么?
【新知导学】:
1、煤、石油、天然气都是日常生活中常见的燃料,,而体现这一性质时,他们都会因燃烧而生成了新的物质,发生了 变化,说明这些燃料都具有 性,该性质是煤、石油、天然气的 性质。
2、衣服洗净之后都要凉干。其中的水份会蒸发而就成水蒸汽,并没有生成新物质,只是物质的状态发生了改变,该变化是 变化,体现水受热易蒸发。是水的 性质。
二、合作、研讨与点拨
二、化学研究物质的性质
活动一、(1).物理性质
物质 就能表现出来的性质叫物理性质,
如物质的 等都属于物理性质。
(2).化学性质
物质 表现出来的性质叫化学性质,
如物质的可燃性、助燃性、稳定性、氧化性、还原性、酸碱性、毒性都属于 。
金刚石硬度大,加工成钻石很困难,这是金刚石的 性质;灼热的金刚石可以在液态氧中燃烧是金刚石的 性质。
例题:
1.水是大家熟悉的物质请你说出水的物理性质(至少说5点)
。
2.如何鉴别下列物质?写出鉴别的依据(方法、操作、现象、结论)。
(1)食盐和白糖 尝味道 取样尝味道 咸的是食盐,甜的是白糖 ;
您将食盐和白糖鉴别开来的方法是: ;
(2)蒸馏水和酒精 ;
(3)铁片和锌片 ;
(4)铜片和铝片 ;
(5)澄清石灰水和自来水 ;
(6)二氧化碳和氮气 ;
(7)石膏和碳酸氢铵 ;
(8)塑料和陶瓷 。
(一)化学研究化学变化中的能量变化
活动二、
1、大量事实表明,化学变化伴随着能量的吸收或释放。
持续加热的反应、光合作用、电解水等通常是吸热反应
燃烧,缓慢氧化等通常是放热反应
2、化学变化过程中伴随着不同能量形式的相互转化
如:动植物的呼吸是 能转变成 能;
煤、石油的燃烧是 能转变成 能和 能,
干电池放电时是 能转变成 能,
电池充电时是 能转变成 能;
绿色植物的光合作用是 能转变成 能。
三、总结、反思与提升
1. 怎样区分物理性质与化学性质?
2. 怎样区分物质的变化和性质?在语言叙述上,性质常用哪些词语描述?
3.发光发热的变化一定是化学变化吗?举例说明。
4.爆炸一定都是化学变化吗?例如,轮胎爆炸属于____________变化,
火药爆炸属于___________变化。
四、自检、反馈与巩固
【当堂检测】
【布置作业】完成【课后训练】
五、【板书设计】
六、【教学反思】
1.2 化学研究些什么第3课时
教学目标
1.知道物质发生变化时伴随着能量的变化;
2.学会对常见物质的物理、化学性质进行描述;
3.了解物质的组成与结构对性质的影响。
教学重点
了解物质的组成与结构。
教学难点
了解物质的组成与结构。
教学过程:
【情景创设】在日常生活中,我们经常会遇到这样的现象:燃着的火柴熄灭后在火柴梗上附有黑色物质;在蜡烛火焰上方放置玻璃片,在玻璃片的下方可以看到黑色物质;烧烤会导致食物的表面变焦,烧烤时间越长,变焦的程度越大。你是否想过,这些物质的组成相同吗?为什么上述过程中均会产生黑色物质?
【明确目标】
一、回顾、预习与交流
【旧知回顾】:
1、空气中含有 、 、 、 等多种气体
2、红磷燃烧消耗了空气中得的 ,生成了 固体
3、混合物是 如
( http: / / www.21cnjy.com ) 纯净物是 如
【新知导学】:
二、合作、研讨与点拨
活动一、(一)空气中氧气体积含量的测定
1.实验原理:利用固体红磷燃烧消耗了 ( http: / / www.21cnjy.com )密闭容器中的氧气,生成五氧化二磷固体,使容器内 减小。打开止水夹后,在大气压作用下,水进入集气瓶的体积约 消耗掉的气体体积。
2.实验装置:如图所示。
3.实验探究
实验步骤 实验现象
①检查装置气密性,将导气管的一端插入水中, 。 在导管口 说明气密性良好。
②将集气瓶的容积划分为5等份,并加以标记
③把燃烧匙内的足量红磷点燃后,迅速伸入集气瓶内,塞紧橡皮塞。 红磷继续燃烧产生浓厚的 ,放出热量。
④待集气瓶冷却到室温后,把导管插入盛水的烧杯中,打开止水夹 水进入集气瓶,其体积约占集气瓶容积的 。
4.实验问题思考
(1)红磷在集气瓶中燃烧,消耗的气体是 ;
(2)红磷在集气瓶中未能全部燃烧,说明了 ;
(3)集气瓶中剩余的气体是氮气吗? ;
(4)打开止水夹后,为什么集气瓶中能吸 ( http: / / www.21cnjy.com )入约占集气瓶容积1/5的水? 。
5.实验结论: 。
活动二、(二)混合物和纯净物:
纯净物:是由 物质组成,如 、
、水都是纯净物;
混合物:是由 的物质混合而成的,如 、糖水、煤、石油都是混合物。
(三)拓展视野
阅读P14完成下列问题
国科学家 ( http: / / www.21cnjy.com ) 和 国化学家 分别制得了氧气。 国化学家 得出了空气是由 和 组成
三、总结、反思与提升
1.空气成分:
科学家通过各种实验测定,说明空气是 、 、
、 水蒸气和其他气体组成。
提示:在通常情况下,空气中各种成分的比值保持相对稳定,不是固定不变的。
2. 问题讨论,展示提升
对“思考与交流”中“空气中氧气体积含量的测定”实验讨论:
(1)该实验为什么不宜用蜡烛代替红磷?通常对该实验的反应物选择有什么要求?
(2)你认为该实验获得成功的关键步骤有哪些?
(3)该实验有时测得氧气的体积远小于(或大于)空气体积的1/5,出现误差的原因可能有哪些?
偏小的原因:
;
偏大的原因:
。
四、自检、反馈与巩固
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.2 化学研究些什么第4课时
教学目标
1.知道物质发生变化时伴随着能量的变化;
2.学会对常见物质的物理、化学性质进行描述;
3.了解物质的组成与结构对性质的影响.
教学重点
了解物质的组成与结构。
教学难点
了解物质的组成与结构。
教学过程:
【情景创设】在日常生活中,我们经 ( http: / / www.21cnjy.com )常会遇到这样的现象:燃着的火柴熄灭后在火柴梗上附有黑色物质;在蜡烛火焰上方放置玻璃片,在玻璃片的下方可以看到黑色物质;烧烤会导致食物的表面变焦,烧烤时间越长,变焦的程度越大。你是否想过,这些物质的组成相同吗?为什么上述过程中均会产生黑色物质?
【明确目标】
【学习过程】
一、回顾、预习与交流
【旧知回顾】:
1. 碳酸氢铵分解过程是_____________(填“放热”或“吸热”)过程。
2、空气中含 、 、 、 、水蒸气等物质,其中氧气约占 、氮气约占 。
【新知导学】:
1. 铜可用来制导线,说明铜具有哪些性质?酒精具有可燃性,酒精可用来干什么?
二、思考、交流与点拨
活动一、(二)化学研究物质的结构
组成与结构决定物质的性质。
1.从宏观看,物质是由组成物质的基本要素 组成的,如氧气由 元素组成的,金刚石由 元素组成,二氧化碳由 和 元素组成,碳酸氢铵由 、 、 、
四种元素组成。
2.取少量葡萄糖、砂糖、面粉分别放在燃烧匙中,在酒精灯上加热,观察到的现象是 ,现象说明了葡萄糖、砂糖、面粉中都含有 元素。
3. 一种物质可以通过化学变化变成其他物质,但反应物及生成物中应含有同种元素。
4.从微观看,任何物质都由 构成的,各种物质都有一定的组成与结构,组成与结构决定物质的性质。
根据教材P16图1-22、1-23,推测金刚石与石墨的有关性质:
材料 你推测的有关性质
金刚石
石墨
你推测的依据什么? 。
活动二、(三)化学研究物质的用途与制法
1.历史上几项重要的化学研究成果(阅读课本有关内容)
历史上许多科学家在科学研究领域作出重大贡献,请把左栏与右栏相关的项目用短线连结起来。
左栏 右栏
导电塑料 居里夫妇
得出空气是由氧气、氮气组成 门捷列夫
发表元素周期表 拉瓦锡
研究炸药改进了引爆装置 中国
发现放射性的钋和镭 三位科学家
首次人工合成了结晶牛胰岛素 诺贝尔
三、总结、反思与提升
1、用“性质”和“用途”填空。
物质的__________决定物质的__________,物质的_______体现了物质的__________。物质的组成与结构决定物质的 。
2、从化学角度分析“点石成金”的可能性。
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
第3节 怎样学习和研究化学
1.3 怎样学习和研究化学第1课时
教学目标
1.了解化学仪器的使用
2.掌握化学实验基本操作
教学重点
化学实验基本操作
教学难点
化学实验基本操作中注意事项
教学过程:
【情景创设】播放化学实验室视频
【明确目标】
一、回顾、预习与交流
【旧知回顾】:
预习课本P137-P138
【新知导学】:
二、合作、研讨与点拨
活动一:药品的取用
(1)药品取用“三”原则:
①“三不原则”:不能用手拿药品;不能把鼻孔凑近容器口去闻药品的气味;不得品尝任何药品的味道。(简单地概括就是: )
②节约原则:严格按实验规定用量取用药品。如果没有说明用量,一般取最少量,液体 ,固体 。
③处理原则:实验时剩余的药品不能放回原瓶;不要随意丢弃;更不要拿出实验室。
(2)药品取用方法
固体药品:①块状:用 夹取;操作要领是:“一平、二放、三慢竖”(将试管横放.用镊子将块状固体药品放入试管口,然后慢慢地将试管竖立起来,使块状固体缓缓滑至试管底部)。
②粉末状:用 (或 )取用;操作要领是:“一斜、二送、三直立”(将试管倾斜,把盛有药品的药匙或纸槽送入试管底邵,然后使试管直立起来,让药品落入试管底部)。
液体药品:
1.倾倒操作要领是:“取下瓶塞 着放,标签 缓慢倒,用完盖紧原处放。”
2.胶头滴管:用于吸取和滴加少量液体
注意事项:①先排空再吸液 ②悬空垂直放在试管口上方,以免沾污染滴管
③吸取液体后,应保持胶头在上,不能向下或平放,防止液体倒流,沾污试剂或腐蚀胶头;
④除吸同一试剂外,用过后应立即洗净,再去吸取其他药品(防止试剂相互污染。
⑤滴瓶上的滴管与瓶配套使用,滴液后应立即插入原瓶内,不得弄脏,也不必用水冲冼。
3.用量筒量取液体体积的方法:① ( http: / / www.21cnjy.com )读数时,应将量筒放置平稳,并使视线与液面凹面最 处保持水平,②应根据量取液体体积的多少,选用大小适当的量筒。
注意事项:不能加热,不能作为反应容器,也不能用作配制或稀释溶液的容器。
气体药品: 1.集气瓶 2. 气囊
三、总结、反思与提升
你还有哪些能够获得气体的方法?
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.3 怎样学习和研究化学第2课时
教学目标
1. 认识化学实验在学习和研究化学中的重要性;
2.通过铜绿的性质探究实验了解常用的实验仪器,掌握实验基本操作。
3.通过实验认识铜绿的性质
教学重点
研究铜绿的两个实验。
教学难点
铜绿两个实验的基本实验操作。
教学过程:
【情景创设】播放化学实验室视频
【明确目标】
一、回顾、预习与交流
【旧知回顾】:
1、药品取用方法(往试管里加固体药品或倾倒液体药品)
固体药品:①块状:用 夹取;操作要领是:“一平、二放、三慢竖”
②粉末状:用 (或 )取用;操作要领是:“一斜、二送、三直立”
液体药品:操作要领是:“取下瓶塞 着放,标签 缓慢倒,用完盖紧原处放。
2、掌握化学实验中常用仪器的特征和用途,有利于开展化学学习和研究。
(1)请从下列常见仪器图示中,选择恰当的字母序号填空并注明仪器名称。
( http: / / www.21cnjy.com )
A B C D E F G H I
①可以直接在酒精灯火焰上加热的玻璃仪器是 ;
②镁条燃烧时,用来夹持镁条的仪器是 ;
③用酒精灯加热时需要垫上石棉网的仪器是 ;
④取用粉末状固体药品用到的仪器是 ;
⑤吸取和滴加少量液体试剂的仪器是 ;
⑥排空气法收集气体用到的玻璃仪器是 ;
【新知导学】:
二、合作、研讨与点拨
活动一:物质的加热。
(1)酒精灯的使用方法:①禁止向 的酒精灯里添加乙醇;②要用火柴点燃,禁止用 点燃另一只酒精灯;③用 加热;④熄灭时,用 灭,不能用嘴吹;⑤盛酒精量不能超过酒精灯容积的2/3,也不得少于1/4。
(2)给物质加热的方法及注意事项:①加热玻璃仪器时,要把容器壁外的水擦干;②很热的容器不要立即用冷水冲洗.以免受热不匀而破裂;③给盛有液体的试管加热时,试管内液体的量不可超过试管容积的 ;④加热前应先 试管;⑤试管应 放在外焰上;⑥试管口不能朝着 的方向;⑦给试管里的固体药品加热时,试管口要略向 倾斜,受热均匀后再固定加热。
(3)给液体物质加热的仪器可用试管、烧杯、烧瓶等;给固体物质加热,可用干燥的试管。
可直接受热的:试管、蒸发皿、燃烧匙、坩埚等
能间接受热的:烧杯、烧瓶(加热时,需加石棉网)
活动二:玻璃仪器的洗涤。
洗涤方法:①倒去废物(要倒在指定的容器内);②用水冲洗并加以振荡;③用试管刷刷洗;④再用水冲洗。如果玻璃仪器内壁上附着不溶于水的碱、碳酸盐、碱性氧化物等,可先用稀盐酸溶解,再用水冲洗;如果玻璃仪器内壁附有油污,可先用少量纯碱溶液或洗衣粉刷洗,再用水冲洗。
洗涤干净的标准:内外壁附着的水既不聚成水滴,也无成股水流下。
活动三:连接仪器装置
①. 玻璃导管插入塞子
②. 玻璃导管插入胶皮管
③. 塞子塞进容器口
活动四:检查装置气密性
连接好仪器后,先将导管一 ( http: / / www.21cnjy.com )端伸入水中,再用双手紧握容器外壁。如果导管口有气泡冒出,松开手冷却后形成 液柱,说明装置气密性良好。
三、总结、反思与提升
1.使用酒精灯时要注意什么问题?
2.如何取用固体药品和液体药品?
3.使用量筒时要注意什么?
4.同学们到实验室做完实验后,老师检查发现有许多试管破了,请同学们分析一下,可能是哪些原因导致了试管破裂。
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.3 怎样学习和研究化学第3课时
教学目标
1.了解化学仪器的使用
2.掌握化学实验基本操作
教学重点
化学实验基本操作
教学难点
化学实验基本操作中注意事项
教学过程:
【情景创设】播放化学实验室视频
【明确目标】
【回顾、预习与交流】
一、回顾、预习与交流
1.药品取用的“三不原则”是什么?
2.药品取用若没有说明用量,固体和液体分别取多少?
3.实验剩余的药品怎么处理?
4.酒精灯使用时要注意什么问题?
5、给液体加热要注意什么?
6、给固体物质加热要注意什么?
7、气密性如何检查?
二、合作、研讨与点拨
活动一:天平的正确使用方法
称量时,左盘放置_______,右盘放置______。M物=M码 M游码
若物码倒置,则M物=M码 M游码
2、交流讨论:“称一未知质量的药品质量”与“称一定质量的药品”有何异同?
( http: / / www.21cnjy.com )
活动二:过滤与蒸发
1、过滤
(1)过滤:是一种________________________________________的操作
(2)所需仪器: _______________________________________;
(3)操作要点: 一___ ( http: / / www.21cnjy.com )____________________________________;
二_______________________________________;
三 ____________________________________;
(4)过滤过程中玻璃棒的作用:___________________________________;
(5)交流讨论:某同学在进行过滤时,发现过滤了两次仍然浑浊,你认为原因可能有哪些?
( http: / / www.21cnjy.com )
2、蒸发
(1)所需仪器:_______________________________________;
(2)操作要点:一_______________________________________;
二___________________________________;
三 ________________________________________;
(3)蒸发过程中玻璃棒的作用:___________________________________;
三、总结、反思与提升
1、称取5.8克食盐溶解于44.2克水中得到食盐水,并贮存于细口瓶中,贴上标签,注明溶液名称。
2、完成粗盐提纯实验,感知基本实验操作。会分析实验失败可能的原因。
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.3 怎样学习和研究化学第4课时
教学目标
1.使学生学会运用科学探究的方法探究镁的性质;;
2.通过铜绿的性质探究实验了解常用的实验仪器,掌握实验基本操作。
3.通过实验认识铜绿的性质。
教学重点
运用科学探究的方法探究镁的性质。
教学难点
科学探究的一般过程。
教学过程:
【情景创设】
【明确目标】
一、回顾、预习与交流
【交流预习内容】
1.药品取用的“三不原则”是什么?
2.药品取用若没有说明用量,固体和液体分别取多少?
3.实验剩余的药品怎么处理?
4.酒精灯使用时要注意什么问题?
二、合作、研讨与点拨
活动一:探究镁的性质。
1.撕开小段镁条,仔细观察,小结出镁的物理性质有:___________________________
2..镁的化学性质一(与氧气作用)
实验步骤 实验现象 实验结论或解释
1取小段镁条,用砂纸打磨
2点燃酒精灯
3用坩埚钳夹持住打磨过的镁条,点燃并移置石棉网上方
4熄灭酒精灯,处理实验废渣
5洗涤试管,整理好实验台
实验结论: 。
镁的化学性质二(与酸作用)
实验步骤 实验现象 实验结论或解释
1取小段镁条,用砂纸打磨
2将打磨过的镁条置于试管内,将其中逐滴滴加稀盐酸
3处理实验废液,洗涤试管,整理好实验台
实验结论: 。
活动二、铜绿的物理性质
1、铜绿是一种 色 体,主要成分是 ,盐酸是一种 色 体
2.铜绿的化学性质一(与酸的作用)
实验步骤 实验现象 实验结论或解释
1取适量铜绿于试管内
2将其中逐滴滴加稀盐酸
3处理实验废液,洗涤试管,整理好实验台
实验结论: 。
铜绿的化学性质二(受热分解)
实验步骤 实验现象 实验结论或解释
1取适量的铜绿放入试管中
2点燃酒精灯
3用试管夹夹住试管
4用酒精灯外焰加热
5熄灭酒精灯
6处理实验废渣,洗涤试管,整理好实验台
实验结论: 。
活动三、科学探究的一般步骤
科学探究的一般过程是①提出问题;② ;③设计方案;④ ;⑤反思评价得出结论
三、【总结、反思与提升】
1.镁条与酸反应,为什么用砂纸打磨打磨?
2.镁条燃烧的实验中,石棉网的作用是什么?
3.铜绿受热常用右图所示实验装置,请思考用该装置进行实验时能观察到哪些现象?在实验操作时需要注意哪些问题?
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
第1节 化学给我们带来什么
1.1化学给我们带来什么第1课时
教学目标:
1、认识学习、研究化学的意义;
2、认识碳酸氢铵的性质
3、知道碳酸氢铵受热后减少的原因及贮存的注意事项。
教学重点:
1、通过碳酸氢铵受热分解实验知道化学能帮助我们正确认识物质。
教学难点
1. 从碳酸氢铵受热分解实验总结出碳酸氢铵存贮注意事项;
2.让学生初步认识到性质、用途及保存等方面的关系
教学过程:
【情景创设】投影
提出下列问题:怎样才能使天空 ( http: / / www.21cnjy.com )变蓝?河水变得清澈?物质变得更丰富?生活变得更美好?……你的美好愿望正在通过化学家的智慧和辛勤劳动逐渐实现。
【明确学习目标】
一、回顾、预习与交流
【交流预习内容】
1、学习和研究化学可以帮助我们正确地 ,合理地 ,
高效地 。
2、思考下列说法是否正确:
点石成金 ( ) 水能变成油 ( )
发功使铝变成金( ) 抽烟有利于头脑清醒( )
用铁锅比铝锅炒菜对人体好( ) 化肥使用越多越好 ( )
农药不能用 ( ) 煤气燃烧时火越红越好( )
在牛奶中添加三聚氰胺有利于儿童身体健康 ( )
【新知导学】:
【思考与交流】
二、合作、研讨与点拨
(一)化学帮助我们正确认识物质
1、正确认识碳酸氢铵
活动一、碳酸氢铵的溶解
①碳酸氢铵是 色 状固体,将少量的碳酸氢铵固体放入足量的水中并用玻璃棒搅拌,现象是
,说明碳酸氢铵 溶于水。
活动二 、碳酸氢铵的加热②
( http: / / www.21cnjy.com )②如右图取少量的碳酸氢铵固体放入蒸发皿中并用酒精灯加热,
可观察到的现象 。
说明碳酸氢铵 易分解。
结论:碳酸氢铵减少的原因是
总结:通过以上活动你对碳酸氢铵的认识是
,你认为碳酸氢铵应_______________保存。
( http: / / www.21cnjy.com )活动三、碳酸氢铵的加热③
③若用如右图所示的装置加热碳酸氢铵,可以观察到的
实验现象是 。
(提示:CO2能使澄清石灰水变浑浊)
思考1:碳酸氢铵受热分解生成物有哪些?
思考2:实验结束时,应该先将导管从烧杯中取出,还是先熄灭酒精灯?为什么?
小结:加热碳酸氢铵的文字表达式为
提示:表达式就是哪些反应物在什么条件下反应 ( http: / / www.21cnjy.com )生成哪些产物,物质间用“+”号连接,读作“和”;反应和生成物间用“=”号或“→”,读作“生成”,并在上面写上反应条件。
三、总结、反思与提升
1、日常生活中,物质的保存也有学问。请你仿照下例说出物质贮存的一些注意事项。
例:受热易分解的物质应放在阴凉的地方
___________________ ;
。
2、符号表达式:
加热碳酸氢铵的符号表达式:
(提示:将文字表达式中的物质的中文名改成对应的物质的化学式(化学符号)就成了符号表达式)
四、自检、反馈与巩固
【课堂作业】
【作业布置】家庭作业课后训练
五、【板书设计】
六、【教学反思】
1.1化学给我们带来什么第2课时
教学目标
1、了解氮气的性质和用途
2、了解延长材料使用,减少资源消耗的措施,特别是铁资源的保护;
3、了解化学促进科学技术的发展。
教学重点
1、了解延长材料使用,减少资源消耗的措施,特别是铁资源的保护;
2、了解化学促进科学技术的发展。
教学难点
1. 铁生锈实验总结出铁生锈的条件
2.铁资源的保护
教学过程:
【情景创设】投影
【明确学习目标】、
一、回顾、预习与交流
【旧知回顾】:
①碳酸氢铵是 色固体,将少量的碳酸氢铵固体放入足量的水中并用玻璃棒搅拌,现象是
,说明碳酸氢铵 溶于水。
( http: / / www.21cnjy.com )②取少量的碳酸氢铵固体放入蒸发皿中并放在酒精灯上加热,可观察到的现象 。说明碳酸氢铵 易分解。
③若用如右图所示的装置加热碳酸氢铵,可以观察到的
( http: / / www.21cnjy.com )实验现象是
。
(提示:CO2能使澄清石灰水变浑浊)
思考1:碳酸氢铵受热分解生成物有哪些?
思考2:实验结束时,应该先将导管从烧杯中取出,
还是先熄灭酒精灯?为什么?
小结:加热碳酸氢铵的文字表达式为
【新知导学】:
化学帮助我们 物质;
化学指导人类 资源;
化学促进科学技术的 。
二、合作、研讨与点拨
(二)化学指导人类合理利用资源
1.空气中的氮气资源
活动一、阅读教材第4页理解氮气的性质与用途
空气中的氮气很 ,在常温下很 (难或易)与其他物质发生反应
( http: / / www.21cnjy.com )氮气用途有 、 、 、
2.延长材料使用时间,减少资源消耗。
活动二、铁生锈条件的探究实验
阅读教材P5,观察实验,完成下列填空:
据估计,世界上每年都有将近总产量 钢铁锈蚀,造成巨大
经济损失。
探究铁生锈的条件,叙述图中实验现象
,
解释发生此现象的原因是
。
结论:铁在 作用下易生锈,铁与_________ 溶液接触后更易生锈。
拓展:(1)上述实验为什么用红墨水?你还能设计出其他原理相同的实验吗?
(2)应该如何防止铁生锈?
(三)化学促进科学技术的发展
活动三、阅读教材P第6~7页,小组合作交流完成下列问题:
1.人类社会文明和进步离不开化学
历史学家有时以一种新材料出现划分时代:
如 时代、 时代、 时代、 时代。
在古代,我国的化学工艺就已有相当的成就例如, 的制造; 冶炼与应用 发明, 烧制都是举世闻名的。我国在 代会制青铜器
2.化学的发展促进社会生产的发展
化学为工业的发展提供了更多的 ,为农业生产提供了 ,为人类战胜疾病提供了 。
三、总结、反思与提升
1、铁生锈的条件是什么?日常生活中使用哪些措施可以防止钢铁生锈?
2、食品包装袋中充有氮气,其原理是什么?有的充的是二氧化碳,你有办法鉴别
出到底充的是哪种气体吗?
四、自检、反馈与巩固
【当堂检测】
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
第2节 化学研究些什么
1.2 化学研究些什么第1课时
教学目标
1、了解化学研究的内容;
2、知道物理变化、化学变化的概念
3、正确判断日常生活中常见的典型的变化所属类型
教学重点
物理变化、化学变化的本质区别,并依此判断变化类型
教学难点
物理变化和化学变化的判断。
教学过程:
【情景创设】步入化学的殿堂,展现在你面 ( http: / / www.21cnjy.com )前的是一幅幅与物质有关的美丽画卷。它将告诉你化学研究的内容:各种各样的物质是怎样构成的,会发生哪些变化,是用什么方法来合成的?学习化学,你对自然界和社会的发展会有更多更新的认识;学了化学,你会发现化学其实就在你身边。【明确学习目标】
【交流预习内容】
一、回顾、预习与交流
【旧知回顾】:
回忆前面所学内容,回答下列问题:
1.碳酸氢铵加热后变成了什么?此变化过程中伴随哪些现象?写出反应的文字表达式?
2.教材P5铁生锈的实验中铁变成了什么?此变化过程中伴随的现象有哪些?铁生锈的条件是什么?如何防止铁制品生锈?
【新知导学】:
1、化学是一门以实验为基础,研究物质的 与 、
与 、 与 等基础自然科学。
2、研究的对象是 ,研究的工具是: ,研究内容是:
二、合作、研讨与点拨
一、化学研究物质的变化
活动一、1.蜡烛燃烧实验
阅读教材P9“活动与探究”,观察实验现象,完成课本中的表格
思考:
(1)火焰上压白瓷板观察出现现象,分析原因是什么?
(2)吹灭火焰后出现的白烟是什么?请设计简单实验证明自己的猜想。
(3)“蜡炬成灰泪始干”中的“灰”中含有哪些物质?
2.物理变化
的变化属于物理变化,
例如 、 都属于物理变化。
3.化学变化 的变化属于化学变化,
例如 、 都属于化学变化。
4.化学变化常伴随的现象
在化学变化中,常伴随一些现象如
等等,这些现象有助于我们判断物质是否发生了化学变化。
但有上述现象的反应不一定是化学变化。请举例说明?
5.物理变化和化学变化的本质区别是 。
例题:下列变化属于物理变化的是 ,
属于化学变化的是 。(填序号)
A.汽油挥发; B.木材做成课桌; C.食物腐败;
D.钢铁生锈; E.樟脑丸逐渐消失; F.烧制陶器;
G.汽油去油污; H.植物的光合作用; L.灯泡通电后发光发热
6.物理变化与化学变化的联系是 。
三、总结、反思与提升
1. 怎样区分物理变化与化学变化?两者之间有什么联系?
3.发光发热的变化一定是化学变化吗?举例说明。
4.爆炸一定都是化学变化吗?例如,轮胎爆炸属于 变化,
火药爆炸属于___________变化。
四、自检、反馈与巩固
【课堂作业】
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.2 化学研究些什么第2课时
教学目标
1.能正确判断物理性质和化学性质。
2.学会描写物质性质的方法;
3.能正确判断物理性质与化学性质
教学重点
物理变化与化学变化的根本区别,性质与变化的判断方法。
教学难点
性质和变化的判断(关键词)
教学过程:
【情景创设】人类对物质组成的认识经历了漫长的历史时期,比如空气看不见,也摸不
着,甚至都不知道它的存在,物质组成是化学研究的内容之一
【明确学习目标】
一、回顾、预习与交流
【旧知回顾】:
判断变化类型的根本依据是什么?还可由哪些经验上的方法进行判断?
2.某固体物质受热后变化为该物质的气态,这种变化属于 ( )
A.一定是物理变化
B.一定是化学变化
C.可能是物理变化,也可能是化学变化
D.既不是物理变化,也不是化学变化
3、蜡烛燃烧过程发生了什么变化?您判断的依据分别是什么?
【新知导学】:
1、煤、石油、天然气都是日常生活中常见的燃料,,而体现这一性质时,他们都会因燃烧而生成了新的物质,发生了 变化,说明这些燃料都具有 性,该性质是煤、石油、天然气的 性质。
2、衣服洗净之后都要凉干。其中的水份会蒸发而就成水蒸汽,并没有生成新物质,只是物质的状态发生了改变,该变化是 变化,体现水受热易蒸发。是水的 性质。
二、合作、研讨与点拨
二、化学研究物质的性质
活动一、(1).物理性质
物质 就能表现出来的性质叫物理性质,
如物质的 等都属于物理性质。
(2).化学性质
物质 表现出来的性质叫化学性质,
如物质的可燃性、助燃性、稳定性、氧化性、还原性、酸碱性、毒性都属于 。
金刚石硬度大,加工成钻石很困难,这是金刚石的 性质;灼热的金刚石可以在液态氧中燃烧是金刚石的 性质。
例题:
1.水是大家熟悉的物质请你说出水的物理性质(至少说5点)
。
2.如何鉴别下列物质?写出鉴别的依据(方法、操作、现象、结论)。
(1)食盐和白糖 尝味道 取样尝味道 咸的是食盐,甜的是白糖 ;
您将食盐和白糖鉴别开来的方法是: ;
(2)蒸馏水和酒精 ;
(3)铁片和锌片 ;
(4)铜片和铝片 ;
(5)澄清石灰水和自来水 ;
(6)二氧化碳和氮气 ;
(7)石膏和碳酸氢铵 ;
(8)塑料和陶瓷 。
(一)化学研究化学变化中的能量变化
活动二、
1、大量事实表明,化学变化伴随着能量的吸收或释放。
持续加热的反应、光合作用、电解水等通常是吸热反应
燃烧,缓慢氧化等通常是放热反应
2、化学变化过程中伴随着不同能量形式的相互转化
如:动植物的呼吸是 能转变成 能;
煤、石油的燃烧是 能转变成 能和 能,
干电池放电时是 能转变成 能,
电池充电时是 能转变成 能;
绿色植物的光合作用是 能转变成 能。
三、总结、反思与提升
1. 怎样区分物理性质与化学性质?
2. 怎样区分物质的变化和性质?在语言叙述上,性质常用哪些词语描述?
3.发光发热的变化一定是化学变化吗?举例说明。
4.爆炸一定都是化学变化吗?例如,轮胎爆炸属于____________变化,
火药爆炸属于___________变化。
四、自检、反馈与巩固
【当堂检测】
【布置作业】完成【课后训练】
五、【板书设计】
六、【教学反思】
1.2 化学研究些什么第3课时
教学目标
1.知道物质发生变化时伴随着能量的变化;
2.学会对常见物质的物理、化学性质进行描述;
3.了解物质的组成与结构对性质的影响。
教学重点
了解物质的组成与结构。
教学难点
了解物质的组成与结构。
教学过程:
【情景创设】在日常生活中,我们经常会遇到这样的现象:燃着的火柴熄灭后在火柴梗上附有黑色物质;在蜡烛火焰上方放置玻璃片,在玻璃片的下方可以看到黑色物质;烧烤会导致食物的表面变焦,烧烤时间越长,变焦的程度越大。你是否想过,这些物质的组成相同吗?为什么上述过程中均会产生黑色物质?
【明确目标】
一、回顾、预习与交流
【旧知回顾】:
1、空气中含有 、 、 、 等多种气体
2、红磷燃烧消耗了空气中得的 ,生成了 固体
3、混合物是 如
( http: / / www.21cnjy.com ) 纯净物是 如
【新知导学】:
二、合作、研讨与点拨
活动一、(一)空气中氧气体积含量的测定
1.实验原理:利用固体红磷燃烧消耗了 ( http: / / www.21cnjy.com )密闭容器中的氧气,生成五氧化二磷固体,使容器内 减小。打开止水夹后,在大气压作用下,水进入集气瓶的体积约 消耗掉的气体体积。
2.实验装置:如图所示。
3.实验探究
实验步骤 实验现象
①检查装置气密性,将导气管的一端插入水中, 。 在导管口 说明气密性良好。
②将集气瓶的容积划分为5等份,并加以标记
③把燃烧匙内的足量红磷点燃后,迅速伸入集气瓶内,塞紧橡皮塞。 红磷继续燃烧产生浓厚的 ,放出热量。
④待集气瓶冷却到室温后,把导管插入盛水的烧杯中,打开止水夹 水进入集气瓶,其体积约占集气瓶容积的 。
4.实验问题思考
(1)红磷在集气瓶中燃烧,消耗的气体是 ;
(2)红磷在集气瓶中未能全部燃烧,说明了 ;
(3)集气瓶中剩余的气体是氮气吗? ;
(4)打开止水夹后,为什么集气瓶中能吸 ( http: / / www.21cnjy.com )入约占集气瓶容积1/5的水? 。
5.实验结论: 。
活动二、(二)混合物和纯净物:
纯净物:是由 物质组成,如 、
、水都是纯净物;
混合物:是由 的物质混合而成的,如 、糖水、煤、石油都是混合物。
(三)拓展视野
阅读P14完成下列问题
国科学家 ( http: / / www.21cnjy.com ) 和 国化学家 分别制得了氧气。 国化学家 得出了空气是由 和 组成
三、总结、反思与提升
1.空气成分:
科学家通过各种实验测定,说明空气是 、 、
、 水蒸气和其他气体组成。
提示:在通常情况下,空气中各种成分的比值保持相对稳定,不是固定不变的。
2. 问题讨论,展示提升
对“思考与交流”中“空气中氧气体积含量的测定”实验讨论:
(1)该实验为什么不宜用蜡烛代替红磷?通常对该实验的反应物选择有什么要求?
(2)你认为该实验获得成功的关键步骤有哪些?
(3)该实验有时测得氧气的体积远小于(或大于)空气体积的1/5,出现误差的原因可能有哪些?
偏小的原因:
;
偏大的原因:
。
四、自检、反馈与巩固
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.2 化学研究些什么第4课时
教学目标
1.知道物质发生变化时伴随着能量的变化;
2.学会对常见物质的物理、化学性质进行描述;
3.了解物质的组成与结构对性质的影响.
教学重点
了解物质的组成与结构。
教学难点
了解物质的组成与结构。
教学过程:
【情景创设】在日常生活中,我们经 ( http: / / www.21cnjy.com )常会遇到这样的现象:燃着的火柴熄灭后在火柴梗上附有黑色物质;在蜡烛火焰上方放置玻璃片,在玻璃片的下方可以看到黑色物质;烧烤会导致食物的表面变焦,烧烤时间越长,变焦的程度越大。你是否想过,这些物质的组成相同吗?为什么上述过程中均会产生黑色物质?
【明确目标】
【学习过程】
一、回顾、预习与交流
【旧知回顾】:
1. 碳酸氢铵分解过程是_____________(填“放热”或“吸热”)过程。
2、空气中含 、 、 、 、水蒸气等物质,其中氧气约占 、氮气约占 。
【新知导学】:
1. 铜可用来制导线,说明铜具有哪些性质?酒精具有可燃性,酒精可用来干什么?
二、思考、交流与点拨
活动一、(二)化学研究物质的结构
组成与结构决定物质的性质。
1.从宏观看,物质是由组成物质的基本要素 组成的,如氧气由 元素组成的,金刚石由 元素组成,二氧化碳由 和 元素组成,碳酸氢铵由 、 、 、
四种元素组成。
2.取少量葡萄糖、砂糖、面粉分别放在燃烧匙中,在酒精灯上加热,观察到的现象是 ,现象说明了葡萄糖、砂糖、面粉中都含有 元素。
3. 一种物质可以通过化学变化变成其他物质,但反应物及生成物中应含有同种元素。
4.从微观看,任何物质都由 构成的,各种物质都有一定的组成与结构,组成与结构决定物质的性质。
根据教材P16图1-22、1-23,推测金刚石与石墨的有关性质:
材料 你推测的有关性质
金刚石
石墨
你推测的依据什么? 。
活动二、(三)化学研究物质的用途与制法
1.历史上几项重要的化学研究成果(阅读课本有关内容)
历史上许多科学家在科学研究领域作出重大贡献,请把左栏与右栏相关的项目用短线连结起来。
左栏 右栏
导电塑料 居里夫妇
得出空气是由氧气、氮气组成 门捷列夫
发表元素周期表 拉瓦锡
研究炸药改进了引爆装置 中国
发现放射性的钋和镭 三位科学家
首次人工合成了结晶牛胰岛素 诺贝尔
三、总结、反思与提升
1、用“性质”和“用途”填空。
物质的__________决定物质的__________,物质的_______体现了物质的__________。物质的组成与结构决定物质的 。
2、从化学角度分析“点石成金”的可能性。
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
第3节 怎样学习和研究化学
1.3 怎样学习和研究化学第1课时
教学目标
1.了解化学仪器的使用
2.掌握化学实验基本操作
教学重点
化学实验基本操作
教学难点
化学实验基本操作中注意事项
教学过程:
【情景创设】播放化学实验室视频
【明确目标】
一、回顾、预习与交流
【旧知回顾】:
预习课本P137-P138
【新知导学】:
二、合作、研讨与点拨
活动一:药品的取用
(1)药品取用“三”原则:
①“三不原则”:不能用手拿药品;不能把鼻孔凑近容器口去闻药品的气味;不得品尝任何药品的味道。(简单地概括就是: )
②节约原则:严格按实验规定用量取用药品。如果没有说明用量,一般取最少量,液体 ,固体 。
③处理原则:实验时剩余的药品不能放回原瓶;不要随意丢弃;更不要拿出实验室。
(2)药品取用方法
固体药品:①块状:用 夹取;操作要领是:“一平、二放、三慢竖”(将试管横放.用镊子将块状固体药品放入试管口,然后慢慢地将试管竖立起来,使块状固体缓缓滑至试管底部)。
②粉末状:用 (或 )取用;操作要领是:“一斜、二送、三直立”(将试管倾斜,把盛有药品的药匙或纸槽送入试管底邵,然后使试管直立起来,让药品落入试管底部)。
液体药品:
1.倾倒操作要领是:“取下瓶塞 着放,标签 缓慢倒,用完盖紧原处放。”
2.胶头滴管:用于吸取和滴加少量液体
注意事项:①先排空再吸液 ②悬空垂直放在试管口上方,以免沾污染滴管
③吸取液体后,应保持胶头在上,不能向下或平放,防止液体倒流,沾污试剂或腐蚀胶头;
④除吸同一试剂外,用过后应立即洗净,再去吸取其他药品(防止试剂相互污染。
⑤滴瓶上的滴管与瓶配套使用,滴液后应立即插入原瓶内,不得弄脏,也不必用水冲冼。
3.用量筒量取液体体积的方法:① ( http: / / www.21cnjy.com )读数时,应将量筒放置平稳,并使视线与液面凹面最 处保持水平,②应根据量取液体体积的多少,选用大小适当的量筒。
注意事项:不能加热,不能作为反应容器,也不能用作配制或稀释溶液的容器。
气体药品: 1.集气瓶 2. 气囊
三、总结、反思与提升
你还有哪些能够获得气体的方法?
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.3 怎样学习和研究化学第2课时
教学目标
1. 认识化学实验在学习和研究化学中的重要性;
2.通过铜绿的性质探究实验了解常用的实验仪器,掌握实验基本操作。
3.通过实验认识铜绿的性质
教学重点
研究铜绿的两个实验。
教学难点
铜绿两个实验的基本实验操作。
教学过程:
【情景创设】播放化学实验室视频
【明确目标】
一、回顾、预习与交流
【旧知回顾】:
1、药品取用方法(往试管里加固体药品或倾倒液体药品)
固体药品:①块状:用 夹取;操作要领是:“一平、二放、三慢竖”
②粉末状:用 (或 )取用;操作要领是:“一斜、二送、三直立”
液体药品:操作要领是:“取下瓶塞 着放,标签 缓慢倒,用完盖紧原处放。
2、掌握化学实验中常用仪器的特征和用途,有利于开展化学学习和研究。
(1)请从下列常见仪器图示中,选择恰当的字母序号填空并注明仪器名称。
( http: / / www.21cnjy.com )
A B C D E F G H I
①可以直接在酒精灯火焰上加热的玻璃仪器是 ;
②镁条燃烧时,用来夹持镁条的仪器是 ;
③用酒精灯加热时需要垫上石棉网的仪器是 ;
④取用粉末状固体药品用到的仪器是 ;
⑤吸取和滴加少量液体试剂的仪器是 ;
⑥排空气法收集气体用到的玻璃仪器是 ;
【新知导学】:
二、合作、研讨与点拨
活动一:物质的加热。
(1)酒精灯的使用方法:①禁止向 的酒精灯里添加乙醇;②要用火柴点燃,禁止用 点燃另一只酒精灯;③用 加热;④熄灭时,用 灭,不能用嘴吹;⑤盛酒精量不能超过酒精灯容积的2/3,也不得少于1/4。
(2)给物质加热的方法及注意事项:①加热玻璃仪器时,要把容器壁外的水擦干;②很热的容器不要立即用冷水冲洗.以免受热不匀而破裂;③给盛有液体的试管加热时,试管内液体的量不可超过试管容积的 ;④加热前应先 试管;⑤试管应 放在外焰上;⑥试管口不能朝着 的方向;⑦给试管里的固体药品加热时,试管口要略向 倾斜,受热均匀后再固定加热。
(3)给液体物质加热的仪器可用试管、烧杯、烧瓶等;给固体物质加热,可用干燥的试管。
可直接受热的:试管、蒸发皿、燃烧匙、坩埚等
能间接受热的:烧杯、烧瓶(加热时,需加石棉网)
活动二:玻璃仪器的洗涤。
洗涤方法:①倒去废物(要倒在指定的容器内);②用水冲洗并加以振荡;③用试管刷刷洗;④再用水冲洗。如果玻璃仪器内壁上附着不溶于水的碱、碳酸盐、碱性氧化物等,可先用稀盐酸溶解,再用水冲洗;如果玻璃仪器内壁附有油污,可先用少量纯碱溶液或洗衣粉刷洗,再用水冲洗。
洗涤干净的标准:内外壁附着的水既不聚成水滴,也无成股水流下。
活动三:连接仪器装置
①. 玻璃导管插入塞子
②. 玻璃导管插入胶皮管
③. 塞子塞进容器口
活动四:检查装置气密性
连接好仪器后,先将导管一 ( http: / / www.21cnjy.com )端伸入水中,再用双手紧握容器外壁。如果导管口有气泡冒出,松开手冷却后形成 液柱,说明装置气密性良好。
三、总结、反思与提升
1.使用酒精灯时要注意什么问题?
2.如何取用固体药品和液体药品?
3.使用量筒时要注意什么?
4.同学们到实验室做完实验后,老师检查发现有许多试管破了,请同学们分析一下,可能是哪些原因导致了试管破裂。
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.3 怎样学习和研究化学第3课时
教学目标
1.了解化学仪器的使用
2.掌握化学实验基本操作
教学重点
化学实验基本操作
教学难点
化学实验基本操作中注意事项
教学过程:
【情景创设】播放化学实验室视频
【明确目标】
【回顾、预习与交流】
一、回顾、预习与交流
1.药品取用的“三不原则”是什么?
2.药品取用若没有说明用量,固体和液体分别取多少?
3.实验剩余的药品怎么处理?
4.酒精灯使用时要注意什么问题?
5、给液体加热要注意什么?
6、给固体物质加热要注意什么?
7、气密性如何检查?
二、合作、研讨与点拨
活动一:天平的正确使用方法
称量时,左盘放置_______,右盘放置______。M物=M码 M游码
若物码倒置,则M物=M码 M游码
2、交流讨论:“称一未知质量的药品质量”与“称一定质量的药品”有何异同?
( http: / / www.21cnjy.com )
活动二:过滤与蒸发
1、过滤
(1)过滤:是一种________________________________________的操作
(2)所需仪器: _______________________________________;
(3)操作要点: 一___ ( http: / / www.21cnjy.com )____________________________________;
二_______________________________________;
三 ____________________________________;
(4)过滤过程中玻璃棒的作用:___________________________________;
(5)交流讨论:某同学在进行过滤时,发现过滤了两次仍然浑浊,你认为原因可能有哪些?
( http: / / www.21cnjy.com )
2、蒸发
(1)所需仪器:_______________________________________;
(2)操作要点:一_______________________________________;
二___________________________________;
三 ________________________________________;
(3)蒸发过程中玻璃棒的作用:___________________________________;
三、总结、反思与提升
1、称取5.8克食盐溶解于44.2克水中得到食盐水,并贮存于细口瓶中,贴上标签,注明溶液名称。
2、完成粗盐提纯实验,感知基本实验操作。会分析实验失败可能的原因。
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
1.3 怎样学习和研究化学第4课时
教学目标
1.使学生学会运用科学探究的方法探究镁的性质;;
2.通过铜绿的性质探究实验了解常用的实验仪器,掌握实验基本操作。
3.通过实验认识铜绿的性质。
教学重点
运用科学探究的方法探究镁的性质。
教学难点
科学探究的一般过程。
教学过程:
【情景创设】
【明确目标】
一、回顾、预习与交流
【交流预习内容】
1.药品取用的“三不原则”是什么?
2.药品取用若没有说明用量,固体和液体分别取多少?
3.实验剩余的药品怎么处理?
4.酒精灯使用时要注意什么问题?
二、合作、研讨与点拨
活动一:探究镁的性质。
1.撕开小段镁条,仔细观察,小结出镁的物理性质有:___________________________
2..镁的化学性质一(与氧气作用)
实验步骤 实验现象 实验结论或解释
1取小段镁条,用砂纸打磨
2点燃酒精灯
3用坩埚钳夹持住打磨过的镁条,点燃并移置石棉网上方
4熄灭酒精灯,处理实验废渣
5洗涤试管,整理好实验台
实验结论: 。
镁的化学性质二(与酸作用)
实验步骤 实验现象 实验结论或解释
1取小段镁条,用砂纸打磨
2将打磨过的镁条置于试管内,将其中逐滴滴加稀盐酸
3处理实验废液,洗涤试管,整理好实验台
实验结论: 。
活动二、铜绿的物理性质
1、铜绿是一种 色 体,主要成分是 ,盐酸是一种 色 体
2.铜绿的化学性质一(与酸的作用)
实验步骤 实验现象 实验结论或解释
1取适量铜绿于试管内
2将其中逐滴滴加稀盐酸
3处理实验废液,洗涤试管,整理好实验台
实验结论: 。
铜绿的化学性质二(受热分解)
实验步骤 实验现象 实验结论或解释
1取适量的铜绿放入试管中
2点燃酒精灯
3用试管夹夹住试管
4用酒精灯外焰加热
5熄灭酒精灯
6处理实验废渣,洗涤试管,整理好实验台
实验结论: 。
活动三、科学探究的一般步骤
科学探究的一般过程是①提出问题;② ;③设计方案;④ ;⑤反思评价得出结论
三、【总结、反思与提升】
1.镁条与酸反应,为什么用砂纸打磨打磨?
2.镁条燃烧的实验中,石棉网的作用是什么?
3.铜绿受热常用右图所示实验装置,请思考用该装置进行实验时能观察到哪些现象?在实验操作时需要注意哪些问题?
四、自检、反馈与提升
【课堂小结】学生总结,并完成导学案达标检测部分
【作业布置】导学案课后训练部分
五、【板书设计】
六、【教学反思】
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
