2024年中考化学专题课件:第11讲 构成物质的微粒 元素 物质的分类(共56张PPT)
文档属性
| 名称 | 2024年中考化学专题课件:第11讲 构成物质的微粒 元素 物质的分类(共56张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-05 00:00:00 | ||
图片预览











文档简介
(共56张PPT)
2024年中考化学专题课件
第11讲 构成物质的微粒 元素 物质的分类
知识点1 构成物质的微粒
1.分子
(1)概念:分子是保持物质__________的一种微粒。
(2)常见的由分子构成的物质:①常温下的所有气体(稀有气体除
外)。②一些非气态的物质,如酒精、水、蔗糖。
化学性质
(3)分子的基本性质:①分子总是在不断地______。分子质量越小,
运动得越____;温度越高,分子运动得越____。②分子之间存在着______。
③分子的质量和体积都很____。④同种分子构成的物质化学性质相同,不
同种分子构成的物质化学性质不同。
【温馨提示】分子的基本性质:①可解释物质的溶解、蒸发、扩散,
所有闻到气味的现象。②可解释物质的三态变化、物体的热胀冷缩。
运动
快
快
间隔
小
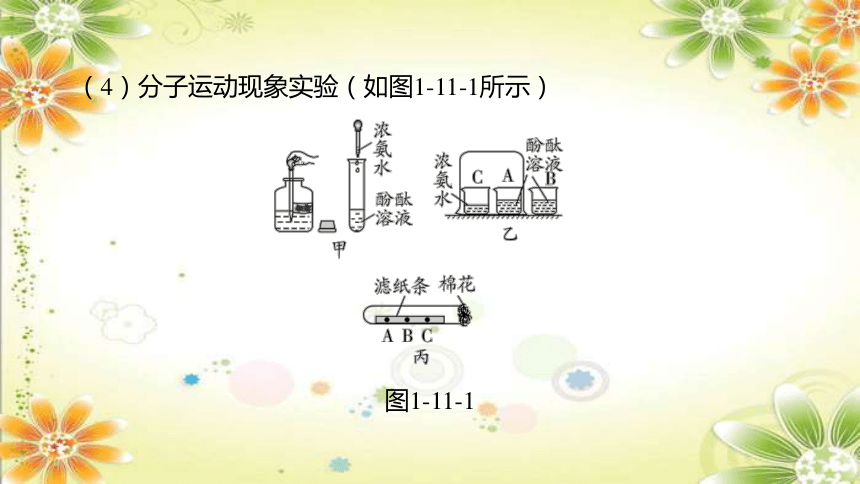
(4)分子运动现象实验(如图1-11-1所示)
图1-11-1
实验现象:图甲中__________________________。图乙中____________
_________________________________。
原因分析:浓氨水有挥发性,氨气分子运动到A烧杯中与水反应生成
氨水,氨水显碱性,可以使无色酚酞溶液变红。
改进实验:如图丙所示,滤纸条上滴无色酚酞溶液,棉花上滴浓氨水。
实验现象:______________________________________________。改
进实验的优点:__________。
浓氨水使无色酚酞溶液变红
A烧杯中无色酚酞溶液变红,B烧杯中无明显现象
滤纸条上滴有无色酚酞溶液的点从右向左依次变红
节省药品
2.原子
(1)概念:原子是__________中的最小微粒。
(2)常见的由原子构成的物质:①金属。②一些固态(常温)物质,
如金刚石、石墨、硅。
化学变化
(3)原子结构
等量关系:原子序数________________ __________
质子数
电子数
核电荷数
【温馨提示】(1)质子数和中子数无等量关系,质子数不一定等于
中子数。(2)不是所有原子核中都有中子,氢原子的原子核中就没有中
子。(3)原子中原子核带的正电荷和核外电子带的负电荷数量相等、电
性相反,所以整个原子对外不显电性。
原子结构示意图如图1-11-2所示(以镁原子为例)
图1-11-2
(4)相对原子质量
概念:一个原子的实际质量与一种碳原子(碳)质量的 的比值。
相对原子质量
单位为___,通常省略不写。 相对原子质量 ________ ________。
1
质子数
中子数
3.离子
(1)概念:带电的原子或原子团。
(2)常见的由离子构成的物质:、 。
(3)表示方法:在元素符号的右上角用“ ”或“-”号表示离子的电性,
数字表示离子的电荷数。______在前,__________在后,数字为1时,省
略不写。
数字
正、负号
(4)分类:①带正电的原子或原子团叫________,如钾离子
(____),钙离子(______),镁离子(______)。
②带负电的原子或原子团叫________,如氯离子(____),氧离子
(_____),氟离子(____)。
(5)意义: 中5表示___________; 2表示_________________
___________。
阳离子
阴离子
5个镁离子
1个镁离子带2个单位的正电荷
知识点2 元素
1.概念:元素是具有相同__________(即________)的一类______的总称。
2.分类
核电荷数
质子数
原子
3.特征:(1)________决定元素的种类,______________决定元素的
化学性质。(2)元素是宏观概念,讲种类,讲质量,不讲个数。(3)化
学反应前后,元素的______不变。
4.书写:由两个字母表示的元素符号第一个字母一定要______,第二
个字母要______,如、 。
5.意义:(1)宏观上表示一种元素。(2)微观上表示一个原子。如
表示________,___________。
【温馨提示】元素符号前面加数字只表示微观含义,如 表示3个铁
原子。
质子数
最外层电子数
种类
大写
小写
氢元素
1个氢原子
6.元素周期表
俄国化学家__________根据元素原子核电荷数依次递增的顺序给元素
编号,编制出了元素周期表。
横行:每一个横行叫一个周期,共有七个周期。
纵列:每一个纵列叫一个族,共有18个纵列,16个族。
门捷列夫
如图1-11-3所示,77表示________, 是元素符号,铱是元素名称,
该元素属于______元素, 是______________。
图1-11-3
质子数
金属
相对原子质量
规律:同一横行(周期)________数相等,____________数从左到右
依次递增一个。元素由金属元素过渡到非金属元素再到稀有气体元素结尾
(第一周期除外)。
同一纵列____________数相等,元素化学性质相似。
电子层
最外层电子
最外层电子
知识点3 物质的分类
【温馨提示】单质是由同种元素组成的纯净物,但由同种元素组成的
物质不一定属于单质,如氧气和臭氧,金刚石和石墨。
重难点突破
01
重点1 微粒结构示意图
1.原子结构示意图
(1)原子结构示意图的认识(图2-11-1)
图2-11-1
决定元素种类:________
决定原子的质量:________________
决定元素的化学性质:____________
__________
质子数
质子数和中子数
原子的最外
层电子数
(2)三决定
【温馨提示】(1)最外层电子数相同,化学性质不一定都相同,如
、 最外层电子数为2。 (2)最外层电子数不同,化学性质有可能相
似,如、 均为稳定结构。
2.离子结构示意图的认识
与原子示意图的区别:当质子数______电子数时,则为原子结构示意
图;当质子数________电子数时,则为离子结构示意图。 当质子数 电
子数时,则为阳离子,如; 当质子数 电子数时,则为阴离子,如
。
等于
不等于
重点2 分子和原子的区别和联系
微粒 分子 原子
相同 点 ①具有微观粒子的共性 ②同种分子(或原子)化学性质相同,不同种分子(或原子)化学 性质不同 ③都具有种类和数量的含义
微粒 分子 原子
不同 点 ①分子是保持物质化学性质的一 种微粒 ②在化学反应中,分子可以分为 原子,原子又可以重新结合成新 的分子 ③分子可以直接构成物质 ①原子是化学变化中的最小微粒
②在化学变化中,原子不可分,不能变为其他原子
③原子可以构成分子,也可以直接构成物质
续表
微粒 分子 原子
联系
续表
易混淆点1
1.氧化物中一定含氧元素,但含氧元素的化合物不一定是氧化物,如
、 是化合物不属于氧化物。
2.有机物一定含碳元素,但含碳元素的化合物不一定是有机物,如
、、 和碳酸盐属于无机物。
3.洁净的空气、干净的矿泉水都是混合物,冰水共存物属于纯净物。
易混淆点2
1.分子是保持物质化学性质的一种微粒,不保持物质的物理性质。
2.稀有气体元素原子的最外层电子数不一定都是8,如 的最外层电
子数是2。
3.原子不一定都是由质子、中子和电子构成的,如氢原子核内没有中子。
4.同种元素的原子的核电荷数一定相同,但核电荷数相同的微粒不一
定是同种元素。
陕西中考链接
02
1.(2023·陕西中考)我国科学家首次突破以二氧化碳为原料获得淀粉的
人工合成工艺技术。其中关键一步反应的微观示意图如图2-11-2所示。
下列有关上述反应的说法不正确的是( )
A
图2-11-2
A.反应涉及6种物质
B.反应前后各类原子的数目不变
C.反应有利于“低碳”目标的落实
D.参加反应的反应物的分子数目比为
1
2
3
4
5
6
7
8
2.(2022·陕西中考)化学物质使世界异彩纷呈。下列物质属于化合物的
是( )
B
A.红色的葡萄酒 B.紫色的高锰酸钾
C.淡蓝色的液氧 D.银白色的不锈钢
3.(2022·陕西中考)从分子、原子角度认识物质是化学科学的重要特征。
下列物质中含有多种分子的是( )
B
A.甲烷 B.空气 C.冰水 D.黄金
1
2
3
4
5
6
7
8
4.(2021·陕西中考)分辨物质是学习化学的基本要求。下列物质属于氧
化物的是( )
B
A.醋 B.冰 C.土 D.银
1
2
3
4
5
6
7
8
5.(2021·陕西中考)宏观辨识与微观探析是化学学科的核心素养之一。
对下列事实的微观解释不正确的是( )
A.金刚石和石墨的物理性质差异大——碳原子的排列方式不同
B.夏天汽车轮胎爆炸——轮胎内气体分子变大
C.化学反应前后各物质质量总和不变——反应前后原子的种类、数目、质
量均不改变
D.氯化钠溶液能导电——溶液中存在可自由移动的离子
B
1
2
3
4
5
6
7
8
6.(2020·陕西中考)认识物质是学习化学的基础。下列物质属于单质的
是( )
C
A.空气 B.干冰 C.液氧 D.生铁
1
2
3
4
5
6
7
8
7.(2023·陕西中考)碳、氢、氧、氮是地球的生命元素。下列说法正确
的是( )
D
A.碳元素能形成多种单质和化合物,其化合物都是有机物
B.氧离子的结构示意图为 ,符号是
C.由氢元素和氧元素组成的物质一定是水,水是由分子构成的
D.这四种元素可以组成铵态氮肥,其不能与碱性物质混合施用
1
2
3
4
5
6
7
8
图2-11-3
8.(2021·陕西中考)“宏观、微观、符号”是
学习化学的重要内容和方法。图2-11-3中甲、乙、
丙是三个变化过程的微观示意图,下列各项分
析正确的是( )
D
A.三个过程发生的均是化学变化
B.图示的所有物质均为化合物
C.三个变化前后原子、分子、离子数目均发生
了改变
D.三个变化后的物质中均含有同一种分子
1
2
3
4
5
6
7
8
核心素养培优
03
1.(2023·广西中考)向液化石油气中添加具有特殊臭味的乙硫醇,一旦
液化石油气泄漏,就能闻到这种臭味,及时采取安全措施。闻到臭味是因
为( )
A
A.分子在不断地运动 B.分子之间有间隔
C.分子的质量很小 D.分子的体积很小
2.(2023·长沙中考)2022年诺贝尔化学奖授予三位科学家,他们研究功
能分子,搭建出复杂的分子结构。下列关于分子的说法正确的是( )
B
A.物质一定是由分子构成的 B.通常分子的质量和体积都很小
C.水变成冰以后分子停止了运动 D.构成和 的分子相同
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3.(2023·黑龙江中考)下列客观事实对应的微观解释错误的是( )
B
A.端午时节,粽叶飘香——分子总是在不断运动着
B.蔗糖放入水中溶解——蔗糖分子分解了
C.氧气和液氧都能支持燃烧——构成物质的分子相同,其化学性质相同
D.水壶中的水烧开沸腾后,壶盖被顶起——水分子间的间隔增大
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
图2-11-4
4.(2023·恩施中考)嫦娥五号带回的月壤中含有大量安
全无污染的核聚变原料 (如图2-11-4所示)。下列
关于 的说法正确的是( )
D
A. 是一种新元素
B. 原子中含有1个质子,2个电子
C. 原子中含有3个质子,没有中子
D. 原子中含有2个质子,1个中子,2个电子
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
图2-11-5
5.(2023·内江中考)图2-11-5为铝原子结构示意图。下
列关于铝原子的说法正确的是( )
D
A.图中“ ”表示铝原子带正电
B.铝原子的质量主要集中在核外13个电子上
C.铝原子在化学反应中易得到电子
D.铝原子核外有3个电子层
6.(2023·随州中考)与元素的化学性质关系最密切的是( )
D
A.元素的相对原子质量 B.元素的核电荷数
C.原子的核外电子数 D.原子的最外层电子数
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
7.(2023·安徽中考)图2-11-6是钠与氯气反应生成氯化钠的示意图。下
列相关说法正确的是( )
B
图2-11-6
A.氯化钠固体由分子构成
B.反应中一个钠原子失去一个
电子,形成相对稳定结构
C.氯原子核外有两个电子层
D.反应中变成 ,证明化学
反应中元素种类发生改变
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
8.(2023·威海中考)碘元素是人体合成甲状腺激素的必要成分。碘元素
在元素周期表中的部分信息及碘原子、氯原子的原子结构示意图如图2-11-
7所示。下列说法不正确的是( )
A
图2-11-7
A.碘的相对原子质量为
B.碘原子在化学反应中易得电子
C.碘元素和氯元素化学性质相似
D.碘元素和氯元素的本质区别是原
子的质子数不同
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
9.(2023· 某校真题)“分类”是认识物质世界的一种重要方法。下列物质
的分类正确的是( )
D
A.赤铁矿、生石灰——氧化物 B.纯碱、烧碱——碱
C.合金、合成纤维——合成材料 D.甲烷、乙醇——有机物
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
图2-11-8
10.(2023·兰州中考)我国科研团队合作完成的
“镁离子电池”项目荣获2022年国际“镁未来技术奖”。
图2-11-8是镁元素的相关信息,下列相关说法不正
确的是( )
D
A.
B.镁属于金属元素
C.镁元素的相对原子质量为24.31
D.在化学反应中,镁原子易失去2个电子变成
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
11.(2023·绥化中考)图中不同小球代表不同原子,其中能表示化合物的
是( )
B
A. B. C. D.
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
图2-11-9
12.(2023·滨州中考)元素周期
表是学习和研究化学的重要工具。
图2-11-9甲中①②为氧元素、铝元
素在元素周期表中的信息示意图,
图2-11-9乙是四种微粒的结构示意
图。请据图回答下列问题。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(1)氧元素位于元素周期表的第____周期,铝元素属于______
(填“金属”或“非金属”)元素。
(2)C微粒是________(填“原子”“阴离子”或“阳离子”);若D是原子,
则 ___。
(3)A、B、C、D中属于同种元素的是____(填字母,下同)。
(4)A微粒的化学性质与图中___微粒的化学性质相似。
二
金属
阴离子
8
B
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
13.(2023·齐齐哈尔中考)宏观和微观相结合是认识物质结构与性质的
重要方法之一。请据图2-11-10回答下列问题。
图2-11-10
(1)图甲是锌元素在元素周期表中的
部分信息,由图可知锌的相对原子质量
是_______。缺锌会引起食欲不振,生
长迟缓,发育不良,锌元素属于人体所
需的______(填“常量”或“微量”)元素。
65.38
微量
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(2)图乙是几种元素的微粒结构示意图,其中具有相对稳定结构的微粒
是____(填字母)。D形成离子的符号是____。 元素处于元素周期表中
第____周期。
四
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
14.(2023·郴州中考)图2-11-11为元素周期表的部分结构。请据图回答
下列问题。
图2-11-11
(1)硅元素在元素周期表中位于第____周期。
(2)表中有两种金属元素,其金属活动性较强的是____(填元素符号)。
三
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(3)画出②的原子结构示意图:_ _______。
(4)表中化学性质最稳定的元素是____(填序号)。
(5)元素①③⑥组成的化合物的化学式为_________。
④
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
15.(2023·岳阳中考)元素周期表是学习和研究化学的重要工具,下面
是元素周期表的部分内容,请根据下表回答问题。
族 周 期 0 0
1 氢1. 008 ⅡA ⅢA ⅣA ⅤA 氦
4.003
2 锂6. 941 铍9. 012 硼1 0.81 碳1 2.01 氮1 4.01 氧1 6.00 氟1 9.00 氖
20.18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3 钠 22.99 镁24.31 铝 26.98 硅 28.09 磷 30.97 硫 32.06 氯 35.45 氩
39.95
(1)发现了元素周期律并编制出元素周期表的化学家是___(填字母)。
A.门捷列夫 B.拉瓦锡
C.道尔顿 D.阿伏加德罗
A
续表
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子
质量为_______。
(3)已知某微粒的结构示意图为 ,请写出该微粒的符号:_____。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化
学式为______。
(5)表中和 的化学性质相似的原因是________________________。
19.00
原子的最外层电子数相同
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
谢 谢
2024年中考化学专题课件
第11讲 构成物质的微粒 元素 物质的分类
知识点1 构成物质的微粒
1.分子
(1)概念:分子是保持物质__________的一种微粒。
(2)常见的由分子构成的物质:①常温下的所有气体(稀有气体除
外)。②一些非气态的物质,如酒精、水、蔗糖。
化学性质
(3)分子的基本性质:①分子总是在不断地______。分子质量越小,
运动得越____;温度越高,分子运动得越____。②分子之间存在着______。
③分子的质量和体积都很____。④同种分子构成的物质化学性质相同,不
同种分子构成的物质化学性质不同。
【温馨提示】分子的基本性质:①可解释物质的溶解、蒸发、扩散,
所有闻到气味的现象。②可解释物质的三态变化、物体的热胀冷缩。
运动
快
快
间隔
小
(4)分子运动现象实验(如图1-11-1所示)
图1-11-1
实验现象:图甲中__________________________。图乙中____________
_________________________________。
原因分析:浓氨水有挥发性,氨气分子运动到A烧杯中与水反应生成
氨水,氨水显碱性,可以使无色酚酞溶液变红。
改进实验:如图丙所示,滤纸条上滴无色酚酞溶液,棉花上滴浓氨水。
实验现象:______________________________________________。改
进实验的优点:__________。
浓氨水使无色酚酞溶液变红
A烧杯中无色酚酞溶液变红,B烧杯中无明显现象
滤纸条上滴有无色酚酞溶液的点从右向左依次变红
节省药品
2.原子
(1)概念:原子是__________中的最小微粒。
(2)常见的由原子构成的物质:①金属。②一些固态(常温)物质,
如金刚石、石墨、硅。
化学变化
(3)原子结构
等量关系:原子序数________________ __________
质子数
电子数
核电荷数
【温馨提示】(1)质子数和中子数无等量关系,质子数不一定等于
中子数。(2)不是所有原子核中都有中子,氢原子的原子核中就没有中
子。(3)原子中原子核带的正电荷和核外电子带的负电荷数量相等、电
性相反,所以整个原子对外不显电性。
原子结构示意图如图1-11-2所示(以镁原子为例)
图1-11-2
(4)相对原子质量
概念:一个原子的实际质量与一种碳原子(碳)质量的 的比值。
相对原子质量
单位为___,通常省略不写。 相对原子质量 ________ ________。
1
质子数
中子数
3.离子
(1)概念:带电的原子或原子团。
(2)常见的由离子构成的物质:、 。
(3)表示方法:在元素符号的右上角用“ ”或“-”号表示离子的电性,
数字表示离子的电荷数。______在前,__________在后,数字为1时,省
略不写。
数字
正、负号
(4)分类:①带正电的原子或原子团叫________,如钾离子
(____),钙离子(______),镁离子(______)。
②带负电的原子或原子团叫________,如氯离子(____),氧离子
(_____),氟离子(____)。
(5)意义: 中5表示___________; 2表示_________________
___________。
阳离子
阴离子
5个镁离子
1个镁离子带2个单位的正电荷
知识点2 元素
1.概念:元素是具有相同__________(即________)的一类______的总称。
2.分类
核电荷数
质子数
原子
3.特征:(1)________决定元素的种类,______________决定元素的
化学性质。(2)元素是宏观概念,讲种类,讲质量,不讲个数。(3)化
学反应前后,元素的______不变。
4.书写:由两个字母表示的元素符号第一个字母一定要______,第二
个字母要______,如、 。
5.意义:(1)宏观上表示一种元素。(2)微观上表示一个原子。如
表示________,___________。
【温馨提示】元素符号前面加数字只表示微观含义,如 表示3个铁
原子。
质子数
最外层电子数
种类
大写
小写
氢元素
1个氢原子
6.元素周期表
俄国化学家__________根据元素原子核电荷数依次递增的顺序给元素
编号,编制出了元素周期表。
横行:每一个横行叫一个周期,共有七个周期。
纵列:每一个纵列叫一个族,共有18个纵列,16个族。
门捷列夫
如图1-11-3所示,77表示________, 是元素符号,铱是元素名称,
该元素属于______元素, 是______________。
图1-11-3
质子数
金属
相对原子质量
规律:同一横行(周期)________数相等,____________数从左到右
依次递增一个。元素由金属元素过渡到非金属元素再到稀有气体元素结尾
(第一周期除外)。
同一纵列____________数相等,元素化学性质相似。
电子层
最外层电子
最外层电子
知识点3 物质的分类
【温馨提示】单质是由同种元素组成的纯净物,但由同种元素组成的
物质不一定属于单质,如氧气和臭氧,金刚石和石墨。
重难点突破
01
重点1 微粒结构示意图
1.原子结构示意图
(1)原子结构示意图的认识(图2-11-1)
图2-11-1
决定元素种类:________
决定原子的质量:________________
决定元素的化学性质:____________
__________
质子数
质子数和中子数
原子的最外
层电子数
(2)三决定
【温馨提示】(1)最外层电子数相同,化学性质不一定都相同,如
、 最外层电子数为2。 (2)最外层电子数不同,化学性质有可能相
似,如、 均为稳定结构。
2.离子结构示意图的认识
与原子示意图的区别:当质子数______电子数时,则为原子结构示意
图;当质子数________电子数时,则为离子结构示意图。 当质子数 电
子数时,则为阳离子,如; 当质子数 电子数时,则为阴离子,如
。
等于
不等于
重点2 分子和原子的区别和联系
微粒 分子 原子
相同 点 ①具有微观粒子的共性 ②同种分子(或原子)化学性质相同,不同种分子(或原子)化学 性质不同 ③都具有种类和数量的含义
微粒 分子 原子
不同 点 ①分子是保持物质化学性质的一 种微粒 ②在化学反应中,分子可以分为 原子,原子又可以重新结合成新 的分子 ③分子可以直接构成物质 ①原子是化学变化中的最小微粒
②在化学变化中,原子不可分,不能变为其他原子
③原子可以构成分子,也可以直接构成物质
续表
微粒 分子 原子
联系
续表
易混淆点1
1.氧化物中一定含氧元素,但含氧元素的化合物不一定是氧化物,如
、 是化合物不属于氧化物。
2.有机物一定含碳元素,但含碳元素的化合物不一定是有机物,如
、、 和碳酸盐属于无机物。
3.洁净的空气、干净的矿泉水都是混合物,冰水共存物属于纯净物。
易混淆点2
1.分子是保持物质化学性质的一种微粒,不保持物质的物理性质。
2.稀有气体元素原子的最外层电子数不一定都是8,如 的最外层电
子数是2。
3.原子不一定都是由质子、中子和电子构成的,如氢原子核内没有中子。
4.同种元素的原子的核电荷数一定相同,但核电荷数相同的微粒不一
定是同种元素。
陕西中考链接
02
1.(2023·陕西中考)我国科学家首次突破以二氧化碳为原料获得淀粉的
人工合成工艺技术。其中关键一步反应的微观示意图如图2-11-2所示。
下列有关上述反应的说法不正确的是( )
A
图2-11-2
A.反应涉及6种物质
B.反应前后各类原子的数目不变
C.反应有利于“低碳”目标的落实
D.参加反应的反应物的分子数目比为
1
2
3
4
5
6
7
8
2.(2022·陕西中考)化学物质使世界异彩纷呈。下列物质属于化合物的
是( )
B
A.红色的葡萄酒 B.紫色的高锰酸钾
C.淡蓝色的液氧 D.银白色的不锈钢
3.(2022·陕西中考)从分子、原子角度认识物质是化学科学的重要特征。
下列物质中含有多种分子的是( )
B
A.甲烷 B.空气 C.冰水 D.黄金
1
2
3
4
5
6
7
8
4.(2021·陕西中考)分辨物质是学习化学的基本要求。下列物质属于氧
化物的是( )
B
A.醋 B.冰 C.土 D.银
1
2
3
4
5
6
7
8
5.(2021·陕西中考)宏观辨识与微观探析是化学学科的核心素养之一。
对下列事实的微观解释不正确的是( )
A.金刚石和石墨的物理性质差异大——碳原子的排列方式不同
B.夏天汽车轮胎爆炸——轮胎内气体分子变大
C.化学反应前后各物质质量总和不变——反应前后原子的种类、数目、质
量均不改变
D.氯化钠溶液能导电——溶液中存在可自由移动的离子
B
1
2
3
4
5
6
7
8
6.(2020·陕西中考)认识物质是学习化学的基础。下列物质属于单质的
是( )
C
A.空气 B.干冰 C.液氧 D.生铁
1
2
3
4
5
6
7
8
7.(2023·陕西中考)碳、氢、氧、氮是地球的生命元素。下列说法正确
的是( )
D
A.碳元素能形成多种单质和化合物,其化合物都是有机物
B.氧离子的结构示意图为 ,符号是
C.由氢元素和氧元素组成的物质一定是水,水是由分子构成的
D.这四种元素可以组成铵态氮肥,其不能与碱性物质混合施用
1
2
3
4
5
6
7
8
图2-11-3
8.(2021·陕西中考)“宏观、微观、符号”是
学习化学的重要内容和方法。图2-11-3中甲、乙、
丙是三个变化过程的微观示意图,下列各项分
析正确的是( )
D
A.三个过程发生的均是化学变化
B.图示的所有物质均为化合物
C.三个变化前后原子、分子、离子数目均发生
了改变
D.三个变化后的物质中均含有同一种分子
1
2
3
4
5
6
7
8
核心素养培优
03
1.(2023·广西中考)向液化石油气中添加具有特殊臭味的乙硫醇,一旦
液化石油气泄漏,就能闻到这种臭味,及时采取安全措施。闻到臭味是因
为( )
A
A.分子在不断地运动 B.分子之间有间隔
C.分子的质量很小 D.分子的体积很小
2.(2023·长沙中考)2022年诺贝尔化学奖授予三位科学家,他们研究功
能分子,搭建出复杂的分子结构。下列关于分子的说法正确的是( )
B
A.物质一定是由分子构成的 B.通常分子的质量和体积都很小
C.水变成冰以后分子停止了运动 D.构成和 的分子相同
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3.(2023·黑龙江中考)下列客观事实对应的微观解释错误的是( )
B
A.端午时节,粽叶飘香——分子总是在不断运动着
B.蔗糖放入水中溶解——蔗糖分子分解了
C.氧气和液氧都能支持燃烧——构成物质的分子相同,其化学性质相同
D.水壶中的水烧开沸腾后,壶盖被顶起——水分子间的间隔增大
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
图2-11-4
4.(2023·恩施中考)嫦娥五号带回的月壤中含有大量安
全无污染的核聚变原料 (如图2-11-4所示)。下列
关于 的说法正确的是( )
D
A. 是一种新元素
B. 原子中含有1个质子,2个电子
C. 原子中含有3个质子,没有中子
D. 原子中含有2个质子,1个中子,2个电子
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
图2-11-5
5.(2023·内江中考)图2-11-5为铝原子结构示意图。下
列关于铝原子的说法正确的是( )
D
A.图中“ ”表示铝原子带正电
B.铝原子的质量主要集中在核外13个电子上
C.铝原子在化学反应中易得到电子
D.铝原子核外有3个电子层
6.(2023·随州中考)与元素的化学性质关系最密切的是( )
D
A.元素的相对原子质量 B.元素的核电荷数
C.原子的核外电子数 D.原子的最外层电子数
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
7.(2023·安徽中考)图2-11-6是钠与氯气反应生成氯化钠的示意图。下
列相关说法正确的是( )
B
图2-11-6
A.氯化钠固体由分子构成
B.反应中一个钠原子失去一个
电子,形成相对稳定结构
C.氯原子核外有两个电子层
D.反应中变成 ,证明化学
反应中元素种类发生改变
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
8.(2023·威海中考)碘元素是人体合成甲状腺激素的必要成分。碘元素
在元素周期表中的部分信息及碘原子、氯原子的原子结构示意图如图2-11-
7所示。下列说法不正确的是( )
A
图2-11-7
A.碘的相对原子质量为
B.碘原子在化学反应中易得电子
C.碘元素和氯元素化学性质相似
D.碘元素和氯元素的本质区别是原
子的质子数不同
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
9.(2023· 某校真题)“分类”是认识物质世界的一种重要方法。下列物质
的分类正确的是( )
D
A.赤铁矿、生石灰——氧化物 B.纯碱、烧碱——碱
C.合金、合成纤维——合成材料 D.甲烷、乙醇——有机物
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
图2-11-8
10.(2023·兰州中考)我国科研团队合作完成的
“镁离子电池”项目荣获2022年国际“镁未来技术奖”。
图2-11-8是镁元素的相关信息,下列相关说法不正
确的是( )
D
A.
B.镁属于金属元素
C.镁元素的相对原子质量为24.31
D.在化学反应中,镁原子易失去2个电子变成
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
11.(2023·绥化中考)图中不同小球代表不同原子,其中能表示化合物的
是( )
B
A. B. C. D.
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
图2-11-9
12.(2023·滨州中考)元素周期
表是学习和研究化学的重要工具。
图2-11-9甲中①②为氧元素、铝元
素在元素周期表中的信息示意图,
图2-11-9乙是四种微粒的结构示意
图。请据图回答下列问题。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(1)氧元素位于元素周期表的第____周期,铝元素属于______
(填“金属”或“非金属”)元素。
(2)C微粒是________(填“原子”“阴离子”或“阳离子”);若D是原子,
则 ___。
(3)A、B、C、D中属于同种元素的是____(填字母,下同)。
(4)A微粒的化学性质与图中___微粒的化学性质相似。
二
金属
阴离子
8
B
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
13.(2023·齐齐哈尔中考)宏观和微观相结合是认识物质结构与性质的
重要方法之一。请据图2-11-10回答下列问题。
图2-11-10
(1)图甲是锌元素在元素周期表中的
部分信息,由图可知锌的相对原子质量
是_______。缺锌会引起食欲不振,生
长迟缓,发育不良,锌元素属于人体所
需的______(填“常量”或“微量”)元素。
65.38
微量
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(2)图乙是几种元素的微粒结构示意图,其中具有相对稳定结构的微粒
是____(填字母)。D形成离子的符号是____。 元素处于元素周期表中
第____周期。
四
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
14.(2023·郴州中考)图2-11-11为元素周期表的部分结构。请据图回答
下列问题。
图2-11-11
(1)硅元素在元素周期表中位于第____周期。
(2)表中有两种金属元素,其金属活动性较强的是____(填元素符号)。
三
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(3)画出②的原子结构示意图:_ _______。
(4)表中化学性质最稳定的元素是____(填序号)。
(5)元素①③⑥组成的化合物的化学式为_________。
④
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
15.(2023·岳阳中考)元素周期表是学习和研究化学的重要工具,下面
是元素周期表的部分内容,请根据下表回答问题。
族 周 期 0 0
1 氢1. 008 ⅡA ⅢA ⅣA ⅤA 氦
4.003
2 锂6. 941 铍9. 012 硼1 0.81 碳1 2.01 氮1 4.01 氧1 6.00 氟1 9.00 氖
20.18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3 钠 22.99 镁24.31 铝 26.98 硅 28.09 磷 30.97 硫 32.06 氯 35.45 氩
39.95
(1)发现了元素周期律并编制出元素周期表的化学家是___(填字母)。
A.门捷列夫 B.拉瓦锡
C.道尔顿 D.阿伏加德罗
A
续表
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子
质量为_______。
(3)已知某微粒的结构示意图为 ,请写出该微粒的符号:_____。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化
学式为______。
(5)表中和 的化学性质相似的原因是________________________。
19.00
原子的最外层电子数相同
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
谢 谢
同课章节目录
