7.1.1碳原子的成键特点 甲烷课件(共28张ppt)化学人教版(2019)必修第二册
文档属性
| 名称 | 7.1.1碳原子的成键特点 甲烷课件(共28张ppt)化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 44.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-05 00:00:00 | ||
图片预览




文档简介
(共28张PPT)
课时1 碳原子的成键特点 甲烷
第七章 有机化合物
第一节 认识有机化合物
学习目标
1、掌握有机化合物的概念,熟悉有机化合物中碳原子的成键特点,初步了解有机物种类繁多的原因
2、掌握甲烷的结构、性质及用途
硫及其化合物的研究思路
非金属单质
非金属氧化物
酸
盐
SO2
SO3
S
H2SO3
H2SO4
研究每一种物质的方法:价态和类别两个角度
SO32-
SO42-
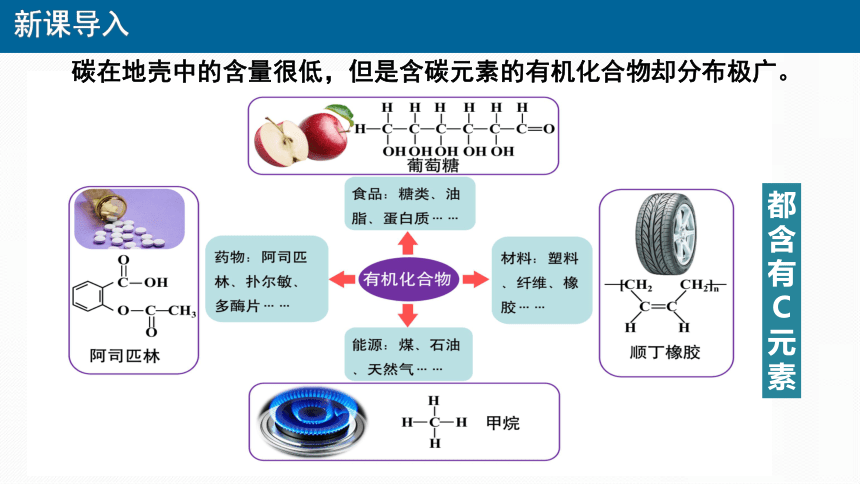
都含有C元素
新课导入
碳在地壳中的含量很低,但是含碳元素的有机化合物却分布极广。
探究课堂
任务一:有机化合物
一般把含碳元素的化合物称为有机化合物,简称为有机物 。
1、定义:
但不是所有含碳的化合物都是有机物。
注意:CO、CO2、H2CO3、碳酸盐、碳酸氢盐、金属碳化物, 简单碳化物(如:SiC) CN-,SCN- (如:KSCN)等虽含有碳元素,其性质跟无机物很相似,把它们归为无机物。
3、烃:
有机物的种类很多,我们把只含碳、氢元素的有机物叫烃。
除碳元素,一般还含H、O、N、S、P、卤素等元素。
2、组成:
目前发现和合成的物质,绝大多数是有机物,超过了1亿种!
探究课堂
任务二:有机物中碳原子的成键特点
1、请书写碳原子的原子结构示意图、碳原子的电子式。
2 4
+6
.
·C·
˙
2、甲烷(CH4)属于烷烃,是最简单的有机化合物,请书写其电子式和结构式。
3、思考碳原子具有怎样的结构和成键特点?
碳原子最外层有4个电子,不易得到或失去电子,而易通过共价键与碳原子或其它非金属原子相结合,易形成4个共价键。
探究课堂
C
C
H
H
H
H
H
H
C
C
H
H
H
H
H
H
C
C
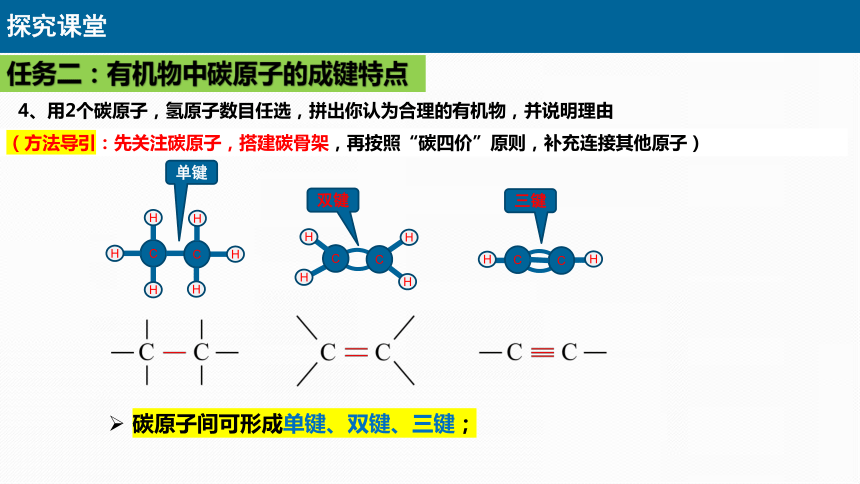
(方法导引:先关注碳原子,搭建碳骨架,再按照“碳四价”原则,补充连接其他原子)
单键
双键
三键
4、用2个碳原子,氢原子数目任选,拼出你认为合理的有机物,并说明理由
任务二:有机物中碳原子的成键特点
碳原子间可形成单键、双键、三键;
探究课堂
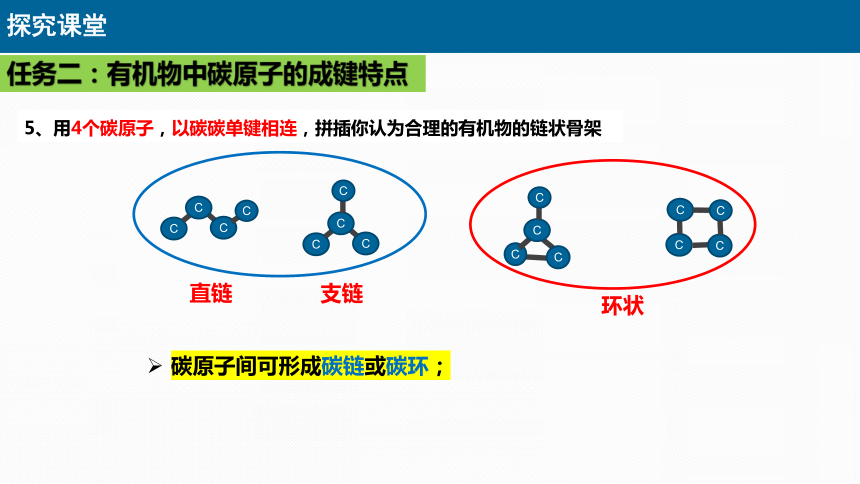
5、用4个碳原子,以碳碳单键相连,拼插你认为合理的有机物的链状骨架
C
C
C
C
C
C
C
C
C
C
C
C
C
C
C
C
直链
环状
支链
任务二:有机物中碳原子的成键特点
碳原子间可形成碳链或碳环;
探究课堂
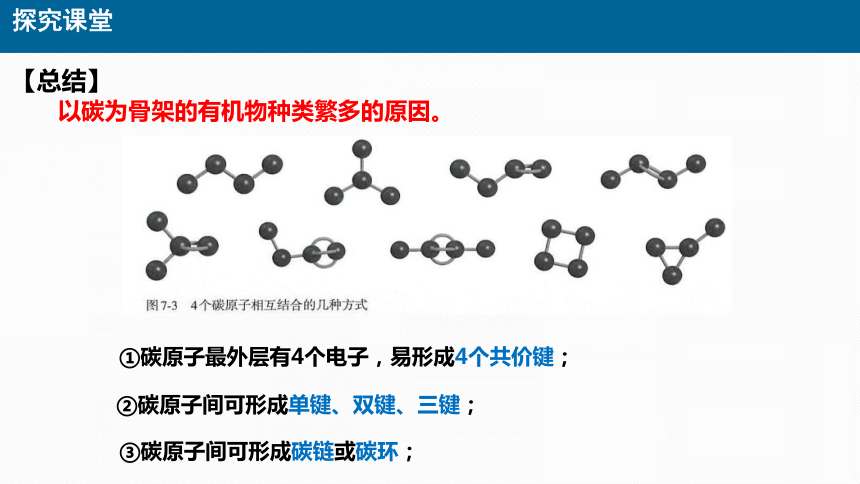
【总结】
以碳为骨架的有机物种类繁多的原因。
①碳原子最外层有4个电子,易形成4个共价键;
②碳原子间可形成单键、双键、三键;
③碳原子间可形成碳链或碳环;
探究课堂
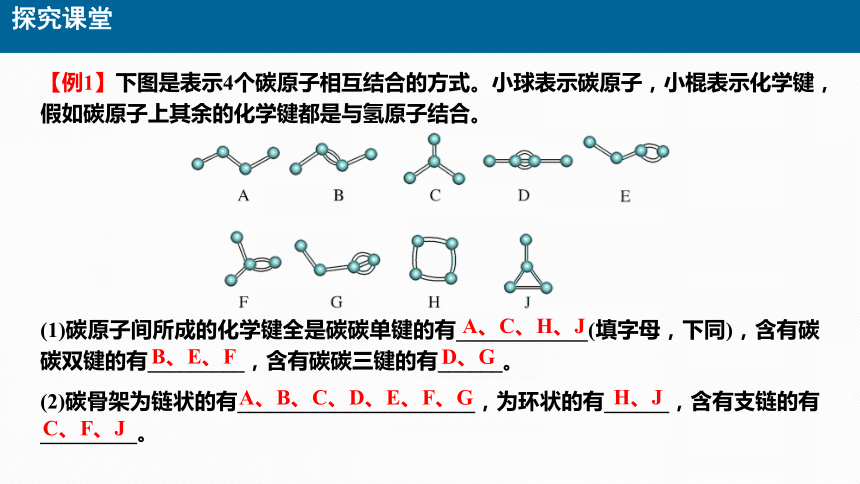
【例1】下图是表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合。
(1)碳原子间所成的化学键全是碳碳单键的有____________(填字母,下同),含有碳碳双键的有_________,含有碳碳三键的有______。
A、C、H、J
B、E、F
D、G
(2)碳骨架为链状的有______________________,为环状的有______,含有支链的有_________。
A、B、C、D、E、F、G
H、J
C、F、J
探究课堂
3000年前甲烷的记载:《周易》“泽中有火。”
……我在湖边淤泥中收集到一种无色、无味气体,用木棒搅动淤泥,让冒出的气泡通入倒扣的、充满水的瓶中。点燃这种气体,火焰呈蓝色,燃烧较慢,且和氢气的燃烧不同……
1776年,意大利物理学家伏特在湖边淤泥中收集到甲烷
无色无味气体
密度比空气小
极难溶于水
甲烷物理性质
甲烷的发现之旅
任务三:最简单的烷烃----甲烷
1790年,英国医生奥斯汀发表甲烷燃烧报告:甲烷燃烧生成水和二氧化碳,确定甲烷是碳氢化合物,随后科学家测得分子式。
1858年,德国化学家凯库勒提出了碳原子是四价的概念,俄国的布特列洛夫提出了分子中原子排列的状况
结构式仅能表明各原子的连接顺序,不能体现空间位置关系
甲烷的结构到底是怎么样的呢?
甲烷的发现之旅
探究课堂
1874年,荷兰化学家范特霍夫也在为这个问题苦恼着。。。。
氢原子
碳原子
化学键
你能帮范特霍夫搭建一些甲烷结构吗?
甲烷的发现之旅
绝世天才
物理化学创始人
第一届诺贝尔奖得主
探究课堂
范特霍夫温馨提示:
他认为:自然界中一切稳定的结构都趋向于最小能量状态,这种情况只有当氢原子均匀地分布在碳原子周围的空间时才能达到。
∠HCH=90°或180°
∠HCH=109°28’
平面正方形
正四面体
1874年,范特霍夫提出了甲烷为正四面体的假说
甲烷的发现之旅
探究课堂
正四面体
20世纪,利用X射线和电子衍射测得甲烷结构信息:
(1)碳原子位于正四面体的中心,4个氢原子位于正四面体的4个顶点上。
(2)4个C—H的键长和键能相同,相互之间夹角相等都为109°28’
1916年路易斯确定甲烷的电子式
球棍模型
填充模型
甲烷的发现之旅
探究课堂
分子结构示意图:
球棍模型
填充模型
化学式: CH4
电子式:
结构式:
1、甲烷的结构
结构特点
(1)碳原子位于正四面体的中心,4个氢原子位于正四面体的4个顶点上。
(2)4个C—H的键长和键能相同,相互之间夹角相等,都为109°28’。
甲烷的发现之旅
探究课堂
探究课堂
通常情况下,烷烃比较稳定,与强酸、强碱或高锰酸钾等强氧化剂不发生反应。
稳定性
2、甲烷的化学性质
探究课堂
1885年,罗伯特·本生发明了一种能安全燃烧混合天然气和空气的装置:本生灯,本生灯的大范围推广也使得人们开始把天然气应用于烹饪和取暖,天然气逐渐走进千家万户.
烷烃的稳定性是相对的,在特定的条件下,烷烃也会发生某些反应。
(1)氧化反应——可燃性
CH4 + 2O2 CO2 + 2H2O
点燃
甲烷可以在空气中完全燃烧,发生氧化反应,
生成二氧化碳和水,并放出大量的热。
明亮的淡蓝色火焰,放出大量的热。无烟
煤矿中的爆炸事故多与甲烷气体爆炸有关。
为了保证安全生产,必须采取通风、严禁烟火等措施。点燃之前要验纯。
现象:
结论:
化学方程式:
注意:有机反应方程式书写用“ → ”不用“=”
探究课堂
1930年,美国杜邦公司的米奇利利用甲烷合成了一种神秘物质,很快全世界几乎所有的冰箱、空调都用上了它,你知道它的成分吗?
氟利昂
CCl2F2
【实验7-1】取两支试管,均通过排饱和NaCl溶液的方法收集半试管CH4,和半试管Cl2,分别用铁架台固定好(如图7-8)。将其中一支试管用铝箔套上,另一支试管放在光亮处(不要放在日光直射的地方)。静置,比较两支试管内的现象。
(2)甲烷的取代反应
探究课堂
探究课堂
实验现象 原因分析
无光照
光照
无明显变化
无光照该反应不能发生
试管内气体颜色变浅
氯气逐渐消耗
试管壁上有油状液滴
生成不溶于水的液体
试管中液面上升
生成的气体溶于水中使试管内压强减小
水槽中有固体析出
Cl-饱和
可能观察到白雾
生成了易溶于水的HCl气体
探究课堂
反应中的HCl是如何形成的?
Cl—Cl
+
光
C
H
H
H
Cl
Cl
H
+
CH4 + Cl2 CH3Cl + HCl
光
用途
状态
沸点
水溶性
一氯甲烷(CH3Cl)
常温下是气体
难溶于水
-24.2 ℃
可用作溶剂、冷冻剂、香料等
探究课堂
Cl—Cl
+
光
C
H
H
Cl
Cl
H
+
用途
状态
沸点
水溶性
二氯甲烷(CH2Cl2)
C
H
H
H
Cl
Cl
CH3Cl + Cl2 CH2Cl2 + HCl
光
常温下是油状液体
难溶于水
39.8 ℃
用作牙科局部麻醉剂
探究课堂
CH2Cl2 + Cl2 CHCl3 + HCl
光
Cl—Cl
+
光
C
H
Cl
Cl
H
+
用途
状态
沸点
水溶性
三氯甲烷(CHCl3)
C
H
H
Cl
Cl
Cl
Cl
难溶于水
61.7 ℃
主要用来生产氟利昂,常用作有机溶剂
常温下是油状液体
探究课堂
CH2Cl3 + Cl2 CCl4 + HCl
光
Cl—Cl
+
光
C
Cl
Cl
H
+
用途
状态
沸点
水溶性
四氯化碳(CCl4)
C
H
Cl
Cl
Cl
Cl
Cl
Cl
难溶于水
76.5 ℃
主要用作优良的溶剂
常温下是油状液体
探究课堂
Cl2与CH4反应生成了五种产物:CH3Cl、CH2Cl2、CHCl3、CCl4、HCl。
其中___________最多。有机产物中只有___________在常温下是气体,其他均为液体。
HCl
CH3Cl
有机物分子里某些原子或原子团被其他原子或原子团所替代的反应叫做取代反应。
特点:
一上一下,取而代之
反应的条件:
b. 与气态的纯卤素单质反应 X2(g)
a. 光照(不宜太强,以免爆炸)
探究课堂
2022年美国的“清洁”炭黑制造商投资3亿多美元的资金,用来支持甲烷为原料的“下一代”氢、和碳项目的研发。
该公司通过商业规模的甲烷热解的突破性专利技术生产氢气和炭黑
CH4 C + 2H2
高温
(3)甲烷的热分解
探究课堂
取代反应 置换反应
定义 有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应 一种单质跟一种化合物反应,生成另一种化合物和另一种单质的反应。
反应物 一种化合物和一种单质或化合物(反应物中至少有一种是有机物) 一种单质和一种化合物
生成物 一般生成两种化合物 另一种化合物和另一种单质
电子转移 不一定发生电子转移,因此不一定是氧化还原反应 一定发生电子的转移
反应特点 很多反应是可逆反应,副反应较多,用“→” 连接 一般是不可逆反应,用“=”连接
取代反应与置换反应的区别
探究课堂
课时1 碳原子的成键特点 甲烷
第七章 有机化合物
第一节 认识有机化合物
学习目标
1、掌握有机化合物的概念,熟悉有机化合物中碳原子的成键特点,初步了解有机物种类繁多的原因
2、掌握甲烷的结构、性质及用途
硫及其化合物的研究思路
非金属单质
非金属氧化物
酸
盐
SO2
SO3
S
H2SO3
H2SO4
研究每一种物质的方法:价态和类别两个角度
SO32-
SO42-
都含有C元素
新课导入
碳在地壳中的含量很低,但是含碳元素的有机化合物却分布极广。
探究课堂
任务一:有机化合物
一般把含碳元素的化合物称为有机化合物,简称为有机物 。
1、定义:
但不是所有含碳的化合物都是有机物。
注意:CO、CO2、H2CO3、碳酸盐、碳酸氢盐、金属碳化物, 简单碳化物(如:SiC) CN-,SCN- (如:KSCN)等虽含有碳元素,其性质跟无机物很相似,把它们归为无机物。
3、烃:
有机物的种类很多,我们把只含碳、氢元素的有机物叫烃。
除碳元素,一般还含H、O、N、S、P、卤素等元素。
2、组成:
目前发现和合成的物质,绝大多数是有机物,超过了1亿种!
探究课堂
任务二:有机物中碳原子的成键特点
1、请书写碳原子的原子结构示意图、碳原子的电子式。
2 4
+6
.
·C·
˙
2、甲烷(CH4)属于烷烃,是最简单的有机化合物,请书写其电子式和结构式。
3、思考碳原子具有怎样的结构和成键特点?
碳原子最外层有4个电子,不易得到或失去电子,而易通过共价键与碳原子或其它非金属原子相结合,易形成4个共价键。
探究课堂
C
C
H
H
H
H
H
H
C
C
H
H
H
H
H
H
C
C
(方法导引:先关注碳原子,搭建碳骨架,再按照“碳四价”原则,补充连接其他原子)
单键
双键
三键
4、用2个碳原子,氢原子数目任选,拼出你认为合理的有机物,并说明理由
任务二:有机物中碳原子的成键特点
碳原子间可形成单键、双键、三键;
探究课堂
5、用4个碳原子,以碳碳单键相连,拼插你认为合理的有机物的链状骨架
C
C
C
C
C
C
C
C
C
C
C
C
C
C
C
C
直链
环状
支链
任务二:有机物中碳原子的成键特点
碳原子间可形成碳链或碳环;
探究课堂
【总结】
以碳为骨架的有机物种类繁多的原因。
①碳原子最外层有4个电子,易形成4个共价键;
②碳原子间可形成单键、双键、三键;
③碳原子间可形成碳链或碳环;
探究课堂
【例1】下图是表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合。
(1)碳原子间所成的化学键全是碳碳单键的有____________(填字母,下同),含有碳碳双键的有_________,含有碳碳三键的有______。
A、C、H、J
B、E、F
D、G
(2)碳骨架为链状的有______________________,为环状的有______,含有支链的有_________。
A、B、C、D、E、F、G
H、J
C、F、J
探究课堂
3000年前甲烷的记载:《周易》“泽中有火。”
……我在湖边淤泥中收集到一种无色、无味气体,用木棒搅动淤泥,让冒出的气泡通入倒扣的、充满水的瓶中。点燃这种气体,火焰呈蓝色,燃烧较慢,且和氢气的燃烧不同……
1776年,意大利物理学家伏特在湖边淤泥中收集到甲烷
无色无味气体
密度比空气小
极难溶于水
甲烷物理性质
甲烷的发现之旅
任务三:最简单的烷烃----甲烷
1790年,英国医生奥斯汀发表甲烷燃烧报告:甲烷燃烧生成水和二氧化碳,确定甲烷是碳氢化合物,随后科学家测得分子式。
1858年,德国化学家凯库勒提出了碳原子是四价的概念,俄国的布特列洛夫提出了分子中原子排列的状况
结构式仅能表明各原子的连接顺序,不能体现空间位置关系
甲烷的结构到底是怎么样的呢?
甲烷的发现之旅
探究课堂
1874年,荷兰化学家范特霍夫也在为这个问题苦恼着。。。。
氢原子
碳原子
化学键
你能帮范特霍夫搭建一些甲烷结构吗?
甲烷的发现之旅
绝世天才
物理化学创始人
第一届诺贝尔奖得主
探究课堂
范特霍夫温馨提示:
他认为:自然界中一切稳定的结构都趋向于最小能量状态,这种情况只有当氢原子均匀地分布在碳原子周围的空间时才能达到。
∠HCH=90°或180°
∠HCH=109°28’
平面正方形
正四面体
1874年,范特霍夫提出了甲烷为正四面体的假说
甲烷的发现之旅
探究课堂
正四面体
20世纪,利用X射线和电子衍射测得甲烷结构信息:
(1)碳原子位于正四面体的中心,4个氢原子位于正四面体的4个顶点上。
(2)4个C—H的键长和键能相同,相互之间夹角相等都为109°28’
1916年路易斯确定甲烷的电子式
球棍模型
填充模型
甲烷的发现之旅
探究课堂
分子结构示意图:
球棍模型
填充模型
化学式: CH4
电子式:
结构式:
1、甲烷的结构
结构特点
(1)碳原子位于正四面体的中心,4个氢原子位于正四面体的4个顶点上。
(2)4个C—H的键长和键能相同,相互之间夹角相等,都为109°28’。
甲烷的发现之旅
探究课堂
探究课堂
通常情况下,烷烃比较稳定,与强酸、强碱或高锰酸钾等强氧化剂不发生反应。
稳定性
2、甲烷的化学性质
探究课堂
1885年,罗伯特·本生发明了一种能安全燃烧混合天然气和空气的装置:本生灯,本生灯的大范围推广也使得人们开始把天然气应用于烹饪和取暖,天然气逐渐走进千家万户.
烷烃的稳定性是相对的,在特定的条件下,烷烃也会发生某些反应。
(1)氧化反应——可燃性
CH4 + 2O2 CO2 + 2H2O
点燃
甲烷可以在空气中完全燃烧,发生氧化反应,
生成二氧化碳和水,并放出大量的热。
明亮的淡蓝色火焰,放出大量的热。无烟
煤矿中的爆炸事故多与甲烷气体爆炸有关。
为了保证安全生产,必须采取通风、严禁烟火等措施。点燃之前要验纯。
现象:
结论:
化学方程式:
注意:有机反应方程式书写用“ → ”不用“=”
探究课堂
1930年,美国杜邦公司的米奇利利用甲烷合成了一种神秘物质,很快全世界几乎所有的冰箱、空调都用上了它,你知道它的成分吗?
氟利昂
CCl2F2
【实验7-1】取两支试管,均通过排饱和NaCl溶液的方法收集半试管CH4,和半试管Cl2,分别用铁架台固定好(如图7-8)。将其中一支试管用铝箔套上,另一支试管放在光亮处(不要放在日光直射的地方)。静置,比较两支试管内的现象。
(2)甲烷的取代反应
探究课堂
探究课堂
实验现象 原因分析
无光照
光照
无明显变化
无光照该反应不能发生
试管内气体颜色变浅
氯气逐渐消耗
试管壁上有油状液滴
生成不溶于水的液体
试管中液面上升
生成的气体溶于水中使试管内压强减小
水槽中有固体析出
Cl-饱和
可能观察到白雾
生成了易溶于水的HCl气体
探究课堂
反应中的HCl是如何形成的?
Cl—Cl
+
光
C
H
H
H
Cl
Cl
H
+
CH4 + Cl2 CH3Cl + HCl
光
用途
状态
沸点
水溶性
一氯甲烷(CH3Cl)
常温下是气体
难溶于水
-24.2 ℃
可用作溶剂、冷冻剂、香料等
探究课堂
Cl—Cl
+
光
C
H
H
Cl
Cl
H
+
用途
状态
沸点
水溶性
二氯甲烷(CH2Cl2)
C
H
H
H
Cl
Cl
CH3Cl + Cl2 CH2Cl2 + HCl
光
常温下是油状液体
难溶于水
39.8 ℃
用作牙科局部麻醉剂
探究课堂
CH2Cl2 + Cl2 CHCl3 + HCl
光
Cl—Cl
+
光
C
H
Cl
Cl
H
+
用途
状态
沸点
水溶性
三氯甲烷(CHCl3)
C
H
H
Cl
Cl
Cl
Cl
难溶于水
61.7 ℃
主要用来生产氟利昂,常用作有机溶剂
常温下是油状液体
探究课堂
CH2Cl3 + Cl2 CCl4 + HCl
光
Cl—Cl
+
光
C
Cl
Cl
H
+
用途
状态
沸点
水溶性
四氯化碳(CCl4)
C
H
Cl
Cl
Cl
Cl
Cl
Cl
难溶于水
76.5 ℃
主要用作优良的溶剂
常温下是油状液体
探究课堂
Cl2与CH4反应生成了五种产物:CH3Cl、CH2Cl2、CHCl3、CCl4、HCl。
其中___________最多。有机产物中只有___________在常温下是气体,其他均为液体。
HCl
CH3Cl
有机物分子里某些原子或原子团被其他原子或原子团所替代的反应叫做取代反应。
特点:
一上一下,取而代之
反应的条件:
b. 与气态的纯卤素单质反应 X2(g)
a. 光照(不宜太强,以免爆炸)
探究课堂
2022年美国的“清洁”炭黑制造商投资3亿多美元的资金,用来支持甲烷为原料的“下一代”氢、和碳项目的研发。
该公司通过商业规模的甲烷热解的突破性专利技术生产氢气和炭黑
CH4 C + 2H2
高温
(3)甲烷的热分解
探究课堂
取代反应 置换反应
定义 有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应 一种单质跟一种化合物反应,生成另一种化合物和另一种单质的反应。
反应物 一种化合物和一种单质或化合物(反应物中至少有一种是有机物) 一种单质和一种化合物
生成物 一般生成两种化合物 另一种化合物和另一种单质
电子转移 不一定发生电子转移,因此不一定是氧化还原反应 一定发生电子的转移
反应特点 很多反应是可逆反应,副反应较多,用“→” 连接 一般是不可逆反应,用“=”连接
取代反应与置换反应的区别
探究课堂
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
