第七章第二节 乙烯与有机高分子材料训练题(含解析)2023-2024学年高一化学人教版(2019)必修第二册
文档属性
| 名称 | 第七章第二节 乙烯与有机高分子材料训练题(含解析)2023-2024学年高一化学人教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-05 00:00:00 | ||
图片预览



文档简介
第二节 乙烯与有机高分子材料
时间:75分钟 满分:100分
一、单选题(每题3分,共45分)
1.化学与生活、环境密切相关。下列说法错误的是
A.以二氧化碳为原料合成淀粉有助于实现“碳达峰”和“碳中和”
B.防控新冠病毒所用消毒酒精的主要成分为乙酸
C.酱油中添加铁强化剂,可减少缺铁性贫血的发生
D.工业上合成氯乙烷采用加成反应比采用取代反应更符合绿色化学理念
2.既能够用于鉴别甲烷和乙烯,又能除去甲烷中乙烯的试剂是
A.溴水 B.点燃 C.通入Cl2 D.酸性高锰酸钾溶液
3.下列物质中,不能通过乙烯的加成反应一步制得的是
A. B. C. D.
4.由乙烯推测丙烯(CH3CH=CH2)的结构或性质,正确的是
A.分子中3个碳原子在同一直线上 B.分子中所有原子在同一平面上
C.不能使酸性高锰酸钾溶液褪色 D.能发生加聚反应
5.下列反应属于加成反应的是
A.C2H4+3O22CO2+2H2O B.CH2=CH2+H2→CH3CH3
C.2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ D.CH3CH2OHCH2=CH2↑+H2O
6.下列有关说法中,正确的是
A.塑料、纤维和橡胶都属于合成材料
B.聚氯乙烯可制成薄膜、软管等,其单体是CHCl=CHCl
C.互为同系物
D.合成顺丁橡胶()的单体是CH2=CH—CH=CH2
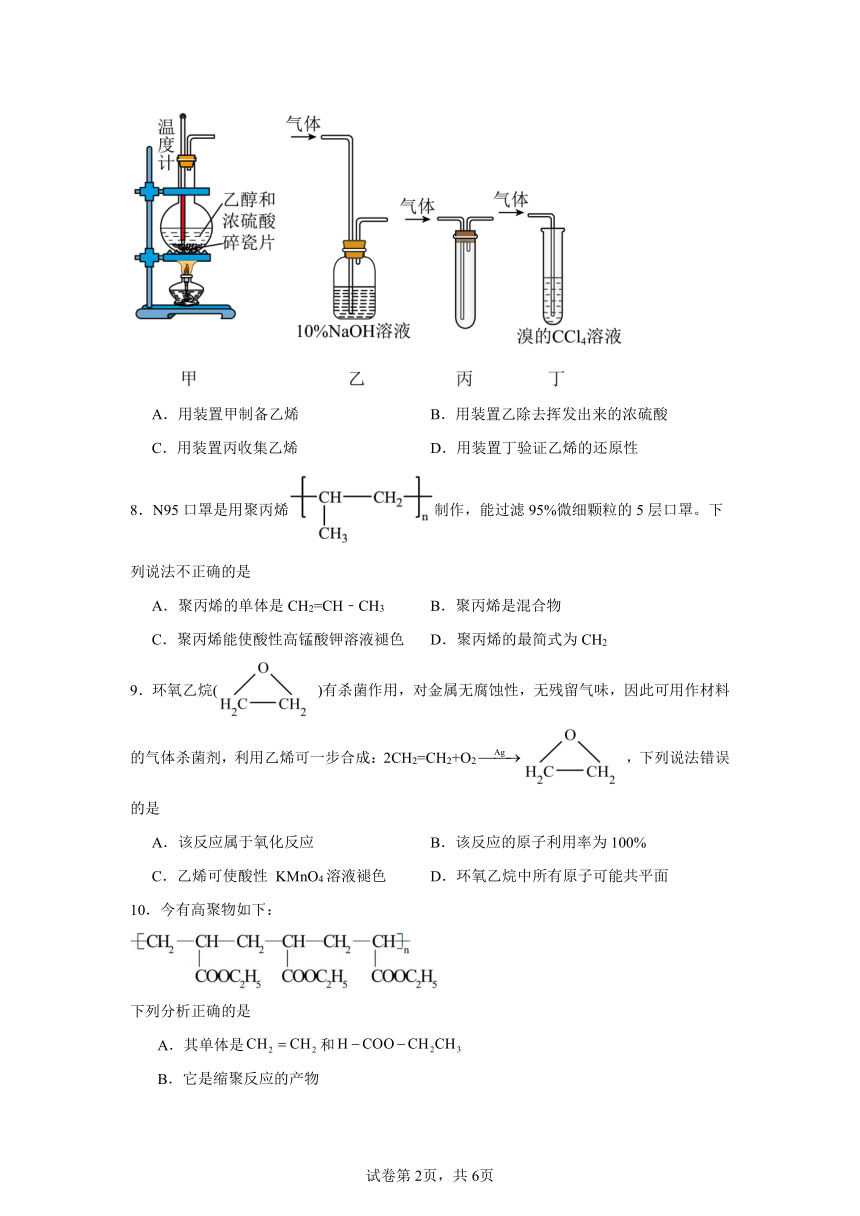
7.实验室欲制备少量乙烯并验证其性质,下列说法中正确的是
A.用装置甲制备乙烯 B.用装置乙除去挥发出来的浓硫酸
C.用装置丙收集乙烯 D.用装置丁验证乙烯的还原性
8.N95口罩是用聚丙烯制作,能过滤95%微细颗粒的5层口罩。下列说法不正确的是
A.聚丙烯的单体是CH2=CH﹣CH3 B.聚丙烯是混合物
C.聚丙烯能使酸性高锰酸钾溶液褪色 D.聚丙烯的最简式为CH2
9.环氧乙烷( )有杀菌作用,对金属无腐蚀性,无残留气味,因此可用作材料的气体杀菌剂,利用乙烯可一步合成:2CH2=CH2+O2 ,下列说法错误的是
A.该反应属于氧化反应 B.该反应的原子利用率为100%
C.乙烯可使酸性 KMnO4溶液褪色 D.环氧乙烷中所有原子可能共平面
10.今有高聚物如下:
下列分析正确的是
A.其单体是和
B.它是缩聚反应的产物
C.其单体是
D.链节是
11.下列关于乙烯的性质及结构的叙述中正确的是
A.将乙烯通入水中即可转化为乙醇
B.1mol乙烯与氯气完全加成,然后与氯气发生取代反应,一共需要3mol氯气
C.乙烯能被酸性溶液氧化,说明乙烯分子中含有碳碳双键
D.乙烯容易与溴水发生反应,1mol乙烯与溴单质发生加成反应,消耗1mol溴单质,说明乙烯分子中含有一个碳碳双键
12.下列高分子化合物是由两种单体通过加聚反应而制得的是( )
A.
B.
C.
D.
13.相同状况下,1体积某气态烃只能与1体积Cl2发生加成反应,生成氯代烷,1 mol此氯代烷可与4 mol Cl2发生完全取代反应,则该烃的结构简式为( )
A.CH2=CH2
B.CH3CH=CH2
C.CH3CH3
D.CH2=CH—CH=CH2
14.下列实验操作能达到实验目的的是
实验操作 实验目的
A.向两只试管中各加入5mL5%H2O2溶液向其中一只试管中加入1mL饱和FeCl3溶液,观察现象 验证FeCl3能催化H2O2分解
B.将甲烷和乙烯的混合气体通过酸性高锰酸钾洗气瓶 除去甲烷中混有的乙烯气体
C.向某未知溶液中滴加NaOH溶液,加热,生成气体用湿润的蓝色石蕊试纸检验 检验溶液中铵根离子
D.向5mL0.1KI溶液中滴入0.1FeCl3溶液5~6滴,加2mLCCl4振荡,静置后取上层清液滴加KSCN溶液,观察现象 验证Fe3+与的反应有一定限度
A.A B.B C.C D.D
15.某烃的结构简式为,若分子中共线碳原子数为a,可能共面的碳原子数最多为b,含四面体结构的碳原子数为c,则a、b、c分别是( )
A.3、4、5 B.3、10、4
C.3、14、4 D.4、10、4
二、填空题(共55分)
16.乙烯是世界上产量最大的化学产品之一,世界上已将乙烯产量作为衡量一个国家石油化工发展水平的重要标志之一。如图是有关乙烯的一些变化,根据乙烯的转化图,完成下列问题:
(1)乙烯的电子式 。
(2)①③的反应类型为 、 。
(3)丙的结构简式为 ,丁中的官能团为 。
(4)反应②的化学方程式为 。
(5)写出用丁及其它物质反应生成乙醛的化学方程式 。
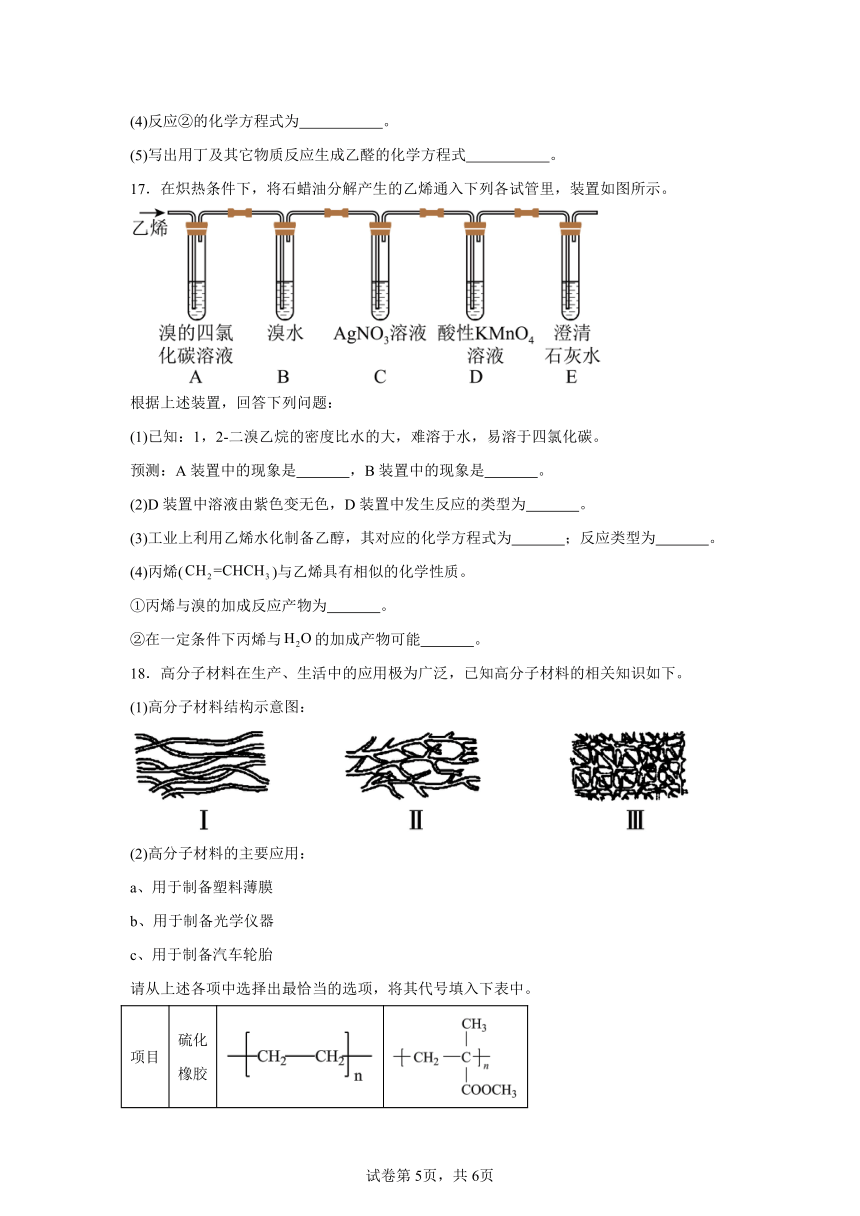
17.在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
根据上述装置,回答下列问题:
(1)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是 ,B装置中的现象是 。
(2)D装置中溶液由紫色变无色,D装置中发生反应的类型为 。
(3)工业上利用乙烯水化制备乙醇,其对应的化学方程式为 ;反应类型为 。
(4)丙烯()与乙烯具有相似的化学性质。
①丙烯与溴的加成反应产物为 。
②在一定条件下丙烯与的加成产物可能 。
18.高分子材料在生产、生活中的应用极为广泛,已知高分子材料的相关知识如下。
(1)高分子材料结构示意图:
(2)高分子材料的主要应用:
a、用于制备塑料薄膜
b、用于制备光学仪器
c、用于制备汽车轮胎
请从上述各项中选择出最恰当的选项,将其代号填入下表中。
项目 硫化 橡胶
结构
用途
三、解答题
19.在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
根据上述装置,回答下列问题:
(1)C装置的作用是 。
(2)已知:1,2—二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是 ,B装置中的现象是 。分离A装置中产物的操作名称是 ,分离B装置中产物需要的玻璃仪器名称是 。
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为 。教材中用溴的四氯化碳溶液替代溴水与乙烯反应,其目的是 。
(4)写出A装置中发生反应的化学方程式 ,反应类型为 。E装置的作用是 ,当观察到 现象时能验证E装置功能。
(5)做乙烯燃烧实验之前必须进行的操作是 ,可能观察到的现象是 。
(6)丙烯(CH2=CHCH3)与乙烯具有相似的化学性质(写结构简式)。
①丙烯与Br2的加成产物为 。
②在一定条件下丙烯与H2O的加成产物可能为 。
试卷第6页,共6页
试卷第5页,共6页
参考答案:
1.B
【详解】A以二氧化碳为原料合成淀粉可以减少空气中的二氧化碳,有助于实现“碳达峰”和“碳中和”,A正确;
B.防控新冠病毒所用消毒酒精的主要成分为乙醇,B错误;
C.铁是补血剂,酱油中添加铁强化剂,可减少缺铁性贫血的发生,C正确;
D.加成反应得到的氯乙烷产物单一,没有副反应,取代反应生成的氯乙烷产物有多个,副产物多,难以分离,工业上合成氯乙烷采用加成反应比采用取代反应更符合绿色化学理念,D正确;
答案选B。
2.A
【详解】A.甲烷与溴水不能反应,因而溴水不褪色;乙烯能够与溴水发生加成反应产生无色液体物质CH2Br-CH2Br而使溴水褪色,故可以使用溴水鉴别两种物质。也可以根据甲烷与溴水不反应,仍为气体,但乙烯与溴水反应变为液体CH2Br-CH2Br而与甲烷分离,故溴水也能除去甲烷中乙烯,A正确;
B.在点燃时,甲烷燃烧使火焰呈淡蓝色,乙烯燃烧时火焰明亮,并伴有黑烟,二者燃烧现象不同可以鉴别;但由于二者都能与氧气在点燃时发生反应,因此不能用于除去甲烷中乙烯,B错误;
C.甲烷与氯气在通常情况下不能反应,乙烯与Cl2也不能发生反应,因此不能用Cl2鉴别二者,C错误;
D.在通常情况下甲烷性质稳定,不能与酸性高锰酸钾溶液反应,因而溶液不褪色;乙烯可以被酸性高锰酸钾溶液氧化而使溶液褪色,因此可以使用酸性高锰酸钾溶液鉴别二者;但乙烯被酸性高锰酸钾溶液氧化产生CO2气体,又导致甲烷中混入新的杂质,故不能用于除杂,D错误;
故合理选项是A。
3.A
【详解】A.乙烯先与水发生加成反应生成乙醇,乙醇再氧化可生成,A符合题意;
B.乙烯在催化剂作用下与水发生加成反应,可生成,B不符合题意;
C.乙烯与HCl在催化剂作用下发生加成反应,可生成,C不符合题意;
D.乙烯与溴的四氯化碳溶液发生加成反应,可生成,D不符合题意;
故选A。
4.D
【详解】A.乙烯是平面形结构,键角是120°,丙烯分子中也含有碳碳双键所以丙烯分子中的3个碳原子在同一平面内,但不在同一条直线上,A错误;
B.由于含有甲基,所以分子中所有原子不可能在同一平面上,B错误;
C.丙烯中含有碳碳双键,能使溴水或酸性高锰酸钾溶液褪色,C错误;
D.含有碳碳双键的有机物都能发生加聚反应,D正确;
故答案选D。
5.B
【分析】有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应.
【详解】A.C2H4与氧气发生氧化反应生成二氧化碳和水,不属于加成反应,故A错误;
B.乙烯中含有碳碳双键,与氢气反应生成乙烷,属于加成反应,故B正确;
C.乙醇与钠发生置换反应,不属于加成反应,故C错误;
D.乙醇发生消去反应生成乙烯和水,属于消去反应,故D错误;
故选:B。
6.D
【详解】A. 塑料、合成纤维和合成橡胶都属于合成材料,天然纤维和天然橡胶都不属于合成材料,故A错误;
B. 聚氯乙烯可制成薄膜、软管等,其单体是CH2=CHCl,故B错误;
C. 分别属于醇类和酚类,结构不相似,不能互为同系物,故C错误;
D. 合成顺丁橡胶()的单体是CH2=CH—CH=CH2,故D正确;
故选D。
7.A
【详解】A.无水乙醇和浓硫酸的混合液迅速加热到170°C时制取乙烯,温度计伸入液体中,碎瓷片可防倒吸,可用装置甲制备乙烯,故选A;
B.浓硫酸不挥发,装置乙为洗气瓶,用装置乙除杂,除乙烯中的二氧化硫、二氧化碳等,故不选B;
C.乙烯的密度和空气的密度相近,不能用排空气法收集乙烯,故不选C;
D.乙烯和溴发生加成反应,若用装置丁验证乙烯的还原性,应选用酸性高锰酸钾溶液,故不选D;
选A。
8.C
【详解】
A.聚丙烯的单体是丙烯,即CH2=CHCH3,A正确;
B.聚丙烯是高分子,是多种聚合度不同的分子混合而成的混合物,B正确;
C.聚丙烯是丙烯聚合后的生成物,没有碳碳双键,不能使酸性高锰酸钾溶液褪色,C错误;
D.由结构可知,聚丙烯的最简式为CH2,D正确;
故选C。
9.D
【详解】A.加氧去氢的反应属于氧化反应,A正确;
B.由2CH2=CH2+O2 可知,生成物只有一种,反应的原子利用率为100%,B正确;
C.乙烯中含有碳碳双键,可使酸性 KMnO4溶液褪色,C正确;
D.环氧乙烷分子中C均为四面体结构,所有原子不可能共平面,D错误;
故选D。
10.C
【详解】
A.结构简式为,因此属于加聚产物,则该高聚物单体是CH2=CHCOOC2H5,A错误;
B.链节中主链上只有碳原子,为加聚反应生成的高聚物,B错误;
C.凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半链闭合即可,所以该高聚物单体是CH2=CHCOOC2H5,C正确;
D.链节为单体转变为在化学组成上能够重复的最小单位,该高聚物链节是,D错误;
答案选C。
11.D
【详解】A.乙烯在催化剂、加热等条件下与水发生加成反应可转化为乙醇,A错误;
B.1mol乙烯与1mol氯气完全加成生成,然后再与4mol氯气发生完全取代,一共需要5mol氯气,B错误;
C.碳碳双键、碳碳三键等官能团均可使酸性高锰酸钾溶液褪色,乙烯能被酸性溶液氧化,只能说明乙烯分子中可能含有碳碳双键,C错误;
D.1mol乙烯与溴单质发生加成反应,消耗1mol溴单质,说明乙烯分子中含有一个碳碳双键,D正确;
故选D。
12.B
【详解】A. 主链链节上有4个碳原子,且有一个碳碳双键,可知它的单体是一种二烯烃,A项不符合题意;
B. 主链链节上有4个碳原子,但碳与碳之间都以单键结合,所以它的单体是两种单烯烃,且通过加聚反应制得,B项符合题意;
C. 主链链节上只有2个碳原子,它的单体肯定只有一种,C项不符合题意;
D. 主链上有,D是由两种氨基酸单体缩合而成的,D项不符合题意;
答案选B。
【点睛】解答本题时要注意高聚物单体的推断方法,推断单体时,一定要先判断是加聚产物还是缩聚产物,并找准分离处。
(1)加聚产物单体判断:加聚产物的主链一般全为碳原子,按“凡双键,四个碳;无双键,两个碳”的规律画线断键,然后半键闭合、单双键互换。
(2)缩聚产物单体判断
13.A
【详解】根据题目中该烃加成反应所需氯气的量判断该烃分子中只含有一个双键,又根据氯代烷1mol可与4mol氯气发生完全的取代反应,判断该加成产物分子中只含有4个氢原子,A选项符合题意。故答案为A。
14.D
【详解】A.两只试管中各加入5mL5%的双氧水溶液,其中一只试管中加入1mL饱和氯化铁溶液,另一只试管中不加,另一个试管中应该加入等量的蒸馏水,否则无法起到对照作用,A错误;
B.乙烯与酸性高锰酸钾反应生成二氧化碳,除去乙烯的同时混入了新的杂质气体,B错误;
C.检验氨气应该用湿润的红色石蕊试纸而不是蓝色石蕊试纸,C错误;
D.5mL0.1mol/L的KI溶液中滴入0.1mol/L的FeCl35-6滴,氯化铁不足,两者反应后加入CCl4振荡,上层清液滴加KSCN溶液,溶液变血红色,说明溶液中存在铁离子,即可证明铁离子与碘离子的反应存在限度,D正确;
故答案选D。
15.C
【分析】,首先利用乙烯模型中键角为,乙炔模型为直线,苯环键角为,将有机物的结构写成上图。4、7、8号三个碳原子一定共线;苯环和2、3、4、5、7号碳原子构成的乙烯面可以共面;以四个单键与其他原子连接的碳原子为四面体结构。
【详解】4、7、8号三个碳原子一定共线,所以共线碳原子为3;苯环和2、3、4、5、7号碳原子构成的乙烯面可以共面,一共有11个碳原子,因为4、7、8号三个碳原子一定共线,所以8号碳原子一定也在这个面内(12个碳共面了),1号、6号碳原子也可以在这个面内(14个碳共面了);以四个单键与其他原子连接的碳原子为四面体结构,有1号、2号、5号、6号碳原子符合。
答案选C。
【点睛】在分析共线共面问题时,要利用几个模型:乙烯的6个原子共面,乙炔的4个原子共线,苯的12个原子共面,甲烷的五个原子中最多3个共面;另外要看清题目问的是最多还是至少。
16.(1)
(2) 加成反应 加成反应
(3)
(4)
(5)
【分析】乙烯和氯化氢发生加成反应生成甲,甲是CH3CH2Cl;乙烯燃烧生成二氧化碳和水;乙烯和溴水发生加成反应生成,丙是;乙烯和水发生加成反应生成乙醇,丁是乙醇;
【详解】(1)乙烯分子中含有碳碳双键,乙烯的电子式为;
(2)①是乙烯和HCl发生加成反应生成CH3CH2Cl;③是乙烯和溴发生加成反应生成1,2-二溴乙烷;
(3)丙是1,2-二溴乙烷,结构简式为,丁是CH3CH2OH,官能团为羟基;
(4)反应②是乙烯燃烧生成二氧化碳和水,反应的化学方程式为;
(5)乙醇发生催化氧化生成乙醛和水,反应的化学方程式为。
17.(1) 溶液褪色,液体不分层 溶液褪色,液体分层
(2)氧化反应
(3) CH2=CH2+ H2O CH3CH2OH 加成反应
(4) CH2BrCHBrCH3 CH2(OH)CH2CH3、CH3CH(OH)CH3
【分析】由实验装置可知,A中乙烯与溴发生加成反应,溴的四氯化碳溶液褪色;B中乙烯与溴水发生加成反应,溴水褪色;C中乙烯与硝酸银溶液不反应,但C可检验挥发的溴;D中乙烯被高锰酸钾氧化,溶液褪色;E中石灰水变浑浊,可知乙烯被高锰酸钾氧化生成二氧化碳。
【详解】(1)A、B装置中乙烯与溴发生加成反应均生成有机物CH2BrCH2Br,CH2BrCH2Br能溶于四氯化碳、不溶于水,故现象分别为:溴的四氯化碳溶液褪色液体不分层;溴水褪色液体分层。
(2)D装置中溶液由紫色变无色,是D装置中高锰酸钾被乙烯还原,乙烯被氧化,发生反应的类型为氧化反应。
(3)乙烯水化制备乙醇,乙烯与水发加成反应,反应方程式为CH2=CH2+ H2O CH3CH2OH。
(4)①丙烯中含碳碳双键,与溴发生加成反应:CH2=CHCH3+Br2→CH2BrCHBrCH3,产物为CH2BrCHBrCH3。
②在一定条件下丙烯与H2O的加成反应可能为CH2=CHCH3+H2O→CH3CH(OH)CH3或CH2=CHCH3+H2O→CH2(OH)CH2CH3,产物为:CH3CH(OH)CH3或CH2(OH)CH2CH3。
18. Ⅲ Ⅰ Ⅱ c a b
【详解】硫化橡胶是立体网状结构,故对应图像Ⅲ,橡胶用于制备汽车轮胎;聚乙烯是线型结构,故对应图像Ⅰ,聚乙烯通过加聚反应,可以制得塑料薄膜;是支链型结构,故对应图像Ⅱ,有机玻璃可以用于制备光学仪器;答案为:Ⅲ;Ⅰ;Ⅱ;c;a;b。
19.(1)检验B装置中是否有溴挥发出来
(2) 橙色褪去,液体不分层 橙黄色褪去,液体分层 蒸馏 分液漏斗、烧杯、玻璃棒
(3) 氧化反应 避免溴与水反应的产物对实验产生干扰
(4) CH2=CH2+Br2→ 加成反应 检验乙烯与酸性KMnO4溶液反应的产物二氧化碳 澄清石灰水变浑浊
(5) 检验乙烯的纯度 产生明亮火焰并伴有黑烟
(6) 、HO—CH2CH2CH3
【分析】乙烯通入溴的四氯化碳溶液发生加成反应而使其褪色,通入溴水发生氧化还原反应而使其褪色,装置C确认从溴水出来的乙烯没有溴气体杂质,乙烯通入酸性KMnO4溶液发生氧化反应而使其褪色,氧化产物CO2进入装置E,是澄清石灰水变浑浊。
【详解】(1)据分析,C装置的作用是检验B装置中是否有溴挥发出来。
(2)A装置中乙烯与溴发生加成反应生成1,2—二溴乙烷,B装置中乙烯与溴水发生氧化还原反应,由题给信息可预测,A装置中的现象是橙色褪去,液体不分层;B装置中的现象是橙黄色褪去,液体分层;1,2—二溴乙烷易溶于四氯化碳,分离A装置中产物要用蒸馏;1,2—二溴乙烷密度比水的大,难溶于水,分离B装置中产物要用分液,需要的玻璃仪器有分液漏斗、烧杯、玻璃棒。
(3)D装置中乙烯通入酸性KMnO4溶液发生氧化反应,溶液由紫色变无色,发生反应的类型为氧化反应;由于溴与水也会反应,教材中用溴的四氯化碳溶液替代溴水与乙烯反应,其目的是避免溴与水反应的产物对实验产生干扰。
(4)A装置中乙烯通入溴的四氯化碳溶液发生加成反应,反应的化学方程式:CH2=CH2+Br2→;反应类型为加成反应;据分析,E装置的作用是检验乙烯与酸性KMnO4溶液反应的产物二氧化碳;当观察到澄清石灰水变浑浊时能验证E装置功能。
(5)为了实验安全,防止爆炸危险的发生,做乙烯燃烧实验之前必须进行的操作是检验乙烯的纯度;乙烯含碳量较高,燃烧时可能观察到的现象是:产生明亮火焰并伴有黑烟。
(6)丙烯的结构简式是,①丙烯中碳碳双键与Br2加成,产物为:;②在一定条件下丙烯与H2O加成,H2O的-OH可能加在碳碳双键的任一碳原子上,产物可能为:、HO—CH2CH2CH3。
答案第8页,共9页
答案第9页,共9页
时间:75分钟 满分:100分
一、单选题(每题3分,共45分)
1.化学与生活、环境密切相关。下列说法错误的是
A.以二氧化碳为原料合成淀粉有助于实现“碳达峰”和“碳中和”
B.防控新冠病毒所用消毒酒精的主要成分为乙酸
C.酱油中添加铁强化剂,可减少缺铁性贫血的发生
D.工业上合成氯乙烷采用加成反应比采用取代反应更符合绿色化学理念
2.既能够用于鉴别甲烷和乙烯,又能除去甲烷中乙烯的试剂是
A.溴水 B.点燃 C.通入Cl2 D.酸性高锰酸钾溶液
3.下列物质中,不能通过乙烯的加成反应一步制得的是
A. B. C. D.
4.由乙烯推测丙烯(CH3CH=CH2)的结构或性质,正确的是
A.分子中3个碳原子在同一直线上 B.分子中所有原子在同一平面上
C.不能使酸性高锰酸钾溶液褪色 D.能发生加聚反应
5.下列反应属于加成反应的是
A.C2H4+3O22CO2+2H2O B.CH2=CH2+H2→CH3CH3
C.2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ D.CH3CH2OHCH2=CH2↑+H2O
6.下列有关说法中,正确的是
A.塑料、纤维和橡胶都属于合成材料
B.聚氯乙烯可制成薄膜、软管等,其单体是CHCl=CHCl
C.互为同系物
D.合成顺丁橡胶()的单体是CH2=CH—CH=CH2
7.实验室欲制备少量乙烯并验证其性质,下列说法中正确的是
A.用装置甲制备乙烯 B.用装置乙除去挥发出来的浓硫酸
C.用装置丙收集乙烯 D.用装置丁验证乙烯的还原性
8.N95口罩是用聚丙烯制作,能过滤95%微细颗粒的5层口罩。下列说法不正确的是
A.聚丙烯的单体是CH2=CH﹣CH3 B.聚丙烯是混合物
C.聚丙烯能使酸性高锰酸钾溶液褪色 D.聚丙烯的最简式为CH2
9.环氧乙烷( )有杀菌作用,对金属无腐蚀性,无残留气味,因此可用作材料的气体杀菌剂,利用乙烯可一步合成:2CH2=CH2+O2 ,下列说法错误的是
A.该反应属于氧化反应 B.该反应的原子利用率为100%
C.乙烯可使酸性 KMnO4溶液褪色 D.环氧乙烷中所有原子可能共平面
10.今有高聚物如下:
下列分析正确的是
A.其单体是和
B.它是缩聚反应的产物
C.其单体是
D.链节是
11.下列关于乙烯的性质及结构的叙述中正确的是
A.将乙烯通入水中即可转化为乙醇
B.1mol乙烯与氯气完全加成,然后与氯气发生取代反应,一共需要3mol氯气
C.乙烯能被酸性溶液氧化,说明乙烯分子中含有碳碳双键
D.乙烯容易与溴水发生反应,1mol乙烯与溴单质发生加成反应,消耗1mol溴单质,说明乙烯分子中含有一个碳碳双键
12.下列高分子化合物是由两种单体通过加聚反应而制得的是( )
A.
B.
C.
D.
13.相同状况下,1体积某气态烃只能与1体积Cl2发生加成反应,生成氯代烷,1 mol此氯代烷可与4 mol Cl2发生完全取代反应,则该烃的结构简式为( )
A.CH2=CH2
B.CH3CH=CH2
C.CH3CH3
D.CH2=CH—CH=CH2
14.下列实验操作能达到实验目的的是
实验操作 实验目的
A.向两只试管中各加入5mL5%H2O2溶液向其中一只试管中加入1mL饱和FeCl3溶液,观察现象 验证FeCl3能催化H2O2分解
B.将甲烷和乙烯的混合气体通过酸性高锰酸钾洗气瓶 除去甲烷中混有的乙烯气体
C.向某未知溶液中滴加NaOH溶液,加热,生成气体用湿润的蓝色石蕊试纸检验 检验溶液中铵根离子
D.向5mL0.1KI溶液中滴入0.1FeCl3溶液5~6滴,加2mLCCl4振荡,静置后取上层清液滴加KSCN溶液,观察现象 验证Fe3+与的反应有一定限度
A.A B.B C.C D.D
15.某烃的结构简式为,若分子中共线碳原子数为a,可能共面的碳原子数最多为b,含四面体结构的碳原子数为c,则a、b、c分别是( )
A.3、4、5 B.3、10、4
C.3、14、4 D.4、10、4
二、填空题(共55分)
16.乙烯是世界上产量最大的化学产品之一,世界上已将乙烯产量作为衡量一个国家石油化工发展水平的重要标志之一。如图是有关乙烯的一些变化,根据乙烯的转化图,完成下列问题:
(1)乙烯的电子式 。
(2)①③的反应类型为 、 。
(3)丙的结构简式为 ,丁中的官能团为 。
(4)反应②的化学方程式为 。
(5)写出用丁及其它物质反应生成乙醛的化学方程式 。
17.在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
根据上述装置,回答下列问题:
(1)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是 ,B装置中的现象是 。
(2)D装置中溶液由紫色变无色,D装置中发生反应的类型为 。
(3)工业上利用乙烯水化制备乙醇,其对应的化学方程式为 ;反应类型为 。
(4)丙烯()与乙烯具有相似的化学性质。
①丙烯与溴的加成反应产物为 。
②在一定条件下丙烯与的加成产物可能 。
18.高分子材料在生产、生活中的应用极为广泛,已知高分子材料的相关知识如下。
(1)高分子材料结构示意图:
(2)高分子材料的主要应用:
a、用于制备塑料薄膜
b、用于制备光学仪器
c、用于制备汽车轮胎
请从上述各项中选择出最恰当的选项,将其代号填入下表中。
项目 硫化 橡胶
结构
用途
三、解答题
19.在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
根据上述装置,回答下列问题:
(1)C装置的作用是 。
(2)已知:1,2—二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是 ,B装置中的现象是 。分离A装置中产物的操作名称是 ,分离B装置中产物需要的玻璃仪器名称是 。
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为 。教材中用溴的四氯化碳溶液替代溴水与乙烯反应,其目的是 。
(4)写出A装置中发生反应的化学方程式 ,反应类型为 。E装置的作用是 ,当观察到 现象时能验证E装置功能。
(5)做乙烯燃烧实验之前必须进行的操作是 ,可能观察到的现象是 。
(6)丙烯(CH2=CHCH3)与乙烯具有相似的化学性质(写结构简式)。
①丙烯与Br2的加成产物为 。
②在一定条件下丙烯与H2O的加成产物可能为 。
试卷第6页,共6页
试卷第5页,共6页
参考答案:
1.B
【详解】A以二氧化碳为原料合成淀粉可以减少空气中的二氧化碳,有助于实现“碳达峰”和“碳中和”,A正确;
B.防控新冠病毒所用消毒酒精的主要成分为乙醇,B错误;
C.铁是补血剂,酱油中添加铁强化剂,可减少缺铁性贫血的发生,C正确;
D.加成反应得到的氯乙烷产物单一,没有副反应,取代反应生成的氯乙烷产物有多个,副产物多,难以分离,工业上合成氯乙烷采用加成反应比采用取代反应更符合绿色化学理念,D正确;
答案选B。
2.A
【详解】A.甲烷与溴水不能反应,因而溴水不褪色;乙烯能够与溴水发生加成反应产生无色液体物质CH2Br-CH2Br而使溴水褪色,故可以使用溴水鉴别两种物质。也可以根据甲烷与溴水不反应,仍为气体,但乙烯与溴水反应变为液体CH2Br-CH2Br而与甲烷分离,故溴水也能除去甲烷中乙烯,A正确;
B.在点燃时,甲烷燃烧使火焰呈淡蓝色,乙烯燃烧时火焰明亮,并伴有黑烟,二者燃烧现象不同可以鉴别;但由于二者都能与氧气在点燃时发生反应,因此不能用于除去甲烷中乙烯,B错误;
C.甲烷与氯气在通常情况下不能反应,乙烯与Cl2也不能发生反应,因此不能用Cl2鉴别二者,C错误;
D.在通常情况下甲烷性质稳定,不能与酸性高锰酸钾溶液反应,因而溶液不褪色;乙烯可以被酸性高锰酸钾溶液氧化而使溶液褪色,因此可以使用酸性高锰酸钾溶液鉴别二者;但乙烯被酸性高锰酸钾溶液氧化产生CO2气体,又导致甲烷中混入新的杂质,故不能用于除杂,D错误;
故合理选项是A。
3.A
【详解】A.乙烯先与水发生加成反应生成乙醇,乙醇再氧化可生成,A符合题意;
B.乙烯在催化剂作用下与水发生加成反应,可生成,B不符合题意;
C.乙烯与HCl在催化剂作用下发生加成反应,可生成,C不符合题意;
D.乙烯与溴的四氯化碳溶液发生加成反应,可生成,D不符合题意;
故选A。
4.D
【详解】A.乙烯是平面形结构,键角是120°,丙烯分子中也含有碳碳双键所以丙烯分子中的3个碳原子在同一平面内,但不在同一条直线上,A错误;
B.由于含有甲基,所以分子中所有原子不可能在同一平面上,B错误;
C.丙烯中含有碳碳双键,能使溴水或酸性高锰酸钾溶液褪色,C错误;
D.含有碳碳双键的有机物都能发生加聚反应,D正确;
故答案选D。
5.B
【分析】有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应.
【详解】A.C2H4与氧气发生氧化反应生成二氧化碳和水,不属于加成反应,故A错误;
B.乙烯中含有碳碳双键,与氢气反应生成乙烷,属于加成反应,故B正确;
C.乙醇与钠发生置换反应,不属于加成反应,故C错误;
D.乙醇发生消去反应生成乙烯和水,属于消去反应,故D错误;
故选:B。
6.D
【详解】A. 塑料、合成纤维和合成橡胶都属于合成材料,天然纤维和天然橡胶都不属于合成材料,故A错误;
B. 聚氯乙烯可制成薄膜、软管等,其单体是CH2=CHCl,故B错误;
C. 分别属于醇类和酚类,结构不相似,不能互为同系物,故C错误;
D. 合成顺丁橡胶()的单体是CH2=CH—CH=CH2,故D正确;
故选D。
7.A
【详解】A.无水乙醇和浓硫酸的混合液迅速加热到170°C时制取乙烯,温度计伸入液体中,碎瓷片可防倒吸,可用装置甲制备乙烯,故选A;
B.浓硫酸不挥发,装置乙为洗气瓶,用装置乙除杂,除乙烯中的二氧化硫、二氧化碳等,故不选B;
C.乙烯的密度和空气的密度相近,不能用排空气法收集乙烯,故不选C;
D.乙烯和溴发生加成反应,若用装置丁验证乙烯的还原性,应选用酸性高锰酸钾溶液,故不选D;
选A。
8.C
【详解】
A.聚丙烯的单体是丙烯,即CH2=CHCH3,A正确;
B.聚丙烯是高分子,是多种聚合度不同的分子混合而成的混合物,B正确;
C.聚丙烯是丙烯聚合后的生成物,没有碳碳双键,不能使酸性高锰酸钾溶液褪色,C错误;
D.由结构可知,聚丙烯的最简式为CH2,D正确;
故选C。
9.D
【详解】A.加氧去氢的反应属于氧化反应,A正确;
B.由2CH2=CH2+O2 可知,生成物只有一种,反应的原子利用率为100%,B正确;
C.乙烯中含有碳碳双键,可使酸性 KMnO4溶液褪色,C正确;
D.环氧乙烷分子中C均为四面体结构,所有原子不可能共平面,D错误;
故选D。
10.C
【详解】
A.结构简式为,因此属于加聚产物,则该高聚物单体是CH2=CHCOOC2H5,A错误;
B.链节中主链上只有碳原子,为加聚反应生成的高聚物,B错误;
C.凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半链闭合即可,所以该高聚物单体是CH2=CHCOOC2H5,C正确;
D.链节为单体转变为在化学组成上能够重复的最小单位,该高聚物链节是,D错误;
答案选C。
11.D
【详解】A.乙烯在催化剂、加热等条件下与水发生加成反应可转化为乙醇,A错误;
B.1mol乙烯与1mol氯气完全加成生成,然后再与4mol氯气发生完全取代,一共需要5mol氯气,B错误;
C.碳碳双键、碳碳三键等官能团均可使酸性高锰酸钾溶液褪色,乙烯能被酸性溶液氧化,只能说明乙烯分子中可能含有碳碳双键,C错误;
D.1mol乙烯与溴单质发生加成反应,消耗1mol溴单质,说明乙烯分子中含有一个碳碳双键,D正确;
故选D。
12.B
【详解】A. 主链链节上有4个碳原子,且有一个碳碳双键,可知它的单体是一种二烯烃,A项不符合题意;
B. 主链链节上有4个碳原子,但碳与碳之间都以单键结合,所以它的单体是两种单烯烃,且通过加聚反应制得,B项符合题意;
C. 主链链节上只有2个碳原子,它的单体肯定只有一种,C项不符合题意;
D. 主链上有,D是由两种氨基酸单体缩合而成的,D项不符合题意;
答案选B。
【点睛】解答本题时要注意高聚物单体的推断方法,推断单体时,一定要先判断是加聚产物还是缩聚产物,并找准分离处。
(1)加聚产物单体判断:加聚产物的主链一般全为碳原子,按“凡双键,四个碳;无双键,两个碳”的规律画线断键,然后半键闭合、单双键互换。
(2)缩聚产物单体判断
13.A
【详解】根据题目中该烃加成反应所需氯气的量判断该烃分子中只含有一个双键,又根据氯代烷1mol可与4mol氯气发生完全的取代反应,判断该加成产物分子中只含有4个氢原子,A选项符合题意。故答案为A。
14.D
【详解】A.两只试管中各加入5mL5%的双氧水溶液,其中一只试管中加入1mL饱和氯化铁溶液,另一只试管中不加,另一个试管中应该加入等量的蒸馏水,否则无法起到对照作用,A错误;
B.乙烯与酸性高锰酸钾反应生成二氧化碳,除去乙烯的同时混入了新的杂质气体,B错误;
C.检验氨气应该用湿润的红色石蕊试纸而不是蓝色石蕊试纸,C错误;
D.5mL0.1mol/L的KI溶液中滴入0.1mol/L的FeCl35-6滴,氯化铁不足,两者反应后加入CCl4振荡,上层清液滴加KSCN溶液,溶液变血红色,说明溶液中存在铁离子,即可证明铁离子与碘离子的反应存在限度,D正确;
故答案选D。
15.C
【分析】,首先利用乙烯模型中键角为,乙炔模型为直线,苯环键角为,将有机物的结构写成上图。4、7、8号三个碳原子一定共线;苯环和2、3、4、5、7号碳原子构成的乙烯面可以共面;以四个单键与其他原子连接的碳原子为四面体结构。
【详解】4、7、8号三个碳原子一定共线,所以共线碳原子为3;苯环和2、3、4、5、7号碳原子构成的乙烯面可以共面,一共有11个碳原子,因为4、7、8号三个碳原子一定共线,所以8号碳原子一定也在这个面内(12个碳共面了),1号、6号碳原子也可以在这个面内(14个碳共面了);以四个单键与其他原子连接的碳原子为四面体结构,有1号、2号、5号、6号碳原子符合。
答案选C。
【点睛】在分析共线共面问题时,要利用几个模型:乙烯的6个原子共面,乙炔的4个原子共线,苯的12个原子共面,甲烷的五个原子中最多3个共面;另外要看清题目问的是最多还是至少。
16.(1)
(2) 加成反应 加成反应
(3)
(4)
(5)
【分析】乙烯和氯化氢发生加成反应生成甲,甲是CH3CH2Cl;乙烯燃烧生成二氧化碳和水;乙烯和溴水发生加成反应生成,丙是;乙烯和水发生加成反应生成乙醇,丁是乙醇;
【详解】(1)乙烯分子中含有碳碳双键,乙烯的电子式为;
(2)①是乙烯和HCl发生加成反应生成CH3CH2Cl;③是乙烯和溴发生加成反应生成1,2-二溴乙烷;
(3)丙是1,2-二溴乙烷,结构简式为,丁是CH3CH2OH,官能团为羟基;
(4)反应②是乙烯燃烧生成二氧化碳和水,反应的化学方程式为;
(5)乙醇发生催化氧化生成乙醛和水,反应的化学方程式为。
17.(1) 溶液褪色,液体不分层 溶液褪色,液体分层
(2)氧化反应
(3) CH2=CH2+ H2O CH3CH2OH 加成反应
(4) CH2BrCHBrCH3 CH2(OH)CH2CH3、CH3CH(OH)CH3
【分析】由实验装置可知,A中乙烯与溴发生加成反应,溴的四氯化碳溶液褪色;B中乙烯与溴水发生加成反应,溴水褪色;C中乙烯与硝酸银溶液不反应,但C可检验挥发的溴;D中乙烯被高锰酸钾氧化,溶液褪色;E中石灰水变浑浊,可知乙烯被高锰酸钾氧化生成二氧化碳。
【详解】(1)A、B装置中乙烯与溴发生加成反应均生成有机物CH2BrCH2Br,CH2BrCH2Br能溶于四氯化碳、不溶于水,故现象分别为:溴的四氯化碳溶液褪色液体不分层;溴水褪色液体分层。
(2)D装置中溶液由紫色变无色,是D装置中高锰酸钾被乙烯还原,乙烯被氧化,发生反应的类型为氧化反应。
(3)乙烯水化制备乙醇,乙烯与水发加成反应,反应方程式为CH2=CH2+ H2O CH3CH2OH。
(4)①丙烯中含碳碳双键,与溴发生加成反应:CH2=CHCH3+Br2→CH2BrCHBrCH3,产物为CH2BrCHBrCH3。
②在一定条件下丙烯与H2O的加成反应可能为CH2=CHCH3+H2O→CH3CH(OH)CH3或CH2=CHCH3+H2O→CH2(OH)CH2CH3,产物为:CH3CH(OH)CH3或CH2(OH)CH2CH3。
18. Ⅲ Ⅰ Ⅱ c a b
【详解】硫化橡胶是立体网状结构,故对应图像Ⅲ,橡胶用于制备汽车轮胎;聚乙烯是线型结构,故对应图像Ⅰ,聚乙烯通过加聚反应,可以制得塑料薄膜;是支链型结构,故对应图像Ⅱ,有机玻璃可以用于制备光学仪器;答案为:Ⅲ;Ⅰ;Ⅱ;c;a;b。
19.(1)检验B装置中是否有溴挥发出来
(2) 橙色褪去,液体不分层 橙黄色褪去,液体分层 蒸馏 分液漏斗、烧杯、玻璃棒
(3) 氧化反应 避免溴与水反应的产物对实验产生干扰
(4) CH2=CH2+Br2→ 加成反应 检验乙烯与酸性KMnO4溶液反应的产物二氧化碳 澄清石灰水变浑浊
(5) 检验乙烯的纯度 产生明亮火焰并伴有黑烟
(6) 、HO—CH2CH2CH3
【分析】乙烯通入溴的四氯化碳溶液发生加成反应而使其褪色,通入溴水发生氧化还原反应而使其褪色,装置C确认从溴水出来的乙烯没有溴气体杂质,乙烯通入酸性KMnO4溶液发生氧化反应而使其褪色,氧化产物CO2进入装置E,是澄清石灰水变浑浊。
【详解】(1)据分析,C装置的作用是检验B装置中是否有溴挥发出来。
(2)A装置中乙烯与溴发生加成反应生成1,2—二溴乙烷,B装置中乙烯与溴水发生氧化还原反应,由题给信息可预测,A装置中的现象是橙色褪去,液体不分层;B装置中的现象是橙黄色褪去,液体分层;1,2—二溴乙烷易溶于四氯化碳,分离A装置中产物要用蒸馏;1,2—二溴乙烷密度比水的大,难溶于水,分离B装置中产物要用分液,需要的玻璃仪器有分液漏斗、烧杯、玻璃棒。
(3)D装置中乙烯通入酸性KMnO4溶液发生氧化反应,溶液由紫色变无色,发生反应的类型为氧化反应;由于溴与水也会反应,教材中用溴的四氯化碳溶液替代溴水与乙烯反应,其目的是避免溴与水反应的产物对实验产生干扰。
(4)A装置中乙烯通入溴的四氯化碳溶液发生加成反应,反应的化学方程式:CH2=CH2+Br2→;反应类型为加成反应;据分析,E装置的作用是检验乙烯与酸性KMnO4溶液反应的产物二氧化碳;当观察到澄清石灰水变浑浊时能验证E装置功能。
(5)为了实验安全,防止爆炸危险的发生,做乙烯燃烧实验之前必须进行的操作是检验乙烯的纯度;乙烯含碳量较高,燃烧时可能观察到的现象是:产生明亮火焰并伴有黑烟。
(6)丙烯的结构简式是,①丙烯中碳碳双键与Br2加成,产物为:;②在一定条件下丙烯与H2O加成,H2O的-OH可能加在碳碳双键的任一碳原子上,产物可能为:、HO—CH2CH2CH3。
答案第8页,共9页
答案第9页,共9页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
