化学人教版(2019)必修第二册7.1.2烷烃的结构(共22张ppt)(任务驱动)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.1.2烷烃的结构(共22张ppt)(任务驱动) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-06 00:00:00 | ||
图片预览




文档简介
(共22张PPT)
人教版必修第二册
第七章 有机化合物
第一节 认识有机化合物
第2课时 烷烃的结构
学习目标
1、通过甲烷结构迁移能说出烷烃的定义并能辨别烷烃结构特点,会准确判断烷烃的结构简式并能书写烷烃的结构简式。
2、能归纳烷烃的物理性质递变性、化学性质相似性
3、能复述同系物的定义,会应用同系物的概念处理相关问题
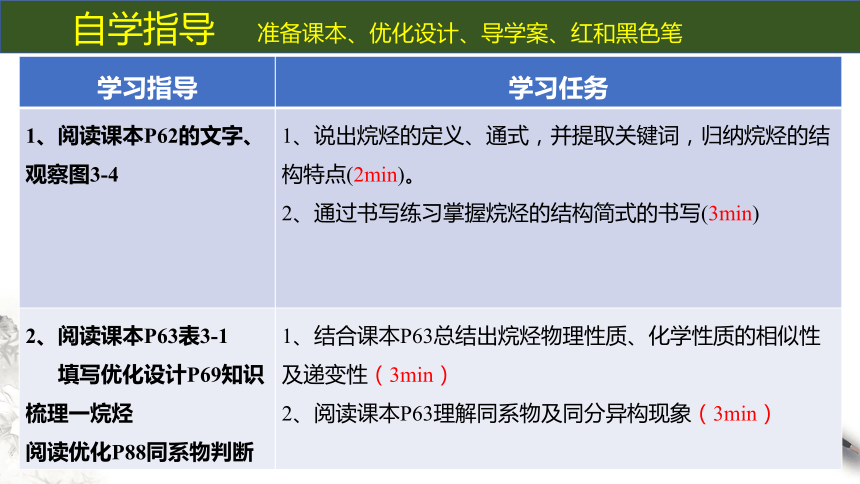
学习指导 学习任务
1、阅读课本P62的文字、观察图3-4 1、说出烷烃的定义、通式,并提取关键词,归纳烷烃的结构特点(2min)。
2、通过书写练习掌握烷烃的结构简式的书写(3min)
2、阅读课本P63表3-1 填写优化设计P69知识梳理一烷烃 阅读优化P88同系物判断 1、结合课本P63总结出烷烃物理性质、化学性质的相似性及递变性(3min)
2、阅读课本P63理解同系物及同分异构现象(3min)
自学指导 准备课本、优化设计、导学案、红和黑色笔
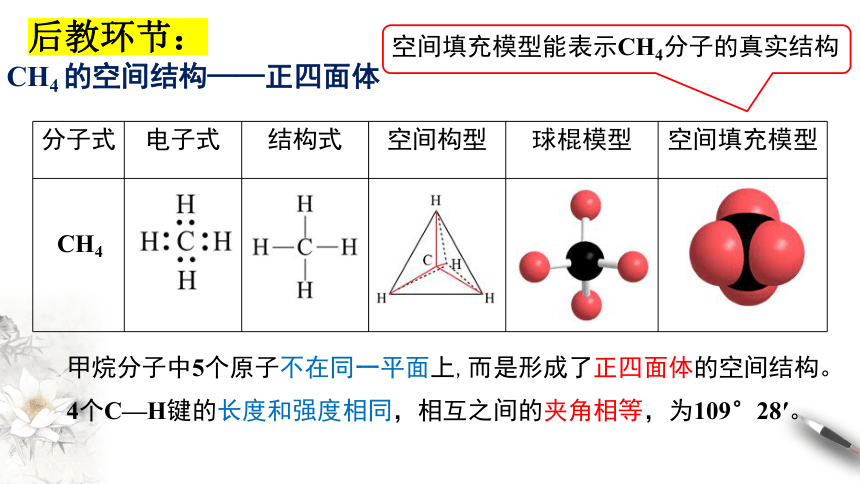
分子式 电子式 结构式 空间构型 球棍模型 空间填充模型
空间填充模型能表示CH4分子的真实结构
CH4 的空间结构——正四面体
甲烷分子中5个原子不在同一平面上,而是形成了正四面体的空间结构。
4个C—H键的长度和强度相同,相互之间的夹角相等,为109°28′。
CH4
后教环节:
仅含碳和氢两种元素的有机化合物称为碳氢化合物,也称为烃。
碳 + 氢 =
烃
tàn qīng
tīng
最简单的烷烃——甲烷
你知道“烃”字的由来吗?
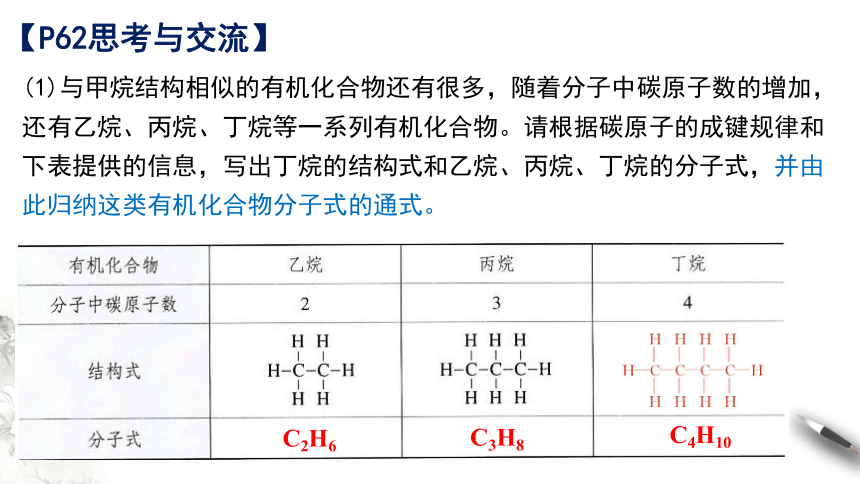
【P62思考与交流】
(1)与甲烷结构相似的有机化合物还有很多,随着分子中碳原子数的增加,还有乙烷、丙烷、丁烷等一系列有机化合物。请根据碳原子的成键规律和下表提供的信息,写出丁烷的结构式和乙烷、丙烷、丁烷的分子式,并由此归纳这类有机化合物分子式的通式。
C2H6
C3H8
C4H10
思考与交流:
(3)结合图 7-6 中的分子结构模型,
总结这类有机化合物的组成和分子结构特点。
只含碳和氢两种元素,分子中的碳原子之间都以单键结合,
碳原子的剩余价键均与氢原子结合,
使碳原子的化合价都达到“饱和”。
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
结构简式:
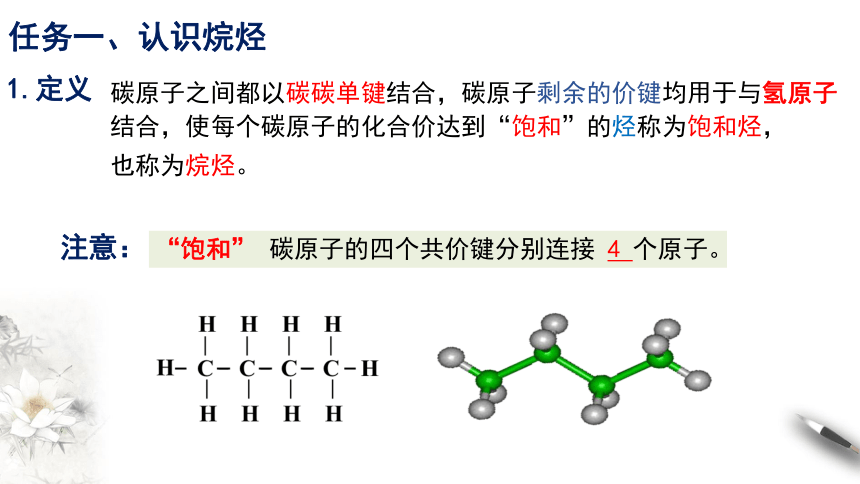
任务一、认识烷烃
1.定义
碳原子之间都以碳碳单键结合,碳原子剩余的价键均用于与氢原子 结合,使每个碳原子的化合价达到“饱和”的烃称为饱和烃,
也称为烷烃。
“饱和” 碳原子的四个共价键分别连接 4 个原子。
注意:
2.分子结构特点
③饱和:
一、烷烃
①元素:
②单键:
④碳骨架:
只含有碳和氢两种元素
碳原子之间只以碳碳单键结合
每个碳原子均形成4个价键,分别连接4个原子
可以是链状结构,也可以是环状结构
高中阶段一般不探讨环烷烃的有关结构和性质
链状烷烃的分子组成通式为
链状烷烃分子中的共价键数为
一、烷烃
3.分子组成通式
CnH2n (n≥3)
CnH2n+2 (n≥1)
(2n+2)+(n-1)=3n+1
烷烃包含链状烷烃和环状烷烃,没有特别注明我们讲的烷烃都是特指链状烷烃
环状烷烃的分子组成通式为
1、下列物质属于有机物的是 ;
下列物质属于烃的是_________________
下列有机物中,属于烷烃的是________
①⑤⑥⑦⑧⑨
⑧⑨
①⑧⑨
①C2H2 ②HCN ③H2CO3
④金刚石 ⑤CH3Cl ⑥CCl4
⑦CH3COOH ⑧CH4
⑨C2H6 ⑩CaCO3 CO2
判断烷烃的标准:
①只含有碳碳单键和碳氢元素
②分子式符合通式CnH2n+2 (n≥1)
思考与讨论
①分别写出它们的分子式和结构简式。
以下是甲烷、乙烷、丙烷和丁烷的球棍模型,思考下列问题。
②甲烷、乙烷、丙烷和丁烷在组成和结构上有什么关系?
结构相似:
分子组成:
碳原子间均以单键结合成链状。
分子式的通式相同;
分子式相差CH2原子团。
二、同系物
2.特点:
分子的形状相似、结构相似、化学性质相似
同类物质:
化学键种类相同,分子式不同、
组成上相差一个或n个CH2原子团(n≥1)。
通式相同:
结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物。
1.定义
1、下列物质中属于同系物的是_________。
① CH2= CH-CH3
② CH4
③ CH3CH2CH3
④ CH3(CH2)5CH(CH3)CH3
⑤
CH2—CH2
CH2—CH2
②③④
注意:
①同系物所含元素种类一定相同,
②同系物分子式一定不相同,一定具有不同的相对分子质量
(相差14n)
③同系物一定符合同一通式,
但符合同一通式的不一定是同系物。
2、下列物质中属于同系物的是 _________。
① CH2=CH-CH3 丙烯 ② CH4 ③ CH3CH2CH3
④ CH3(CH2)5CH(CH3)CH3 ⑤
CH2—CH2
CH2—CH2
②③④
⑤⑦
⑥ CH2=CH2 乙烯
⑦
环丁烷
④同系物必为同一类物质
注意:
①⑥
烷烃中碳碳结合成链状,链状不是“直线状”,而是呈锯齿状,
链上还可分出支链,如图所示。
思考2:烷烃中碳碳结合成链状,链状是不是“直线状”?为什么?
思考1:不同烷烃的含氢量是否相同?谁的含氢量最大?
烷烃是饱和烃,相同碳原子数的有机物分子里,链状烷烃的含氢量最大。
注意
碳链不是一条直线,呈锯齿状
2.写出满足下列条件的烷烃的分子式
(1)分子中含 18 个氢原子的链状烷烃分子式为________。
相对分子质量为 58 的链状烷烃分子式为________。
(2)含碳质量分数最低的烷烃是______;
和 CO2 密度相同的烷烃是_______;
碳、氢质量比为 5∶1 的烷烃是________。
C8H18
C4H10
CH4
C3H8
C5H12
(3) ①烷烃A在同温同压下蒸气的密度是H2的43倍:___________。
②烷烃B的分子中含有200个氢原子:___________。
③一个分子中含有26个电子的烷烃:___________。
C6H14
C99H200
C3H8
烷烃的物理性质
任务二、探究烷烃的物理性质
学生活动1:结合下表数据,思考烷烃的物理性质具有哪些特点和
规律?
几种烷烃的物理性质
名称 结构简式 常温状态 熔沸点(℃) 沸点(℃) 相对密度 水熔性
甲烷 CH4 气 -182.6 -161.7 0.466 不溶
乙烷 CH3CH3 气 -172.0 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -187.1 -42.2 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -135.0 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -129.7 36.1 0.6262 不溶
葵烷 CH3(CH2)8CH3 液 -29.7 174.0 0.730 不溶
十七烷 CH3(CH2)15CH3 固 22 303 0.777 不溶
烷烃的物理性质
任务二、探究烷烃的物理性质
①随分子中碳原子数增加(相对分子质量也在增大),熔、沸点逐渐升高。
②随分子中碳原子数增加,状态由气态→液态→固态,其中常温、常压下碳原子数小于或等于4的烷烃为气态。
③随分子中碳原子数增加(相对分子质量也在增大),密度逐渐增大且均比水的密度小,均难溶于水,易溶于汽油、乙醇、苯等有机溶剂。
④根据教材P63页图7-7可知,当碳原子数相同时,一般支链越多,沸点越低。如沸点:正丁烷>异丁烷。
C1~C4为气态
C5~C16为液态
C17及以上为固态
结构相似,随相对分子质量增大,范德华力逐渐增大
烷烃的物理性质
任务二、探究烷烃的物理性质
学生活动1:探究常温常压下,CH4、C2H6和C3H8一定为气体,C4H10、
C5H12、C6H14一定呈液态吗?
①常温常压下,分子中碳原子数n≤4的烷烃为气态,故C4H10为气态。
②戊烷(C5H12)有三种同分异构体:正戊烷[CH3(CH2)3CH3]熔点-129.7℃、沸点36.1℃、异戊烷[CH3CH2CH(CH3)2]熔点-159.6℃、沸点27.8℃、新戊烷[C(CH3)4]熔点-20℃、沸点9.5℃,因此戊烷中的新戊烷在常温常压下为气体,其余两种为液体
正戊烷
异
戊
烷
新
戊
烷
烷烃的物理性质
【典例1】在1.013×105 Pa下,测得某些烷烃的沸点见下表。据表分
析,下列选项正确的是( )
【解析】由题表信息可知,新戊烷的沸点是9.5 ℃,标准状况下是液体,20 ℃时是气体,A、B项错误;烷烃随碳原子数的增加,熔点升高,C项错误;C5H12的三种同分异构体中,随支链数的增加,沸点降低,D项正确。
D
物质名称及结构简式 沸点/℃
正丁烷CH3(CH2)2CH3 -0.5
正戊烷CH3(CH2)3CH3 36.1
异戊烷 27.8
新戊烷C(CH3)4 9.5
正己烷CH3(CH2)4CH3 69.0
A.在标准状况下,新戊烷是气体B.在1.013×105 Pa、20 ℃时,戊烷
都是液体C.烷烃随碳原子数的增加,熔点降低D.分子式为C5H12的烷烃的同分异构
体中,随支链的增加,沸点降低
烷烃的物理性质
【典例2】在下列5种物质沸点的排列顺序中,正确的是( )
①正丁烷 ②2 甲基丙烷[CH3CH(CH3)CH3] ③戊烷 ④2 甲基丁烷
[CH3CH(CH3)CH2CH3] ⑤2,2 二甲基丙烷[C(CH3)4]
A.①>②>③>④>⑤ B.⑤>④>③>②>①
C.③>④>⑤>①>② D.②>①>⑤>④>③
【解析】有机物同系物中,随着碳原子数的增加,相对分子质量增大,分子间作用力增大,熔、沸点逐渐升高;分子式相同的烃,支链越多,熔、沸点越低。分析各选项,①②均有4个C原子,③④⑤均有5个碳原子,故①②的沸点小于③④⑤的沸点;②有1个支链,而①无,故①>②;③无支链,④有1个支链,⑤有2个支链,故③>④>⑤。综上所述:③>④>⑤>①>②。
C
人教版必修第二册
第七章 有机化合物
第一节 认识有机化合物
第2课时 烷烃的结构
学习目标
1、通过甲烷结构迁移能说出烷烃的定义并能辨别烷烃结构特点,会准确判断烷烃的结构简式并能书写烷烃的结构简式。
2、能归纳烷烃的物理性质递变性、化学性质相似性
3、能复述同系物的定义,会应用同系物的概念处理相关问题
学习指导 学习任务
1、阅读课本P62的文字、观察图3-4 1、说出烷烃的定义、通式,并提取关键词,归纳烷烃的结构特点(2min)。
2、通过书写练习掌握烷烃的结构简式的书写(3min)
2、阅读课本P63表3-1 填写优化设计P69知识梳理一烷烃 阅读优化P88同系物判断 1、结合课本P63总结出烷烃物理性质、化学性质的相似性及递变性(3min)
2、阅读课本P63理解同系物及同分异构现象(3min)
自学指导 准备课本、优化设计、导学案、红和黑色笔
分子式 电子式 结构式 空间构型 球棍模型 空间填充模型
空间填充模型能表示CH4分子的真实结构
CH4 的空间结构——正四面体
甲烷分子中5个原子不在同一平面上,而是形成了正四面体的空间结构。
4个C—H键的长度和强度相同,相互之间的夹角相等,为109°28′。
CH4
后教环节:
仅含碳和氢两种元素的有机化合物称为碳氢化合物,也称为烃。
碳 + 氢 =
烃
tàn qīng
tīng
最简单的烷烃——甲烷
你知道“烃”字的由来吗?
【P62思考与交流】
(1)与甲烷结构相似的有机化合物还有很多,随着分子中碳原子数的增加,还有乙烷、丙烷、丁烷等一系列有机化合物。请根据碳原子的成键规律和下表提供的信息,写出丁烷的结构式和乙烷、丙烷、丁烷的分子式,并由此归纳这类有机化合物分子式的通式。
C2H6
C3H8
C4H10
思考与交流:
(3)结合图 7-6 中的分子结构模型,
总结这类有机化合物的组成和分子结构特点。
只含碳和氢两种元素,分子中的碳原子之间都以单键结合,
碳原子的剩余价键均与氢原子结合,
使碳原子的化合价都达到“饱和”。
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
结构简式:
任务一、认识烷烃
1.定义
碳原子之间都以碳碳单键结合,碳原子剩余的价键均用于与氢原子 结合,使每个碳原子的化合价达到“饱和”的烃称为饱和烃,
也称为烷烃。
“饱和” 碳原子的四个共价键分别连接 4 个原子。
注意:
2.分子结构特点
③饱和:
一、烷烃
①元素:
②单键:
④碳骨架:
只含有碳和氢两种元素
碳原子之间只以碳碳单键结合
每个碳原子均形成4个价键,分别连接4个原子
可以是链状结构,也可以是环状结构
高中阶段一般不探讨环烷烃的有关结构和性质
链状烷烃的分子组成通式为
链状烷烃分子中的共价键数为
一、烷烃
3.分子组成通式
CnH2n (n≥3)
CnH2n+2 (n≥1)
(2n+2)+(n-1)=3n+1
烷烃包含链状烷烃和环状烷烃,没有特别注明我们讲的烷烃都是特指链状烷烃
环状烷烃的分子组成通式为
1、下列物质属于有机物的是 ;
下列物质属于烃的是_________________
下列有机物中,属于烷烃的是________
①⑤⑥⑦⑧⑨
⑧⑨
①⑧⑨
①C2H2 ②HCN ③H2CO3
④金刚石 ⑤CH3Cl ⑥CCl4
⑦CH3COOH ⑧CH4
⑨C2H6 ⑩CaCO3 CO2
判断烷烃的标准:
①只含有碳碳单键和碳氢元素
②分子式符合通式CnH2n+2 (n≥1)
思考与讨论
①分别写出它们的分子式和结构简式。
以下是甲烷、乙烷、丙烷和丁烷的球棍模型,思考下列问题。
②甲烷、乙烷、丙烷和丁烷在组成和结构上有什么关系?
结构相似:
分子组成:
碳原子间均以单键结合成链状。
分子式的通式相同;
分子式相差CH2原子团。
二、同系物
2.特点:
分子的形状相似、结构相似、化学性质相似
同类物质:
化学键种类相同,分子式不同、
组成上相差一个或n个CH2原子团(n≥1)。
通式相同:
结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物。
1.定义
1、下列物质中属于同系物的是_________。
① CH2= CH-CH3
② CH4
③ CH3CH2CH3
④ CH3(CH2)5CH(CH3)CH3
⑤
CH2—CH2
CH2—CH2
②③④
注意:
①同系物所含元素种类一定相同,
②同系物分子式一定不相同,一定具有不同的相对分子质量
(相差14n)
③同系物一定符合同一通式,
但符合同一通式的不一定是同系物。
2、下列物质中属于同系物的是 _________。
① CH2=CH-CH3 丙烯 ② CH4 ③ CH3CH2CH3
④ CH3(CH2)5CH(CH3)CH3 ⑤
CH2—CH2
CH2—CH2
②③④
⑤⑦
⑥ CH2=CH2 乙烯
⑦
环丁烷
④同系物必为同一类物质
注意:
①⑥
烷烃中碳碳结合成链状,链状不是“直线状”,而是呈锯齿状,
链上还可分出支链,如图所示。
思考2:烷烃中碳碳结合成链状,链状是不是“直线状”?为什么?
思考1:不同烷烃的含氢量是否相同?谁的含氢量最大?
烷烃是饱和烃,相同碳原子数的有机物分子里,链状烷烃的含氢量最大。
注意
碳链不是一条直线,呈锯齿状
2.写出满足下列条件的烷烃的分子式
(1)分子中含 18 个氢原子的链状烷烃分子式为________。
相对分子质量为 58 的链状烷烃分子式为________。
(2)含碳质量分数最低的烷烃是______;
和 CO2 密度相同的烷烃是_______;
碳、氢质量比为 5∶1 的烷烃是________。
C8H18
C4H10
CH4
C3H8
C5H12
(3) ①烷烃A在同温同压下蒸气的密度是H2的43倍:___________。
②烷烃B的分子中含有200个氢原子:___________。
③一个分子中含有26个电子的烷烃:___________。
C6H14
C99H200
C3H8
烷烃的物理性质
任务二、探究烷烃的物理性质
学生活动1:结合下表数据,思考烷烃的物理性质具有哪些特点和
规律?
几种烷烃的物理性质
名称 结构简式 常温状态 熔沸点(℃) 沸点(℃) 相对密度 水熔性
甲烷 CH4 气 -182.6 -161.7 0.466 不溶
乙烷 CH3CH3 气 -172.0 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -187.1 -42.2 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -135.0 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -129.7 36.1 0.6262 不溶
葵烷 CH3(CH2)8CH3 液 -29.7 174.0 0.730 不溶
十七烷 CH3(CH2)15CH3 固 22 303 0.777 不溶
烷烃的物理性质
任务二、探究烷烃的物理性质
①随分子中碳原子数增加(相对分子质量也在增大),熔、沸点逐渐升高。
②随分子中碳原子数增加,状态由气态→液态→固态,其中常温、常压下碳原子数小于或等于4的烷烃为气态。
③随分子中碳原子数增加(相对分子质量也在增大),密度逐渐增大且均比水的密度小,均难溶于水,易溶于汽油、乙醇、苯等有机溶剂。
④根据教材P63页图7-7可知,当碳原子数相同时,一般支链越多,沸点越低。如沸点:正丁烷>异丁烷。
C1~C4为气态
C5~C16为液态
C17及以上为固态
结构相似,随相对分子质量增大,范德华力逐渐增大
烷烃的物理性质
任务二、探究烷烃的物理性质
学生活动1:探究常温常压下,CH4、C2H6和C3H8一定为气体,C4H10、
C5H12、C6H14一定呈液态吗?
①常温常压下,分子中碳原子数n≤4的烷烃为气态,故C4H10为气态。
②戊烷(C5H12)有三种同分异构体:正戊烷[CH3(CH2)3CH3]熔点-129.7℃、沸点36.1℃、异戊烷[CH3CH2CH(CH3)2]熔点-159.6℃、沸点27.8℃、新戊烷[C(CH3)4]熔点-20℃、沸点9.5℃,因此戊烷中的新戊烷在常温常压下为气体,其余两种为液体
正戊烷
异
戊
烷
新
戊
烷
烷烃的物理性质
【典例1】在1.013×105 Pa下,测得某些烷烃的沸点见下表。据表分
析,下列选项正确的是( )
【解析】由题表信息可知,新戊烷的沸点是9.5 ℃,标准状况下是液体,20 ℃时是气体,A、B项错误;烷烃随碳原子数的增加,熔点升高,C项错误;C5H12的三种同分异构体中,随支链数的增加,沸点降低,D项正确。
D
物质名称及结构简式 沸点/℃
正丁烷CH3(CH2)2CH3 -0.5
正戊烷CH3(CH2)3CH3 36.1
异戊烷 27.8
新戊烷C(CH3)4 9.5
正己烷CH3(CH2)4CH3 69.0
A.在标准状况下,新戊烷是气体B.在1.013×105 Pa、20 ℃时,戊烷
都是液体C.烷烃随碳原子数的增加,熔点降低D.分子式为C5H12的烷烃的同分异构
体中,随支链的增加,沸点降低
烷烃的物理性质
【典例2】在下列5种物质沸点的排列顺序中,正确的是( )
①正丁烷 ②2 甲基丙烷[CH3CH(CH3)CH3] ③戊烷 ④2 甲基丁烷
[CH3CH(CH3)CH2CH3] ⑤2,2 二甲基丙烷[C(CH3)4]
A.①>②>③>④>⑤ B.⑤>④>③>②>①
C.③>④>⑤>①>② D.②>①>⑤>④>③
【解析】有机物同系物中,随着碳原子数的增加,相对分子质量增大,分子间作用力增大,熔、沸点逐渐升高;分子式相同的烃,支链越多,熔、沸点越低。分析各选项,①②均有4个C原子,③④⑤均有5个碳原子,故①②的沸点小于③④⑤的沸点;②有1个支链,而①无,故①>②;③无支链,④有1个支链,⑤有2个支链,故③>④>⑤。综上所述:③>④>⑤>①>②。
C
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
