化学人教版(2019)选择性必修3 3.1.1卤代烃(共27张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.1.1卤代烃(共27张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-06 00:00:00 | ||
图片预览




文档简介
(共27张PPT)
卤代烃
YOUR SITE HERE
光
FeBr3
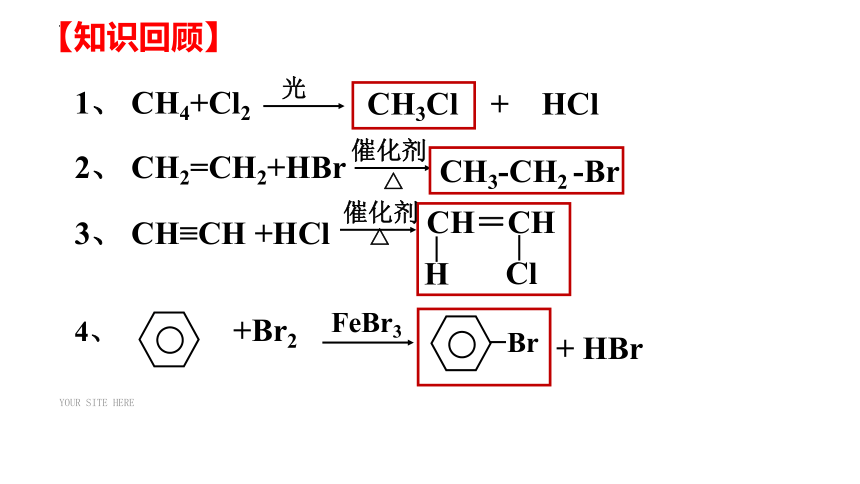
1、 CH4+Cl2
2、 CH2=CH2+HBr
3、 CH≡CH +HCl
4、 +Br2
CH3-CH2 -Br
CH3Cl + HCl
Br
+ HBr
H
CH=CH
Cl
【知识回顾】
催化剂
催化剂
△
△
一、卤代烃
1、定义:
★卤代烃不是烃,而是烃的衍生物。
★表示通式:R—X(X表示卤素原子:F、Cl、Br、I)
烃分子中的氢原子被卤素原子取代后所生成的化合物.
官能团:
卤素原子
2.卤代烃的分类
卤代烃
按卤素原子的种类
,如CH2==CHF
,如CH3CH2Cl
,如CH3CH2Br
,如CH3I
按烃基的种类
饱和卤代烃,如CH3CH2Cl
不饱和卤代烃,如CH2==CHF
芳香卤代烃,如 、
氟代烃
氯代烃
溴代烃
碘代烃
按卤素原子的数目
卤代烃,如CH3Cl
卤代烃,如CH2Cl2
单
多
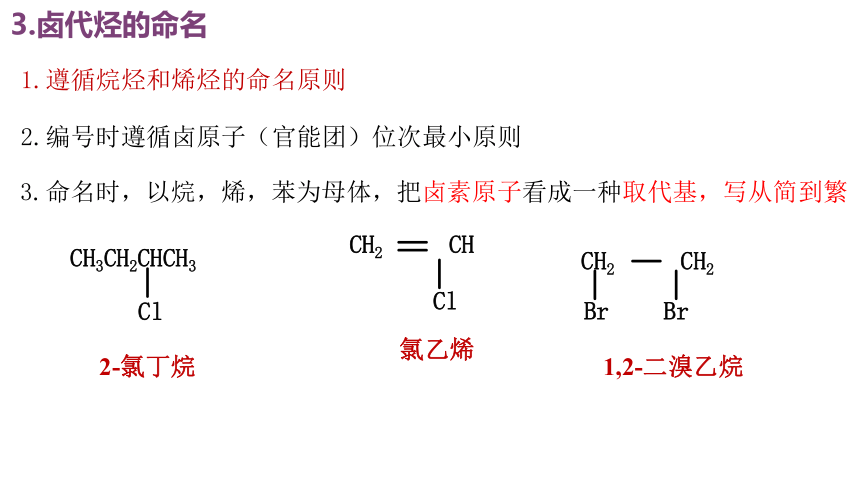
3.卤代烃的命名
2-氯丁烷
氯乙烯
1,2-二溴乙烷
CH3CH2CHCH3
Cl
CH2 CH
Cl
CH2 CH2
Br
Br
2.编号时遵循卤原子(官能团)位次最小原则
3.命名时,以烷,烯,苯为母体,把卤素原子看成一种取代基,写从简到繁
1.遵循烷烃和烯烃的命名原则
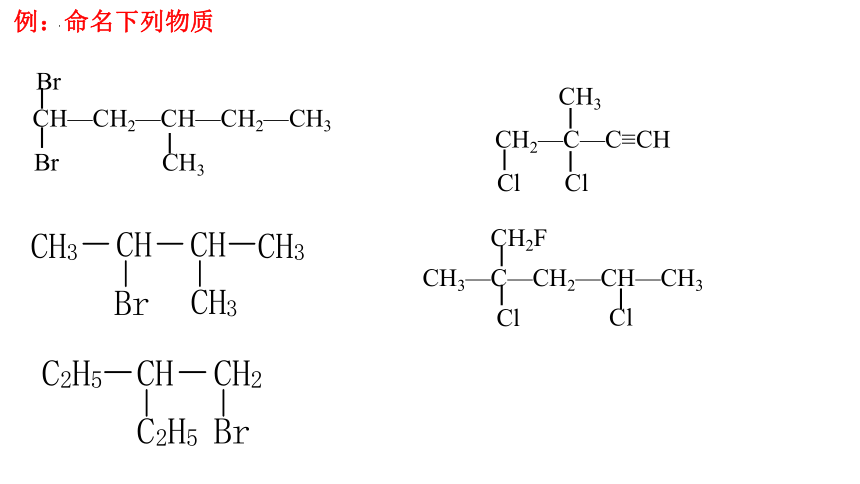
CH—CH2—CH—CH2—CH3
Br
Br
CH3
例:命名下列物质
CH2—C—C≡CH
Cl
CH3
Cl
CH3—C—CH2—CH—CH3
Cl
CH2F
Cl
状态:常温下卤代烃除一氯甲烷、氯乙烯、氯乙烷是气体外,其余均为液体
或固体。
密度:除脂肪烃的一氟代物和一氯代物外,其余液态卤代烃密度一般比水大。
卤代烃的密度随碳原子数目的增加而减小。
溶解性:卤代烃都不溶于水,可溶于有机溶剂。
沸点: 熔沸点大于同碳个数的烃,随碳原子数增多,沸点依次升高(碳原子
数相同时,支链越多沸点越低)。
阅读54页教材,并结合烷烃的物理性质,分析表3-1,总结卤代烃的物理性质及其递变规律。
二.卤代烃的物理性质
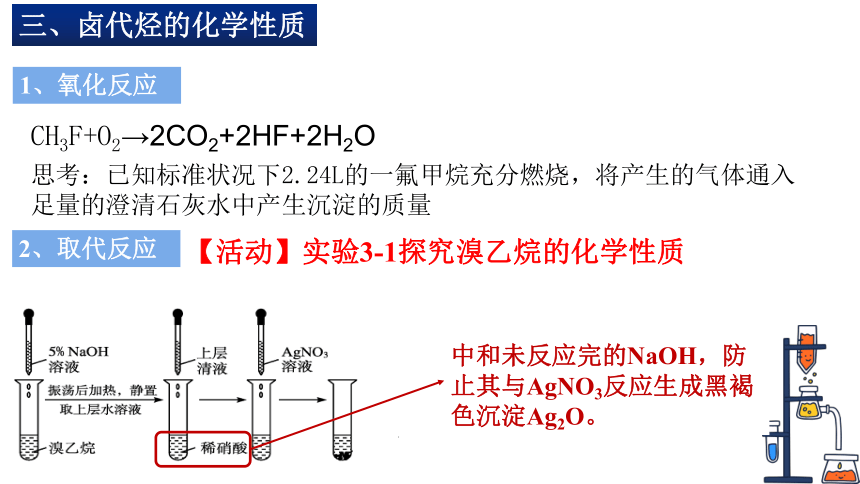
三、卤代烃的化学性质
CH3F+O2→2CO2+2HF+2H2O
思考:已知标准状况下2.24L的一氟甲烷充分燃烧,将产生的气体通入足量的澄清石灰水中产生沉淀的质量
2、取代反应
1、氧化反应
【活动】实验3-1探究溴乙烷的化学性质
中和未反应完的NaOH,防止其与AgNO3反应生成黑褐色沉淀Ag2O。
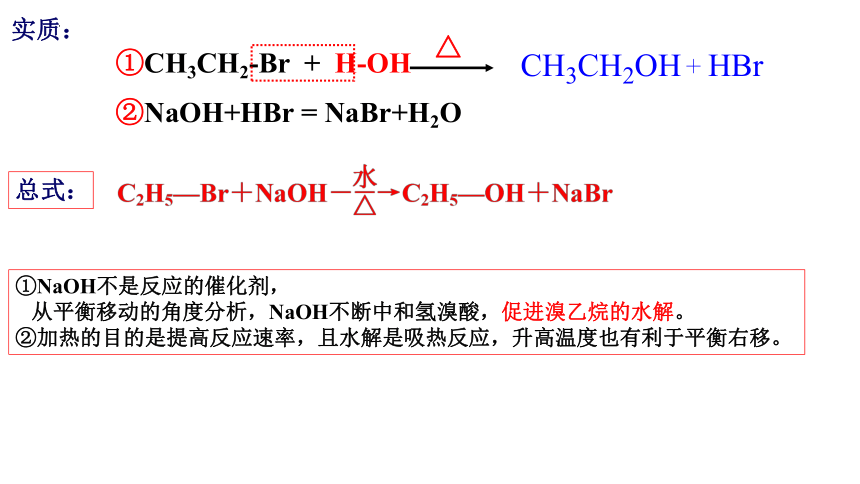
①CH3CH2-Br + H-OH
△
②NaOH+HBr = NaBr+H2O
实质:
总式:
①NaOH不是反应的催化剂,
从平衡移动的角度分析,NaOH不断中和氢溴酸,促进溴乙烷的水解。
②加热的目的是提高反应速率,且水解是吸热反应,升高温度也有利于平衡右移。
CH3CH2CH2Cl+NaOH
水
△
课堂练习:
CH3CHCl2+NaOH
水
△
CH3CCl3+NaOH
水
△
CH3CCl2CH3+NaOH
水
△
总结:1个卤素连C上可得醇
2个卤素连端C可得醛,连中间C可得酮、
3个卤素连同一个C上可得羧酸盐
4个卤素连同一个C上可得碳酸盐
CCl4+NaOH
水
△
水
△
+ NaOH
水
△
+ NaOH
+ NaBr
+ 2 NaBr
2
1、写出下列卤代烃的水解方程式
【即时巩固】
分析卤代烃的结构特点,为什么卤代烃取代反应断的是C-X键?
卤代烃中卤素原子吸引电子能力较强,共用电子对偏向卤素原子,使C—X键具有较强的极性,所以卤代烃具有较强的反应活性,易发生取代反应和消去反应。
【思考与讨论】
例:溴乙烷和乙烷的结构相似,区别在于C-H键与C-Br键的不同。C-Br键为极性键,由于溴原子吸引电子能力强,C-Br键易断裂,使溴原子易被取代。
3、消去反应
醇 (非水环境)
△
①H-C C-H
Br
H
H
H
CH2=CH2↑
+ HBr
Br
H
②NaOH + HBr=NaBr + H2O
总反应式:
CH3CH2Br +NaOH
CH2=CH2↑+ NaBr+ H2O
醇
有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(含H:H2O、HX),生成不饱和(含双键或三键)化合物的反应,叫消去反应。
(1)要有卤素元素(条件强碱醇溶液)例如CH3Br。
(3)有两个邻位碳原子,且碳原子上均有氢原子时,发生消去反应可能生成不同的产物。例如,
发生消去反应的产物为CH3—CH=CH—CH3、CH2 = CH—CH2—CH3。
(2)有邻位碳原子邻位碳原子上存在氢原子例如
卤代烃的消去反应规律
β
α
【问题】卤代烷在不同溶剂中发生反应的情况不同。如何通过实验的方法验 证取代反应和消去反应的产物?
(1)波谱分析:红外光谱法、核磁共振氢谱
(2)①消去反应:已讲
②如图3-3所示,向圆底烧瓶中加入2.0 gNaOH和15mL无水乙醇,搅拌。
再向其中加入5mL1﹣溴丁烷和几片碎瓷片,微热。
将产生的气体通入盛水的试管后,再用酸性高锰酸钾溶液进行检验。
现象:有气泡产生,高锰酸钾溶液褪色
CH3CH2CH2CH2Br
+NaOH
△
醇
CH3CH2CH=CH2↑+NaBr+H2O
结论:
P54【讨论】(1)为什么要在气体通入酸性高锰酸钾溶液前先通入盛水的试管?还可以用什么试剂检验(丁烯)?此时还有必要将气体先通入水中吗?
①水的作用:除去丁烯中混有的乙醇蒸汽。(乙醇可以使酸性高锰酸钾溶液褪色,对丁烯的检验产生干扰)
②可以用溴的CCl4溶液或溴水检验乙烯,由于乙醇不可以使溴的CCl4溶液或溴水褪色,可以不必通过盛水的洗气装置。
课堂练习:
CH2ClCH2Cl+NaOH
乙醇
△
CH3CHClCOOH+NaOH
乙醇
△
口诀:“有醇则无醇,无醇则有醇”
消去反应
取代反应
比较1-溴丁烷的取代反应和消去反应
取代反应 消去反应
反应物
反应条件
生成物
化学键变化
结论
CH3CH2CH2CH2Br+NaOH
CH3CH2CH2CH2Br+NaOH
NaOH水溶液,加热
NaOH醇溶液,加热
CH3CH2CH2CH2OH、NaBr
CH3CH2CH=CH2 、NaBr、H2O
溴丁烷在不同的条件下发生不同类型的反应
1、卤代烃的用途:
溶剂
卤代烃
致冷剂
医用
灭火剂
麻醉剂
农药
七氟丙烷
灭火器
三氯乙烷
修正液
四氯乙烯
干洗剂
DDT
农药
碳氟化合物
人造血液
氟氯代烷
致冷剂
复方氯乙烷气雾剂
阅读课本P57,了解卤代烃的用途和氟氯代烷对环境的危害
(2)制备烯烃或炔烃
RCH2CH2X RCH=CH2
强碱的醇溶液
(1)制备醇:R-X R-OH
强碱的水溶液
2.有机合成的重要原料:
△
△
Br2
光照
NaOH、△
CH3CH2OH
例、以CH3CH2Br 为主要原料制备CH2BrCH2Br
CH3CH2Br
CH2=CH2
CH2BrCH2Br
思路2
思路1
CH3CH2Br
Br2
CH2BrCH2Br
更好!
2、由乙烯为主要原料来制HO-CH2-CH2OH(乙二醇)
1、由溴乙烷为主要原料来制氯乙烷
练一练
按步骤写出方程式,注明反应类型
练1:下列卤代烃在 KOH 醇溶液中加热不反应的是____
② (CH3)2CHCH2Cl
③ ④ CHCl2CH2Br
⑤ (CH3)3CCH2Cl ⑥
⑦ CH2=CHCl
Cl
【结论】①所有的卤代烃都能发生水解反应,
②相邻C上有H的卤代烃才能发生消去反应
①③⑤
练2、下列物质既能发生消去反应,又能发生水解
反应的是( )
A.一氯甲烷
B.1 -溴- 2- 甲基丙烷
C.1- 氯- 2,2- 二甲基丙烷
D.3- 氯 -2,2,4,4 -四甲基戊烷
B
练3、根据下面的反应路线及所给信息填空。
A
Cl2、光照
①
Cl
NaOH、乙醇
△
②
Br2的CCl4溶液
③
B
④
(1)A的结构简式是______名称是__________
(2)①的反应类型是______反应 ②的反应类型是_______反应
(3)反应④的化学方程式是
________________________________
环己烷
取代
消去
Br
Br
+2NaOH
醇
△
+2NaBr+2H2O
3、由
Cl
-
为主要原料制备
OH
HO
2、由乙烯为主要原料来制HO-CH2-CH2OH
1、由溴乙烷为主要原料来制氯乙烷
练一练
按步骤写出方程式,注明反应类型
卤代烃
YOUR SITE HERE
光
FeBr3
1、 CH4+Cl2
2、 CH2=CH2+HBr
3、 CH≡CH +HCl
4、 +Br2
CH3-CH2 -Br
CH3Cl + HCl
Br
+ HBr
H
CH=CH
Cl
【知识回顾】
催化剂
催化剂
△
△
一、卤代烃
1、定义:
★卤代烃不是烃,而是烃的衍生物。
★表示通式:R—X(X表示卤素原子:F、Cl、Br、I)
烃分子中的氢原子被卤素原子取代后所生成的化合物.
官能团:
卤素原子
2.卤代烃的分类
卤代烃
按卤素原子的种类
,如CH2==CHF
,如CH3CH2Cl
,如CH3CH2Br
,如CH3I
按烃基的种类
饱和卤代烃,如CH3CH2Cl
不饱和卤代烃,如CH2==CHF
芳香卤代烃,如 、
氟代烃
氯代烃
溴代烃
碘代烃
按卤素原子的数目
卤代烃,如CH3Cl
卤代烃,如CH2Cl2
单
多
3.卤代烃的命名
2-氯丁烷
氯乙烯
1,2-二溴乙烷
CH3CH2CHCH3
Cl
CH2 CH
Cl
CH2 CH2
Br
Br
2.编号时遵循卤原子(官能团)位次最小原则
3.命名时,以烷,烯,苯为母体,把卤素原子看成一种取代基,写从简到繁
1.遵循烷烃和烯烃的命名原则
CH—CH2—CH—CH2—CH3
Br
Br
CH3
例:命名下列物质
CH2—C—C≡CH
Cl
CH3
Cl
CH3—C—CH2—CH—CH3
Cl
CH2F
Cl
状态:常温下卤代烃除一氯甲烷、氯乙烯、氯乙烷是气体外,其余均为液体
或固体。
密度:除脂肪烃的一氟代物和一氯代物外,其余液态卤代烃密度一般比水大。
卤代烃的密度随碳原子数目的增加而减小。
溶解性:卤代烃都不溶于水,可溶于有机溶剂。
沸点: 熔沸点大于同碳个数的烃,随碳原子数增多,沸点依次升高(碳原子
数相同时,支链越多沸点越低)。
阅读54页教材,并结合烷烃的物理性质,分析表3-1,总结卤代烃的物理性质及其递变规律。
二.卤代烃的物理性质
三、卤代烃的化学性质
CH3F+O2→2CO2+2HF+2H2O
思考:已知标准状况下2.24L的一氟甲烷充分燃烧,将产生的气体通入足量的澄清石灰水中产生沉淀的质量
2、取代反应
1、氧化反应
【活动】实验3-1探究溴乙烷的化学性质
中和未反应完的NaOH,防止其与AgNO3反应生成黑褐色沉淀Ag2O。
①CH3CH2-Br + H-OH
△
②NaOH+HBr = NaBr+H2O
实质:
总式:
①NaOH不是反应的催化剂,
从平衡移动的角度分析,NaOH不断中和氢溴酸,促进溴乙烷的水解。
②加热的目的是提高反应速率,且水解是吸热反应,升高温度也有利于平衡右移。
CH3CH2CH2Cl+NaOH
水
△
课堂练习:
CH3CHCl2+NaOH
水
△
CH3CCl3+NaOH
水
△
CH3CCl2CH3+NaOH
水
△
总结:1个卤素连C上可得醇
2个卤素连端C可得醛,连中间C可得酮、
3个卤素连同一个C上可得羧酸盐
4个卤素连同一个C上可得碳酸盐
CCl4+NaOH
水
△
水
△
+ NaOH
水
△
+ NaOH
+ NaBr
+ 2 NaBr
2
1、写出下列卤代烃的水解方程式
【即时巩固】
分析卤代烃的结构特点,为什么卤代烃取代反应断的是C-X键?
卤代烃中卤素原子吸引电子能力较强,共用电子对偏向卤素原子,使C—X键具有较强的极性,所以卤代烃具有较强的反应活性,易发生取代反应和消去反应。
【思考与讨论】
例:溴乙烷和乙烷的结构相似,区别在于C-H键与C-Br键的不同。C-Br键为极性键,由于溴原子吸引电子能力强,C-Br键易断裂,使溴原子易被取代。
3、消去反应
醇 (非水环境)
△
①H-C C-H
Br
H
H
H
CH2=CH2↑
+ HBr
Br
H
②NaOH + HBr=NaBr + H2O
总反应式:
CH3CH2Br +NaOH
CH2=CH2↑+ NaBr+ H2O
醇
有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(含H:H2O、HX),生成不饱和(含双键或三键)化合物的反应,叫消去反应。
(1)要有卤素元素(条件强碱醇溶液)例如CH3Br。
(3)有两个邻位碳原子,且碳原子上均有氢原子时,发生消去反应可能生成不同的产物。例如,
发生消去反应的产物为CH3—CH=CH—CH3、CH2 = CH—CH2—CH3。
(2)有邻位碳原子邻位碳原子上存在氢原子例如
卤代烃的消去反应规律
β
α
【问题】卤代烷在不同溶剂中发生反应的情况不同。如何通过实验的方法验 证取代反应和消去反应的产物?
(1)波谱分析:红外光谱法、核磁共振氢谱
(2)①消去反应:已讲
②如图3-3所示,向圆底烧瓶中加入2.0 gNaOH和15mL无水乙醇,搅拌。
再向其中加入5mL1﹣溴丁烷和几片碎瓷片,微热。
将产生的气体通入盛水的试管后,再用酸性高锰酸钾溶液进行检验。
现象:有气泡产生,高锰酸钾溶液褪色
CH3CH2CH2CH2Br
+NaOH
△
醇
CH3CH2CH=CH2↑+NaBr+H2O
结论:
P54【讨论】(1)为什么要在气体通入酸性高锰酸钾溶液前先通入盛水的试管?还可以用什么试剂检验(丁烯)?此时还有必要将气体先通入水中吗?
①水的作用:除去丁烯中混有的乙醇蒸汽。(乙醇可以使酸性高锰酸钾溶液褪色,对丁烯的检验产生干扰)
②可以用溴的CCl4溶液或溴水检验乙烯,由于乙醇不可以使溴的CCl4溶液或溴水褪色,可以不必通过盛水的洗气装置。
课堂练习:
CH2ClCH2Cl+NaOH
乙醇
△
CH3CHClCOOH+NaOH
乙醇
△
口诀:“有醇则无醇,无醇则有醇”
消去反应
取代反应
比较1-溴丁烷的取代反应和消去反应
取代反应 消去反应
反应物
反应条件
生成物
化学键变化
结论
CH3CH2CH2CH2Br+NaOH
CH3CH2CH2CH2Br+NaOH
NaOH水溶液,加热
NaOH醇溶液,加热
CH3CH2CH2CH2OH、NaBr
CH3CH2CH=CH2 、NaBr、H2O
溴丁烷在不同的条件下发生不同类型的反应
1、卤代烃的用途:
溶剂
卤代烃
致冷剂
医用
灭火剂
麻醉剂
农药
七氟丙烷
灭火器
三氯乙烷
修正液
四氯乙烯
干洗剂
DDT
农药
碳氟化合物
人造血液
氟氯代烷
致冷剂
复方氯乙烷气雾剂
阅读课本P57,了解卤代烃的用途和氟氯代烷对环境的危害
(2)制备烯烃或炔烃
RCH2CH2X RCH=CH2
强碱的醇溶液
(1)制备醇:R-X R-OH
强碱的水溶液
2.有机合成的重要原料:
△
△
Br2
光照
NaOH、△
CH3CH2OH
例、以CH3CH2Br 为主要原料制备CH2BrCH2Br
CH3CH2Br
CH2=CH2
CH2BrCH2Br
思路2
思路1
CH3CH2Br
Br2
CH2BrCH2Br
更好!
2、由乙烯为主要原料来制HO-CH2-CH2OH(乙二醇)
1、由溴乙烷为主要原料来制氯乙烷
练一练
按步骤写出方程式,注明反应类型
练1:下列卤代烃在 KOH 醇溶液中加热不反应的是____
② (CH3)2CHCH2Cl
③ ④ CHCl2CH2Br
⑤ (CH3)3CCH2Cl ⑥
⑦ CH2=CHCl
Cl
【结论】①所有的卤代烃都能发生水解反应,
②相邻C上有H的卤代烃才能发生消去反应
①③⑤
练2、下列物质既能发生消去反应,又能发生水解
反应的是( )
A.一氯甲烷
B.1 -溴- 2- 甲基丙烷
C.1- 氯- 2,2- 二甲基丙烷
D.3- 氯 -2,2,4,4 -四甲基戊烷
B
练3、根据下面的反应路线及所给信息填空。
A
Cl2、光照
①
Cl
NaOH、乙醇
△
②
Br2的CCl4溶液
③
B
④
(1)A的结构简式是______名称是__________
(2)①的反应类型是______反应 ②的反应类型是_______反应
(3)反应④的化学方程式是
________________________________
环己烷
取代
消去
Br
Br
+2NaOH
醇
△
+2NaBr+2H2O
3、由
Cl
-
为主要原料制备
OH
HO
2、由乙烯为主要原料来制HO-CH2-CH2OH
1、由溴乙烷为主要原料来制氯乙烷
练一练
按步骤写出方程式,注明反应类型
