第七单元 常见的酸和碱 复习题(含答案) 鲁教版化学九年级下册
文档属性
| 名称 | 第七单元 常见的酸和碱 复习题(含答案) 鲁教版化学九年级下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 197.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-07 00:00:00 | ||
图片预览





文档简介
第七单元 常见的酸和碱 复习题附答案 鲁教版化学九年级下册
一、选择题。
1、稀盐酸、稀硫酸具有相似的化学性质,是因为组成中含有 ( )
A.酸根 B.H C.O D.原子团
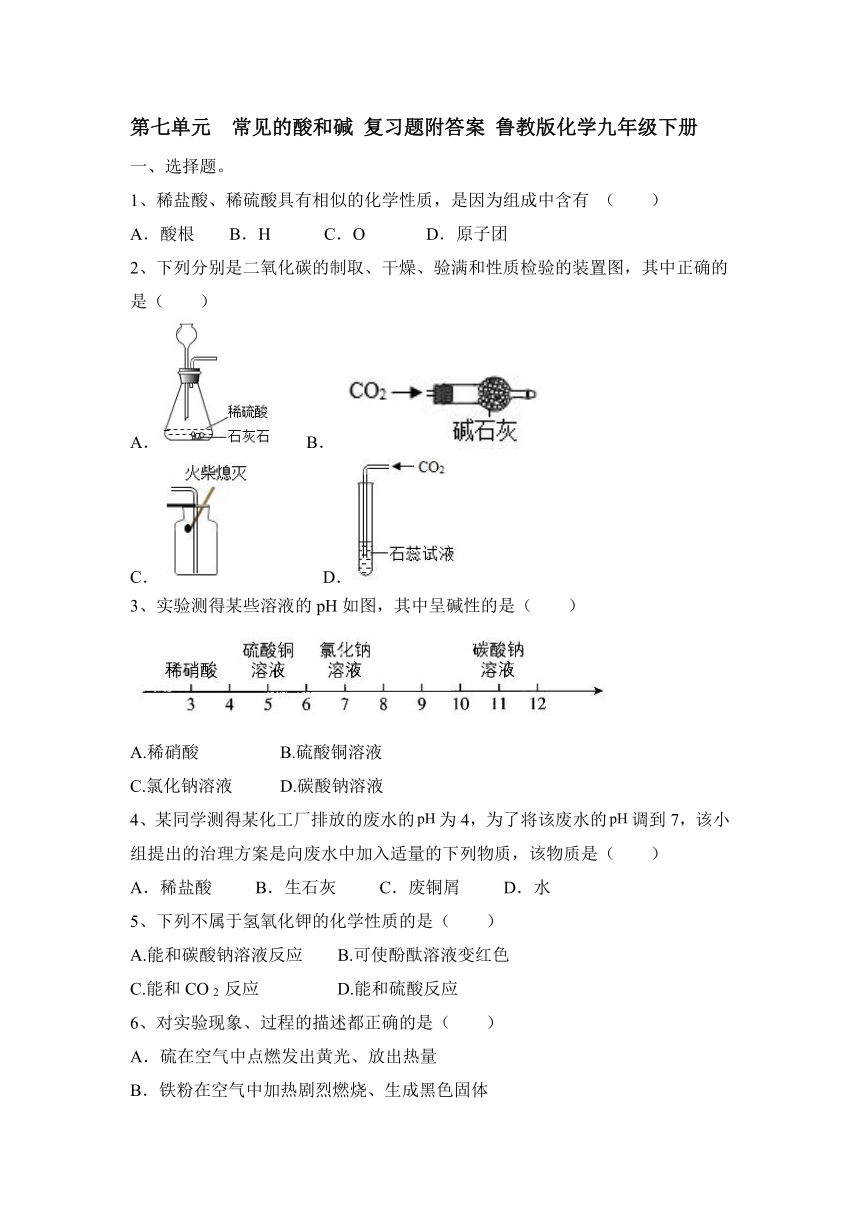
2、下列分别是二氧化碳的制取、干燥、验满和性质检验的装置图,其中正确的是( )
A. B.
C. D.
3、实验测得某些溶液的pH如图,其中呈碱性的是( )
A.稀硝酸 B.硫酸铜溶液
C.氯化钠溶液 D.碳酸钠溶液
4、某同学测得某化工厂排放的废水的为4,为了将该废水的调到7,该小组提出的治理方案是向废水中加入适量的下列物质,该物质是( )
A.稀盐酸 B.生石灰 C.废铜屑 D.水
5、下列不属于氢氧化钾的化学性质的是( )
A.能和碳酸钠溶液反应 B.可使酚酞溶液变红色
C.能和CO 2 反应 D.能和硫酸反应
6、对实验现象、过程的描述都正确的是( )
A.硫在空气中点燃发出黄光、放出热量
B.铁粉在空气中加热剧烈燃烧、生成黑色固体
C.浓硫酸敞口放置溶液的颜色、质量不变
D.烧碱固体放入水中迅速溶解、溶液温度升高
7、下列实验现象描述正确的是( )
A.用木棍蘸取稀硫酸后,木棍变黑
B.打开盛有浓盐酸的试剂瓶,瓶口出现白雾
C.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D.将高锰酸钾放入汽油中,很快溶解形成紫红色溶液
8、下列关于盐酸和硫酸的描述正确的是( )
A.稀盐酸和稀硫酸都能用于除铁锈
B.打开浓盐酸和浓硫酸的试剂瓶塞,瓶口都有白雾
C.向稀盐酸和稀硫酸中滴加BaCl2溶液,都有白色沉淀生成
D.稀释浓硫酸时,应将水沿烧杯壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌
9、使酚酞试液变红的溶液能使紫色石蕊试液呈( )
A.无色 B.蓝色 C.红色 D.紫色
10、室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是( )
A.该图像表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
11、下列有关酸、碱性质和用途的说法不正确的是( )
A.氢氧化钠在生活中可用来去除油污,可做炉具清洁剂
B.氢氧化钠、氢氧化钙化学性质相似,是因为其溶液中都含有金属离子
C.盐酸、硫酸化学性质相似,是因为其溶液中都含有相同的H+
D.用食醋可除去热水瓶胆壁上的水垢
12、下图所示实验操作正确的是( )
A.点燃酒精灯 B.稀释浓硫酸
C.闻气体气味 D.连接玻璃管和橡皮管
13、将10g质量分数为98%的浓硫酸配制成10%的稀硫酸。有关步骤的说法正确的是( )
A.计算需水98g B.量取水时,仰视读数
C.将水注入浓硫酸中,并不断搅拌 D.配制好后,装瓶贴标签
14、下列物质分类正确的是( )
A.混合物:洁净的空气 、黄铜、澄清石灰水
B.酸:盐酸、醋酸、硝酸钠
C.碱:烧碱、纯碱 、熟石灰
D.氧化物:水、氧化铁、碳酸
15、下列水果中酸性最强的是( )
A.苹果pH≈2.9 B.凤梨pH≈4.0
C.香蕉pH≈6.6 D.荔枝pH≈5.0
16、如图两幅微观示意图揭示了化学变化的微观实质。相关说法中错误的是( )
A. 图乙说明中和反应的实质是H+和OH﹣反应生成了H2O
B. 图甲表示的是化合反应
C. 图甲表示的反应中元素的化合价没有改变
D. 上述两图说明化学反应前后原子的种类、数目都不会发生变化
二、填空题。
17、按要求从醋酸,稀硫酸,碳酸,稀盐酸中选择合适的物质,将其化学式填在下列横线上。
(1)汽车铅蓄电池中含有的酸__________(2)食醋中含有的酸___________
(3)人体胃液含有的酸__________(4)一种易分解的酸________
18、化学是一门以实验为基础的科学,化学所取得的丰硕成果与实验的重要作用分不开。结合下列实验仪器回答问题:
(1)写出指定仪器的名称:A_________________;E________________。
(2)上述仪器中稀释浓硫酸还缺少的玻璃仪器是_______________;稀释浓硫酸的正确操作是_______________________________________ ; 若不慎将浓硫酸沾到皮肤上,应立即____________________,然后涂上3%~5%的碳酸氢钠溶液。请写出碳酸氢钠溶液与硫酸反应的化学方程式:_______________________________________。
19、如图所示,在白色点滴板①~⑥的孔穴中,分别滴加2滴紫色石蕊试液。
(1)孔穴⑥中溶液变为蓝色,说明碳酸钾溶液显_____(填“酸性”或“碱性”)。
(2)溶液变为红色的孔穴有_____(填孔穴序号,下同)。
(3)作为空白对照实验的孔穴是_____。
20、中和反应的应用
应 用 领 域 ①医药卫生 胃酸过多,应服用 药物
②改良土壤 向酸性土壤里撒 中和
③处理工业废水 当污水含酸量超标时,可以利用 进行中和处理
④调节溶液的酸碱性 溶液的酸碱性太强或太弱,都可以用适当的碱或酸调节溶液的pH
21、某工业品盐酸中含有H + 、Fe 3+ 、Cl,该盐酸中所含杂质的化学式是________。若溶液中H + 与Cl 的个数比为91:94,则Fe 3+ 与Cl 的个数比是____________。
22、已知:在水溶液中,乙醇(C2H5OH)不发生电离;溴化氢(HBr)电离产生氢离子(H+)和溴离子(Br-);氢氧化钠电离产生钠离子和氢氧根离子。请回答下列问题:
(1)根据这三种溶液的组成推断,溴化氢的水溶液显 性。
(2)写出上述物质之间发生中和反应的化学方程式: 。
第七单元 常见的酸和碱 复习题附答案2023—2024学年鲁教版化学九年级下册
一、选择题。
1、稀盐酸、稀硫酸具有相似的化学性质,是因为组成中含有 ( )
A.酸根 B.H C.O D.原子团
【答案】B
2、下列分别是二氧化碳的制取、干燥、验满和性质检验的装置图,其中正确的是( )
A. B.
C. D.
【答案】D
3、实验测得某些溶液的pH如图,其中呈碱性的是( )
A.稀硝酸 B.硫酸铜溶液
C.氯化钠溶液 D.碳酸钠溶液
【答案】D
4、某同学测得某化工厂排放的废水的为4,为了将该废水的调到7,该小组提出的治理方案是向废水中加入适量的下列物质,该物质是( )
A.稀盐酸 B.生石灰 C.废铜屑 D.水
【答案】B
5、下列不属于氢氧化钾的化学性质的是( )
A.能和碳酸钠溶液反应 B.可使酚酞溶液变红色
C.能和CO 2 反应 D.能和硫酸反应
【答案】A
6、对实验现象、过程的描述都正确的是( )
A.硫在空气中点燃发出黄光、放出热量
B.铁粉在空气中加热剧烈燃烧、生成黑色固体
C.浓硫酸敞口放置溶液的颜色、质量不变
D.烧碱固体放入水中迅速溶解、溶液温度升高
【答案】D
7、下列实验现象描述正确的是( )
A.用木棍蘸取稀硫酸后,木棍变黑
B.打开盛有浓盐酸的试剂瓶,瓶口出现白雾
C.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D.将高锰酸钾放入汽油中,很快溶解形成紫红色溶液
【答案】B
8、下列关于盐酸和硫酸的描述正确的是( )
A.稀盐酸和稀硫酸都能用于除铁锈
B.打开浓盐酸和浓硫酸的试剂瓶塞,瓶口都有白雾
C.向稀盐酸和稀硫酸中滴加BaCl2溶液,都有白色沉淀生成
D.稀释浓硫酸时,应将水沿烧杯壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌
【答案】A
9、使酚酞试液变红的溶液能使紫色石蕊试液呈( )
A.无色 B.蓝色 C.红色 D.紫色
【答案】B
10、室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是( )
A.该图像表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
【答案】C
11、下列有关酸、碱性质和用途的说法不正确的是( )
A.氢氧化钠在生活中可用来去除油污,可做炉具清洁剂
B.氢氧化钠、氢氧化钙化学性质相似,是因为其溶液中都含有金属离子
C.盐酸、硫酸化学性质相似,是因为其溶液中都含有相同的H+
D.用食醋可除去热水瓶胆壁上的水垢
【答案】B
12、下图所示实验操作正确的是( )
A.点燃酒精灯 B.稀释浓硫酸
C.闻气体气味 D.连接玻璃管和橡皮管
【答案】D
13、将10g质量分数为98%的浓硫酸配制成10%的稀硫酸。有关步骤的说法正确的是( )
A.计算需水98g B.量取水时,仰视读数
C.将水注入浓硫酸中,并不断搅拌 D.配制好后,装瓶贴标签
【答案】D
14、下列物质分类正确的是( )
A.混合物:洁净的空气 、黄铜、澄清石灰水
B.酸:盐酸、醋酸、硝酸钠
C.碱:烧碱、纯碱 、熟石灰
D.氧化物:水、氧化铁、碳酸
【答案】A
15、下列水果中酸性最强的是( )
A.苹果pH≈2.9 B.凤梨pH≈4.0
C.香蕉pH≈6.6 D.荔枝pH≈5.0
【答案】A
16、如图两幅微观示意图揭示了化学变化的微观实质。相关说法中错误的是( )
A. 图乙说明中和反应的实质是H+和OH﹣反应生成了H2O
B. 图甲表示的是化合反应
C. 图甲表示的反应中元素的化合价没有改变
D. 上述两图说明化学反应前后原子的种类、数目都不会发生变化
【答案】C
二、填空题。
17、按要求从醋酸,稀硫酸,碳酸,稀盐酸中选择合适的物质,将其化学式填在下列横线上。
(1)汽车铅蓄电池中含有的酸__________(2)食醋中含有的酸___________
(3)人体胃液含有的酸__________(4)一种易分解的酸________
【答案】H2SO4 CH3COOH HCl H2CO3
18、化学是一门以实验为基础的科学,化学所取得的丰硕成果与实验的重要作用分不开。结合下列实验仪器回答问题:
(1)写出指定仪器的名称:A_________________;E________________。
(2)上述仪器中稀释浓硫酸还缺少的玻璃仪器是_______________;稀释浓硫酸的正确操作是_______________________________________ ; 若不慎将浓硫酸沾到皮肤上,应立即____________________,然后涂上3%~5%的碳酸氢钠溶液。请写出碳酸氢钠溶液与硫酸反应的化学方程式:_______________________________________。
【答案】(1)量筒 酒精灯
(2)玻璃棒 将浓硫酸沿着烧杯壁慢慢注入水中,并不断用玻璃棒搅拌
用大量水洗
19、如图所示,在白色点滴板①~⑥的孔穴中,分别滴加2滴紫色石蕊试液。
(1)孔穴⑥中溶液变为蓝色,说明碳酸钾溶液显_____(填“酸性”或“碱性”)。
(2)溶液变为红色的孔穴有_____(填孔穴序号,下同)。
(3)作为空白对照实验的孔穴是_____。
【答案】(1)碱性; (2)②⑤; (3)③
20、中和反应的应用
应 用 领 域 ①医药卫生 胃酸过多,应服用 药物
②改良土壤 向酸性土壤里撒 中和
③处理工业废水 当污水含酸量超标时,可以利用 进行中和处理
④调节溶液的酸碱性 溶液的酸碱性太强或太弱,都可以用适当的碱或酸调节溶液的pH
【答案】碱性; 熟石灰; 熟石灰
21、某工业品盐酸中含有H + 、Fe 3+ 、Cl,该盐酸中所含杂质的化学式是________。若溶液中H + 与Cl 的个数比为91:94,则Fe 3+ 与Cl 的个数比是____________。
【答案】FeCl3 1:94
22、已知:在水溶液中,乙醇(C2H5OH)不发生电离;溴化氢(HBr)电离产生氢离子(H+)和溴离子(Br-);氢氧化钠电离产生钠离子和氢氧根离子。请回答下列问题:
(1)根据这三种溶液的组成推断,溴化氢的水溶液显 性。
(2)写出上述物质之间发生中和反应的化学方程式: 。
【答案】酸
一、选择题。
1、稀盐酸、稀硫酸具有相似的化学性质,是因为组成中含有 ( )
A.酸根 B.H C.O D.原子团
2、下列分别是二氧化碳的制取、干燥、验满和性质检验的装置图,其中正确的是( )
A. B.
C. D.
3、实验测得某些溶液的pH如图,其中呈碱性的是( )
A.稀硝酸 B.硫酸铜溶液
C.氯化钠溶液 D.碳酸钠溶液
4、某同学测得某化工厂排放的废水的为4,为了将该废水的调到7,该小组提出的治理方案是向废水中加入适量的下列物质,该物质是( )
A.稀盐酸 B.生石灰 C.废铜屑 D.水
5、下列不属于氢氧化钾的化学性质的是( )
A.能和碳酸钠溶液反应 B.可使酚酞溶液变红色
C.能和CO 2 反应 D.能和硫酸反应
6、对实验现象、过程的描述都正确的是( )
A.硫在空气中点燃发出黄光、放出热量
B.铁粉在空气中加热剧烈燃烧、生成黑色固体
C.浓硫酸敞口放置溶液的颜色、质量不变
D.烧碱固体放入水中迅速溶解、溶液温度升高
7、下列实验现象描述正确的是( )
A.用木棍蘸取稀硫酸后,木棍变黑
B.打开盛有浓盐酸的试剂瓶,瓶口出现白雾
C.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D.将高锰酸钾放入汽油中,很快溶解形成紫红色溶液
8、下列关于盐酸和硫酸的描述正确的是( )
A.稀盐酸和稀硫酸都能用于除铁锈
B.打开浓盐酸和浓硫酸的试剂瓶塞,瓶口都有白雾
C.向稀盐酸和稀硫酸中滴加BaCl2溶液,都有白色沉淀生成
D.稀释浓硫酸时,应将水沿烧杯壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌
9、使酚酞试液变红的溶液能使紫色石蕊试液呈( )
A.无色 B.蓝色 C.红色 D.紫色
10、室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是( )
A.该图像表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
11、下列有关酸、碱性质和用途的说法不正确的是( )
A.氢氧化钠在生活中可用来去除油污,可做炉具清洁剂
B.氢氧化钠、氢氧化钙化学性质相似,是因为其溶液中都含有金属离子
C.盐酸、硫酸化学性质相似,是因为其溶液中都含有相同的H+
D.用食醋可除去热水瓶胆壁上的水垢
12、下图所示实验操作正确的是( )
A.点燃酒精灯 B.稀释浓硫酸
C.闻气体气味 D.连接玻璃管和橡皮管
13、将10g质量分数为98%的浓硫酸配制成10%的稀硫酸。有关步骤的说法正确的是( )
A.计算需水98g B.量取水时,仰视读数
C.将水注入浓硫酸中,并不断搅拌 D.配制好后,装瓶贴标签
14、下列物质分类正确的是( )
A.混合物:洁净的空气 、黄铜、澄清石灰水
B.酸:盐酸、醋酸、硝酸钠
C.碱:烧碱、纯碱 、熟石灰
D.氧化物:水、氧化铁、碳酸
15、下列水果中酸性最强的是( )
A.苹果pH≈2.9 B.凤梨pH≈4.0
C.香蕉pH≈6.6 D.荔枝pH≈5.0
16、如图两幅微观示意图揭示了化学变化的微观实质。相关说法中错误的是( )
A. 图乙说明中和反应的实质是H+和OH﹣反应生成了H2O
B. 图甲表示的是化合反应
C. 图甲表示的反应中元素的化合价没有改变
D. 上述两图说明化学反应前后原子的种类、数目都不会发生变化
二、填空题。
17、按要求从醋酸,稀硫酸,碳酸,稀盐酸中选择合适的物质,将其化学式填在下列横线上。
(1)汽车铅蓄电池中含有的酸__________(2)食醋中含有的酸___________
(3)人体胃液含有的酸__________(4)一种易分解的酸________
18、化学是一门以实验为基础的科学,化学所取得的丰硕成果与实验的重要作用分不开。结合下列实验仪器回答问题:
(1)写出指定仪器的名称:A_________________;E________________。
(2)上述仪器中稀释浓硫酸还缺少的玻璃仪器是_______________;稀释浓硫酸的正确操作是_______________________________________ ; 若不慎将浓硫酸沾到皮肤上,应立即____________________,然后涂上3%~5%的碳酸氢钠溶液。请写出碳酸氢钠溶液与硫酸反应的化学方程式:_______________________________________。
19、如图所示,在白色点滴板①~⑥的孔穴中,分别滴加2滴紫色石蕊试液。
(1)孔穴⑥中溶液变为蓝色,说明碳酸钾溶液显_____(填“酸性”或“碱性”)。
(2)溶液变为红色的孔穴有_____(填孔穴序号,下同)。
(3)作为空白对照实验的孔穴是_____。
20、中和反应的应用
应 用 领 域 ①医药卫生 胃酸过多,应服用 药物
②改良土壤 向酸性土壤里撒 中和
③处理工业废水 当污水含酸量超标时,可以利用 进行中和处理
④调节溶液的酸碱性 溶液的酸碱性太强或太弱,都可以用适当的碱或酸调节溶液的pH
21、某工业品盐酸中含有H + 、Fe 3+ 、Cl,该盐酸中所含杂质的化学式是________。若溶液中H + 与Cl 的个数比为91:94,则Fe 3+ 与Cl 的个数比是____________。
22、已知:在水溶液中,乙醇(C2H5OH)不发生电离;溴化氢(HBr)电离产生氢离子(H+)和溴离子(Br-);氢氧化钠电离产生钠离子和氢氧根离子。请回答下列问题:
(1)根据这三种溶液的组成推断,溴化氢的水溶液显 性。
(2)写出上述物质之间发生中和反应的化学方程式: 。
第七单元 常见的酸和碱 复习题附答案2023—2024学年鲁教版化学九年级下册
一、选择题。
1、稀盐酸、稀硫酸具有相似的化学性质,是因为组成中含有 ( )
A.酸根 B.H C.O D.原子团
【答案】B
2、下列分别是二氧化碳的制取、干燥、验满和性质检验的装置图,其中正确的是( )
A. B.
C. D.
【答案】D
3、实验测得某些溶液的pH如图,其中呈碱性的是( )
A.稀硝酸 B.硫酸铜溶液
C.氯化钠溶液 D.碳酸钠溶液
【答案】D
4、某同学测得某化工厂排放的废水的为4,为了将该废水的调到7,该小组提出的治理方案是向废水中加入适量的下列物质,该物质是( )
A.稀盐酸 B.生石灰 C.废铜屑 D.水
【答案】B
5、下列不属于氢氧化钾的化学性质的是( )
A.能和碳酸钠溶液反应 B.可使酚酞溶液变红色
C.能和CO 2 反应 D.能和硫酸反应
【答案】A
6、对实验现象、过程的描述都正确的是( )
A.硫在空气中点燃发出黄光、放出热量
B.铁粉在空气中加热剧烈燃烧、生成黑色固体
C.浓硫酸敞口放置溶液的颜色、质量不变
D.烧碱固体放入水中迅速溶解、溶液温度升高
【答案】D
7、下列实验现象描述正确的是( )
A.用木棍蘸取稀硫酸后,木棍变黑
B.打开盛有浓盐酸的试剂瓶,瓶口出现白雾
C.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D.将高锰酸钾放入汽油中,很快溶解形成紫红色溶液
【答案】B
8、下列关于盐酸和硫酸的描述正确的是( )
A.稀盐酸和稀硫酸都能用于除铁锈
B.打开浓盐酸和浓硫酸的试剂瓶塞,瓶口都有白雾
C.向稀盐酸和稀硫酸中滴加BaCl2溶液,都有白色沉淀生成
D.稀释浓硫酸时,应将水沿烧杯壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌
【答案】A
9、使酚酞试液变红的溶液能使紫色石蕊试液呈( )
A.无色 B.蓝色 C.红色 D.紫色
【答案】B
10、室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是( )
A.该图像表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
【答案】C
11、下列有关酸、碱性质和用途的说法不正确的是( )
A.氢氧化钠在生活中可用来去除油污,可做炉具清洁剂
B.氢氧化钠、氢氧化钙化学性质相似,是因为其溶液中都含有金属离子
C.盐酸、硫酸化学性质相似,是因为其溶液中都含有相同的H+
D.用食醋可除去热水瓶胆壁上的水垢
【答案】B
12、下图所示实验操作正确的是( )
A.点燃酒精灯 B.稀释浓硫酸
C.闻气体气味 D.连接玻璃管和橡皮管
【答案】D
13、将10g质量分数为98%的浓硫酸配制成10%的稀硫酸。有关步骤的说法正确的是( )
A.计算需水98g B.量取水时,仰视读数
C.将水注入浓硫酸中,并不断搅拌 D.配制好后,装瓶贴标签
【答案】D
14、下列物质分类正确的是( )
A.混合物:洁净的空气 、黄铜、澄清石灰水
B.酸:盐酸、醋酸、硝酸钠
C.碱:烧碱、纯碱 、熟石灰
D.氧化物:水、氧化铁、碳酸
【答案】A
15、下列水果中酸性最强的是( )
A.苹果pH≈2.9 B.凤梨pH≈4.0
C.香蕉pH≈6.6 D.荔枝pH≈5.0
【答案】A
16、如图两幅微观示意图揭示了化学变化的微观实质。相关说法中错误的是( )
A. 图乙说明中和反应的实质是H+和OH﹣反应生成了H2O
B. 图甲表示的是化合反应
C. 图甲表示的反应中元素的化合价没有改变
D. 上述两图说明化学反应前后原子的种类、数目都不会发生变化
【答案】C
二、填空题。
17、按要求从醋酸,稀硫酸,碳酸,稀盐酸中选择合适的物质,将其化学式填在下列横线上。
(1)汽车铅蓄电池中含有的酸__________(2)食醋中含有的酸___________
(3)人体胃液含有的酸__________(4)一种易分解的酸________
【答案】H2SO4 CH3COOH HCl H2CO3
18、化学是一门以实验为基础的科学,化学所取得的丰硕成果与实验的重要作用分不开。结合下列实验仪器回答问题:
(1)写出指定仪器的名称:A_________________;E________________。
(2)上述仪器中稀释浓硫酸还缺少的玻璃仪器是_______________;稀释浓硫酸的正确操作是_______________________________________ ; 若不慎将浓硫酸沾到皮肤上,应立即____________________,然后涂上3%~5%的碳酸氢钠溶液。请写出碳酸氢钠溶液与硫酸反应的化学方程式:_______________________________________。
【答案】(1)量筒 酒精灯
(2)玻璃棒 将浓硫酸沿着烧杯壁慢慢注入水中,并不断用玻璃棒搅拌
用大量水洗
19、如图所示,在白色点滴板①~⑥的孔穴中,分别滴加2滴紫色石蕊试液。
(1)孔穴⑥中溶液变为蓝色,说明碳酸钾溶液显_____(填“酸性”或“碱性”)。
(2)溶液变为红色的孔穴有_____(填孔穴序号,下同)。
(3)作为空白对照实验的孔穴是_____。
【答案】(1)碱性; (2)②⑤; (3)③
20、中和反应的应用
应 用 领 域 ①医药卫生 胃酸过多,应服用 药物
②改良土壤 向酸性土壤里撒 中和
③处理工业废水 当污水含酸量超标时,可以利用 进行中和处理
④调节溶液的酸碱性 溶液的酸碱性太强或太弱,都可以用适当的碱或酸调节溶液的pH
【答案】碱性; 熟石灰; 熟石灰
21、某工业品盐酸中含有H + 、Fe 3+ 、Cl,该盐酸中所含杂质的化学式是________。若溶液中H + 与Cl 的个数比为91:94,则Fe 3+ 与Cl 的个数比是____________。
【答案】FeCl3 1:94
22、已知:在水溶液中,乙醇(C2H5OH)不发生电离;溴化氢(HBr)电离产生氢离子(H+)和溴离子(Br-);氢氧化钠电离产生钠离子和氢氧根离子。请回答下列问题:
(1)根据这三种溶液的组成推断,溴化氢的水溶液显 性。
(2)写出上述物质之间发生中和反应的化学方程式: 。
【答案】酸
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
