2.3 芳香烃 课件 (共52张PPT)2023-2024学年高二下学期化学人教版(2019)选择性必修3
文档属性
| 名称 | 2.3 芳香烃 课件 (共52张PPT)2023-2024学年高二下学期化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 51.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-08 09:38:21 | ||
图片预览









文档简介
(共52张PPT)
第二章 烃
第三节 芳香烃
柑橘类水果表面凹凸不平,密密麻麻分布着许多小孔,这些小孔可产生芳香烃,可溶解橡胶。
芳香烃:在烃类化合物中,含有一个或多个 的化合物。最简单的芳香烃为 。
苯环
苯
一、苯
颜色:
无色
气味:
特殊气味
状态:
液体
熔点:
5.5℃
沸点:
80.1℃
密度:
比水小
毒性:
有毒
溶解性:
其他:
(一)苯的物理性质
不溶于水
易挥发、标况下为固体、是一种常见的有机溶剂
(二)苯的分子结构
【实验2-1】向两支各盛有2 mL苯的试管中分别加入酸性高锰酸钾溶液和溴水,用力振荡,观察现象。 教材P43
【实验2-1】向两支各盛有2 mL苯的试管中分别加入酸性高锰酸钾溶液和溴水,用力振荡,观察现象。
试剂 实验现象 实验结论
酸性高锰酸钾溶液
溴水
★溴在苯中的溶解度比在水中的大,因此苯能将溴从水中萃取出来。
苯不能被酸性高锰酸钾溶液氧化,也不与溴水反应,
苯分子具有不同于烯烃和炔烃的特殊结构
(二)苯的分子结构
(1)苯分子为平面正六边形结构,其中的6个碳原子均采取sp2杂化,分别与氢原子及相邻碳原子以σ键结合,键间夹角均为120o,连接成六元环状。
(2)每个碳碳键的键长相等,都是139pm,介于碳碳单键和碳碳双键的键长之间。
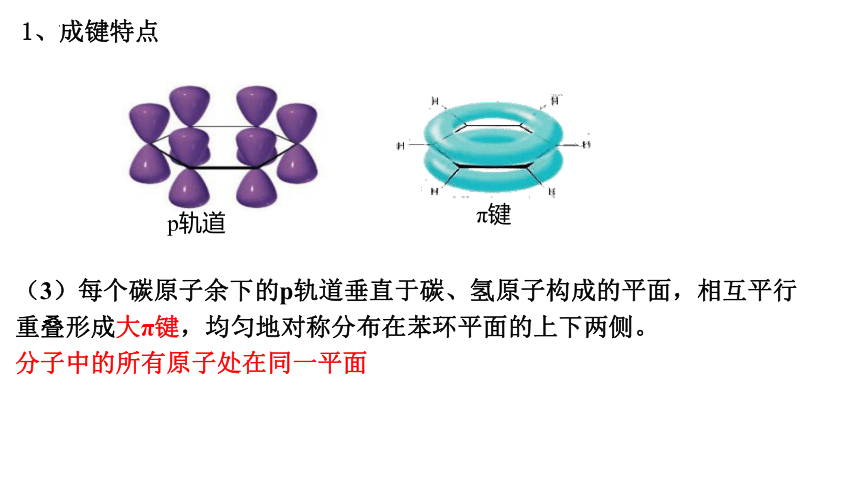
1、成键特点
(3)每个碳原子余下的p轨道垂直于碳、氢原子构成的平面,相互平行重叠形成大π键,均匀地对称分布在苯环平面的上下两侧。
分子中的所有原子处在同一平面
p轨道
π键
1、成键特点
2、表示方式
①分子式:
②结构简式:
③空间结构:
C6H6
或
②结构式:
②最简式:
CH
(三)苯的化学性质
在通常情况下不易发生烯烃和炔烃所容易发生的加成反应,在一定条件下可发生氧化、加成和取代反应。
1、氧化反应:能燃烧、不能使酸性KMnO4溶液褪色
火焰明亮,伴有浓重的黑烟 (与乙炔相同)
2C6H6 + 15O2 12CO2 + 6H2O
点燃
2、取代反应
+ Br2
FeBr3
+ HBr
Br
纯净的溴苯是一种无色液态,有特殊的气味,不溶于水,密度比水大,常因溶有溴单质而呈褐色。
(1)卤代反应:苯与液溴
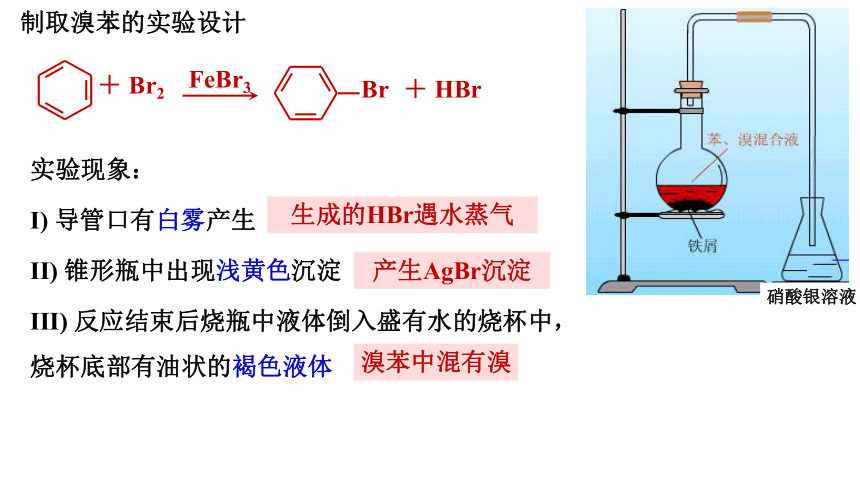
★制取溴苯的实验设计
+ Br2
FeBr3
+ HBr
Br
已知:①苯、液溴在铁屑作用下剧烈反应生成溴苯,且放出热量;
②液溴、苯等有挥发性。
反应中加入的是铁粉,实际起催化作用的是FeBr3
长导管:
冷凝回流、导气
尾气处理
导管末端不能伸入到液面中防止倒吸
制取溴苯的实验设计
+ Br2
FeBr3
+ HBr
Br
实验现象:
I) 导管口有白雾产生
II) 锥形瓶中出现浅黄色沉淀
III) 反应结束后烧瓶中液体倒入盛有水的烧杯中,烧杯底部有油状的褐色液体
生成的HBr遇水蒸气
产生AgBr沉淀
溴苯中混有溴
硝酸银溶液
【思考】何获得纯净的溴苯?
产物中可能含
有溴苯、苯、
HBr和Br2
试剂:
操作:
目的:
水
分液
除HBr
HBr水溶液
溴苯
苯、溴
试剂:
操作:
目的:
NaOH
分液
除Br2
NaBr溶液
NaBrO溶液
溴苯
苯
操作:
目的:
溴苯
苯
蒸馏
除苯
水洗分液、碱洗分液、蒸馏
除去溶解在溴苯中的液溴,以提纯溴苯
吸收检验HBr
吸收HBr,防止污染环境
防止倒吸
冷凝回流、导气
【练习】2.溴苯是不溶于水的液体,常温下不与酸、碱反应,可用如图装置制取(该反应放出热量)。制取时观察到烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现等现象。下列说法正确的是
A.向反应后的锥形瓶中的“蒸馏水”加入AgNO3溶液,若出
现浅黄色沉淀, 即可证明苯与溴一定发生了取代反应
B.白雾出现是因为HBr易挥发且极易溶于水
C.装置图中长直玻璃导管的作用只是导气
D.溴苯中溶有少量的溴,可用CCl4萃取后分液除去
B
D
校本P41
4.实验室制备溴苯的反应装置如图,下列关于实验操作或叙述错误的( )
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中,装置b中液体呈浅红色
C.装置c中碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
2、取代反应:
①纯净的硝基苯是一种无色液态,有苦杏仁气味,不溶于水,密度比水的大,常因溶有NO2而呈微黄色。
(2)硝化反应:在浓硫酸、50~60oC,可与浓硝酸发生
硝基苯
②浓硫酸的作用:催化剂和脱水剂。
“浴热”容易控制恒温,且易使被加热物质受热均匀
长导管:
冷凝回流、导气
混合混酸时,一定要将浓硫酸沿器壁缓缓注入浓硝酸中,并不断振荡使之混合均匀。
【思考】如何获得纯净的硝基苯?
产物中可能含有
硝基苯、苯、硫酸、硝酸、NO2
试剂:
操作:
目的:
水
分液
除酸
酸液
硝基苯
苯
残余酸
试剂:
操作:
目的:
NaOH
分液
除酸
盐溶液
硝基苯
苯
操作:
目的:
溴苯
苯
蒸馏
除苯
水洗分液、碱洗分液、蒸馏
校本P38
3.实验室制取硝基苯的反应装置如图所示,下列关于实验操作的叙述错误的是( )
A.试剂加入顺序:先加浓硝酸,再加浓硫酸,最后加入苯
B.实验时,水浴温度需控制在50~60 ℃
C.长玻璃导管兼起冷凝回流苯和硝酸的作用,以提高反应物的转化率
D.反应后的混合液经水洗、碱溶液洗涤、结晶,得到硝基苯
D
A
校本P40
2.下列说法正确的是( )
A.硝基苯可由苯与浓硝酸、浓硫酸的混合物在一定条件下发生取代反应来制取
B.硝基苯中碳原子均采取sp杂化
C.硝基苯有毒,密度比水的小,可从水面上“捞出”
D.苯与硝基苯都属于芳香烃
(3)磺化反应:
苯磺酸
苯磺酸易溶于水,是一种强酸,可以看作是硫酸分子里的一个羟基被苯环取代的产物。
磺化反应被广泛应用于制备合成洗涤剂。
苯与浓硫酸在70~80℃发生取代反应
2、取代反应:
+ HO SO3H
+ H2O
SO3H
Δ
3、加成反应
苯的大π键比较稳定,通常状态下不易发生加成反应,在以Pt、Ni等为催化剂并加热的条件下,苯能与氢气发生加成反应。
+ 3H2
Ni
环己烷
D
校本P38
1.(2023·塔城高二质检)下列关于苯的性质的叙述不正确的是( )
A.苯是无色带有特殊气味的液体
B.常温下苯是一种不溶于水且密度小于水的液体
C.苯在一定条件下能与溴发生取代反应
D.苯不含真正的双键,故不能发生加成反应
A
校本P38
2.(2023·黄冈高二月考)下列说法正确的是( )
A.苯分子中有碳氢单键,故能发生取代反应
B.可用苯萃取溴水中的Br2,分液时有机层从分液漏斗下端放出
C.苯分子能使酸性KMnO4溶液褪色
D.苯不能因反应使溴水褪色,说明苯分子中存在碳碳单键,不存在碳碳双键
【思考】苯的分子结构实际上不具有单键和双键的简单交替结构,可以作为证据的事实有哪些?
苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键,事实:
①苯分子中6个碳原子之间的键完全相同(键长相等),且一氯代物只有一种。
②苯不能使酸性KMnO4溶液褪色。
③苯在FeBr3存在的条件下与液溴发生取代反应。
④ 和 是同一种物质。
【练习】苯可发生如图所示反应,下列叙述错误的是
A.反应①为取代反应,向反应后的液体中加入水,有机产物在上层
B.反应②为氧化反应,反应现象是火焰明亮并伴有浓烟
C.反应③为取代反应,有机产物是一种芳香族化合物
D.反应④中1 mol苯最多与3 mol H2在加热、催化剂作用下发生加成反应
A
二、苯的同系物
1、 概念:
苯环上的氢原子被烷基取代所得到的一系列产物
2、苯的同系物结构特点:
分子中只有一个苯环
与苯环相连接的全部是烷基
CH3
CH2CH3
CH=CH2
CH3—CH—CH—CH3
OH
(一)组成和结构
A
3、通式:CnH2n-6 (n≥7)
甲苯 乙苯 邻二甲苯 间二甲苯 对二甲苯
4、习惯命名:
苯的同系物的命名是以苯作为母体的,其他基团作为取代基
5、系统命名:
将苯环上的6个碳原子编号,以某个甲基所在的碳原子的位置为1号,
选取最小位次号给另一个甲基编号。
1,2-二甲苯
1,3-二甲苯
1,4-二甲苯
【练习】对下列物质命名
6、 苯的同系物的同分异构体
试写成分子式为C9H12属于苯的同系物的同分异构体?
表2 2 常见的苯的同系物及其部分物理性质
苯的同系物
CH3
C2H5
CH3
CH3
CH3
CH3
CH3
CH3
名称
熔点/℃
沸点/℃
密度/(g·cm 3)
甲苯
乙苯
邻二甲苯
(1,2-二甲苯)
间二甲苯
(1,3-二甲苯)
对二甲苯
(1,4-二甲苯)
95
95
25
48
13
111
136
144
139
138
0.867
0.867
0.880
0.864
0.861
(二)物理性质
(1)一般具有类似苯的气味的无色液体,不溶于水,易溶于有机溶剂,密度比水的小。
(2)随碳原子数增多,熔、沸点依次升高。
【实验2-2】教材P46
(三)化学性质
实验内容 实验现象 解释
(1)向两只分别盛有2 mL苯和甲苯的试管中各加入几滴溴水,静置
(2)将上述试管用力振荡,静置
(3)向两只分别盛有2 mL苯和甲苯的试管中各加入酸性高锰酸钾溶液,静置
(4)将上述试管用力振荡,静置
苯和甲苯的性质比较
【实验2-2】教材P46
实验内容 实验现象 解释
(1)向两只分别盛有2 mL苯和甲苯的试管中各加入几滴溴水,静置
(2)将上述试管用力振荡,静置
(3)向两只盛有2 mL苯和甲苯的试管中各加入酸性高锰酸钾溶液,静置
(4)将上述试管用力振荡,静置
两支试管中的液体均分层,上层为无色的有机层,下层均是溴水
苯和甲苯都不溶于水,密度都比水小
两支试管中的液体均分层,上层为橙色,下层无色
溴在苯和甲苯中的溶解度比在水中的大
两支试管中均分层,上层为无色的有机层,下层均是紫色酸性高锰酸钾溶液
苯和甲苯都不溶于水,密度都比水小
盛有甲苯的试管中溶液褪色,盛有苯的试管中无明显变化
甲苯可以酸性高锰酸钾溶液反应,而苯不与其反应
(三)化学性质
现象:火焰明亮并带有浓烟。
1、氧化反应
(1)燃烧
(2)甲苯能使酸性KMnO4溶液褪色,这是由于甲苯上的甲基被酸性KMnO4氧化的结果(侧链氧化)。
★苯环对烃基的影响:
受苯环的影响,苯的同系物中作为侧链的烃基的活动性有所增强
CH2
CH
CH3
CH3
CH2
CH2
CH3
这些能使酸性高锰酸钾溶液褪色
CH3
C
CH3
CH3
CH3
C
CH2CH3
CH3
这些不能使酸性高锰酸钾溶液褪色
★侧链烃基中与苯环直接相连的碳原子上有氢原子,该烃基就能被酸性高锰酸钾溶液氧化,且与烷基的多少和大小无关。
★烃基对苯环的影响:
受烃基的影响,苯环的活动性有所增强,较易发生多元取代反应,同时 CH3会使苯环上位于甲基邻、对位上的H原子易于取代。
2、取代反应
(1)硝化反应(以甲苯为例)
甲苯与浓硝酸和浓硫酸的混合物在加热条件下可以发生取代反应,生成一硝基取代物、二硝基取代物和三硝基取代物,硝基取代的位置均以甲基的邻、对位为主。
+3HNO3
浓硫酸
Δ
+ 3H2O
CH3
CH3
NO2
NO2
O2N
2,4,6-三硝基甲苯又叫TNT,是一种淡黄色晶体,不溶于水,它是一种烈性炸药,广泛用于国防、开矿、建筑等。
甲苯与浓硝酸和浓硫酸的混合物在加热条件下反应生成2,4,6-三硝基甲苯
教材P48
(2)卤代反应(以甲苯为例)
a:光照条件下,苯的同系物的取代反应发生在烷基侧链上;
b:溴化铁作催化剂,苯的同系物的取代反应发生在苯环上烷基的邻、对位上。
苯环和侧链都能发生取代反应,但条件不同。
3、加成反应(以甲苯为例)
在一定条件下甲苯与H2发生加成反应,生成甲基环己烷。
B
校本P40
2.(2023·漳州高二质检)可用于鉴别苯和甲苯的试剂或方法是( )
A.液溴和铁粉
B.酸性KMnO4溶液
C.溴水
D.在空气中燃烧
校本P40
3.下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是( )
A.甲苯通过硝化反应生成2,4,6-三硝基甲苯
B.甲苯能使酸性高锰酸钾溶液褪色
C.甲苯燃烧时产生很浓的黑烟
D.1 mol甲苯与3 mol氢气发生加成反应
A
C
芳香烃
苯
苯的同系物
平面正六边形,不含碳碳双键
分子中含一个苯环、侧链为烷基
易取代,难加成,可燃烧,不能使酸性高锰酸钾溶液褪色
易取代,难加成,可燃烧,大部分能使酸性高锰酸钾溶液褪色
性质差异原因:原子团相互影响
结构特点
化学性质
【小结】
三、稠环芳香烃 教材P48【资料卡片】
1、定义
由两个或两个以上的苯环共用相邻的两个碳原子的芳香烃是稠环芳香烃。
2、常见稠环芳香烃
萘
蒽
菲
C10H8
C14H10
C14H10
无色片状晶体,有特殊气味,熔点80℃,易升华,不溶于水。重要化工原料,可用于下生产增塑剂、农药、染料等
无色晶体,易升华,不溶于水。
合成染料的重要原料
【思考】萘的一氯代物有 种,萘的二氯代物有 种
“定一移一”
Cl
Cl
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
第二章 烃
第三节 芳香烃
柑橘类水果表面凹凸不平,密密麻麻分布着许多小孔,这些小孔可产生芳香烃,可溶解橡胶。
芳香烃:在烃类化合物中,含有一个或多个 的化合物。最简单的芳香烃为 。
苯环
苯
一、苯
颜色:
无色
气味:
特殊气味
状态:
液体
熔点:
5.5℃
沸点:
80.1℃
密度:
比水小
毒性:
有毒
溶解性:
其他:
(一)苯的物理性质
不溶于水
易挥发、标况下为固体、是一种常见的有机溶剂
(二)苯的分子结构
【实验2-1】向两支各盛有2 mL苯的试管中分别加入酸性高锰酸钾溶液和溴水,用力振荡,观察现象。 教材P43
【实验2-1】向两支各盛有2 mL苯的试管中分别加入酸性高锰酸钾溶液和溴水,用力振荡,观察现象。
试剂 实验现象 实验结论
酸性高锰酸钾溶液
溴水
★溴在苯中的溶解度比在水中的大,因此苯能将溴从水中萃取出来。
苯不能被酸性高锰酸钾溶液氧化,也不与溴水反应,
苯分子具有不同于烯烃和炔烃的特殊结构
(二)苯的分子结构
(1)苯分子为平面正六边形结构,其中的6个碳原子均采取sp2杂化,分别与氢原子及相邻碳原子以σ键结合,键间夹角均为120o,连接成六元环状。
(2)每个碳碳键的键长相等,都是139pm,介于碳碳单键和碳碳双键的键长之间。
1、成键特点
(3)每个碳原子余下的p轨道垂直于碳、氢原子构成的平面,相互平行重叠形成大π键,均匀地对称分布在苯环平面的上下两侧。
分子中的所有原子处在同一平面
p轨道
π键
1、成键特点
2、表示方式
①分子式:
②结构简式:
③空间结构:
C6H6
或
②结构式:
②最简式:
CH
(三)苯的化学性质
在通常情况下不易发生烯烃和炔烃所容易发生的加成反应,在一定条件下可发生氧化、加成和取代反应。
1、氧化反应:能燃烧、不能使酸性KMnO4溶液褪色
火焰明亮,伴有浓重的黑烟 (与乙炔相同)
2C6H6 + 15O2 12CO2 + 6H2O
点燃
2、取代反应
+ Br2
FeBr3
+ HBr
Br
纯净的溴苯是一种无色液态,有特殊的气味,不溶于水,密度比水大,常因溶有溴单质而呈褐色。
(1)卤代反应:苯与液溴
★制取溴苯的实验设计
+ Br2
FeBr3
+ HBr
Br
已知:①苯、液溴在铁屑作用下剧烈反应生成溴苯,且放出热量;
②液溴、苯等有挥发性。
反应中加入的是铁粉,实际起催化作用的是FeBr3
长导管:
冷凝回流、导气
尾气处理
导管末端不能伸入到液面中防止倒吸
制取溴苯的实验设计
+ Br2
FeBr3
+ HBr
Br
实验现象:
I) 导管口有白雾产生
II) 锥形瓶中出现浅黄色沉淀
III) 反应结束后烧瓶中液体倒入盛有水的烧杯中,烧杯底部有油状的褐色液体
生成的HBr遇水蒸气
产生AgBr沉淀
溴苯中混有溴
硝酸银溶液
【思考】何获得纯净的溴苯?
产物中可能含
有溴苯、苯、
HBr和Br2
试剂:
操作:
目的:
水
分液
除HBr
HBr水溶液
溴苯
苯、溴
试剂:
操作:
目的:
NaOH
分液
除Br2
NaBr溶液
NaBrO溶液
溴苯
苯
操作:
目的:
溴苯
苯
蒸馏
除苯
水洗分液、碱洗分液、蒸馏
除去溶解在溴苯中的液溴,以提纯溴苯
吸收检验HBr
吸收HBr,防止污染环境
防止倒吸
冷凝回流、导气
【练习】2.溴苯是不溶于水的液体,常温下不与酸、碱反应,可用如图装置制取(该反应放出热量)。制取时观察到烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现等现象。下列说法正确的是
A.向反应后的锥形瓶中的“蒸馏水”加入AgNO3溶液,若出
现浅黄色沉淀, 即可证明苯与溴一定发生了取代反应
B.白雾出现是因为HBr易挥发且极易溶于水
C.装置图中长直玻璃导管的作用只是导气
D.溴苯中溶有少量的溴,可用CCl4萃取后分液除去
B
D
校本P41
4.实验室制备溴苯的反应装置如图,下列关于实验操作或叙述错误的( )
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中,装置b中液体呈浅红色
C.装置c中碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
2、取代反应:
①纯净的硝基苯是一种无色液态,有苦杏仁气味,不溶于水,密度比水的大,常因溶有NO2而呈微黄色。
(2)硝化反应:在浓硫酸、50~60oC,可与浓硝酸发生
硝基苯
②浓硫酸的作用:催化剂和脱水剂。
“浴热”容易控制恒温,且易使被加热物质受热均匀
长导管:
冷凝回流、导气
混合混酸时,一定要将浓硫酸沿器壁缓缓注入浓硝酸中,并不断振荡使之混合均匀。
【思考】如何获得纯净的硝基苯?
产物中可能含有
硝基苯、苯、硫酸、硝酸、NO2
试剂:
操作:
目的:
水
分液
除酸
酸液
硝基苯
苯
残余酸
试剂:
操作:
目的:
NaOH
分液
除酸
盐溶液
硝基苯
苯
操作:
目的:
溴苯
苯
蒸馏
除苯
水洗分液、碱洗分液、蒸馏
校本P38
3.实验室制取硝基苯的反应装置如图所示,下列关于实验操作的叙述错误的是( )
A.试剂加入顺序:先加浓硝酸,再加浓硫酸,最后加入苯
B.实验时,水浴温度需控制在50~60 ℃
C.长玻璃导管兼起冷凝回流苯和硝酸的作用,以提高反应物的转化率
D.反应后的混合液经水洗、碱溶液洗涤、结晶,得到硝基苯
D
A
校本P40
2.下列说法正确的是( )
A.硝基苯可由苯与浓硝酸、浓硫酸的混合物在一定条件下发生取代反应来制取
B.硝基苯中碳原子均采取sp杂化
C.硝基苯有毒,密度比水的小,可从水面上“捞出”
D.苯与硝基苯都属于芳香烃
(3)磺化反应:
苯磺酸
苯磺酸易溶于水,是一种强酸,可以看作是硫酸分子里的一个羟基被苯环取代的产物。
磺化反应被广泛应用于制备合成洗涤剂。
苯与浓硫酸在70~80℃发生取代反应
2、取代反应:
+ HO SO3H
+ H2O
SO3H
Δ
3、加成反应
苯的大π键比较稳定,通常状态下不易发生加成反应,在以Pt、Ni等为催化剂并加热的条件下,苯能与氢气发生加成反应。
+ 3H2
Ni
环己烷
D
校本P38
1.(2023·塔城高二质检)下列关于苯的性质的叙述不正确的是( )
A.苯是无色带有特殊气味的液体
B.常温下苯是一种不溶于水且密度小于水的液体
C.苯在一定条件下能与溴发生取代反应
D.苯不含真正的双键,故不能发生加成反应
A
校本P38
2.(2023·黄冈高二月考)下列说法正确的是( )
A.苯分子中有碳氢单键,故能发生取代反应
B.可用苯萃取溴水中的Br2,分液时有机层从分液漏斗下端放出
C.苯分子能使酸性KMnO4溶液褪色
D.苯不能因反应使溴水褪色,说明苯分子中存在碳碳单键,不存在碳碳双键
【思考】苯的分子结构实际上不具有单键和双键的简单交替结构,可以作为证据的事实有哪些?
苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键,事实:
①苯分子中6个碳原子之间的键完全相同(键长相等),且一氯代物只有一种。
②苯不能使酸性KMnO4溶液褪色。
③苯在FeBr3存在的条件下与液溴发生取代反应。
④ 和 是同一种物质。
【练习】苯可发生如图所示反应,下列叙述错误的是
A.反应①为取代反应,向反应后的液体中加入水,有机产物在上层
B.反应②为氧化反应,反应现象是火焰明亮并伴有浓烟
C.反应③为取代反应,有机产物是一种芳香族化合物
D.反应④中1 mol苯最多与3 mol H2在加热、催化剂作用下发生加成反应
A
二、苯的同系物
1、 概念:
苯环上的氢原子被烷基取代所得到的一系列产物
2、苯的同系物结构特点:
分子中只有一个苯环
与苯环相连接的全部是烷基
CH3
CH2CH3
CH=CH2
CH3—CH—CH—CH3
OH
(一)组成和结构
A
3、通式:CnH2n-6 (n≥7)
甲苯 乙苯 邻二甲苯 间二甲苯 对二甲苯
4、习惯命名:
苯的同系物的命名是以苯作为母体的,其他基团作为取代基
5、系统命名:
将苯环上的6个碳原子编号,以某个甲基所在的碳原子的位置为1号,
选取最小位次号给另一个甲基编号。
1,2-二甲苯
1,3-二甲苯
1,4-二甲苯
【练习】对下列物质命名
6、 苯的同系物的同分异构体
试写成分子式为C9H12属于苯的同系物的同分异构体?
表2 2 常见的苯的同系物及其部分物理性质
苯的同系物
CH3
C2H5
CH3
CH3
CH3
CH3
CH3
CH3
名称
熔点/℃
沸点/℃
密度/(g·cm 3)
甲苯
乙苯
邻二甲苯
(1,2-二甲苯)
间二甲苯
(1,3-二甲苯)
对二甲苯
(1,4-二甲苯)
95
95
25
48
13
111
136
144
139
138
0.867
0.867
0.880
0.864
0.861
(二)物理性质
(1)一般具有类似苯的气味的无色液体,不溶于水,易溶于有机溶剂,密度比水的小。
(2)随碳原子数增多,熔、沸点依次升高。
【实验2-2】教材P46
(三)化学性质
实验内容 实验现象 解释
(1)向两只分别盛有2 mL苯和甲苯的试管中各加入几滴溴水,静置
(2)将上述试管用力振荡,静置
(3)向两只分别盛有2 mL苯和甲苯的试管中各加入酸性高锰酸钾溶液,静置
(4)将上述试管用力振荡,静置
苯和甲苯的性质比较
【实验2-2】教材P46
实验内容 实验现象 解释
(1)向两只分别盛有2 mL苯和甲苯的试管中各加入几滴溴水,静置
(2)将上述试管用力振荡,静置
(3)向两只盛有2 mL苯和甲苯的试管中各加入酸性高锰酸钾溶液,静置
(4)将上述试管用力振荡,静置
两支试管中的液体均分层,上层为无色的有机层,下层均是溴水
苯和甲苯都不溶于水,密度都比水小
两支试管中的液体均分层,上层为橙色,下层无色
溴在苯和甲苯中的溶解度比在水中的大
两支试管中均分层,上层为无色的有机层,下层均是紫色酸性高锰酸钾溶液
苯和甲苯都不溶于水,密度都比水小
盛有甲苯的试管中溶液褪色,盛有苯的试管中无明显变化
甲苯可以酸性高锰酸钾溶液反应,而苯不与其反应
(三)化学性质
现象:火焰明亮并带有浓烟。
1、氧化反应
(1)燃烧
(2)甲苯能使酸性KMnO4溶液褪色,这是由于甲苯上的甲基被酸性KMnO4氧化的结果(侧链氧化)。
★苯环对烃基的影响:
受苯环的影响,苯的同系物中作为侧链的烃基的活动性有所增强
CH2
CH
CH3
CH3
CH2
CH2
CH3
这些能使酸性高锰酸钾溶液褪色
CH3
C
CH3
CH3
CH3
C
CH2CH3
CH3
这些不能使酸性高锰酸钾溶液褪色
★侧链烃基中与苯环直接相连的碳原子上有氢原子,该烃基就能被酸性高锰酸钾溶液氧化,且与烷基的多少和大小无关。
★烃基对苯环的影响:
受烃基的影响,苯环的活动性有所增强,较易发生多元取代反应,同时 CH3会使苯环上位于甲基邻、对位上的H原子易于取代。
2、取代反应
(1)硝化反应(以甲苯为例)
甲苯与浓硝酸和浓硫酸的混合物在加热条件下可以发生取代反应,生成一硝基取代物、二硝基取代物和三硝基取代物,硝基取代的位置均以甲基的邻、对位为主。
+3HNO3
浓硫酸
Δ
+ 3H2O
CH3
CH3
NO2
NO2
O2N
2,4,6-三硝基甲苯又叫TNT,是一种淡黄色晶体,不溶于水,它是一种烈性炸药,广泛用于国防、开矿、建筑等。
甲苯与浓硝酸和浓硫酸的混合物在加热条件下反应生成2,4,6-三硝基甲苯
教材P48
(2)卤代反应(以甲苯为例)
a:光照条件下,苯的同系物的取代反应发生在烷基侧链上;
b:溴化铁作催化剂,苯的同系物的取代反应发生在苯环上烷基的邻、对位上。
苯环和侧链都能发生取代反应,但条件不同。
3、加成反应(以甲苯为例)
在一定条件下甲苯与H2发生加成反应,生成甲基环己烷。
B
校本P40
2.(2023·漳州高二质检)可用于鉴别苯和甲苯的试剂或方法是( )
A.液溴和铁粉
B.酸性KMnO4溶液
C.溴水
D.在空气中燃烧
校本P40
3.下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是( )
A.甲苯通过硝化反应生成2,4,6-三硝基甲苯
B.甲苯能使酸性高锰酸钾溶液褪色
C.甲苯燃烧时产生很浓的黑烟
D.1 mol甲苯与3 mol氢气发生加成反应
A
C
芳香烃
苯
苯的同系物
平面正六边形,不含碳碳双键
分子中含一个苯环、侧链为烷基
易取代,难加成,可燃烧,不能使酸性高锰酸钾溶液褪色
易取代,难加成,可燃烧,大部分能使酸性高锰酸钾溶液褪色
性质差异原因:原子团相互影响
结构特点
化学性质
【小结】
三、稠环芳香烃 教材P48【资料卡片】
1、定义
由两个或两个以上的苯环共用相邻的两个碳原子的芳香烃是稠环芳香烃。
2、常见稠环芳香烃
萘
蒽
菲
C10H8
C14H10
C14H10
无色片状晶体,有特殊气味,熔点80℃,易升华,不溶于水。重要化工原料,可用于下生产增塑剂、农药、染料等
无色晶体,易升华,不溶于水。
合成染料的重要原料
【思考】萘的一氯代物有 种,萘的二氯代物有 种
“定一移一”
Cl
Cl
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
