元素周期律(共28张PPT) 第2课时-2023-2024学年高一化学必修第一册
文档属性
| 名称 | 元素周期律(共28张PPT) 第2课时-2023-2024学年高一化学必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 24.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-08 00:00:00 | ||
图片预览






文档简介
(共28张PPT)
环节一:新课导入
人教版·必修1·第四章·第二节
元素周期律
第2课时元素周期表和
元素周期律的应用
学习目标
1、能够分析归纳同周期同主族元素结构位置和性质递变性规律
2、能够根据元素周期律构建“结构-位置-性质”三者之间关系,构
建元素推断阶梯模型
3、能运用元素“结构-位置-性质”模型分析预测元素位置和性质
公
知识导航
(1)元素性质与原子结构位置三者
之间的联系;(2)能利用元素在元
本节重点
素周期表中的位置和原子结构分
析、预测、比较元素及其化合物的
性质
本节难点
元素“位、构、性”
模型构建
01
新课导入
02
建构"位置-结构-性质"认识模型
CONTENTS
03
探究元素周期表和元素周期律的
目录
÷非3
应用
04
绘制元素推断的应用模型畅想
末来元素周期表
22:34
WIFI)
32%0■
史诗巨制回顾百年元素周期表发现史
。
公1人正在看
见心
十关注
@j
6
00:00/02:57
四
萬
大家知道止人是谁吗?
倍速
自动
.化学史说--回顾发展中的元素周期表
第一部分第二部分第三部分
第四部分
1.1789年,拉瓦锡发表了人类历史上第一张《元素分类表》。在这张表中,他
将当时已知的33种元素分成4类。
2.1829年,德国化学家德贝莱纳根据元素性质的相似性提出"三元素组"学说。
3.1864年,德国人迈尔发表了《六元素表》,他按物理性质和相对原子质量递
增的顺序把性质相似的元素每六种分入一族。
4.1865年,纽兰兹独立地进行化学元素的分类研究;在研究中他发现了一个很
有趣的现象;当元素按"原子量"递增的顺序排列起来时,每隔八个元素,元素
的物理性质和化学性质就会重复出现。由此他将各种元素按着"原子量"递增的
顺序排列起来,形成了若干族系的周期。纽兰兹称这一规律为"八音律”。
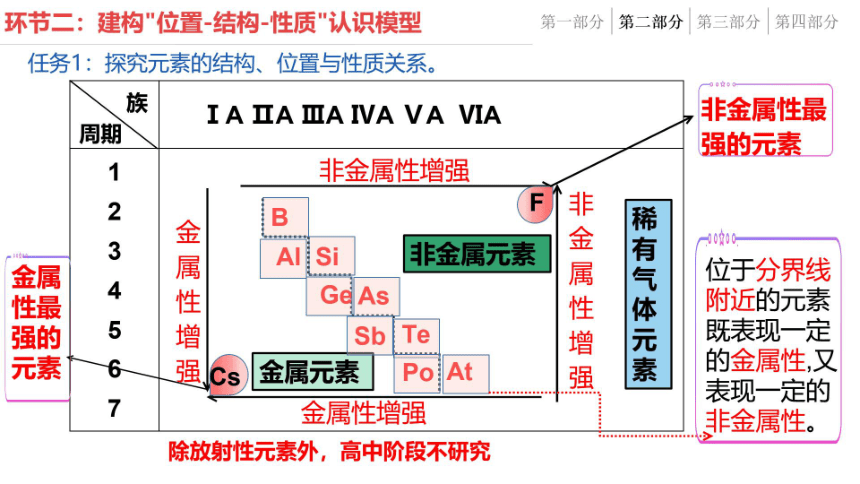
环节二:建构"位置-结构-性质"认识模型
第一部分第二部分
第三部分
第四部分
任务1:探究元素的结构、位置与性质关系
族
IA
IA
ⅢA
IVA
VA
VIA
周期
电子层数相同,核电荷数依次增大一,原子半径依次增大
非金属性依次增强
2
3
核电荷数依次
最外层数相同
电子层数数依次增多
原子半径依次增大
B
Si
非金属元素
4
金属性增强
Gd
As
非金属性增强
原子半径依次减小
最外层数相同
5
增大。
Sb
Te
电子层数数依次减少
核电荷数依次减小。
6
■■■■■
7
金属元素
Po
At
金属性增强
电子层数相同,核电荷数依次减小,」
原子半径依次减小
环节一:新课导入
人教版·必修1·第四章·第二节
元素周期律
第2课时元素周期表和
元素周期律的应用
学习目标
1、能够分析归纳同周期同主族元素结构位置和性质递变性规律
2、能够根据元素周期律构建“结构-位置-性质”三者之间关系,构
建元素推断阶梯模型
3、能运用元素“结构-位置-性质”模型分析预测元素位置和性质
公
知识导航
(1)元素性质与原子结构位置三者
之间的联系;(2)能利用元素在元
本节重点
素周期表中的位置和原子结构分
析、预测、比较元素及其化合物的
性质
本节难点
元素“位、构、性”
模型构建
01
新课导入
02
建构"位置-结构-性质"认识模型
CONTENTS
03
探究元素周期表和元素周期律的
目录
÷非3
应用
04
绘制元素推断的应用模型畅想
末来元素周期表
22:34
WIFI)
32%0■
史诗巨制回顾百年元素周期表发现史
。
公1人正在看
见心
十关注
@j
6
00:00/02:57
四
萬
大家知道止人是谁吗?
倍速
自动
.化学史说--回顾发展中的元素周期表
第一部分第二部分第三部分
第四部分
1.1789年,拉瓦锡发表了人类历史上第一张《元素分类表》。在这张表中,他
将当时已知的33种元素分成4类。
2.1829年,德国化学家德贝莱纳根据元素性质的相似性提出"三元素组"学说。
3.1864年,德国人迈尔发表了《六元素表》,他按物理性质和相对原子质量递
增的顺序把性质相似的元素每六种分入一族。
4.1865年,纽兰兹独立地进行化学元素的分类研究;在研究中他发现了一个很
有趣的现象;当元素按"原子量"递增的顺序排列起来时,每隔八个元素,元素
的物理性质和化学性质就会重复出现。由此他将各种元素按着"原子量"递增的
顺序排列起来,形成了若干族系的周期。纽兰兹称这一规律为"八音律”。
环节二:建构"位置-结构-性质"认识模型
第一部分第二部分
第三部分
第四部分
任务1:探究元素的结构、位置与性质关系
族
IA
IA
ⅢA
IVA
VA
VIA
周期
电子层数相同,核电荷数依次增大一,原子半径依次增大
非金属性依次增强
2
3
核电荷数依次
最外层数相同
电子层数数依次增多
原子半径依次增大
B
Si
非金属元素
4
金属性增强
Gd
As
非金属性增强
原子半径依次减小
最外层数相同
5
增大。
Sb
Te
电子层数数依次减少
核电荷数依次减小。
6
■■■■■
7
金属元素
Po
At
金属性增强
电子层数相同,核电荷数依次减小,」
原子半径依次减小
