胺和酰胺-高考化学考前专项练习试题(含答案)
文档属性
| 名称 | 胺和酰胺-高考化学考前专项练习试题(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-10 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
胺和酰胺
共18题,满分100分
题号 一 二 三 总分
得分
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请注意保持试卷整洁
一、单选题(共50分)
1.(本题5分)2020年8月19日发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》中指出,氯喹类药物可用于治疗新冠肺炎。氯喹和羟基氯喹的结构分别如图1和图2所示,对这两种化合物的描述错误的是
A.氯喹的化学式为C18H26N3Cl,羟基氯喹的化学式为C18H26N3OCl
B.与足量的H2发生加成反应后,两分子中的手性碳原子数相等
C.加入NaOH溶液并加热,再加入AgNO3溶液后生成白色沉淀,可证明氯喹或羟基氯喹中含有氯原子
D.为增大溶解度,易于被人体吸收,经常把氯喹或羟基氯喹与硫酸、盐酸或磷酸制成盐类
2.(本题5分)化合物Z是一种制备抗癌药的中间体,其合成方法如下。下列说法正确的是
A.1molX分子中含6mol碳氮σ键 B.Y分子中所有原子可能共平面
C.Z不能和NaOH溶液发生反应 D.Z分子中含有1个手性碳原子
3.(本题5分)下列反应的化学方程式或离子方程式不正确的是
A.氯气和水反应: Cl2+H2O H+ +Cl-+ HClO
B.向氨水中滴入少量硫酸铜溶液: Cu2+ +2NH3·H2O =Cu(OH)2↓+2
C.铜片上电镀银的总反应: Ag (阳极) Ag (阴极)
D.苯甲酰胺和盐酸反应:
4.(本题5分)以邻苯二酚为原料的某合成路线如图:
下列说法不正确的是
A.I→II是取代反应
B.II与III互为同分异构体
C.预测可以发生反应
D.1molIV最多能与1mol浓HCl反应,最多能与3molNaOH反应
5.(本题5分)2020年6月26日是第三十三个国际禁毒日,主题是“健康人生,绿色无毒”。冰毒,新型毒品的一种,又名甲基安非他明,是一种无味或微有苦味的透明结晶体,纯品很像冰糖,形似冰,故俗称冰毒。甲基苯丙胺是制作冰毒的原料,已知甲基苯丙胺的结构(键线式)如图,下列说法不正确的是
A.甲基苯丙胺的分子式为C10H15N B.甲基苯丙胺能与酸反应
C.甲基苯丙胺的核磁共振氢谱中共有7种信号峰 D.甲基苯丙胺分子中只有一种官能团
6.(本题5分)核酸采样管里的红色液体叫病毒核酸保存液,其主要成分是胍盐和少量的双咪唑烷,并添加一种酸碱指示剂酚红,酚红在中性环境中显红色,如果保存液被污染,pH降低,就会由红色变黄。一种胍盐、双咪唑烷和酚红的分子结构如图所示,以下说法中不正确的是
A.盐酸胍的化学式为,属于盐类
B.双咪唑丁烷可以与羧酸反应生成酰胺
C.双咪唑丁烷常用作配体,其配位原子是N
D.酚红中的苯环上的一氯代物有6种
7.(本题5分)用芳纶纤维PPTA(结构如图)制成的军用防护服具有耐用、轻便、防弹、阻燃以及良好的环境适应性和伪装性等特点。下列说法正确的是
A.PPTA中含有两种官能团
B.PPTA在一定条件下能发生水解反应
C.PPTA的单体一定为
D.PPTA能与反应,不能与盐酸反应
8.(本题5分)我国瑶族的一一个支系一蓝靛瑶族因穿着靛蓝染制成的土布而得名。靛蓝是一种染料,其分子结构如图所示,下列有关靛蓝分子说法不正确的是
A.能与酸反应生成盐 B.能发生取代、加成、水解反应
C.分子式为C16H10N2O2 D.所有C原子可能共平面
9.(本题5分)卡莫氟具有抑制病毒复制的效果,其结构简式如图所示。下列关于卡莫氟的说法错误的是
A.分子式为
B.该物质中含有的官能团有碳碳双键、酰胺基和碳氟键
C.该物质既能发生加成反应,又能发生取代反应
D.该物质与足量溶液反应时最多消耗
10.(本题5分)抗癌试剂和抑制剂的结构简式如图所示。下列叙述错误的是
A.E分子的不饱和度为5
B.E分子中碳原子都是杂化
C.能发生取代反应和消去反应
D.的分子式为
二、判断题(共20分)
11.(本题4分)氯胺的水解产物为和。(______)
12.(本题4分)胺的通式一般写作R-NH2。( )
13.(本题4分)胺类化合物具有碱性。( )
14.(本题4分)可以看作酰胺。(______)
15.(本题4分)甲胺的结构简式为OHC-NH2。( )
三、解答题(共30分)
16.(本题10分)对氯甲苯是生产农药、医药染料的重要中间体,实验室常用对甲基苯胺和亚硝酸钠在冷的无机酸溶液中生成重氮盐,制得的重氮盐再进一步取代即可制得对氯甲苯,其反应原理如下:
实验相关数据:
物质 相对分子质量 密度 沸点/℃ 溶解度
对甲基苯胺 107 0.97 197.4 微溶于水
环己烷 84 0.78 80.7 难溶于水
对氯甲苯 126.5 1.07 159.2 难溶于水,易溶于乙醚、环己烷等有机溶剂
实验步骤:
(一)重氮盐溶液的制备
在烧杯中依次加入15 mL水、15 mL浓盐酸、5.35 g对甲基苯胺,加热至固体充分溶解,将溶液置于冰盐浴中,用玻璃棒不断搅拌至糊状,在0 ℃条件下边搅拌边滴入80% 溶液,用淀粉-KI试纸检验混合液,若试纸变蓝则不必再加溶液。
(二)对氯甲苯的制备
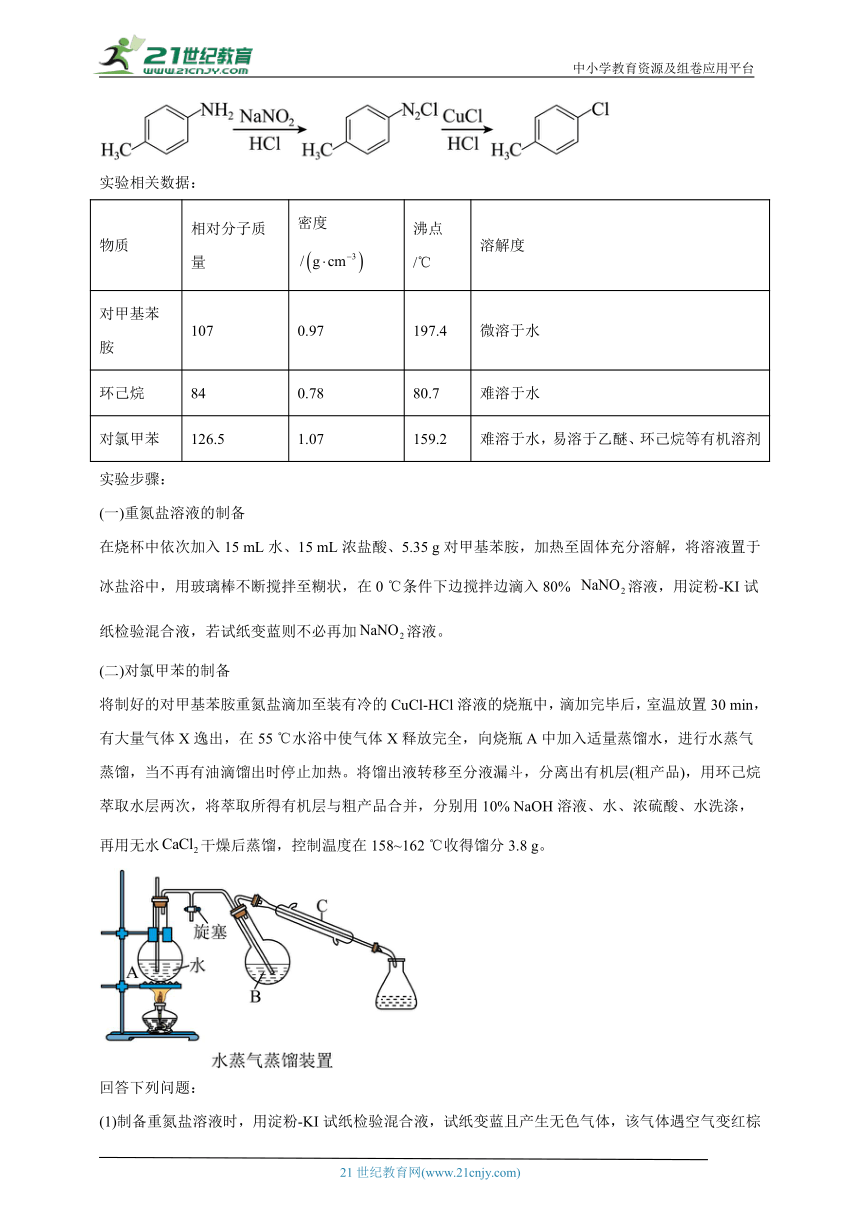
将制好的对甲基苯胺重氮盐滴加至装有冷的CuCl-HCl溶液的烧瓶中,滴加完毕后,室温放置30 min,有大量气体X逸出,在55 ℃水浴中使气体X释放完全,向烧瓶A中加入适量蒸馏水,进行水蒸气蒸馏,当不再有油滴馏出时停止加热。将馏出液转移至分液漏斗,分离出有机层(粗产品),用环己烷萃取水层两次,将萃取所得有机层与粗产品合并,分别用10% NaOH溶液、水、浓硫酸、水洗涤,再用无水干燥后蒸馏,控制温度在158~162 ℃收得馏分3.8 g。
回答下列问题:
(1)制备重氮盐溶液时,用淀粉-KI试纸检验混合液,试纸变蓝且产生无色气体,该气体遇空气变红棕色,导致试纸变蓝的反应的化学方程式为 。
(2)仪器C的名称为 ,A中玻璃管的作用为 。
(3)用环己烷萃取水层时,所得有机层从分液漏斗 (填“上口”或“下口”)放出,将萃取所得有机层与粗产品合并的目的是 。
(4)粗产品经干燥后,先用 (填序号)蒸馏由低沸点杂质,再控制温度在158~162 ℃改用 (填序号)收集馏分。
A.直形冷凝管 B.球形冷凝管 C.空气冷凝管
(5)对氯甲苯的产率为 (保留两位有效数字)。
17.(本题10分)邻苯二甲酰亚胺(PIMD)是一种重要的亚胺,是Gabriel合成法制备胺的原料。某实验室模拟氨水法以邻苯二甲酸酐为原料制备PIMD。
反应原理:
实验装置如图:
相关物质的物理性质如表:
物质 相对分子质量 熔点/℃ 沸点/℃ 溶解性
邻苯二甲酸酐 148 131~134 284 不溶于冷水,微溶于热水,稍溶于乙醇
邻苯二甲酰亚胺 147 232~235 366 微溶于热水,易溶于乙醇,易溶于碱溶液
实验步骤:
I.向250mL三颈烧瓶中加入74.0g邻苯二甲酸酐,边搅拌边滴入50.0mL浓氨水(稍过量),加热至80℃-95℃,待固体完全溶解后停止加热。将三颈烧瓶右端口所连装置取下改为蒸馏装置,继续加热,将溶液中的水及过量的氨蒸馏回收,此时烧瓶中有白色固体析出。
Ⅱ.继续升温至235℃-240℃,固体熔化,反应60分钟后,停止加热。冷却至室温,热水洗涤固体、抽滤、烘干,得到粗品白色粉末72.2g。
Ⅲ.向白色粉末中加入适量乙醇,加热回流使固体恰好溶解, ,将滤液降温冷却,有白色晶体析出,抽滤、洗涤、烘干后得白色晶体59.2g。
请回答下列问题:
(1)仪器A的名称为 ,仪器A中盛装的试剂是 。(填标号)
a.碱石灰 b.五氧化二磷 c.浓硫酸
(2)步骤Ⅱ所得粗品中的杂质主要为 。
(3)邻苯二甲酸酐的熔沸点远低于邻苯二甲酰亚胺,原因可能是 。
(4)步骤Ⅲ的目的是利用重结晶进一步提纯邻苯二甲酰亚胺,该步骤中划线部分应补全的操作是 。选择乙醇作为提纯溶剂的主要原因是 。
(5)本实验中邻苯二甲酰亚胺的产率最接近于 。(填标号)
a.85% b.80% c.75% d.70%
(6)邻苯二甲酰亚胺还可以用由邻二甲苯与氨气、氧气在加热条件下催化反应一步制得,写出该反应的化学方程式: 。
18.(本题10分)乙酰苯胺()有止痛、退热的功能,在实验室按以下流程进行制备。
I.查阅资料:苯胺易被氧化,乙酰苯胺在碱性条件下水解,其他物质的有关性质如下表。
名称 熔点/℃ 沸点/℃ 溶解度/g(20℃)
水 乙醇
苯胺 -6.3 184 3.4 任意比混溶
冰醋酸 16.6 118 任意比混溶 任意比混溶
乙酰苯胺 114.3 304 0.46(温度越高,溶解度越大) 36.9
Ⅱ.制备过程:
(1)原理与装置。
实验装置如图。在三颈烧瓶中先加入锌粒和冰醋酸,然后用恒压滴液漏斗滴加苯胺。
①球形冷凝管的作用是 ,冷凝水的进水口为 (填“M”或“N”)。
②加入锌粒,除了防止暴沸外,还能起到的作用是 。
③写出该制备方法的主要反应方程式 。
④制备过程中温度计控制示数在左右的原因是 。
(2)制得粗产品。
实验流程包括:,其中最合适的“洗涤”是 (填标号)。
a.的乙醇溶液 b.溶液 c.冰水 d.热水
(3)重结晶提纯。
粗产品溶于沸水中配成饱和溶液再加入少量蒸馏水加入活性炭脱色加热煮沸 冷却结晶过滤一洗涤干燥,得到产品。
Ⅲ.计算产率。
(4)已知:产率=,本实验中乙酰苯胺的产率为 (保留两位有效数字)。
参考答案:
1.C
【详解】A.由结构简式可知,氯喹的化学式为C18H26N3Cl,羟基氯喹的化学式为C18H26N3OCl,故A正确;
B.与足量的氢气发生加成反应后,所得产物都有如图*所示的5个手性碳原子:、,故B正确;
C.检验氯喹或羟基氯喹中含有氯原子时,应该先加入氢氧化钠溶液,共热后,为防止氢氧根离子干扰氯离子检验,应先加入硝酸酸化使溶液呈酸性,再加入硝酸银溶液,若生成白色沉淀,就可证明氯喹或羟基氯喹中含有氯原子,故C错误;
D.在氯喹和羟基氯喹中都含有亚氨基,能够与酸形成配位键而结合在一起,使物质在水中溶解度大大增加,从而更容易被人体吸收,故D正确;
故选C。
2.A
【详解】A.单键全是σ键,三键含一个σ键,结合X的结构简式可知,1molX分子中含6mol碳氮σ键,A正确;
B.Y分子中含有饱和碳原子,所有原子不可能共平面,B错误;
C.Z分子中含有,可与NaOH溶液发生水解反应,C错误;
D.手性碳原子为饱和碳原子,且碳原子连有4个不同的基团,因此Z分子中不含有手性碳原子,D错误;
答案选A。
3.B
【详解】A.氯气和水反应生成盐酸和次氯酸,反应的离子方程式是,故A正确;
B.稀氨水中滴入少量CuSO4溶液,反应生成[Cu(NH3)4]2+络离子,离子方程式为Cu2++4NH3 H2O═[Cu(NH3)4]2++4H2O,故B错误;
C.铜片上电镀银,阳极反应式为Ag-e-=Ag+,阴极反应式为Ag++e-=Ag,总反应:,故C正确;
D.苯甲酰胺和盐酸反应生成苯甲酸和氯化铵,反应的离子方程式是;
故D正确;
故选B。
4.D
【详解】A.对比有机物结构,可知Ⅰ→Ⅱ过程中酚羟基上氢原子被-COCH2Cl替代,反应类型为取代反应,A正确;
B.Ⅱ与Ⅲ分子式相同、结构不相同,二者互为同分异构体,B正确;
C.类比Ⅱ→Ⅲ的转化,预测可以发生反应,C正确;
D.亚氨基、醇羟基能与HCl反应,故1molIV最多能与2mol浓HCl反应,酚羟基与NaOH发生中和反应,1molIV最多能与2molNaOH反应,D错误;
故答案为:D。
5.C
【详解】A.由甲基苯丙胺的结构简式可知其分子式为C10H15N,A正确;
B.甲基苯丙胺分子中存在亚氨基(-NH-),能与酸反应,B正确;
C.甲基苯丙胺分子中等效氢原子共含有8种(),所以核磁共振氢谱中共有8种信号峰,C错误;
D.甲基苯丙胺分子中只有亚氨基(-NH-)一种官能团,D正确;
故选C。
6.B
【详解】A.根据结构信息,盐酸胍的化学式为,属于盐类,A正确;
B.双咪唑丁烷属于烃的衍生物,不含胺基或亚胺基,不可以与羧酸反应生成酰胺,B错误;
C.双咪唑丁烷中的氮原子含有孤对电子,常用作配体,配位原子是N,C正确;
D.根据酚红的结构,其苯环上有6种氢原子、则苯环上的一氯代物有6种,D正确;
故选B。
7.B
【详解】A.PPTA中含有氨基、羧基、酰胺基三种官能团,A错误;
B.PPTA中的酰胺基在一定条件下能发生水解反应,B正确;
C.PPTA的单体为 、 ,C错误;
D.PPTA中含有氨基、羧基、酰胺基,羧基可以和碳酸氢钠反应,氨基可以和盐酸反应,D错误;
故选B。
8.B
【详解】A.分子中亚氨基能和酸反应生成盐,故A正确;
B.具有苯、酮、烯烃及氨的性质,该有机物中亚氨基能发生取代反应,碳碳双键和苯环能发生加成反应,该有机物中不含酰胺键、卤原子或酯基,不能发生水解反应,故B错误;
C.分子中C、H、N、O原子个数依次是16、10、2、2,分子式为C16H10N2O2,故C正确;
D.苯环上所有原子、碳碳双键之间连接的原子共平面,所以该分子中所有碳原子可能共平面,故D正确;
故选:B。
9.D
【详解】A.由结构简式可知,卡莫氟的分子式为,A项正确;
B.由结构简式可知,该物质中含有的官能团有:碳碳双键、酰胺基和碳氟键,B项正确;
C.该物质中含有碳碳双键,可发生加成反应,含有酰胺基,可发生水解反应,即取代反应,C项正确;
D.该物质水解时可断裂的化学键的位置如图所示,故该物质与足量溶液反应时最多消耗,D项错误;
答案选D。
10.C
【详解】A.E分子中含有5个环,不饱和度为5,故A正确;
B.E分子中碳原子均为单键碳,都是杂化,故B正确;
C.中含有氨基能发生取代反应,不能发生消去反应,故C错误;
D.根据的结构简式,可知分子式为,故D正确;
选C。
11.错误
【详解】氯胺中Cl元素化合价为+1,水解产物为和HClO,故上述说法错误。
12.正确
【详解】胺是氨分子中氢原子被烃基取代的产物,故其通式可表示为R-NH2,则上述表示方法正确、合理。
13.正确
【详解】胺类化合物中,氮原子有未共用电子对,能接受质子,因此胺具有碱性,与酸反应生成盐;该说法正确。
14.正确
【详解】酰胺是羧酸分子中羟基被氨基所替代得到的化合物,其结构一般为,而可看成(H2CO3)分子中羟基被氨基所替代得到的化合物,故可以看作酰胺,说法正确。
15.错误
【详解】甲胺的结构简式为CH3NH2,故错误;
16.(1)
(2) 直形冷凝管 平衡气压
(3) 上口 提高对氯甲苯的产率
(4) A C
(5)60%
【分析】浓盐酸、对甲基苯胺、溶液反应制备甲基苯胺重氮盐溶液。对甲基苯胺重氮盐滴加至装有冷的CuCl-HCl溶液的烧瓶中反应生成高对氯甲苯,反应完成后,向烧瓶中加入适量蒸馏水,进行水蒸气蒸馏,当不再有油滴馏出时停止加热。将馏出液用环己烷萃取水层两次,将萃取所得有机层与粗产品合并,洗涤、干燥后蒸馏,控制温度在158~162 ℃收得馏分即为高对氯甲苯产品。
【详解】(1)制备重氮盐溶液时,用淀粉-KI试纸检验混合液,试纸变蓝,说明生成了,产生无色气体,该气体遇空气变红棕色,说明生成的气体为NO,可知亚硝酸根离子把碘离子氧化为碘单质,反应的化学方程式为。
(2)根据图示,仪器C的名称为直形冷凝管;A中玻璃管与空气连通,则A的作用为平衡气压。
(3)环己烷的密度小于水,用环己烷作萃取剂萃取分液时,先从下口放出水层,再从上口倒出有机层,将萃取所得有机层与粗产品合并,可以减少产物损耗,提高对氯甲苯的产率。
(4)直形冷凝管冷凝效果好,但是馏分沸点高于140 ℃时,直形冷凝管内外温差大,容易碎裂,应该换成空气冷凝管,故粗产品经干燥后,先用直形冷凝管蒸馏出低沸点杂质(环己烷),再控制温度在158~162 ℃改用空气冷凝管收集馏分。
(5)5.35 g对甲基苯胺的物质的量为 ,理论上生成对氯甲苯得物质的量为0.05mol,则对氯甲苯的产率为 。
17.(1) 球形干燥管 b
(2)苯二甲酸酐
(3)两者均为分子晶体,邻苯二甲酰亚胺能形成分子间氢键,使分子间作用力增大,熔点更高
(4) 趁热过滤,并用乙醇洗涤沉淀 减小邻苯二甲酸酐的溶解量,使分离更加完全,且乙醇易挥发,便于干燥
(5)a
(6) +NH3+3O2 +4H2O
【分析】由题给流程可知,装置甲中发生的反应为邻苯二甲酸酐与氨水在80~95℃的热水浴中发生取代反应生成邻氨甲酰苯甲酸,邻氨甲酰苯甲酸在加热条件下发生取代反应生成邻苯二甲酰亚胺,用于除去所得固体中的水分,除水所得固体经冷却,洗涤、抽滤烘干,进一步提纯得固体邻苯二甲酰亚胺,据此分析解题。
【详解】(1)由题干实验装置图可知,仪器A的名称为球形干燥管,实验中仪器A的作用为吸收尾气NH3,球形干燥管只能盛放固体,故其中盛装的试剂是五氧化二磷,故答案为:球形干燥管;b;
(2)由题干表格信息可知,邻苯二甲酸酐不溶于冷水,微溶于热水,稍溶于乙醇,可知步骤Ⅱ所得粗品中的杂质主要为邻苯二甲酸酐,故答案为:苯二甲酸酐;
(3)邻苯二甲酰亚胺可形成分子间氢键,使其分子间作用力增大,熔点更高,故答案为:两者均为分子晶体,邻苯二甲酰亚胺能形成分子间氢键,使分子间作用力增大,熔点更高;
(4)由题干表格信息可知,邻苯二甲酸酐不溶于冷水,微溶于热水,稍溶于乙醇,而邻苯二甲酰亚胺微溶于热水,易溶于乙醇,易溶于碱溶液,故Ⅲ.向白色粉末中加入适量乙醇,加热回流使固体恰好溶解,趁热过滤,并用乙醇洗涤沉淀,将滤液降温冷却,有白色晶体析出,抽滤、洗涤、烘干后得白色晶体,选择乙醇作为提纯溶剂的主要原因是减小邻苯二甲酸酐的溶解量,使分离更加完全,且乙醇易挥发,便于干燥,故答案为:趁热过滤,并用乙醇洗涤沉淀;减小邻苯二甲酸酐的溶解量,使分离更加完全,且乙醇易挥发,便于干燥;
(5)由题意可知,74.0g邻苯二甲酸酐制得59.2g邻苯二甲酰亚胺,则邻苯二甲酰亚胺的产率为×100%=89.37%,接近85%,故答案为:a;
(6)由题意可知,邻二甲苯与氨气、空气在加热条件下催化反应生成邻苯二甲酰亚胺和水,反应的化学方程式为:+NH3+3O2 +4H2O,故答案为:+NH3+3O2 +4H2O。
18.(1) 冷凝回流(减少苯胺和冰醋酸蒸出) N 防止苯胺被氧化 冰醋酸具有挥发性,温度高于,冰醋酸蒸出,降低了原料的利用率;温度低于,不利于蒸出水,影响了乙酰苯胺产率的提高
(2)c
(3)趁热过滤
(4)
【分析】根据题干信息,根据原理C6H5-NH2 + CH3COOHC6H5–NHCOCH3+ H2O制备乙酰苯胺,以苯胺和冰醋酸为原料,控温加热1h后趁热倒入冷水,析出晶体后抽滤、洗涤、干燥得到粗产品,洗涤时需注意温度越高,乙酰苯胺溶解度越大,且在碱性条件下易水解,可选用冰水洗涤,再重结晶得到产品,据此分析解答问题。
【详解】(1)①球形冷凝管的作用是冷凝回流(减少苯胺和冰醋酸蒸出),冷凝水下进上出,则进水口为N。
②根据题干信息,苯胺易被氧化,而锌粒可与酸反应生成氢气,形成氢气环境,从而防止苯胺被氧化,则加入锌粒还能起到的作用是防止苯胺被氧化。
③该制备方法的主要反应方程式C6H5-NH2 + CH3COOHC6H5–NHCOCH3+ H2O。
④制备过程中温度计控制示数在左右的原因是:已知冰醋酸具有挥发性,因此温度过高,冰醋酸蒸出,降低了反应物的利用率,但温度过低,不利于蒸出水,所以将温度控制在约105℃时。
(2)由于乙酰苯胺易溶于酒精,在水中温度越高,乙酰苯胺溶解度越大,且在碱性条件下易水解,故选用冰水洗涤,故选c。
(3)由表格数据可知,该晶体可通过冷却结晶获得。重结晶时,将粗产品溶于沸水中配成饱和溶液,再加入少量蒸馏水,加入活性炭脱色,接着加热煮沸,趁热过滤后冷却结晶,再过滤、洗涤、干燥得到最终产品,故答案为:趁热过滤。
(4)根据分析,制备乙酰苯胺的实验原理为C6H5-NH2 + CH3COOHC6H5–NHCOCH3+ H2O,以0.11mol的苯胺和0.26mol的冰醋酸为原料,可知冰醋酸过量,根据反应方程式可求得理论上制得的乙酰苯胺的物质的量为0.11mol,则质量为0.11mol×135g/mol=14.85g,则根据公式产率=可知,乙酰苯胺的产率为×100%≈67%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
胺和酰胺
共18题,满分100分
题号 一 二 三 总分
得分
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请注意保持试卷整洁
一、单选题(共50分)
1.(本题5分)2020年8月19日发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》中指出,氯喹类药物可用于治疗新冠肺炎。氯喹和羟基氯喹的结构分别如图1和图2所示,对这两种化合物的描述错误的是
A.氯喹的化学式为C18H26N3Cl,羟基氯喹的化学式为C18H26N3OCl
B.与足量的H2发生加成反应后,两分子中的手性碳原子数相等
C.加入NaOH溶液并加热,再加入AgNO3溶液后生成白色沉淀,可证明氯喹或羟基氯喹中含有氯原子
D.为增大溶解度,易于被人体吸收,经常把氯喹或羟基氯喹与硫酸、盐酸或磷酸制成盐类
2.(本题5分)化合物Z是一种制备抗癌药的中间体,其合成方法如下。下列说法正确的是
A.1molX分子中含6mol碳氮σ键 B.Y分子中所有原子可能共平面
C.Z不能和NaOH溶液发生反应 D.Z分子中含有1个手性碳原子
3.(本题5分)下列反应的化学方程式或离子方程式不正确的是
A.氯气和水反应: Cl2+H2O H+ +Cl-+ HClO
B.向氨水中滴入少量硫酸铜溶液: Cu2+ +2NH3·H2O =Cu(OH)2↓+2
C.铜片上电镀银的总反应: Ag (阳极) Ag (阴极)
D.苯甲酰胺和盐酸反应:
4.(本题5分)以邻苯二酚为原料的某合成路线如图:
下列说法不正确的是
A.I→II是取代反应
B.II与III互为同分异构体
C.预测可以发生反应
D.1molIV最多能与1mol浓HCl反应,最多能与3molNaOH反应
5.(本题5分)2020年6月26日是第三十三个国际禁毒日,主题是“健康人生,绿色无毒”。冰毒,新型毒品的一种,又名甲基安非他明,是一种无味或微有苦味的透明结晶体,纯品很像冰糖,形似冰,故俗称冰毒。甲基苯丙胺是制作冰毒的原料,已知甲基苯丙胺的结构(键线式)如图,下列说法不正确的是
A.甲基苯丙胺的分子式为C10H15N B.甲基苯丙胺能与酸反应
C.甲基苯丙胺的核磁共振氢谱中共有7种信号峰 D.甲基苯丙胺分子中只有一种官能团
6.(本题5分)核酸采样管里的红色液体叫病毒核酸保存液,其主要成分是胍盐和少量的双咪唑烷,并添加一种酸碱指示剂酚红,酚红在中性环境中显红色,如果保存液被污染,pH降低,就会由红色变黄。一种胍盐、双咪唑烷和酚红的分子结构如图所示,以下说法中不正确的是
A.盐酸胍的化学式为,属于盐类
B.双咪唑丁烷可以与羧酸反应生成酰胺
C.双咪唑丁烷常用作配体,其配位原子是N
D.酚红中的苯环上的一氯代物有6种
7.(本题5分)用芳纶纤维PPTA(结构如图)制成的军用防护服具有耐用、轻便、防弹、阻燃以及良好的环境适应性和伪装性等特点。下列说法正确的是
A.PPTA中含有两种官能团
B.PPTA在一定条件下能发生水解反应
C.PPTA的单体一定为
D.PPTA能与反应,不能与盐酸反应
8.(本题5分)我国瑶族的一一个支系一蓝靛瑶族因穿着靛蓝染制成的土布而得名。靛蓝是一种染料,其分子结构如图所示,下列有关靛蓝分子说法不正确的是
A.能与酸反应生成盐 B.能发生取代、加成、水解反应
C.分子式为C16H10N2O2 D.所有C原子可能共平面
9.(本题5分)卡莫氟具有抑制病毒复制的效果,其结构简式如图所示。下列关于卡莫氟的说法错误的是
A.分子式为
B.该物质中含有的官能团有碳碳双键、酰胺基和碳氟键
C.该物质既能发生加成反应,又能发生取代反应
D.该物质与足量溶液反应时最多消耗
10.(本题5分)抗癌试剂和抑制剂的结构简式如图所示。下列叙述错误的是
A.E分子的不饱和度为5
B.E分子中碳原子都是杂化
C.能发生取代反应和消去反应
D.的分子式为
二、判断题(共20分)
11.(本题4分)氯胺的水解产物为和。(______)
12.(本题4分)胺的通式一般写作R-NH2。( )
13.(本题4分)胺类化合物具有碱性。( )
14.(本题4分)可以看作酰胺。(______)
15.(本题4分)甲胺的结构简式为OHC-NH2。( )
三、解答题(共30分)
16.(本题10分)对氯甲苯是生产农药、医药染料的重要中间体,实验室常用对甲基苯胺和亚硝酸钠在冷的无机酸溶液中生成重氮盐,制得的重氮盐再进一步取代即可制得对氯甲苯,其反应原理如下:
实验相关数据:
物质 相对分子质量 密度 沸点/℃ 溶解度
对甲基苯胺 107 0.97 197.4 微溶于水
环己烷 84 0.78 80.7 难溶于水
对氯甲苯 126.5 1.07 159.2 难溶于水,易溶于乙醚、环己烷等有机溶剂
实验步骤:
(一)重氮盐溶液的制备
在烧杯中依次加入15 mL水、15 mL浓盐酸、5.35 g对甲基苯胺,加热至固体充分溶解,将溶液置于冰盐浴中,用玻璃棒不断搅拌至糊状,在0 ℃条件下边搅拌边滴入80% 溶液,用淀粉-KI试纸检验混合液,若试纸变蓝则不必再加溶液。
(二)对氯甲苯的制备
将制好的对甲基苯胺重氮盐滴加至装有冷的CuCl-HCl溶液的烧瓶中,滴加完毕后,室温放置30 min,有大量气体X逸出,在55 ℃水浴中使气体X释放完全,向烧瓶A中加入适量蒸馏水,进行水蒸气蒸馏,当不再有油滴馏出时停止加热。将馏出液转移至分液漏斗,分离出有机层(粗产品),用环己烷萃取水层两次,将萃取所得有机层与粗产品合并,分别用10% NaOH溶液、水、浓硫酸、水洗涤,再用无水干燥后蒸馏,控制温度在158~162 ℃收得馏分3.8 g。
回答下列问题:
(1)制备重氮盐溶液时,用淀粉-KI试纸检验混合液,试纸变蓝且产生无色气体,该气体遇空气变红棕色,导致试纸变蓝的反应的化学方程式为 。
(2)仪器C的名称为 ,A中玻璃管的作用为 。
(3)用环己烷萃取水层时,所得有机层从分液漏斗 (填“上口”或“下口”)放出,将萃取所得有机层与粗产品合并的目的是 。
(4)粗产品经干燥后,先用 (填序号)蒸馏由低沸点杂质,再控制温度在158~162 ℃改用 (填序号)收集馏分。
A.直形冷凝管 B.球形冷凝管 C.空气冷凝管
(5)对氯甲苯的产率为 (保留两位有效数字)。
17.(本题10分)邻苯二甲酰亚胺(PIMD)是一种重要的亚胺,是Gabriel合成法制备胺的原料。某实验室模拟氨水法以邻苯二甲酸酐为原料制备PIMD。
反应原理:
实验装置如图:
相关物质的物理性质如表:
物质 相对分子质量 熔点/℃ 沸点/℃ 溶解性
邻苯二甲酸酐 148 131~134 284 不溶于冷水,微溶于热水,稍溶于乙醇
邻苯二甲酰亚胺 147 232~235 366 微溶于热水,易溶于乙醇,易溶于碱溶液
实验步骤:
I.向250mL三颈烧瓶中加入74.0g邻苯二甲酸酐,边搅拌边滴入50.0mL浓氨水(稍过量),加热至80℃-95℃,待固体完全溶解后停止加热。将三颈烧瓶右端口所连装置取下改为蒸馏装置,继续加热,将溶液中的水及过量的氨蒸馏回收,此时烧瓶中有白色固体析出。
Ⅱ.继续升温至235℃-240℃,固体熔化,反应60分钟后,停止加热。冷却至室温,热水洗涤固体、抽滤、烘干,得到粗品白色粉末72.2g。
Ⅲ.向白色粉末中加入适量乙醇,加热回流使固体恰好溶解, ,将滤液降温冷却,有白色晶体析出,抽滤、洗涤、烘干后得白色晶体59.2g。
请回答下列问题:
(1)仪器A的名称为 ,仪器A中盛装的试剂是 。(填标号)
a.碱石灰 b.五氧化二磷 c.浓硫酸
(2)步骤Ⅱ所得粗品中的杂质主要为 。
(3)邻苯二甲酸酐的熔沸点远低于邻苯二甲酰亚胺,原因可能是 。
(4)步骤Ⅲ的目的是利用重结晶进一步提纯邻苯二甲酰亚胺,该步骤中划线部分应补全的操作是 。选择乙醇作为提纯溶剂的主要原因是 。
(5)本实验中邻苯二甲酰亚胺的产率最接近于 。(填标号)
a.85% b.80% c.75% d.70%
(6)邻苯二甲酰亚胺还可以用由邻二甲苯与氨气、氧气在加热条件下催化反应一步制得,写出该反应的化学方程式: 。
18.(本题10分)乙酰苯胺()有止痛、退热的功能,在实验室按以下流程进行制备。
I.查阅资料:苯胺易被氧化,乙酰苯胺在碱性条件下水解,其他物质的有关性质如下表。
名称 熔点/℃ 沸点/℃ 溶解度/g(20℃)
水 乙醇
苯胺 -6.3 184 3.4 任意比混溶
冰醋酸 16.6 118 任意比混溶 任意比混溶
乙酰苯胺 114.3 304 0.46(温度越高,溶解度越大) 36.9
Ⅱ.制备过程:
(1)原理与装置。
实验装置如图。在三颈烧瓶中先加入锌粒和冰醋酸,然后用恒压滴液漏斗滴加苯胺。
①球形冷凝管的作用是 ,冷凝水的进水口为 (填“M”或“N”)。
②加入锌粒,除了防止暴沸外,还能起到的作用是 。
③写出该制备方法的主要反应方程式 。
④制备过程中温度计控制示数在左右的原因是 。
(2)制得粗产品。
实验流程包括:,其中最合适的“洗涤”是 (填标号)。
a.的乙醇溶液 b.溶液 c.冰水 d.热水
(3)重结晶提纯。
粗产品溶于沸水中配成饱和溶液再加入少量蒸馏水加入活性炭脱色加热煮沸 冷却结晶过滤一洗涤干燥,得到产品。
Ⅲ.计算产率。
(4)已知:产率=,本实验中乙酰苯胺的产率为 (保留两位有效数字)。
参考答案:
1.C
【详解】A.由结构简式可知,氯喹的化学式为C18H26N3Cl,羟基氯喹的化学式为C18H26N3OCl,故A正确;
B.与足量的氢气发生加成反应后,所得产物都有如图*所示的5个手性碳原子:、,故B正确;
C.检验氯喹或羟基氯喹中含有氯原子时,应该先加入氢氧化钠溶液,共热后,为防止氢氧根离子干扰氯离子检验,应先加入硝酸酸化使溶液呈酸性,再加入硝酸银溶液,若生成白色沉淀,就可证明氯喹或羟基氯喹中含有氯原子,故C错误;
D.在氯喹和羟基氯喹中都含有亚氨基,能够与酸形成配位键而结合在一起,使物质在水中溶解度大大增加,从而更容易被人体吸收,故D正确;
故选C。
2.A
【详解】A.单键全是σ键,三键含一个σ键,结合X的结构简式可知,1molX分子中含6mol碳氮σ键,A正确;
B.Y分子中含有饱和碳原子,所有原子不可能共平面,B错误;
C.Z分子中含有,可与NaOH溶液发生水解反应,C错误;
D.手性碳原子为饱和碳原子,且碳原子连有4个不同的基团,因此Z分子中不含有手性碳原子,D错误;
答案选A。
3.B
【详解】A.氯气和水反应生成盐酸和次氯酸,反应的离子方程式是,故A正确;
B.稀氨水中滴入少量CuSO4溶液,反应生成[Cu(NH3)4]2+络离子,离子方程式为Cu2++4NH3 H2O═[Cu(NH3)4]2++4H2O,故B错误;
C.铜片上电镀银,阳极反应式为Ag-e-=Ag+,阴极反应式为Ag++e-=Ag,总反应:,故C正确;
D.苯甲酰胺和盐酸反应生成苯甲酸和氯化铵,反应的离子方程式是;
故D正确;
故选B。
4.D
【详解】A.对比有机物结构,可知Ⅰ→Ⅱ过程中酚羟基上氢原子被-COCH2Cl替代,反应类型为取代反应,A正确;
B.Ⅱ与Ⅲ分子式相同、结构不相同,二者互为同分异构体,B正确;
C.类比Ⅱ→Ⅲ的转化,预测可以发生反应,C正确;
D.亚氨基、醇羟基能与HCl反应,故1molIV最多能与2mol浓HCl反应,酚羟基与NaOH发生中和反应,1molIV最多能与2molNaOH反应,D错误;
故答案为:D。
5.C
【详解】A.由甲基苯丙胺的结构简式可知其分子式为C10H15N,A正确;
B.甲基苯丙胺分子中存在亚氨基(-NH-),能与酸反应,B正确;
C.甲基苯丙胺分子中等效氢原子共含有8种(),所以核磁共振氢谱中共有8种信号峰,C错误;
D.甲基苯丙胺分子中只有亚氨基(-NH-)一种官能团,D正确;
故选C。
6.B
【详解】A.根据结构信息,盐酸胍的化学式为,属于盐类,A正确;
B.双咪唑丁烷属于烃的衍生物,不含胺基或亚胺基,不可以与羧酸反应生成酰胺,B错误;
C.双咪唑丁烷中的氮原子含有孤对电子,常用作配体,配位原子是N,C正确;
D.根据酚红的结构,其苯环上有6种氢原子、则苯环上的一氯代物有6种,D正确;
故选B。
7.B
【详解】A.PPTA中含有氨基、羧基、酰胺基三种官能团,A错误;
B.PPTA中的酰胺基在一定条件下能发生水解反应,B正确;
C.PPTA的单体为 、 ,C错误;
D.PPTA中含有氨基、羧基、酰胺基,羧基可以和碳酸氢钠反应,氨基可以和盐酸反应,D错误;
故选B。
8.B
【详解】A.分子中亚氨基能和酸反应生成盐,故A正确;
B.具有苯、酮、烯烃及氨的性质,该有机物中亚氨基能发生取代反应,碳碳双键和苯环能发生加成反应,该有机物中不含酰胺键、卤原子或酯基,不能发生水解反应,故B错误;
C.分子中C、H、N、O原子个数依次是16、10、2、2,分子式为C16H10N2O2,故C正确;
D.苯环上所有原子、碳碳双键之间连接的原子共平面,所以该分子中所有碳原子可能共平面,故D正确;
故选:B。
9.D
【详解】A.由结构简式可知,卡莫氟的分子式为,A项正确;
B.由结构简式可知,该物质中含有的官能团有:碳碳双键、酰胺基和碳氟键,B项正确;
C.该物质中含有碳碳双键,可发生加成反应,含有酰胺基,可发生水解反应,即取代反应,C项正确;
D.该物质水解时可断裂的化学键的位置如图所示,故该物质与足量溶液反应时最多消耗,D项错误;
答案选D。
10.C
【详解】A.E分子中含有5个环,不饱和度为5,故A正确;
B.E分子中碳原子均为单键碳,都是杂化,故B正确;
C.中含有氨基能发生取代反应,不能发生消去反应,故C错误;
D.根据的结构简式,可知分子式为,故D正确;
选C。
11.错误
【详解】氯胺中Cl元素化合价为+1,水解产物为和HClO,故上述说法错误。
12.正确
【详解】胺是氨分子中氢原子被烃基取代的产物,故其通式可表示为R-NH2,则上述表示方法正确、合理。
13.正确
【详解】胺类化合物中,氮原子有未共用电子对,能接受质子,因此胺具有碱性,与酸反应生成盐;该说法正确。
14.正确
【详解】酰胺是羧酸分子中羟基被氨基所替代得到的化合物,其结构一般为,而可看成(H2CO3)分子中羟基被氨基所替代得到的化合物,故可以看作酰胺,说法正确。
15.错误
【详解】甲胺的结构简式为CH3NH2,故错误;
16.(1)
(2) 直形冷凝管 平衡气压
(3) 上口 提高对氯甲苯的产率
(4) A C
(5)60%
【分析】浓盐酸、对甲基苯胺、溶液反应制备甲基苯胺重氮盐溶液。对甲基苯胺重氮盐滴加至装有冷的CuCl-HCl溶液的烧瓶中反应生成高对氯甲苯,反应完成后,向烧瓶中加入适量蒸馏水,进行水蒸气蒸馏,当不再有油滴馏出时停止加热。将馏出液用环己烷萃取水层两次,将萃取所得有机层与粗产品合并,洗涤、干燥后蒸馏,控制温度在158~162 ℃收得馏分即为高对氯甲苯产品。
【详解】(1)制备重氮盐溶液时,用淀粉-KI试纸检验混合液,试纸变蓝,说明生成了,产生无色气体,该气体遇空气变红棕色,说明生成的气体为NO,可知亚硝酸根离子把碘离子氧化为碘单质,反应的化学方程式为。
(2)根据图示,仪器C的名称为直形冷凝管;A中玻璃管与空气连通,则A的作用为平衡气压。
(3)环己烷的密度小于水,用环己烷作萃取剂萃取分液时,先从下口放出水层,再从上口倒出有机层,将萃取所得有机层与粗产品合并,可以减少产物损耗,提高对氯甲苯的产率。
(4)直形冷凝管冷凝效果好,但是馏分沸点高于140 ℃时,直形冷凝管内外温差大,容易碎裂,应该换成空气冷凝管,故粗产品经干燥后,先用直形冷凝管蒸馏出低沸点杂质(环己烷),再控制温度在158~162 ℃改用空气冷凝管收集馏分。
(5)5.35 g对甲基苯胺的物质的量为 ,理论上生成对氯甲苯得物质的量为0.05mol,则对氯甲苯的产率为 。
17.(1) 球形干燥管 b
(2)苯二甲酸酐
(3)两者均为分子晶体,邻苯二甲酰亚胺能形成分子间氢键,使分子间作用力增大,熔点更高
(4) 趁热过滤,并用乙醇洗涤沉淀 减小邻苯二甲酸酐的溶解量,使分离更加完全,且乙醇易挥发,便于干燥
(5)a
(6) +NH3+3O2 +4H2O
【分析】由题给流程可知,装置甲中发生的反应为邻苯二甲酸酐与氨水在80~95℃的热水浴中发生取代反应生成邻氨甲酰苯甲酸,邻氨甲酰苯甲酸在加热条件下发生取代反应生成邻苯二甲酰亚胺,用于除去所得固体中的水分,除水所得固体经冷却,洗涤、抽滤烘干,进一步提纯得固体邻苯二甲酰亚胺,据此分析解题。
【详解】(1)由题干实验装置图可知,仪器A的名称为球形干燥管,实验中仪器A的作用为吸收尾气NH3,球形干燥管只能盛放固体,故其中盛装的试剂是五氧化二磷,故答案为:球形干燥管;b;
(2)由题干表格信息可知,邻苯二甲酸酐不溶于冷水,微溶于热水,稍溶于乙醇,可知步骤Ⅱ所得粗品中的杂质主要为邻苯二甲酸酐,故答案为:苯二甲酸酐;
(3)邻苯二甲酰亚胺可形成分子间氢键,使其分子间作用力增大,熔点更高,故答案为:两者均为分子晶体,邻苯二甲酰亚胺能形成分子间氢键,使分子间作用力增大,熔点更高;
(4)由题干表格信息可知,邻苯二甲酸酐不溶于冷水,微溶于热水,稍溶于乙醇,而邻苯二甲酰亚胺微溶于热水,易溶于乙醇,易溶于碱溶液,故Ⅲ.向白色粉末中加入适量乙醇,加热回流使固体恰好溶解,趁热过滤,并用乙醇洗涤沉淀,将滤液降温冷却,有白色晶体析出,抽滤、洗涤、烘干后得白色晶体,选择乙醇作为提纯溶剂的主要原因是减小邻苯二甲酸酐的溶解量,使分离更加完全,且乙醇易挥发,便于干燥,故答案为:趁热过滤,并用乙醇洗涤沉淀;减小邻苯二甲酸酐的溶解量,使分离更加完全,且乙醇易挥发,便于干燥;
(5)由题意可知,74.0g邻苯二甲酸酐制得59.2g邻苯二甲酰亚胺,则邻苯二甲酰亚胺的产率为×100%=89.37%,接近85%,故答案为:a;
(6)由题意可知,邻二甲苯与氨气、空气在加热条件下催化反应生成邻苯二甲酰亚胺和水,反应的化学方程式为:+NH3+3O2 +4H2O,故答案为:+NH3+3O2 +4H2O。
18.(1) 冷凝回流(减少苯胺和冰醋酸蒸出) N 防止苯胺被氧化 冰醋酸具有挥发性,温度高于,冰醋酸蒸出,降低了原料的利用率;温度低于,不利于蒸出水,影响了乙酰苯胺产率的提高
(2)c
(3)趁热过滤
(4)
【分析】根据题干信息,根据原理C6H5-NH2 + CH3COOHC6H5–NHCOCH3+ H2O制备乙酰苯胺,以苯胺和冰醋酸为原料,控温加热1h后趁热倒入冷水,析出晶体后抽滤、洗涤、干燥得到粗产品,洗涤时需注意温度越高,乙酰苯胺溶解度越大,且在碱性条件下易水解,可选用冰水洗涤,再重结晶得到产品,据此分析解答问题。
【详解】(1)①球形冷凝管的作用是冷凝回流(减少苯胺和冰醋酸蒸出),冷凝水下进上出,则进水口为N。
②根据题干信息,苯胺易被氧化,而锌粒可与酸反应生成氢气,形成氢气环境,从而防止苯胺被氧化,则加入锌粒还能起到的作用是防止苯胺被氧化。
③该制备方法的主要反应方程式C6H5-NH2 + CH3COOHC6H5–NHCOCH3+ H2O。
④制备过程中温度计控制示数在左右的原因是:已知冰醋酸具有挥发性,因此温度过高,冰醋酸蒸出,降低了反应物的利用率,但温度过低,不利于蒸出水,所以将温度控制在约105℃时。
(2)由于乙酰苯胺易溶于酒精,在水中温度越高,乙酰苯胺溶解度越大,且在碱性条件下易水解,故选用冰水洗涤,故选c。
(3)由表格数据可知,该晶体可通过冷却结晶获得。重结晶时,将粗产品溶于沸水中配成饱和溶液,再加入少量蒸馏水,加入活性炭脱色,接着加热煮沸,趁热过滤后冷却结晶,再过滤、洗涤、干燥得到最终产品,故答案为:趁热过滤。
(4)根据分析,制备乙酰苯胺的实验原理为C6H5-NH2 + CH3COOHC6H5–NHCOCH3+ H2O,以0.11mol的苯胺和0.26mol的冰醋酸为原料,可知冰醋酸过量,根据反应方程式可求得理论上制得的乙酰苯胺的物质的量为0.11mol,则质量为0.11mol×135g/mol=14.85g,则根据公式产率=可知,乙酰苯胺的产率为×100%≈67%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
