烯烃-高考化学考前专项练习试题(含解析)
文档属性
| 名称 | 烯烃-高考化学考前专项练习试题(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 773.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-13 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
烯烃
共18题,满分100分
题号 一 二 三 总分
得分
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请注意保持试卷整洁
一、单选题(共50分)
1.(本题5分)二氰乙炔在氧气中充分燃烧可达到4990℃,这是目前人类通过化学反应可达到的极限最高温度。下列有关二氰乙炔的说法不正确的是
A.该物质能发生加聚反应 B.分子中所有原子在一条直线上
C.该物质可能用于制作炸药 D.碳氮三键比碳碳三键键长长
2.(本题5分)丁香油酚的结构简式是 ,该物质不应有的化学性质是
①可以燃烧;②可以跟溴加成;③可以使酸性KMnO4溶液褪色;④可以跟NaHCO3 溶液反应;⑤可以跟NaOH溶液反应;⑥可以在碱性条件下水解
A.①③ B.③⑥ C.④⑤ D.④⑥
3.(本题5分)丙烯(CH2=CH—CH3)是合成聚丙烯塑料的化工原料,下列有关说法错误的是
A.丙烯合成聚丙烯属于加聚反应
B.聚丙烯的链节为—CH2—CH—CH3—
C.聚丙烯属于塑料类有机高分子材料
D.聚丙烯的相对分子质量为42n(n为聚合度)
4.(本题5分)下列有关有机物说法不正确的是( )
A.等质量的苯乙烯和聚苯乙烯燃烧耗氧量相同
B.四苯基乙烯( )中所有碳原子一定处于同一平面
C.1 mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3 mol、4 mol、1 mol
D.1molβ 紫罗兰酮( )与1molBr2发生加成反应可得3种产物
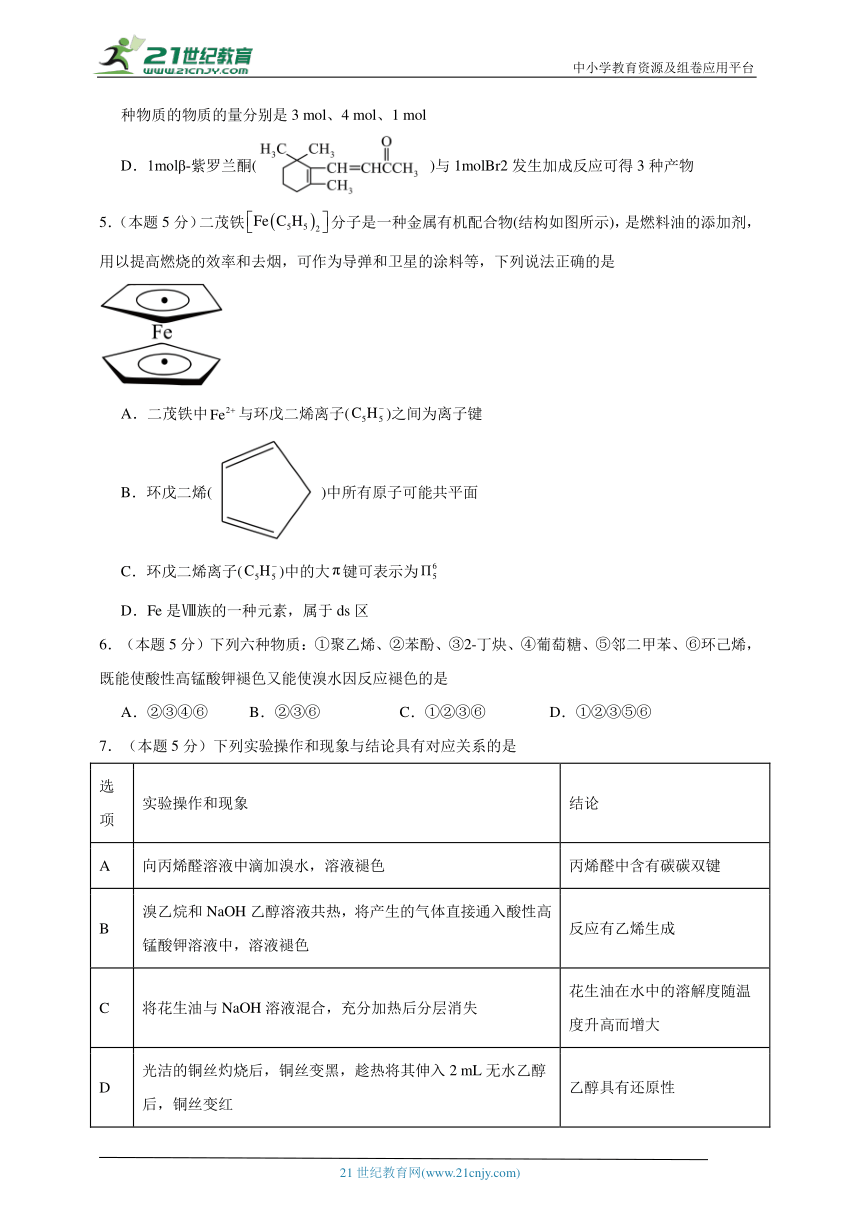
5.(本题5分)二茂铁分子是一种金属有机配合物(结构如图所示),是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等,下列说法正确的是
A.二茂铁中与环戊二烯离子()之间为离子键
B.环戊二烯( )中所有原子可能共平面
C.环戊二烯离子()中的大键可表示为
D.Fe是Ⅷ族的一种元素,属于ds区
6.(本题5分)下列六种物质:①聚乙烯、②苯酚、③2-丁炔、④葡萄糖、⑤邻二甲苯、⑥环己烯,既能使酸性高锰酸钾褪色又能使溴水因反应褪色的是
A.②③④⑥ B.②③⑥ C.①②③⑥ D.①②③⑤⑥
7.(本题5分)下列实验操作和现象与结论具有对应关系的是
选项 实验操作和现象 结论
A 向丙烯醛溶液中滴加溴水,溶液褪色 丙烯醛中含有碳碳双键
B 溴乙烷和NaOH乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中,溶液褪色 反应有乙烯生成
C 将花生油与NaOH溶液混合,充分加热后分层消失 花生油在水中的溶解度随温度升高而增大
D 光洁的铜丝灼烧后,铜丝变黑,趁热将其伸入2 mL无水乙醇后,铜丝变红 乙醇具有还原性
A.A B.B C.C D.D
8.(本题5分)某有机物的结构简式如图所示,关于该有机物,下列叙述不正确的是
A.一定条件下,能发生加聚反应
B.1mol该有机物与溴水发生反应,消耗Br2的物质的量为1mol
C.该有机物有三种官能团
D.该有机物苯环上的一个H被Cl取代,有3种产物
9.(本题5分)甲同学给分子式为C12H26的某烷烃命名为“2,4-二甲基-3,5-二乙基己烷”,乙同学认为甲同学命名错误,有关该烷烃的说法,你认为正确的是
A.该烷烃正确名称应为:2,4,5-三甲基-3-乙基庚烷
B.该烷烃分子中含有5个支链
C.该烷烃的一氯代物有10钟
D.该烷烃可以看成是11种不同类型的单烯烃与氢气加成后的产物
10.(本题5分)化学与生产、生活、科技等方面密切相关,下列有关说法正确的是
A.废弃的聚乙烯塑料属于可回收垃圾,能使溴水褪色
B.“鲲龙”水陆两栖飞机的燃料—“航空煤油”主要由烃的衍生物组成
C.“墨子号”卫星成功发射实现了光纤量子通信,生产光纤的原料为晶体硅
D.复方氯乙烷气雾剂可用于快速镇痛
二、判断题(共20分)
11.(本题4分)聚丙烯属于有机高分子化合物。(_______)
12.(本题4分)乙烯、聚乙烯都能使酸性高锰酸钾溶液褪色。(___)
13.(本题4分)能发生加成反应,一定条件下最多可与三倍物质的量的氢气加成。(____)
14.(本题4分)分子通式为CnH2n的烃一定属于烯烃。(___)
15.(本题4分)煤中含有芳香烃,可以通过干馏的方法得到芳香烃。(_______)
三、解答题(共30分)
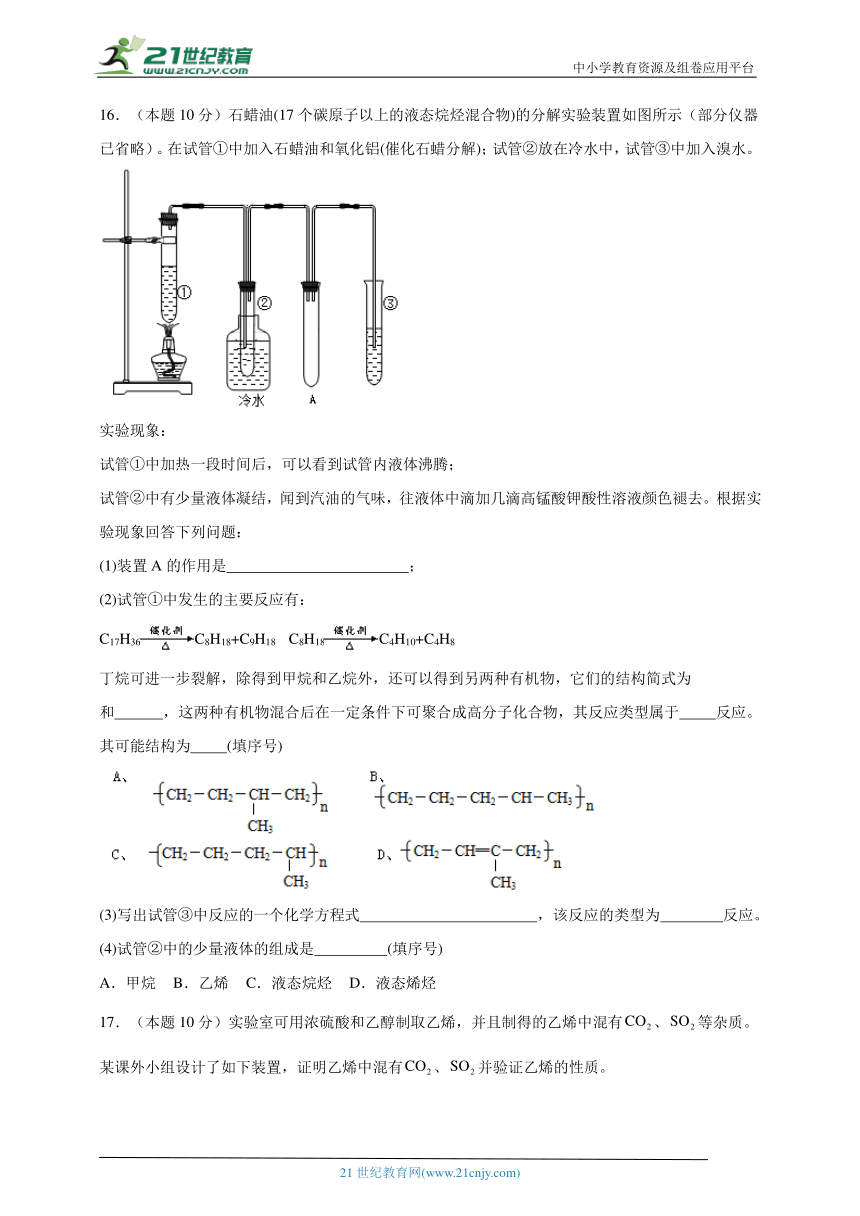
16.(本题10分)石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水。
实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。根据实验现象回答下列问题:
(1)装置A的作用是 ;
(2)试管①中发生的主要反应有:
C17H36C8H18+C9H18 C8H18C4H10+C4H8
丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为 和 ,这两种有机物混合后在一定条件下可聚合成高分子化合物,其反应类型属于 反应。其可能结构为 (填序号)
(3)写出试管③中反应的一个化学方程式 ,该反应的类型为 反应。
(4)试管②中的少量液体的组成是 (填序号)
A.甲烷 B.乙烯 C.液态烷烃 D.液态烯烃
17.(本题10分)实验室可用浓硫酸和乙醇制取乙烯,并且制得的乙烯中混有、等杂质。某课外小组设计了如下装置,证明乙烯中混有、并验证乙烯的性质。
回答下列问题∶
(1)若要检验所得气体含有可将混合气体直接通入 (填代号,下同)装置;若要检验混合气体中含有,可将气体干燥后通过 ,也可将混合气体先通过 再通过F,观察到F中的现象为 ,反应方程式为 。
(2)若将混合气体依次通过B、E、D、E,发现D前面的石灰水无明显变化、D后面的石灰水变浑浊。请用离子方程式表示D装置中的反应∶
(3)用上述装置,若要一次性将三种气体全部检验出来,则检验的先后顺序是 。(填序号)
a、、、 b、、、 c、、、
(4)已知某高分子化合物如下,试写出加聚生成该化合物的单体(结构简式) 。
(5)分子式为C8H10的芳香烃形成的一氯代物有 种同分异构体。
18.(本题10分)乙炔是一种重要的化工原料。
(1)实验室制乙炔的化学方程式为 ;用此法制取乙炔,应选择图中的 填选项字母)作为发生装置。
(2)乙炔可以用于合成聚氯乙烯,流程为:乙炔有机物X聚氯乙烯。
①的反应类型为 ;②的化学方程式为 。
参考答案:
1.D
【详解】A.二氰乙炔含不饱和键,故可发生加聚反应,A正确;
B.以乙炔为母体,可知所有原子在一条直线上,B正确;
C.由于该物质燃烧产生大量的热量,故可能产生热爆炸,从而用于制作炸药,C正确;
D.同为三键,氮原子半径小于碳原子半径,故碳氮三键比碳碳三键键长短,D错误;
故选D。
2.D
【详解】
3.B
【分析】丙烯合成聚丙烯()的反应类型为加聚反应,聚丙烯的链节为,聚合度为n。
【详解】A.丙烯合成聚丙烯的反应类型为加聚反应,A正确;
B.聚丙烯的链节为,B错误;
C.聚丙烯是有机高分子,属于塑料类有机高分子材料,C正确;
D.聚丙烯的链节为,共有n个,相对分子质量为42n,D正确;
故选B。
4.B
【详解】A. 苯乙烯和聚苯乙烯的最简式都是CH,故等质量的苯乙烯和聚苯乙烯燃烧耗氧量相同,故A正确;
B.单键可以旋转,故每个苯环碳原子与双键碳原子可能共平面,但所有碳原子不一定处于同一平面,故B错误;
C.分子内的酚羟基、醇羟基、羧基都能与Na反应,酚羟基、羧基都能与NaOH反应,且酯基水解后生成的酚羟基、羧基均消耗NaOH,只有羧基与NaHCO3溶液反应,故C正确;
D. 与Br2起加成反应,可以发生1,2-加成反应,也可能发生1,4-加成反应,所以加1mol β-紫罗兰酮 与1mol Br2发生加成反应可得到3种不同产物,故D正确。
故答案选B。
5.C
【详解】A.由图可知,二茂铁中具有空轨道的亚铁离子与具有孤对电子的环戊二烯离子形成配位键,故A错误;
B.由结构简式可知,环戊二烯分子中含有空间构型为四面体形的饱和碳原子,分子中所有原子不可能共平面,故B错误;
C.环戊二烯离子中碳原子的杂化方式都为sp2,未杂化的p电子形成的大π键,故C正确;
D.铁元素位于元素周期表第四周期Ⅷ族,基态铁原子的价电子排布式为3d64s2,则铁元素位于d区,故D错误;
故选C。
6.B
【详解】①聚乙烯不含有双键,聚乙烯与高锰酸钾和溴水均不反应,错误;
②苯酚可以被高锰酸钾氧化,可与溴水生成三溴苯酚而褪色,正确;
③2-丁炔含有的碳碳三键既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,正确;
④葡萄糖分子中含有醛基,能使酸性高锰酸钾褪色,但是不能使溴水反应而褪色,错误;
⑤邻二甲苯与高锰酸钾反应使酸性高锰酸钾溶液褪色,可使溴水发生萃取而褪色,但与溴水不反应,错误;
⑥环己烯含有的碳碳双键既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,正确;
故选B。
7.D
【详解】A.碳碳双键、醛基都能与溴水反应,向丙烯醛溶液中滴加溴水,溶液褪色,碳碳双键和醛基均能使溴水褪色,不能说明丙烯醛中含有碳碳双键,A项不符合题意;
B.溴乙烷和NaOH乙醇溶液共热,产生的气体中含有乙醇蒸气,乙醇、乙烯都能使酸性高锰酸钾溶液褪色,高锰酸钾溶液褪色不能说明有乙烯生成,B项不符合题意;
C.将花生油与NaOH溶液混合,充分加热后分层消失,是由于油脂在碱性条件下水解生成了易溶于水的高级脂肪酸钠和甘油,C项不符合题意;
D.光洁的铜丝灼烧后,铜丝变黑,趁热将其伸入2 mL无水乙醇后,铜丝变红说明乙醇具有还原性,将CuO还原为Cu,D符合题意;
故选D。
8.C
【详解】A.该有机物中含有碳碳双键,故在一定条件下能发生加聚反应,A正确 ;
B.1个该有机物分子中含有1个碳碳双键,故1mol该有机物与溴水发生反应,消耗Br2的物质的量为1mol,B正确;
C.该有机物只含有碳碳双键和氯原子两种官能团,C错误;
D.该有机物苯环上的一个H被Cl取代有邻、间、对三种位置关系,有3种产物,D正确;
故选C。
9.A
【详解】A.根据甲同学的命名可判断该烷烃的结构简式为:,其正确名称应为2,4,5-三甲基-3-乙基庚烷,故A项正确;
B.分子中有4个支链,B项错;
C.该烷烃分子中共含11种类型的氢原子,因此一氯代物有11种,C项错误;
D.该烷烃中相邻碳原子上都有氢原子的可看成是烯烃加成后的产物,去氢之后还原的烯烃共有10种,故D项错误。
答案选A。
10.D
【详解】A.聚乙烯分子中不含有碳碳双键,不能与溴水发生加成反应使溴水褪色,故A错误;
B.航空煤油是由碳原子个数较多的烃类化合物组成的混合物,故B错误;
C.光导纤维的主要成分是二氧化硅,所以生产光纤的原料为二氧化硅,故C错误;
D.液态氯乙烷汽化时吸收大量热,有冷冻麻醉作用,可以迅速产生止痛的效果,故D正确;
答案选D。
11.正确
【详解】相对分子质量在10000以上的为高分子,可选用缩聚反应、加聚反应得到有机高分子化合物,聚丙烯是由丙烯通过加聚反应而得的有机高分子化合物,答案正确;
12.错误
【详解】乙烯分子中含有碳碳双键,乙烯能使酸性高锰酸钾溶液褪色;聚乙烯分子中不含碳碳双键,聚乙烯不能使酸性高锰酸钾溶液褪色;故上述说法错误。
13.错误
【详解】在一定条件下,苯环和碳碳双键都可与氢气发生加成反应,1 mol该物质含有1 mol苯环和1 mol碳碳双键,1 mol该有机物最多可与4 mol氢气加成,故错误。
14.错误
【详解】通式为CnH2n的有机物属于烯烃或环烷烃,不一定是烯烃,故错误。
15.错误
【详解】煤是由有机物和少量的无机物组成的复杂混合物,煤干馏是将煤隔绝空气加高温使之分解,得到焦炭、煤焦油、煤气,煤的干馏属于化学变化,煤中不含有芳香烃。答案:错误。
16. 防止试管③中的液体倒吸到试管②中 CH2=CH2 CH3CH=CH2 加聚 AC CH2=CH2+Br2→CH2BrCH2Br(CH3CH=CH2+Br2→CH3CHBrCH2Br) 加成 CD
【详解】(1)CH2=CH-CH3和CH2=CH2能与溴水发生加成反应,使气压降低,发生倒吸,装置A的作用是防止试管③中液体倒吸回试管②中;
(2)丁烷的两种裂解方式为:C4H10→CH4+CH2=CHCH3,C4H10→C2H6+CH2=CH2,如果是乙烯和丙烯之间发生加聚反应,由于碳原子之间的连接顺序可以有和两种结构简式,分别为A、C结构,故答案为AC;
(3)CH2=CH-CH3和CH2=CH2能与溴水发生加成反应,反应方程式为;
(4)石蜡在催化剂氧化铝存在下,加热可以裂化为短链的气态饱和烃和不饱和烃,还有液态的饱和烃和不饱和烃,故答案为CD。
17. C G B 溴水橙红色褪去 CH2=CH2+Br2BrCH2CH2Br 5CH2=CH2+12+36H+=10CO2+12Mn2++28H2O a CH2=CH-CH=CH2、CH2=CHCH3和 14
【分析】本实验的目的是用实验的方法来检验所得产物中含有的杂质气体SO2、CO2,并验证乙烯的性质,制备乙烯发生的反应为:CH3CH2OHCH2=CH2↑+H2O,B可以用于除去乙烯中的SO2、CO2,C可以用于检验SO2,D可以用于检验乙烯或SO2,E可用于检验CO2或SO2,F可用于检验乙烯或SO2,G可用于检验乙烯,据此分析解题。
【详解】(1)由于乙烯和SO2均能使酸性高锰酸钾溶液和溴水褪色,只有SO2能使品红溶液褪色,故若要检验所得气体含有可将混合气体直接通入C装置;若要检验混合气体中含有,由于此时含有SO2,乙烯和SO2均能使酸性高锰酸钾溶液和溴水褪色,但SO2不与溴的四氯化碳溶液反应,为了检验乙烯可将混合气体干燥后通过溴的四氯化碳溶液;也可先除去SO2再检验,即也可将混合气体先通过B再通过F,观察到F中的现象为溴水橙红色褪去,即乙烯和溴发生加成反应,故反应方程式为CH2=CH2+Br2BrCH2CH2Br,故答案为:C;G;B;溴水橙红色褪去;CH2=CH2+Br2BrCH2CH2Br;
(2)若将混合气体依次通过B、E、D、E,发现D前面的石灰水无明显变化、D后面的石灰水变浑浊,D前面的石灰水无明显变化说明乙醇碳化生成的二氧化碳和二氧化硫都被氢氧化钠吸收,D后面的石灰水变浑浊,说明混合气体通入到酸性的高锰酸钾中发生反应产生了能够使澄清石灰水变浑浊的气体,而乙烯含有碳碳双键具有还原性,能被酸性高锰酸钾溶液氧化成CO2,D装置中反应的离子方程式为:5CH2=CH2+12+36H+=10CO2+12Mn2++28H2O,故答案为:5CH2=CH2+12+36H+=10CO2+12Mn2++28H2O;
(3) 若要一次性将三种气体全部检验出来,可以将混合气体干燥后通入盛有溴的四氯化碳的洗气瓶,若洗气瓶褪色,则证明乙烯存在;然后通入品红溶液,若品红褪色,则证明二氧化硫存在;二氧化硫、二氧化碳都能使澄清石灰水变浑浊,所以应先利用酸性高锰酸钾除去二氧化硫,然后通入澄清石灰水,若石灰水变浑浊,则证明存在二氧化碳,
故答案为:a;
(4)根据加聚产物找单体的方法可知,加聚生成高分子化合物
的单体为:CH2=CH-CH=CH2、CH2=CHCH3和,故答案为:CH2=CH-CH=CH2、CH2=CHCH3和;
(5)分子式为C8H10的芳香烃的同分异构体有:乙苯、邻二甲苯、间二甲苯和对二甲苯四种,而每一种的一氯代物又分别有:5种、3种、4种和2种,故一共形成的一氯代物有5+3+4+2=14种同分异构体,故答案为:14。
18. CaC2+2H2O→Ca(OH)2+C2H2↑ B 加成反应 nCH2=CHCl
【分析】实验室用电石与水的反应制备乙炔,反应的化学方程式:CaC2+2H2O → Ca(OH)2+C2H2↑,乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯发生加聚反应生成聚氯乙烯,据此分析解答。
【详解】(1)实验室用电石与水的反应制备乙炔,反应的化学方程式:CaC2+2H2O → Ca(OH)2+C2H2↑,电石与水的反应很剧烈,且放出大量热,不宜用启普发生器或简易的启普发生器作发生装置,应该用分液漏斗将饱和食盐水缓慢滴加到电石上,以控制反应速率,故答案选B。
(2)乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯发生加聚反应生成聚氯乙烯,则①的反应类型为加成反应,②的化学方程式为:nCH2=CHCl。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
烯烃
共18题,满分100分
题号 一 二 三 总分
得分
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请注意保持试卷整洁
一、单选题(共50分)
1.(本题5分)二氰乙炔在氧气中充分燃烧可达到4990℃,这是目前人类通过化学反应可达到的极限最高温度。下列有关二氰乙炔的说法不正确的是
A.该物质能发生加聚反应 B.分子中所有原子在一条直线上
C.该物质可能用于制作炸药 D.碳氮三键比碳碳三键键长长
2.(本题5分)丁香油酚的结构简式是 ,该物质不应有的化学性质是
①可以燃烧;②可以跟溴加成;③可以使酸性KMnO4溶液褪色;④可以跟NaHCO3 溶液反应;⑤可以跟NaOH溶液反应;⑥可以在碱性条件下水解
A.①③ B.③⑥ C.④⑤ D.④⑥
3.(本题5分)丙烯(CH2=CH—CH3)是合成聚丙烯塑料的化工原料,下列有关说法错误的是
A.丙烯合成聚丙烯属于加聚反应
B.聚丙烯的链节为—CH2—CH—CH3—
C.聚丙烯属于塑料类有机高分子材料
D.聚丙烯的相对分子质量为42n(n为聚合度)
4.(本题5分)下列有关有机物说法不正确的是( )
A.等质量的苯乙烯和聚苯乙烯燃烧耗氧量相同
B.四苯基乙烯( )中所有碳原子一定处于同一平面
C.1 mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3 mol、4 mol、1 mol
D.1molβ 紫罗兰酮( )与1molBr2发生加成反应可得3种产物
5.(本题5分)二茂铁分子是一种金属有机配合物(结构如图所示),是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等,下列说法正确的是
A.二茂铁中与环戊二烯离子()之间为离子键
B.环戊二烯( )中所有原子可能共平面
C.环戊二烯离子()中的大键可表示为
D.Fe是Ⅷ族的一种元素,属于ds区
6.(本题5分)下列六种物质:①聚乙烯、②苯酚、③2-丁炔、④葡萄糖、⑤邻二甲苯、⑥环己烯,既能使酸性高锰酸钾褪色又能使溴水因反应褪色的是
A.②③④⑥ B.②③⑥ C.①②③⑥ D.①②③⑤⑥
7.(本题5分)下列实验操作和现象与结论具有对应关系的是
选项 实验操作和现象 结论
A 向丙烯醛溶液中滴加溴水,溶液褪色 丙烯醛中含有碳碳双键
B 溴乙烷和NaOH乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中,溶液褪色 反应有乙烯生成
C 将花生油与NaOH溶液混合,充分加热后分层消失 花生油在水中的溶解度随温度升高而增大
D 光洁的铜丝灼烧后,铜丝变黑,趁热将其伸入2 mL无水乙醇后,铜丝变红 乙醇具有还原性
A.A B.B C.C D.D
8.(本题5分)某有机物的结构简式如图所示,关于该有机物,下列叙述不正确的是
A.一定条件下,能发生加聚反应
B.1mol该有机物与溴水发生反应,消耗Br2的物质的量为1mol
C.该有机物有三种官能团
D.该有机物苯环上的一个H被Cl取代,有3种产物
9.(本题5分)甲同学给分子式为C12H26的某烷烃命名为“2,4-二甲基-3,5-二乙基己烷”,乙同学认为甲同学命名错误,有关该烷烃的说法,你认为正确的是
A.该烷烃正确名称应为:2,4,5-三甲基-3-乙基庚烷
B.该烷烃分子中含有5个支链
C.该烷烃的一氯代物有10钟
D.该烷烃可以看成是11种不同类型的单烯烃与氢气加成后的产物
10.(本题5分)化学与生产、生活、科技等方面密切相关,下列有关说法正确的是
A.废弃的聚乙烯塑料属于可回收垃圾,能使溴水褪色
B.“鲲龙”水陆两栖飞机的燃料—“航空煤油”主要由烃的衍生物组成
C.“墨子号”卫星成功发射实现了光纤量子通信,生产光纤的原料为晶体硅
D.复方氯乙烷气雾剂可用于快速镇痛
二、判断题(共20分)
11.(本题4分)聚丙烯属于有机高分子化合物。(_______)
12.(本题4分)乙烯、聚乙烯都能使酸性高锰酸钾溶液褪色。(___)
13.(本题4分)能发生加成反应,一定条件下最多可与三倍物质的量的氢气加成。(____)
14.(本题4分)分子通式为CnH2n的烃一定属于烯烃。(___)
15.(本题4分)煤中含有芳香烃,可以通过干馏的方法得到芳香烃。(_______)
三、解答题(共30分)
16.(本题10分)石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水。
实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。根据实验现象回答下列问题:
(1)装置A的作用是 ;
(2)试管①中发生的主要反应有:
C17H36C8H18+C9H18 C8H18C4H10+C4H8
丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为 和 ,这两种有机物混合后在一定条件下可聚合成高分子化合物,其反应类型属于 反应。其可能结构为 (填序号)
(3)写出试管③中反应的一个化学方程式 ,该反应的类型为 反应。
(4)试管②中的少量液体的组成是 (填序号)
A.甲烷 B.乙烯 C.液态烷烃 D.液态烯烃
17.(本题10分)实验室可用浓硫酸和乙醇制取乙烯,并且制得的乙烯中混有、等杂质。某课外小组设计了如下装置,证明乙烯中混有、并验证乙烯的性质。
回答下列问题∶
(1)若要检验所得气体含有可将混合气体直接通入 (填代号,下同)装置;若要检验混合气体中含有,可将气体干燥后通过 ,也可将混合气体先通过 再通过F,观察到F中的现象为 ,反应方程式为 。
(2)若将混合气体依次通过B、E、D、E,发现D前面的石灰水无明显变化、D后面的石灰水变浑浊。请用离子方程式表示D装置中的反应∶
(3)用上述装置,若要一次性将三种气体全部检验出来,则检验的先后顺序是 。(填序号)
a、、、 b、、、 c、、、
(4)已知某高分子化合物如下,试写出加聚生成该化合物的单体(结构简式) 。
(5)分子式为C8H10的芳香烃形成的一氯代物有 种同分异构体。
18.(本题10分)乙炔是一种重要的化工原料。
(1)实验室制乙炔的化学方程式为 ;用此法制取乙炔,应选择图中的 填选项字母)作为发生装置。
(2)乙炔可以用于合成聚氯乙烯,流程为:乙炔有机物X聚氯乙烯。
①的反应类型为 ;②的化学方程式为 。
参考答案:
1.D
【详解】A.二氰乙炔含不饱和键,故可发生加聚反应,A正确;
B.以乙炔为母体,可知所有原子在一条直线上,B正确;
C.由于该物质燃烧产生大量的热量,故可能产生热爆炸,从而用于制作炸药,C正确;
D.同为三键,氮原子半径小于碳原子半径,故碳氮三键比碳碳三键键长短,D错误;
故选D。
2.D
【详解】
3.B
【分析】丙烯合成聚丙烯()的反应类型为加聚反应,聚丙烯的链节为,聚合度为n。
【详解】A.丙烯合成聚丙烯的反应类型为加聚反应,A正确;
B.聚丙烯的链节为,B错误;
C.聚丙烯是有机高分子,属于塑料类有机高分子材料,C正确;
D.聚丙烯的链节为,共有n个,相对分子质量为42n,D正确;
故选B。
4.B
【详解】A. 苯乙烯和聚苯乙烯的最简式都是CH,故等质量的苯乙烯和聚苯乙烯燃烧耗氧量相同,故A正确;
B.单键可以旋转,故每个苯环碳原子与双键碳原子可能共平面,但所有碳原子不一定处于同一平面,故B错误;
C.分子内的酚羟基、醇羟基、羧基都能与Na反应,酚羟基、羧基都能与NaOH反应,且酯基水解后生成的酚羟基、羧基均消耗NaOH,只有羧基与NaHCO3溶液反应,故C正确;
D. 与Br2起加成反应,可以发生1,2-加成反应,也可能发生1,4-加成反应,所以加1mol β-紫罗兰酮 与1mol Br2发生加成反应可得到3种不同产物,故D正确。
故答案选B。
5.C
【详解】A.由图可知,二茂铁中具有空轨道的亚铁离子与具有孤对电子的环戊二烯离子形成配位键,故A错误;
B.由结构简式可知,环戊二烯分子中含有空间构型为四面体形的饱和碳原子,分子中所有原子不可能共平面,故B错误;
C.环戊二烯离子中碳原子的杂化方式都为sp2,未杂化的p电子形成的大π键,故C正确;
D.铁元素位于元素周期表第四周期Ⅷ族,基态铁原子的价电子排布式为3d64s2,则铁元素位于d区,故D错误;
故选C。
6.B
【详解】①聚乙烯不含有双键,聚乙烯与高锰酸钾和溴水均不反应,错误;
②苯酚可以被高锰酸钾氧化,可与溴水生成三溴苯酚而褪色,正确;
③2-丁炔含有的碳碳三键既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,正确;
④葡萄糖分子中含有醛基,能使酸性高锰酸钾褪色,但是不能使溴水反应而褪色,错误;
⑤邻二甲苯与高锰酸钾反应使酸性高锰酸钾溶液褪色,可使溴水发生萃取而褪色,但与溴水不反应,错误;
⑥环己烯含有的碳碳双键既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,正确;
故选B。
7.D
【详解】A.碳碳双键、醛基都能与溴水反应,向丙烯醛溶液中滴加溴水,溶液褪色,碳碳双键和醛基均能使溴水褪色,不能说明丙烯醛中含有碳碳双键,A项不符合题意;
B.溴乙烷和NaOH乙醇溶液共热,产生的气体中含有乙醇蒸气,乙醇、乙烯都能使酸性高锰酸钾溶液褪色,高锰酸钾溶液褪色不能说明有乙烯生成,B项不符合题意;
C.将花生油与NaOH溶液混合,充分加热后分层消失,是由于油脂在碱性条件下水解生成了易溶于水的高级脂肪酸钠和甘油,C项不符合题意;
D.光洁的铜丝灼烧后,铜丝变黑,趁热将其伸入2 mL无水乙醇后,铜丝变红说明乙醇具有还原性,将CuO还原为Cu,D符合题意;
故选D。
8.C
【详解】A.该有机物中含有碳碳双键,故在一定条件下能发生加聚反应,A正确 ;
B.1个该有机物分子中含有1个碳碳双键,故1mol该有机物与溴水发生反应,消耗Br2的物质的量为1mol,B正确;
C.该有机物只含有碳碳双键和氯原子两种官能团,C错误;
D.该有机物苯环上的一个H被Cl取代有邻、间、对三种位置关系,有3种产物,D正确;
故选C。
9.A
【详解】A.根据甲同学的命名可判断该烷烃的结构简式为:,其正确名称应为2,4,5-三甲基-3-乙基庚烷,故A项正确;
B.分子中有4个支链,B项错;
C.该烷烃分子中共含11种类型的氢原子,因此一氯代物有11种,C项错误;
D.该烷烃中相邻碳原子上都有氢原子的可看成是烯烃加成后的产物,去氢之后还原的烯烃共有10种,故D项错误。
答案选A。
10.D
【详解】A.聚乙烯分子中不含有碳碳双键,不能与溴水发生加成反应使溴水褪色,故A错误;
B.航空煤油是由碳原子个数较多的烃类化合物组成的混合物,故B错误;
C.光导纤维的主要成分是二氧化硅,所以生产光纤的原料为二氧化硅,故C错误;
D.液态氯乙烷汽化时吸收大量热,有冷冻麻醉作用,可以迅速产生止痛的效果,故D正确;
答案选D。
11.正确
【详解】相对分子质量在10000以上的为高分子,可选用缩聚反应、加聚反应得到有机高分子化合物,聚丙烯是由丙烯通过加聚反应而得的有机高分子化合物,答案正确;
12.错误
【详解】乙烯分子中含有碳碳双键,乙烯能使酸性高锰酸钾溶液褪色;聚乙烯分子中不含碳碳双键,聚乙烯不能使酸性高锰酸钾溶液褪色;故上述说法错误。
13.错误
【详解】在一定条件下,苯环和碳碳双键都可与氢气发生加成反应,1 mol该物质含有1 mol苯环和1 mol碳碳双键,1 mol该有机物最多可与4 mol氢气加成,故错误。
14.错误
【详解】通式为CnH2n的有机物属于烯烃或环烷烃,不一定是烯烃,故错误。
15.错误
【详解】煤是由有机物和少量的无机物组成的复杂混合物,煤干馏是将煤隔绝空气加高温使之分解,得到焦炭、煤焦油、煤气,煤的干馏属于化学变化,煤中不含有芳香烃。答案:错误。
16. 防止试管③中的液体倒吸到试管②中 CH2=CH2 CH3CH=CH2 加聚 AC CH2=CH2+Br2→CH2BrCH2Br(CH3CH=CH2+Br2→CH3CHBrCH2Br) 加成 CD
【详解】(1)CH2=CH-CH3和CH2=CH2能与溴水发生加成反应,使气压降低,发生倒吸,装置A的作用是防止试管③中液体倒吸回试管②中;
(2)丁烷的两种裂解方式为:C4H10→CH4+CH2=CHCH3,C4H10→C2H6+CH2=CH2,如果是乙烯和丙烯之间发生加聚反应,由于碳原子之间的连接顺序可以有和两种结构简式,分别为A、C结构,故答案为AC;
(3)CH2=CH-CH3和CH2=CH2能与溴水发生加成反应,反应方程式为;
(4)石蜡在催化剂氧化铝存在下,加热可以裂化为短链的气态饱和烃和不饱和烃,还有液态的饱和烃和不饱和烃,故答案为CD。
17. C G B 溴水橙红色褪去 CH2=CH2+Br2BrCH2CH2Br 5CH2=CH2+12+36H+=10CO2+12Mn2++28H2O a CH2=CH-CH=CH2、CH2=CHCH3和 14
【分析】本实验的目的是用实验的方法来检验所得产物中含有的杂质气体SO2、CO2,并验证乙烯的性质,制备乙烯发生的反应为:CH3CH2OHCH2=CH2↑+H2O,B可以用于除去乙烯中的SO2、CO2,C可以用于检验SO2,D可以用于检验乙烯或SO2,E可用于检验CO2或SO2,F可用于检验乙烯或SO2,G可用于检验乙烯,据此分析解题。
【详解】(1)由于乙烯和SO2均能使酸性高锰酸钾溶液和溴水褪色,只有SO2能使品红溶液褪色,故若要检验所得气体含有可将混合气体直接通入C装置;若要检验混合气体中含有,由于此时含有SO2,乙烯和SO2均能使酸性高锰酸钾溶液和溴水褪色,但SO2不与溴的四氯化碳溶液反应,为了检验乙烯可将混合气体干燥后通过溴的四氯化碳溶液;也可先除去SO2再检验,即也可将混合气体先通过B再通过F,观察到F中的现象为溴水橙红色褪去,即乙烯和溴发生加成反应,故反应方程式为CH2=CH2+Br2BrCH2CH2Br,故答案为:C;G;B;溴水橙红色褪去;CH2=CH2+Br2BrCH2CH2Br;
(2)若将混合气体依次通过B、E、D、E,发现D前面的石灰水无明显变化、D后面的石灰水变浑浊,D前面的石灰水无明显变化说明乙醇碳化生成的二氧化碳和二氧化硫都被氢氧化钠吸收,D后面的石灰水变浑浊,说明混合气体通入到酸性的高锰酸钾中发生反应产生了能够使澄清石灰水变浑浊的气体,而乙烯含有碳碳双键具有还原性,能被酸性高锰酸钾溶液氧化成CO2,D装置中反应的离子方程式为:5CH2=CH2+12+36H+=10CO2+12Mn2++28H2O,故答案为:5CH2=CH2+12+36H+=10CO2+12Mn2++28H2O;
(3) 若要一次性将三种气体全部检验出来,可以将混合气体干燥后通入盛有溴的四氯化碳的洗气瓶,若洗气瓶褪色,则证明乙烯存在;然后通入品红溶液,若品红褪色,则证明二氧化硫存在;二氧化硫、二氧化碳都能使澄清石灰水变浑浊,所以应先利用酸性高锰酸钾除去二氧化硫,然后通入澄清石灰水,若石灰水变浑浊,则证明存在二氧化碳,
故答案为:a;
(4)根据加聚产物找单体的方法可知,加聚生成高分子化合物
的单体为:CH2=CH-CH=CH2、CH2=CHCH3和,故答案为:CH2=CH-CH=CH2、CH2=CHCH3和;
(5)分子式为C8H10的芳香烃的同分异构体有:乙苯、邻二甲苯、间二甲苯和对二甲苯四种,而每一种的一氯代物又分别有:5种、3种、4种和2种,故一共形成的一氯代物有5+3+4+2=14种同分异构体,故答案为:14。
18. CaC2+2H2O→Ca(OH)2+C2H2↑ B 加成反应 nCH2=CHCl
【分析】实验室用电石与水的反应制备乙炔,反应的化学方程式:CaC2+2H2O → Ca(OH)2+C2H2↑,乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯发生加聚反应生成聚氯乙烯,据此分析解答。
【详解】(1)实验室用电石与水的反应制备乙炔,反应的化学方程式:CaC2+2H2O → Ca(OH)2+C2H2↑,电石与水的反应很剧烈,且放出大量热,不宜用启普发生器或简易的启普发生器作发生装置,应该用分液漏斗将饱和食盐水缓慢滴加到电石上,以控制反应速率,故答案选B。
(2)乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯发生加聚反应生成聚氯乙烯,则①的反应类型为加成反应,②的化学方程式为:nCH2=CHCl。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
