四川省成都市树德中学2023-2024学年高二下学期期中考试 化学(PDF版含答案)
文档属性
| 名称 | 四川省成都市树德中学2023-2024学年高二下学期期中考试 化学(PDF版含答案) |
|
|
| 格式 | |||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-13 00:00:00 | ||
图片预览

文档简介
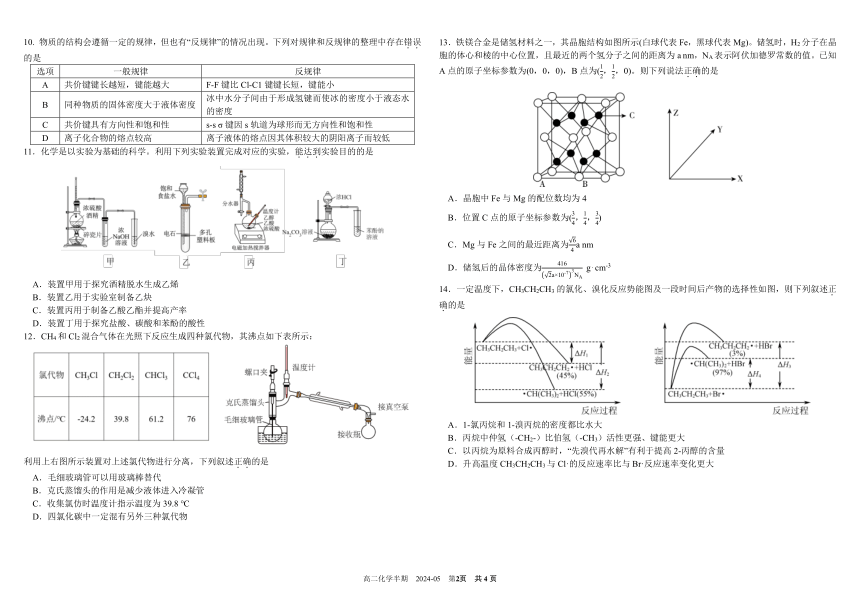
树德中学高 2022 级高二下学期半期考试化学试题 A.装置甲用于分离苯和溴苯
B.装置乙用于分离装有 C60 的“杯酚”和溶解了 C70 的甲苯
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Fe 56 Zn 65 C.装置丙用于用浓 KI 溶液去除 CCl4 中的 I2
第 I 卷(选择题) D.装置丁用于重结晶法提纯苯甲酸
一、选择题:本题共 14 小题,每小题 3 分,共 42 分。 6.10-羟基喜树碱具有抗癌作用,其结构简式如图。下列有关该化合物的
1.生活与化学密切相关。下列关于生活中的化学描述错.误.的是 说法错.误.的是
A.壁虎在天花板上爬行自如——壁虎的脚与墙体之间存在范德华力 A.有三种含氧官能团,分别为羟基、酯基、羰基
B.氯乙烷用于运动中的急性损伤——氯乙烷沸点较低而易汽化 B.可与 FeCl3溶液发生显色反应
C.氧炔焰用于焊接或切割金属——乙炔燃烧大量放热 C.该物质只有 1 个手性碳原子
D.液晶材料用于电视的显示器——液晶属于液态 D.1 mol Na 和足量该物质反应可生成标准状况下 11.2 L H2
2.化学符号的正确表达是“化学人”交流的基础。下列相关化学用语表述正.确.的是 7.下列有机物命名错.误.的是
A.只含有一种等效氢的 C5H12,可命名为 2,2—二甲基丙烷
A.醛基的电子式: B.基态氧原子最高能级的电子排布式:2p 22p 1 1x y 2pz
B.所有碳原子都在同一条直线上的 C4H6,可命名为 2—丁炔
C.所有碳原子位于同一个平面的 C6H12,可命名为 2,3—二甲基—2—丁烯
C.1-丁烯的实验式:CnH2n D.镁原子最外层电子的电子云轮廓图: D.分子式为 C9H12 的芳香烃,若苯环上的一氯代物只有一种,可命名为 2,4,6—三甲苯
8.下列有机合成路线设计合.理.的是
3.教材插图往往承载着重要的教学信息。下列有关教材插图的说法正.确.的是
A.
B.
Cl 浓H
C.CH =CH-CH=CH 2→CH ClCHClCH=CH 2
SO
42 2 2 2 →CH2 =CClCH=CH △ 2
A.图甲:环己烷常以如图所示的“船式”结构存在,是因为“船式”结构更稳定
B.图乙:金刚石以共价键形成三维骨架结构,是金刚石易锤击的主要原因 D.
C.图丙:一些高分子材料如聚乙炔能导电的原因和石墨能导电的原因不同
D.图丁:苯由于形成大 π 键而使苯中无独立的碳碳单键和双键,且共 6 个原子共平面 9.短周期元素 R、X、Y、Z 均属于第三周期主族元素,它们的最高价氧化物分别与水反应可得四种溶液,
4.设 NA为阿伏伽德罗常数的值,下列说法错.误.的是 浓度均为 0.01 mol/L 的上述四种溶液的 pH 与对应元素原子半径的关系如图所示。下列说法错.误.的是
A.标准状况下,22.4 L O3 含有的非极性 σ 键的数目为 2 NA
B.1 mol [Cu(H2O)4]2+中含有的键合电子数为 24 NA
C.1 mol 碳正离子( +CH3)含有的质子数为 9 NA
D.14 g 乙烯和丙烯的混合气体中含有 C-H σ 键的数目为 2 NA
5.分离提纯是开展物质的组成、性质等研究的基础。下列有关装置及其用途错.误.的是
A.同周期中第一电离能大于 Z 元素的有 3 种
B.X 和 Y 形成的化合物中 X 的杂化方式不一定为 sp3 杂化
C.Z 和 R 组成的化合物 R2Z8 中,含有离子键和非极性共价键
D.X 元素形成的正四面体结构的物质中,键角为 109°28′
高二化学半期 2024-05 第1页 共 4 页
10. 物质的结构会遵循一定的规律,但也有“反规律”的情况出现。下列对规律和反规律的整理中存在错.误. 13.铁镁合金是储氢材料之一,其晶胞结构如图所示(白球代表 Fe,黑球代表 Mg)。储氢时,H2 分子在晶
的是 胞的体心和棱的中心位置,且最近的两个氢分子之间的距离为 a nm,NA表示阿伏加德罗常数的值。已知
1 1
选项 一般规律 反规律 A 点的原子坐标参数为(0,0,0),B 点为( , ,0)。则下列说法正确的是
2 2 ..
A 共价键键长越短,键能越大 F-F 键比 Cl-C1 键键长短,键能小
冰中水分子间由于形成氢键而使冰的密度小于液态水
B 同种物质的固体密度大于液体密度
的密度
C 共价键具有方向性和饱和性 s-s σ 键因 s 轨道为球形而无方向性和饱和性
D 离子化合物的熔点较高 离子液体的熔点因其体积较大的阴阳离子而较低
11.化学是以实验为基础的科学。利用下列实验装置完成对应的实验,能.达.到.实验目的的是
A.晶胞中 Fe 与 Mg 的配位数均为 4
3 1 3
B.位置 C 点的原子坐标参数为( , , )
4 4 4
√6
C.Mg 与 Fe 之间的最近距离为 a nm
4
416
D.储氢后的晶体密度为 g cm-3
( -7
3
√2a×10 ) NA
A.装置甲用于探究酒精脱水生成乙烯
14.一定温度下,CH3CH2CH3 的氯化、溴化反应势能图及一段时间后产物的选择性如图,则下列叙述正.
B.装置乙用于实验室制备乙炔
确的是
C.装置丙用于制备乙酸乙酯并提高产率 .
D.装置丁用于探究盐酸、碳酸和苯酚的酸性
12.CH4 和 Cl2 混合气体在光照下反应生成四种氯代物,其沸点如下表所示:
A.1-氯丙烷和 1-溴丙烷的密度都比水大
B.丙烷中仲氢(-CH2-)比伯氢(-CH3)活性更强、键能更大
C.以丙烷为原料合成丙醇时,“先溴代再水解”有利于提高 2-丙醇的含量
利用上右图所示装置对上述氯代物进行分离,下列叙述正.确.的是 D.升高温度 CH3CH2CH3与 Cl·的反应速率比与 Br·反应速率变化更大
A.毛细玻璃管可以用玻璃棒替代
B.克氏蒸馏头的作用是减少液体进入冷凝管
C.收集氯仿时温度计指示温度为 39.8 ℃
D.四氯化碳中一定混有另外三种氯代物
高二化学半期 2024-05 第2页 共 4 页
第 II 卷(非选择题) 16.(14 分)三乙氧基甲烷[HC(OC2H5)3]主要用作医药中间体和感光材料,氯仿和乙醇钠(易溶于乙醇)在
二、非选择题:本题共 4 小题,共 58 分。 60 ℃~65 ℃的无水条件下反应可以制取三乙氧基甲烷并得到氯化钠,实验室模拟该制备的装置(夹持仪
15.(14 分)晒制蓝图时,技术人员常将 K3[Fe(C2O4)3]·3H2O 作为感光剂,光照易分解,后以 器省略)、步骤及反应方程式如下:
K3[Fe(CN)6]溶液为显色剂进行显色,回答下列问题:
(1)K3[Fe(C2O4)3]中 Fe(III)的价层电子排布图为: 。
(2)[Fe(C 3-2O4)3] 的结构如图所示,1 mol 该配离子中含有的 σ 键数目为: NA,中心离子的配体数与
配位数之比为: 。
步骤①:将 14.0 g 氯仿和过量乙醇加入圆底烧瓶中,磁力搅拌均匀;
(3)下列操作有利于制备 K3[Fe(C2O4)3]·3H2O 大晶体的是 (填字母)。 步骤②:6.9 g 钠切成小块,加入反应器后不搅拌,保持钠浮在液面上反应;
a.快速降温冷却结晶 b.常温缓慢冷却结晶 c.避光结晶 步骤③:反应结束后用吸滤法过滤出固体,并对该固体进行洗涤,将洗涤液合并入滤液后进行操作 X,
d.搅拌 e.玻璃棒适当刮擦试管内壁提供晶核 得到纯净的三乙氧基甲烷。
(4)显色剂显色时会生成一种蓝色沉淀,该蓝色沉淀的化学名称为: ,该蓝色沉淀中存在的作 已知:HC(OC2H5)3 熔点-76 ℃,沸点 146 ℃,密度约为 0.9 g cm-3,能溶于乙醇等有机溶剂,遇明火、高
用力类型有_______________。 热等有燃烧或爆炸危险。
(5)生成的蓝色沉淀的晶胞由 8 个如图所示的小立方体构成(K+未标出)。 按要求回答下列问题:
(1)球形冷凝管内冷凝水应从 端通入(填“a”或“b”)。
(2)步骤①中加入的无水乙醇是理论量的多倍,多余乙醇的作用是 ,磁力搅拌
的作用是搅拌和_______________。
(3)为保证反应持续进行,需控制一定温度,但反应过程中不需要加热,其原因是 。
(4)步骤②中钠切成小块再分批放入的原因是 。
(5)回流时,若回流装置中气雾的上升高度过高,应采取的措施是 。
(6)步骤③中过滤出的固体为 (填化学式),洗涤时所用试剂为___________,操作 X 为
_________。
①该晶胞中 CN-的 N 采取_____杂化方式,每个 Fen+都处于 CN-的__________(填写形状)配位空隙中。
(7)已知 M(CHCl3)=119.5 g/mol,M[HC(OC2H5)3]=148 g/mol。若收集到 10.00 mL 三乙氧基甲烷,其产率
②已知 K+位于小立方体的体心,但不是每个小立方体的体心都含有 K+。根据化学式推断,该蓝色物质的
最接近_______(填字母)。
一个晶胞中含有 K+的个数为 。
a.30% b.40% c.50% d.60%
高二化学半期 2024-05 第3页 共 4 页
17.(16 分)利用炼锌钴渣[主要含 Co(OH)2、FeSO4、NiSO4 和 Zn、Cu 单质]协同制备 Co(OH)3和高纯 Zn 18.(14 分)碳骨架的构建是有机合成的重要任务之一。某同学从基础化工原料乙烯出发,针对二酮 H 设
的流程如下。 计了如下合成路线:
(1)Co 元素在周期表中的位置是: ,Zn 位于元素周期表的 区。
(2)写出“酸浸”过程 Co(OH)2 发生反应的化学方程式: 。
(3)“沉铁”过程 CaCO3 的作用是: 。
(4)“沉镍”过程 pH 对溶液中 Co(II)、Ni(II)含量的影响如下图。
回答下列问题:
(1)B 中所含官能团的名称为__________,D→E 的转化还可在一定温度下、浓硫酸作催化剂下完成,在此
条件下,浓硫酸的作用除了催化剂外还有___________。
(2)D 的同分异构体中,与其具有相同官能团的有 种(不考虑对映异构),其中核磁共振氢谱有三组
①由图判断,应调节 pH= 。 峰,峰面积之比为 9:2:1 的结构简式为 。
②该过程 Co2+可能发生的反应如下: (3)F 还可由 E 与溴水发生加成反应后的产物通过取代反应获得,写出取代反应的化学方程式:
Co2++6NH3 H2O = [Co(NH ) ]
2+
3 6 +6H2 1=10
5 。
Co2+ +2NH3 H2O=Co(OH) +2NH
+ K (4)G→H 的反应原理可表示如下: 2 4 2
(已知:25℃时,Kb(NH ·H -4.73 2O)=10 ,Ksp[Co(OH) ]=10-152 )
则 K = ,[Co(NH ) ]2+2 3 6 为: (填“热力学”或“动力学”)产物。
(5)写出“沉钴”过程生成 Co(OH)3 的离子方程式: 。 G→H 的转化还需一种反应物,根据以上反应原理写出另一反应物的结构简式 。
(6)写出“电解”过程阴极生成 Zn 的电极反应式: 。
(7)金属 Zn 的晶胞如图,密度为 ρ g/cm3,则阿伏加德罗常数 NA= mol-1(用代数式表示)。 (5)已知: ,H
在该信息条件下易发生分子内缩合从而构建双环结构,产物为 I( )和另一种有机产物 J,
有机产物 J 的结构简式为 。若经此路线由 H 合成 I,存在的问题有 (填字母)。
a.原子利用率低 b.严重污染环境 c.反应条件苛刻 d.产物难以分离
高二化学半期 2024-05 第4页 共 4 页
树德中学高 2022 级高二下学期半期考试化学试题参考答案及评分标准
1-14 题每题 3 分
1 2 3 4 5 6 7 8 9 10 11 12 13 14 (4) (2 分)
D B B A D A D D D C C B C C
15、(14 分)
(1) (1 分,未标 3d 不得分)
(2)21(1 分);1:2(2 分,未化简不扣分)
(3)b、c、e(2 分,多选或错选不得分,漏选扣 1 分)
(5) (2 分);ad(2 分,多选或错选不得分,漏选扣 1 分)
(4)铁氰化亚铁钾或亚铁氰化铁钾(1 分,字错不得分);离子键、(极性)共价键(2 分,多写或
错写不得分,漏写扣 1 分)
(5)①sp(1 分);(正)八面体(2 分) ②4(2 分)
16、(14 分)
(1)a(1 分)
(2)作溶剂,溶解乙醇钠,增大反应物间的接触面积,提高反应速率(1 分,意对即可);防暴沸
(1 分,字错不得分)
(3)钠与乙醇反应过程放热,可维持温度或该反应为放热反应(2 分,意对即可)
(4)钠与乙醇反应放热,防止放热过多引起爆炸(2 分,意对即可,未答到防止过热引起爆炸扣 1
分)
(5)降低温度(2 分,意对即可)
(6)NaCl(1 分,写名称不得分);(无水)乙醇(1 分);蒸馏(1 分)
(7)c(2 分)
17、(16 分)
(1)第四周期 VIII 族(2 分,周期答对 1 分,族答对 1 分,分开给分;“第四周期”写成“第 4 周期”
不扣分);ds(1 分)
(2)H2SO4 + Co(OH)2 == CoSO4 + 2H2O(2 分,若 CoSO4打了沉淀符号,扣 1 分)
(3)调节 pH(1 分)
(4)10(1 分) 1×105.6(2 分,未用科学计数法表达不扣分) 动力学(1 分)
(5)2[Co(NH ) ]2++SO2-3 6 5 +4OH
+H2 = 2Co(OH)3 ↓ +SO
2-
4 +12NH3↑(2 分,未打气体符号或沉淀
符号的扣 1 分;方程式未配平的不得分)
(6)[Zn(OH) ]2-4 +2e
= Zn+4OH (2 分,[Zn(OH) 2-4] 配离子的书写未打中括号的不扣分)
130×1030
(7) (2 分,sin60°若换算出来,不扣分)
a2×ρ×sin60°
18、(14 分)
(1)溴原子或碳溴键(1 分,写成卤素原子或碳卤键不得分);脱水剂(1 分)
(2)7(2 分) (2 分)
(3) (2 分)
高二化学半期 2024-05 第5页 共 4 页
B.装置乙用于分离装有 C60 的“杯酚”和溶解了 C70 的甲苯
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Fe 56 Zn 65 C.装置丙用于用浓 KI 溶液去除 CCl4 中的 I2
第 I 卷(选择题) D.装置丁用于重结晶法提纯苯甲酸
一、选择题:本题共 14 小题,每小题 3 分,共 42 分。 6.10-羟基喜树碱具有抗癌作用,其结构简式如图。下列有关该化合物的
1.生活与化学密切相关。下列关于生活中的化学描述错.误.的是 说法错.误.的是
A.壁虎在天花板上爬行自如——壁虎的脚与墙体之间存在范德华力 A.有三种含氧官能团,分别为羟基、酯基、羰基
B.氯乙烷用于运动中的急性损伤——氯乙烷沸点较低而易汽化 B.可与 FeCl3溶液发生显色反应
C.氧炔焰用于焊接或切割金属——乙炔燃烧大量放热 C.该物质只有 1 个手性碳原子
D.液晶材料用于电视的显示器——液晶属于液态 D.1 mol Na 和足量该物质反应可生成标准状况下 11.2 L H2
2.化学符号的正确表达是“化学人”交流的基础。下列相关化学用语表述正.确.的是 7.下列有机物命名错.误.的是
A.只含有一种等效氢的 C5H12,可命名为 2,2—二甲基丙烷
A.醛基的电子式: B.基态氧原子最高能级的电子排布式:2p 22p 1 1x y 2pz
B.所有碳原子都在同一条直线上的 C4H6,可命名为 2—丁炔
C.所有碳原子位于同一个平面的 C6H12,可命名为 2,3—二甲基—2—丁烯
C.1-丁烯的实验式:CnH2n D.镁原子最外层电子的电子云轮廓图: D.分子式为 C9H12 的芳香烃,若苯环上的一氯代物只有一种,可命名为 2,4,6—三甲苯
8.下列有机合成路线设计合.理.的是
3.教材插图往往承载着重要的教学信息。下列有关教材插图的说法正.确.的是
A.
B.
Cl 浓H
C.CH =CH-CH=CH 2→CH ClCHClCH=CH 2
SO
42 2 2 2 →CH2 =CClCH=CH △ 2
A.图甲:环己烷常以如图所示的“船式”结构存在,是因为“船式”结构更稳定
B.图乙:金刚石以共价键形成三维骨架结构,是金刚石易锤击的主要原因 D.
C.图丙:一些高分子材料如聚乙炔能导电的原因和石墨能导电的原因不同
D.图丁:苯由于形成大 π 键而使苯中无独立的碳碳单键和双键,且共 6 个原子共平面 9.短周期元素 R、X、Y、Z 均属于第三周期主族元素,它们的最高价氧化物分别与水反应可得四种溶液,
4.设 NA为阿伏伽德罗常数的值,下列说法错.误.的是 浓度均为 0.01 mol/L 的上述四种溶液的 pH 与对应元素原子半径的关系如图所示。下列说法错.误.的是
A.标准状况下,22.4 L O3 含有的非极性 σ 键的数目为 2 NA
B.1 mol [Cu(H2O)4]2+中含有的键合电子数为 24 NA
C.1 mol 碳正离子( +CH3)含有的质子数为 9 NA
D.14 g 乙烯和丙烯的混合气体中含有 C-H σ 键的数目为 2 NA
5.分离提纯是开展物质的组成、性质等研究的基础。下列有关装置及其用途错.误.的是
A.同周期中第一电离能大于 Z 元素的有 3 种
B.X 和 Y 形成的化合物中 X 的杂化方式不一定为 sp3 杂化
C.Z 和 R 组成的化合物 R2Z8 中,含有离子键和非极性共价键
D.X 元素形成的正四面体结构的物质中,键角为 109°28′
高二化学半期 2024-05 第1页 共 4 页
10. 物质的结构会遵循一定的规律,但也有“反规律”的情况出现。下列对规律和反规律的整理中存在错.误. 13.铁镁合金是储氢材料之一,其晶胞结构如图所示(白球代表 Fe,黑球代表 Mg)。储氢时,H2 分子在晶
的是 胞的体心和棱的中心位置,且最近的两个氢分子之间的距离为 a nm,NA表示阿伏加德罗常数的值。已知
1 1
选项 一般规律 反规律 A 点的原子坐标参数为(0,0,0),B 点为( , ,0)。则下列说法正确的是
2 2 ..
A 共价键键长越短,键能越大 F-F 键比 Cl-C1 键键长短,键能小
冰中水分子间由于形成氢键而使冰的密度小于液态水
B 同种物质的固体密度大于液体密度
的密度
C 共价键具有方向性和饱和性 s-s σ 键因 s 轨道为球形而无方向性和饱和性
D 离子化合物的熔点较高 离子液体的熔点因其体积较大的阴阳离子而较低
11.化学是以实验为基础的科学。利用下列实验装置完成对应的实验,能.达.到.实验目的的是
A.晶胞中 Fe 与 Mg 的配位数均为 4
3 1 3
B.位置 C 点的原子坐标参数为( , , )
4 4 4
√6
C.Mg 与 Fe 之间的最近距离为 a nm
4
416
D.储氢后的晶体密度为 g cm-3
( -7
3
√2a×10 ) NA
A.装置甲用于探究酒精脱水生成乙烯
14.一定温度下,CH3CH2CH3 的氯化、溴化反应势能图及一段时间后产物的选择性如图,则下列叙述正.
B.装置乙用于实验室制备乙炔
确的是
C.装置丙用于制备乙酸乙酯并提高产率 .
D.装置丁用于探究盐酸、碳酸和苯酚的酸性
12.CH4 和 Cl2 混合气体在光照下反应生成四种氯代物,其沸点如下表所示:
A.1-氯丙烷和 1-溴丙烷的密度都比水大
B.丙烷中仲氢(-CH2-)比伯氢(-CH3)活性更强、键能更大
C.以丙烷为原料合成丙醇时,“先溴代再水解”有利于提高 2-丙醇的含量
利用上右图所示装置对上述氯代物进行分离,下列叙述正.确.的是 D.升高温度 CH3CH2CH3与 Cl·的反应速率比与 Br·反应速率变化更大
A.毛细玻璃管可以用玻璃棒替代
B.克氏蒸馏头的作用是减少液体进入冷凝管
C.收集氯仿时温度计指示温度为 39.8 ℃
D.四氯化碳中一定混有另外三种氯代物
高二化学半期 2024-05 第2页 共 4 页
第 II 卷(非选择题) 16.(14 分)三乙氧基甲烷[HC(OC2H5)3]主要用作医药中间体和感光材料,氯仿和乙醇钠(易溶于乙醇)在
二、非选择题:本题共 4 小题,共 58 分。 60 ℃~65 ℃的无水条件下反应可以制取三乙氧基甲烷并得到氯化钠,实验室模拟该制备的装置(夹持仪
15.(14 分)晒制蓝图时,技术人员常将 K3[Fe(C2O4)3]·3H2O 作为感光剂,光照易分解,后以 器省略)、步骤及反应方程式如下:
K3[Fe(CN)6]溶液为显色剂进行显色,回答下列问题:
(1)K3[Fe(C2O4)3]中 Fe(III)的价层电子排布图为: 。
(2)[Fe(C 3-2O4)3] 的结构如图所示,1 mol 该配离子中含有的 σ 键数目为: NA,中心离子的配体数与
配位数之比为: 。
步骤①:将 14.0 g 氯仿和过量乙醇加入圆底烧瓶中,磁力搅拌均匀;
(3)下列操作有利于制备 K3[Fe(C2O4)3]·3H2O 大晶体的是 (填字母)。 步骤②:6.9 g 钠切成小块,加入反应器后不搅拌,保持钠浮在液面上反应;
a.快速降温冷却结晶 b.常温缓慢冷却结晶 c.避光结晶 步骤③:反应结束后用吸滤法过滤出固体,并对该固体进行洗涤,将洗涤液合并入滤液后进行操作 X,
d.搅拌 e.玻璃棒适当刮擦试管内壁提供晶核 得到纯净的三乙氧基甲烷。
(4)显色剂显色时会生成一种蓝色沉淀,该蓝色沉淀的化学名称为: ,该蓝色沉淀中存在的作 已知:HC(OC2H5)3 熔点-76 ℃,沸点 146 ℃,密度约为 0.9 g cm-3,能溶于乙醇等有机溶剂,遇明火、高
用力类型有_______________。 热等有燃烧或爆炸危险。
(5)生成的蓝色沉淀的晶胞由 8 个如图所示的小立方体构成(K+未标出)。 按要求回答下列问题:
(1)球形冷凝管内冷凝水应从 端通入(填“a”或“b”)。
(2)步骤①中加入的无水乙醇是理论量的多倍,多余乙醇的作用是 ,磁力搅拌
的作用是搅拌和_______________。
(3)为保证反应持续进行,需控制一定温度,但反应过程中不需要加热,其原因是 。
(4)步骤②中钠切成小块再分批放入的原因是 。
(5)回流时,若回流装置中气雾的上升高度过高,应采取的措施是 。
(6)步骤③中过滤出的固体为 (填化学式),洗涤时所用试剂为___________,操作 X 为
_________。
①该晶胞中 CN-的 N 采取_____杂化方式,每个 Fen+都处于 CN-的__________(填写形状)配位空隙中。
(7)已知 M(CHCl3)=119.5 g/mol,M[HC(OC2H5)3]=148 g/mol。若收集到 10.00 mL 三乙氧基甲烷,其产率
②已知 K+位于小立方体的体心,但不是每个小立方体的体心都含有 K+。根据化学式推断,该蓝色物质的
最接近_______(填字母)。
一个晶胞中含有 K+的个数为 。
a.30% b.40% c.50% d.60%
高二化学半期 2024-05 第3页 共 4 页
17.(16 分)利用炼锌钴渣[主要含 Co(OH)2、FeSO4、NiSO4 和 Zn、Cu 单质]协同制备 Co(OH)3和高纯 Zn 18.(14 分)碳骨架的构建是有机合成的重要任务之一。某同学从基础化工原料乙烯出发,针对二酮 H 设
的流程如下。 计了如下合成路线:
(1)Co 元素在周期表中的位置是: ,Zn 位于元素周期表的 区。
(2)写出“酸浸”过程 Co(OH)2 发生反应的化学方程式: 。
(3)“沉铁”过程 CaCO3 的作用是: 。
(4)“沉镍”过程 pH 对溶液中 Co(II)、Ni(II)含量的影响如下图。
回答下列问题:
(1)B 中所含官能团的名称为__________,D→E 的转化还可在一定温度下、浓硫酸作催化剂下完成,在此
条件下,浓硫酸的作用除了催化剂外还有___________。
(2)D 的同分异构体中,与其具有相同官能团的有 种(不考虑对映异构),其中核磁共振氢谱有三组
①由图判断,应调节 pH= 。 峰,峰面积之比为 9:2:1 的结构简式为 。
②该过程 Co2+可能发生的反应如下: (3)F 还可由 E 与溴水发生加成反应后的产物通过取代反应获得,写出取代反应的化学方程式:
Co2++6NH3 H2O = [Co(NH ) ]
2+
3 6 +6H2 1=10
5 。
Co2+ +2NH3 H2O=Co(OH) +2NH
+ K (4)G→H 的反应原理可表示如下: 2 4 2
(已知:25℃时,Kb(NH ·H -4.73 2O)=10 ,Ksp[Co(OH) ]=10-152 )
则 K = ,[Co(NH ) ]2+2 3 6 为: (填“热力学”或“动力学”)产物。
(5)写出“沉钴”过程生成 Co(OH)3 的离子方程式: 。 G→H 的转化还需一种反应物,根据以上反应原理写出另一反应物的结构简式 。
(6)写出“电解”过程阴极生成 Zn 的电极反应式: 。
(7)金属 Zn 的晶胞如图,密度为 ρ g/cm3,则阿伏加德罗常数 NA= mol-1(用代数式表示)。 (5)已知: ,H
在该信息条件下易发生分子内缩合从而构建双环结构,产物为 I( )和另一种有机产物 J,
有机产物 J 的结构简式为 。若经此路线由 H 合成 I,存在的问题有 (填字母)。
a.原子利用率低 b.严重污染环境 c.反应条件苛刻 d.产物难以分离
高二化学半期 2024-05 第4页 共 4 页
树德中学高 2022 级高二下学期半期考试化学试题参考答案及评分标准
1-14 题每题 3 分
1 2 3 4 5 6 7 8 9 10 11 12 13 14 (4) (2 分)
D B B A D A D D D C C B C C
15、(14 分)
(1) (1 分,未标 3d 不得分)
(2)21(1 分);1:2(2 分,未化简不扣分)
(3)b、c、e(2 分,多选或错选不得分,漏选扣 1 分)
(5) (2 分);ad(2 分,多选或错选不得分,漏选扣 1 分)
(4)铁氰化亚铁钾或亚铁氰化铁钾(1 分,字错不得分);离子键、(极性)共价键(2 分,多写或
错写不得分,漏写扣 1 分)
(5)①sp(1 分);(正)八面体(2 分) ②4(2 分)
16、(14 分)
(1)a(1 分)
(2)作溶剂,溶解乙醇钠,增大反应物间的接触面积,提高反应速率(1 分,意对即可);防暴沸
(1 分,字错不得分)
(3)钠与乙醇反应过程放热,可维持温度或该反应为放热反应(2 分,意对即可)
(4)钠与乙醇反应放热,防止放热过多引起爆炸(2 分,意对即可,未答到防止过热引起爆炸扣 1
分)
(5)降低温度(2 分,意对即可)
(6)NaCl(1 分,写名称不得分);(无水)乙醇(1 分);蒸馏(1 分)
(7)c(2 分)
17、(16 分)
(1)第四周期 VIII 族(2 分,周期答对 1 分,族答对 1 分,分开给分;“第四周期”写成“第 4 周期”
不扣分);ds(1 分)
(2)H2SO4 + Co(OH)2 == CoSO4 + 2H2O(2 分,若 CoSO4打了沉淀符号,扣 1 分)
(3)调节 pH(1 分)
(4)10(1 分) 1×105.6(2 分,未用科学计数法表达不扣分) 动力学(1 分)
(5)2[Co(NH ) ]2++SO2-3 6 5 +4OH
+H2 = 2Co(OH)3 ↓ +SO
2-
4 +12NH3↑(2 分,未打气体符号或沉淀
符号的扣 1 分;方程式未配平的不得分)
(6)[Zn(OH) ]2-4 +2e
= Zn+4OH (2 分,[Zn(OH) 2-4] 配离子的书写未打中括号的不扣分)
130×1030
(7) (2 分,sin60°若换算出来,不扣分)
a2×ρ×sin60°
18、(14 分)
(1)溴原子或碳溴键(1 分,写成卤素原子或碳卤键不得分);脱水剂(1 分)
(2)7(2 分) (2 分)
(3) (2 分)
高二化学半期 2024-05 第5页 共 4 页
同课章节目录
