1.2 化学研究些什么(2)-2023-2024学年沪教版九年级上册化学同步讲义及练习(含解析)
文档属性
| 名称 | 1.2 化学研究些什么(2)-2023-2024学年沪教版九年级上册化学同步讲义及练习(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-14 00:00:00 | ||
图片预览



文档简介
九年级上册化学同步精品讲义及练习
1.2 化学研究些什么(2)
姓名:_________ 班级:_________ 学号:_________
1. 了解空气的组成,掌握测定空气中氧气体积的实验原理、步骤及注意事项。
2. 掌握纯净物和混合物的概念,能对常见的物质进行简单分类。
二、化学研究物质的组成和结构
1.空气中含有________、________、二氧化碳等多种气体。
2.红磷在空气中燃烧生成________(________色固体)。
3.混合物是由________物质混合而成的,纯净物只由________物质组成的。纯净物______(填“有”或“没
有”,下同)固定的组成,混合物________固定的组成,各成分的含量可以改变;
4. 从宏观上讲物质都是由________组成的,有的物质由一种元素组成,如氧气由_____元素组成;有的物质由多种元素组成,如水是由_____组成。从微观上讲:各种物质都是由_____构成的;各种物质都具有一定的组成与结构。化学变化(化学反应)过程中,元素的种类是_____(填“会”或“不会”)发生改变的。
三、化学研究物质的用途与制法
1.物质的_____决定物质的用途,而物质的用途又能反应物质的_____。
2.历史上著名的化家学及其主要成就:_____发表元素周期表,_____发现放射性的钋和镭,_____研究炸药,改进引爆装置,_____研究空气成分。
3.制作钻石的材料是_____,制作电池电极的材料是_____,制作铅笔笔芯的材料是_____。
【例1】用如图装置可验证空气中O2的含量。下列说法不正确的是( )
A.实验中红磷必须足量
B.该实验所用的红磷不可用木炭代替
C.待反应装置冷却至室温打开弹簧夹
D.打开弹簧夹后,集气瓶中水面最终上升至2处
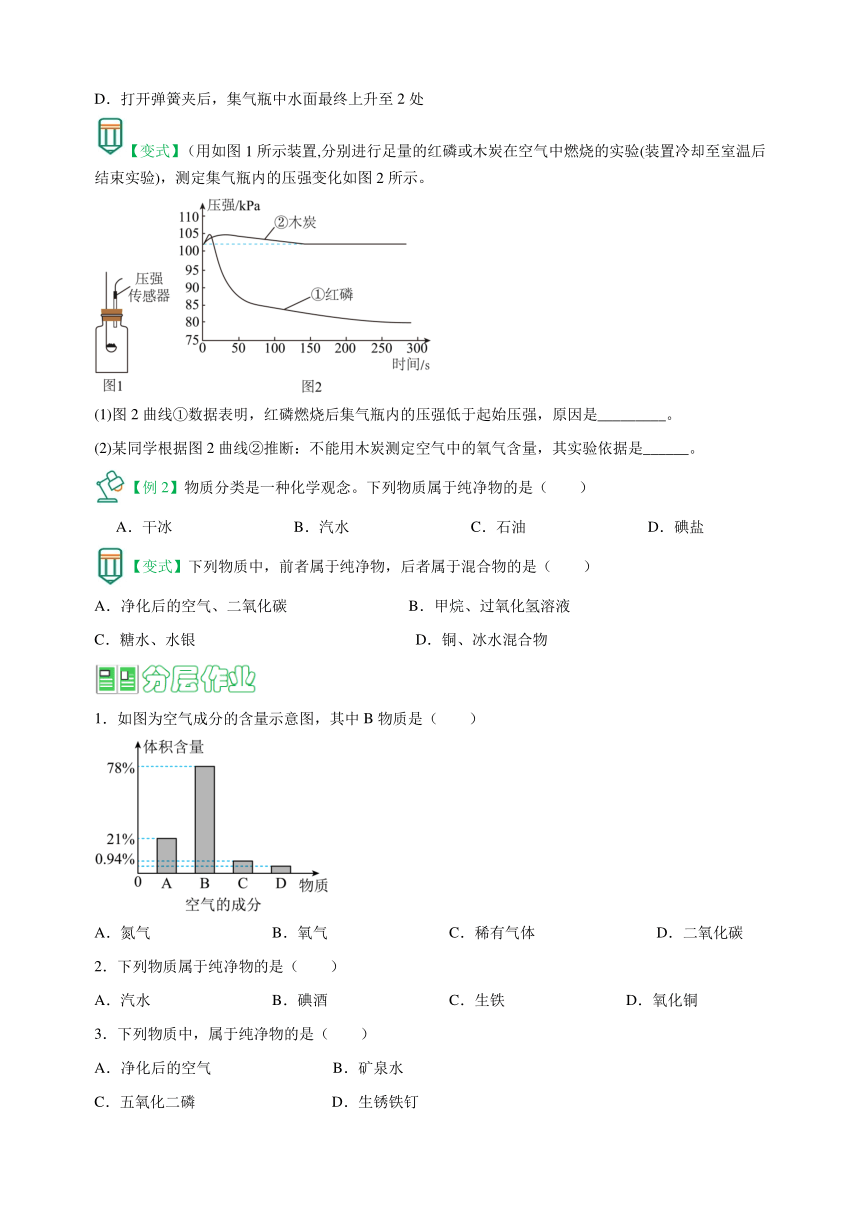
【变式】(用如图1所示装置,分别进行足量的红磷或木炭在空气中燃烧的实验(装置冷却至室温后结束实验),测定集气瓶内的压强变化如图2所示。
(1)图2曲线①数据表明,红磷燃烧后集气瓶内的压强低于起始压强,原因是_________。
(2)某同学根据图2曲线②推断:不能用木炭测定空气中的氧气含量,其实验依据是______。
【例2】物质分类是一种化学观念。下列物质属于纯净物的是( )
A.干冰 B.汽水 C.石油 D.碘盐
【变式】下列物质中,前者属于纯净物,后者属于混合物的是( )
A.净化后的空气、二氧化碳 B.甲烷、过氧化氢溶液
C.糖水、水银 D.铜、冰水混合物
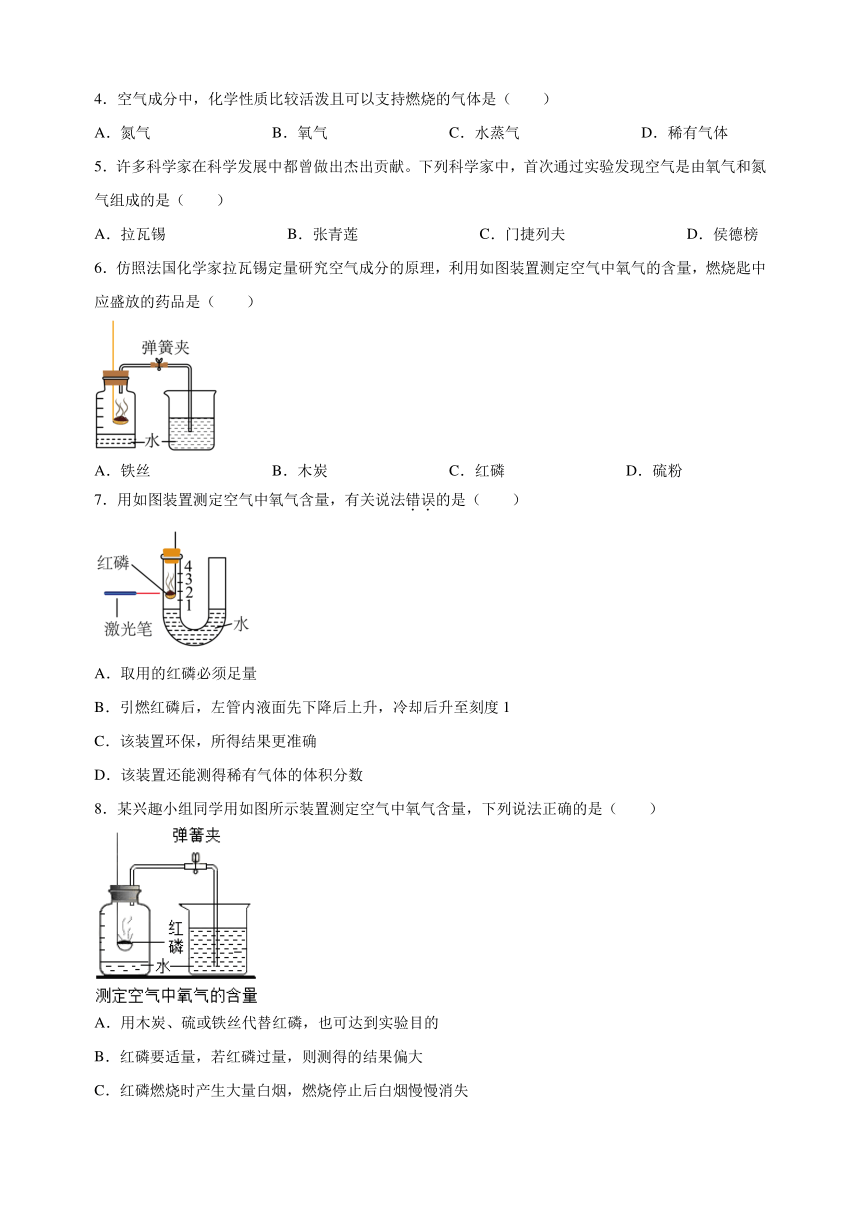
1.如图为空气成分的含量示意图,其中B物质是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
2.下列物质属于纯净物的是( )
A.汽水 B.碘酒 C.生铁 D.氧化铜
3.下列物质中,属于纯净物的是( )
A.净化后的空气 B.矿泉水
C.五氧化二磷 D.生锈铁钉
4.空气成分中,化学性质比较活泼且可以支持燃烧的气体是( )
A.氮气 B.氧气 C.水蒸气 D.稀有气体
5.许多科学家在科学发展中都曾做出杰出贡献。下列科学家中,首次通过实验发现空气是由氧气和氮气组成的是( )
A.拉瓦锡 B.张青莲 C.门捷列夫 D.侯德榜
6.仿照法国化学家拉瓦锡定量研究空气成分的原理,利用如图装置测定空气中氧气的含量,燃烧匙中应盛放的药品是( )
A.铁丝 B.木炭 C.红磷 D.硫粉
7.用如图装置测定空气中氧气含量,有关说法错误的是( )
A.取用的红磷必须足量
B.引燃红磷后,左管内液面先下降后上升,冷却后升至刻度1
C.该装置环保,所得结果更准确
D.该装置还能测得稀有气体的体积分数
8.某兴趣小组同学用如图所示装置测定空气中氧气含量,下列说法正确的是( )
A.用木炭、硫或铁丝代替红磷,也可达到实验目的
B.红磷要适量,若红磷过量,则测得的结果偏大
C.红磷燃烧时产生大量白烟,燃烧停止后白烟慢慢消失
D.该实验说明:氧气约占空气总质量的五分之一
9.通过实验测定空气中氧气含量的科学家是( )
A.门捷列夫B.达尔文C.拉瓦锡 D.牛顿
10.下列有关空气成分的说法,错误的是( )
A.氮气常用作保护气 B.二氧化碳含量少、作用大
C.洁净的空气是纯净物 D.空气的主要成分是氮气和氧气
11.绚丽多彩的世界离不开化学家的贡献。下列说法不正确的是( )
A.波义耳发现了元素周期律 B.拉瓦锡得出空气组成
C.诺贝尔研究炸药 D.侯德榜发明联合制碱法
16.下列科学家及其成就对应不正确的是( )
A.屠呦呦:发现青蒿素治疗疟疾新疗法
B.侯德榜:发明了联合制碱法
C.门捷列夫:定量研究空气的成分
D.张青莲:测定了铱、镝等几种元素相对原子质量的新值
17.拉瓦锡通过实验研究了空气的成分。同学们在实验室仿照拉瓦锡的实验原理,用如图所示实验测定了空气中氧气的含量。对此实验的下列说法正确的是( )
A.该实验不需要在密闭容器中进行
B.红磷可用木炭等可燃性固体代替
C.实验中观察到产生了大量的白烟
D.点燃红磷伸入集气瓶中后立即打开弹簧夹
18.某化学兴趣小组在学完氧气的性质后,在老师的指导下做用不同燃料测定空气里氧气的含量的实验:分别在图甲所示装置的燃烧匙内放置铁粉、红磷(均足量),电加热引燃。氧气含量随时间变化情况如图乙和图丙所示。
(1)温度传感器显示,实验过程中瓶内温度均_______(填“升高”或“降低”)。
(2)待铁粉熄灭并恢复至室温后,打开弹簧夹,进入瓶内水的体积约占原水面上方容积的_______。
(3)分析图乙、图丙可知,实验中消耗氧气速率更快、更彻底的是_______(填“铁粉”或“红磷”) 。
19.某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究。
(1)如上左图所示装置和药品进行实验,可观察到的现象是:__________,打开止水夹后看到___________红磷燃烧反应的文字表达式为___________。
(2)小明同学认为可用木炭代替红磷测定空气中氧气的含量,小丽同学认为不可以,其原因是_________。
(3)小组内同学还对该实验进行了如下改进如图已知试管容积为。
实验的操作步骤如下:
①点燃酒精灯。
②撤去酒精灯,待试管冷却后松开弹簧夹。
③将少量红磷平装入试管中,将的注射器活塞置于刻度处,并按上图中所示的连接方式固定好,再将弹簧夹紧橡皮管。
④读取注射器活塞的数据。
你认为正确的实验操作顺序是___________填序号注射器活塞将从刻度处慢慢前移到约为___________刻度处才停止。请写出一条改进后的优点___________。
(4)小芳同学用镁条代替红磷来测定空气中氧气的含量。结果却发现倒吸的水量远远超过集气瓶的五分之一,小组内同学帮她仔细检查,发现装置的气密性及操作步骤均无问题。你认为造成此现象的原因可能是___________。
(5)小组内同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是___________。
20.现用下面两种方法来测量空气中氧气含量,实验装置如图所示。(说明:实验中集气瓶内壁的铁粉除氧剂是用水湿润后均匀涂附上去的,主要是除去空气中氧气,其中的辅助成分不干扰实验)
(1)实验中,红磷燃烧熄灭后,集气瓶冷却至室温,打开K,水能倒吸入集气瓶的原因是____;
(2)红磷在集气瓶中燃烧的文字表达式为________。
(3)为提高实验的准确性,以上两个实验都需要注意的事项是________(写一点),
(4)如将燃烧匙中红磷换成硫粉,实验能否成功?为什么?_______。
(5)实验过程中,连接数字传感器,测得实验一、实验二中氧气的体积分数随时间变化的关系分别对应下面图1、图2,依据图1、图2信息,______(填“实验1”或“实验2”)的测定方法更准确,判断依据是________;
(6)小明利用实验二,8分钟后测得的数据如下表:请计算出空气中氧气含量_____(计算结果保留一位小数)。
实验前的体积 实验后的体积
集气瓶内空气 烧杯内蒸馏水 烧杯内剩余蒸馏水
131mL 90.0ml 63.6mL
参考答案
二、化学研究物质的组成和结构
1.空气中含有氮气、氧气、二氧化碳等多种气体。
2.红磷在空气中燃烧生成五氧化二磷(白色固体)。
3.混合物是由两种或两种以上物质混合而成的,纯净物只由一种物质组成的。纯净物 有 (填“有”或“没
有”,下同)固定的组成,混合物 没有 固定的组成,各成分的含量可以改变;
4. 从宏观上讲物质都是由元素组成的,有的物质由一种元素组成,如氧气由 氧 元素组成;有的物质由多种元素组成,如水是由 氢元素、氧元素 组成。从微观上讲:各种物质都是由微粒构成的;各种物质都具有一定的组成与结构。化学变化(化学反应)过程中,元素的种类是不会(填“会”或“不会”)发生改变的。
三、化学研究物质的用途与制法
1.物质的性质决定物质的用途,而物质的用途又能反应物质的性质。
2.历史上著名的化家学及其主要成就:门捷列夫发表元素周期表,居里夫人发现放射性的钋和镭,诺贝尔研究炸药,改进引爆装置,拉瓦锡研究空气成分。
3.制作钻石的材料是 金刚石 ,制作电池电极的材料是 石墨 ,制作铅笔笔芯的材料是 石墨 。
【例1】D
【详解】A、实验中红磷应足量,确保氧气完全反应,故说法正确;
B、木炭燃烧会生成二氧化碳气体,装置内的压强不变,因此该实验所用的红磷不可用木炭代替,故说法正确;
C、待反应装置冷却至室温打开弹簧夹,以防瓶内气体膨胀导致测定结果偏小,故说法正确;
D、集气瓶中水面最终上升至1处,说明氧气约占空气总体积的五分之一,能表明O2含量,故说法错误。故选D。
【变式】 (1)红磷燃烧消耗集气瓶内的氧气,产生五氧化二磷固体,气体质量减小,压强也减小
(2)燃烧消耗氧气的同时产生气体,容器内气压几乎不变,没有产生压强差
【详解】(1)图2曲线①数据表明,红磷燃烧后集气瓶内的压强低于起始压强,原因是红磷燃烧消耗集气瓶内的氧气,产生五氧化二磷固体,气体质量减小,压强也减小;
(2)某同学根据图2曲线②推断:不能用木炭测定空气中的氧气含量,其实验依据是燃烧消耗氧气的同时产生气体,容器内气压几乎不变,没有产生压强差。
【例2】(2023·黑龙江绥化·校考模拟预测)物质分类是一种化学观念。下列物质属于纯净物的是
A.干冰 B.汽水 C.石油 D.碘盐
【答案】A
【分析】纯净物是指由一种单质或一种化合物组成的物质;混合物是由两种或多种物质混合而成的物质。
【详解】A、干冰是固态的二氧化碳,只含一种物质,属于纯净物,故A符合题意;
B、汽水中有水、二氧化碳等,属于混合物,故B不符合题意;
C、石油中有多种物质,属于混合物,故C不符合题意;
D、碘盐中含有食盐、碘酸钾等物质,属于混合物,故D不符合题意。故选A。
【变式】B
【详解】A、净化后的空气含有多种气体组成属于混合物;二氧化碳是由一种物质组成属于纯净物,不符合题意;
B、甲烷是由一种物质组成属于纯净物;过氧化氢溶液含有过氧化氢和水,由多种物质组成属于混合物,符合题意;
C、糖水是由糖和水组成属于混合物;水银是由一种物质组成属于纯净物,不符合题意;
D、铜是由一种物质组成属于纯净物;冰水混合物都是水是由一种物质组成属于纯净物,不符合题意;
故选:B。
1. A
【详解】由图可知B物质是空气中含量最多的物质,空气中氮气的体积分数为78%,是空气中含量最多的物质。故选A。
2. D
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成。
【详解】A、汽水中有水、碳酸等物质,属于混合物;故A错误;
B、碘酒是碘的酒精溶液,属于混合物;故B错误;
C、生铁是铁的合金,属于混合物;故C错误;
D、氧化铜是一种物质,属于纯净物;故D正确。故选D。
3. C
【分析】由同种物质组成的是纯净物,由不同种物质组成的是混合物。
【详解】A. 净化后的空气由不同种物质组成,属于混合物,此选项不符合题意;
B. 矿泉水由不同种物质组成,属于混合物,此选项不符合题意;
C. 五氧化二磷由同种物质组成,属于纯净物,此选项符合题意;
D. 生锈铁钉由不同种物质组成,属于混合物,此选项不符合题意。故选C。
4. B
【详解】A、氮气化学性质稳定,不能燃烧,不支持燃烧,不符合题意;
B、氧气化学性质比较活泼,具有助燃性,能支持燃烧,符合题意;
C、水蒸气不能燃烧、不支持燃烧,不符合题意;
D、稀有气体化学性质稳定,不能燃烧、不支持燃烧,不符合题意。故选B。
5. A
【详解】A.法国拉瓦锡是首次通过实验发现空气是由氧气和氮气组成的科学家,A正确;
B.我国的张青莲在测定相对原子质量方面,作出了很大的贡献,B错误;
C.门捷列夫发现了元素周期律,C错误;
D.侯德榜发明了联合制碱法,D错误。故选A。
6. C
【详解】A.因为铁丝不能在空气燃烧,故A错误;
B.木炭燃烧会生成二氧化碳导致两边压强变化不明显,故B错误;
C.红磷燃烧会消耗氧气,集气瓶中的液面会上升五分之一,故C正确;
D.硫燃烧会生成二氧化硫导致两边压强变化不明显,故D错误;故答案为:C
【点睛】可以用来测定空气中氧气含量的物质应该具备的条件是:能和空气中的氧气反应,生成物是固体,不能和空气中的其它物质发生化学反应。
7. D
【详解】A、取用的红磷必须足量,才能将装置内氧气耗尽,否则会导致实验结果偏小,不符合题意;
B、引燃红磷后,红磷燃烧,放出大量的热,装置内气体受热膨胀,压强增大,左管内液面下降,待完全反应后,逐渐冷却至室温,由于消耗了氧气,装置内压强减小,故左管内液面上升,氧气约占空气体积的,故冷却后升至刻度1,不符合题意;
C、该装置在密闭容器中进行,反应生成的五氧化二磷不会逸出,比较环保,且避免了盛有点燃红磷的燃烧匙伸入集气瓶中时,气体的受热膨胀逸出,误差小,不符合题意;
D、该装置是通过红磷燃烧消耗氧气,测定空气中氧气的含量,无法测得稀有气体的体积分数,符合题意。故选D。
8. C
【详解】A、木炭燃烧生成二氧化碳,硫燃烧生成二氧化硫,导致水不能进入集气瓶,铁不能空气中燃烧,都不能测定氧气含量,故选项A错误;
B、红磷应该足量或过量,确保集气瓶中的氧气完全反应,实验结果更准确,故选项B错误;
C、红磷燃烧时产生大量白烟,燃烧停止后白烟慢慢消失,是因为白烟是五氧化二磷,能够溶解在水中,故选项C正确;
D、该实验测得氧气约占空气总体积(不是总质量)的五分之一,故选项D正确;故选:C。
9. C
【详解】A、门捷列夫在化学上的主要贡献是发现了元素周期律,并编制出元素周期表,故选项错误;
B、达尔文提出了进化论,故选项错误;
C、拉瓦锡首先通过实验得出空气是由氮气和氧气组成的结论,故选项正确;
D、牛顿发现了力学定律,故选项错误。故选:C。
10. C
【详解】A、氮气化学性质稳定,可用作保护气,说法正确,不符合题意;
B、二氧化碳含量少,是光合作用的主要原料,作用大,说法正确,不符合题意;
C、洁净的空气包含氮气、氧气、二氧化碳、稀有气体等多种物质,属于混合物,说法错误,符合题意;
D、氮气体积占空气体积的78%,氧气体积占空气体积的21%,因此空气的主要成分是氮气和氧气,说法正确,不符合题意。故选C。
11. B
【详解】A、门捷列夫发现了元素周期律,故A错误;
B、拉瓦锡得出空气是由氮气和氧气组成的,故B正确;
C、诺贝尔研究炸药,改进引爆装置,故C正确;
D、侯德榜发明联合制碱法,故D正确。故选A。
16. C
【详解】A、屠呦呦发现青蒿素治疗疟疾新疗法,选项正确;
B、侯德榜发明了联合制碱法,选项正确;
C、门捷列夫发现并绘制出元素周期表,选项错误;
D、张青莲测定了铱、镝等几种元素相对原子质量的新值,选项正确;故选:C
17. C
【详解】A、测定空气中氧气含量的实验需要在密闭容器中进行,否则外部空气进入或装置内空气逸出都会影响实验的准确。不符合题意;
B、木炭燃烧生成二氧化碳气体,不能形成准确的压强差,不能代替红磷。不符合题意;
C、红磷和氧气点燃生成五氧化二磷固体,所以看到产生大量的白烟。符合题意;
B、点燃红磷伸入集气瓶中后等红磷熄灭,温度恢复到室温后才能打开弹簧夹。不符合题意;故选C。
18. (1)升高(2)五分之一(3)铁粉
【详解】(1)红磷、铁粉燃烧都放热,故温度传感器显示,实验过程中瓶内温度均升高;
(2)铁粉燃烧消耗氧气,由于氧气约占空气体积的五分之一,故待铁粉熄灭并恢复至室温后,打开弹簧夹,进入瓶内的水约占原水面上方空间体积的五分之一;
(3)根据图乙、图丙可知,实验结束,铁粉燃烧后氧气含量为0.5%,红磷燃烧后氧气含量为3%,故实验中消耗氧气更彻底的是铁粉;铁粉反应,氧气减少的快,反应完全所需时间比短,故消耗氧气速率更快的是铁粉。
19. (1) 红磷燃烧,发出黄色火焰,产生大量的白烟,同时放热 水倒吸入约占集气瓶容积的1/5
(2)木炭燃烧生成二氧化碳气体,装置内压强不变
(3) ③①②④ 3mL 数据更容易获取
(4)镁条不仅仅能够与氧气反应,而且还能和氮气反应
(5)物质在空气中能否燃烧以及燃烧后生成物的状态等
【解析】(1)如上左图所示装置为红磷燃烧,可观察到的现象是:红磷燃烧,发出黄色火焰,产生大量的白烟,同时放热,打开止水夹后看到,水倒吸入约占集气瓶容积的1/5;红磷燃烧生成五氧化二磷,其文字表达式为。
(2)小明同学认为可用木炭代替红磷测定空气中氧气的含量,小丽同学认为不可以,其原因是木炭燃烧生成二氧化碳气体,装置内压强不变。
(3)依据实验的具体过程可知该实验的操作步骤应该是将少量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按图中所示的连接方式固定好,再将弹簧夹紧橡皮管;点燃酒精灯;撤去酒精灯,待试管冷却后松开弹簧夹;读取注射器活塞的数据,故正确的实验操作顺序是③①②④,由于空气中氧气的含量约为空气体积的,而试管的容积是35mL,当其内氧气被耗尽时气体减少的体积为:,所以活塞所处的刻度值为,对应用注射器进行实验的改进,相对先前的实验,数据更容易获取。
(4)镁条不仅仅能够与氧气反应,而且还能和氮气反应,这样就造成进入液体的体积远远超过。
(5)用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的选择上要考虑的是物质在空气中能否燃烧以及燃烧后生成物的状态等。
20. (1)红磷燃烧消耗了氧气,装置内压强减小
(2)
(3)红磷和铁粉除氧剂需足量或装置不漏气
(4)否,因为硫在空气中燃烧生成二氧化硫,二氧化硫是气体,化学反应前后,压强变化不大
(5) 实验2 实验2消耗氧气更彻底
(6)20.2%
【详解】(1)实验中,红磷燃烧熄灭后,集气瓶冷却至室温,打开K,由于红磷燃烧消耗了氧气,装置内压强减小,故水能倒吸入集气瓶;
(2)红磷燃烧生成五氧化二磷,该反应的文字表达式为:;
(3)为提高实验的准确性,以上两个实验都需要注意的事项是红磷和铁粉除氧剂需足量,才能将氧气完全耗尽,还需注意装置不漏气,否则会导致实验结果偏小;
(4)硫在空气中燃烧生成二氧化硫,二氧化硫是气体,化学反应前后,压强变化不大,无法测定空气中氧气含量,故实验不能成功;
(5)由图1、图2可知,实验2消耗氧气更彻底,测定方法更准确;
(6)空气中氧气含量为:。
1.2 化学研究些什么(2)
姓名:_________ 班级:_________ 学号:_________
1. 了解空气的组成,掌握测定空气中氧气体积的实验原理、步骤及注意事项。
2. 掌握纯净物和混合物的概念,能对常见的物质进行简单分类。
二、化学研究物质的组成和结构
1.空气中含有________、________、二氧化碳等多种气体。
2.红磷在空气中燃烧生成________(________色固体)。
3.混合物是由________物质混合而成的,纯净物只由________物质组成的。纯净物______(填“有”或“没
有”,下同)固定的组成,混合物________固定的组成,各成分的含量可以改变;
4. 从宏观上讲物质都是由________组成的,有的物质由一种元素组成,如氧气由_____元素组成;有的物质由多种元素组成,如水是由_____组成。从微观上讲:各种物质都是由_____构成的;各种物质都具有一定的组成与结构。化学变化(化学反应)过程中,元素的种类是_____(填“会”或“不会”)发生改变的。
三、化学研究物质的用途与制法
1.物质的_____决定物质的用途,而物质的用途又能反应物质的_____。
2.历史上著名的化家学及其主要成就:_____发表元素周期表,_____发现放射性的钋和镭,_____研究炸药,改进引爆装置,_____研究空气成分。
3.制作钻石的材料是_____,制作电池电极的材料是_____,制作铅笔笔芯的材料是_____。
【例1】用如图装置可验证空气中O2的含量。下列说法不正确的是( )
A.实验中红磷必须足量
B.该实验所用的红磷不可用木炭代替
C.待反应装置冷却至室温打开弹簧夹
D.打开弹簧夹后,集气瓶中水面最终上升至2处
【变式】(用如图1所示装置,分别进行足量的红磷或木炭在空气中燃烧的实验(装置冷却至室温后结束实验),测定集气瓶内的压强变化如图2所示。
(1)图2曲线①数据表明,红磷燃烧后集气瓶内的压强低于起始压强,原因是_________。
(2)某同学根据图2曲线②推断:不能用木炭测定空气中的氧气含量,其实验依据是______。
【例2】物质分类是一种化学观念。下列物质属于纯净物的是( )
A.干冰 B.汽水 C.石油 D.碘盐
【变式】下列物质中,前者属于纯净物,后者属于混合物的是( )
A.净化后的空气、二氧化碳 B.甲烷、过氧化氢溶液
C.糖水、水银 D.铜、冰水混合物
1.如图为空气成分的含量示意图,其中B物质是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
2.下列物质属于纯净物的是( )
A.汽水 B.碘酒 C.生铁 D.氧化铜
3.下列物质中,属于纯净物的是( )
A.净化后的空气 B.矿泉水
C.五氧化二磷 D.生锈铁钉
4.空气成分中,化学性质比较活泼且可以支持燃烧的气体是( )
A.氮气 B.氧气 C.水蒸气 D.稀有气体
5.许多科学家在科学发展中都曾做出杰出贡献。下列科学家中,首次通过实验发现空气是由氧气和氮气组成的是( )
A.拉瓦锡 B.张青莲 C.门捷列夫 D.侯德榜
6.仿照法国化学家拉瓦锡定量研究空气成分的原理,利用如图装置测定空气中氧气的含量,燃烧匙中应盛放的药品是( )
A.铁丝 B.木炭 C.红磷 D.硫粉
7.用如图装置测定空气中氧气含量,有关说法错误的是( )
A.取用的红磷必须足量
B.引燃红磷后,左管内液面先下降后上升,冷却后升至刻度1
C.该装置环保,所得结果更准确
D.该装置还能测得稀有气体的体积分数
8.某兴趣小组同学用如图所示装置测定空气中氧气含量,下列说法正确的是( )
A.用木炭、硫或铁丝代替红磷,也可达到实验目的
B.红磷要适量,若红磷过量,则测得的结果偏大
C.红磷燃烧时产生大量白烟,燃烧停止后白烟慢慢消失
D.该实验说明:氧气约占空气总质量的五分之一
9.通过实验测定空气中氧气含量的科学家是( )
A.门捷列夫B.达尔文C.拉瓦锡 D.牛顿
10.下列有关空气成分的说法,错误的是( )
A.氮气常用作保护气 B.二氧化碳含量少、作用大
C.洁净的空气是纯净物 D.空气的主要成分是氮气和氧气
11.绚丽多彩的世界离不开化学家的贡献。下列说法不正确的是( )
A.波义耳发现了元素周期律 B.拉瓦锡得出空气组成
C.诺贝尔研究炸药 D.侯德榜发明联合制碱法
16.下列科学家及其成就对应不正确的是( )
A.屠呦呦:发现青蒿素治疗疟疾新疗法
B.侯德榜:发明了联合制碱法
C.门捷列夫:定量研究空气的成分
D.张青莲:测定了铱、镝等几种元素相对原子质量的新值
17.拉瓦锡通过实验研究了空气的成分。同学们在实验室仿照拉瓦锡的实验原理,用如图所示实验测定了空气中氧气的含量。对此实验的下列说法正确的是( )
A.该实验不需要在密闭容器中进行
B.红磷可用木炭等可燃性固体代替
C.实验中观察到产生了大量的白烟
D.点燃红磷伸入集气瓶中后立即打开弹簧夹
18.某化学兴趣小组在学完氧气的性质后,在老师的指导下做用不同燃料测定空气里氧气的含量的实验:分别在图甲所示装置的燃烧匙内放置铁粉、红磷(均足量),电加热引燃。氧气含量随时间变化情况如图乙和图丙所示。
(1)温度传感器显示,实验过程中瓶内温度均_______(填“升高”或“降低”)。
(2)待铁粉熄灭并恢复至室温后,打开弹簧夹,进入瓶内水的体积约占原水面上方容积的_______。
(3)分析图乙、图丙可知,实验中消耗氧气速率更快、更彻底的是_______(填“铁粉”或“红磷”) 。
19.某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究。
(1)如上左图所示装置和药品进行实验,可观察到的现象是:__________,打开止水夹后看到___________红磷燃烧反应的文字表达式为___________。
(2)小明同学认为可用木炭代替红磷测定空气中氧气的含量,小丽同学认为不可以,其原因是_________。
(3)小组内同学还对该实验进行了如下改进如图已知试管容积为。
实验的操作步骤如下:
①点燃酒精灯。
②撤去酒精灯,待试管冷却后松开弹簧夹。
③将少量红磷平装入试管中,将的注射器活塞置于刻度处,并按上图中所示的连接方式固定好,再将弹簧夹紧橡皮管。
④读取注射器活塞的数据。
你认为正确的实验操作顺序是___________填序号注射器活塞将从刻度处慢慢前移到约为___________刻度处才停止。请写出一条改进后的优点___________。
(4)小芳同学用镁条代替红磷来测定空气中氧气的含量。结果却发现倒吸的水量远远超过集气瓶的五分之一,小组内同学帮她仔细检查,发现装置的气密性及操作步骤均无问题。你认为造成此现象的原因可能是___________。
(5)小组内同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是___________。
20.现用下面两种方法来测量空气中氧气含量,实验装置如图所示。(说明:实验中集气瓶内壁的铁粉除氧剂是用水湿润后均匀涂附上去的,主要是除去空气中氧气,其中的辅助成分不干扰实验)
(1)实验中,红磷燃烧熄灭后,集气瓶冷却至室温,打开K,水能倒吸入集气瓶的原因是____;
(2)红磷在集气瓶中燃烧的文字表达式为________。
(3)为提高实验的准确性,以上两个实验都需要注意的事项是________(写一点),
(4)如将燃烧匙中红磷换成硫粉,实验能否成功?为什么?_______。
(5)实验过程中,连接数字传感器,测得实验一、实验二中氧气的体积分数随时间变化的关系分别对应下面图1、图2,依据图1、图2信息,______(填“实验1”或“实验2”)的测定方法更准确,判断依据是________;
(6)小明利用实验二,8分钟后测得的数据如下表:请计算出空气中氧气含量_____(计算结果保留一位小数)。
实验前的体积 实验后的体积
集气瓶内空气 烧杯内蒸馏水 烧杯内剩余蒸馏水
131mL 90.0ml 63.6mL
参考答案
二、化学研究物质的组成和结构
1.空气中含有氮气、氧气、二氧化碳等多种气体。
2.红磷在空气中燃烧生成五氧化二磷(白色固体)。
3.混合物是由两种或两种以上物质混合而成的,纯净物只由一种物质组成的。纯净物 有 (填“有”或“没
有”,下同)固定的组成,混合物 没有 固定的组成,各成分的含量可以改变;
4. 从宏观上讲物质都是由元素组成的,有的物质由一种元素组成,如氧气由 氧 元素组成;有的物质由多种元素组成,如水是由 氢元素、氧元素 组成。从微观上讲:各种物质都是由微粒构成的;各种物质都具有一定的组成与结构。化学变化(化学反应)过程中,元素的种类是不会(填“会”或“不会”)发生改变的。
三、化学研究物质的用途与制法
1.物质的性质决定物质的用途,而物质的用途又能反应物质的性质。
2.历史上著名的化家学及其主要成就:门捷列夫发表元素周期表,居里夫人发现放射性的钋和镭,诺贝尔研究炸药,改进引爆装置,拉瓦锡研究空气成分。
3.制作钻石的材料是 金刚石 ,制作电池电极的材料是 石墨 ,制作铅笔笔芯的材料是 石墨 。
【例1】D
【详解】A、实验中红磷应足量,确保氧气完全反应,故说法正确;
B、木炭燃烧会生成二氧化碳气体,装置内的压强不变,因此该实验所用的红磷不可用木炭代替,故说法正确;
C、待反应装置冷却至室温打开弹簧夹,以防瓶内气体膨胀导致测定结果偏小,故说法正确;
D、集气瓶中水面最终上升至1处,说明氧气约占空气总体积的五分之一,能表明O2含量,故说法错误。故选D。
【变式】 (1)红磷燃烧消耗集气瓶内的氧气,产生五氧化二磷固体,气体质量减小,压强也减小
(2)燃烧消耗氧气的同时产生气体,容器内气压几乎不变,没有产生压强差
【详解】(1)图2曲线①数据表明,红磷燃烧后集气瓶内的压强低于起始压强,原因是红磷燃烧消耗集气瓶内的氧气,产生五氧化二磷固体,气体质量减小,压强也减小;
(2)某同学根据图2曲线②推断:不能用木炭测定空气中的氧气含量,其实验依据是燃烧消耗氧气的同时产生气体,容器内气压几乎不变,没有产生压强差。
【例2】(2023·黑龙江绥化·校考模拟预测)物质分类是一种化学观念。下列物质属于纯净物的是
A.干冰 B.汽水 C.石油 D.碘盐
【答案】A
【分析】纯净物是指由一种单质或一种化合物组成的物质;混合物是由两种或多种物质混合而成的物质。
【详解】A、干冰是固态的二氧化碳,只含一种物质,属于纯净物,故A符合题意;
B、汽水中有水、二氧化碳等,属于混合物,故B不符合题意;
C、石油中有多种物质,属于混合物,故C不符合题意;
D、碘盐中含有食盐、碘酸钾等物质,属于混合物,故D不符合题意。故选A。
【变式】B
【详解】A、净化后的空气含有多种气体组成属于混合物;二氧化碳是由一种物质组成属于纯净物,不符合题意;
B、甲烷是由一种物质组成属于纯净物;过氧化氢溶液含有过氧化氢和水,由多种物质组成属于混合物,符合题意;
C、糖水是由糖和水组成属于混合物;水银是由一种物质组成属于纯净物,不符合题意;
D、铜是由一种物质组成属于纯净物;冰水混合物都是水是由一种物质组成属于纯净物,不符合题意;
故选:B。
1. A
【详解】由图可知B物质是空气中含量最多的物质,空气中氮气的体积分数为78%,是空气中含量最多的物质。故选A。
2. D
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成。
【详解】A、汽水中有水、碳酸等物质,属于混合物;故A错误;
B、碘酒是碘的酒精溶液,属于混合物;故B错误;
C、生铁是铁的合金,属于混合物;故C错误;
D、氧化铜是一种物质,属于纯净物;故D正确。故选D。
3. C
【分析】由同种物质组成的是纯净物,由不同种物质组成的是混合物。
【详解】A. 净化后的空气由不同种物质组成,属于混合物,此选项不符合题意;
B. 矿泉水由不同种物质组成,属于混合物,此选项不符合题意;
C. 五氧化二磷由同种物质组成,属于纯净物,此选项符合题意;
D. 生锈铁钉由不同种物质组成,属于混合物,此选项不符合题意。故选C。
4. B
【详解】A、氮气化学性质稳定,不能燃烧,不支持燃烧,不符合题意;
B、氧气化学性质比较活泼,具有助燃性,能支持燃烧,符合题意;
C、水蒸气不能燃烧、不支持燃烧,不符合题意;
D、稀有气体化学性质稳定,不能燃烧、不支持燃烧,不符合题意。故选B。
5. A
【详解】A.法国拉瓦锡是首次通过实验发现空气是由氧气和氮气组成的科学家,A正确;
B.我国的张青莲在测定相对原子质量方面,作出了很大的贡献,B错误;
C.门捷列夫发现了元素周期律,C错误;
D.侯德榜发明了联合制碱法,D错误。故选A。
6. C
【详解】A.因为铁丝不能在空气燃烧,故A错误;
B.木炭燃烧会生成二氧化碳导致两边压强变化不明显,故B错误;
C.红磷燃烧会消耗氧气,集气瓶中的液面会上升五分之一,故C正确;
D.硫燃烧会生成二氧化硫导致两边压强变化不明显,故D错误;故答案为:C
【点睛】可以用来测定空气中氧气含量的物质应该具备的条件是:能和空气中的氧气反应,生成物是固体,不能和空气中的其它物质发生化学反应。
7. D
【详解】A、取用的红磷必须足量,才能将装置内氧气耗尽,否则会导致实验结果偏小,不符合题意;
B、引燃红磷后,红磷燃烧,放出大量的热,装置内气体受热膨胀,压强增大,左管内液面下降,待完全反应后,逐渐冷却至室温,由于消耗了氧气,装置内压强减小,故左管内液面上升,氧气约占空气体积的,故冷却后升至刻度1,不符合题意;
C、该装置在密闭容器中进行,反应生成的五氧化二磷不会逸出,比较环保,且避免了盛有点燃红磷的燃烧匙伸入集气瓶中时,气体的受热膨胀逸出,误差小,不符合题意;
D、该装置是通过红磷燃烧消耗氧气,测定空气中氧气的含量,无法测得稀有气体的体积分数,符合题意。故选D。
8. C
【详解】A、木炭燃烧生成二氧化碳,硫燃烧生成二氧化硫,导致水不能进入集气瓶,铁不能空气中燃烧,都不能测定氧气含量,故选项A错误;
B、红磷应该足量或过量,确保集气瓶中的氧气完全反应,实验结果更准确,故选项B错误;
C、红磷燃烧时产生大量白烟,燃烧停止后白烟慢慢消失,是因为白烟是五氧化二磷,能够溶解在水中,故选项C正确;
D、该实验测得氧气约占空气总体积(不是总质量)的五分之一,故选项D正确;故选:C。
9. C
【详解】A、门捷列夫在化学上的主要贡献是发现了元素周期律,并编制出元素周期表,故选项错误;
B、达尔文提出了进化论,故选项错误;
C、拉瓦锡首先通过实验得出空气是由氮气和氧气组成的结论,故选项正确;
D、牛顿发现了力学定律,故选项错误。故选:C。
10. C
【详解】A、氮气化学性质稳定,可用作保护气,说法正确,不符合题意;
B、二氧化碳含量少,是光合作用的主要原料,作用大,说法正确,不符合题意;
C、洁净的空气包含氮气、氧气、二氧化碳、稀有气体等多种物质,属于混合物,说法错误,符合题意;
D、氮气体积占空气体积的78%,氧气体积占空气体积的21%,因此空气的主要成分是氮气和氧气,说法正确,不符合题意。故选C。
11. B
【详解】A、门捷列夫发现了元素周期律,故A错误;
B、拉瓦锡得出空气是由氮气和氧气组成的,故B正确;
C、诺贝尔研究炸药,改进引爆装置,故C正确;
D、侯德榜发明联合制碱法,故D正确。故选A。
16. C
【详解】A、屠呦呦发现青蒿素治疗疟疾新疗法,选项正确;
B、侯德榜发明了联合制碱法,选项正确;
C、门捷列夫发现并绘制出元素周期表,选项错误;
D、张青莲测定了铱、镝等几种元素相对原子质量的新值,选项正确;故选:C
17. C
【详解】A、测定空气中氧气含量的实验需要在密闭容器中进行,否则外部空气进入或装置内空气逸出都会影响实验的准确。不符合题意;
B、木炭燃烧生成二氧化碳气体,不能形成准确的压强差,不能代替红磷。不符合题意;
C、红磷和氧气点燃生成五氧化二磷固体,所以看到产生大量的白烟。符合题意;
B、点燃红磷伸入集气瓶中后等红磷熄灭,温度恢复到室温后才能打开弹簧夹。不符合题意;故选C。
18. (1)升高(2)五分之一(3)铁粉
【详解】(1)红磷、铁粉燃烧都放热,故温度传感器显示,实验过程中瓶内温度均升高;
(2)铁粉燃烧消耗氧气,由于氧气约占空气体积的五分之一,故待铁粉熄灭并恢复至室温后,打开弹簧夹,进入瓶内的水约占原水面上方空间体积的五分之一;
(3)根据图乙、图丙可知,实验结束,铁粉燃烧后氧气含量为0.5%,红磷燃烧后氧气含量为3%,故实验中消耗氧气更彻底的是铁粉;铁粉反应,氧气减少的快,反应完全所需时间比短,故消耗氧气速率更快的是铁粉。
19. (1) 红磷燃烧,发出黄色火焰,产生大量的白烟,同时放热 水倒吸入约占集气瓶容积的1/5
(2)木炭燃烧生成二氧化碳气体,装置内压强不变
(3) ③①②④ 3mL 数据更容易获取
(4)镁条不仅仅能够与氧气反应,而且还能和氮气反应
(5)物质在空气中能否燃烧以及燃烧后生成物的状态等
【解析】(1)如上左图所示装置为红磷燃烧,可观察到的现象是:红磷燃烧,发出黄色火焰,产生大量的白烟,同时放热,打开止水夹后看到,水倒吸入约占集气瓶容积的1/5;红磷燃烧生成五氧化二磷,其文字表达式为。
(2)小明同学认为可用木炭代替红磷测定空气中氧气的含量,小丽同学认为不可以,其原因是木炭燃烧生成二氧化碳气体,装置内压强不变。
(3)依据实验的具体过程可知该实验的操作步骤应该是将少量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按图中所示的连接方式固定好,再将弹簧夹紧橡皮管;点燃酒精灯;撤去酒精灯,待试管冷却后松开弹簧夹;读取注射器活塞的数据,故正确的实验操作顺序是③①②④,由于空气中氧气的含量约为空气体积的,而试管的容积是35mL,当其内氧气被耗尽时气体减少的体积为:,所以活塞所处的刻度值为,对应用注射器进行实验的改进,相对先前的实验,数据更容易获取。
(4)镁条不仅仅能够与氧气反应,而且还能和氮气反应,这样就造成进入液体的体积远远超过。
(5)用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的选择上要考虑的是物质在空气中能否燃烧以及燃烧后生成物的状态等。
20. (1)红磷燃烧消耗了氧气,装置内压强减小
(2)
(3)红磷和铁粉除氧剂需足量或装置不漏气
(4)否,因为硫在空气中燃烧生成二氧化硫,二氧化硫是气体,化学反应前后,压强变化不大
(5) 实验2 实验2消耗氧气更彻底
(6)20.2%
【详解】(1)实验中,红磷燃烧熄灭后,集气瓶冷却至室温,打开K,由于红磷燃烧消耗了氧气,装置内压强减小,故水能倒吸入集气瓶;
(2)红磷燃烧生成五氧化二磷,该反应的文字表达式为:;
(3)为提高实验的准确性,以上两个实验都需要注意的事项是红磷和铁粉除氧剂需足量,才能将氧气完全耗尽,还需注意装置不漏气,否则会导致实验结果偏小;
(4)硫在空气中燃烧生成二氧化硫,二氧化硫是气体,化学反应前后,压强变化不大,无法测定空气中氧气含量,故实验不能成功;
(5)由图1、图2可知,实验2消耗氧气更彻底,测定方法更准确;
(6)空气中氧气含量为:。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
