3.3.2乙酸 课件(共18张PPT) 化学鲁科版(2019)必修第二册
文档属性
| 名称 | 3.3.2乙酸 课件(共18张PPT) 化学鲁科版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-15 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
乙 酸
第3节 饮食中的有机化合物
第2课时
学业要求与核心素养
1.能从原子、分子角度认识乙酸的组成、结构,掌握乙酸的物理性质和化学性质(宏观辨识与微观探析)
2.认识官能团与物质性质的关系,形成结构决定性质的学科理念(证据推理与模型认知)
3.掌握酯化反应的原理和实验操作,会书写酯化反应的化学方程式(科学探究与创新意识)
4.养成安全意识和严禁的科学态度,提高科学素养和生活质量,形成节约适度、绿色低碳的生活方式(科学态度与社会责任)
目 录
1.必备知识 对点掌握
2.课堂探究 能力提升
必备知识 对点掌握
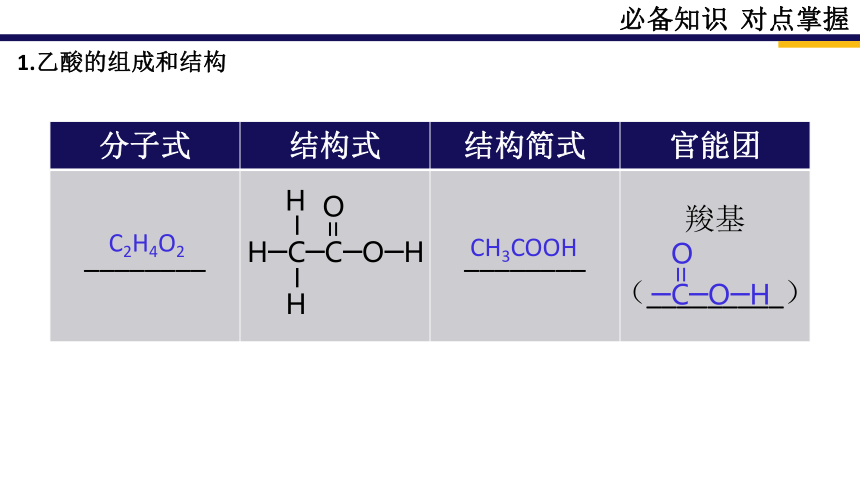
1.乙酸的组成和结构
分子式 结构式 结构简式 官能团
________ ________ 羧基
(_________)
H─C─C─O─H
─
─
=
H
O
H
C2H4O2
CH3COOH
─C─O─H
=
O
必备知识 对点掌握
2.性质
颜色 状态 气味 溶解性 熔点 俗称
无色 液体 刺激性 __溶于水 16.6℃ 冰醋酸
(1)乙酸的物理性质
易
必备知识 对点掌握
2.性质
(2)乙酸的化学性质
①酸的通性
CH3COOH
石蕊溶液
现象:__________
活泼金属(如Na)
_______________________________________
碱性氧化物(如CaO)
碱(如NaOH)
盐(如Na2CO3)
_______________________________________
_______________________________________
_______________________________________
变红
2CH3COOH+2Na → 2CH3COONa+H2↑
2CH3COOH+CaO → (CH3COO)2Ca+H2O
CH3COOH+NaOH → CH3COONa+H2O
CH3COOH+Na2CO3 → 2CH3COONa+H2O+CO2↑
必备知识 对点掌握
2.性质
(2)乙酸的化学性质
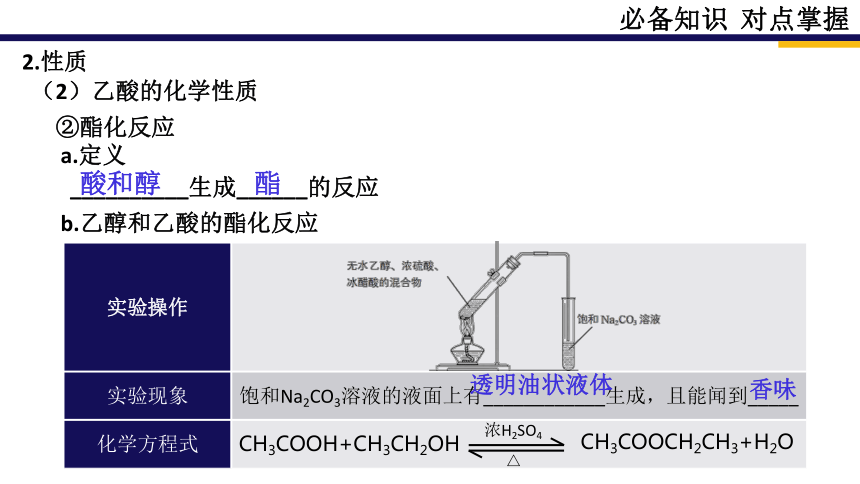
②酯化反应
a.定义
__________生成______的反应
b.乙醇和乙酸的酯化反应
实验操作
实验现象 饱和Na2CO3溶液的液面上有____________生成,且能闻到_____
化学方程式
CH3COOH+CH3CH2OH
浓H2SO4
△
CH3COOCH2CH3+H2O
酸和醇
酯
透明油状液体
香味
必备知识 对点掌握
思考感悟
1.用食醋浸泡有水垢(主要成分为CaCO3)的暖瓶或水壶,可以清除其中的水垢。这是利用了醋酸的什么性质?通过这个事实你能比较出醋酸与碳酸的酸性强弱吗?
用食醋清除水垢是利用了醋酸的酸性,它之所以能清除水垢是因为醋酸能与CaCO3发生反应:2CH3COOH+CaCO3 → (CH3COO)2Ca+H2O+CO2↑
该反应的发生可以说明醋酸的酸性比碳酸的酸性强
必备知识 对点掌握
思考感悟
2.乙酸与乙醇的酯化反应实验装置中,导管末端为何不伸入饱和Na2CO3溶液液面以下?
3.酯化反应属于取代反应吗?
防止倒吸而炸裂试管
属于
必备知识 对点掌握
课堂检测
1.判断正误
(1)可以用水鉴别苯、乙醇、乙酸。
(2)可以用食醋除去水壶中的水垢(以CaCO3为主)。
(3)在酯化反应中,加入过量的乙醇可以使乙酸完全转化为乙酸乙酯。
(4)可以用饱和NaCO3溶液除去乙酸乙酯中的乙醇和乙酸。
( )
( )
( )
( )
×
√
×
√
必备知识 对点掌握
课堂检测
2.分别将一小块钠投入下列物质中,能生成氢气,但生成氢气的速率最慢的是( )
A.盐酸 B.稀硫酸 C.乙醇 D.水
3.下列对酯化反应理解不正确的是( )
A.酯化反应的产物只有酯
B.酯化反应可看成是取代反应的一种
C.酯化反应是有限度的
D.浓硫酸可做酯化反应的催化剂
C
C
目 录
1.必备知识 对点掌握
2.课堂探究 能力提升
课堂探究 能力提升
在做完制取乙酸乙酯的试验后,某化学兴趣小组对实验装置进行了如下改进:
实验探究
探究1:球形干燥管有何作用?
探究2:向试管①中加入试剂时,能否先加入浓硫酸,再加入乙醇和乙酸?
探究3:加热时要求小火缓慢、均匀加热,为什么?还可以采取什么加热方式?
防止倒吸
不能,先加入浓硫酸,再加入乙醇和乙酸,相当于在稀释浓硫酸,会使液体沸腾,使硫酸液滴向四周飞溅
目的:防止乙酸、乙醇的大量挥发和液体的沸腾
还可以用水浴加热的方式进行加热
课堂探究 能力提升
1.羟基氢的活泼性比较
核心归纳
乙醇 水 碳酸 乙酸
羟基氢的活泼性 电离程度
酸碱性
与Na
与NaOH
与NaHCO3
逐渐增强
不电离
中性
中性
部分电离
部分电离
部分电离
弱酸性
弱酸性
√
√
√
√
√
√
√
×
×
×
×
×
课堂探究 能力提升
2.酯化反应
核心归纳
(1)实质:
(2)特点:
(3)试剂加入顺序:
(4)碎瓷片作用:
(5)浓硫酸作用:
(6)饱和Na2CO3作用:
酸脱羟基醇脱氢
可逆反应、取代反应
防止暴沸
乙醇→浓硫酸→乙酸
催化剂、吸水剂
①降低乙酸乙酯的溶解度,便于分层得到酯
②中和挥发出来的乙酸
③溶解挥发出来的乙醇
课堂探究 能力提升
特
提
别
醒
羟基、羧基个数与生成气体的定量关系
(1)Na可以和所有的羟基反应,且物质的量的关系为2Na~2(─OH)~H2
(2)Na2CO3、NaHCO3和─COOH反应产生CO2,物质的量的关系为:
Na2CO3~2(─COOH)~CO2,NaHCO3~─COOH~CO2
课堂探究 能力提升
(不定项)分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是( )
典例体验
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
方法规律:有机物的官能团决定有机物的性质,根据有机物的结构可预测其性质
BC
本 课 结 束
乙 酸
第3节 饮食中的有机化合物
第2课时
学业要求与核心素养
1.能从原子、分子角度认识乙酸的组成、结构,掌握乙酸的物理性质和化学性质(宏观辨识与微观探析)
2.认识官能团与物质性质的关系,形成结构决定性质的学科理念(证据推理与模型认知)
3.掌握酯化反应的原理和实验操作,会书写酯化反应的化学方程式(科学探究与创新意识)
4.养成安全意识和严禁的科学态度,提高科学素养和生活质量,形成节约适度、绿色低碳的生活方式(科学态度与社会责任)
目 录
1.必备知识 对点掌握
2.课堂探究 能力提升
必备知识 对点掌握
1.乙酸的组成和结构
分子式 结构式 结构简式 官能团
________ ________ 羧基
(_________)
H─C─C─O─H
─
─
=
H
O
H
C2H4O2
CH3COOH
─C─O─H
=
O
必备知识 对点掌握
2.性质
颜色 状态 气味 溶解性 熔点 俗称
无色 液体 刺激性 __溶于水 16.6℃ 冰醋酸
(1)乙酸的物理性质
易
必备知识 对点掌握
2.性质
(2)乙酸的化学性质
①酸的通性
CH3COOH
石蕊溶液
现象:__________
活泼金属(如Na)
_______________________________________
碱性氧化物(如CaO)
碱(如NaOH)
盐(如Na2CO3)
_______________________________________
_______________________________________
_______________________________________
变红
2CH3COOH+2Na → 2CH3COONa+H2↑
2CH3COOH+CaO → (CH3COO)2Ca+H2O
CH3COOH+NaOH → CH3COONa+H2O
CH3COOH+Na2CO3 → 2CH3COONa+H2O+CO2↑
必备知识 对点掌握
2.性质
(2)乙酸的化学性质
②酯化反应
a.定义
__________生成______的反应
b.乙醇和乙酸的酯化反应
实验操作
实验现象 饱和Na2CO3溶液的液面上有____________生成,且能闻到_____
化学方程式
CH3COOH+CH3CH2OH
浓H2SO4
△
CH3COOCH2CH3+H2O
酸和醇
酯
透明油状液体
香味
必备知识 对点掌握
思考感悟
1.用食醋浸泡有水垢(主要成分为CaCO3)的暖瓶或水壶,可以清除其中的水垢。这是利用了醋酸的什么性质?通过这个事实你能比较出醋酸与碳酸的酸性强弱吗?
用食醋清除水垢是利用了醋酸的酸性,它之所以能清除水垢是因为醋酸能与CaCO3发生反应:2CH3COOH+CaCO3 → (CH3COO)2Ca+H2O+CO2↑
该反应的发生可以说明醋酸的酸性比碳酸的酸性强
必备知识 对点掌握
思考感悟
2.乙酸与乙醇的酯化反应实验装置中,导管末端为何不伸入饱和Na2CO3溶液液面以下?
3.酯化反应属于取代反应吗?
防止倒吸而炸裂试管
属于
必备知识 对点掌握
课堂检测
1.判断正误
(1)可以用水鉴别苯、乙醇、乙酸。
(2)可以用食醋除去水壶中的水垢(以CaCO3为主)。
(3)在酯化反应中,加入过量的乙醇可以使乙酸完全转化为乙酸乙酯。
(4)可以用饱和NaCO3溶液除去乙酸乙酯中的乙醇和乙酸。
( )
( )
( )
( )
×
√
×
√
必备知识 对点掌握
课堂检测
2.分别将一小块钠投入下列物质中,能生成氢气,但生成氢气的速率最慢的是( )
A.盐酸 B.稀硫酸 C.乙醇 D.水
3.下列对酯化反应理解不正确的是( )
A.酯化反应的产物只有酯
B.酯化反应可看成是取代反应的一种
C.酯化反应是有限度的
D.浓硫酸可做酯化反应的催化剂
C
C
目 录
1.必备知识 对点掌握
2.课堂探究 能力提升
课堂探究 能力提升
在做完制取乙酸乙酯的试验后,某化学兴趣小组对实验装置进行了如下改进:
实验探究
探究1:球形干燥管有何作用?
探究2:向试管①中加入试剂时,能否先加入浓硫酸,再加入乙醇和乙酸?
探究3:加热时要求小火缓慢、均匀加热,为什么?还可以采取什么加热方式?
防止倒吸
不能,先加入浓硫酸,再加入乙醇和乙酸,相当于在稀释浓硫酸,会使液体沸腾,使硫酸液滴向四周飞溅
目的:防止乙酸、乙醇的大量挥发和液体的沸腾
还可以用水浴加热的方式进行加热
课堂探究 能力提升
1.羟基氢的活泼性比较
核心归纳
乙醇 水 碳酸 乙酸
羟基氢的活泼性 电离程度
酸碱性
与Na
与NaOH
与NaHCO3
逐渐增强
不电离
中性
中性
部分电离
部分电离
部分电离
弱酸性
弱酸性
√
√
√
√
√
√
√
×
×
×
×
×
课堂探究 能力提升
2.酯化反应
核心归纳
(1)实质:
(2)特点:
(3)试剂加入顺序:
(4)碎瓷片作用:
(5)浓硫酸作用:
(6)饱和Na2CO3作用:
酸脱羟基醇脱氢
可逆反应、取代反应
防止暴沸
乙醇→浓硫酸→乙酸
催化剂、吸水剂
①降低乙酸乙酯的溶解度,便于分层得到酯
②中和挥发出来的乙酸
③溶解挥发出来的乙醇
课堂探究 能力提升
特
提
别
醒
羟基、羧基个数与生成气体的定量关系
(1)Na可以和所有的羟基反应,且物质的量的关系为2Na~2(─OH)~H2
(2)Na2CO3、NaHCO3和─COOH反应产生CO2,物质的量的关系为:
Na2CO3~2(─COOH)~CO2,NaHCO3~─COOH~CO2
课堂探究 能力提升
(不定项)分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是( )
典例体验
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
方法规律:有机物的官能团决定有机物的性质,根据有机物的结构可预测其性质
BC
本 课 结 束
