人教版九年级上册(新)第三单元《课题3 元素》课件
文档属性
| 名称 | 人教版九年级上册(新)第三单元《课题3 元素》课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-11-24 00:00:00 | ||
图片预览






文档简介
课件30张PPT。《元素》课件
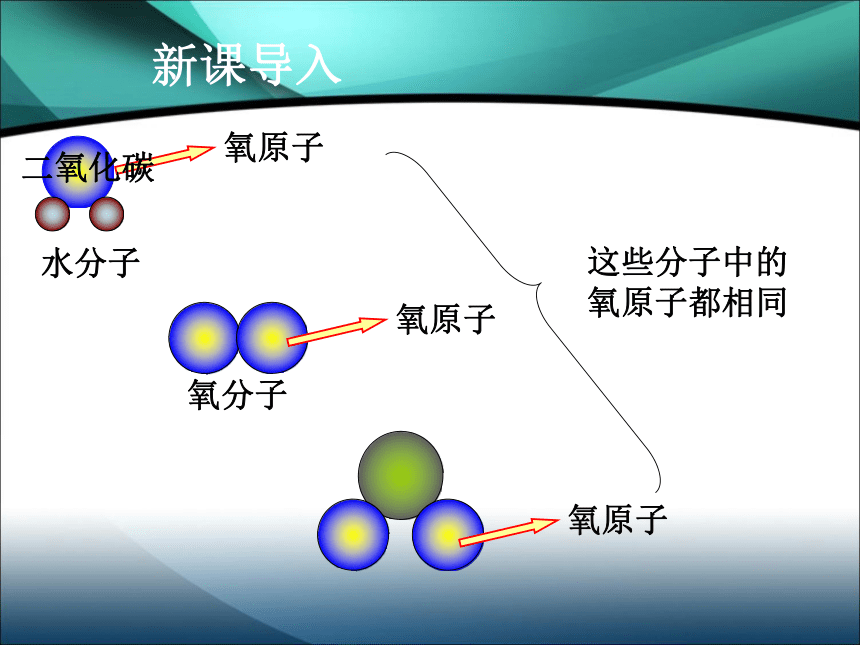
(第1课时)氧气是由 组成。新课导入氧元素氧气新课导入水是由 组成。氢、氧两种元素水氧原子氧原子氧原子这些分子中的
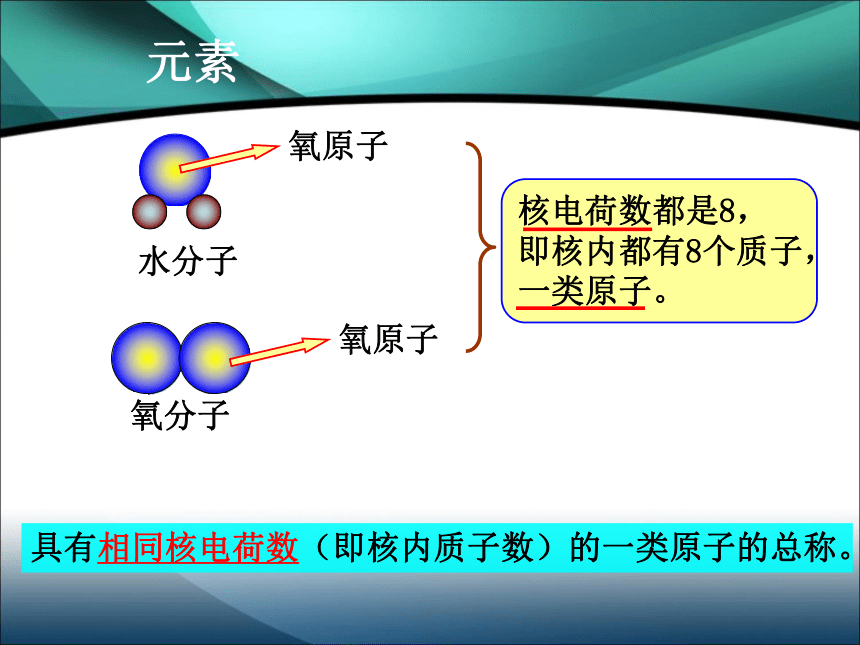
氧原子都相同新课导入二氧化碳元素具有相同核电荷数(即核内质子数)的一类原子的总称。氧原子氧原子物质的种类:2000 多万种
元素的种类:100 余种元素金属元素 —— 钠(Na)、镁(Mg)、
铝(Al)、铁(Fe)、
汞(Hg)、金(Au )……
非金属元素—— 碳(C)、氮(N)、
氧(O)、硫(S)、
氯( Cl )……
稀有气体元素—— 氦(He)、氖(Ne)、
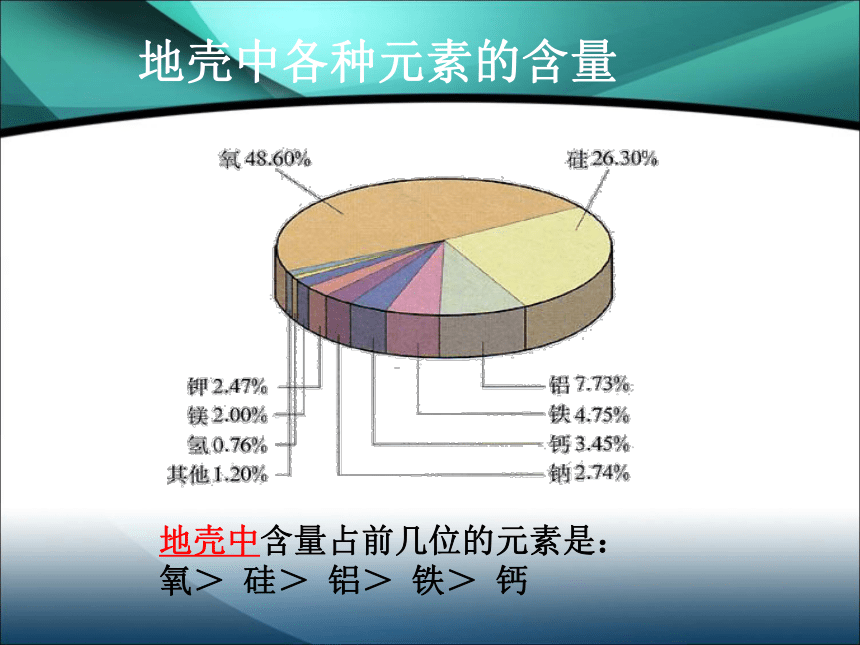
氩(Ar)……元素的分类:地壳中含量占前几位的元素是:
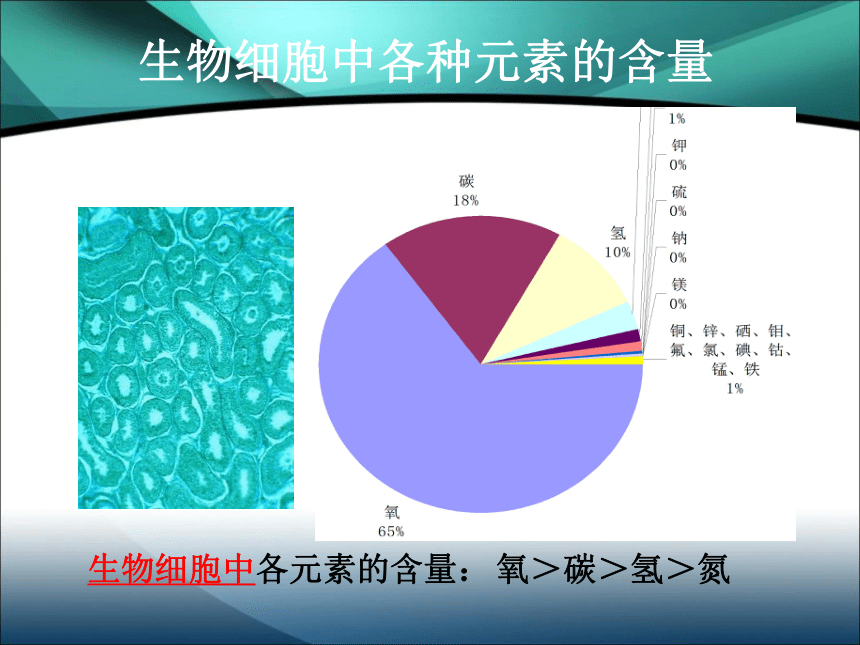
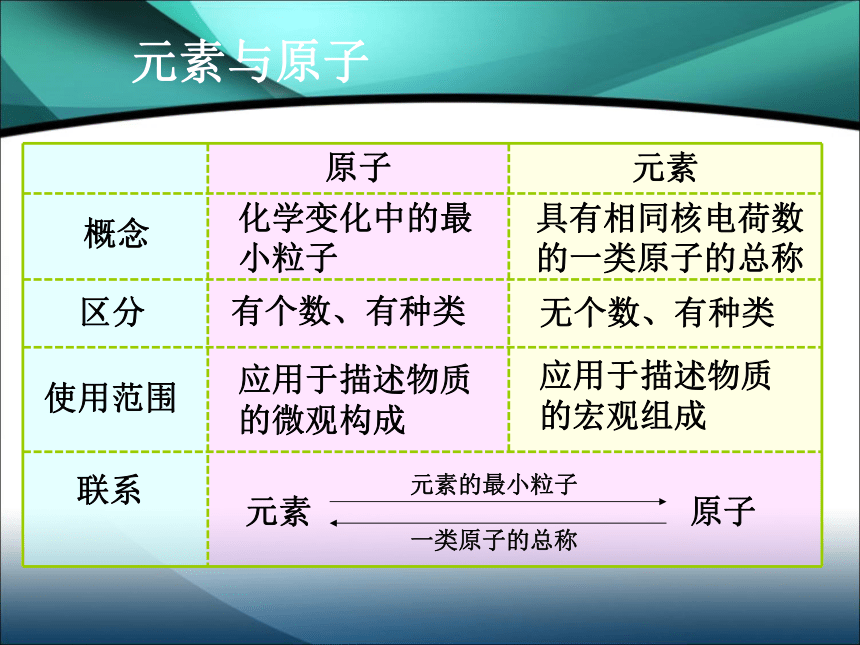
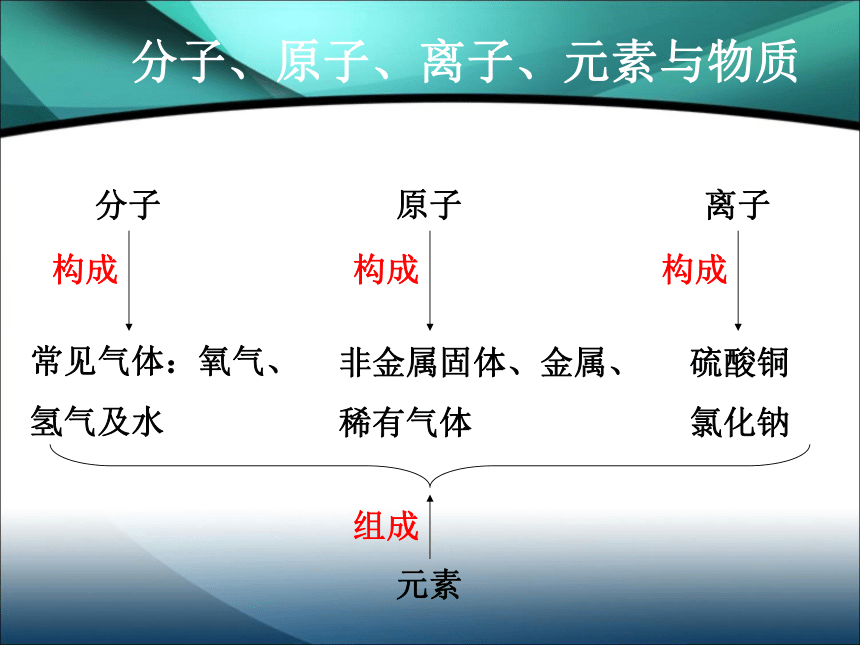
氧> 硅> 铝> 铁> 钙地壳中各种元素的含量生物细胞中各元素的含量:氧>碳>氢>氮生物细胞中各种元素的含量奶类豆类钙片——补钙动物肝脏黑木耳蛋类——补铁身边的元素元素与原子化学变化中的最小粒子具有相同核电荷数的一类原子的总称概念 区分 使用范围联系 有个数、有种类无个数、有种类应用于描述物质的宏观组成应用于描述物质的微观构成元素元素的最小粒子原子一类原子的总称分子构成常见气体:氧气、
氢气及水原子非金属固体、金属、
稀有气体构成离子硫酸铜
氯化钠构成元素分子、原子、离子、元素与物质组成元素就是具有相同核电荷数(即核内质子数)的一类原子的总称。
元素与原子的联系与区别:
课堂小结化学变化中的最小粒子具有相同核电荷数的一类原子的总称概念 区分 使用范围联系 有个数、有种类无个数、有种类描述物质宏观组成描述物质微观构成元素元素的最小粒子原子一类原子的总称1.一种元素与另一种元素最本质的区别在于( )。
A.质子数 B.中子数
C.电子数 D.相对原子质量A 2.决定元素种类的粒子是( )。
A.质子数 B.中子数
C.电子数 D.最外层电子数A3.同种元素的原子一定相同的是( )。
A.相对原子质量 B.质子数
C.中子数 D.电子数B课堂练习《元素》课件
(第2课时)知识回顾1.具有 (即 )一类原子的总称。质子数相同核电荷数2.地壳中含量最多的元素是 。生物细胞中含量最多的元素是 。氧元素氧元素3.决定元素种类的是 。核电荷数历史上,道尔顿曾用图形加字母的方式作为元素符号。 元素符号元素符号的发展:元素符号常见元素中英文名称对照表元素符号的书写:(1)由一个字母表示的元素符号要大写,如氢H、氧O、氮N。
(2)由两个字母表示的元素符号第一个字母要大写,第二个字母要小写如氦He、铁Fe、锌Zn、钙Ca、氯Cl、氦He、镁Mg。 (1)表示一种元素;
(2)表示该元素的一个原子。HFe例如:氢元素一个氢原子铁元素一个铁原子铁元素符号的意义:2H3Fe两个氢原子三个铁原子元素符号的书写:记住并会正确书写下列元素符号:
氢 氦 碳 氮 氧 氟 氖
H He C N O F Ne
钠 镁 铝 硅 磷 硫 氯
Na Mg Al Si P S Cl
氩 钾 钙 锰 铁 铜 锌
Ar K Ca Mn Fe Cu Zn
银 钡 汞 金
Ag Ba Hg Au元素符号的书写:元素周期表简介 1869年2月,俄国化学家门捷列夫发现了他的第一张元素周期表,表中除收入了当时已知的63种元素外,还给尚未发现的元素留下了27个空位,并大胆地预言了11种未知的新元素和它们在元素周期表的位置,同时根据它们的性质取了名字,如类铝、类硼、类硅等,后来都得到了验证。门捷列夫7个横行18个纵列(周期)(族)原子序数= 核电荷数金属元素区非金属元素区元素周期表的意义:(1)为寻找新元素提供了理论依据。
(2)由于元素周期表中位置越接近的元素化学性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、催化剂、农药)。半导体材料课堂小结(1)由一个字母表示的元素符号要大写如氢H、氧O。
(2)由两个字母表示的元素符号第一个字母要大
写,第二个字母要小写如氦He、铁Fe、锌Zn 。 元素符号的书写:元素符号的含义:(1)表示一种元素;
(2)表示该元素的一个原子。元素周期表课堂练习:1.下列两组符号可以组合成哪些元素的符号?并说出元素的类别。
⑴ A B C M N
⑵ a u e l g2.如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。试回答下列问题:
(1)钠元素的原子序数为 ,画出它的原子结构示意图为
(2)A、B、C中属于同种元素的粒子是 。11B和C课堂练习:
(第1课时)氧气是由 组成。新课导入氧元素氧气新课导入水是由 组成。氢、氧两种元素水氧原子氧原子氧原子这些分子中的
氧原子都相同新课导入二氧化碳元素具有相同核电荷数(即核内质子数)的一类原子的总称。氧原子氧原子物质的种类:2000 多万种
元素的种类:100 余种元素金属元素 —— 钠(Na)、镁(Mg)、
铝(Al)、铁(Fe)、
汞(Hg)、金(Au )……
非金属元素—— 碳(C)、氮(N)、
氧(O)、硫(S)、
氯( Cl )……
稀有气体元素—— 氦(He)、氖(Ne)、
氩(Ar)……元素的分类:地壳中含量占前几位的元素是:
氧> 硅> 铝> 铁> 钙地壳中各种元素的含量生物细胞中各元素的含量:氧>碳>氢>氮生物细胞中各种元素的含量奶类豆类钙片——补钙动物肝脏黑木耳蛋类——补铁身边的元素元素与原子化学变化中的最小粒子具有相同核电荷数的一类原子的总称概念 区分 使用范围联系 有个数、有种类无个数、有种类应用于描述物质的宏观组成应用于描述物质的微观构成元素元素的最小粒子原子一类原子的总称分子构成常见气体:氧气、
氢气及水原子非金属固体、金属、
稀有气体构成离子硫酸铜
氯化钠构成元素分子、原子、离子、元素与物质组成元素就是具有相同核电荷数(即核内质子数)的一类原子的总称。
元素与原子的联系与区别:
课堂小结化学变化中的最小粒子具有相同核电荷数的一类原子的总称概念 区分 使用范围联系 有个数、有种类无个数、有种类描述物质宏观组成描述物质微观构成元素元素的最小粒子原子一类原子的总称1.一种元素与另一种元素最本质的区别在于( )。
A.质子数 B.中子数
C.电子数 D.相对原子质量A 2.决定元素种类的粒子是( )。
A.质子数 B.中子数
C.电子数 D.最外层电子数A3.同种元素的原子一定相同的是( )。
A.相对原子质量 B.质子数
C.中子数 D.电子数B课堂练习《元素》课件
(第2课时)知识回顾1.具有 (即 )一类原子的总称。质子数相同核电荷数2.地壳中含量最多的元素是 。生物细胞中含量最多的元素是 。氧元素氧元素3.决定元素种类的是 。核电荷数历史上,道尔顿曾用图形加字母的方式作为元素符号。 元素符号元素符号的发展:元素符号常见元素中英文名称对照表元素符号的书写:(1)由一个字母表示的元素符号要大写,如氢H、氧O、氮N。
(2)由两个字母表示的元素符号第一个字母要大写,第二个字母要小写如氦He、铁Fe、锌Zn、钙Ca、氯Cl、氦He、镁Mg。 (1)表示一种元素;
(2)表示该元素的一个原子。HFe例如:氢元素一个氢原子铁元素一个铁原子铁元素符号的意义:2H3Fe两个氢原子三个铁原子元素符号的书写:记住并会正确书写下列元素符号:
氢 氦 碳 氮 氧 氟 氖
H He C N O F Ne
钠 镁 铝 硅 磷 硫 氯
Na Mg Al Si P S Cl
氩 钾 钙 锰 铁 铜 锌
Ar K Ca Mn Fe Cu Zn
银 钡 汞 金
Ag Ba Hg Au元素符号的书写:元素周期表简介 1869年2月,俄国化学家门捷列夫发现了他的第一张元素周期表,表中除收入了当时已知的63种元素外,还给尚未发现的元素留下了27个空位,并大胆地预言了11种未知的新元素和它们在元素周期表的位置,同时根据它们的性质取了名字,如类铝、类硼、类硅等,后来都得到了验证。门捷列夫7个横行18个纵列(周期)(族)原子序数= 核电荷数金属元素区非金属元素区元素周期表的意义:(1)为寻找新元素提供了理论依据。
(2)由于元素周期表中位置越接近的元素化学性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、催化剂、农药)。半导体材料课堂小结(1)由一个字母表示的元素符号要大写如氢H、氧O。
(2)由两个字母表示的元素符号第一个字母要大
写,第二个字母要小写如氦He、铁Fe、锌Zn 。 元素符号的书写:元素符号的含义:(1)表示一种元素;
(2)表示该元素的一个原子。元素周期表课堂练习:1.下列两组符号可以组合成哪些元素的符号?并说出元素的类别。
⑴ A B C M N
⑵ a u e l g2.如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。试回答下列问题:
(1)钠元素的原子序数为 ,画出它的原子结构示意图为
(2)A、B、C中属于同种元素的粒子是 。11B和C课堂练习:
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
