2025江苏版新教材化学高考第一轮基础练习--专题六 非金属及其化合物 拓展训练(含答案)
文档属性
| 名称 | 2025江苏版新教材化学高考第一轮基础练习--专题六 非金属及其化合物 拓展训练(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 809.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-16 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
2025江苏版新教材化学高考第一轮
专题六 非金属及其化合物
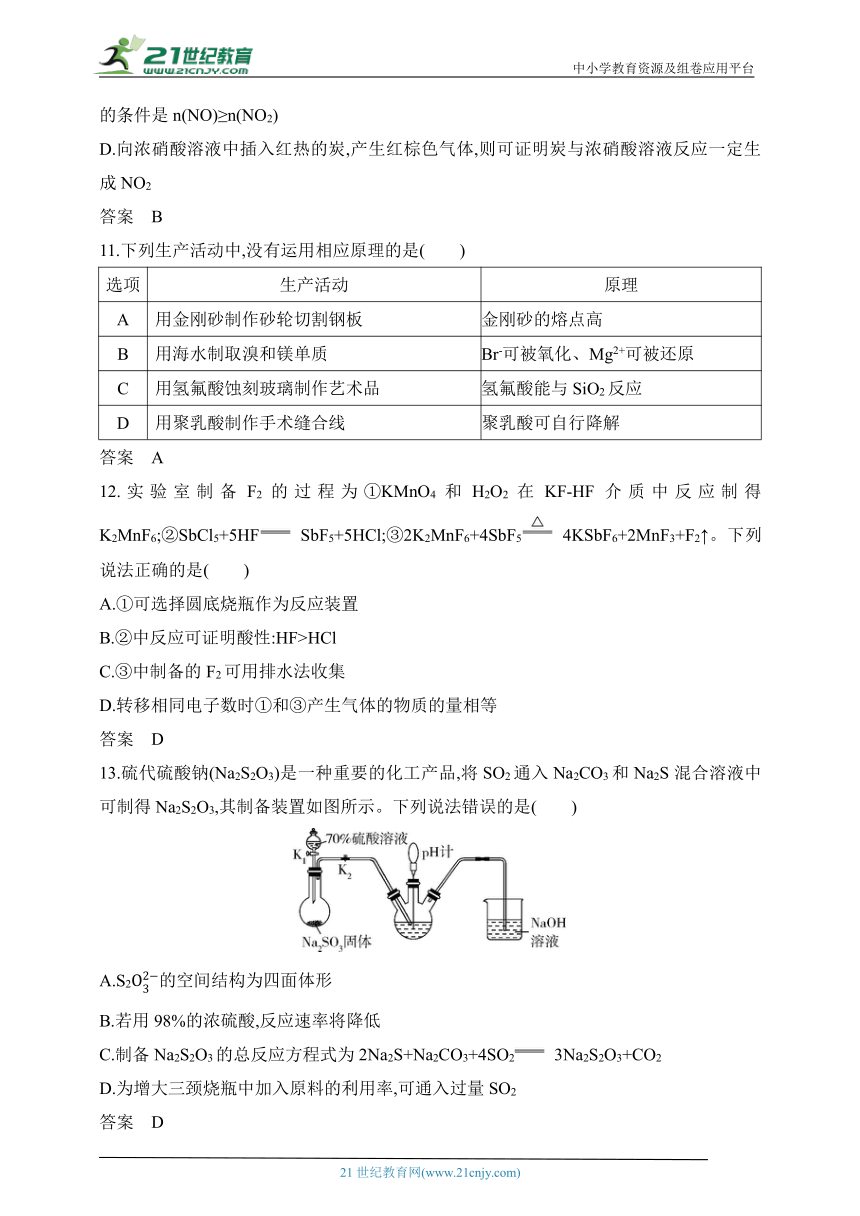
1.考古遗迹和历史文物是历史的见证,反映了古代人民丰富多彩的生活。下列文物属于无机非金属材料的是 ( )
铜烤炉 黄花梨云 龙纹条案 三彩骑卧 驼陶俑 山居图 扇面
A B C D
答案 C
5. “空气吹出法”海水提溴的工艺流程如图,下列说法错误的是( )
A.进入吹出塔前,Br-被氧化为Br2
B.吸收塔中SO2作还原剂
C.经过吸收塔后,溴元素得到富集
D.两次通入水蒸气的作用都是参加反应
答案 D
3.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与b可生成SO2
B.SO2通入紫色石蕊溶液先变红后褪色
C.c在空气中燃烧生成SO2
D.d既可被氧化,也可被还原
答案 B
4.下列有关含氮化合物的反应中,对应的离子方程式书写正确的是( )
A.将过量SO2通入冷氨水中:NH3·H2O+SO2 HS
B.室温下用稀硝酸溶解铜:Cu+4H++2N Cu2++2NO2↑+2H2O
C.NO2溶于水制硝酸:2NO2+2H2O H++N+NO
D.等体积、等浓度的NH4HSO4溶液与NaOH溶液混合:N+OH- NH3·H2O
答案 A
5.含氯化合物的反应具有多样性。下列有关反应的离子方程式书写不正确的是( )
A.将Cl2通入冷的石灰乳中制备漂白粉:Cl2+2OH- Cl-+ClO-+H2O
B.向AgCl悬浊液中通入NH3:AgCl+2NH3 [Ag(NH3)2]++Cl-
C.利用MnO2和浓盐酸反应制备Cl2:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
D.将SO2通入酸性NaClO3溶液中制备ClO2:2Cl+SO2 2ClO2+S
答案 A
6.陶土网是由两片铁丝网夹着一张浸泡过陶土水后晾干的棉布制成,其功能和石棉网一样,但安全性更高,对人体的危害性更小。下列说法错误的是( )
A.陶土和石棉都是硅酸盐材料
B.陶土性质稳定,在高温下不易分解
C.蒸发实验中,蒸发皿需垫上陶土网再加热
D.一种石棉化学式为Mg6Si4O10(OH)8,其氧化物形式可写为3MgO·2SiO2·2H2O
答案 C
7.我国航天技术的进步离不开新技术和新材料的应用。下列说法正确的是( )
A.飞船建造通常用镁、铝、钛等合金,合金的熔点一定比各成分金属低
B.火箭使用碳纳米管可以减轻火箭质量,这种材料属于有机高分子材料
C.飞船船体覆盖的耐高温陶瓷材料属于新型无机非金属材料
D.太阳能电池翼伸展机构关键部件用到的SiC属于硅酸盐材料
答案 C
8.氯元素的化合价与部分物质类别的对应关系如图所示,据图判断下列说法错误的是( )
A.c在光照条件下很容易分解
B.b不是酸性氧化物,因为它没有对应的含氧酸
C.图中a、b、c、d、e五种物质中均含有共价键,且c、d、e属于电解质
D.将a通入NaOH溶液中,已知生成NaCl、NaClO和d的混合物,若n(NaClO)与n(d)之比为3∶1,则氧化剂与还原剂的物质的量之比为2∶1
答案 B
9.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与足量Cu加热反应后,剩余溶液加入碳酸氢钠溶液有气体放出
B.SO2通入紫色石蕊试液先变红后褪色
C.b溶液在空气中久置后溶液变浑浊
D.d既可被氧化,也可被还原
答案 B
10.空气中的氮气可通过人工固氮获得氨气,氨气是重要的化工原料,通过氨氧化法可制得硝酸,反应过程如下图:
N2NH3NONO2HNO3
硝酸是一种强氧化性酸,制硝酸工业产生的尾气中含有氮氧化物(NOx),应处理后才能排放。下列说法正确的是( )
A.BaSO3固体能溶于稀硝酸,生成Ba(NO3)2,同时放出SO2气体
B.工业上,当转化①的反应达到平衡时,需不断地从混合气体中分离出NH3,将未反应的原料气送回合成塔以提高原料的利用率
C.工业尾气中NOx常用碱液吸收处理,NO、NO2的混合气体能被足量烧碱溶液完全吸收的条件是n(NO)≥n(NO2)
D.向浓硝酸溶液中插入红热的炭,产生红棕色气体,则可证明炭与浓硝酸溶液反应一定生成NO2
答案 B
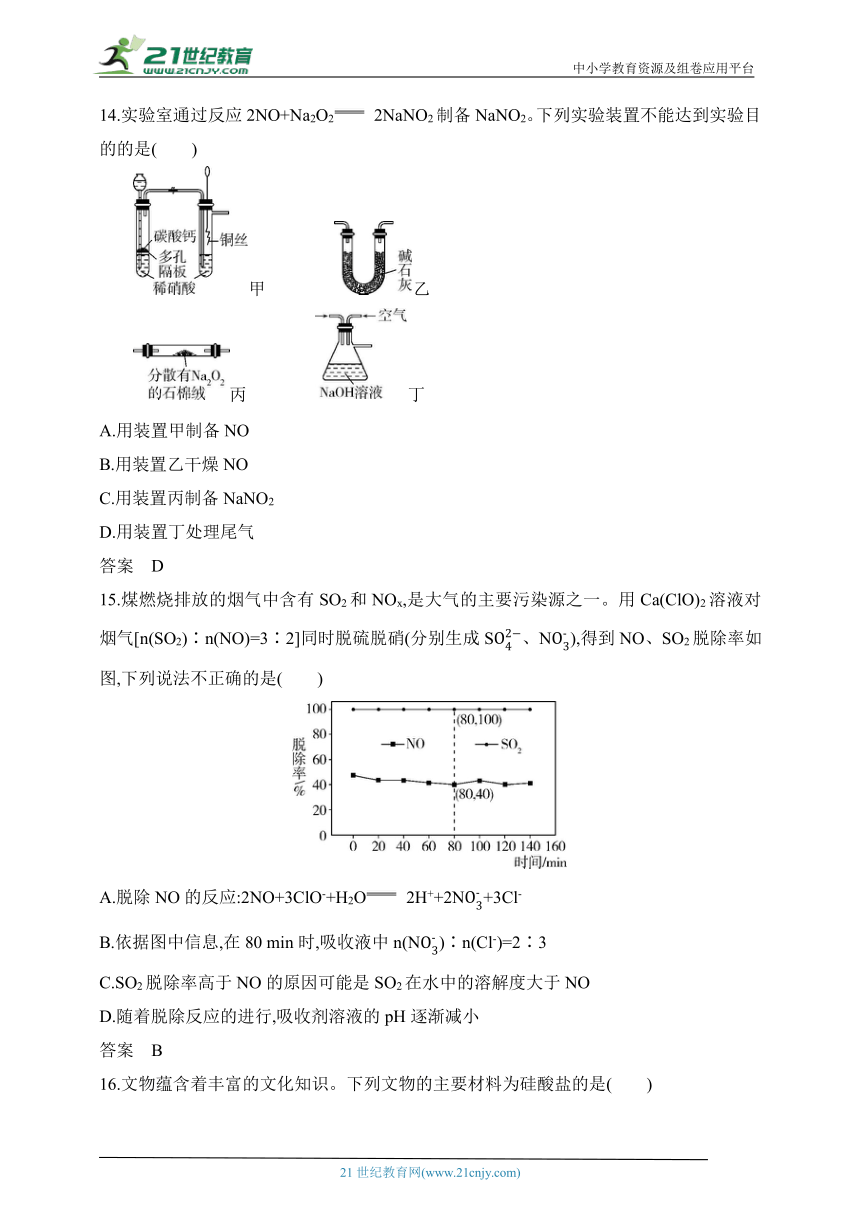
11.下列生产活动中,没有运用相应原理的是( )
选项 生产活动 原理
A 用金刚砂制作砂轮切割钢板 金刚砂的熔点高
B 用海水制取溴和镁单质 Br-可被氧化、Mg2+可被还原
C 用氢氟酸蚀刻玻璃制作艺术品 氢氟酸能与SiO2反应
D 用聚乳酸制作手术缝合线 聚乳酸可自行降解
答案 A
12.实验室制备F2的过程为①KMnO4和H2O2在KF-HF介质中反应制得K2MnF6;②SbCl5+5HF SbF5+5HCl;③2K2MnF6+4SbF5 4KSbF6+2MnF3+F2↑。下列说法正确的是( )
A.①可选择圆底烧瓶作为反应装置
B.②中反应可证明酸性:HF>HCl
C.③中制备的F2可用排水法收集
D.转移相同电子数时①和③产生气体的物质的量相等
答案 D
13.硫代硫酸钠(Na2S2O3)是一种重要的化工产品,将SO2通入Na2CO3和Na2S混合溶液中可制得Na2S2O3,其制备装置如图所示。下列说法错误的是( )
A.S2的空间结构为四面体形
B.若用98%的浓硫酸,反应速率将降低
C.制备Na2S2O3的总反应方程式为2Na2S+Na2CO3+4SO2 3Na2S2O3+CO2
D.为增大三颈烧瓶中加入原料的利用率,可通入过量SO2
答案 D
14.实验室通过反应2NO+Na2O2 2NaNO2制备NaNO2。下列实验装置不能达到实验目的的是( )
甲 乙
丙 丁
A.用装置甲制备NO
B.用装置乙干燥NO
C.用装置丙制备NaNO2
D.用装置丁处理尾气
答案 D
15.煤燃烧排放的烟气中含有SO2和NOx,是大气的主要污染源之一。用Ca(ClO)2溶液对烟气[n(SO2)∶n(NO)=3∶2]同时脱硫脱硝(分别生成S、N),得到NO、SO2脱除率如图,下列说法不正确的是( )
A.脱除NO的反应:2NO+3ClO-+H2O 2H++2N+3Cl-
B.依据图中信息,在80 min时,吸收液中n(N)∶n(Cl-)=2∶3
C.SO2脱除率高于NO的原因可能是SO2在水中的溶解度大于NO
D.随着脱除反应的进行,吸收剂溶液的pH逐渐减小
答案 B
16.文物蕴含着丰富的文化知识。下列文物的主要材料为硅酸盐的是( )
A.春秋箕形方孔脊铜炭铲 B.西晋青瓷羊形四系壶
C.宋双鱼纹银盘 D.《写生花鸟草虫图册》
答案 B
17.NaClO2是一种重要的杀菌消毒剂,一种生产NaClO2的工艺流程如下图所示。已知:“有效氯含量”是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。下列说法错误的是( )
A.该生产过程中,有三处涉及氧化还原反应
B.在电解过程中,NaClO2是还原产物
C.“尾气吸收”反应中,氧化剂与还原剂的物质的量之比为1∶2
D.NaClO2的“有效氯含量”约为1.57 g
答案 C
18.某同学利用如图所示装置探究SO2的性质。下列有关叙述错误的是( )
A.碳酸钠溶液呈碱性,通入SO2前试管①中溶液呈红色
B.持续通入SO2,试管①中溶液的颜色会慢慢褪去
C.通入SO2后,试管②中溶液的红色会褪去,加热试管②,会恢复红色
D.可以用氯化钡溶液进行尾气处理,得到BaSO3沉淀
答案 D
19.自然界中时刻存在着氮的转化。下图为N2分子在催化剂作用下发生一系列转化示意图。
下列叙述正确的是( )
A.N2→NH3,NH3→NO均属于氮的固定
B.使用催化剂a、b均可以提高单位时间内生成物的产量
C.催化剂a、b表面均发生了极性共价键的断裂
D.在催化剂a作用下,氮原子发生了氧化反应
答案 B
20.部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断合理的是( )
A.a可以与少量b'反应有白雾产生
B.工业上通过a→b→c→d→e来制备HNO3
C.浓a'溶液和浓d'溶液反应可以得到b',浓a'溶液和浓c'溶液反应得不到b'
D.加热d'的固态钾盐可以产生O2
答案 D
专题六 非金属及其化合物
1.考古遗迹和历史文物是历史的见证,反映了古代人民丰富多彩的生活。下列文物属于无机非金属材料的是 ( )
铜烤炉 黄花梨云 龙纹条案 三彩骑卧 驼陶俑 山居图 扇面
A B C D
答案 C
5. “空气吹出法”海水提溴的工艺流程如图,下列说法错误的是( )
A.进入吹出塔前,Br-被氧化为Br2
B.吸收塔中SO2作还原剂
C.经过吸收塔后,溴元素得到富集
D.两次通入水蒸气的作用都是参加反应
答案 D
3.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与b可生成SO2
B.SO2通入紫色石蕊溶液先变红后褪色
C.c在空气中燃烧生成SO2
D.d既可被氧化,也可被还原
答案 B
4.下列有关含氮化合物的反应中,对应的离子方程式书写正确的是( )
A.将过量SO2通入冷氨水中:NH3·H2O+SO2 HS
B.室温下用稀硝酸溶解铜:Cu+4H++2N Cu2++2NO2↑+2H2O
C.NO2溶于水制硝酸:2NO2+2H2O H++N+NO
D.等体积、等浓度的NH4HSO4溶液与NaOH溶液混合:N+OH- NH3·H2O
答案 A
5.含氯化合物的反应具有多样性。下列有关反应的离子方程式书写不正确的是( )
A.将Cl2通入冷的石灰乳中制备漂白粉:Cl2+2OH- Cl-+ClO-+H2O
B.向AgCl悬浊液中通入NH3:AgCl+2NH3 [Ag(NH3)2]++Cl-
C.利用MnO2和浓盐酸反应制备Cl2:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
D.将SO2通入酸性NaClO3溶液中制备ClO2:2Cl+SO2 2ClO2+S
答案 A
6.陶土网是由两片铁丝网夹着一张浸泡过陶土水后晾干的棉布制成,其功能和石棉网一样,但安全性更高,对人体的危害性更小。下列说法错误的是( )
A.陶土和石棉都是硅酸盐材料
B.陶土性质稳定,在高温下不易分解
C.蒸发实验中,蒸发皿需垫上陶土网再加热
D.一种石棉化学式为Mg6Si4O10(OH)8,其氧化物形式可写为3MgO·2SiO2·2H2O
答案 C
7.我国航天技术的进步离不开新技术和新材料的应用。下列说法正确的是( )
A.飞船建造通常用镁、铝、钛等合金,合金的熔点一定比各成分金属低
B.火箭使用碳纳米管可以减轻火箭质量,这种材料属于有机高分子材料
C.飞船船体覆盖的耐高温陶瓷材料属于新型无机非金属材料
D.太阳能电池翼伸展机构关键部件用到的SiC属于硅酸盐材料
答案 C
8.氯元素的化合价与部分物质类别的对应关系如图所示,据图判断下列说法错误的是( )
A.c在光照条件下很容易分解
B.b不是酸性氧化物,因为它没有对应的含氧酸
C.图中a、b、c、d、e五种物质中均含有共价键,且c、d、e属于电解质
D.将a通入NaOH溶液中,已知生成NaCl、NaClO和d的混合物,若n(NaClO)与n(d)之比为3∶1,则氧化剂与还原剂的物质的量之比为2∶1
答案 B
9.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与足量Cu加热反应后,剩余溶液加入碳酸氢钠溶液有气体放出
B.SO2通入紫色石蕊试液先变红后褪色
C.b溶液在空气中久置后溶液变浑浊
D.d既可被氧化,也可被还原
答案 B
10.空气中的氮气可通过人工固氮获得氨气,氨气是重要的化工原料,通过氨氧化法可制得硝酸,反应过程如下图:
N2NH3NONO2HNO3
硝酸是一种强氧化性酸,制硝酸工业产生的尾气中含有氮氧化物(NOx),应处理后才能排放。下列说法正确的是( )
A.BaSO3固体能溶于稀硝酸,生成Ba(NO3)2,同时放出SO2气体
B.工业上,当转化①的反应达到平衡时,需不断地从混合气体中分离出NH3,将未反应的原料气送回合成塔以提高原料的利用率
C.工业尾气中NOx常用碱液吸收处理,NO、NO2的混合气体能被足量烧碱溶液完全吸收的条件是n(NO)≥n(NO2)
D.向浓硝酸溶液中插入红热的炭,产生红棕色气体,则可证明炭与浓硝酸溶液反应一定生成NO2
答案 B
11.下列生产活动中,没有运用相应原理的是( )
选项 生产活动 原理
A 用金刚砂制作砂轮切割钢板 金刚砂的熔点高
B 用海水制取溴和镁单质 Br-可被氧化、Mg2+可被还原
C 用氢氟酸蚀刻玻璃制作艺术品 氢氟酸能与SiO2反应
D 用聚乳酸制作手术缝合线 聚乳酸可自行降解
答案 A
12.实验室制备F2的过程为①KMnO4和H2O2在KF-HF介质中反应制得K2MnF6;②SbCl5+5HF SbF5+5HCl;③2K2MnF6+4SbF5 4KSbF6+2MnF3+F2↑。下列说法正确的是( )
A.①可选择圆底烧瓶作为反应装置
B.②中反应可证明酸性:HF>HCl
C.③中制备的F2可用排水法收集
D.转移相同电子数时①和③产生气体的物质的量相等
答案 D
13.硫代硫酸钠(Na2S2O3)是一种重要的化工产品,将SO2通入Na2CO3和Na2S混合溶液中可制得Na2S2O3,其制备装置如图所示。下列说法错误的是( )
A.S2的空间结构为四面体形
B.若用98%的浓硫酸,反应速率将降低
C.制备Na2S2O3的总反应方程式为2Na2S+Na2CO3+4SO2 3Na2S2O3+CO2
D.为增大三颈烧瓶中加入原料的利用率,可通入过量SO2
答案 D
14.实验室通过反应2NO+Na2O2 2NaNO2制备NaNO2。下列实验装置不能达到实验目的的是( )
甲 乙
丙 丁
A.用装置甲制备NO
B.用装置乙干燥NO
C.用装置丙制备NaNO2
D.用装置丁处理尾气
答案 D
15.煤燃烧排放的烟气中含有SO2和NOx,是大气的主要污染源之一。用Ca(ClO)2溶液对烟气[n(SO2)∶n(NO)=3∶2]同时脱硫脱硝(分别生成S、N),得到NO、SO2脱除率如图,下列说法不正确的是( )
A.脱除NO的反应:2NO+3ClO-+H2O 2H++2N+3Cl-
B.依据图中信息,在80 min时,吸收液中n(N)∶n(Cl-)=2∶3
C.SO2脱除率高于NO的原因可能是SO2在水中的溶解度大于NO
D.随着脱除反应的进行,吸收剂溶液的pH逐渐减小
答案 B
16.文物蕴含着丰富的文化知识。下列文物的主要材料为硅酸盐的是( )
A.春秋箕形方孔脊铜炭铲 B.西晋青瓷羊形四系壶
C.宋双鱼纹银盘 D.《写生花鸟草虫图册》
答案 B
17.NaClO2是一种重要的杀菌消毒剂,一种生产NaClO2的工艺流程如下图所示。已知:“有效氯含量”是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。下列说法错误的是( )
A.该生产过程中,有三处涉及氧化还原反应
B.在电解过程中,NaClO2是还原产物
C.“尾气吸收”反应中,氧化剂与还原剂的物质的量之比为1∶2
D.NaClO2的“有效氯含量”约为1.57 g
答案 C
18.某同学利用如图所示装置探究SO2的性质。下列有关叙述错误的是( )
A.碳酸钠溶液呈碱性,通入SO2前试管①中溶液呈红色
B.持续通入SO2,试管①中溶液的颜色会慢慢褪去
C.通入SO2后,试管②中溶液的红色会褪去,加热试管②,会恢复红色
D.可以用氯化钡溶液进行尾气处理,得到BaSO3沉淀
答案 D
19.自然界中时刻存在着氮的转化。下图为N2分子在催化剂作用下发生一系列转化示意图。
下列叙述正确的是( )
A.N2→NH3,NH3→NO均属于氮的固定
B.使用催化剂a、b均可以提高单位时间内生成物的产量
C.催化剂a、b表面均发生了极性共价键的断裂
D.在催化剂a作用下,氮原子发生了氧化反应
答案 B
20.部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断合理的是( )
A.a可以与少量b'反应有白雾产生
B.工业上通过a→b→c→d→e来制备HNO3
C.浓a'溶液和浓d'溶液反应可以得到b',浓a'溶液和浓c'溶液反应得不到b'
D.加热d'的固态钾盐可以产生O2
答案 D
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025江苏版新教材化学高考第一轮
专题六 非金属及其化合物
1.考古遗迹和历史文物是历史的见证,反映了古代人民丰富多彩的生活。下列文物属于无机非金属材料的是 ( )
铜烤炉 黄花梨云 龙纹条案 三彩骑卧 驼陶俑 山居图 扇面
A B C D
答案 C
5. “空气吹出法”海水提溴的工艺流程如图,下列说法错误的是( )
A.进入吹出塔前,Br-被氧化为Br2
B.吸收塔中SO2作还原剂
C.经过吸收塔后,溴元素得到富集
D.两次通入水蒸气的作用都是参加反应
答案 D
3.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与b可生成SO2
B.SO2通入紫色石蕊溶液先变红后褪色
C.c在空气中燃烧生成SO2
D.d既可被氧化,也可被还原
答案 B
4.下列有关含氮化合物的反应中,对应的离子方程式书写正确的是( )
A.将过量SO2通入冷氨水中:NH3·H2O+SO2 HS
B.室温下用稀硝酸溶解铜:Cu+4H++2N Cu2++2NO2↑+2H2O
C.NO2溶于水制硝酸:2NO2+2H2O H++N+NO
D.等体积、等浓度的NH4HSO4溶液与NaOH溶液混合:N+OH- NH3·H2O
答案 A
5.含氯化合物的反应具有多样性。下列有关反应的离子方程式书写不正确的是( )
A.将Cl2通入冷的石灰乳中制备漂白粉:Cl2+2OH- Cl-+ClO-+H2O
B.向AgCl悬浊液中通入NH3:AgCl+2NH3 [Ag(NH3)2]++Cl-
C.利用MnO2和浓盐酸反应制备Cl2:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
D.将SO2通入酸性NaClO3溶液中制备ClO2:2Cl+SO2 2ClO2+S
答案 A
6.陶土网是由两片铁丝网夹着一张浸泡过陶土水后晾干的棉布制成,其功能和石棉网一样,但安全性更高,对人体的危害性更小。下列说法错误的是( )
A.陶土和石棉都是硅酸盐材料
B.陶土性质稳定,在高温下不易分解
C.蒸发实验中,蒸发皿需垫上陶土网再加热
D.一种石棉化学式为Mg6Si4O10(OH)8,其氧化物形式可写为3MgO·2SiO2·2H2O
答案 C
7.我国航天技术的进步离不开新技术和新材料的应用。下列说法正确的是( )
A.飞船建造通常用镁、铝、钛等合金,合金的熔点一定比各成分金属低
B.火箭使用碳纳米管可以减轻火箭质量,这种材料属于有机高分子材料
C.飞船船体覆盖的耐高温陶瓷材料属于新型无机非金属材料
D.太阳能电池翼伸展机构关键部件用到的SiC属于硅酸盐材料
答案 C
8.氯元素的化合价与部分物质类别的对应关系如图所示,据图判断下列说法错误的是( )
A.c在光照条件下很容易分解
B.b不是酸性氧化物,因为它没有对应的含氧酸
C.图中a、b、c、d、e五种物质中均含有共价键,且c、d、e属于电解质
D.将a通入NaOH溶液中,已知生成NaCl、NaClO和d的混合物,若n(NaClO)与n(d)之比为3∶1,则氧化剂与还原剂的物质的量之比为2∶1
答案 B
9.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与足量Cu加热反应后,剩余溶液加入碳酸氢钠溶液有气体放出
B.SO2通入紫色石蕊试液先变红后褪色
C.b溶液在空气中久置后溶液变浑浊
D.d既可被氧化,也可被还原
答案 B
10.空气中的氮气可通过人工固氮获得氨气,氨气是重要的化工原料,通过氨氧化法可制得硝酸,反应过程如下图:
N2NH3NONO2HNO3
硝酸是一种强氧化性酸,制硝酸工业产生的尾气中含有氮氧化物(NOx),应处理后才能排放。下列说法正确的是( )
A.BaSO3固体能溶于稀硝酸,生成Ba(NO3)2,同时放出SO2气体
B.工业上,当转化①的反应达到平衡时,需不断地从混合气体中分离出NH3,将未反应的原料气送回合成塔以提高原料的利用率
C.工业尾气中NOx常用碱液吸收处理,NO、NO2的混合气体能被足量烧碱溶液完全吸收的条件是n(NO)≥n(NO2)
D.向浓硝酸溶液中插入红热的炭,产生红棕色气体,则可证明炭与浓硝酸溶液反应一定生成NO2
答案 B
11.下列生产活动中,没有运用相应原理的是( )
选项 生产活动 原理
A 用金刚砂制作砂轮切割钢板 金刚砂的熔点高
B 用海水制取溴和镁单质 Br-可被氧化、Mg2+可被还原
C 用氢氟酸蚀刻玻璃制作艺术品 氢氟酸能与SiO2反应
D 用聚乳酸制作手术缝合线 聚乳酸可自行降解
答案 A
12.实验室制备F2的过程为①KMnO4和H2O2在KF-HF介质中反应制得K2MnF6;②SbCl5+5HF SbF5+5HCl;③2K2MnF6+4SbF5 4KSbF6+2MnF3+F2↑。下列说法正确的是( )
A.①可选择圆底烧瓶作为反应装置
B.②中反应可证明酸性:HF>HCl
C.③中制备的F2可用排水法收集
D.转移相同电子数时①和③产生气体的物质的量相等
答案 D
13.硫代硫酸钠(Na2S2O3)是一种重要的化工产品,将SO2通入Na2CO3和Na2S混合溶液中可制得Na2S2O3,其制备装置如图所示。下列说法错误的是( )
A.S2的空间结构为四面体形
B.若用98%的浓硫酸,反应速率将降低
C.制备Na2S2O3的总反应方程式为2Na2S+Na2CO3+4SO2 3Na2S2O3+CO2
D.为增大三颈烧瓶中加入原料的利用率,可通入过量SO2
答案 D
14.实验室通过反应2NO+Na2O2 2NaNO2制备NaNO2。下列实验装置不能达到实验目的的是( )
甲 乙
丙 丁
A.用装置甲制备NO
B.用装置乙干燥NO
C.用装置丙制备NaNO2
D.用装置丁处理尾气
答案 D
15.煤燃烧排放的烟气中含有SO2和NOx,是大气的主要污染源之一。用Ca(ClO)2溶液对烟气[n(SO2)∶n(NO)=3∶2]同时脱硫脱硝(分别生成S、N),得到NO、SO2脱除率如图,下列说法不正确的是( )
A.脱除NO的反应:2NO+3ClO-+H2O 2H++2N+3Cl-
B.依据图中信息,在80 min时,吸收液中n(N)∶n(Cl-)=2∶3
C.SO2脱除率高于NO的原因可能是SO2在水中的溶解度大于NO
D.随着脱除反应的进行,吸收剂溶液的pH逐渐减小
答案 B
16.文物蕴含着丰富的文化知识。下列文物的主要材料为硅酸盐的是( )
A.春秋箕形方孔脊铜炭铲 B.西晋青瓷羊形四系壶
C.宋双鱼纹银盘 D.《写生花鸟草虫图册》
答案 B
17.NaClO2是一种重要的杀菌消毒剂,一种生产NaClO2的工艺流程如下图所示。已知:“有效氯含量”是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。下列说法错误的是( )
A.该生产过程中,有三处涉及氧化还原反应
B.在电解过程中,NaClO2是还原产物
C.“尾气吸收”反应中,氧化剂与还原剂的物质的量之比为1∶2
D.NaClO2的“有效氯含量”约为1.57 g
答案 C
18.某同学利用如图所示装置探究SO2的性质。下列有关叙述错误的是( )
A.碳酸钠溶液呈碱性,通入SO2前试管①中溶液呈红色
B.持续通入SO2,试管①中溶液的颜色会慢慢褪去
C.通入SO2后,试管②中溶液的红色会褪去,加热试管②,会恢复红色
D.可以用氯化钡溶液进行尾气处理,得到BaSO3沉淀
答案 D
19.自然界中时刻存在着氮的转化。下图为N2分子在催化剂作用下发生一系列转化示意图。
下列叙述正确的是( )
A.N2→NH3,NH3→NO均属于氮的固定
B.使用催化剂a、b均可以提高单位时间内生成物的产量
C.催化剂a、b表面均发生了极性共价键的断裂
D.在催化剂a作用下,氮原子发生了氧化反应
答案 B
20.部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断合理的是( )
A.a可以与少量b'反应有白雾产生
B.工业上通过a→b→c→d→e来制备HNO3
C.浓a'溶液和浓d'溶液反应可以得到b',浓a'溶液和浓c'溶液反应得不到b'
D.加热d'的固态钾盐可以产生O2
答案 D
专题六 非金属及其化合物
1.考古遗迹和历史文物是历史的见证,反映了古代人民丰富多彩的生活。下列文物属于无机非金属材料的是 ( )
铜烤炉 黄花梨云 龙纹条案 三彩骑卧 驼陶俑 山居图 扇面
A B C D
答案 C
5. “空气吹出法”海水提溴的工艺流程如图,下列说法错误的是( )
A.进入吹出塔前,Br-被氧化为Br2
B.吸收塔中SO2作还原剂
C.经过吸收塔后,溴元素得到富集
D.两次通入水蒸气的作用都是参加反应
答案 D
3.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与b可生成SO2
B.SO2通入紫色石蕊溶液先变红后褪色
C.c在空气中燃烧生成SO2
D.d既可被氧化,也可被还原
答案 B
4.下列有关含氮化合物的反应中,对应的离子方程式书写正确的是( )
A.将过量SO2通入冷氨水中:NH3·H2O+SO2 HS
B.室温下用稀硝酸溶解铜:Cu+4H++2N Cu2++2NO2↑+2H2O
C.NO2溶于水制硝酸:2NO2+2H2O H++N+NO
D.等体积、等浓度的NH4HSO4溶液与NaOH溶液混合:N+OH- NH3·H2O
答案 A
5.含氯化合物的反应具有多样性。下列有关反应的离子方程式书写不正确的是( )
A.将Cl2通入冷的石灰乳中制备漂白粉:Cl2+2OH- Cl-+ClO-+H2O
B.向AgCl悬浊液中通入NH3:AgCl+2NH3 [Ag(NH3)2]++Cl-
C.利用MnO2和浓盐酸反应制备Cl2:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
D.将SO2通入酸性NaClO3溶液中制备ClO2:2Cl+SO2 2ClO2+S
答案 A
6.陶土网是由两片铁丝网夹着一张浸泡过陶土水后晾干的棉布制成,其功能和石棉网一样,但安全性更高,对人体的危害性更小。下列说法错误的是( )
A.陶土和石棉都是硅酸盐材料
B.陶土性质稳定,在高温下不易分解
C.蒸发实验中,蒸发皿需垫上陶土网再加热
D.一种石棉化学式为Mg6Si4O10(OH)8,其氧化物形式可写为3MgO·2SiO2·2H2O
答案 C
7.我国航天技术的进步离不开新技术和新材料的应用。下列说法正确的是( )
A.飞船建造通常用镁、铝、钛等合金,合金的熔点一定比各成分金属低
B.火箭使用碳纳米管可以减轻火箭质量,这种材料属于有机高分子材料
C.飞船船体覆盖的耐高温陶瓷材料属于新型无机非金属材料
D.太阳能电池翼伸展机构关键部件用到的SiC属于硅酸盐材料
答案 C
8.氯元素的化合价与部分物质类别的对应关系如图所示,据图判断下列说法错误的是( )
A.c在光照条件下很容易分解
B.b不是酸性氧化物,因为它没有对应的含氧酸
C.图中a、b、c、d、e五种物质中均含有共价键,且c、d、e属于电解质
D.将a通入NaOH溶液中,已知生成NaCl、NaClO和d的混合物,若n(NaClO)与n(d)之比为3∶1,则氧化剂与还原剂的物质的量之比为2∶1
答案 B
9.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与足量Cu加热反应后,剩余溶液加入碳酸氢钠溶液有气体放出
B.SO2通入紫色石蕊试液先变红后褪色
C.b溶液在空气中久置后溶液变浑浊
D.d既可被氧化,也可被还原
答案 B
10.空气中的氮气可通过人工固氮获得氨气,氨气是重要的化工原料,通过氨氧化法可制得硝酸,反应过程如下图:
N2NH3NONO2HNO3
硝酸是一种强氧化性酸,制硝酸工业产生的尾气中含有氮氧化物(NOx),应处理后才能排放。下列说法正确的是( )
A.BaSO3固体能溶于稀硝酸,生成Ba(NO3)2,同时放出SO2气体
B.工业上,当转化①的反应达到平衡时,需不断地从混合气体中分离出NH3,将未反应的原料气送回合成塔以提高原料的利用率
C.工业尾气中NOx常用碱液吸收处理,NO、NO2的混合气体能被足量烧碱溶液完全吸收的条件是n(NO)≥n(NO2)
D.向浓硝酸溶液中插入红热的炭,产生红棕色气体,则可证明炭与浓硝酸溶液反应一定生成NO2
答案 B
11.下列生产活动中,没有运用相应原理的是( )
选项 生产活动 原理
A 用金刚砂制作砂轮切割钢板 金刚砂的熔点高
B 用海水制取溴和镁单质 Br-可被氧化、Mg2+可被还原
C 用氢氟酸蚀刻玻璃制作艺术品 氢氟酸能与SiO2反应
D 用聚乳酸制作手术缝合线 聚乳酸可自行降解
答案 A
12.实验室制备F2的过程为①KMnO4和H2O2在KF-HF介质中反应制得K2MnF6;②SbCl5+5HF SbF5+5HCl;③2K2MnF6+4SbF5 4KSbF6+2MnF3+F2↑。下列说法正确的是( )
A.①可选择圆底烧瓶作为反应装置
B.②中反应可证明酸性:HF>HCl
C.③中制备的F2可用排水法收集
D.转移相同电子数时①和③产生气体的物质的量相等
答案 D
13.硫代硫酸钠(Na2S2O3)是一种重要的化工产品,将SO2通入Na2CO3和Na2S混合溶液中可制得Na2S2O3,其制备装置如图所示。下列说法错误的是( )
A.S2的空间结构为四面体形
B.若用98%的浓硫酸,反应速率将降低
C.制备Na2S2O3的总反应方程式为2Na2S+Na2CO3+4SO2 3Na2S2O3+CO2
D.为增大三颈烧瓶中加入原料的利用率,可通入过量SO2
答案 D
14.实验室通过反应2NO+Na2O2 2NaNO2制备NaNO2。下列实验装置不能达到实验目的的是( )
甲 乙
丙 丁
A.用装置甲制备NO
B.用装置乙干燥NO
C.用装置丙制备NaNO2
D.用装置丁处理尾气
答案 D
15.煤燃烧排放的烟气中含有SO2和NOx,是大气的主要污染源之一。用Ca(ClO)2溶液对烟气[n(SO2)∶n(NO)=3∶2]同时脱硫脱硝(分别生成S、N),得到NO、SO2脱除率如图,下列说法不正确的是( )
A.脱除NO的反应:2NO+3ClO-+H2O 2H++2N+3Cl-
B.依据图中信息,在80 min时,吸收液中n(N)∶n(Cl-)=2∶3
C.SO2脱除率高于NO的原因可能是SO2在水中的溶解度大于NO
D.随着脱除反应的进行,吸收剂溶液的pH逐渐减小
答案 B
16.文物蕴含着丰富的文化知识。下列文物的主要材料为硅酸盐的是( )
A.春秋箕形方孔脊铜炭铲 B.西晋青瓷羊形四系壶
C.宋双鱼纹银盘 D.《写生花鸟草虫图册》
答案 B
17.NaClO2是一种重要的杀菌消毒剂,一种生产NaClO2的工艺流程如下图所示。已知:“有效氯含量”是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。下列说法错误的是( )
A.该生产过程中,有三处涉及氧化还原反应
B.在电解过程中,NaClO2是还原产物
C.“尾气吸收”反应中,氧化剂与还原剂的物质的量之比为1∶2
D.NaClO2的“有效氯含量”约为1.57 g
答案 C
18.某同学利用如图所示装置探究SO2的性质。下列有关叙述错误的是( )
A.碳酸钠溶液呈碱性,通入SO2前试管①中溶液呈红色
B.持续通入SO2,试管①中溶液的颜色会慢慢褪去
C.通入SO2后,试管②中溶液的红色会褪去,加热试管②,会恢复红色
D.可以用氯化钡溶液进行尾气处理,得到BaSO3沉淀
答案 D
19.自然界中时刻存在着氮的转化。下图为N2分子在催化剂作用下发生一系列转化示意图。
下列叙述正确的是( )
A.N2→NH3,NH3→NO均属于氮的固定
B.使用催化剂a、b均可以提高单位时间内生成物的产量
C.催化剂a、b表面均发生了极性共价键的断裂
D.在催化剂a作用下,氮原子发生了氧化反应
答案 B
20.部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断合理的是( )
A.a可以与少量b'反应有白雾产生
B.工业上通过a→b→c→d→e来制备HNO3
C.浓a'溶液和浓d'溶液反应可以得到b',浓a'溶液和浓c'溶液反应得不到b'
D.加热d'的固态钾盐可以产生O2
答案 D
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
