福建省宁德市霞浦县第七中学2015-2016学年高二上学期期中考试化学(文)试题
文档属性
| 名称 | 福建省宁德市霞浦县第七中学2015-2016学年高二上学期期中考试化学(文)试题 |

|
|
| 格式 | zip | ||
| 文件大小 | 452.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-11-28 00:00:00 | ||
图片预览


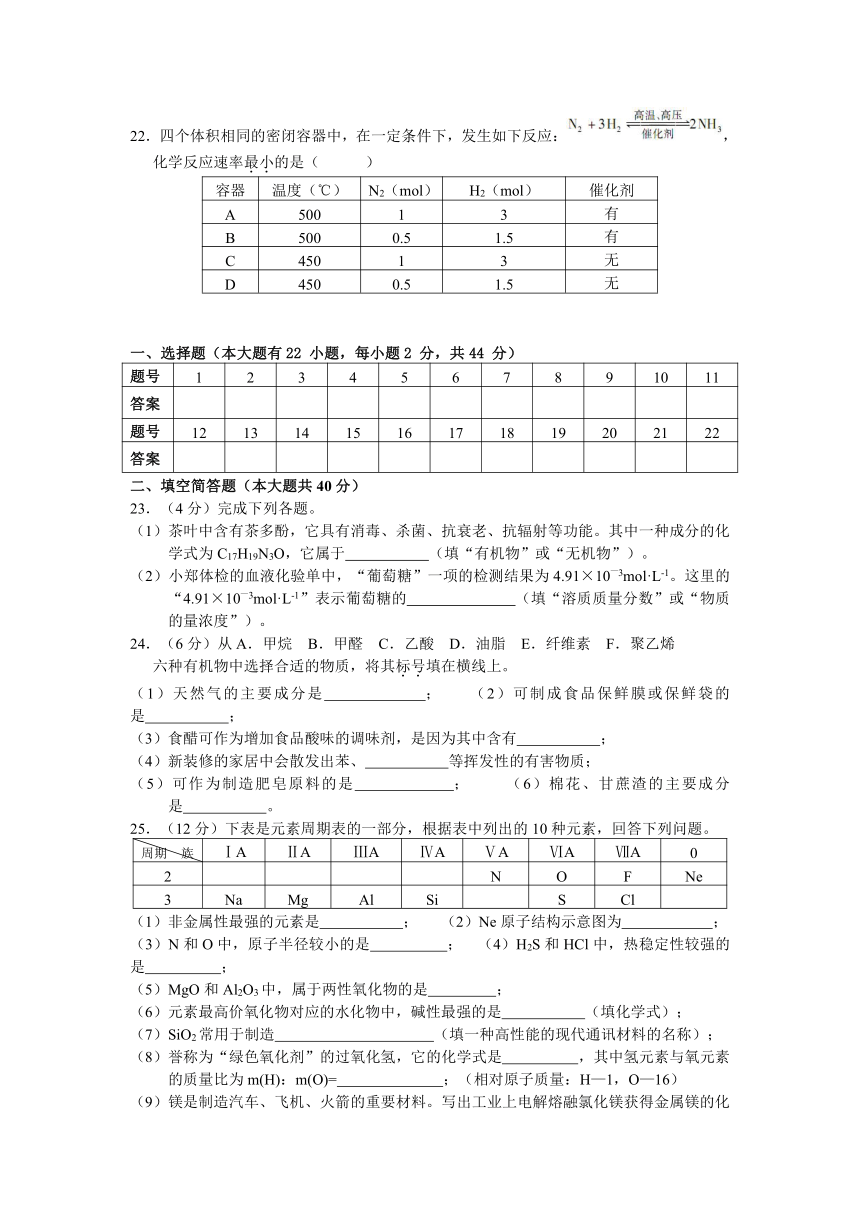
文档简介
福建省霞浦七中2015-2016学年第一学期期中质量检测
高二化学(文科)试卷
(考试时间:90分钟;满分:100分)
第I卷 (选择题 44分)
一、选择题(本大题有22小题,每小题2分,共44分。每小题只有一个正确答案)
1.2013年入冬以来福建多地出现雾霾天气。下列做法有利于减少雾霾产生的是( )
A.露天焚烧垃圾 B.大力发展火力发电 C.乱砍滥伐树木 D.开发利用太阳能
2.下列物质属于纯净物的是( )
A.空气 B.煤炭 C.液氯 D.海水
3.下列化合物中,既有离子键又有共价键的是( )
A.H2O B.NaCl C.NaOH D.HCl
4.要使垃圾中宝贵的再生资源得到充分利用,必须对垃圾进行分类。下图为垃圾分类标志,塑料垃圾属于( )
5.NA为阿伏伽德罗常数,下列物质所含分子数最多的是( )
A.0.8molCH4 B.8.8gCO2(CO2摩尔质量为44g.mol-1)
C.标准状况下4.48L的O2 D.含NA个氢分子的H2
6.能大量共存于同一溶液的离子组是( )
A.K+、H+、HCO3— B.Cu2+、Na+、OH— C.Na+、Cl—、NO3— D.Ag+、Cl—、SO42—
7.下列对人体健康无害的是( )
A.用工业石蜡给瓜子美容 B.用工业酒精(含甲醇)配兑饮用酒
C.食用加碘盐预防碘缺乏病 D.食用亚硝酸盐超标的腊肉
8.下列反应的离子方程式书写正确的是( )
A.-氢氧化钠溶液与稀硝酸反应:OH-+ H+ == H2O
B.溴化钾溶液中通入氯气:Br-+ C12 == Br2+ Cl
C.稀盐酸与碳酸钙反应:2H+ + CO32-== H2O + CO2↑
D.铁粉与稀硫酸反应:Fe + H+ = Fe3++ H2↑
9.下列微粒互为同位素的是( )
A.NO和 NO2 B. 168O和188O C.O2和O3 D.CH4和C2H6
10.某饮料的配料表:纯净水、蔗糖、苹果汁、维生素C、乳酸钙。该饮料不含有的营养素是( )
A.糖类 B.油脂 C.水 D.维生素
11.实验室配制250mL 0.5mo1·L-1NaCl溶液,不需要用到的仪器是( )
12.只用一种试剂,可以一次性鉴别NH4Cl、NaCl、Na2SO4三种溶液,这种试剂是( )
A.Ba(OH)2溶液 B.KCl溶液 C.酚酞溶液 D.盐酸
13.下列现象因发生物理变化引起的是( )
A.活性炭使蓝色墨水褪色 B.盛石灰水的试剂瓶久置后内壁出现白色固体
C.蛋白质灼烧时发出烧焦羽毛的气味 D.湿润红布条置于氯气的集气瓶中,红布条褪色
14.右图是某有机物分子的比例模型(填充模型),其中 代表氢原子, 表示碳原子,
代表氧原子。该有机物的名称是( )
A.乙烷 B.乙烯 C.乙酸 D.乙醇
15.下列关于生活中常见药物的说法,不正确的是( )
A.“胃舒平”是治疗胃酸过多的药物 B.“阿司匹林”是解热镇痛和消炎的药物
C.“创可贴”是小伤口的外用消炎药物 D.“风油精”是包治百病的药物
16.下列物质属于天然高分子的是( )
A.聚氯乙烯 B.蚕丝 C.塑料 D.合成橡胶
17.铝粉和氧化铁粉末在高温条件下发生铝热反应,该反应放出大量的热,用于焊接铁轨。反应的化学方程式为:2Al+Fe2O32Fe+Al2O3 ,对该反应的下列说法正确的是( )
A.Fe2O3是氧化剂 B.铁元素的化合价升高
C.Fe2O3中铁元素的化合价为+2价 D.Fe2O3发生氧化反应
18.日常生活中常用到化学知识。下列说法不正确的是( )
A.碳酸钡可用作医疗上的“钡餐” B.明矾可用作净水剂
C.高温蒸煮碗筷可杀菌消毒 D.热纯碱溶液可清洗油污
19.下列属于加成反应的是( )
A.CH4+Cl2CH3Cl+HCl
B.CH3COOH + CH3CH2OH→ CH3COOC2H5 + H2O
C.
D.CH2=CH2+Br2→BrCH2CH2Br
20.关于右图所示的原电池,下列说法不正确的是( )
A.铜片为正极,锌片为负极 B.锌片溶解,质量减少
C.该装置将化学能转化为电能 D.电子由铜片经导线流向锌片
21.下列实验操作正确的是( )
A.用嘴吹灭燃着的酒精灯 B.用量筒量取5.0mL浓硫酸并在量筒中稀释
C.给试管里的固体加热时,试管口略向下倾斜 D.用托盘天平称量固体质量时,砝码放在左盘
22.四个体积相同的密闭容器中,在一定条件下,发生如下反应:,化学反应速率最小的是( )
容器 温度(℃) N2(mol) H2(mol) 催化剂
A 500 1 3 有
B 500 0.5 1.5 有
C 450 1 3 无
D 450 0.5 1.5 无
一、选择题(本大题有22 小题,每小题2 分,共44 分)
题号 1 2 3 4 5 6 7 8 9 10 11
答案
题号 12 13 14 15 16 17 18 19 20 21 22
答案
二、填空简答题(本大题共40分)
23.(4分)完成下列各题。
(1)茶叶中含有茶多酚,它具有消毒、杀菌 ( http: / / www.21cnjy.com )、抗衰老、抗辐射等功能。其中一种成分的化学式为C17H19N3O,它属于 (填“有机物”或“无机物”)。
(2)小郑体检的血液化验单中,“葡萄糖”一 ( http: / / www.21cnjy.com )项的检测结果为4.91×10—3mol·L-1。这里的“4.91×10—3mol·L-1”表示葡萄糖的 (填“溶质质量分数”或“物质的量浓度”)。
24.(6分)从A.甲烷 B.甲醛 C.乙酸 D.油脂 E.纤维素 F.聚乙烯
六种有机物中选择合适的物质,将其标号填在横线上。
(1)天然气的主要成分是 ; (2)可制成食品保鲜膜或保鲜袋的是 ;
(3)食醋可作为增加食品酸味的调味剂,是因为其中含有 ;
(4)新装修的家居中会散发出苯、 等挥发性的有害物质;
(5)可作为制造肥皂原料的是 ; (6)棉花、甘蔗渣的主要成分是 。
25.(12分)下表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
周期 族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
2 N O F Ne
3 Na Mg Al Si S Cl
(1)非金属性最强的元素是 ; (2)Ne原子结构示意图为 ;
(3)N和O中,原子半径较小的是 ; (4)H2S和HCl中,热稳定性较强的是 ;
(5)MgO和Al2O3中,属于两性氧化物的是 ;
(6)元素最高价氧化物对应的水化物中,碱性最强的是 (填化学式);
(7)SiO2常用于制造 (填一种高性能的现代通讯材料的名称);
(8)誉称为“绿色氧化剂”的过氧化氢,它的 ( http: / / www.21cnjy.com )化学式是 ,其中氢元素与氧元素的质量比为m(H):m(O)= ;(相对原子质量:H—1,O—16)
(9)镁是制造汽车、飞机、 ( http: / / www.21cnjy.com )火箭的重要材料。写出工业上电解熔融氯化镁获得金属镁的化学方程式: 。
26.(6分)完成下列各题。
(1)写出木炭与浓硫酸在加热条件下反应的化学方程式:
。
(2)乙醇(C2H5OH)是一种优良燃料,写出它在空气中完全燃烧的化学方程式:
。
27.(6分)某化学兴趣小组对坚铝(主要成分是Al、Mg、Cu等)进行如下图所示的实验。
(1)(I)和(II)步骤中分离溶液和沉淀的操作名称是 ;
(2)固体A中主要含有 ;固体B是 (填化学式);
(3)滤液Y中的阴离子除OH—、Cl—外,还有 ;
(4)写出(IV)步骤反应的化学方程式: 。
28.(6分)简要回答下列问题。
(1)鉴别胶体与溶液的最简便方法是 。
(2)常温下,浓硝酸可以用铁质容器密封盛放的原因是 。
(3)3月22日是“世界水日”,水是生 ( http: / / www.21cnjy.com )命之源,没有水九没有生命。请你提出一种有利于保护水资源的措施: 。
三、实验探究题(本大题共16分)
29.(4分)为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格。
实验目的 试剂及方法
证明地瓜中有淀粉
除去CO2中混有的少量CO
检验FeCl2溶液是否变质
除去Na2CO3固体中NaHCO3
供选择的化学试剂及实验方法
A.加热
B.滴加碘水
C.加入KSCN溶液
D.通过灼热的CuO
30.(12分)实验室用Na2SO3和70%硫酸溶液反应制取SO2,某研究性学习小组设计如下实验,制取并探究SO2的性质。(制取SO2反应原理为:Na2SO3+2H2SO4=Na2SO4+SO2↑+H2O)
【探究实验】(1)甲装置中a仪器的名称是 。
(2)实验中若生成若生成标准状况下1.12LSO2,则需要Na2SO3 g参加反应。
(已知:Na2SO3的摩尔质量为126g·mol-1)
(3)①若X是品红溶液,气体通过乙装置,观察到的现象是 ;
②若X是酸性KMnO4溶液,气体通过乙装置,观察到溶液褪色,说明SO2具有 。
A.酸性 B.还原性 C.漂白性
(4)丁装置中NaOH溶液的作用是吸收多余的SO2,请将其中反应的化学方程式补充完整:
SO2 + NaOH = + H2O
【实验讨论】(5)若X是浓硫酸,用于干燥SO2气体,在丙处选用下图所示的收集装置,
A、B两位同学的连接方式为:
A同学:SO2气体从a导管通入集气瓶中。
B同学:SO2气体从b导管通入集气瓶中。
正确的收集装置是 (填“A”或“B”)同学的连接方式。
(已知:同等条件下SO2的密度大于空气)
【知识应用】
(6)向盛有水的烧杯中通入SO2, ( http: / / www.21cnjy.com )所得溶液的pH (填“>”或“=”或“<”)7。SO2是形成酸雨的主要物质,请你提出一种减少SO2对空气污染的可行措施:
。
霞浦七中2015-2016学年第一学期期中质量检测
化学试卷参考答案与评分标准
第Ⅰ卷(选择题 44分)
选择题(本大题有22小题,每小题2分,共44分。每小题只有一个正确答案)
1.D 2.C 3.C 4.A 5.D 6.C 7.C 8.A 9.B 10.B
11.B 12.A 13.A 14.D 15.D 16.B 17.A 18.A 19.D 20.D
21.C 22.D
第Ⅱ卷 (非选择题 56分)
二、填空简答题(本大题共40分)
23.(1)有机物(2分) (2)物质的量浓度(2分)
24. ⑴A ⑵F ⑶C ⑷B ⑸D ⑹E
(若填写相应的物质名称或化学式也给分 每空各1分,共6分)
25. ⑴F(或氟)(1分)
⑵(1分) ⑶O(或氧原子)(1分)
⑷HCl(或盐酸) (1分) ⑸Al2O3(或氧化铝) ( 1分)
⑹NaOH (1分) ⑺光导纤维(或光纤) (1分)
⑻H2O2 (1分)
1:16 (2分)
⑼MgCl2(熔融)=======Mg+Cl2 (2分)
26、2H2SO4(浓) + CCO2↑ + 2SO2↑+ 2H2O (3分)
C2H5OH+3O2 ———>2CO2 +3H2O (3分)
27、⑴过滤 ( 1分) ⑵Cu(或铜) ( 1分)
⑶[Al(OH)4 ]_ ( 1分) ⑷2Al(OH)3Al2O3+3H2O (2分)
28、⑴利用丁达尔效应(或丁达尔现象或用可见光束通过分散性,观察到光亮的通路的为胶体 (2分)
⑵在常温下,浓硝酸会使铁 ( http: / / www.21cnjy.com )钝化,阻止内部金属进一步发生反应(或在常温下,铁遇浓硝酸时会在表面生成致密的氧化膜而发生钝化,从而阻止内部金属进一步发生反应) (2分)
⑶①节约用水(洗衣、洗菜、淘米的水用来浇花、冲马桶等)
②减少对水资源的污染(不往水源倒垃圾、不任意排放污水、合理使用化肥农药等)
③致力于污水的治理
(以上任选其一或其它合理答案也给分) (2分)
三、实验探究题:(本题共共16分)
29.B D C A (每空各1分,共4分)
30. ⑴分液漏斗 ( 1分)
⑵6.3 (2分)
⑶①品红溶液褪色 ( 1分)
②B(或还原性) ( 1分)
⑷1、2、1、1 ( 1分)
Na2SO3 ( 1分)
⑸A (2分)
⑹<①减少化石燃料的使用 ( http: / / www.21cnjy.com )②对SO2的排放加以控制③改善能源结构、开发利用清洁能源④工业上对煤进行脱硫处理⑤对SO2气体进行处理货回收利用(以上任选其一或其它合理答案也给分)(2分)
光照
+10
2
8
通电
点燃
高二化学(文科)试卷
(考试时间:90分钟;满分:100分)
第I卷 (选择题 44分)
一、选择题(本大题有22小题,每小题2分,共44分。每小题只有一个正确答案)
1.2013年入冬以来福建多地出现雾霾天气。下列做法有利于减少雾霾产生的是( )
A.露天焚烧垃圾 B.大力发展火力发电 C.乱砍滥伐树木 D.开发利用太阳能
2.下列物质属于纯净物的是( )
A.空气 B.煤炭 C.液氯 D.海水
3.下列化合物中,既有离子键又有共价键的是( )
A.H2O B.NaCl C.NaOH D.HCl
4.要使垃圾中宝贵的再生资源得到充分利用,必须对垃圾进行分类。下图为垃圾分类标志,塑料垃圾属于( )
5.NA为阿伏伽德罗常数,下列物质所含分子数最多的是( )
A.0.8molCH4 B.8.8gCO2(CO2摩尔质量为44g.mol-1)
C.标准状况下4.48L的O2 D.含NA个氢分子的H2
6.能大量共存于同一溶液的离子组是( )
A.K+、H+、HCO3— B.Cu2+、Na+、OH— C.Na+、Cl—、NO3— D.Ag+、Cl—、SO42—
7.下列对人体健康无害的是( )
A.用工业石蜡给瓜子美容 B.用工业酒精(含甲醇)配兑饮用酒
C.食用加碘盐预防碘缺乏病 D.食用亚硝酸盐超标的腊肉
8.下列反应的离子方程式书写正确的是( )
A.-氢氧化钠溶液与稀硝酸反应:OH-+ H+ == H2O
B.溴化钾溶液中通入氯气:Br-+ C12 == Br2+ Cl
C.稀盐酸与碳酸钙反应:2H+ + CO32-== H2O + CO2↑
D.铁粉与稀硫酸反应:Fe + H+ = Fe3++ H2↑
9.下列微粒互为同位素的是( )
A.NO和 NO2 B. 168O和188O C.O2和O3 D.CH4和C2H6
10.某饮料的配料表:纯净水、蔗糖、苹果汁、维生素C、乳酸钙。该饮料不含有的营养素是( )
A.糖类 B.油脂 C.水 D.维生素
11.实验室配制250mL 0.5mo1·L-1NaCl溶液,不需要用到的仪器是( )
12.只用一种试剂,可以一次性鉴别NH4Cl、NaCl、Na2SO4三种溶液,这种试剂是( )
A.Ba(OH)2溶液 B.KCl溶液 C.酚酞溶液 D.盐酸
13.下列现象因发生物理变化引起的是( )
A.活性炭使蓝色墨水褪色 B.盛石灰水的试剂瓶久置后内壁出现白色固体
C.蛋白质灼烧时发出烧焦羽毛的气味 D.湿润红布条置于氯气的集气瓶中,红布条褪色
14.右图是某有机物分子的比例模型(填充模型),其中 代表氢原子, 表示碳原子,
代表氧原子。该有机物的名称是( )
A.乙烷 B.乙烯 C.乙酸 D.乙醇
15.下列关于生活中常见药物的说法,不正确的是( )
A.“胃舒平”是治疗胃酸过多的药物 B.“阿司匹林”是解热镇痛和消炎的药物
C.“创可贴”是小伤口的外用消炎药物 D.“风油精”是包治百病的药物
16.下列物质属于天然高分子的是( )
A.聚氯乙烯 B.蚕丝 C.塑料 D.合成橡胶
17.铝粉和氧化铁粉末在高温条件下发生铝热反应,该反应放出大量的热,用于焊接铁轨。反应的化学方程式为:2Al+Fe2O32Fe+Al2O3 ,对该反应的下列说法正确的是( )
A.Fe2O3是氧化剂 B.铁元素的化合价升高
C.Fe2O3中铁元素的化合价为+2价 D.Fe2O3发生氧化反应
18.日常生活中常用到化学知识。下列说法不正确的是( )
A.碳酸钡可用作医疗上的“钡餐” B.明矾可用作净水剂
C.高温蒸煮碗筷可杀菌消毒 D.热纯碱溶液可清洗油污
19.下列属于加成反应的是( )
A.CH4+Cl2CH3Cl+HCl
B.CH3COOH + CH3CH2OH→ CH3COOC2H5 + H2O
C.
D.CH2=CH2+Br2→BrCH2CH2Br
20.关于右图所示的原电池,下列说法不正确的是( )
A.铜片为正极,锌片为负极 B.锌片溶解,质量减少
C.该装置将化学能转化为电能 D.电子由铜片经导线流向锌片
21.下列实验操作正确的是( )
A.用嘴吹灭燃着的酒精灯 B.用量筒量取5.0mL浓硫酸并在量筒中稀释
C.给试管里的固体加热时,试管口略向下倾斜 D.用托盘天平称量固体质量时,砝码放在左盘
22.四个体积相同的密闭容器中,在一定条件下,发生如下反应:,化学反应速率最小的是( )
容器 温度(℃) N2(mol) H2(mol) 催化剂
A 500 1 3 有
B 500 0.5 1.5 有
C 450 1 3 无
D 450 0.5 1.5 无
一、选择题(本大题有22 小题,每小题2 分,共44 分)
题号 1 2 3 4 5 6 7 8 9 10 11
答案
题号 12 13 14 15 16 17 18 19 20 21 22
答案
二、填空简答题(本大题共40分)
23.(4分)完成下列各题。
(1)茶叶中含有茶多酚,它具有消毒、杀菌 ( http: / / www.21cnjy.com )、抗衰老、抗辐射等功能。其中一种成分的化学式为C17H19N3O,它属于 (填“有机物”或“无机物”)。
(2)小郑体检的血液化验单中,“葡萄糖”一 ( http: / / www.21cnjy.com )项的检测结果为4.91×10—3mol·L-1。这里的“4.91×10—3mol·L-1”表示葡萄糖的 (填“溶质质量分数”或“物质的量浓度”)。
24.(6分)从A.甲烷 B.甲醛 C.乙酸 D.油脂 E.纤维素 F.聚乙烯
六种有机物中选择合适的物质,将其标号填在横线上。
(1)天然气的主要成分是 ; (2)可制成食品保鲜膜或保鲜袋的是 ;
(3)食醋可作为增加食品酸味的调味剂,是因为其中含有 ;
(4)新装修的家居中会散发出苯、 等挥发性的有害物质;
(5)可作为制造肥皂原料的是 ; (6)棉花、甘蔗渣的主要成分是 。
25.(12分)下表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
周期 族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
2 N O F Ne
3 Na Mg Al Si S Cl
(1)非金属性最强的元素是 ; (2)Ne原子结构示意图为 ;
(3)N和O中,原子半径较小的是 ; (4)H2S和HCl中,热稳定性较强的是 ;
(5)MgO和Al2O3中,属于两性氧化物的是 ;
(6)元素最高价氧化物对应的水化物中,碱性最强的是 (填化学式);
(7)SiO2常用于制造 (填一种高性能的现代通讯材料的名称);
(8)誉称为“绿色氧化剂”的过氧化氢,它的 ( http: / / www.21cnjy.com )化学式是 ,其中氢元素与氧元素的质量比为m(H):m(O)= ;(相对原子质量:H—1,O—16)
(9)镁是制造汽车、飞机、 ( http: / / www.21cnjy.com )火箭的重要材料。写出工业上电解熔融氯化镁获得金属镁的化学方程式: 。
26.(6分)完成下列各题。
(1)写出木炭与浓硫酸在加热条件下反应的化学方程式:
。
(2)乙醇(C2H5OH)是一种优良燃料,写出它在空气中完全燃烧的化学方程式:
。
27.(6分)某化学兴趣小组对坚铝(主要成分是Al、Mg、Cu等)进行如下图所示的实验。
(1)(I)和(II)步骤中分离溶液和沉淀的操作名称是 ;
(2)固体A中主要含有 ;固体B是 (填化学式);
(3)滤液Y中的阴离子除OH—、Cl—外,还有 ;
(4)写出(IV)步骤反应的化学方程式: 。
28.(6分)简要回答下列问题。
(1)鉴别胶体与溶液的最简便方法是 。
(2)常温下,浓硝酸可以用铁质容器密封盛放的原因是 。
(3)3月22日是“世界水日”,水是生 ( http: / / www.21cnjy.com )命之源,没有水九没有生命。请你提出一种有利于保护水资源的措施: 。
三、实验探究题(本大题共16分)
29.(4分)为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格。
实验目的 试剂及方法
证明地瓜中有淀粉
除去CO2中混有的少量CO
检验FeCl2溶液是否变质
除去Na2CO3固体中NaHCO3
供选择的化学试剂及实验方法
A.加热
B.滴加碘水
C.加入KSCN溶液
D.通过灼热的CuO
30.(12分)实验室用Na2SO3和70%硫酸溶液反应制取SO2,某研究性学习小组设计如下实验,制取并探究SO2的性质。(制取SO2反应原理为:Na2SO3+2H2SO4=Na2SO4+SO2↑+H2O)
【探究实验】(1)甲装置中a仪器的名称是 。
(2)实验中若生成若生成标准状况下1.12LSO2,则需要Na2SO3 g参加反应。
(已知:Na2SO3的摩尔质量为126g·mol-1)
(3)①若X是品红溶液,气体通过乙装置,观察到的现象是 ;
②若X是酸性KMnO4溶液,气体通过乙装置,观察到溶液褪色,说明SO2具有 。
A.酸性 B.还原性 C.漂白性
(4)丁装置中NaOH溶液的作用是吸收多余的SO2,请将其中反应的化学方程式补充完整:
SO2 + NaOH = + H2O
【实验讨论】(5)若X是浓硫酸,用于干燥SO2气体,在丙处选用下图所示的收集装置,
A、B两位同学的连接方式为:
A同学:SO2气体从a导管通入集气瓶中。
B同学:SO2气体从b导管通入集气瓶中。
正确的收集装置是 (填“A”或“B”)同学的连接方式。
(已知:同等条件下SO2的密度大于空气)
【知识应用】
(6)向盛有水的烧杯中通入SO2, ( http: / / www.21cnjy.com )所得溶液的pH (填“>”或“=”或“<”)7。SO2是形成酸雨的主要物质,请你提出一种减少SO2对空气污染的可行措施:
。
霞浦七中2015-2016学年第一学期期中质量检测
化学试卷参考答案与评分标准
第Ⅰ卷(选择题 44分)
选择题(本大题有22小题,每小题2分,共44分。每小题只有一个正确答案)
1.D 2.C 3.C 4.A 5.D 6.C 7.C 8.A 9.B 10.B
11.B 12.A 13.A 14.D 15.D 16.B 17.A 18.A 19.D 20.D
21.C 22.D
第Ⅱ卷 (非选择题 56分)
二、填空简答题(本大题共40分)
23.(1)有机物(2分) (2)物质的量浓度(2分)
24. ⑴A ⑵F ⑶C ⑷B ⑸D ⑹E
(若填写相应的物质名称或化学式也给分 每空各1分,共6分)
25. ⑴F(或氟)(1分)
⑵(1分) ⑶O(或氧原子)(1分)
⑷HCl(或盐酸) (1分) ⑸Al2O3(或氧化铝) ( 1分)
⑹NaOH (1分) ⑺光导纤维(或光纤) (1分)
⑻H2O2 (1分)
1:16 (2分)
⑼MgCl2(熔融)=======Mg+Cl2 (2分)
26、2H2SO4(浓) + CCO2↑ + 2SO2↑+ 2H2O (3分)
C2H5OH+3O2 ———>2CO2 +3H2O (3分)
27、⑴过滤 ( 1分) ⑵Cu(或铜) ( 1分)
⑶[Al(OH)4 ]_ ( 1分) ⑷2Al(OH)3Al2O3+3H2O (2分)
28、⑴利用丁达尔效应(或丁达尔现象或用可见光束通过分散性,观察到光亮的通路的为胶体 (2分)
⑵在常温下,浓硝酸会使铁 ( http: / / www.21cnjy.com )钝化,阻止内部金属进一步发生反应(或在常温下,铁遇浓硝酸时会在表面生成致密的氧化膜而发生钝化,从而阻止内部金属进一步发生反应) (2分)
⑶①节约用水(洗衣、洗菜、淘米的水用来浇花、冲马桶等)
②减少对水资源的污染(不往水源倒垃圾、不任意排放污水、合理使用化肥农药等)
③致力于污水的治理
(以上任选其一或其它合理答案也给分) (2分)
三、实验探究题:(本题共共16分)
29.B D C A (每空各1分,共4分)
30. ⑴分液漏斗 ( 1分)
⑵6.3 (2分)
⑶①品红溶液褪色 ( 1分)
②B(或还原性) ( 1分)
⑷1、2、1、1 ( 1分)
Na2SO3 ( 1分)
⑸A (2分)
⑹<①减少化石燃料的使用 ( http: / / www.21cnjy.com )②对SO2的排放加以控制③改善能源结构、开发利用清洁能源④工业上对煤进行脱硫处理⑤对SO2气体进行处理货回收利用(以上任选其一或其它合理答案也给分)(2分)
光照
+10
2
8
通电
点燃
同课章节目录
