广西钦州市2023-2024学年高二下学期期中考试化学试题(含答案)
文档属性
| 名称 | 广西钦州市2023-2024学年高二下学期期中考试化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 761.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-20 00:00:00 | ||
图片预览


文档简介
钦州市2023-2024学年高二下学期期中考试化学
可能用到的相对原子质量:H-1 B-11 C-12 N-14 O-16 Si-28
一.选择题(每小题只有一个正确答案,每小题3分,共42分)
1.科教兴国,“可上九天揽月,可下五洋捉鳖”。下列说法正确的是( )
A.“嫦娥石”(主要由Ca、Fe、P、O和Y元素组成)是中国首次在月球上发现的新矿物,其中基态Ca原子最外层原子轨道的电子云图:
B.火星全球影像彩图显示了火星表土颜色,表土中含有的铁元素可用原子光谱法鉴定
C.的填充模型:
D.“深地一号”为进军万米深度提供核心装备,制造钻头用的金刚石属于金属晶体
2.现有四种元素,其中两种元素基态原子的电子排布式如下:
①②,另两种元素的价电子排布式为③④,则下列有关比较中正确的是( )
A.原子半径:①>②>④>③ B.第一电离能:④>③>②>①
C.电负性:④>③>②>① D.最高正化合价:④>③=②>①
3.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是( )
A.W元素在周期表的P区
B.元素非金属性的顺序为X>Y>Z
C.Y的最高价氧化物的水化物的晶体是分子晶体
D.该新化合物中Y不满足8电子稳定结构
4.设为阿伏加德罗常数的值,下列说法正确的是( )
A.晶体中键的数目为
B.标准状况下,中含有极性共价键数目为
C.聚乙烯中含有的键数目为
D.配离子中含键数目为
5.实验室中可用或来检验,下列说法正确的是( )
A.铁元素位于周期表第四周期第ⅧB族,属于ds区
B.与溶液混合,得到的配合物中,提供空轨道的是,配位原子是,配位数是6
C.中含有离子键、极性共价键和非极性共价键
D.与反应可得到一种蓝色沉淀,该沉淀物质晶胞的结构如图所示(未画出),则一个晶胞中的个数为4
6.下列叙述正确的是( )
A.属于烯烃的同分异构体有5种(不考虑立体异构)
B.立方烷()的六氯取代物有6种
C.乙烯和1,3-丁二烯互为同系物
D.三联苯()的一氯代物有6种
7.经研究发现白蚁信息素有①()和②(),家蚕的信息素为③。下列说法中不正确的是( )
A.①的名称是2,4-二甲基-1-庚烯②的名称是3,7-二甲基-1-辛烯
B.②和①属于同系物
C.③与氢气加成产物有3种
D.三种信息素均能使溴的四氯化碳溶液褪色
8.下列实验方案不合理的是( )
A.除去乙烷中的乙烯,可用溶液
B.分离苯和溴苯的混合物,可用蒸馏法
C.用饱和溶液除去乙酸乙酯中混有的乙酸等
D.可用水来鉴别苯、乙醇、四氯化碳
9.下列命名正确的是( )
A.2-乙基丙烷 B.2,2,3-三甲基戊烷
C.2-甲基-2-丙烯 D.溴乙烷
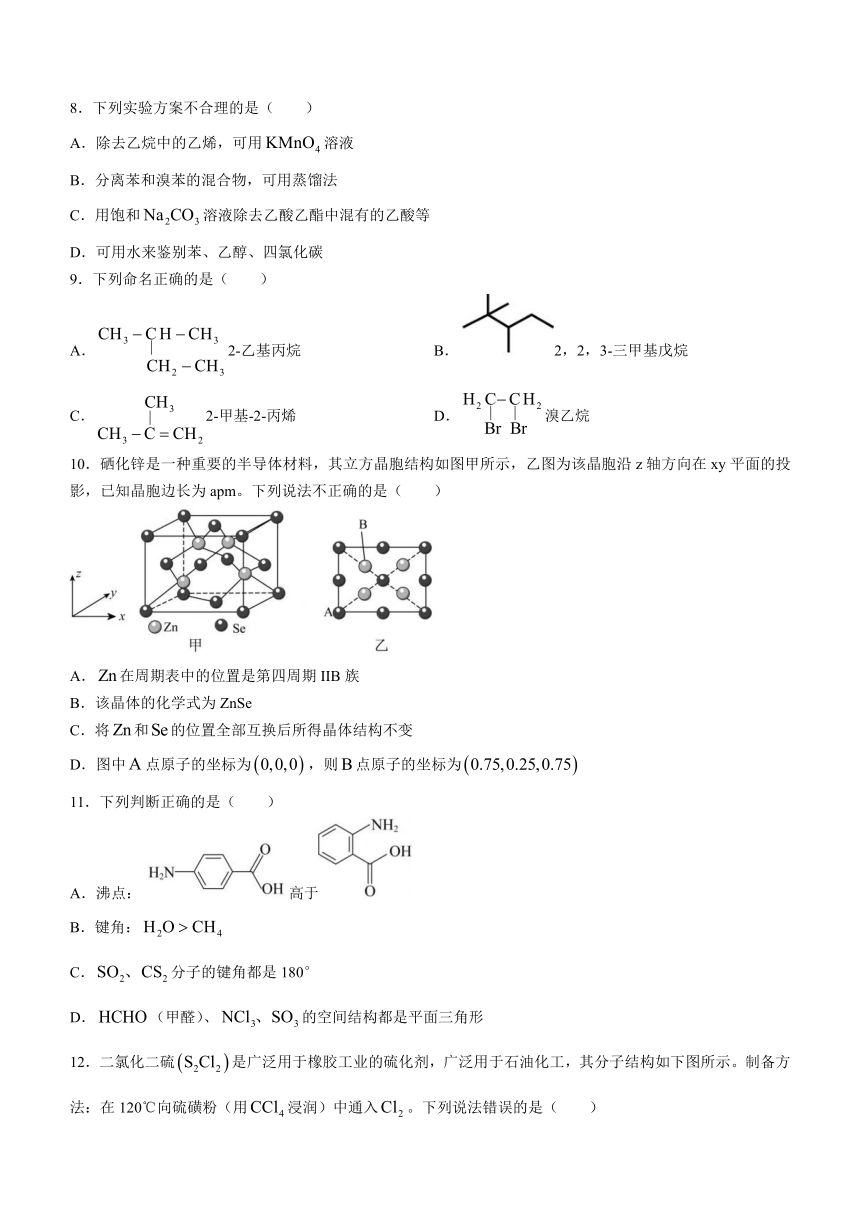
10.硒化锌是一种重要的半导体材料,其立方晶胞结构如图甲所示,乙图为该晶胞沿z轴方向在xy平面的投影,已知晶胞边长为apm。下列说法不正确的是( )
A.在周期表中的位置是第四周期IIB族
B.该晶体的化学式为ZnSe
C.将和的位置全部互换后所得晶体结构不变
D.图中点原子的坐标为,则点原子的坐标为
11.下列判断正确的是( )
A.沸点:高于
B.键角:
C.分子的键角都是180°
D.(甲醛)、的空间结构都是平面三角形
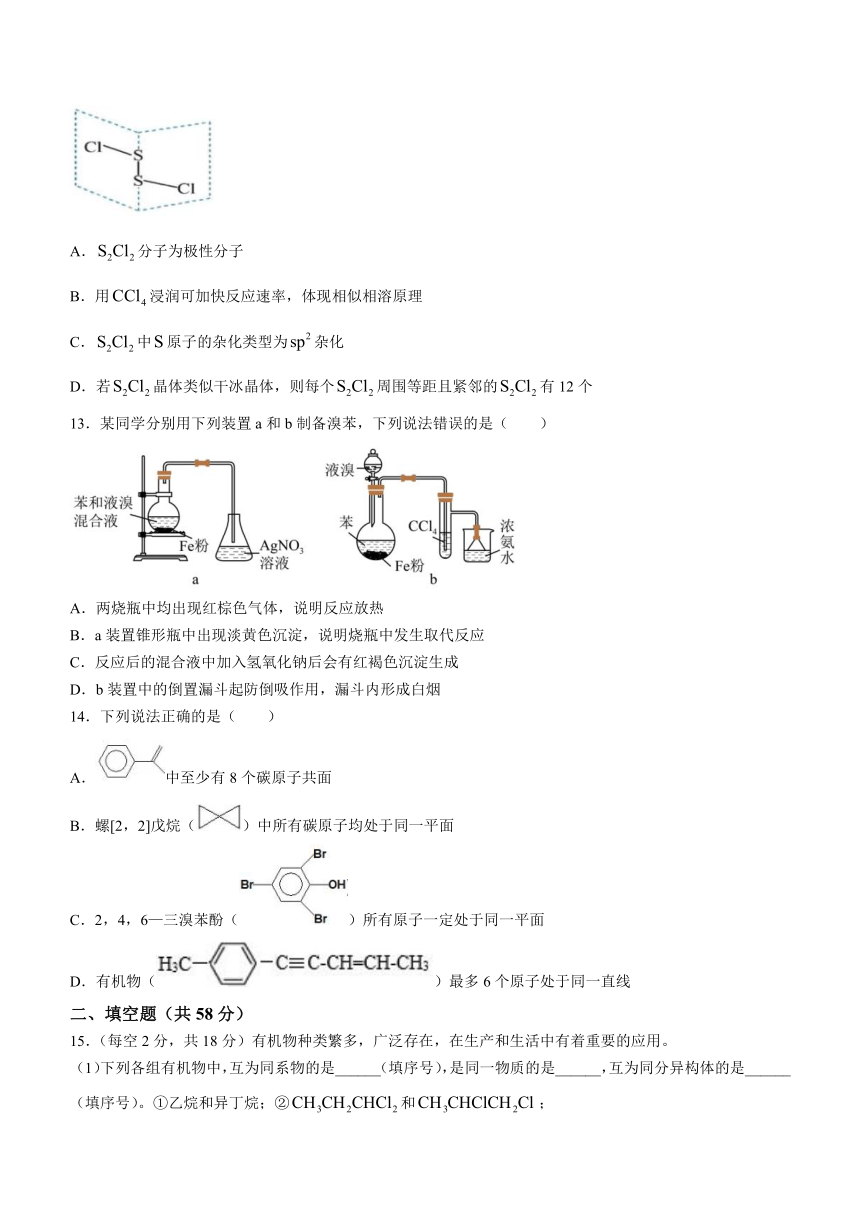
12.二氯化二硫是广泛用于橡胶工业的硫化剂,广泛用于石油化工,其分子结构如下图所示。制备方法:在120℃向硫磺粉(用浸润)中通入。下列说法错误的是( )
A.分子为极性分子
B.用浸润可加快反应速率,体现相似相溶原理
C.中原子的杂化类型为杂化
D.若晶体类似干冰晶体,则每个周围等距且紧邻的有12个
13.某同学分别用下列装置a和b制备溴苯,下列说法错误的是( )
A.两烧瓶中均出现红棕色气体,说明反应放热
B.a装置锥形瓶中出现淡黄色沉淀,说明烧瓶中发生取代反应
C.反应后的混合液中加入氢氧化钠后会有红褐色沉淀生成
D.b装置中的倒置漏斗起防倒吸作用,漏斗内形成白烟
14.下列说法正确的是( )
A.中至少有8个碳原子共面
B.螺[2,2]戊烷()中所有碳原子均处于同一平面
C.2,4,6—三溴苯酚()所有原子一定处于同一平面
D.有机物()最多6个原子处于同一直线
二、填空题(共58分)
15.(每空2分,共18分)有机物种类繁多,广泛存在,在生产和生活中有着重要的应用。
(1)下列各组有机物中,互为同系物的是______(填序号),是同一物质的是______,互为同分异构体的是______(填序号)。①乙烷和异丁烷;②和;
③和;④二甲醚和乙醇;⑤和;
(2)某芳香烃的分子式为,它可能有的同分异构体共______种,其中一溴代物只有两种的是______(结构简式)。
(3)某学习小组研究含氧衍生物A的组成和结构,研究过程如下:称取9gA在足量氧气中充分燃烧,并使产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g,对A进行波谱分析,结果如下:
①由质谱图可知A的分子式为______,结合红外光谱和核磁共振氢谱可知A的结构简式为______,该分子中有______个手性碳原子。
(2)经消去反应可以得到,则发生加聚反应后所得产物的结构简式为______.
16.(每空2分,共14分)
Ⅰ:(I)原子序数依次增大的五种短周期元素,其中是原子半径最小的元素,和的基态原子能级所含成单电子数均为的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)三种元素的第一电离能由大到小的顺序是______.
(2)与所含键的比值为______.
(3)根据等电子体理论可以预测-的空间构型为______.
Ⅱ:铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(4)可以与、有机分子等形成配合物。基态的电子排布式为______.
(5)普鲁士蓝俗称铁蓝,结构如图甲所示(未画出),平均每两个立方体中含有一个,该晶体的化学式为______。又知该晶体中铁元素有价和价两种,则与的个数比为______。
(6)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为______。
17.(每空2分,共14分)硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)硼酸()是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
①硼酸中B原子的杂化轨道类型为______。
②硼酸晶体中存在的作用力有范德华力和______。
③加热时,硼酸的溶解度增大,主要原因是______。
(2)硼氢化钠是有机化学中的一种常用还原剂,的空间构型是______.
(3)硼化镁晶体在时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如下图(左)是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为______。
(4)金刚石的晶胞如上图(右)。立方氮化硼的结构与金刚石相似,已知晶胞边长为apm,则氮原子与硼原子间的最短距离是______pm,立方氮化硼的密度是______。(只要求列算式,不必计算出数值,阿伏加德罗常数用表示)。
18.(每空2分,共12分)芳香化合物A是一种基本化工原料,可以从煤和石油中得到。A、B、C、D、E的转化关系如图所示:
回答下列问题:
(1)A的化学名称是______。
(2)A→B的反应类型是______,在该反应的副产物中,与B互为同分异构体的副产物的结构简式为______。
(3)A→C的化学方程式为______。
(4)A与酸性溶液反应可得到D,D中所含官能团名称是______,写出D的结构简式:______。
钦州市2023-2024学年高二下学期期中考试化学答案
1-5 BCCDD 6-10 ACABD 11-14 ACBD
15.(每空2分,共18分)(1)①⑤ ③ ②④
(2)4
(3)① 1
16.(每空2分,共14分)
(1) (2) (3)直线形
(4) (5) (6)
17.(每空2分,共14分)
(1) 氢键、共价键 加热破坏了硼酸分子之间的氢键
(2)正四面体 (3)
(4)
18.(每空2分,共12分)
(1)邻二甲苯(或1,2-二甲基苯) (2)取代反应
(3)(或)
(4)羧基
可能用到的相对原子质量:H-1 B-11 C-12 N-14 O-16 Si-28
一.选择题(每小题只有一个正确答案,每小题3分,共42分)
1.科教兴国,“可上九天揽月,可下五洋捉鳖”。下列说法正确的是( )
A.“嫦娥石”(主要由Ca、Fe、P、O和Y元素组成)是中国首次在月球上发现的新矿物,其中基态Ca原子最外层原子轨道的电子云图:
B.火星全球影像彩图显示了火星表土颜色,表土中含有的铁元素可用原子光谱法鉴定
C.的填充模型:
D.“深地一号”为进军万米深度提供核心装备,制造钻头用的金刚石属于金属晶体
2.现有四种元素,其中两种元素基态原子的电子排布式如下:
①②,另两种元素的价电子排布式为③④,则下列有关比较中正确的是( )
A.原子半径:①>②>④>③ B.第一电离能:④>③>②>①
C.电负性:④>③>②>① D.最高正化合价:④>③=②>①
3.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是( )
A.W元素在周期表的P区
B.元素非金属性的顺序为X>Y>Z
C.Y的最高价氧化物的水化物的晶体是分子晶体
D.该新化合物中Y不满足8电子稳定结构
4.设为阿伏加德罗常数的值,下列说法正确的是( )
A.晶体中键的数目为
B.标准状况下,中含有极性共价键数目为
C.聚乙烯中含有的键数目为
D.配离子中含键数目为
5.实验室中可用或来检验,下列说法正确的是( )
A.铁元素位于周期表第四周期第ⅧB族,属于ds区
B.与溶液混合,得到的配合物中,提供空轨道的是,配位原子是,配位数是6
C.中含有离子键、极性共价键和非极性共价键
D.与反应可得到一种蓝色沉淀,该沉淀物质晶胞的结构如图所示(未画出),则一个晶胞中的个数为4
6.下列叙述正确的是( )
A.属于烯烃的同分异构体有5种(不考虑立体异构)
B.立方烷()的六氯取代物有6种
C.乙烯和1,3-丁二烯互为同系物
D.三联苯()的一氯代物有6种
7.经研究发现白蚁信息素有①()和②(),家蚕的信息素为③。下列说法中不正确的是( )
A.①的名称是2,4-二甲基-1-庚烯②的名称是3,7-二甲基-1-辛烯
B.②和①属于同系物
C.③与氢气加成产物有3种
D.三种信息素均能使溴的四氯化碳溶液褪色
8.下列实验方案不合理的是( )
A.除去乙烷中的乙烯,可用溶液
B.分离苯和溴苯的混合物,可用蒸馏法
C.用饱和溶液除去乙酸乙酯中混有的乙酸等
D.可用水来鉴别苯、乙醇、四氯化碳
9.下列命名正确的是( )
A.2-乙基丙烷 B.2,2,3-三甲基戊烷
C.2-甲基-2-丙烯 D.溴乙烷
10.硒化锌是一种重要的半导体材料,其立方晶胞结构如图甲所示,乙图为该晶胞沿z轴方向在xy平面的投影,已知晶胞边长为apm。下列说法不正确的是( )
A.在周期表中的位置是第四周期IIB族
B.该晶体的化学式为ZnSe
C.将和的位置全部互换后所得晶体结构不变
D.图中点原子的坐标为,则点原子的坐标为
11.下列判断正确的是( )
A.沸点:高于
B.键角:
C.分子的键角都是180°
D.(甲醛)、的空间结构都是平面三角形
12.二氯化二硫是广泛用于橡胶工业的硫化剂,广泛用于石油化工,其分子结构如下图所示。制备方法:在120℃向硫磺粉(用浸润)中通入。下列说法错误的是( )
A.分子为极性分子
B.用浸润可加快反应速率,体现相似相溶原理
C.中原子的杂化类型为杂化
D.若晶体类似干冰晶体,则每个周围等距且紧邻的有12个
13.某同学分别用下列装置a和b制备溴苯,下列说法错误的是( )
A.两烧瓶中均出现红棕色气体,说明反应放热
B.a装置锥形瓶中出现淡黄色沉淀,说明烧瓶中发生取代反应
C.反应后的混合液中加入氢氧化钠后会有红褐色沉淀生成
D.b装置中的倒置漏斗起防倒吸作用,漏斗内形成白烟
14.下列说法正确的是( )
A.中至少有8个碳原子共面
B.螺[2,2]戊烷()中所有碳原子均处于同一平面
C.2,4,6—三溴苯酚()所有原子一定处于同一平面
D.有机物()最多6个原子处于同一直线
二、填空题(共58分)
15.(每空2分,共18分)有机物种类繁多,广泛存在,在生产和生活中有着重要的应用。
(1)下列各组有机物中,互为同系物的是______(填序号),是同一物质的是______,互为同分异构体的是______(填序号)。①乙烷和异丁烷;②和;
③和;④二甲醚和乙醇;⑤和;
(2)某芳香烃的分子式为,它可能有的同分异构体共______种,其中一溴代物只有两种的是______(结构简式)。
(3)某学习小组研究含氧衍生物A的组成和结构,研究过程如下:称取9gA在足量氧气中充分燃烧,并使产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g,对A进行波谱分析,结果如下:
①由质谱图可知A的分子式为______,结合红外光谱和核磁共振氢谱可知A的结构简式为______,该分子中有______个手性碳原子。
(2)经消去反应可以得到,则发生加聚反应后所得产物的结构简式为______.
16.(每空2分,共14分)
Ⅰ:(I)原子序数依次增大的五种短周期元素,其中是原子半径最小的元素,和的基态原子能级所含成单电子数均为的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)三种元素的第一电离能由大到小的顺序是______.
(2)与所含键的比值为______.
(3)根据等电子体理论可以预测-的空间构型为______.
Ⅱ:铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(4)可以与、有机分子等形成配合物。基态的电子排布式为______.
(5)普鲁士蓝俗称铁蓝,结构如图甲所示(未画出),平均每两个立方体中含有一个,该晶体的化学式为______。又知该晶体中铁元素有价和价两种,则与的个数比为______。
(6)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为______。
17.(每空2分,共14分)硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)硼酸()是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
①硼酸中B原子的杂化轨道类型为______。
②硼酸晶体中存在的作用力有范德华力和______。
③加热时,硼酸的溶解度增大,主要原因是______。
(2)硼氢化钠是有机化学中的一种常用还原剂,的空间构型是______.
(3)硼化镁晶体在时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如下图(左)是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为______。
(4)金刚石的晶胞如上图(右)。立方氮化硼的结构与金刚石相似,已知晶胞边长为apm,则氮原子与硼原子间的最短距离是______pm,立方氮化硼的密度是______。(只要求列算式,不必计算出数值,阿伏加德罗常数用表示)。
18.(每空2分,共12分)芳香化合物A是一种基本化工原料,可以从煤和石油中得到。A、B、C、D、E的转化关系如图所示:
回答下列问题:
(1)A的化学名称是______。
(2)A→B的反应类型是______,在该反应的副产物中,与B互为同分异构体的副产物的结构简式为______。
(3)A→C的化学方程式为______。
(4)A与酸性溶液反应可得到D,D中所含官能团名称是______,写出D的结构简式:______。
钦州市2023-2024学年高二下学期期中考试化学答案
1-5 BCCDD 6-10 ACABD 11-14 ACBD
15.(每空2分,共18分)(1)①⑤ ③ ②④
(2)4
(3)① 1
16.(每空2分,共14分)
(1) (2) (3)直线形
(4) (5) (6)
17.(每空2分,共14分)
(1) 氢键、共价键 加热破坏了硼酸分子之间的氢键
(2)正四面体 (3)
(4)
18.(每空2分,共12分)
(1)邻二甲苯(或1,2-二甲基苯) (2)取代反应
(3)(或)
(4)羧基
同课章节目录
