2024年山东省济南市市中区四校九年级下学期中考模拟化学试卷(含答案)
文档属性
| 名称 | 2024年山东省济南市市中区四校九年级下学期中考模拟化学试卷(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 538.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-20 00:00:00 | ||
图片预览




文档简介
山东省济南市市中区四校2024届九年级下学期中考模拟化学试卷
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.奇妙的化学,几乎无处不在,时刻影响着我们的生活,不断推动着人类社会向前发展。下列过程中没有发生化学变化的是( )
A.生石灰制熟石灰 B.膜法淡化海水
C.高粱制成烧酒 D.铁矿石炼成铁
2.“碳中和”是使碳排放与碳吸收达平衡,实现二氧化碳相对“零排放”。为了实现“碳中和”,下列做法不正确的是( )
A.露天焚烧农作物秸秆以增加肥效 B.废旧书籍、报纸分类回收再利用
C.循环利用制造燃料、尿素 D.大力植树造林,严禁乱砍滥伐森林
3.化学与我们的健康、生产、生活息息相关。下列说法中,不正确的是( )
A.洒出的酒精在桌上燃烧起来,立刻用湿抹布扑灭
B.为防止食品变质,可用甲醛溶液来浸泡海产品
C.用灼烧闻气味的方法,可以区分棉制品和羊毛制品
D.用蒸馏的方法,可以得到净化程度较高的水
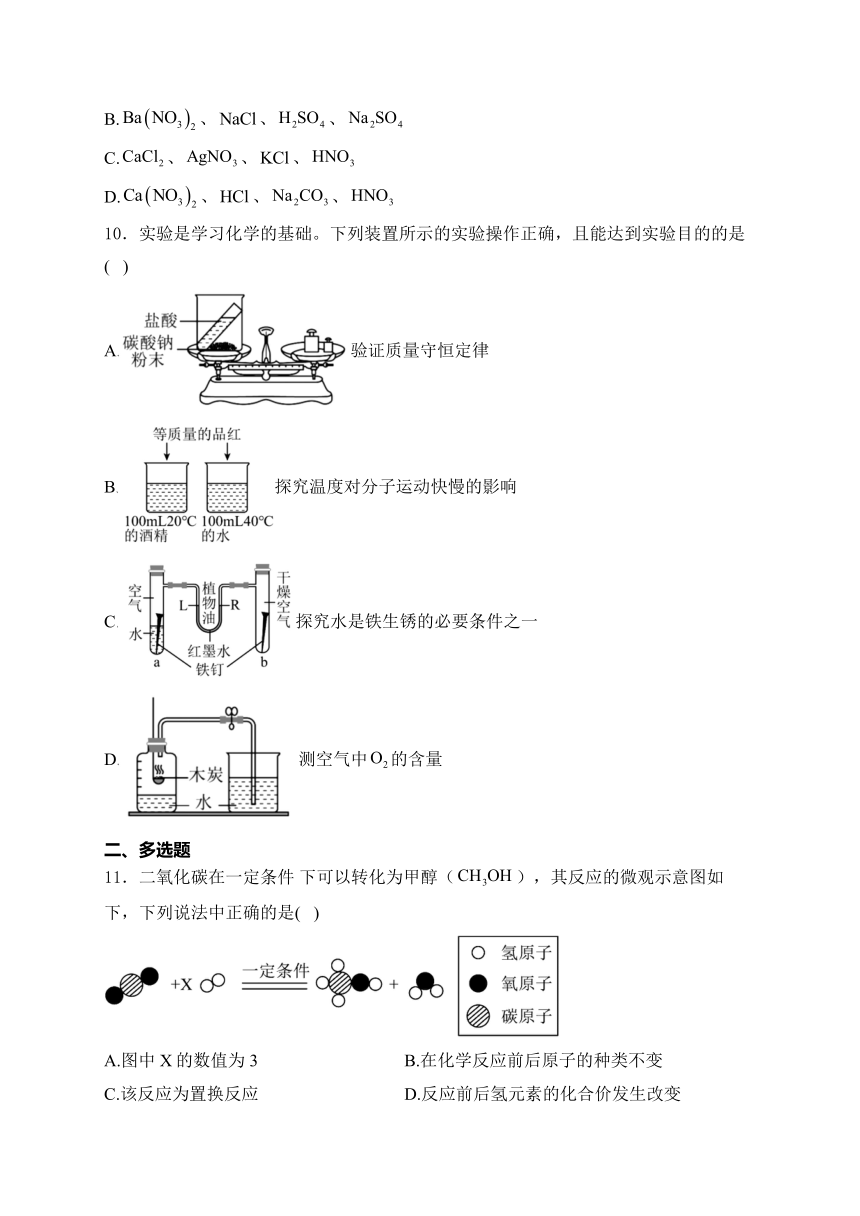
4.规范的实验操作是实验成功的保障。下列基本实验操作中,正确的是( )
A.吸取液体药品 B.验满二氧化碳
C.稀释浓硫酸 D.过滤黄泥水
5.下列事实,不能作为相应微粒基本性质观点证据的是( )
A.蔗糖放入水中溶解——蔗糖分子在不断运动
B.水分解得到氢气和氧气——化学变化中分子是可分
C.和具有不同的化学性质——构成它们的分子不同
D.向1L黄豆中倒入1L大米体积小于2L——分子之间存在间隔
6.“中国高铁”已成为我国外交的新名片,高铁车身主要采用镍铬奥氏体不锈钢制成。下图为铬元素在元素周期表中的信息及其原子结构示意图。下列说法不正确的是( )
A.铬元素属于金属元素
B.铬元素的原子序数为24
C.铬的相对原子质量是52.00g
D.铬原子在化学变化中易失去电子
7.化学观念是化学学科核心素养的重要内容。下列说法中,正确的是( )
A.利用化学反应可以改变原子的种类和数目
B.某物质的饱和溶液比不饱和溶液含溶质更多
C.物质的结构决定其性质,性质决定其用途
D.不同元素种类之间的本质区别是中子数不同
8.下列对主题知识的归纳,完全正确的是( )
A化学与健康 B化学与农业
①鸡蛋、大豆,瘦肉中富含蛋白质 ②人们常用酒精消毒是利用酒精可以使蛋白质变性的性质 ①用铁桶配制农药波尔多液 ②农业上可用熟石灰来改良酸性土壤
C化学与材料 D化学与生活
①塑料,合金,合成橡胶都属于合成材料 ②用灼烧闻气味的方法鉴别羊毛线与纯棉线 ①炒菜时油锅着火用水浇灭 ②苏打是焙制糕点的发酵粉成分之一
A.A B.B C.C D.D
9.下列各组物质的溶液,不用其他试剂,用观察或组内物质相互混合的方法就能鉴别出来的是( )
A.、、、
B.、、、
C.、、、
D.、、、
10.实验是学习化学的基础。下列装置所示的实验操作正确,且能达到实验目的的是( )
A.验证质量守恒定律
B.探究温度对分子运动快慢的影响
C.探究水是铁生锈的必要条件之一
D.测空气中的含量
二、多选题
11.二氧化碳在一定条件 下可以转化为甲醇(),其反应的微观示意图如下,下列说法中正确的是( )
A.图中X的数值为3 B.在化学反应前后原子的种类不变
C.该反应为置换反应 D.反应前后氢元素的化合价发生改变
12.推理与归纳是研究和学习化学重要方法。下列说法中,正确的是( )
A.溶液具有均一、稳定性,所以均一、稳定的液体一定是溶液
B.中和反应生成盐和水,但生成盐和水的反应不一定是中和反应
C.碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定是碱性溶液
D.活泼金属与酸反应能生成气体,所以与酸反应生成气体的物质一定是活泼金属
13.为除去下列各物质中混有的少量杂质,采用的相应除杂方案中,不正确的是( )
物质 杂质 除杂方案
A 通过足量灼热的木炭
B 高温煅烧,充分反应
C 溶液 加入适量溶液
D 溶液 加入过量溶液,过滤
A.A B.B C.C D.D
14.为探究金属与盐的反应,向与的混合溶液中加入ag某金属M的粉末,充分反应,过滤,分别向滤渣和滤液中加入适量稀盐酸,如下图所示。
通过分析图中信息进行判断,下列说法中,合理的是( )
A.滤液中一定没有银离子
B.加入的金属M可能是单质铁
C.滤渣的质量一定小于ag
D.滤渣中一定含有金属单质、、M
15.(乙醇)是一种燃料,在氧气中完全燃烧,生成和,但若不完全燃烧,会产生有毒的,若乙醇不完全燃烧得到燃烧产物、、的总质量为25.2g,其中为10.8g,下列实验分析正确的是( )
A.不完全燃烧就不遵守质量守恒定律 B.消耗的乙醇质量是9.2g
C.生成的和的质量比为7:11 D.燃烧中消耗的的质量为16g
三、填空题
16.按要求从硝酸钾、氢气、氧化钙、氢氧化铜中选择合适的物质,将其化学式填写在相应的横线上。
(1)①一种清洁燃料______
②一种食品干燥剂______
③一种复合肥料______
④一种难溶性的碱______
(2)眼镜戴久了,镜架上会产生铜锈,其主要成分是碱式碳酸铜[],它是一种绿色的固体粉末。
①铜锈属于______(填“纯净物”或“混合物”)。小凯同学认为:铜的锈蚀是铜与水、氧气共同作用的结果。对于这个结论你认为还应补充的一个重要的影响因素是______(填化学式)。
②碱式碳酸铜[]中碳、氧两元素的质量之比为______(填写最简整数比)。
(3)化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔。1摩尔任何物质中含有构成它的微粒个数都是个,1摩尔任何物质的质量是以g为单位,数值上都等于该物质的相对分子质量。例如1摩尔水的各种量关系如图。计算:
①1摩尔水的水分子中氧原子质量______g。
②1摩尔葡萄糖()的质量为______g。
17.新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如下图所示:
(1)①纳米级粉在氧气中能容易燃烧生成黑色固体,此黑色固体化学式为______。
②在制备纳米级粉的工艺流程中,不参与反应,根据的化学性质,推测流程中的作用是______。
③上述制备纳米级铁粉的化学方程式是______,反应前后铁元素的化合价______(填“升高”、“不变”“降低”之一)。
④纳米级铁粉能吸附水中的某些污染物,吸附后经沉降、______(填操作名称)可除去污染物。
⑤该流程中,12.7kg氯化亚铁固体理论上能制得纳米级粉的质量是______kg。
(2)我国化学家侯德榜创立了侯氏制碱法,开创了世界制碱工业的新纪元,该技术中生成的同时得到副产品。和的溶解度曲线如图所示。
①在℃时,的溶解度______的溶解度(填“>”、“<”或“=”)。
②在℃时,向盛有50g水的烧杯中加入12g充分溶解,此时溶液的溶质质量分数为______(精确到0.1%)。若升温至℃(不考虑水分蒸发),所得溶液中溶质与溶剂的质量之比为______(填写最简整数比)。
③将℃时不同质量的两物质的饱和溶液同时升温至℃,下列说法正确的是______(填字母)。
A.℃时,溶液与溶液的质量相等
B.℃时,溶液与溶液都不饱和溶液
C.℃时,溶液中溶质的质量小于溶液中溶质的质量
D.℃时,溶液的溶质质量分数小于溶液的溶质质量分数
18.下图所示为实验室中常见的气体制备、净化和收集实验的部分仪器。
试根据要求回答下列问题:
(1)已知在常温下气体、水蒸气都能与反应产生,其中与反应的化学方程式为:。某兴趣小组的同学们为探究与反应的产物,所选装置按“A→D→B→E→F”的顺序连接(实验前检验装置的气密性,假设所发生的化学反应都完全充分进行)。
①请写出仪器A中用石灰石和稀盐酸制备的化学方程式______。
②装置中B的作用是______;F的作用是______。
③若检验有生成,可将带火星的木条放在装置a处,观察到的现象是______。
④a处的氧气可用G装置来收集氧气,能用这种方法收集氧气的原因是______。
⑤将E装置反应后的固体物质溶于水配成溶液,然后向该溶液中加入足量的下列______(填序号)试剂就可以证明有生成。
A.稀盐酸 B.溶液 C.溶液 D.澄清的石灰水
(2)用干燥纯净的氧气对纤维素的组成进行分析探究实验(资料显示纤维素只含C、H、O三种元素)。所选装置按“氧气→E→B→C→F”的顺序连接(实验前检验装置的气密性,假设所发生的化学反应都完全充分进行)。
①装置E的玻璃管中放入纤维素试样的质量为wg,充分反应后,测得装置B的质量增加ag,装置C的质量增加bg,则纤维素中氧元素的质量为______g(计算结果用含字母的代数式表示)。
②若实验中使用的氧气未干燥,这样测算出的纤维素中碳元素与氢元素的质量比与实际值比较将______(填“偏大”“偏小”“基本一致”“无法确定”之一)。
19.如图所示“天宫号”化学空间站的舱室分别代表初中化学常见物质。图中“→”表示转化关系,“—”表示相互能反应,所涉及反应均为初中常见的化学反应。已知A是最常用的溶剂,D的俗名叫烧碱,E是人体胃液中含有的酸,A、B、E、F分别属于四种不同类别的化合物,C是由三种元素组成的化合物。
(1)①A的化学式为______。
②C与F反应的类型是______反应。(填”化合”“分解”“置换”“复分解”之一)
③C→D反应的化学方程式为______。
④空间站迎来了首批访问者,他们搭乘的载人舱X与连接舱C成功对接(如上图所示),则载人舱X代表的物质可能是______(填序号)。
A.C B. C. D.
(2)已知某固体样品A可能是和或两者之一,另有一固体样品B,其中可能含有、、、四种物质中的一种或多种,按下图所示进行探究实验,出现的现象如图中所示。(设过程中所有可能发生的反应都恰好完全进行)
试根据实验过程和图示提供的信息,进行分析推理,回答下列问题:
①气体C的化学式为______,沉淀F的颜色为______。
②溶液H中,一定大量存在的阴离子有______种(填数字)。
③写出过程③中产生沉淀I的化学方程式______。
④固体样品B中一定不存在的物质是______(填化学式),得出此结论的理由是______。
四、实验题
20.化学兴趣小组认为,在实验室可用氢氧化钠溶液吸收多余二氧化碳,从而实现实验室二氧化碳的“零排放”。小组同学对吸收后溶液中溶质的成分产生兴趣并进行探究。
【查阅资料】①与溶液反应过程中,当过量时,会继续反应生成;
②溶液呈弱碱性,一般不与溶液反应,与稀盐酸反应产生气体;
③溶液呈中性。
【提出问题】氢氧化钠溶液吸收二氧化碳气体后,溶液中溶质的成分是什么?
【作出猜想】猜想①:、;
猜想②:;
猜想③;、;
猜想④:。
【进行实验】
步骤1:取少量待测液于试管中,加入溶液,产生白色沉淀;
步骤2:继续加入溶液至不再产生沉淀,过滤,取滤液向其中加入适量稀盐酸,无气泡产生;
步骤3:另取步骤2的少量滤液,向其中滴入无色酚酞溶液,无色酚酞溶液变红。
【结论分析】
(1)步骤1的目的是验证猜想______(填写“①”“②”“③”“④”之一)是否正确。
(2)根据上述实验结果可以推断,氢氧化钠溶液吸收二氧化碳气体后,溶液中溶质的成分是______(填化学式)。
(3)如果去掉步骤2中的“加入适量稀盐酸”,上述实验的最终结论不可靠,理由是______。
为测定某纯碱样品的纯度(杂质为),某小组同学取样品12.0g,将其全部放入一洁净的烧杯中,然后加入足量蒸馏水,搅拌,使固体完全溶解。再向烧杯中逐滴加入溶质质量分数为10.0%的溶液,反应过程中产生沉淀的质量与所滴入溶液的质量关系如图所示。试回答:
(4)当加入溶液50.0g时(即A点),所得溶液中一定存在的溶质是______(填化学式)。
(5)试通过化学方程式计算样品中的质量分数。(计算结果精确至0.1%)
参考答案
1.答案:B
解析:
2.答案:A
解析:
3.答案:B
解析:
4.答案:C
解析:
5.答案:D
解析:
6.答案:C
解析:
7.答案:C
解析:
8.答案:A
解析:
9.答案:A
解析:
10.答案:C
解析:
11.答案:ABD
解析:
12.答案:BC
解析:
13.答案:ACD
解析:
14.答案:AD
解析:
15.答案:BCD
解析:
16.答案:(1);;;
(2)混合物;;3:20
(3)16;180
解析:
17.答案:(1)①
②隔绝氧气防止生成的纳米级铁粉被氧化
③;降低
④过滤
⑤设12.7kg氯化亚铁固体理论上能制得纳米级粉的质量是x,
x=5.6kg
答:12.7kg氯化亚铁固体理论上能制得纳米级粉的质量是5.6kg。
(2)①=
②16.7%;6:25
③BD
解析:
18.答案:(1)①
②吸收水分,防止与水发生反应;吸收空气中的二氧化碳和水,防止对实验造成干扰
③带火星的木条复燃
④氧气的密度比空气大
⑤AD
(2)①
②偏小
解析:
19.答案:(1)①
②复分解
③
④B
(2)①;白色
②3
③
④;若样品B中存在硫酸铜,则溶液E中不含有氢氧化钠,步骤③中不会生成气体G
解析:
20.答案:(1)④
(2)、
(3)溶液呈弱碱性,也能使无色酚酞试液变红,影响氢氧化钠的鉴别
(4)、
(5)根据图示可知,加入氯化钙的质量为111g时,碳酸钠恰好完全反应
设样品中碳酸钠的质量为x
x=10.6
样品中碳酸钠的质量分数为:
答:样品中的质量分数为88.3%。
解析:
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.奇妙的化学,几乎无处不在,时刻影响着我们的生活,不断推动着人类社会向前发展。下列过程中没有发生化学变化的是( )
A.生石灰制熟石灰 B.膜法淡化海水
C.高粱制成烧酒 D.铁矿石炼成铁
2.“碳中和”是使碳排放与碳吸收达平衡,实现二氧化碳相对“零排放”。为了实现“碳中和”,下列做法不正确的是( )
A.露天焚烧农作物秸秆以增加肥效 B.废旧书籍、报纸分类回收再利用
C.循环利用制造燃料、尿素 D.大力植树造林,严禁乱砍滥伐森林
3.化学与我们的健康、生产、生活息息相关。下列说法中,不正确的是( )
A.洒出的酒精在桌上燃烧起来,立刻用湿抹布扑灭
B.为防止食品变质,可用甲醛溶液来浸泡海产品
C.用灼烧闻气味的方法,可以区分棉制品和羊毛制品
D.用蒸馏的方法,可以得到净化程度较高的水
4.规范的实验操作是实验成功的保障。下列基本实验操作中,正确的是( )
A.吸取液体药品 B.验满二氧化碳
C.稀释浓硫酸 D.过滤黄泥水
5.下列事实,不能作为相应微粒基本性质观点证据的是( )
A.蔗糖放入水中溶解——蔗糖分子在不断运动
B.水分解得到氢气和氧气——化学变化中分子是可分
C.和具有不同的化学性质——构成它们的分子不同
D.向1L黄豆中倒入1L大米体积小于2L——分子之间存在间隔
6.“中国高铁”已成为我国外交的新名片,高铁车身主要采用镍铬奥氏体不锈钢制成。下图为铬元素在元素周期表中的信息及其原子结构示意图。下列说法不正确的是( )
A.铬元素属于金属元素
B.铬元素的原子序数为24
C.铬的相对原子质量是52.00g
D.铬原子在化学变化中易失去电子
7.化学观念是化学学科核心素养的重要内容。下列说法中,正确的是( )
A.利用化学反应可以改变原子的种类和数目
B.某物质的饱和溶液比不饱和溶液含溶质更多
C.物质的结构决定其性质,性质决定其用途
D.不同元素种类之间的本质区别是中子数不同
8.下列对主题知识的归纳,完全正确的是( )
A化学与健康 B化学与农业
①鸡蛋、大豆,瘦肉中富含蛋白质 ②人们常用酒精消毒是利用酒精可以使蛋白质变性的性质 ①用铁桶配制农药波尔多液 ②农业上可用熟石灰来改良酸性土壤
C化学与材料 D化学与生活
①塑料,合金,合成橡胶都属于合成材料 ②用灼烧闻气味的方法鉴别羊毛线与纯棉线 ①炒菜时油锅着火用水浇灭 ②苏打是焙制糕点的发酵粉成分之一
A.A B.B C.C D.D
9.下列各组物质的溶液,不用其他试剂,用观察或组内物质相互混合的方法就能鉴别出来的是( )
A.、、、
B.、、、
C.、、、
D.、、、
10.实验是学习化学的基础。下列装置所示的实验操作正确,且能达到实验目的的是( )
A.验证质量守恒定律
B.探究温度对分子运动快慢的影响
C.探究水是铁生锈的必要条件之一
D.测空气中的含量
二、多选题
11.二氧化碳在一定条件 下可以转化为甲醇(),其反应的微观示意图如下,下列说法中正确的是( )
A.图中X的数值为3 B.在化学反应前后原子的种类不变
C.该反应为置换反应 D.反应前后氢元素的化合价发生改变
12.推理与归纳是研究和学习化学重要方法。下列说法中,正确的是( )
A.溶液具有均一、稳定性,所以均一、稳定的液体一定是溶液
B.中和反应生成盐和水,但生成盐和水的反应不一定是中和反应
C.碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定是碱性溶液
D.活泼金属与酸反应能生成气体,所以与酸反应生成气体的物质一定是活泼金属
13.为除去下列各物质中混有的少量杂质,采用的相应除杂方案中,不正确的是( )
物质 杂质 除杂方案
A 通过足量灼热的木炭
B 高温煅烧,充分反应
C 溶液 加入适量溶液
D 溶液 加入过量溶液,过滤
A.A B.B C.C D.D
14.为探究金属与盐的反应,向与的混合溶液中加入ag某金属M的粉末,充分反应,过滤,分别向滤渣和滤液中加入适量稀盐酸,如下图所示。
通过分析图中信息进行判断,下列说法中,合理的是( )
A.滤液中一定没有银离子
B.加入的金属M可能是单质铁
C.滤渣的质量一定小于ag
D.滤渣中一定含有金属单质、、M
15.(乙醇)是一种燃料,在氧气中完全燃烧,生成和,但若不完全燃烧,会产生有毒的,若乙醇不完全燃烧得到燃烧产物、、的总质量为25.2g,其中为10.8g,下列实验分析正确的是( )
A.不完全燃烧就不遵守质量守恒定律 B.消耗的乙醇质量是9.2g
C.生成的和的质量比为7:11 D.燃烧中消耗的的质量为16g
三、填空题
16.按要求从硝酸钾、氢气、氧化钙、氢氧化铜中选择合适的物质,将其化学式填写在相应的横线上。
(1)①一种清洁燃料______
②一种食品干燥剂______
③一种复合肥料______
④一种难溶性的碱______
(2)眼镜戴久了,镜架上会产生铜锈,其主要成分是碱式碳酸铜[],它是一种绿色的固体粉末。
①铜锈属于______(填“纯净物”或“混合物”)。小凯同学认为:铜的锈蚀是铜与水、氧气共同作用的结果。对于这个结论你认为还应补充的一个重要的影响因素是______(填化学式)。
②碱式碳酸铜[]中碳、氧两元素的质量之比为______(填写最简整数比)。
(3)化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔。1摩尔任何物质中含有构成它的微粒个数都是个,1摩尔任何物质的质量是以g为单位,数值上都等于该物质的相对分子质量。例如1摩尔水的各种量关系如图。计算:
①1摩尔水的水分子中氧原子质量______g。
②1摩尔葡萄糖()的质量为______g。
17.新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如下图所示:
(1)①纳米级粉在氧气中能容易燃烧生成黑色固体,此黑色固体化学式为______。
②在制备纳米级粉的工艺流程中,不参与反应,根据的化学性质,推测流程中的作用是______。
③上述制备纳米级铁粉的化学方程式是______,反应前后铁元素的化合价______(填“升高”、“不变”“降低”之一)。
④纳米级铁粉能吸附水中的某些污染物,吸附后经沉降、______(填操作名称)可除去污染物。
⑤该流程中,12.7kg氯化亚铁固体理论上能制得纳米级粉的质量是______kg。
(2)我国化学家侯德榜创立了侯氏制碱法,开创了世界制碱工业的新纪元,该技术中生成的同时得到副产品。和的溶解度曲线如图所示。
①在℃时,的溶解度______的溶解度(填“>”、“<”或“=”)。
②在℃时,向盛有50g水的烧杯中加入12g充分溶解,此时溶液的溶质质量分数为______(精确到0.1%)。若升温至℃(不考虑水分蒸发),所得溶液中溶质与溶剂的质量之比为______(填写最简整数比)。
③将℃时不同质量的两物质的饱和溶液同时升温至℃,下列说法正确的是______(填字母)。
A.℃时,溶液与溶液的质量相等
B.℃时,溶液与溶液都不饱和溶液
C.℃时,溶液中溶质的质量小于溶液中溶质的质量
D.℃时,溶液的溶质质量分数小于溶液的溶质质量分数
18.下图所示为实验室中常见的气体制备、净化和收集实验的部分仪器。
试根据要求回答下列问题:
(1)已知在常温下气体、水蒸气都能与反应产生,其中与反应的化学方程式为:。某兴趣小组的同学们为探究与反应的产物,所选装置按“A→D→B→E→F”的顺序连接(实验前检验装置的气密性,假设所发生的化学反应都完全充分进行)。
①请写出仪器A中用石灰石和稀盐酸制备的化学方程式______。
②装置中B的作用是______;F的作用是______。
③若检验有生成,可将带火星的木条放在装置a处,观察到的现象是______。
④a处的氧气可用G装置来收集氧气,能用这种方法收集氧气的原因是______。
⑤将E装置反应后的固体物质溶于水配成溶液,然后向该溶液中加入足量的下列______(填序号)试剂就可以证明有生成。
A.稀盐酸 B.溶液 C.溶液 D.澄清的石灰水
(2)用干燥纯净的氧气对纤维素的组成进行分析探究实验(资料显示纤维素只含C、H、O三种元素)。所选装置按“氧气→E→B→C→F”的顺序连接(实验前检验装置的气密性,假设所发生的化学反应都完全充分进行)。
①装置E的玻璃管中放入纤维素试样的质量为wg,充分反应后,测得装置B的质量增加ag,装置C的质量增加bg,则纤维素中氧元素的质量为______g(计算结果用含字母的代数式表示)。
②若实验中使用的氧气未干燥,这样测算出的纤维素中碳元素与氢元素的质量比与实际值比较将______(填“偏大”“偏小”“基本一致”“无法确定”之一)。
19.如图所示“天宫号”化学空间站的舱室分别代表初中化学常见物质。图中“→”表示转化关系,“—”表示相互能反应,所涉及反应均为初中常见的化学反应。已知A是最常用的溶剂,D的俗名叫烧碱,E是人体胃液中含有的酸,A、B、E、F分别属于四种不同类别的化合物,C是由三种元素组成的化合物。
(1)①A的化学式为______。
②C与F反应的类型是______反应。(填”化合”“分解”“置换”“复分解”之一)
③C→D反应的化学方程式为______。
④空间站迎来了首批访问者,他们搭乘的载人舱X与连接舱C成功对接(如上图所示),则载人舱X代表的物质可能是______(填序号)。
A.C B. C. D.
(2)已知某固体样品A可能是和或两者之一,另有一固体样品B,其中可能含有、、、四种物质中的一种或多种,按下图所示进行探究实验,出现的现象如图中所示。(设过程中所有可能发生的反应都恰好完全进行)
试根据实验过程和图示提供的信息,进行分析推理,回答下列问题:
①气体C的化学式为______,沉淀F的颜色为______。
②溶液H中,一定大量存在的阴离子有______种(填数字)。
③写出过程③中产生沉淀I的化学方程式______。
④固体样品B中一定不存在的物质是______(填化学式),得出此结论的理由是______。
四、实验题
20.化学兴趣小组认为,在实验室可用氢氧化钠溶液吸收多余二氧化碳,从而实现实验室二氧化碳的“零排放”。小组同学对吸收后溶液中溶质的成分产生兴趣并进行探究。
【查阅资料】①与溶液反应过程中,当过量时,会继续反应生成;
②溶液呈弱碱性,一般不与溶液反应,与稀盐酸反应产生气体;
③溶液呈中性。
【提出问题】氢氧化钠溶液吸收二氧化碳气体后,溶液中溶质的成分是什么?
【作出猜想】猜想①:、;
猜想②:;
猜想③;、;
猜想④:。
【进行实验】
步骤1:取少量待测液于试管中,加入溶液,产生白色沉淀;
步骤2:继续加入溶液至不再产生沉淀,过滤,取滤液向其中加入适量稀盐酸,无气泡产生;
步骤3:另取步骤2的少量滤液,向其中滴入无色酚酞溶液,无色酚酞溶液变红。
【结论分析】
(1)步骤1的目的是验证猜想______(填写“①”“②”“③”“④”之一)是否正确。
(2)根据上述实验结果可以推断,氢氧化钠溶液吸收二氧化碳气体后,溶液中溶质的成分是______(填化学式)。
(3)如果去掉步骤2中的“加入适量稀盐酸”,上述实验的最终结论不可靠,理由是______。
为测定某纯碱样品的纯度(杂质为),某小组同学取样品12.0g,将其全部放入一洁净的烧杯中,然后加入足量蒸馏水,搅拌,使固体完全溶解。再向烧杯中逐滴加入溶质质量分数为10.0%的溶液,反应过程中产生沉淀的质量与所滴入溶液的质量关系如图所示。试回答:
(4)当加入溶液50.0g时(即A点),所得溶液中一定存在的溶质是______(填化学式)。
(5)试通过化学方程式计算样品中的质量分数。(计算结果精确至0.1%)
参考答案
1.答案:B
解析:
2.答案:A
解析:
3.答案:B
解析:
4.答案:C
解析:
5.答案:D
解析:
6.答案:C
解析:
7.答案:C
解析:
8.答案:A
解析:
9.答案:A
解析:
10.答案:C
解析:
11.答案:ABD
解析:
12.答案:BC
解析:
13.答案:ACD
解析:
14.答案:AD
解析:
15.答案:BCD
解析:
16.答案:(1);;;
(2)混合物;;3:20
(3)16;180
解析:
17.答案:(1)①
②隔绝氧气防止生成的纳米级铁粉被氧化
③;降低
④过滤
⑤设12.7kg氯化亚铁固体理论上能制得纳米级粉的质量是x,
x=5.6kg
答:12.7kg氯化亚铁固体理论上能制得纳米级粉的质量是5.6kg。
(2)①=
②16.7%;6:25
③BD
解析:
18.答案:(1)①
②吸收水分,防止与水发生反应;吸收空气中的二氧化碳和水,防止对实验造成干扰
③带火星的木条复燃
④氧气的密度比空气大
⑤AD
(2)①
②偏小
解析:
19.答案:(1)①
②复分解
③
④B
(2)①;白色
②3
③
④;若样品B中存在硫酸铜,则溶液E中不含有氢氧化钠,步骤③中不会生成气体G
解析:
20.答案:(1)④
(2)、
(3)溶液呈弱碱性,也能使无色酚酞试液变红,影响氢氧化钠的鉴别
(4)、
(5)根据图示可知,加入氯化钙的质量为111g时,碳酸钠恰好完全反应
设样品中碳酸钠的质量为x
x=10.6
样品中碳酸钠的质量分数为:
答:样品中的质量分数为88.3%。
解析:
同课章节目录
