山西省太原市第五中学校2023-2024学年高一下学期5月月考化学试题(含答案)
文档属性
| 名称 | 山西省太原市第五中学校2023-2024学年高一下学期5月月考化学试题(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 577.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-20 00:00:00 | ||
图片预览



文档简介
太原市第五中学校2023-2024学年高一下学期5月月考
化学(试题)
可能用到的相对原子质量:H 1 C 12
一、选择题:本题共14个小题,1-9题每小题3分,10-14题每小题4分,共47分。
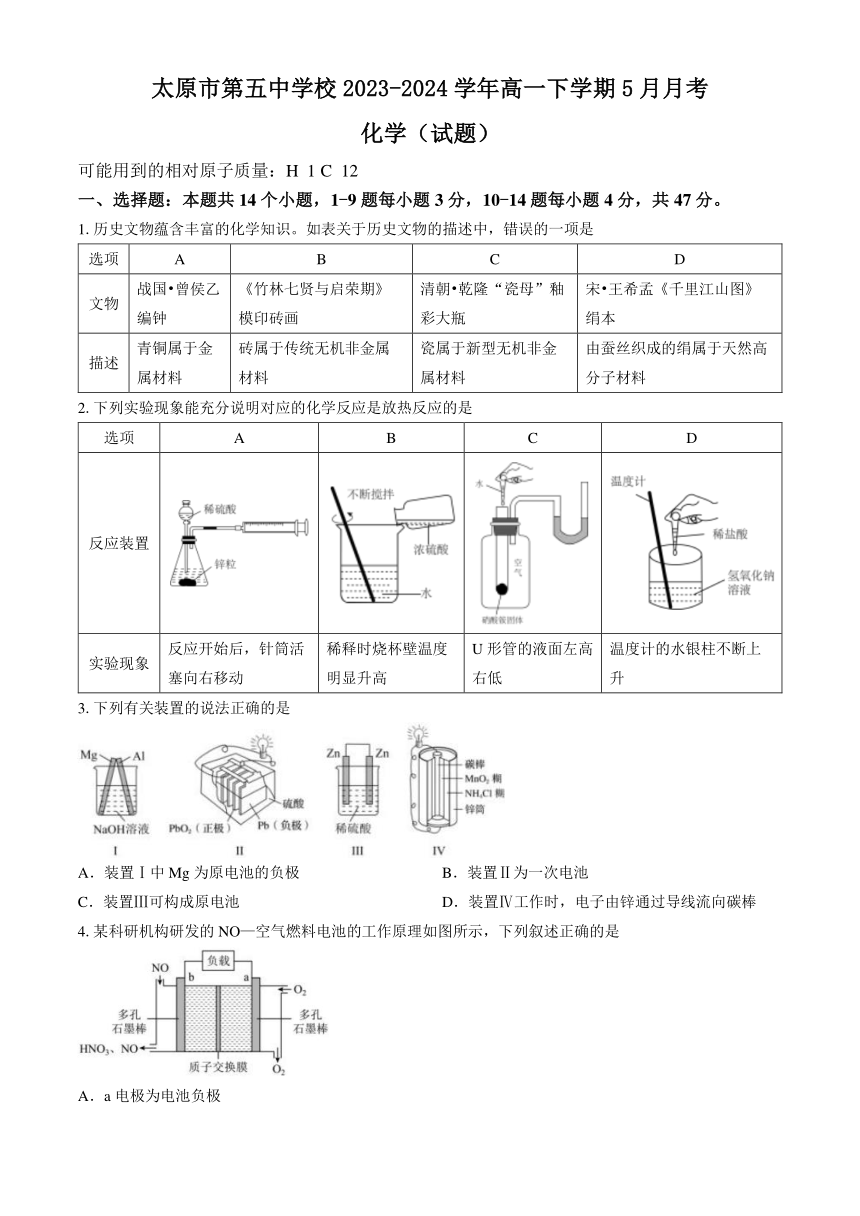
1.历史文物蕴含丰富的化学知识。如表关于历史文物的描述中,错误的一项是
选项 A B C D
文物 战国 曾侯乙编钟 《竹林七贤与启荣期》模印砖画 清朝 乾隆“瓷母”釉彩大瓶 宋 王希孟《千里江山图》绢本
描述 青铜属于金属材料 砖属于传统无机非金属材料 瓷属于新型无机非金属材料 由蚕丝织成的绢属于天然高分子材料
2.下列实验现象能充分说明对应的化学反应是放热反应的是
选项 A B C D
反应装置
实验现象 反应开始后,针筒活塞向右移动 稀释时烧杯壁温度明显升高 U形管的液面左高右低 温度计的水银柱不断上升
3.下列有关装置的说法正确的是
A.装置Ⅰ中Mg为原电池的负极 B.装置Ⅱ为一次电池
C.装置Ⅲ可构成原电池 D.装置Ⅳ工作时,电子由锌通过导线流向碳棒
4.某科研机构研发的NO—空气燃料电池的工作原理如图所示,下列叙述正确的是
A.a电极为电池负极
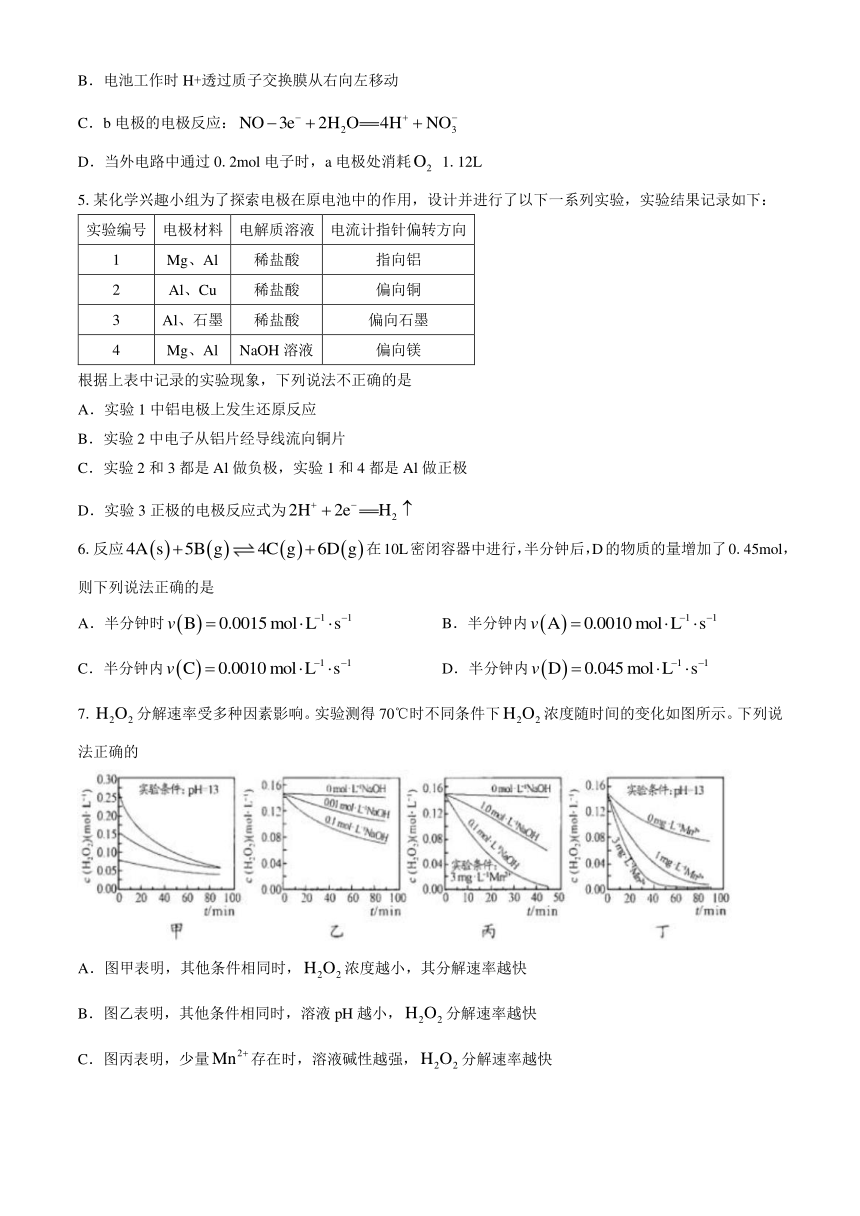
B.电池工作时H+透过质子交换膜从右向左移动
C.b电极的电极反应:
D.当外电路中通过0.2mol电子时,a电极处消耗 1.12L
5.某化学兴趣小组为了探索电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
实验编号 电极材料 电解质溶液 电流计指针偏转方向
1 Mg、Al 稀盐酸 指向铝
2 Al、Cu 稀盐酸 偏向铜
3 Al、石墨 稀盐酸 偏向石墨
4 Mg、Al NaOH溶液 偏向镁
根据上表中记录的实验现象,下列说法不正确的是
A.实验1中铝电极上发生还原反应
B.实验2中电子从铝片经导线流向铜片
C.实验2和3都是Al做负极,实验1和4都是Al做正极
D.实验3正极的电极反应式为
6.反应在10L密闭容器中进行,半分钟后,D的物质的量增加了0.45mol,则下列说法正确的是
A.半分钟时 B.半分钟内
C.半分钟内 D.半分钟内
7.分解速率受多种因素影响。实验测得70℃时不同条件下浓度随时间的变化如图所示。下列说法正确的
A.图甲表明,其他条件相同时,浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,分解速率越快
C.图丙表明,少量存在时,溶液碱性越强,分解速率越快
D.图丙和图丁表明,碱性溶液中,对分解速率的影响大
8.100mL 3mol/L硫酸溶液与过量锌粉反应,在一定温度下,为了减缓反应进行的速率,又不影响生成氢气的总量,可向反应物中加入适量的
A.碳酸钠溶液 B.醋酸钠溶液 C.溶液 D.1mol/L的硫酸溶液
9.已知:。现将体积比为1∶2的和的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.混合气体总物质的量保持不变 B.混合气体密度保持不变
C.(g)和(g)的体积比保持不变 D.每消耗1mol ,同时消耗0.5mol (g)
10.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是
A.反应在0~10s内,用Z表示的反应速率为0.158
B.反应在0~10s内,X的物质的量浓度减少了0.79
C.反应进行到10s时,Y的转化率为79.0%
D.反应的化学方程式为
11.下列物质的沸点由高到低排列的顺序是
① ② ③ ④
A.②④①③ B.④②①③ C.④②③① D.②④③①1
12.北京奥运会祥云火炬的主要燃料为丙烷,下列关于丙烷的说法正确的是
A.丙烷分子中3个碳原子在一条直线上 B.丙烷可以与溴水发生取代反应
C.丙烷在空气中燃烧只可能生成和 D.常温常压下,22g丙烷所含氢原子数为4
13.下列关于乙烯与聚乙烯的说法,正确的是
A.乙烯与聚乙烯都是纯净物
B.乙烯通过加成聚合反应得到聚乙烯,聚乙烯也可以通过降解得到乙烯
C.相同质量的乙烯与聚乙烯,完全燃烧所需要的氧气质量也相同
D.乙烯与聚乙烯,都能使酸性溶液褪色
14.化学是材料科学的基础,下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.制造特种防护服的芳纶纤维属于有机高分子材料
C.氧化铝熔点高,常用于制造耐高温材料
D.制造5G芯片的氮化铝属于无机非金属材料
二、非选择题:本题共5个小题,共53分。
15.(5分)
下列各组物质:①和 ②和 ③和
④和 ⑤癸烷和十六烷
⑥和
⑦和(在横线上填相应的序号)
(1)互为同位素的是 ;
(2)互为同分异构体的是 ;
(3)互为同素异形体的是 ;
(4)互为同系物的是 ;
(5)同一种物质的是 。
16.(15分)
(1)在某一容积为2L的密闭容器中,某一反应中A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化曲线如图所示:
回答下列问题:
①该反应的化学方程式为 。
②前2min用A的浓度变化表示的化学反应速率为 。在2min时,图像发生改变的原因是 (填字母)。
A.增大压强 B.降低温度 C.加入催化剂 D.增加A的物质的量
(2)在100℃时,将0.01mol的四氧化二氮气体充入0.1L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
时间/s 浓度/() 0 20 40 60 80 100
0.100 0.070 0.050 a b
0.000 0.060 0.120 0.120 0.120
试填空:
①该反应的化学方程式: ,达到平衡时四氧化二氮的转化率为 ,表中 ;a b。(填“>”“<”或“=”)
②在0~20s内,四氧化二氮的平均反应速率为 ,哪一时间段(指0~20、20~40、40~60、60~80、80~100s)反应速率最大? ,原因是
17.(10分)
二氯二氢硅()常用于外延法工艺中重要的硅源。该物质易燃、有毒,与水接触易水解,沸点为8.2℃。在铜催化作用下,HCl与硅在250~260℃反应可以制得。
(1)利用浓硫酸、浓盐酸为原料,选用A装置制取HCl,利用了浓硫酸的 性。
(2)D装置中生成二氯二氢硅的化学方程式为 。
(3)按照气体从左到右的方向,制取的装置(h处用止水夹夹好)连接顺序为a→( )→( )→( )→( )→( )→( )→( )(填仪器接口的字母,其中装置C用到2次)。
(4)按从左到右的顺序,前面装置C中装的药品为 ,后面装置C的作用为
。
(5)反应除生成二氯二氢硅之外,还会生成和 、 等。
18.(13分)
烷烃是一类有机化合物,分子中的碳原子都以碳碳单键相连,其余的价键都与氢结合而成的化合物,按要求回答下列与烷烃有关问题。
(1)上图均能表示甲烷的分子结构,对号入座(填字母):甲烷的球棍模型是 ,甲烷的电子式是 。
(2)有 种结构,证明甲烷不是平面结构,而是 结构。
(3)写出乙烷与氯气在光照条件下生成一氯乙烷的反应方程式 ,(2分)该反应的反应类型为 ;1mol乙烷与足量氯气在光照条件下充分反应,最多可生成HCl的物质的量 mol。(2分)
(4)已知戊烷有3种同分异构体,它们的结构简式分别为: ,(3分)上述同分异构体中,沸点最低的是 (写结构简式)。
19.(10分)
以作催化剂,可用乙烯脱除烟气中并回收单质硫。某兴趣小组同学设计实验验证该反应并检验产物中的,实验装置(夹持装置已略)如图所示:
已知:硫在20℃和50℃之间升华。
回答下列问题:
(1)装置a中的作用是 。(答出2点即可)
(2)装置b中有S、、生成,则发生反应的化学方程式为
。
(3)装置c用冷水水浴的目的是 。
(4)有同学认为可将溴水换成酸性高锰酸钾溶液,你认为是否可行,说明你的理由
。
(5)装置e中品红溶液的作用是 。
高一化学答案
一、选择题(1-9题每题3分10-14题每题4分)
1C 2D 3D 4C 5C 6C 7D 8B 9C 10C 11A 12D 13C 14A
二、非选择题
15.(5分,每空1分,每空全写对才得1分)
(1)互为同位素的是③;
(2)互为同分异构体的是④⑥;
(3)互为同素异形体的是①;
(4)互为同系物的是⑤
(5)同一种物质的是②⑦。
16.(15分)
(1)①(2分,连接符号写错扣1分,系数有错全错)
②0.1(2分,单位错0分) AC(1分,都对才有分)
(2)①(2分,连接符号写错扣1分) 60% > =
②0.0015(2分,单位错0分) 0~20s 开始时反应物的浓度最大
17.(10分)
(1)吸水
(2)(2分,条件占1分)
(3)d e f g b c d(2分,全对得2分,否则0分)
(4)或无水 尾气处理和防止空气中的水蒸气进入B中(2分,不全扣1分)
(5)
18.(13分,除标注外每空1分)
(1)C;B
(2)1;正四面体
(3)(2分,条件连接符号占1分);取代反应;6
(4)、、(3分,各1分);
19.(10分,每空2分)
(1)调控气流速度、使和乙烯混合均匀、干燥气体(没写全扣1分)
(2)(条件连接符号占1分)
(3)冷凝S蒸汽,收集S
(4)乙烯能被酸性溶液氧化成,对后面检验产物中的有干扰
(5)检验是否除尽
化学(试题)
可能用到的相对原子质量:H 1 C 12
一、选择题:本题共14个小题,1-9题每小题3分,10-14题每小题4分,共47分。
1.历史文物蕴含丰富的化学知识。如表关于历史文物的描述中,错误的一项是
选项 A B C D
文物 战国 曾侯乙编钟 《竹林七贤与启荣期》模印砖画 清朝 乾隆“瓷母”釉彩大瓶 宋 王希孟《千里江山图》绢本
描述 青铜属于金属材料 砖属于传统无机非金属材料 瓷属于新型无机非金属材料 由蚕丝织成的绢属于天然高分子材料
2.下列实验现象能充分说明对应的化学反应是放热反应的是
选项 A B C D
反应装置
实验现象 反应开始后,针筒活塞向右移动 稀释时烧杯壁温度明显升高 U形管的液面左高右低 温度计的水银柱不断上升
3.下列有关装置的说法正确的是
A.装置Ⅰ中Mg为原电池的负极 B.装置Ⅱ为一次电池
C.装置Ⅲ可构成原电池 D.装置Ⅳ工作时,电子由锌通过导线流向碳棒
4.某科研机构研发的NO—空气燃料电池的工作原理如图所示,下列叙述正确的是
A.a电极为电池负极
B.电池工作时H+透过质子交换膜从右向左移动
C.b电极的电极反应:
D.当外电路中通过0.2mol电子时,a电极处消耗 1.12L
5.某化学兴趣小组为了探索电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
实验编号 电极材料 电解质溶液 电流计指针偏转方向
1 Mg、Al 稀盐酸 指向铝
2 Al、Cu 稀盐酸 偏向铜
3 Al、石墨 稀盐酸 偏向石墨
4 Mg、Al NaOH溶液 偏向镁
根据上表中记录的实验现象,下列说法不正确的是
A.实验1中铝电极上发生还原反应
B.实验2中电子从铝片经导线流向铜片
C.实验2和3都是Al做负极,实验1和4都是Al做正极
D.实验3正极的电极反应式为
6.反应在10L密闭容器中进行,半分钟后,D的物质的量增加了0.45mol,则下列说法正确的是
A.半分钟时 B.半分钟内
C.半分钟内 D.半分钟内
7.分解速率受多种因素影响。实验测得70℃时不同条件下浓度随时间的变化如图所示。下列说法正确的
A.图甲表明,其他条件相同时,浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,分解速率越快
C.图丙表明,少量存在时,溶液碱性越强,分解速率越快
D.图丙和图丁表明,碱性溶液中,对分解速率的影响大
8.100mL 3mol/L硫酸溶液与过量锌粉反应,在一定温度下,为了减缓反应进行的速率,又不影响生成氢气的总量,可向反应物中加入适量的
A.碳酸钠溶液 B.醋酸钠溶液 C.溶液 D.1mol/L的硫酸溶液
9.已知:。现将体积比为1∶2的和的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.混合气体总物质的量保持不变 B.混合气体密度保持不变
C.(g)和(g)的体积比保持不变 D.每消耗1mol ,同时消耗0.5mol (g)
10.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是
A.反应在0~10s内,用Z表示的反应速率为0.158
B.反应在0~10s内,X的物质的量浓度减少了0.79
C.反应进行到10s时,Y的转化率为79.0%
D.反应的化学方程式为
11.下列物质的沸点由高到低排列的顺序是
① ② ③ ④
A.②④①③ B.④②①③ C.④②③① D.②④③①1
12.北京奥运会祥云火炬的主要燃料为丙烷,下列关于丙烷的说法正确的是
A.丙烷分子中3个碳原子在一条直线上 B.丙烷可以与溴水发生取代反应
C.丙烷在空气中燃烧只可能生成和 D.常温常压下,22g丙烷所含氢原子数为4
13.下列关于乙烯与聚乙烯的说法,正确的是
A.乙烯与聚乙烯都是纯净物
B.乙烯通过加成聚合反应得到聚乙烯,聚乙烯也可以通过降解得到乙烯
C.相同质量的乙烯与聚乙烯,完全燃烧所需要的氧气质量也相同
D.乙烯与聚乙烯,都能使酸性溶液褪色
14.化学是材料科学的基础,下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.制造特种防护服的芳纶纤维属于有机高分子材料
C.氧化铝熔点高,常用于制造耐高温材料
D.制造5G芯片的氮化铝属于无机非金属材料
二、非选择题:本题共5个小题,共53分。
15.(5分)
下列各组物质:①和 ②和 ③和
④和 ⑤癸烷和十六烷
⑥和
⑦和(在横线上填相应的序号)
(1)互为同位素的是 ;
(2)互为同分异构体的是 ;
(3)互为同素异形体的是 ;
(4)互为同系物的是 ;
(5)同一种物质的是 。
16.(15分)
(1)在某一容积为2L的密闭容器中,某一反应中A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化曲线如图所示:
回答下列问题:
①该反应的化学方程式为 。
②前2min用A的浓度变化表示的化学反应速率为 。在2min时,图像发生改变的原因是 (填字母)。
A.增大压强 B.降低温度 C.加入催化剂 D.增加A的物质的量
(2)在100℃时,将0.01mol的四氧化二氮气体充入0.1L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
时间/s 浓度/() 0 20 40 60 80 100
0.100 0.070 0.050 a b
0.000 0.060 0.120 0.120 0.120
试填空:
①该反应的化学方程式: ,达到平衡时四氧化二氮的转化率为 ,表中 ;a b。(填“>”“<”或“=”)
②在0~20s内,四氧化二氮的平均反应速率为 ,哪一时间段(指0~20、20~40、40~60、60~80、80~100s)反应速率最大? ,原因是
17.(10分)
二氯二氢硅()常用于外延法工艺中重要的硅源。该物质易燃、有毒,与水接触易水解,沸点为8.2℃。在铜催化作用下,HCl与硅在250~260℃反应可以制得。
(1)利用浓硫酸、浓盐酸为原料,选用A装置制取HCl,利用了浓硫酸的 性。
(2)D装置中生成二氯二氢硅的化学方程式为 。
(3)按照气体从左到右的方向,制取的装置(h处用止水夹夹好)连接顺序为a→( )→( )→( )→( )→( )→( )→( )(填仪器接口的字母,其中装置C用到2次)。
(4)按从左到右的顺序,前面装置C中装的药品为 ,后面装置C的作用为
。
(5)反应除生成二氯二氢硅之外,还会生成和 、 等。
18.(13分)
烷烃是一类有机化合物,分子中的碳原子都以碳碳单键相连,其余的价键都与氢结合而成的化合物,按要求回答下列与烷烃有关问题。
(1)上图均能表示甲烷的分子结构,对号入座(填字母):甲烷的球棍模型是 ,甲烷的电子式是 。
(2)有 种结构,证明甲烷不是平面结构,而是 结构。
(3)写出乙烷与氯气在光照条件下生成一氯乙烷的反应方程式 ,(2分)该反应的反应类型为 ;1mol乙烷与足量氯气在光照条件下充分反应,最多可生成HCl的物质的量 mol。(2分)
(4)已知戊烷有3种同分异构体,它们的结构简式分别为: ,(3分)上述同分异构体中,沸点最低的是 (写结构简式)。
19.(10分)
以作催化剂,可用乙烯脱除烟气中并回收单质硫。某兴趣小组同学设计实验验证该反应并检验产物中的,实验装置(夹持装置已略)如图所示:
已知:硫在20℃和50℃之间升华。
回答下列问题:
(1)装置a中的作用是 。(答出2点即可)
(2)装置b中有S、、生成,则发生反应的化学方程式为
。
(3)装置c用冷水水浴的目的是 。
(4)有同学认为可将溴水换成酸性高锰酸钾溶液,你认为是否可行,说明你的理由
。
(5)装置e中品红溶液的作用是 。
高一化学答案
一、选择题(1-9题每题3分10-14题每题4分)
1C 2D 3D 4C 5C 6C 7D 8B 9C 10C 11A 12D 13C 14A
二、非选择题
15.(5分,每空1分,每空全写对才得1分)
(1)互为同位素的是③;
(2)互为同分异构体的是④⑥;
(3)互为同素异形体的是①;
(4)互为同系物的是⑤
(5)同一种物质的是②⑦。
16.(15分)
(1)①(2分,连接符号写错扣1分,系数有错全错)
②0.1(2分,单位错0分) AC(1分,都对才有分)
(2)①(2分,连接符号写错扣1分) 60% > =
②0.0015(2分,单位错0分) 0~20s 开始时反应物的浓度最大
17.(10分)
(1)吸水
(2)(2分,条件占1分)
(3)d e f g b c d(2分,全对得2分,否则0分)
(4)或无水 尾气处理和防止空气中的水蒸气进入B中(2分,不全扣1分)
(5)
18.(13分,除标注外每空1分)
(1)C;B
(2)1;正四面体
(3)(2分,条件连接符号占1分);取代反应;6
(4)、、(3分,各1分);
19.(10分,每空2分)
(1)调控气流速度、使和乙烯混合均匀、干燥气体(没写全扣1分)
(2)(条件连接符号占1分)
(3)冷凝S蒸汽,收集S
(4)乙烯能被酸性溶液氧化成,对后面检验产物中的有干扰
(5)检验是否除尽
同课章节目录
