2025广东版新教材化学高考第一轮基础练习--专题二 物质的量(含答案)
文档属性
| 名称 | 2025广东版新教材化学高考第一轮基础练习--专题二 物质的量(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 445.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-26 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
2025广东版新教材化学高考第一轮
专题二 物质的量
五年高考
考点过关练
考点1 物质的量和气体摩尔体积
1.(2022广东,9,2分)我国科学家进行了如图所示的碳循环研究。下列说法正确的是( )
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C.1 mol CO中含有6.02×1024个电子
D.22.4 L CO2被还原生成1 mol CO
2.(2023全国甲,10,6分)NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.0.50 mol异丁烷分子中共价键的数目为6.5NA
B.标准状况下,2.24 L SO3中电子的数目为4.00NA
C.1.0 L pH=2的H2SO4溶液中H+的数目为0.02NA
D.1.0 L 1.0 mol·L-1的Na2CO3溶液中C的数目为1.0NA
3.(2023海南,6,2分)NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.2.4 g镁条在空气中充分燃烧,转移的电子数目为0.2NA
B.5.6 g铁粉与0.1 L 1 mol·L-1 HCl溶液充分反应,产生的气体分子数目为0.1NA
C.标准状况下,2.24 L SO2与1.12 L O2充分反应,生成的SO3分子数目为0.1NA
D.1.7 g NH3完全溶于1 L H2O所得溶液中,NH3·H2O数目为0.1NA
4.(2022海南,7,2分)在2.8 g Fe中加入100 mL 3 mol·L-1 HCl溶液,Fe完全溶解。NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.反应转移电子为0.1 mol
B.HCl溶液中Cl-数为3NA
C.2.8 g 56Fe含有的中子数为1.3NA
D.反应生成标准状况下气体3.36 L
5.(2021广东,11,4分)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 mol CHCl3含有C—Cl键的数目为3NA
B.1 L 1.0 mol/L的盐酸含有阴离子总数为2NA
C.11.2 L NO与11.2 L O2混合后的分子数目为NA
D.23 g Na与足量H2O反应生成的H2分子数目为NA
6.(2022浙江6月选考,12,2分)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.12 g NaHSO4中含有0.2NA个阳离子
B.11.2 L乙烷和丙烯的混合气体中所含碳氢键数为3NA
C.8 g CH4含有中子数为3NA
D.0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,HI分子总数为0.2NA
7.(2022辽宁,3,3分)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1.8 g 18O中含有的中子数为NA
B.28 g C2H4分子中含有的σ键数目为4NA
C.标准状况下,22.4 L HCl气体中H+数目为NA
D.pH=12的Na2CO3溶液中OH-数目为0.01NA
考点2 物质的量浓度
8.(2021广东,7,2分)测定浓硫酸试剂中H2SO4含量的主要操作包括:①量取一定量的浓硫酸,稀释;②转移定容得待测液;③移取20.00 mL待测液,用0.100 0 mol/L的NaOH溶液滴定。上述操作中,不需要用到的仪器为 ( )
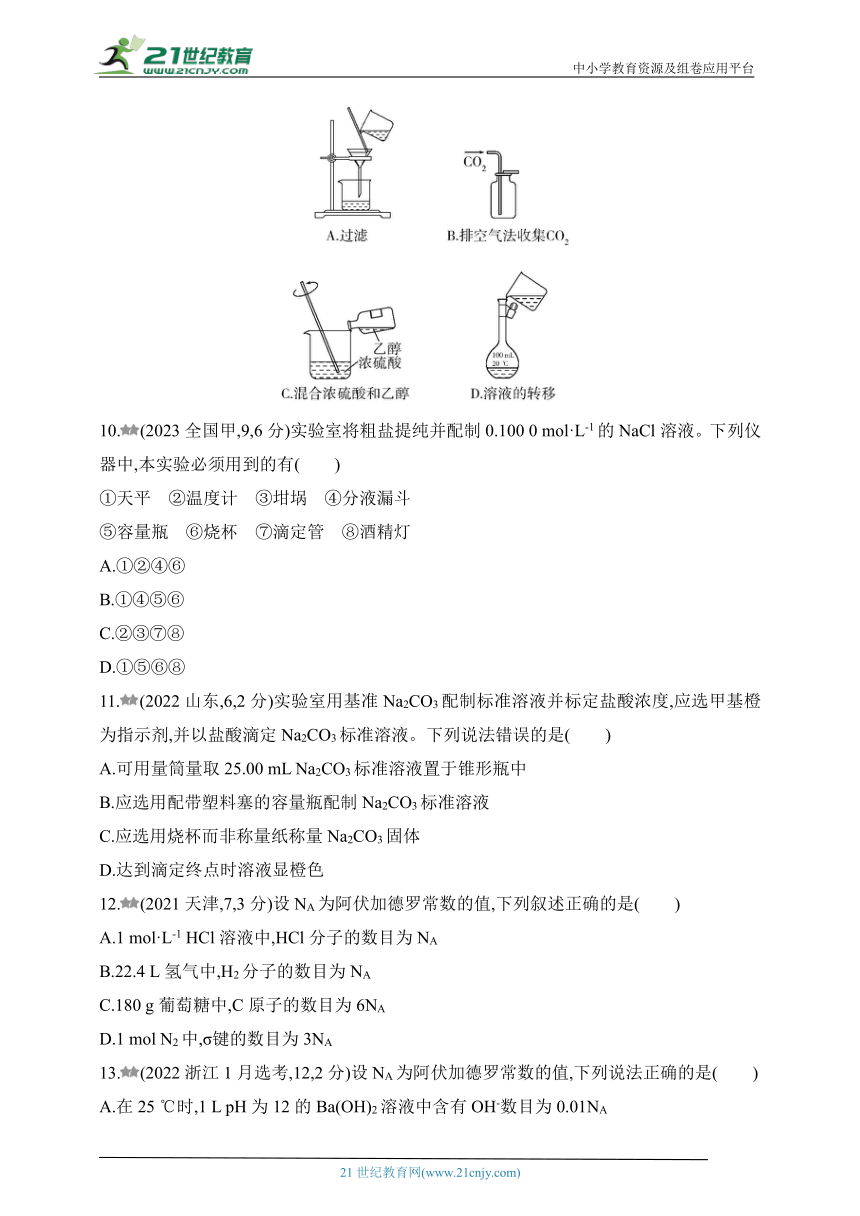
9.(2022海南,3,2分)下列实验操作规范的是( )
10.(2023全国甲,9,6分)实验室将粗盐提纯并配制0.100 0 mol·L-1的NaCl溶液。下列仪器中,本实验必须用到的有( )
①天平 ②温度计 ③坩埚 ④分液漏斗
⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥
B.①④⑤⑥
C.②③⑦⑧
D.①⑤⑥⑧
11.(2022山东,6,2分)实验室用基准Na2CO3配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定Na2CO3标准溶液。下列说法错误的是( )
A.可用量筒量取25.00 mL Na2CO3标准溶液置于锥形瓶中
B.应选用配带塑料塞的容量瓶配制Na2CO3标准溶液
C.应选用烧杯而非称量纸称量Na2CO3固体
D.达到滴定终点时溶液显橙色
12.(2021天津,7,3分)设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.1 mol·L-1 HCl溶液中,HCl分子的数目为NA
B.22.4 L氢气中,H2分子的数目为NA
C.180 g葡萄糖中,C原子的数目为6NA
D.1 mol N2中,σ键的数目为3NA
13.(2022浙江1月选考,12,2分)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.在25 ℃时,1 L pH为12的Ba(OH)2溶液中含有OH-数目为0.01NA
B.1.8 g重水(D2O)中所含质子数为NA
C.足量的浓盐酸与8.7 g MnO2反应,转移电子的数目为0.4NA
D.32 g甲醇的分子中含有C—H键的数目为4NA
考法强化练
考法 阿伏加德罗常数的应用
1.(2023辽宁,5,3分)我国古代四大发明之一黑火药的爆炸反应为S+2KNO3+3C K2S+N2↑+3CO2↑。设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.11.2 L CO2含π键数目为NA
B.每生成2.8 g N2转移电子数目为NA
C.0.1 mol KNO3晶体中含离子数目为0.2NA
D.1 L 0.1 mol·L-1 K2S溶液中含S2-数目为0.1NA
2.(2022重庆,5,3分)工业上用N2和H2合成NH3 。NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.消耗14 g N2生成NH3分子数为2NA
B.消耗1 mol H2生成N—H键数为2NA
C.生成标准状况下22.4 L NH3,电子转移数为2NA
D.氧化1 mol NH3生成NO,需O2分子数为2NA
3.(2022河北,4,3分)NA是阿伏加德罗常数的值。下列说法正确的是( )
A.3.9 g Na2O2与足量水反应,转移电子个数为0.1NA
B.1.2 g Mg在空气中燃烧生成MgO和Mg3N2,转移电子个数为0.1NA
C.2.7 g Al与足量NaOH溶液反应,生成H2的个数为0.1NA
D.6.0 g SiO2与足量NaOH溶液反应,所得溶液中Si的个数为0.1NA
4.(2021河北,7,3分)NA是阿伏加德罗常数的值。下列说法错误的是( )
A.22.4 L(标准状况)氟气所含的质子数为18NA
B.1 mol碘蒸气和1 mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73 g,则转移电子数为NA
D.1 L 1 mol·L-1溴化铵水溶液中N与H+离子数之和大于NA
5.(2023浙江6月选考,7,3分)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.4.4 g C2H4O中含有σ键数目最多为0.7NA
B.1.7 g H2O2中含有氧原子数为0.2NA
C.向1 L 0.1 mol·L-1 CH3COOH溶液通氨气至中性,铵根离子数为0.1NA
D.标准状况下,11.2 L Cl2通入水中,溶液中氯离子数为0.5NA
6.(2023广东,11,4分)设NA为阿伏加德罗常数的值。侯氏制碱法涉及NaCl、NH4Cl和NaHCO3等物质。下列叙述正确的是( )
A.1 mol NH4Cl含有的共价键数目为5NA
B.1 mol NaHCO3完全分解,得到的CO2分子数目为2NA
C.体积为1 L的1 mol·L-1 NaHCO3溶液中,HC数目为NA
D.NaCl和NH4Cl的混合物中含1 mol Cl-,则混合物中质子数为28NA
7.(2022福建,3,4分)常温常压下,电化学还原制氨气的总反应方程式如下:
2N2+6H2O 4NH3+3O2
设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.9 g水中含有的孤电子对数为2NA
B.每产生34 g NH3,N2失去的电子数为6NA
C.1 mol·L-1氨水中,含有的NH3·H2O分子数少于NA
D.消耗11.2 L N2(已折算为标准状况)时,产生的O2分子数为0.75NA
三年模拟
考点强化练
考点1 物质的量和气体摩尔体积
1.(2024届执信中学10月月考,5)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.78 g Na2O2与足量水完全反应,转移电子数为2NA
B.1 L 0.1 mol·L-1的Na2CO3溶液含C的数目为0.1NA
C.1 mol 分子中所含σ键数为3NA
D.标准状况下,2.24 L CCl4所含氯原子数为0.4NA
2.(2024届广州阶段训练,13)氮化硅(Si3N4)常用作飞船返回舱耐高温结构材料,可由石英和焦炭在高温的氮气中通过以下反应制备:3SiO2+6C+2N2 Si3N4+6CO。下列说法不正确的是( )
A.Si3N4中氮元素的化合价为-3
B.该反应中氮气为氧化剂
C.1 mol CO中含有6.02×1024个电子
D.每消耗标准状况下11.2 L的N2,最多生成0.25 mol Si3N4
3.(2024届广东四校联考9月月考,11)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.一定条件下,1 mol N2与3 mol H2充分反应,生成NH3的分子数为2NA
B.18 g CH2D2含有的中子数为10NA
C.1 mol白磷(P4)中所含共价键数目为6NA
D.常温常压下,46 g NO2中所含的分子数为NA
4.(2023珠海一中二模,9)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,11.2 L HF所含的原子总数为NA
B.用惰性电极电解CuSO4溶液,当阳极产生22.4 L气体时,转移的电子数为4NA
C.2 L 0.1 mol·L-1 Na2SiO3溶液中含的数目为0.2NA
D.向1 L 0.5 mol·L-1盐酸中通入NH3至中性(忽略溶液体积变化),此时N个数为0.5NA
考点2 物质的量浓度
5.(2024届华南师大附中第一次月考,4)实验室为配制0.10 mol·L-1的稀硫酸,不需要用到的仪器是( )
6.(2024届清中、河中、北中、惠中、阳中、茂中6校第一次联考,11)设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A.28 g由乙烯和环丁烷组成的混合气体中含有的原子数为6NA
B.常温下,5.4 g铝片投入足量的浓硫酸中,铝失去的电子数为0.6NA
C.1 L 0.1 mol·L-1 K2CO3溶液中含有 C的数目为0.1NA
D.室温下pH=11的NaClO溶液中,由水电离出的OH-数目为0.001NA
7.(2024届惠州一调,6)反应NH4Cl+NaNO2 NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。设NA为阿伏加德罗常数的值。下列说法不正确的是( )
A.0.1 mol N2中含有π键数目为0.2NA
B.18 g H2O中所含电子数目为10NA
C.常温时,pH=8的NaNO2溶液中所含OH-的数目为10-6NA
D.上述反应中,每生成0.1 mol N2转移的电子数目为0.3NA
考法综合练
考法 阿伏加德罗常数的应用
1.(2023广东四校联考,10)用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2 L甲烷含氢原子数目为2NA
B.1 L 0.1 mol·L-1NH4Cl溶液中阳离子的总数小于0.1NA
C.1 mol Na2O2与足量的SO2反应转移电子数为NA
D.1 mol SiO2含有的共价键数目为2NA
2.(2023广州二模,7)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.1 mol SiHCl3含有Si—Cl键的数目为3NA
B.24 g Mg与稀硫酸完全反应,转移的电子数目为NA
C.1 L 1.0 mol·L-1NaHSO4溶液含有阴离子的总数为2NA
D.11.2 L NO与11.2 L O2混合后分子的数目为NA
3.(2023梅州质检二,12)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.0.1 mol 27Al3+中含有的电子数为1.3NA
B.100 mL 1 mol·L-1 Na2S溶液中含有的阴离子数目小于0.1NA
C.标准状况下,22.4 L乙炔中含有的σ键数目为5NA
D.23 g Na与足量的氧气反应转移电子数目为NA
4.(2023广东二模,7)铜可以溶解在氨水和过氧化氢的混合溶液中,反应的离子方程式为Cu+H2O2+4NH3·H2O [Cu(NH3)4]2++2OH-+4H2O。设NA为阿伏加德罗常数的值,下列有关说法不正确的是( )
A.1 mol基态铜原子的最外层电子数为NA
B.每生成18 g H2O转移的电子数为0.5NA
C.标准状况下,22.4 L NH3溶于水,所得溶液中NH3·H2O分子数小于NA
D.100 mL 1 mol·L-1的过氧化氢溶液中含有的氧原子数为0.2NA
5.(2023广州天河综合测试二,11)设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,11.2 L Cl2溶于水生成Cl-的数目为0.5NA
B.25 ℃时,1 L pH=8的CH3COONa溶液中水电离出的OH-数目为10-8NA
C.等物质的量的Al分别与足量盐酸和NaOH溶液反应,转移的电子数均为3NA
D.常温常压下,3.4 g羟基(—OH)所含的电子数目为1.8NA
6.(2023佛山质检二,8)绿矾(FeSO4·7H2O)分解可制备铁红,同时产生SO2、SO3和H2O。设NA为阿伏加德罗常数的值,下列说法错误的是( )
A.1 L 1 mol·L-1FeSO4溶液含有的阳离子数大于NA
B.0.5 mol三聚SO3分子()中含有σ键数目为6NA
C.绿矾分解生成16 g Fe2O3时,转移电子数为0.2NA
D.22.4 L SO2溶于水,溶液中H2SO3、的数目总和为NA
7.(2023湖南师大附中二模,6)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4 L CHCl3所含的分子数为NA
B.向FeBr2溶液中通入适量氯气,当有1 mol Br2生成时,共转移的电子数可能为4NA
C.标准状况下,11.2 L NH3溶于水形成的溶液中、NH3·H2O的微粒数之和为0.5NA
D.3.2 g Cu与S完全反应,转移的电子数为0.1NA
专题二 物质的量
五年高考
考点过关练
考点1 物质的量和气体摩尔体积
1.(2022广东,9,2分)我国科学家进行了如图所示的碳循环研究。下列说法正确的是( )
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C.1 mol CO中含有6.02×1024个电子
D.22.4 L CO2被还原生成1 mol CO
答案 A
2.(2023全国甲,10,6分)NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.0.50 mol异丁烷分子中共价键的数目为6.5NA
B.标准状况下,2.24 L SO3中电子的数目为4.00NA
C.1.0 L pH=2的H2SO4溶液中H+的数目为0.02NA
D.1.0 L 1.0 mol·L-1的Na2CO3溶液中C的数目为1.0NA
答案 A
3.(2023海南,6,2分)NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.2.4 g镁条在空气中充分燃烧,转移的电子数目为0.2NA
B.5.6 g铁粉与0.1 L 1 mol·L-1 HCl溶液充分反应,产生的气体分子数目为0.1NA
C.标准状况下,2.24 L SO2与1.12 L O2充分反应,生成的SO3分子数目为0.1NA
D.1.7 g NH3完全溶于1 L H2O所得溶液中,NH3·H2O数目为0.1NA
答案 A
4.(2022海南,7,2分)在2.8 g Fe中加入100 mL 3 mol·L-1 HCl溶液,Fe完全溶解。NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.反应转移电子为0.1 mol
B.HCl溶液中Cl-数为3NA
C.2.8 g 56Fe含有的中子数为1.3NA
D.反应生成标准状况下气体3.36 L
答案 A
5.(2021广东,11,4分)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 mol CHCl3含有C—Cl键的数目为3NA
B.1 L 1.0 mol/L的盐酸含有阴离子总数为2NA
C.11.2 L NO与11.2 L O2混合后的分子数目为NA
D.23 g Na与足量H2O反应生成的H2分子数目为NA
答案 A
6.(2022浙江6月选考,12,2分)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.12 g NaHSO4中含有0.2NA个阳离子
B.11.2 L乙烷和丙烯的混合气体中所含碳氢键数为3NA
C.8 g CH4含有中子数为3NA
D.0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,HI分子总数为0.2NA
答案 C
7.(2022辽宁,3,3分)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1.8 g 18O中含有的中子数为NA
B.28 g C2H4分子中含有的σ键数目为4NA
C.标准状况下,22.4 L HCl气体中H+数目为NA
D.pH=12的Na2CO3溶液中OH-数目为0.01NA
答案 A
考点2 物质的量浓度
8.(2021广东,7,2分)测定浓硫酸试剂中H2SO4含量的主要操作包括:①量取一定量的浓硫酸,稀释;②转移定容得待测液;③移取20.00 mL待测液,用0.100 0 mol/L的NaOH溶液滴定。上述操作中,不需要用到的仪器为 ( )
答案 B
9.(2022海南,3,2分)下列实验操作规范的是( )
答案 B
10.(2023全国甲,9,6分)实验室将粗盐提纯并配制0.100 0 mol·L-1的NaCl溶液。下列仪器中,本实验必须用到的有( )
①天平 ②温度计 ③坩埚 ④分液漏斗
⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥
B.①④⑤⑥
C.②③⑦⑧
D.①⑤⑥⑧
答案 D
11.(2022山东,6,2分)实验室用基准Na2CO3配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定Na2CO3标准溶液。下列说法错误的是( )
A.可用量筒量取25.00 mL Na2CO3标准溶液置于锥形瓶中
B.应选用配带塑料塞的容量瓶配制Na2CO3标准溶液
C.应选用烧杯而非称量纸称量Na2CO3固体
D.达到滴定终点时溶液显橙色
答案 A
12.(2021天津,7,3分)设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.1 mol·L-1 HCl溶液中,HCl分子的数目为NA
B.22.4 L氢气中,H2分子的数目为NA
C.180 g葡萄糖中,C原子的数目为6NA
D.1 mol N2中,σ键的数目为3NA
答案 C
13.(2022浙江1月选考,12,2分)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.在25 ℃时,1 L pH为12的Ba(OH)2溶液中含有OH-数目为0.01NA
B.1.8 g重水(D2O)中所含质子数为NA
C.足量的浓盐酸与8.7 g MnO2反应,转移电子的数目为0.4NA
D.32 g甲醇的分子中含有C—H键的数目为4NA
答案 A
考法强化练
考法 阿伏加德罗常数的应用
1.(2023辽宁,5,3分)我国古代四大发明之一黑火药的爆炸反应为S+2KNO3+3C K2S+N2↑+3CO2↑。设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.11.2 L CO2含π键数目为NA
B.每生成2.8 g N2转移电子数目为NA
C.0.1 mol KNO3晶体中含离子数目为0.2NA
D.1 L 0.1 mol·L-1 K2S溶液中含S2-数目为0.1NA
答案 C
2.(2022重庆,5,3分)工业上用N2和H2合成NH3 。NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.消耗14 g N2生成NH3分子数为2NA
B.消耗1 mol H2生成N—H键数为2NA
C.生成标准状况下22.4 L NH3,电子转移数为2NA
D.氧化1 mol NH3生成NO,需O2分子数为2NA
答案 B
3.(2022河北,4,3分)NA是阿伏加德罗常数的值。下列说法正确的是( )
A.3.9 g Na2O2与足量水反应,转移电子个数为0.1NA
B.1.2 g Mg在空气中燃烧生成MgO和Mg3N2,转移电子个数为0.1NA
C.2.7 g Al与足量NaOH溶液反应,生成H2的个数为0.1NA
D.6.0 g SiO2与足量NaOH溶液反应,所得溶液中Si的个数为0.1NA
答案 B
4.(2021河北,7,3分)NA是阿伏加德罗常数的值。下列说法错误的是( )
A.22.4 L(标准状况)氟气所含的质子数为18NA
B.1 mol碘蒸气和1 mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73 g,则转移电子数为NA
D.1 L 1 mol·L-1溴化铵水溶液中N与H+离子数之和大于NA
答案 C
5.(2023浙江6月选考,7,3分)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.4.4 g C2H4O中含有σ键数目最多为0.7NA
B.1.7 g H2O2中含有氧原子数为0.2NA
C.向1 L 0.1 mol·L-1 CH3COOH溶液通氨气至中性,铵根离子数为0.1NA
D.标准状况下,11.2 L Cl2通入水中,溶液中氯离子数为0.5NA
答案 A
6.(2023广东,11,4分)设NA为阿伏加德罗常数的值。侯氏制碱法涉及NaCl、NH4Cl和NaHCO3等物质。下列叙述正确的是( )
A.1 mol NH4Cl含有的共价键数目为5NA
B.1 mol NaHCO3完全分解,得到的CO2分子数目为2NA
C.体积为1 L的1 mol·L-1 NaHCO3溶液中,HC数目为NA
D.NaCl和NH4Cl的混合物中含1 mol Cl-,则混合物中质子数为28NA
答案 D
7.(2022福建,3,4分)常温常压下,电化学还原制氨气的总反应方程式如下:
2N2+6H2O 4NH3+3O2
设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.9 g水中含有的孤电子对数为2NA
B.每产生34 g NH3,N2失去的电子数为6NA
C.1 mol·L-1氨水中,含有的NH3·H2O分子数少于NA
D.消耗11.2 L N2(已折算为标准状况)时,产生的O2分子数为0.75NA
答案 D
三年模拟
考点强化练
考点1 物质的量和气体摩尔体积
1.(2024届执信中学10月月考,5)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.78 g Na2O2与足量水完全反应,转移电子数为2NA
B.1 L 0.1 mol·L-1的Na2CO3溶液含C的数目为0.1NA
C.1 mol 分子中所含σ键数为3NA
D.标准状况下,2.24 L CCl4所含氯原子数为0.4NA
答案 C
2.(2024届广州阶段训练,13)氮化硅(Si3N4)常用作飞船返回舱耐高温结构材料,可由石英和焦炭在高温的氮气中通过以下反应制备:3SiO2+6C+2N2 Si3N4+6CO。下列说法不正确的是( )
A.Si3N4中氮元素的化合价为-3
B.该反应中氮气为氧化剂
C.1 mol CO中含有6.02×1024个电子
D.每消耗标准状况下11.2 L的N2,最多生成0.25 mol Si3N4
答案 C
3.(2024届广东四校联考9月月考,11)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.一定条件下,1 mol N2与3 mol H2充分反应,生成NH3的分子数为2NA
B.18 g CH2D2含有的中子数为10NA
C.1 mol白磷(P4)中所含共价键数目为6NA
D.常温常压下,46 g NO2中所含的分子数为NA
答案 C
4.(2023珠海一中二模,9)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,11.2 L HF所含的原子总数为NA
B.用惰性电极电解CuSO4溶液,当阳极产生22.4 L气体时,转移的电子数为4NA
C.2 L 0.1 mol·L-1 Na2SiO3溶液中含的数目为0.2NA
D.向1 L 0.5 mol·L-1盐酸中通入NH3至中性(忽略溶液体积变化),此时N个数为0.5NA
答案 D
考点2 物质的量浓度
5.(2024届华南师大附中第一次月考,4)实验室为配制0.10 mol·L-1的稀硫酸,不需要用到的仪器是( )
答案 B
6.(2024届清中、河中、北中、惠中、阳中、茂中6校第一次联考,11)设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A.28 g由乙烯和环丁烷组成的混合气体中含有的原子数为6NA
B.常温下,5.4 g铝片投入足量的浓硫酸中,铝失去的电子数为0.6NA
C.1 L 0.1 mol·L-1 K2CO3溶液中含有 C的数目为0.1NA
D.室温下pH=11的NaClO溶液中,由水电离出的OH-数目为0.001NA
答案 A
7.(2024届惠州一调,6)反应NH4Cl+NaNO2 NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。设NA为阿伏加德罗常数的值。下列说法不正确的是( )
A.0.1 mol N2中含有π键数目为0.2NA
B.18 g H2O中所含电子数目为10NA
C.常温时,pH=8的NaNO2溶液中所含OH-的数目为10-6NA
D.上述反应中,每生成0.1 mol N2转移的电子数目为0.3NA
答案 C
考法综合练
考法 阿伏加德罗常数的应用
1.(2023广东四校联考,10)用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2 L甲烷含氢原子数目为2NA
B.1 L 0.1 mol·L-1NH4Cl溶液中阳离子的总数小于0.1NA
C.1 mol Na2O2与足量的SO2反应转移电子数为NA
D.1 mol SiO2含有的共价键数目为2NA
答案 A
2.(2023广州二模,7)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.1 mol SiHCl3含有Si—Cl键的数目为3NA
B.24 g Mg与稀硫酸完全反应,转移的电子数目为NA
C.1 L 1.0 mol·L-1NaHSO4溶液含有阴离子的总数为2NA
D.11.2 L NO与11.2 L O2混合后分子的数目为NA
答案 A
3.(2023梅州质检二,12)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.0.1 mol 27Al3+中含有的电子数为1.3NA
B.100 mL 1 mol·L-1 Na2S溶液中含有的阴离子数目小于0.1NA
C.标准状况下,22.4 L乙炔中含有的σ键数目为5NA
D.23 g Na与足量的氧气反应转移电子数目为NA
答案 D
4.(2023广东二模,7)铜可以溶解在氨水和过氧化氢的混合溶液中,反应的离子方程式为Cu+H2O2+4NH3·H2O [Cu(NH3)4]2++2OH-+4H2O。设NA为阿伏加德罗常数的值,下列有关说法不正确的是( )
A.1 mol基态铜原子的最外层电子数为NA
B.每生成18 g H2O转移的电子数为0.5NA
C.标准状况下,22.4 L NH3溶于水,所得溶液中NH3·H2O分子数小于NA
D.100 mL 1 mol·L-1的过氧化氢溶液中含有的氧原子数为0.2NA
答案 D
5.(2023广州天河综合测试二,11)设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,11.2 L Cl2溶于水生成Cl-的数目为0.5NA
B.25 ℃时,1 L pH=8的CH3COONa溶液中水电离出的OH-数目为10-8NA
C.等物质的量的Al分别与足量盐酸和NaOH溶液反应,转移的电子数均为3NA
D.常温常压下,3.4 g羟基(—OH)所含的电子数目为1.8NA
答案 D
6.(2023佛山质检二,8)绿矾(FeSO4·7H2O)分解可制备铁红,同时产生SO2、SO3和H2O。设NA为阿伏加德罗常数的值,下列说法错误的是( )
A.1 L 1 mol·L-1FeSO4溶液含有的阳离子数大于NA
B.0.5 mol三聚SO3分子()中含有σ键数目为6NA
C.绿矾分解生成16 g Fe2O3时,转移电子数为0.2NA
D.22.4 L SO2溶于水,溶液中H2SO3、的数目总和为NA
答案 D
7.(2023湖南师大附中二模,6)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4 L CHCl3所含的分子数为NA
B.向FeBr2溶液中通入适量氯气,当有1 mol Br2生成时,共转移的电子数可能为4NA
C.标准状况下,11.2 L NH3溶于水形成的溶液中、NH3·H2O的微粒数之和为0.5NA
D.3.2 g Cu与S完全反应,转移的电子数为0.1NA
答案 B
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025广东版新教材化学高考第一轮
专题二 物质的量
五年高考
考点过关练
考点1 物质的量和气体摩尔体积
1.(2022广东,9,2分)我国科学家进行了如图所示的碳循环研究。下列说法正确的是( )
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C.1 mol CO中含有6.02×1024个电子
D.22.4 L CO2被还原生成1 mol CO
2.(2023全国甲,10,6分)NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.0.50 mol异丁烷分子中共价键的数目为6.5NA
B.标准状况下,2.24 L SO3中电子的数目为4.00NA
C.1.0 L pH=2的H2SO4溶液中H+的数目为0.02NA
D.1.0 L 1.0 mol·L-1的Na2CO3溶液中C的数目为1.0NA
3.(2023海南,6,2分)NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.2.4 g镁条在空气中充分燃烧,转移的电子数目为0.2NA
B.5.6 g铁粉与0.1 L 1 mol·L-1 HCl溶液充分反应,产生的气体分子数目为0.1NA
C.标准状况下,2.24 L SO2与1.12 L O2充分反应,生成的SO3分子数目为0.1NA
D.1.7 g NH3完全溶于1 L H2O所得溶液中,NH3·H2O数目为0.1NA
4.(2022海南,7,2分)在2.8 g Fe中加入100 mL 3 mol·L-1 HCl溶液,Fe完全溶解。NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.反应转移电子为0.1 mol
B.HCl溶液中Cl-数为3NA
C.2.8 g 56Fe含有的中子数为1.3NA
D.反应生成标准状况下气体3.36 L
5.(2021广东,11,4分)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 mol CHCl3含有C—Cl键的数目为3NA
B.1 L 1.0 mol/L的盐酸含有阴离子总数为2NA
C.11.2 L NO与11.2 L O2混合后的分子数目为NA
D.23 g Na与足量H2O反应生成的H2分子数目为NA
6.(2022浙江6月选考,12,2分)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.12 g NaHSO4中含有0.2NA个阳离子
B.11.2 L乙烷和丙烯的混合气体中所含碳氢键数为3NA
C.8 g CH4含有中子数为3NA
D.0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,HI分子总数为0.2NA
7.(2022辽宁,3,3分)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1.8 g 18O中含有的中子数为NA
B.28 g C2H4分子中含有的σ键数目为4NA
C.标准状况下,22.4 L HCl气体中H+数目为NA
D.pH=12的Na2CO3溶液中OH-数目为0.01NA
考点2 物质的量浓度
8.(2021广东,7,2分)测定浓硫酸试剂中H2SO4含量的主要操作包括:①量取一定量的浓硫酸,稀释;②转移定容得待测液;③移取20.00 mL待测液,用0.100 0 mol/L的NaOH溶液滴定。上述操作中,不需要用到的仪器为 ( )
9.(2022海南,3,2分)下列实验操作规范的是( )
10.(2023全国甲,9,6分)实验室将粗盐提纯并配制0.100 0 mol·L-1的NaCl溶液。下列仪器中,本实验必须用到的有( )
①天平 ②温度计 ③坩埚 ④分液漏斗
⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥
B.①④⑤⑥
C.②③⑦⑧
D.①⑤⑥⑧
11.(2022山东,6,2分)实验室用基准Na2CO3配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定Na2CO3标准溶液。下列说法错误的是( )
A.可用量筒量取25.00 mL Na2CO3标准溶液置于锥形瓶中
B.应选用配带塑料塞的容量瓶配制Na2CO3标准溶液
C.应选用烧杯而非称量纸称量Na2CO3固体
D.达到滴定终点时溶液显橙色
12.(2021天津,7,3分)设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.1 mol·L-1 HCl溶液中,HCl分子的数目为NA
B.22.4 L氢气中,H2分子的数目为NA
C.180 g葡萄糖中,C原子的数目为6NA
D.1 mol N2中,σ键的数目为3NA
13.(2022浙江1月选考,12,2分)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.在25 ℃时,1 L pH为12的Ba(OH)2溶液中含有OH-数目为0.01NA
B.1.8 g重水(D2O)中所含质子数为NA
C.足量的浓盐酸与8.7 g MnO2反应,转移电子的数目为0.4NA
D.32 g甲醇的分子中含有C—H键的数目为4NA
考法强化练
考法 阿伏加德罗常数的应用
1.(2023辽宁,5,3分)我国古代四大发明之一黑火药的爆炸反应为S+2KNO3+3C K2S+N2↑+3CO2↑。设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.11.2 L CO2含π键数目为NA
B.每生成2.8 g N2转移电子数目为NA
C.0.1 mol KNO3晶体中含离子数目为0.2NA
D.1 L 0.1 mol·L-1 K2S溶液中含S2-数目为0.1NA
2.(2022重庆,5,3分)工业上用N2和H2合成NH3 。NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.消耗14 g N2生成NH3分子数为2NA
B.消耗1 mol H2生成N—H键数为2NA
C.生成标准状况下22.4 L NH3,电子转移数为2NA
D.氧化1 mol NH3生成NO,需O2分子数为2NA
3.(2022河北,4,3分)NA是阿伏加德罗常数的值。下列说法正确的是( )
A.3.9 g Na2O2与足量水反应,转移电子个数为0.1NA
B.1.2 g Mg在空气中燃烧生成MgO和Mg3N2,转移电子个数为0.1NA
C.2.7 g Al与足量NaOH溶液反应,生成H2的个数为0.1NA
D.6.0 g SiO2与足量NaOH溶液反应,所得溶液中Si的个数为0.1NA
4.(2021河北,7,3分)NA是阿伏加德罗常数的值。下列说法错误的是( )
A.22.4 L(标准状况)氟气所含的质子数为18NA
B.1 mol碘蒸气和1 mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73 g,则转移电子数为NA
D.1 L 1 mol·L-1溴化铵水溶液中N与H+离子数之和大于NA
5.(2023浙江6月选考,7,3分)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.4.4 g C2H4O中含有σ键数目最多为0.7NA
B.1.7 g H2O2中含有氧原子数为0.2NA
C.向1 L 0.1 mol·L-1 CH3COOH溶液通氨气至中性,铵根离子数为0.1NA
D.标准状况下,11.2 L Cl2通入水中,溶液中氯离子数为0.5NA
6.(2023广东,11,4分)设NA为阿伏加德罗常数的值。侯氏制碱法涉及NaCl、NH4Cl和NaHCO3等物质。下列叙述正确的是( )
A.1 mol NH4Cl含有的共价键数目为5NA
B.1 mol NaHCO3完全分解,得到的CO2分子数目为2NA
C.体积为1 L的1 mol·L-1 NaHCO3溶液中,HC数目为NA
D.NaCl和NH4Cl的混合物中含1 mol Cl-,则混合物中质子数为28NA
7.(2022福建,3,4分)常温常压下,电化学还原制氨气的总反应方程式如下:
2N2+6H2O 4NH3+3O2
设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.9 g水中含有的孤电子对数为2NA
B.每产生34 g NH3,N2失去的电子数为6NA
C.1 mol·L-1氨水中,含有的NH3·H2O分子数少于NA
D.消耗11.2 L N2(已折算为标准状况)时,产生的O2分子数为0.75NA
三年模拟
考点强化练
考点1 物质的量和气体摩尔体积
1.(2024届执信中学10月月考,5)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.78 g Na2O2与足量水完全反应,转移电子数为2NA
B.1 L 0.1 mol·L-1的Na2CO3溶液含C的数目为0.1NA
C.1 mol 分子中所含σ键数为3NA
D.标准状况下,2.24 L CCl4所含氯原子数为0.4NA
2.(2024届广州阶段训练,13)氮化硅(Si3N4)常用作飞船返回舱耐高温结构材料,可由石英和焦炭在高温的氮气中通过以下反应制备:3SiO2+6C+2N2 Si3N4+6CO。下列说法不正确的是( )
A.Si3N4中氮元素的化合价为-3
B.该反应中氮气为氧化剂
C.1 mol CO中含有6.02×1024个电子
D.每消耗标准状况下11.2 L的N2,最多生成0.25 mol Si3N4
3.(2024届广东四校联考9月月考,11)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.一定条件下,1 mol N2与3 mol H2充分反应,生成NH3的分子数为2NA
B.18 g CH2D2含有的中子数为10NA
C.1 mol白磷(P4)中所含共价键数目为6NA
D.常温常压下,46 g NO2中所含的分子数为NA
4.(2023珠海一中二模,9)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,11.2 L HF所含的原子总数为NA
B.用惰性电极电解CuSO4溶液,当阳极产生22.4 L气体时,转移的电子数为4NA
C.2 L 0.1 mol·L-1 Na2SiO3溶液中含的数目为0.2NA
D.向1 L 0.5 mol·L-1盐酸中通入NH3至中性(忽略溶液体积变化),此时N个数为0.5NA
考点2 物质的量浓度
5.(2024届华南师大附中第一次月考,4)实验室为配制0.10 mol·L-1的稀硫酸,不需要用到的仪器是( )
6.(2024届清中、河中、北中、惠中、阳中、茂中6校第一次联考,11)设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A.28 g由乙烯和环丁烷组成的混合气体中含有的原子数为6NA
B.常温下,5.4 g铝片投入足量的浓硫酸中,铝失去的电子数为0.6NA
C.1 L 0.1 mol·L-1 K2CO3溶液中含有 C的数目为0.1NA
D.室温下pH=11的NaClO溶液中,由水电离出的OH-数目为0.001NA
7.(2024届惠州一调,6)反应NH4Cl+NaNO2 NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。设NA为阿伏加德罗常数的值。下列说法不正确的是( )
A.0.1 mol N2中含有π键数目为0.2NA
B.18 g H2O中所含电子数目为10NA
C.常温时,pH=8的NaNO2溶液中所含OH-的数目为10-6NA
D.上述反应中,每生成0.1 mol N2转移的电子数目为0.3NA
考法综合练
考法 阿伏加德罗常数的应用
1.(2023广东四校联考,10)用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2 L甲烷含氢原子数目为2NA
B.1 L 0.1 mol·L-1NH4Cl溶液中阳离子的总数小于0.1NA
C.1 mol Na2O2与足量的SO2反应转移电子数为NA
D.1 mol SiO2含有的共价键数目为2NA
2.(2023广州二模,7)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.1 mol SiHCl3含有Si—Cl键的数目为3NA
B.24 g Mg与稀硫酸完全反应,转移的电子数目为NA
C.1 L 1.0 mol·L-1NaHSO4溶液含有阴离子的总数为2NA
D.11.2 L NO与11.2 L O2混合后分子的数目为NA
3.(2023梅州质检二,12)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.0.1 mol 27Al3+中含有的电子数为1.3NA
B.100 mL 1 mol·L-1 Na2S溶液中含有的阴离子数目小于0.1NA
C.标准状况下,22.4 L乙炔中含有的σ键数目为5NA
D.23 g Na与足量的氧气反应转移电子数目为NA
4.(2023广东二模,7)铜可以溶解在氨水和过氧化氢的混合溶液中,反应的离子方程式为Cu+H2O2+4NH3·H2O [Cu(NH3)4]2++2OH-+4H2O。设NA为阿伏加德罗常数的值,下列有关说法不正确的是( )
A.1 mol基态铜原子的最外层电子数为NA
B.每生成18 g H2O转移的电子数为0.5NA
C.标准状况下,22.4 L NH3溶于水,所得溶液中NH3·H2O分子数小于NA
D.100 mL 1 mol·L-1的过氧化氢溶液中含有的氧原子数为0.2NA
5.(2023广州天河综合测试二,11)设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,11.2 L Cl2溶于水生成Cl-的数目为0.5NA
B.25 ℃时,1 L pH=8的CH3COONa溶液中水电离出的OH-数目为10-8NA
C.等物质的量的Al分别与足量盐酸和NaOH溶液反应,转移的电子数均为3NA
D.常温常压下,3.4 g羟基(—OH)所含的电子数目为1.8NA
6.(2023佛山质检二,8)绿矾(FeSO4·7H2O)分解可制备铁红,同时产生SO2、SO3和H2O。设NA为阿伏加德罗常数的值,下列说法错误的是( )
A.1 L 1 mol·L-1FeSO4溶液含有的阳离子数大于NA
B.0.5 mol三聚SO3分子()中含有σ键数目为6NA
C.绿矾分解生成16 g Fe2O3时,转移电子数为0.2NA
D.22.4 L SO2溶于水,溶液中H2SO3、的数目总和为NA
7.(2023湖南师大附中二模,6)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4 L CHCl3所含的分子数为NA
B.向FeBr2溶液中通入适量氯气,当有1 mol Br2生成时,共转移的电子数可能为4NA
C.标准状况下,11.2 L NH3溶于水形成的溶液中、NH3·H2O的微粒数之和为0.5NA
D.3.2 g Cu与S完全反应,转移的电子数为0.1NA
专题二 物质的量
五年高考
考点过关练
考点1 物质的量和气体摩尔体积
1.(2022广东,9,2分)我国科学家进行了如图所示的碳循环研究。下列说法正确的是( )
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C.1 mol CO中含有6.02×1024个电子
D.22.4 L CO2被还原生成1 mol CO
答案 A
2.(2023全国甲,10,6分)NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.0.50 mol异丁烷分子中共价键的数目为6.5NA
B.标准状况下,2.24 L SO3中电子的数目为4.00NA
C.1.0 L pH=2的H2SO4溶液中H+的数目为0.02NA
D.1.0 L 1.0 mol·L-1的Na2CO3溶液中C的数目为1.0NA
答案 A
3.(2023海南,6,2分)NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.2.4 g镁条在空气中充分燃烧,转移的电子数目为0.2NA
B.5.6 g铁粉与0.1 L 1 mol·L-1 HCl溶液充分反应,产生的气体分子数目为0.1NA
C.标准状况下,2.24 L SO2与1.12 L O2充分反应,生成的SO3分子数目为0.1NA
D.1.7 g NH3完全溶于1 L H2O所得溶液中,NH3·H2O数目为0.1NA
答案 A
4.(2022海南,7,2分)在2.8 g Fe中加入100 mL 3 mol·L-1 HCl溶液,Fe完全溶解。NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.反应转移电子为0.1 mol
B.HCl溶液中Cl-数为3NA
C.2.8 g 56Fe含有的中子数为1.3NA
D.反应生成标准状况下气体3.36 L
答案 A
5.(2021广东,11,4分)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 mol CHCl3含有C—Cl键的数目为3NA
B.1 L 1.0 mol/L的盐酸含有阴离子总数为2NA
C.11.2 L NO与11.2 L O2混合后的分子数目为NA
D.23 g Na与足量H2O反应生成的H2分子数目为NA
答案 A
6.(2022浙江6月选考,12,2分)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.12 g NaHSO4中含有0.2NA个阳离子
B.11.2 L乙烷和丙烯的混合气体中所含碳氢键数为3NA
C.8 g CH4含有中子数为3NA
D.0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,HI分子总数为0.2NA
答案 C
7.(2022辽宁,3,3分)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1.8 g 18O中含有的中子数为NA
B.28 g C2H4分子中含有的σ键数目为4NA
C.标准状况下,22.4 L HCl气体中H+数目为NA
D.pH=12的Na2CO3溶液中OH-数目为0.01NA
答案 A
考点2 物质的量浓度
8.(2021广东,7,2分)测定浓硫酸试剂中H2SO4含量的主要操作包括:①量取一定量的浓硫酸,稀释;②转移定容得待测液;③移取20.00 mL待测液,用0.100 0 mol/L的NaOH溶液滴定。上述操作中,不需要用到的仪器为 ( )
答案 B
9.(2022海南,3,2分)下列实验操作规范的是( )
答案 B
10.(2023全国甲,9,6分)实验室将粗盐提纯并配制0.100 0 mol·L-1的NaCl溶液。下列仪器中,本实验必须用到的有( )
①天平 ②温度计 ③坩埚 ④分液漏斗
⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥
B.①④⑤⑥
C.②③⑦⑧
D.①⑤⑥⑧
答案 D
11.(2022山东,6,2分)实验室用基准Na2CO3配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定Na2CO3标准溶液。下列说法错误的是( )
A.可用量筒量取25.00 mL Na2CO3标准溶液置于锥形瓶中
B.应选用配带塑料塞的容量瓶配制Na2CO3标准溶液
C.应选用烧杯而非称量纸称量Na2CO3固体
D.达到滴定终点时溶液显橙色
答案 A
12.(2021天津,7,3分)设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.1 mol·L-1 HCl溶液中,HCl分子的数目为NA
B.22.4 L氢气中,H2分子的数目为NA
C.180 g葡萄糖中,C原子的数目为6NA
D.1 mol N2中,σ键的数目为3NA
答案 C
13.(2022浙江1月选考,12,2分)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.在25 ℃时,1 L pH为12的Ba(OH)2溶液中含有OH-数目为0.01NA
B.1.8 g重水(D2O)中所含质子数为NA
C.足量的浓盐酸与8.7 g MnO2反应,转移电子的数目为0.4NA
D.32 g甲醇的分子中含有C—H键的数目为4NA
答案 A
考法强化练
考法 阿伏加德罗常数的应用
1.(2023辽宁,5,3分)我国古代四大发明之一黑火药的爆炸反应为S+2KNO3+3C K2S+N2↑+3CO2↑。设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.11.2 L CO2含π键数目为NA
B.每生成2.8 g N2转移电子数目为NA
C.0.1 mol KNO3晶体中含离子数目为0.2NA
D.1 L 0.1 mol·L-1 K2S溶液中含S2-数目为0.1NA
答案 C
2.(2022重庆,5,3分)工业上用N2和H2合成NH3 。NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.消耗14 g N2生成NH3分子数为2NA
B.消耗1 mol H2生成N—H键数为2NA
C.生成标准状况下22.4 L NH3,电子转移数为2NA
D.氧化1 mol NH3生成NO,需O2分子数为2NA
答案 B
3.(2022河北,4,3分)NA是阿伏加德罗常数的值。下列说法正确的是( )
A.3.9 g Na2O2与足量水反应,转移电子个数为0.1NA
B.1.2 g Mg在空气中燃烧生成MgO和Mg3N2,转移电子个数为0.1NA
C.2.7 g Al与足量NaOH溶液反应,生成H2的个数为0.1NA
D.6.0 g SiO2与足量NaOH溶液反应,所得溶液中Si的个数为0.1NA
答案 B
4.(2021河北,7,3分)NA是阿伏加德罗常数的值。下列说法错误的是( )
A.22.4 L(标准状况)氟气所含的质子数为18NA
B.1 mol碘蒸气和1 mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73 g,则转移电子数为NA
D.1 L 1 mol·L-1溴化铵水溶液中N与H+离子数之和大于NA
答案 C
5.(2023浙江6月选考,7,3分)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.4.4 g C2H4O中含有σ键数目最多为0.7NA
B.1.7 g H2O2中含有氧原子数为0.2NA
C.向1 L 0.1 mol·L-1 CH3COOH溶液通氨气至中性,铵根离子数为0.1NA
D.标准状况下,11.2 L Cl2通入水中,溶液中氯离子数为0.5NA
答案 A
6.(2023广东,11,4分)设NA为阿伏加德罗常数的值。侯氏制碱法涉及NaCl、NH4Cl和NaHCO3等物质。下列叙述正确的是( )
A.1 mol NH4Cl含有的共价键数目为5NA
B.1 mol NaHCO3完全分解,得到的CO2分子数目为2NA
C.体积为1 L的1 mol·L-1 NaHCO3溶液中,HC数目为NA
D.NaCl和NH4Cl的混合物中含1 mol Cl-,则混合物中质子数为28NA
答案 D
7.(2022福建,3,4分)常温常压下,电化学还原制氨气的总反应方程式如下:
2N2+6H2O 4NH3+3O2
设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.9 g水中含有的孤电子对数为2NA
B.每产生34 g NH3,N2失去的电子数为6NA
C.1 mol·L-1氨水中,含有的NH3·H2O分子数少于NA
D.消耗11.2 L N2(已折算为标准状况)时,产生的O2分子数为0.75NA
答案 D
三年模拟
考点强化练
考点1 物质的量和气体摩尔体积
1.(2024届执信中学10月月考,5)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.78 g Na2O2与足量水完全反应,转移电子数为2NA
B.1 L 0.1 mol·L-1的Na2CO3溶液含C的数目为0.1NA
C.1 mol 分子中所含σ键数为3NA
D.标准状况下,2.24 L CCl4所含氯原子数为0.4NA
答案 C
2.(2024届广州阶段训练,13)氮化硅(Si3N4)常用作飞船返回舱耐高温结构材料,可由石英和焦炭在高温的氮气中通过以下反应制备:3SiO2+6C+2N2 Si3N4+6CO。下列说法不正确的是( )
A.Si3N4中氮元素的化合价为-3
B.该反应中氮气为氧化剂
C.1 mol CO中含有6.02×1024个电子
D.每消耗标准状况下11.2 L的N2,最多生成0.25 mol Si3N4
答案 C
3.(2024届广东四校联考9月月考,11)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.一定条件下,1 mol N2与3 mol H2充分反应,生成NH3的分子数为2NA
B.18 g CH2D2含有的中子数为10NA
C.1 mol白磷(P4)中所含共价键数目为6NA
D.常温常压下,46 g NO2中所含的分子数为NA
答案 C
4.(2023珠海一中二模,9)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,11.2 L HF所含的原子总数为NA
B.用惰性电极电解CuSO4溶液,当阳极产生22.4 L气体时,转移的电子数为4NA
C.2 L 0.1 mol·L-1 Na2SiO3溶液中含的数目为0.2NA
D.向1 L 0.5 mol·L-1盐酸中通入NH3至中性(忽略溶液体积变化),此时N个数为0.5NA
答案 D
考点2 物质的量浓度
5.(2024届华南师大附中第一次月考,4)实验室为配制0.10 mol·L-1的稀硫酸,不需要用到的仪器是( )
答案 B
6.(2024届清中、河中、北中、惠中、阳中、茂中6校第一次联考,11)设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A.28 g由乙烯和环丁烷组成的混合气体中含有的原子数为6NA
B.常温下,5.4 g铝片投入足量的浓硫酸中,铝失去的电子数为0.6NA
C.1 L 0.1 mol·L-1 K2CO3溶液中含有 C的数目为0.1NA
D.室温下pH=11的NaClO溶液中,由水电离出的OH-数目为0.001NA
答案 A
7.(2024届惠州一调,6)反应NH4Cl+NaNO2 NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。设NA为阿伏加德罗常数的值。下列说法不正确的是( )
A.0.1 mol N2中含有π键数目为0.2NA
B.18 g H2O中所含电子数目为10NA
C.常温时,pH=8的NaNO2溶液中所含OH-的数目为10-6NA
D.上述反应中,每生成0.1 mol N2转移的电子数目为0.3NA
答案 C
考法综合练
考法 阿伏加德罗常数的应用
1.(2023广东四校联考,10)用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2 L甲烷含氢原子数目为2NA
B.1 L 0.1 mol·L-1NH4Cl溶液中阳离子的总数小于0.1NA
C.1 mol Na2O2与足量的SO2反应转移电子数为NA
D.1 mol SiO2含有的共价键数目为2NA
答案 A
2.(2023广州二模,7)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.1 mol SiHCl3含有Si—Cl键的数目为3NA
B.24 g Mg与稀硫酸完全反应,转移的电子数目为NA
C.1 L 1.0 mol·L-1NaHSO4溶液含有阴离子的总数为2NA
D.11.2 L NO与11.2 L O2混合后分子的数目为NA
答案 A
3.(2023梅州质检二,12)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.0.1 mol 27Al3+中含有的电子数为1.3NA
B.100 mL 1 mol·L-1 Na2S溶液中含有的阴离子数目小于0.1NA
C.标准状况下,22.4 L乙炔中含有的σ键数目为5NA
D.23 g Na与足量的氧气反应转移电子数目为NA
答案 D
4.(2023广东二模,7)铜可以溶解在氨水和过氧化氢的混合溶液中,反应的离子方程式为Cu+H2O2+4NH3·H2O [Cu(NH3)4]2++2OH-+4H2O。设NA为阿伏加德罗常数的值,下列有关说法不正确的是( )
A.1 mol基态铜原子的最外层电子数为NA
B.每生成18 g H2O转移的电子数为0.5NA
C.标准状况下,22.4 L NH3溶于水,所得溶液中NH3·H2O分子数小于NA
D.100 mL 1 mol·L-1的过氧化氢溶液中含有的氧原子数为0.2NA
答案 D
5.(2023广州天河综合测试二,11)设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,11.2 L Cl2溶于水生成Cl-的数目为0.5NA
B.25 ℃时,1 L pH=8的CH3COONa溶液中水电离出的OH-数目为10-8NA
C.等物质的量的Al分别与足量盐酸和NaOH溶液反应,转移的电子数均为3NA
D.常温常压下,3.4 g羟基(—OH)所含的电子数目为1.8NA
答案 D
6.(2023佛山质检二,8)绿矾(FeSO4·7H2O)分解可制备铁红,同时产生SO2、SO3和H2O。设NA为阿伏加德罗常数的值,下列说法错误的是( )
A.1 L 1 mol·L-1FeSO4溶液含有的阳离子数大于NA
B.0.5 mol三聚SO3分子()中含有σ键数目为6NA
C.绿矾分解生成16 g Fe2O3时,转移电子数为0.2NA
D.22.4 L SO2溶于水,溶液中H2SO3、的数目总和为NA
答案 D
7.(2023湖南师大附中二模,6)设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4 L CHCl3所含的分子数为NA
B.向FeBr2溶液中通入适量氯气,当有1 mol Br2生成时,共转移的电子数可能为4NA
C.标准状况下,11.2 L NH3溶于水形成的溶液中、NH3·H2O的微粒数之和为0.5NA
D.3.2 g Cu与S完全反应,转移的电子数为0.1NA
答案 B
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
