广东省湛江市雷州市第二中学2023-2024学年高一下学期期中考试化学试卷(含答案)
文档属性
| 名称 | 广东省湛江市雷州市第二中学2023-2024学年高一下学期期中考试化学试卷(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-25 00:00:00 | ||
图片预览



文档简介
2023-2024学年第二学期高一化学期中考试试题
注 意 事 项
考生在答题前请认真阅读本注意事项及各题答题要求
1.本试卷满分为100分,考试时间为75分钟。考试结束后,请将答题卡交回。
2.答题前,请你务必将自己的姓名、学校、考试号等用0.5毫米黑色墨水签字笔填写在答题卡上规定的位置。
3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号和本人是否相符。
4.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮擦干净后,再选涂其他答案。作答非选择题,必须用0.5毫米黑色墨水签字笔在答题卡上的指定位置作答,在其他位置作答一律无效。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 Ca 40 Cu 64 Se 79
一、单项选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。每小题只有一个选项符合题意。
1.“高山流水觅知音”。下列中国古乐器中,主要由硅酸盐材料制成的是
A.九霄环佩木古琴 B.裴李岗文化骨笛 C.商朝后期陶埙 D.曾侯乙青铜编钟
A.A B.B C.C D.D
2.化学处处呈现美。下列说法正确的是
A.舞台上干冰升华时,共价键断裂 B.饱和溶液可析出无水蓝色晶体
C.冰雪融化时破坏的氢键是属于共价键
D.晨雾中的光束如梦如幻,是丁达尔效应带来的美景
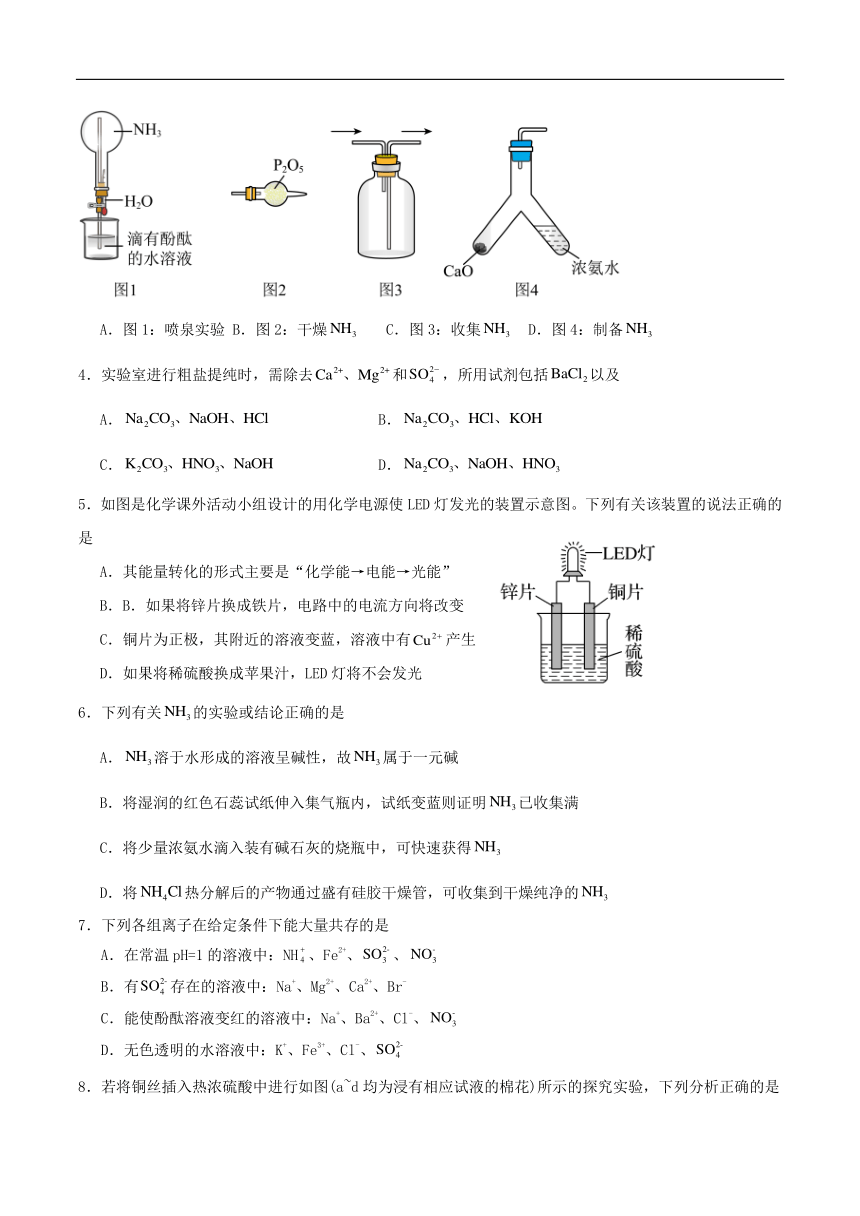
3.1827年,英国科学家法拉第进行了喷泉实验。在此启发下,兴趣小组利用以下装置,进行如下实验。其中,难以达到预期目的的是
A.图1:喷泉实验 B.图2:干燥 C.图3:收集 D.图4:制备
4.实验室进行粗盐提纯时,需除去和,所用试剂包括以及
A. B.
C. D.
5.如图是化学课外活动小组设计的用化学电源使LED灯发光的装置示意图。下列有关该装置的说法正确的是
其能量转化的形式主要是“化学能→电能→光能”
B.如果将锌片换成铁片,电路中的电流方向将改变
C.铜片为正极,其附近的溶液变蓝,溶液中有产生
D.如果将稀硫酸换成苹果汁,LED灯将不会发光
6.下列有关的实验或结论正确的是
A.溶于水形成的溶液呈碱性,故属于一元碱
B.将湿润的红色石蕊试纸伸入集气瓶内,试纸变蓝则证明已收集满
C.将少量浓氨水滴入装有碱石灰的烧瓶中,可快速获得
D.将热分解后的产物通过盛有硅胶干燥管,可收集到干燥纯净的
7.下列各组离子在给定条件下能大量共存的是
A.在常温pH=1的溶液中:NH、Fe2+、、
B.有存在的溶液中:Na+、Mg2+、Ca2+、Br-
C.能使酚酞溶液变红的溶液中:Na+、Ba2+、Cl-、
D.无色透明的水溶液中:K+、Fe3+、Cl-、
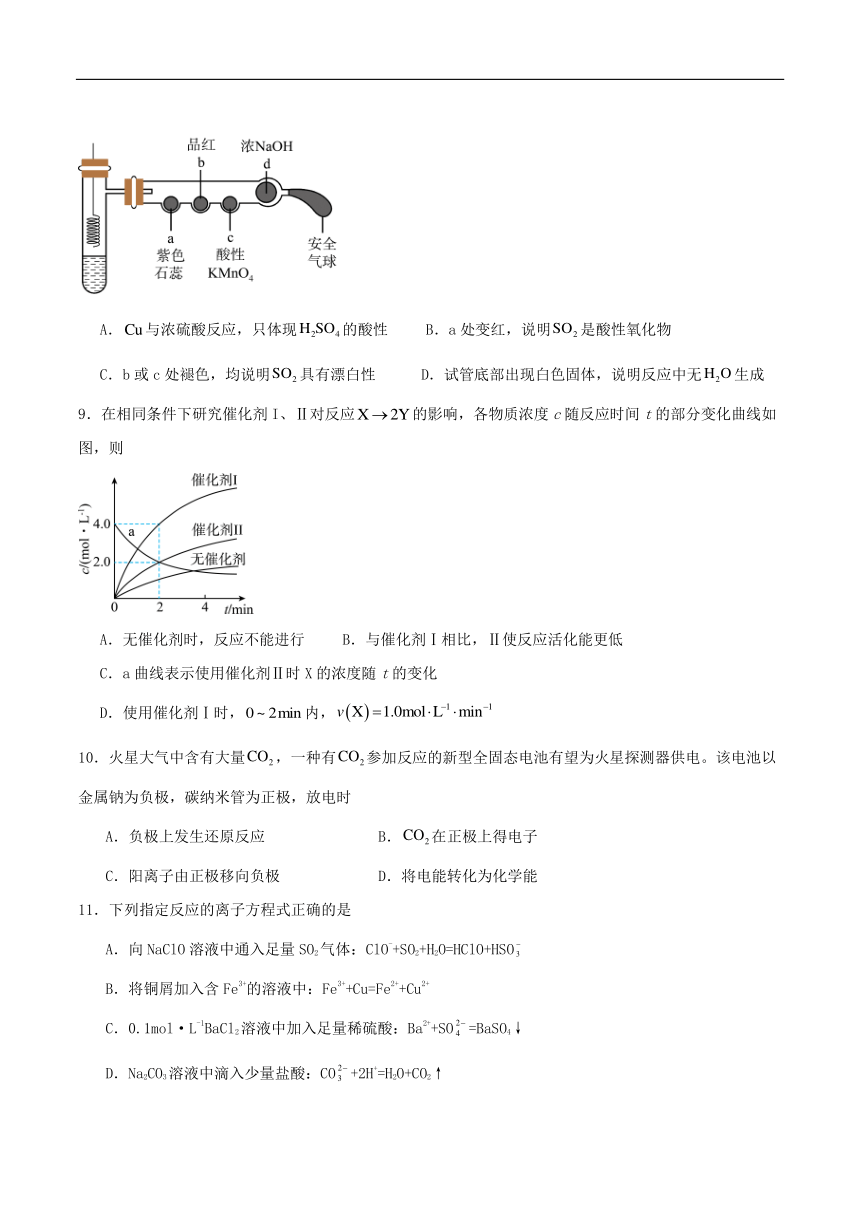
8.若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是
A.与浓硫酸反应,只体现的酸性 B.a处变红,说明是酸性氧化物
C.b或c处褪色,均说明具有漂白性 D.试管底部出现白色固体,说明反应中无生成
9.在相同条件下研究催化剂I、Ⅱ对反应的影响,各物质浓度c随反应时间t的部分变化曲线如图,则
A.无催化剂时,反应不能进行 B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时,内,
10.火星大气中含有大量,一种有参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应 B.在正极上得电子
C.阳离子由正极移向负极 D.将电能转化为化学能
11.下列指定反应的离子方程式正确的是
A.向NaClO溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO
B.将铜屑加入含Fe3+的溶液中:Fe3++Cu=Fe2++Cu2+
C.0.1mol·L-1BaCl2溶液中加入足量稀硫酸:Ba2++SO=BaSO4↓
D.Na2CO3溶液中滴入少量盐酸:CO+2H+=H2O+CO2↑
12.按图装置进行实验。将稀硫酸全部加入Ⅰ中的试管,关闭活塞。下列说法正确的是
A.Ⅰ中试管内的反应,体现的氧化性 B.Ⅱ中品红溶液褪色,体现的还原性
C.在Ⅰ和Ⅲ的试管中,都出现了浑浊现象 D.撤掉水浴,重做实验,Ⅳ中红色更快褪去
13.设表示阿伏加德罗常数,下列叙述中正确的是
A.常温常压下,11.2L氧气所含的原子数为
B.标准状况下,1mol的体积约为22.4L
C.15.6g与过量反应时,转移的电子数为
D.标准状况下,0.5molNO和0.5mol组成的混合气体,体积约为22.4L
14.价类二维图是学习元素化合物的工具,如图a~g分别表示氮元素的不同价态所对应的物质。下列说法错误的是
A.f属于电解质 B.a可转化为c
C.b化学性质稳定,可从空气中提取 D.g受热分解可制取a
15.化学反应的能量变化如图所示,则下列说法正确的是
A.该反应是吸热反应
B.断裂键和键能放出的能量
C.断裂键需要吸收ykJ的能量
D.的总能量高于1molA2和1molB2的总能量
16.负载有和的活性炭,可选择性去除实现废酸的纯化,其工作原理如图。下列说法正确的是
A.作原电池正极
B.电子由经活性炭流向
C.表面发生的电极反应:
D.每消耗标准状况下的,最多去除
二、填空题
17.(一)工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为: 。
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HClSiHCl3+H2,生成物SiHCl3的结构式为: 。
(二)某化学兴趣小组利用下列图示装置探究氨气的性质。
(3)①中湿润的红色石蕊试纸变蓝的原因: (用化学方程式表示)。
(4)向②中滴入浓盐酸,现象为: 。
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式: ,瓶中红棕色气体为 (填化学式)。
(三)某氨氮废水(、)的生物法处理流程如图所示:
(6)检验氨氮废水中含有的方法是: 。
(7)过程Ⅱ在硝化细菌作用下实现的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为: 。
18.某温度时,在2 L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:
(1)该反应的化学方程式为 。
(2)从反应开始至4 min时,A的平均反应速率为 。
(3)反应3Fe(s)+4H2O(g)Fe3O4+4H2(g),在一可变的容积的密闭容器中进行,(填增大、不变、减小)
①保持体积不变,充入N2使体系压强增大,其正反应速率 。
②保持压强不变,充入N2使容器的体积增大,逆反应速率 。
(4)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)===xC(g)+2D(g),经过5 min后测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,C的反应速率是0.1 mol·L-1·min-1,A在5 min末的浓度是 ,x的值是 。
19.工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为和),其反应的化学方程式为,请回答下列问题:
(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是__________。
A.铝粉与氧化铁的反应 B.氯化铵与的反应
C.锌片与稀硫酸的反应 D.钠与冷水的反应
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是__________。
A.充入使容器压强增大,反应速率不变
B.增加焦炭的量可以加快反应速率
C.升高温度,氢气的生成速率加快
D.只要焦炭的量足够,水蒸气的转化率可以达到100%
(3)在体积均为的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和水蒸气,在不同温度下反应的过程如下图所示:
①甲容器中,内的平均反应速率 。
②甲容器中,A点正反应速率 B点的逆反应速率(填“<”“>”或“=”)。
③反应过程中,两个容器温度:甲 乙(填“<” “>”或“=”)。
④乙容器中C点时,的物质的量百分数为 。
(4)在溶液条件下,以H2为原料,可制成一种燃料电池,写出该电池的负极反应式 ,当燃料电池消耗22.4LH2(标况下)时,正极上有 参与反应。
20.治理氮氧化物(NOx)的污染是化学研究的重要课题之一。
I.NO能被灼热的铁粉还原为N2,同时生成FeO,利用下列装置模拟该反应。
已知:①浓硝酸可将NO氧化为NO2;②NaOH溶液能与NO2反应,不与NO反应。
(1)打开A装置分液漏斗活塞,烧瓶中观察到的实验现象有:铜片表面出现无色气泡,铜片逐渐变小、 、烧瓶中溶液由无色变为蓝色。
(2)上述装置接口的连接顺序为:a→___→___→___→___→g→h→b→c→d(按气流方向,用小写字母表示) 。
(3)装置B的作用是 。
(4)装置E中反应的化学方程式为 。
II.已知:(NOx)能与Na2O2反应;NO2和Na2O2都有较强氧化性。为探究NO2与Na2O2反应的产物,提出如下假设:
假设①NO2氧化Na2O2;假设②Na2O2氧化NO2
甲同学设计如图所示实验装置:
请回答下列问题:
(5)甲乙两同学对假设分别进行了验证:
实验操作 现象 结论
甲同学 待试管G中收集满气体,向其中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管,观察现象;并将带火星的木条迅速伸进试管,观察。 红棕色气体迅速消失;木条复燃 假设①正确
乙同学 在F、G之间增加一个M洗气瓶,目的是 ______________ ,重复甲同学的实验操作。 红棕色气体迅速消失,带火星的木条未复燃 假设②正确
请做出正确判断,写出NO2和Na2O2反应的化学方程式___________________________________。
图中单向阀在实现气体单向流通的同时,还有一个作用是 ______________________________。
注 意 事 项
考生在答题前请认真阅读本注意事项及各题答题要求
1.本试卷满分为100分,考试时间为75分钟。考试结束后,请将答题卡交回。
2.答题前,请你务必将自己的姓名、学校、考试号等用0.5毫米黑色墨水签字笔填写在答题卡上规定的位置。
3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号和本人是否相符。
4.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮擦干净后,再选涂其他答案。作答非选择题,必须用0.5毫米黑色墨水签字笔在答题卡上的指定位置作答,在其他位置作答一律无效。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 Ca 40 Cu 64 Se 79
一、单项选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。每小题只有一个选项符合题意。
1.“高山流水觅知音”。下列中国古乐器中,主要由硅酸盐材料制成的是
A.九霄环佩木古琴 B.裴李岗文化骨笛 C.商朝后期陶埙 D.曾侯乙青铜编钟
A.A B.B C.C D.D
2.化学处处呈现美。下列说法正确的是
A.舞台上干冰升华时,共价键断裂 B.饱和溶液可析出无水蓝色晶体
C.冰雪融化时破坏的氢键是属于共价键
D.晨雾中的光束如梦如幻,是丁达尔效应带来的美景
3.1827年,英国科学家法拉第进行了喷泉实验。在此启发下,兴趣小组利用以下装置,进行如下实验。其中,难以达到预期目的的是
A.图1:喷泉实验 B.图2:干燥 C.图3:收集 D.图4:制备
4.实验室进行粗盐提纯时,需除去和,所用试剂包括以及
A. B.
C. D.
5.如图是化学课外活动小组设计的用化学电源使LED灯发光的装置示意图。下列有关该装置的说法正确的是
其能量转化的形式主要是“化学能→电能→光能”
B.如果将锌片换成铁片,电路中的电流方向将改变
C.铜片为正极,其附近的溶液变蓝,溶液中有产生
D.如果将稀硫酸换成苹果汁,LED灯将不会发光
6.下列有关的实验或结论正确的是
A.溶于水形成的溶液呈碱性,故属于一元碱
B.将湿润的红色石蕊试纸伸入集气瓶内,试纸变蓝则证明已收集满
C.将少量浓氨水滴入装有碱石灰的烧瓶中,可快速获得
D.将热分解后的产物通过盛有硅胶干燥管,可收集到干燥纯净的
7.下列各组离子在给定条件下能大量共存的是
A.在常温pH=1的溶液中:NH、Fe2+、、
B.有存在的溶液中:Na+、Mg2+、Ca2+、Br-
C.能使酚酞溶液变红的溶液中:Na+、Ba2+、Cl-、
D.无色透明的水溶液中:K+、Fe3+、Cl-、
8.若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是
A.与浓硫酸反应,只体现的酸性 B.a处变红,说明是酸性氧化物
C.b或c处褪色,均说明具有漂白性 D.试管底部出现白色固体,说明反应中无生成
9.在相同条件下研究催化剂I、Ⅱ对反应的影响,各物质浓度c随反应时间t的部分变化曲线如图,则
A.无催化剂时,反应不能进行 B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时,内,
10.火星大气中含有大量,一种有参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应 B.在正极上得电子
C.阳离子由正极移向负极 D.将电能转化为化学能
11.下列指定反应的离子方程式正确的是
A.向NaClO溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO
B.将铜屑加入含Fe3+的溶液中:Fe3++Cu=Fe2++Cu2+
C.0.1mol·L-1BaCl2溶液中加入足量稀硫酸:Ba2++SO=BaSO4↓
D.Na2CO3溶液中滴入少量盐酸:CO+2H+=H2O+CO2↑
12.按图装置进行实验。将稀硫酸全部加入Ⅰ中的试管,关闭活塞。下列说法正确的是
A.Ⅰ中试管内的反应,体现的氧化性 B.Ⅱ中品红溶液褪色,体现的还原性
C.在Ⅰ和Ⅲ的试管中,都出现了浑浊现象 D.撤掉水浴,重做实验,Ⅳ中红色更快褪去
13.设表示阿伏加德罗常数,下列叙述中正确的是
A.常温常压下,11.2L氧气所含的原子数为
B.标准状况下,1mol的体积约为22.4L
C.15.6g与过量反应时,转移的电子数为
D.标准状况下,0.5molNO和0.5mol组成的混合气体,体积约为22.4L
14.价类二维图是学习元素化合物的工具,如图a~g分别表示氮元素的不同价态所对应的物质。下列说法错误的是
A.f属于电解质 B.a可转化为c
C.b化学性质稳定,可从空气中提取 D.g受热分解可制取a
15.化学反应的能量变化如图所示,则下列说法正确的是
A.该反应是吸热反应
B.断裂键和键能放出的能量
C.断裂键需要吸收ykJ的能量
D.的总能量高于1molA2和1molB2的总能量
16.负载有和的活性炭,可选择性去除实现废酸的纯化,其工作原理如图。下列说法正确的是
A.作原电池正极
B.电子由经活性炭流向
C.表面发生的电极反应:
D.每消耗标准状况下的,最多去除
二、填空题
17.(一)工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为: 。
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HClSiHCl3+H2,生成物SiHCl3的结构式为: 。
(二)某化学兴趣小组利用下列图示装置探究氨气的性质。
(3)①中湿润的红色石蕊试纸变蓝的原因: (用化学方程式表示)。
(4)向②中滴入浓盐酸,现象为: 。
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式: ,瓶中红棕色气体为 (填化学式)。
(三)某氨氮废水(、)的生物法处理流程如图所示:
(6)检验氨氮废水中含有的方法是: 。
(7)过程Ⅱ在硝化细菌作用下实现的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为: 。
18.某温度时,在2 L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:
(1)该反应的化学方程式为 。
(2)从反应开始至4 min时,A的平均反应速率为 。
(3)反应3Fe(s)+4H2O(g)Fe3O4+4H2(g),在一可变的容积的密闭容器中进行,(填增大、不变、减小)
①保持体积不变,充入N2使体系压强增大,其正反应速率 。
②保持压强不变,充入N2使容器的体积增大,逆反应速率 。
(4)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)===xC(g)+2D(g),经过5 min后测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,C的反应速率是0.1 mol·L-1·min-1,A在5 min末的浓度是 ,x的值是 。
19.工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为和),其反应的化学方程式为,请回答下列问题:
(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是__________。
A.铝粉与氧化铁的反应 B.氯化铵与的反应
C.锌片与稀硫酸的反应 D.钠与冷水的反应
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是__________。
A.充入使容器压强增大,反应速率不变
B.增加焦炭的量可以加快反应速率
C.升高温度,氢气的生成速率加快
D.只要焦炭的量足够,水蒸气的转化率可以达到100%
(3)在体积均为的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和水蒸气,在不同温度下反应的过程如下图所示:
①甲容器中,内的平均反应速率 。
②甲容器中,A点正反应速率 B点的逆反应速率(填“<”“>”或“=”)。
③反应过程中,两个容器温度:甲 乙(填“<” “>”或“=”)。
④乙容器中C点时,的物质的量百分数为 。
(4)在溶液条件下,以H2为原料,可制成一种燃料电池,写出该电池的负极反应式 ,当燃料电池消耗22.4LH2(标况下)时,正极上有 参与反应。
20.治理氮氧化物(NOx)的污染是化学研究的重要课题之一。
I.NO能被灼热的铁粉还原为N2,同时生成FeO,利用下列装置模拟该反应。
已知:①浓硝酸可将NO氧化为NO2;②NaOH溶液能与NO2反应,不与NO反应。
(1)打开A装置分液漏斗活塞,烧瓶中观察到的实验现象有:铜片表面出现无色气泡,铜片逐渐变小、 、烧瓶中溶液由无色变为蓝色。
(2)上述装置接口的连接顺序为:a→___→___→___→___→g→h→b→c→d(按气流方向,用小写字母表示) 。
(3)装置B的作用是 。
(4)装置E中反应的化学方程式为 。
II.已知:(NOx)能与Na2O2反应;NO2和Na2O2都有较强氧化性。为探究NO2与Na2O2反应的产物,提出如下假设:
假设①NO2氧化Na2O2;假设②Na2O2氧化NO2
甲同学设计如图所示实验装置:
请回答下列问题:
(5)甲乙两同学对假设分别进行了验证:
实验操作 现象 结论
甲同学 待试管G中收集满气体,向其中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管,观察现象;并将带火星的木条迅速伸进试管,观察。 红棕色气体迅速消失;木条复燃 假设①正确
乙同学 在F、G之间增加一个M洗气瓶,目的是 ______________ ,重复甲同学的实验操作。 红棕色气体迅速消失,带火星的木条未复燃 假设②正确
请做出正确判断,写出NO2和Na2O2反应的化学方程式___________________________________。
图中单向阀在实现气体单向流通的同时,还有一个作用是 ______________________________。
同课章节目录
