化学人教版(2019)必修第二册7.3.1乙醇(共41张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.3.1乙醇(共41张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 140.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-05-30 00:00:00 | ||
图片预览








文档简介
(共41张PPT)
高中化学 人教版必修第二册
第七章 有机化合物
第三节 乙醇与乙酸
第1课时 乙醇
●
学习目标:
1.认识乙醇的结构及其主要性质与应用。
2.理解烃的衍生物、官能团的概念。
●
学习重点:
1.乙醇的结构与重要性质。
2.能设计简单实验方案探究乙醇发生反应的条件和反应方式。
●
学习难点:
分析乙醇及其反应的微观特征,能推测其他醇类的性质。
将进酒
君不见黄河之水天上来,奔流到海不复回。
君不见高堂明镜悲白发,朝如青丝暮成雪。
人生得意须尽欢,莫使金樽空对月。
天生我材必有用,千金散尽还复来。
烹羊宰牛且为乐,会须一饮三百杯。
岑夫子,丹丘生,将进酒,杯莫停。
与君歌一曲,请君为我倾耳听。
钟鼓馔玉不足贵,但愿长醉不愿醒。
古来圣贤皆寂寞,惟有饮者留其名。
陈王昔时宴平乐,斗酒十千恣欢谑。
主人何为言少钱,径须沽取对君酌。
五花马,千金裘,
呼儿将出换美酒,与尔同销万古愁。
酒与传统文化
酒文化博大精深,源远流长,早在几千年前,人类就掌握了发酵法酿酒的技术。
(以上均为体积分数)
医用酒精:含乙醇75%
工业酒精:含乙醇96%
无水酒精:含乙醇99.5%以上
无水乙醇的制备:
普通的工业酒精是含乙醇95.6%,用蒸馏的方法不能将乙醇中的水完全除去。(水和乙醇在95℃形成共沸物)
要制取无水乙醇,实验中可加入生石灰后再进行蒸馏。
可用无水硫酸铜检验乙醇中是否含水
探究课堂
探究课堂
以下说法或事实体现了乙醇哪些物理性质?
1.病人发烧通常用酒精擦拭全身,用此法降温。
2.衣服上沾上少许汽油用酒精可以去除。
3.酒香不怕巷子深。
4.白酒的主要成分是乙醇和水。
5.酒精灯用完后为什么要盖上灯帽
6.用酒泡中药(药酒)—如泡枸杞
(易挥发)
(易挥发、有特殊香味)
(乙醇易溶于水)
(易挥发)
(良好的有机溶剂)
(良好的有机溶剂)
你在生活中还有那些地方用到了酒精,体现了乙醇哪些物理性质?
1.1
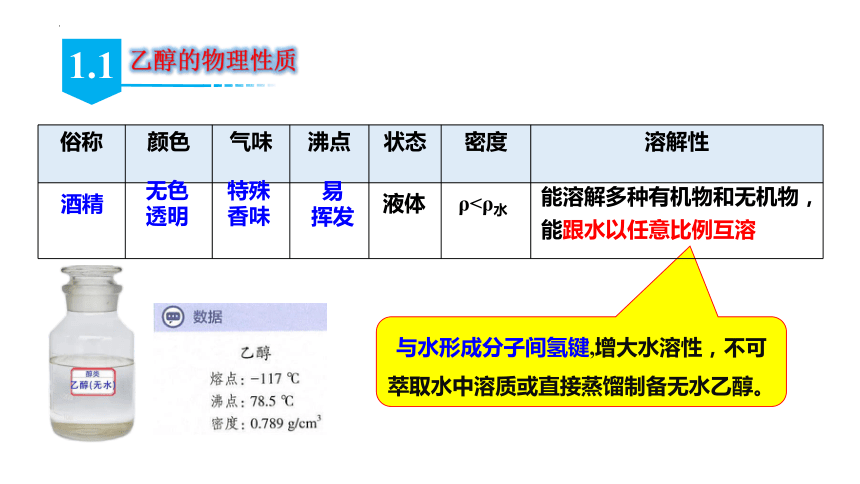
乙醇的物理性质
与水形成分子间氢键,增大水溶性,不可萃取水中溶质或直接蒸馏制备无水乙醇。
俗称 颜色 气味 沸点 状态 密度 溶解性
酒精
无色透明
特殊
香味
液体
ρ<ρ水
易
挥发
能溶解多种有机物和无机物,能跟水以任意比例互溶
对应训练
【典例1】有关乙醇的说法不正确的是( )
A.乙醇溶于水
B.乙醇易挥发
C.医用酒精含乙醇体积分数95%
D.用工业酒精与生石灰通过加热蒸馏的方法制无水酒精
C
【解析】A.乙醇与水分子间能形成氢键,所以乙醇易溶于水,A正确;B.乙醇的沸点低,具有较强的挥发性,B正确;C.医用酒精含乙醇体积分数为75%,95%的乙醇易使细菌表面的蛋白质变性,从而形成硬壳保护膜,不能杀死细菌,C不正确;D.以工业酒精为原料制取无水酒精时,常与生石灰混合,使水与生石灰反应,然后加热蒸馏,D正确;故选C。
对应训练
【典例2】下列有关乙醇的物理性质的应用中,不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药
的有效成分
C.由于乙醇能够以任意比溶于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有“酒香不怕巷子深”的说法
A
【解析】由于乙醇与水互溶,故不能用分液的方法除去乙醇中的水。A项不正确;乙醇提取中草药的有效成分是利用了有机物易溶于乙醇的原理,B项正确;乙醇与水能够以任意比互溶,C项正确;乙醇是一种具有特殊香味、易挥发性的液体,D项正确。故答案选A。
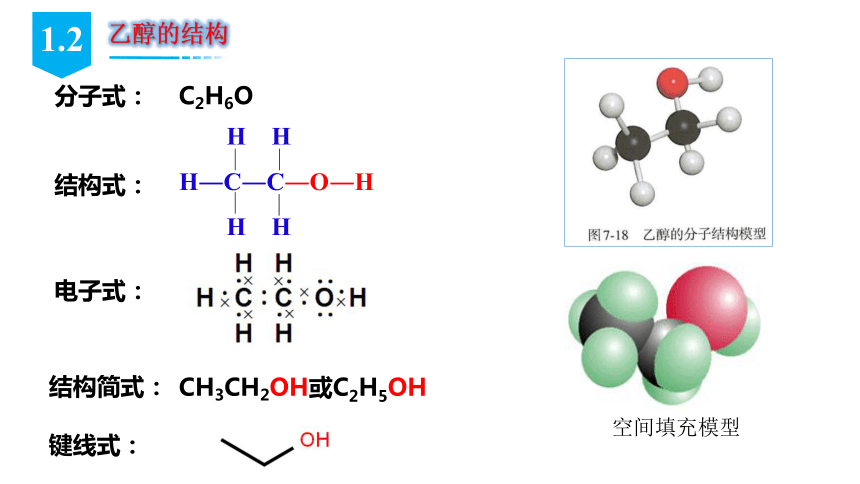
分子式:
H H
H―C―C―O―H
H H
结构式:
结构简式:
CH3CH2OH或C2H5OH
C2H6O
电子式:
空间填充模型
键线式:
1.2
乙醇的结构
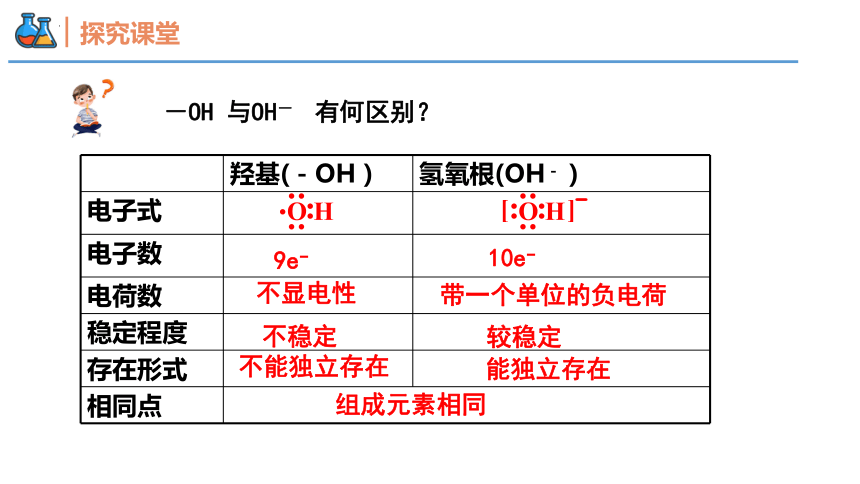
-OH 与OH- 有何区别?
探究课堂
羟基(-OH ) 氢氧根(OH- )
电子式
电子数
电荷数
稳定程度
存在形式
相同点 不显电性
带一个单位的负电荷
不能独立存在
能独立存在
组成元素相同
9e
10e
不稳定
较稳定
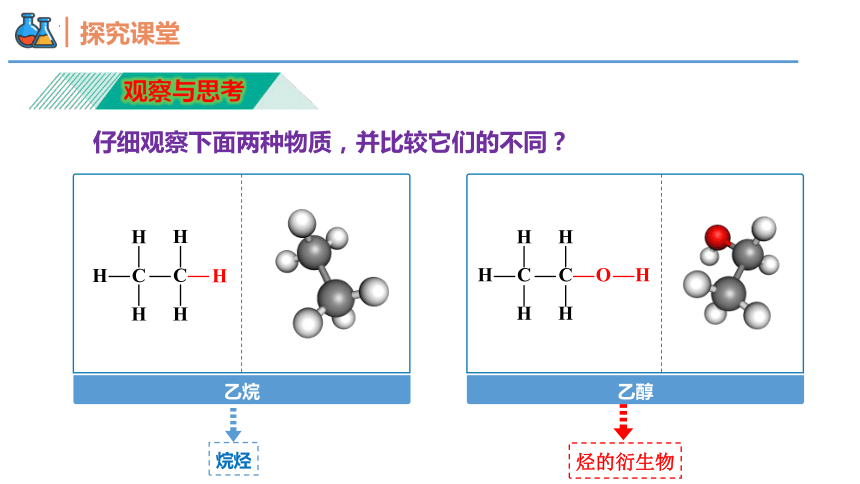
观察与思考
仔细观察下面两种物质,并比较它们的不同?
H
H
H
C
H
H
C
H
乙烷
乙醇
H
H
O
H
C
H
H
C
H
烷烃
烃的衍生物
探究课堂
1.3
烃的衍生物
1.定义:烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称烃的衍生物。如CH3CH2OH、CH3Cl、CH3CH2Br等,其中CH3CH2OH含有氧元素,又叫烃的含氧衍生物。
2.官能团
(1)定义:决定有机化合物_____的原子或原子团。
(2)实例
特性
物质 CH3Cl CH3CH2OH CH2=CH2 CH≡CH
所含官 能团 _____ _____ —C≡C—
官能团的 名称 氯原子 _____ _________ ________
—Cl
—OH
羟基
碳碳双键
碳碳三键
对应训练
【典例1】下列有关乙醇的说法正确的是( )
A.乙醇的结构简式为C2H6O
B.乙醇分子中含有OH-
C.乙醇分子中有2个甲基
D.乙醇中含有官能团羟基
【解析】A.乙醇的结构简式为C2H5OH,故A错误;B.乙醇分子中含有羟基-OH,故B错误;C.乙醇分子的结构简式是CH3CH2OH,分子中有1个甲基,故C错误;D.乙醇结构简式是C2H5OH、二甲醚结构简式是CH3OCH3,分子式相同、结构不同,互为同分异构体,故D正确;选D。
D
对应训练
C
【典例2】下列表示物质结构的化学用语正确的是( )
A.空间充填模型 可以表示甲烷分子,也可以表示四氯化碳分子
B.乙烯C2H4的结构简式:CH2CH2
C.乙醇的结构式是: D.NH3的电子式:
【解析】A.氢原子的原子半径小于碳原子,但氯原子的原子半径大于碳原子,则该空间充填模型可以表示甲烷分子,不可以表示四氯化碳分子,故A错误;B.乙烯的分子式为C2H4,结构简式为CH2=CH2,故B错误;C.乙醇的结构简式为CH3CH2OH,结构式为该结构,故C正确;D.氨气是共价化合物,电子式为 ,故D错误;故选C。
1. 乙醇与钠的反应
实验操作
实验现象
实验结论
①钠开始沉于试管底部,最终慢慢消失,产生无色无味气体;
②烧杯内壁有水珠产生;
③向烧杯中加入澄清石灰水不变浑浊
乙醇与钠反应生成氢气,
化学方程式为2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑
2.1
乙醇的物理性质
乙醇的化学性质原理探析
学生活动1:对比钠与乙醇、水反应的比较实验现象,你能得出什么结
论?填写表格内容。
探究课堂
水与钠反应 乙醇与钠反应
钠的变化
声的现象
气体检验
实验结论
钠粒浮于水面,熔成闪亮的小球,并快速地四处游动,很快消失
钠粒开始沉于试管底部,未熔化,最终慢慢消失
无声响
有“嘶嘶”声响
点燃,发出淡蓝色的火焰
点燃,发出淡蓝色的火焰
钠的密度小于水,熔点低。钠与水剧烈反应,生成氢气。水分子中—OH上的氢原子比较活泼
钠的密度比乙醇的大。钠与乙醇缓慢反应生成氢气。乙醇中羟基上的氢原子相对不活泼
ρ水>ρ钠 > ρ乙醇
探究课堂
探究课堂
① 处O-H键断开
2CH3CH2—O—H +2Na →2CH3CH2ONa +H2↑
注意!
① 断O—H键,发生置换反应或取代反应
② 氢原子活泼性:酸______水______醇
③ 含有 OH的有机物都能与Na反应,如CH3OH等,且1mol OH ~ __________mol H2。
故此反应既可检验—OH的存在,又可用来计算分子中—OH的数目
④ CH3CH2OH是非电解质,不能电离出H+,故不能与碱溶液反应。
>
>
0.5
实验室和生活中酒精的最常见的用途是用作燃料
2CO2 +3H2O
C2H5OH + 3O2
点燃
现象:产生淡蓝色火焰,同时放出大量热。
2. 氧化反应
(1)乙醇燃烧
高温焊接银器或铜器时,表面会生成黑色的氧化物,师傅说:把铜或银器具趁热蘸一下酒精,铜或银会光亮如初!这是为什么呢?
探究课堂
实验操作
实验现象
实验结论
(2)乙醇的催化氧化反应
红色的铜丝 变为黑色 变为红色,闻到刺激性气味
2CH3CH2OH+O2 2CH3CHO+2H2O
乙醇被氧化为乙醛,化学方程式为
Cu/Ag
△
实验探究
【实验7-5】
探究课堂
铜丝红
Δ
变黑
有刺激性气味
插入乙醇溶液中
又变红
Cu
Δ
CuO
乙醛CH3CHO
插入乙醇溶液中
Cu
分析:发生反应 2Cu+O2==2CuO
分析:生成新的物质—乙醛
CuO+CH3CH2OH Cu +CH3CHO+H2O
催化剂
现象及原因探究:
中间产物
探究课堂
②断键机理:
反应历程
2Cu + O2 == 2CuO
C2H5OH+ CuO CH3CHO+ H2O+ Cu
总反应:
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu或Ag
乙醛
2 2 2 2 2
脱去2个H与1个O结合成H2O
2 CH3-C-O-H + O2 2CH3-C-H + 2H2O
H
H
Cu / Ag
O
=
可见,实际起氧化作用的是CuO ,Cu是催化剂
醛基
—CHO
—C—H
O
—COH
探究课堂
Cu
乙醇
乙醛
氧原子
水
H—C—C—O
H
H
H
氢原子
碳原子
探究课堂
-----
-----
① 处O-H键断开
③处C-H键断开
原理分析:
乙醇在被催化氧化时,①③键发生断裂,即乙醇催化氧化反应的实质是脱去与羟基相连的碳原子上的氢原子和羟基上的氢原子,这两个氢原子与氧原子结合形成H2O,若醇分子中与羟基相连的碳原子上无氢原子,则不能被催化氧化。
H
H
O
H
C
H
H
C
H
α
β
CH3
H
O
C
CH3
CH3
H
C
H
α
β
探究课堂
(2)乙醇的催化氧化反应
小结:醇被催化氧化的规律
规律:乙醇催化氧化反应的断键方式可知,醇在有催化剂(铜或银)存在的条件下,可以发生催化氧化反应生成醛,但并不是所有的醇都能被氧化生成醛。
①凡是含有R—CH2OH(R代表烃基)结构的醇,催化氧化成醛:
2R—CH2OH+O2 2R—CHO+2H2O
②凡是含有 结构的醇,在一定条件下也能被催化氧化,但生成物不是醛,而是酮( )
③凡是羟基所连C原子上没有H原子的醇通常情况下不能被催化氧化。
【结论】与—OH相连碳原子上有氢原子的醇才能被催化氧化。
探究课堂
对应训练
【典例1】下列能说明乙醇分子中有一个氢原子与其他氢原子不同的是
( )
A.乙醇能燃烧
B.1molCH3CH2OH与Na完全反应只生成0.5molH2
C.乙醇分子中含有一个氧原子
D.乙醇能溶于水
C
【解析】A项,乙醇燃烧时,所有的氢原子均参与反应生成H2O;B项无法证明题中结论;D项,乙醇氧化成乙醛时,O—H及C—H均参与反应,也无法证明氢原子的不同;C项乙醇与足量钠反应,参与反应的氢原子占醇分子中氢原子的六分之一,说明其中一个氢原子与另外五个不同。
对应训练
【典例2】下列方法中可以证明乙醇分子中有一个氢原子与其他氢原子
不同的是( )
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以制饮料
C.1 mol乙醇与足量的Na作用得0.5 mol H2
D.1 mol乙醇可生成1 mol乙醛
C
【解析】A项,乙醇燃烧时,所有的氢原子均参与反应生成H2O;B项无法证明题中结论;D项,乙醇氧化成乙醛时,O—H及C—H均参与反应,也无法证明氢原子的不同;C项乙醇与足量钠反应,参与反应的氢原子占醇分子中氢原子的六分之一,说明其中一个氢原子与另外五个不同。
反应原理:CH3CH2OH CH3COOH。
KMnO4(紫色)
MnSO4
(无色)
Cr2(SO4)3
硫酸铬 (绿色)
K2Cr2O7
重铬酸钾(橙色)
(3)乙醇与强氧化剂的反应
5CH3CH2OH + 4MnO4- + 12H+ → 5CH3COOH + 4Mn2+ + 11H2O
2Cr2O72-+3CH3CH2OH+16H+ → 4Cr3++3CH3COOH+11H2O
探究课堂
交通警察检查司机是否酒后驾车的装置中,含有橙色的酸性重铬酸钾,当其遇到乙醇时橙色变为绿色,由此可以判断司机是否酒后驾车。
资料卡片
探究课堂
探究课堂
乙醇在人体内究竟发生了哪些化学变化 喝酒上脸的人真能喝吗?“喝酒脸红不伤肝,喝酒脸白才伤肝”是真的吗?为何女性更容易喝醉?究竟谁才是真正的酒神?
生活解密
探究课堂
生活解密
2.3
乙醇的用途
用作燃料
工业
乙醇溶剂
重要的化工原料和溶剂
用作消毒剂
酒精饮料
探究课堂
课堂小结
乙醇
分子组成和结构
用途
分子式
结构式
官能团
C2H6O
—OH
燃料
化工原料
医用消毒剂
物理性质
无色、有特殊香味的液体
密度小于水
易溶于水和有机溶剂
沸点较低,易挥发
化学性质
与强氧化剂反应
氧化反应
置换反应
使酸性高锰酸钾溶液褪色
与羟基相连的碳上必须有氢原子
淡蓝色火焰
乙醇与钠反应
催化氧应
燃烧
对应训练
【典例1】乙醇能发生如下反应:①CH3CH2OH+3O2 2CO2+3H2O;
②2Cu+O2 2CuO,CH3CH2OH+CuO CH3CHO+H2O+Cu。
由以上反应不能得出的结论是( )
A.由反应①②可知,条件不同,乙醇与O2反应的产物不同
B.由反应②可知,Cu是乙醇氧化生成乙醛的催化剂
C.由反应①可知,乙醇燃烧时,碳碳键、碳氢键均断裂
D.由反应②可知,乙醇氧化为乙醛时,只断开氢氧键
D
【解析】由①可知,乙醇在氧气中燃烧生成CO2和H2O,由②可知乙醇与O2在铜作催化剂的条件下反应生成CH3CHO和H2O,条件不同,乙醇与O2反应的产物不同,A正确;由②可知,Cu参与反应,但在反应前后质量和化学性质不变,是催化剂,B正确;由①可知,乙醇燃烧时,碳碳键、碳氢键均断裂,C正确;由②可知,乙醇氧化为乙醛时,断开了氢氧键、碳氢键,D错误。
对应训练
【典例2】按照如图装置持续通入X气体或X蒸气,可以看到a处有红色
物质生成,b处变蓝,c处得到液体(假设每个反应均完全)。下列说法错
误的是( )
A.X可能为CH3CH2OH
B.盛放无水CuSO4固体的仪器是球形干燥管
C.硬质玻璃管中,X发生了氧化反应 D.X可能为NH3
D
【解析】CH3CH2OH与CuO在加热条件下反应:CH3CH2OH+CuO CH3CHO+Cu+H2O,与题干现象相符,A正确;根据实验仪器得到盛放无水CuSO4固体的仪器是球形干燥管,B正确;由实验现象推知CuO发生了还原反应,根据氧化还原反应原理得到X发生氧化反应,C正确2NH3+3CuO N2+3Cu+3H2O,但是实验后c处得不到液体,故D错误。
1.抗击新冠疫情,当前的重要工作是“外防输入,内防反弹”。
下列说法不正确的是( )
A.医用消毒酒精中乙醇的浓度为75%
B.“84”消毒液、二氧化氯泡腾片可用作环境消毒
C.大量喝酒可以预防“新型冠状病毒”
D.生产医用防护口罩的原料聚丙烯纤维属于有机高分子材料
C
【解析】医用消毒酒精中乙醇的浓度为75%,A正确;“84”消毒液中的次氯酸钠和二氧化氯都具有强氧化性,能杀菌消毒,B正确;喝酒对人体有害,与新型冠状病毒无关,且医用酒精消毒为体积分数为75%的酒精,喝的酒达不到这么高的浓度,不可以预防新型冠状病毒,C错误;聚丙烯纤维属于有机高分子材料,D正确;故选C。
2.下列说法正确的是( )
A.乙醇分子是由乙基和氢氧根组成的
B.乙醇是比水轻的液体,与水混合时浮在水面上
C.含乙醇99.5%以上的酒精叫做无水乙醇
D.乙醇可作为提取碘水中碘的萃取剂
C
【解析】乙醇分子可看作由乙基和羟基组成的,A错误;乙醇易溶于水,不能用于提取碘水中碘,B、D错;含乙醇99.5%以上的叫无水乙醇,C正确。
3.有机物在反应中常有原子间的共价键全部或部分断裂,下列
说法正确的是( )
A.与钠反应乙醇分子断裂C-H键
B.酯化反应中乙酸断裂O-H键
C.与氢气加成乙烯断裂C=C键中的一条键
D.催化氧化反应中乙醇断裂C-O键
C
【解析】A.乙醇与钠能反应是因为含有羟基,所以与钠反应乙醇分子断裂O-H键,A错误;B.酯化反应中羧酸脱去羟基,断裂C-O键,B错误;C.乙烯与氢气反应时,C=C双键中的π键断裂,与氢气发生加成反应,C正确;D.催化氧化反应中乙醇C-O键转化为C=O键,断裂的是O-H键、C-H键,D错误;综上所述答案为C。
4.可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法
是( )
A.1 mol C2H5OH 燃烧生成3 mol H2O B.乙醇可以制饮料
C.1 mol C2H5OH 跟足量的Na反应得0.5 mol H2
D.1 mol C2H5OH燃烧生成2 mol CO2
C
【解析】1mol乙醇燃烧所有的氢元素均生成水,不能证明乙醇分子中有一个氢原子与另外氢原子不同,A不选;乙醇制饮料的过程不发生化学反应,不能证明乙醇分子中氢原子不同,B不选;1mol乙醇跟足量的Na作用得0.5molH2,很明显乙醇中的6个氢只有一个能变为氢气,这个氢与其他氢不同,C选;1mol乙醇燃烧生成2molCO2即乙醇燃烧所有的氧元素均生成二氧化碳,但不能证明乙醇分子中有一个氢原子与另外氢原子不同,故D不选。
高中化学 人教版必修第二册
第七章 有机化合物
第三节 乙醇与乙酸
第1课时 乙醇
●
学习目标:
1.认识乙醇的结构及其主要性质与应用。
2.理解烃的衍生物、官能团的概念。
●
学习重点:
1.乙醇的结构与重要性质。
2.能设计简单实验方案探究乙醇发生反应的条件和反应方式。
●
学习难点:
分析乙醇及其反应的微观特征,能推测其他醇类的性质。
将进酒
君不见黄河之水天上来,奔流到海不复回。
君不见高堂明镜悲白发,朝如青丝暮成雪。
人生得意须尽欢,莫使金樽空对月。
天生我材必有用,千金散尽还复来。
烹羊宰牛且为乐,会须一饮三百杯。
岑夫子,丹丘生,将进酒,杯莫停。
与君歌一曲,请君为我倾耳听。
钟鼓馔玉不足贵,但愿长醉不愿醒。
古来圣贤皆寂寞,惟有饮者留其名。
陈王昔时宴平乐,斗酒十千恣欢谑。
主人何为言少钱,径须沽取对君酌。
五花马,千金裘,
呼儿将出换美酒,与尔同销万古愁。
酒与传统文化
酒文化博大精深,源远流长,早在几千年前,人类就掌握了发酵法酿酒的技术。
(以上均为体积分数)
医用酒精:含乙醇75%
工业酒精:含乙醇96%
无水酒精:含乙醇99.5%以上
无水乙醇的制备:
普通的工业酒精是含乙醇95.6%,用蒸馏的方法不能将乙醇中的水完全除去。(水和乙醇在95℃形成共沸物)
要制取无水乙醇,实验中可加入生石灰后再进行蒸馏。
可用无水硫酸铜检验乙醇中是否含水
探究课堂
探究课堂
以下说法或事实体现了乙醇哪些物理性质?
1.病人发烧通常用酒精擦拭全身,用此法降温。
2.衣服上沾上少许汽油用酒精可以去除。
3.酒香不怕巷子深。
4.白酒的主要成分是乙醇和水。
5.酒精灯用完后为什么要盖上灯帽
6.用酒泡中药(药酒)—如泡枸杞
(易挥发)
(易挥发、有特殊香味)
(乙醇易溶于水)
(易挥发)
(良好的有机溶剂)
(良好的有机溶剂)
你在生活中还有那些地方用到了酒精,体现了乙醇哪些物理性质?
1.1
乙醇的物理性质
与水形成分子间氢键,增大水溶性,不可萃取水中溶质或直接蒸馏制备无水乙醇。
俗称 颜色 气味 沸点 状态 密度 溶解性
酒精
无色透明
特殊
香味
液体
ρ<ρ水
易
挥发
能溶解多种有机物和无机物,能跟水以任意比例互溶
对应训练
【典例1】有关乙醇的说法不正确的是( )
A.乙醇溶于水
B.乙醇易挥发
C.医用酒精含乙醇体积分数95%
D.用工业酒精与生石灰通过加热蒸馏的方法制无水酒精
C
【解析】A.乙醇与水分子间能形成氢键,所以乙醇易溶于水,A正确;B.乙醇的沸点低,具有较强的挥发性,B正确;C.医用酒精含乙醇体积分数为75%,95%的乙醇易使细菌表面的蛋白质变性,从而形成硬壳保护膜,不能杀死细菌,C不正确;D.以工业酒精为原料制取无水酒精时,常与生石灰混合,使水与生石灰反应,然后加热蒸馏,D正确;故选C。
对应训练
【典例2】下列有关乙醇的物理性质的应用中,不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药
的有效成分
C.由于乙醇能够以任意比溶于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有“酒香不怕巷子深”的说法
A
【解析】由于乙醇与水互溶,故不能用分液的方法除去乙醇中的水。A项不正确;乙醇提取中草药的有效成分是利用了有机物易溶于乙醇的原理,B项正确;乙醇与水能够以任意比互溶,C项正确;乙醇是一种具有特殊香味、易挥发性的液体,D项正确。故答案选A。
分子式:
H H
H―C―C―O―H
H H
结构式:
结构简式:
CH3CH2OH或C2H5OH
C2H6O
电子式:
空间填充模型
键线式:
1.2
乙醇的结构
-OH 与OH- 有何区别?
探究课堂
羟基(-OH ) 氢氧根(OH- )
电子式
电子数
电荷数
稳定程度
存在形式
相同点 不显电性
带一个单位的负电荷
不能独立存在
能独立存在
组成元素相同
9e
10e
不稳定
较稳定
观察与思考
仔细观察下面两种物质,并比较它们的不同?
H
H
H
C
H
H
C
H
乙烷
乙醇
H
H
O
H
C
H
H
C
H
烷烃
烃的衍生物
探究课堂
1.3
烃的衍生物
1.定义:烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称烃的衍生物。如CH3CH2OH、CH3Cl、CH3CH2Br等,其中CH3CH2OH含有氧元素,又叫烃的含氧衍生物。
2.官能团
(1)定义:决定有机化合物_____的原子或原子团。
(2)实例
特性
物质 CH3Cl CH3CH2OH CH2=CH2 CH≡CH
所含官 能团 _____ _____ —C≡C—
官能团的 名称 氯原子 _____ _________ ________
—Cl
—OH
羟基
碳碳双键
碳碳三键
对应训练
【典例1】下列有关乙醇的说法正确的是( )
A.乙醇的结构简式为C2H6O
B.乙醇分子中含有OH-
C.乙醇分子中有2个甲基
D.乙醇中含有官能团羟基
【解析】A.乙醇的结构简式为C2H5OH,故A错误;B.乙醇分子中含有羟基-OH,故B错误;C.乙醇分子的结构简式是CH3CH2OH,分子中有1个甲基,故C错误;D.乙醇结构简式是C2H5OH、二甲醚结构简式是CH3OCH3,分子式相同、结构不同,互为同分异构体,故D正确;选D。
D
对应训练
C
【典例2】下列表示物质结构的化学用语正确的是( )
A.空间充填模型 可以表示甲烷分子,也可以表示四氯化碳分子
B.乙烯C2H4的结构简式:CH2CH2
C.乙醇的结构式是: D.NH3的电子式:
【解析】A.氢原子的原子半径小于碳原子,但氯原子的原子半径大于碳原子,则该空间充填模型可以表示甲烷分子,不可以表示四氯化碳分子,故A错误;B.乙烯的分子式为C2H4,结构简式为CH2=CH2,故B错误;C.乙醇的结构简式为CH3CH2OH,结构式为该结构,故C正确;D.氨气是共价化合物,电子式为 ,故D错误;故选C。
1. 乙醇与钠的反应
实验操作
实验现象
实验结论
①钠开始沉于试管底部,最终慢慢消失,产生无色无味气体;
②烧杯内壁有水珠产生;
③向烧杯中加入澄清石灰水不变浑浊
乙醇与钠反应生成氢气,
化学方程式为2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑
2.1
乙醇的物理性质
乙醇的化学性质原理探析
学生活动1:对比钠与乙醇、水反应的比较实验现象,你能得出什么结
论?填写表格内容。
探究课堂
水与钠反应 乙醇与钠反应
钠的变化
声的现象
气体检验
实验结论
钠粒浮于水面,熔成闪亮的小球,并快速地四处游动,很快消失
钠粒开始沉于试管底部,未熔化,最终慢慢消失
无声响
有“嘶嘶”声响
点燃,发出淡蓝色的火焰
点燃,发出淡蓝色的火焰
钠的密度小于水,熔点低。钠与水剧烈反应,生成氢气。水分子中—OH上的氢原子比较活泼
钠的密度比乙醇的大。钠与乙醇缓慢反应生成氢气。乙醇中羟基上的氢原子相对不活泼
ρ水>ρ钠 > ρ乙醇
探究课堂
探究课堂
① 处O-H键断开
2CH3CH2—O—H +2Na →2CH3CH2ONa +H2↑
注意!
① 断O—H键,发生置换反应或取代反应
② 氢原子活泼性:酸______水______醇
③ 含有 OH的有机物都能与Na反应,如CH3OH等,且1mol OH ~ __________mol H2。
故此反应既可检验—OH的存在,又可用来计算分子中—OH的数目
④ CH3CH2OH是非电解质,不能电离出H+,故不能与碱溶液反应。
>
>
0.5
实验室和生活中酒精的最常见的用途是用作燃料
2CO2 +3H2O
C2H5OH + 3O2
点燃
现象:产生淡蓝色火焰,同时放出大量热。
2. 氧化反应
(1)乙醇燃烧
高温焊接银器或铜器时,表面会生成黑色的氧化物,师傅说:把铜或银器具趁热蘸一下酒精,铜或银会光亮如初!这是为什么呢?
探究课堂
实验操作
实验现象
实验结论
(2)乙醇的催化氧化反应
红色的铜丝 变为黑色 变为红色,闻到刺激性气味
2CH3CH2OH+O2 2CH3CHO+2H2O
乙醇被氧化为乙醛,化学方程式为
Cu/Ag
△
实验探究
【实验7-5】
探究课堂
铜丝红
Δ
变黑
有刺激性气味
插入乙醇溶液中
又变红
Cu
Δ
CuO
乙醛CH3CHO
插入乙醇溶液中
Cu
分析:发生反应 2Cu+O2==2CuO
分析:生成新的物质—乙醛
CuO+CH3CH2OH Cu +CH3CHO+H2O
催化剂
现象及原因探究:
中间产物
探究课堂
②断键机理:
反应历程
2Cu + O2 == 2CuO
C2H5OH+ CuO CH3CHO+ H2O+ Cu
总反应:
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu或Ag
乙醛
2 2 2 2 2
脱去2个H与1个O结合成H2O
2 CH3-C-O-H + O2 2CH3-C-H + 2H2O
H
H
Cu / Ag
O
=
可见,实际起氧化作用的是CuO ,Cu是催化剂
醛基
—CHO
—C—H
O
—COH
探究课堂
Cu
乙醇
乙醛
氧原子
水
H—C—C—O
H
H
H
氢原子
碳原子
探究课堂
-----
-----
① 处O-H键断开
③处C-H键断开
原理分析:
乙醇在被催化氧化时,①③键发生断裂,即乙醇催化氧化反应的实质是脱去与羟基相连的碳原子上的氢原子和羟基上的氢原子,这两个氢原子与氧原子结合形成H2O,若醇分子中与羟基相连的碳原子上无氢原子,则不能被催化氧化。
H
H
O
H
C
H
H
C
H
α
β
CH3
H
O
C
CH3
CH3
H
C
H
α
β
探究课堂
(2)乙醇的催化氧化反应
小结:醇被催化氧化的规律
规律:乙醇催化氧化反应的断键方式可知,醇在有催化剂(铜或银)存在的条件下,可以发生催化氧化反应生成醛,但并不是所有的醇都能被氧化生成醛。
①凡是含有R—CH2OH(R代表烃基)结构的醇,催化氧化成醛:
2R—CH2OH+O2 2R—CHO+2H2O
②凡是含有 结构的醇,在一定条件下也能被催化氧化,但生成物不是醛,而是酮( )
③凡是羟基所连C原子上没有H原子的醇通常情况下不能被催化氧化。
【结论】与—OH相连碳原子上有氢原子的醇才能被催化氧化。
探究课堂
对应训练
【典例1】下列能说明乙醇分子中有一个氢原子与其他氢原子不同的是
( )
A.乙醇能燃烧
B.1molCH3CH2OH与Na完全反应只生成0.5molH2
C.乙醇分子中含有一个氧原子
D.乙醇能溶于水
C
【解析】A项,乙醇燃烧时,所有的氢原子均参与反应生成H2O;B项无法证明题中结论;D项,乙醇氧化成乙醛时,O—H及C—H均参与反应,也无法证明氢原子的不同;C项乙醇与足量钠反应,参与反应的氢原子占醇分子中氢原子的六分之一,说明其中一个氢原子与另外五个不同。
对应训练
【典例2】下列方法中可以证明乙醇分子中有一个氢原子与其他氢原子
不同的是( )
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以制饮料
C.1 mol乙醇与足量的Na作用得0.5 mol H2
D.1 mol乙醇可生成1 mol乙醛
C
【解析】A项,乙醇燃烧时,所有的氢原子均参与反应生成H2O;B项无法证明题中结论;D项,乙醇氧化成乙醛时,O—H及C—H均参与反应,也无法证明氢原子的不同;C项乙醇与足量钠反应,参与反应的氢原子占醇分子中氢原子的六分之一,说明其中一个氢原子与另外五个不同。
反应原理:CH3CH2OH CH3COOH。
KMnO4(紫色)
MnSO4
(无色)
Cr2(SO4)3
硫酸铬 (绿色)
K2Cr2O7
重铬酸钾(橙色)
(3)乙醇与强氧化剂的反应
5CH3CH2OH + 4MnO4- + 12H+ → 5CH3COOH + 4Mn2+ + 11H2O
2Cr2O72-+3CH3CH2OH+16H+ → 4Cr3++3CH3COOH+11H2O
探究课堂
交通警察检查司机是否酒后驾车的装置中,含有橙色的酸性重铬酸钾,当其遇到乙醇时橙色变为绿色,由此可以判断司机是否酒后驾车。
资料卡片
探究课堂
探究课堂
乙醇在人体内究竟发生了哪些化学变化 喝酒上脸的人真能喝吗?“喝酒脸红不伤肝,喝酒脸白才伤肝”是真的吗?为何女性更容易喝醉?究竟谁才是真正的酒神?
生活解密
探究课堂
生活解密
2.3
乙醇的用途
用作燃料
工业
乙醇溶剂
重要的化工原料和溶剂
用作消毒剂
酒精饮料
探究课堂
课堂小结
乙醇
分子组成和结构
用途
分子式
结构式
官能团
C2H6O
—OH
燃料
化工原料
医用消毒剂
物理性质
无色、有特殊香味的液体
密度小于水
易溶于水和有机溶剂
沸点较低,易挥发
化学性质
与强氧化剂反应
氧化反应
置换反应
使酸性高锰酸钾溶液褪色
与羟基相连的碳上必须有氢原子
淡蓝色火焰
乙醇与钠反应
催化氧应
燃烧
对应训练
【典例1】乙醇能发生如下反应:①CH3CH2OH+3O2 2CO2+3H2O;
②2Cu+O2 2CuO,CH3CH2OH+CuO CH3CHO+H2O+Cu。
由以上反应不能得出的结论是( )
A.由反应①②可知,条件不同,乙醇与O2反应的产物不同
B.由反应②可知,Cu是乙醇氧化生成乙醛的催化剂
C.由反应①可知,乙醇燃烧时,碳碳键、碳氢键均断裂
D.由反应②可知,乙醇氧化为乙醛时,只断开氢氧键
D
【解析】由①可知,乙醇在氧气中燃烧生成CO2和H2O,由②可知乙醇与O2在铜作催化剂的条件下反应生成CH3CHO和H2O,条件不同,乙醇与O2反应的产物不同,A正确;由②可知,Cu参与反应,但在反应前后质量和化学性质不变,是催化剂,B正确;由①可知,乙醇燃烧时,碳碳键、碳氢键均断裂,C正确;由②可知,乙醇氧化为乙醛时,断开了氢氧键、碳氢键,D错误。
对应训练
【典例2】按照如图装置持续通入X气体或X蒸气,可以看到a处有红色
物质生成,b处变蓝,c处得到液体(假设每个反应均完全)。下列说法错
误的是( )
A.X可能为CH3CH2OH
B.盛放无水CuSO4固体的仪器是球形干燥管
C.硬质玻璃管中,X发生了氧化反应 D.X可能为NH3
D
【解析】CH3CH2OH与CuO在加热条件下反应:CH3CH2OH+CuO CH3CHO+Cu+H2O,与题干现象相符,A正确;根据实验仪器得到盛放无水CuSO4固体的仪器是球形干燥管,B正确;由实验现象推知CuO发生了还原反应,根据氧化还原反应原理得到X发生氧化反应,C正确2NH3+3CuO N2+3Cu+3H2O,但是实验后c处得不到液体,故D错误。
1.抗击新冠疫情,当前的重要工作是“外防输入,内防反弹”。
下列说法不正确的是( )
A.医用消毒酒精中乙醇的浓度为75%
B.“84”消毒液、二氧化氯泡腾片可用作环境消毒
C.大量喝酒可以预防“新型冠状病毒”
D.生产医用防护口罩的原料聚丙烯纤维属于有机高分子材料
C
【解析】医用消毒酒精中乙醇的浓度为75%,A正确;“84”消毒液中的次氯酸钠和二氧化氯都具有强氧化性,能杀菌消毒,B正确;喝酒对人体有害,与新型冠状病毒无关,且医用酒精消毒为体积分数为75%的酒精,喝的酒达不到这么高的浓度,不可以预防新型冠状病毒,C错误;聚丙烯纤维属于有机高分子材料,D正确;故选C。
2.下列说法正确的是( )
A.乙醇分子是由乙基和氢氧根组成的
B.乙醇是比水轻的液体,与水混合时浮在水面上
C.含乙醇99.5%以上的酒精叫做无水乙醇
D.乙醇可作为提取碘水中碘的萃取剂
C
【解析】乙醇分子可看作由乙基和羟基组成的,A错误;乙醇易溶于水,不能用于提取碘水中碘,B、D错;含乙醇99.5%以上的叫无水乙醇,C正确。
3.有机物在反应中常有原子间的共价键全部或部分断裂,下列
说法正确的是( )
A.与钠反应乙醇分子断裂C-H键
B.酯化反应中乙酸断裂O-H键
C.与氢气加成乙烯断裂C=C键中的一条键
D.催化氧化反应中乙醇断裂C-O键
C
【解析】A.乙醇与钠能反应是因为含有羟基,所以与钠反应乙醇分子断裂O-H键,A错误;B.酯化反应中羧酸脱去羟基,断裂C-O键,B错误;C.乙烯与氢气反应时,C=C双键中的π键断裂,与氢气发生加成反应,C正确;D.催化氧化反应中乙醇C-O键转化为C=O键,断裂的是O-H键、C-H键,D错误;综上所述答案为C。
4.可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法
是( )
A.1 mol C2H5OH 燃烧生成3 mol H2O B.乙醇可以制饮料
C.1 mol C2H5OH 跟足量的Na反应得0.5 mol H2
D.1 mol C2H5OH燃烧生成2 mol CO2
C
【解析】1mol乙醇燃烧所有的氢元素均生成水,不能证明乙醇分子中有一个氢原子与另外氢原子不同,A不选;乙醇制饮料的过程不发生化学反应,不能证明乙醇分子中氢原子不同,B不选;1mol乙醇跟足量的Na作用得0.5molH2,很明显乙醇中的6个氢只有一个能变为氢气,这个氢与其他氢不同,C选;1mol乙醇燃烧生成2molCO2即乙醇燃烧所有的氧元素均生成二氧化碳,但不能证明乙醇分子中有一个氢原子与另外氢原子不同,故D不选。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
