8.1.1自然资源的开发利用【第一课时】金属资源的开发利用(共20张PPT)
文档属性
| 名称 | 8.1.1自然资源的开发利用【第一课时】金属资源的开发利用(共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 20.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-02 00:00:00 | ||
图片预览






文档简介
(共20张PPT)
金属矿物的开发利用
不同金属的冶炼方法
为什么铝元素在地壳中含量比铜铁元素多得多,为什么却到大约两百年前才开始广泛使用,远在铜器铁器时代之后呢?
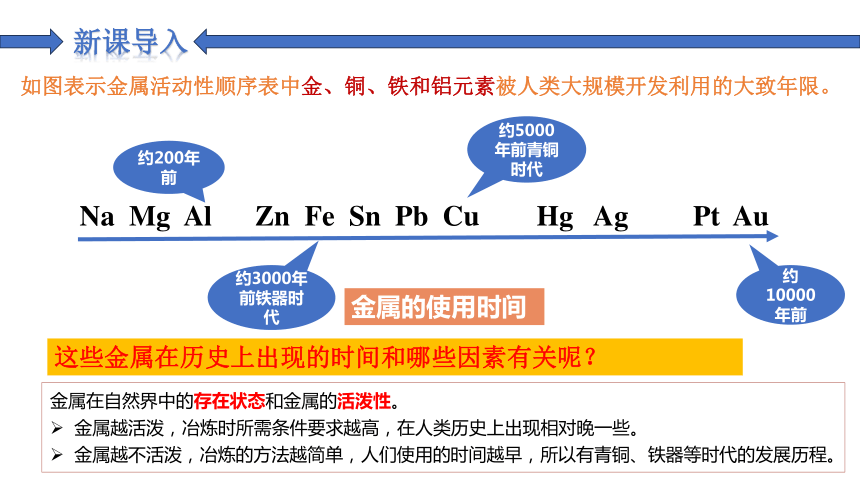
金属的使用时间
Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
约200年前
约3000年前铁器时代
约5000年前青铜时代
约10000年前
金属在自然界中的存在状态和金属的活泼性。
金属越活泼,冶炼时所需条件要求越高,在人类历史上出现相对晚一些。
金属越不活泼,冶炼的方法越简单,人们使用的时间越早,所以有青铜、铁器等时代的发展历程。
如图表示金属活动性顺序表中金、铜、铁和铝元素被人类大规模开发利用的大致年限。
这些金属在历史上出现的时间和哪些因素有关呢?
一、金属元素在自然界的存在形式
· 自然界的金属单质
金Au
银Ag
铜Cu
陨铁Fe
除了金、铂等极少数金属,绝大多数金属元素以化合物的形式存在于自然界。
一、金属元素在自然界的存在形式
· 自然界的金属化合物
蓝铜矿Cu2(OH)2CO3
黄铜矿CuFeS2
黄铁矿FeS2
铝土矿Al2O3
那么,如何从金属矿石中得到我们想要的金属呢?
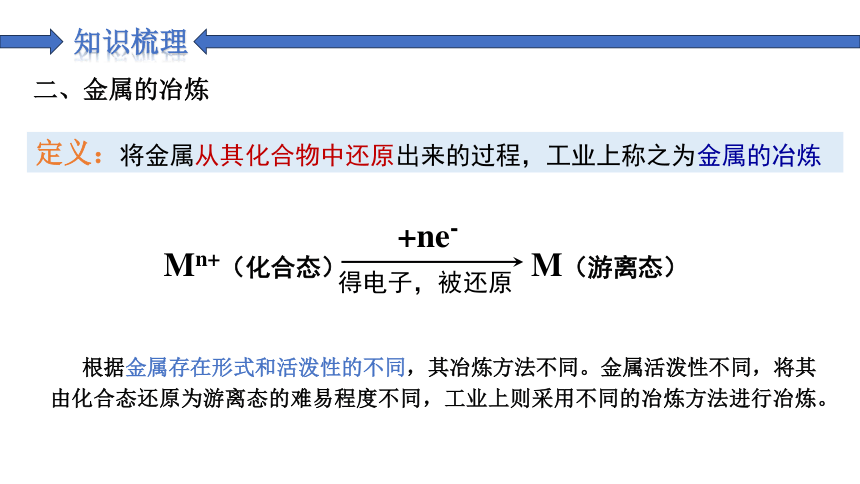
将金属从其化合物中还原出来的过程,工业上称之为金属的冶炼
得电子,被还原
Mn+(化合态) M(游离态)
+ne-
二、金属的冶炼
根据金属存在形式和活泼性的不同,其冶炼方法不同。金属活泼性不同,将其由化合态还原为游离态的难易程度不同,工业上则采用不同的冶炼方法进行冶炼。
定义:
二、金属的冶炼
1、物理方法
富集法
适用范围:很不活泼的金属,如Au、Pt
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
淘金,指淘金者们打捞起河里或湖里的淤泥后,在淘盘将淤泥洗涤,以便找出淤泥里的天然金沙。
《浪淘沙》-刘禹锡
千淘万漉虽辛苦,吹尽狂沙始到金。
美人首饰侯王印,尽是沙中浪底来。
淘金原理:金的密度比沙大
二、金属的冶炼
2、化学方法
热分解法
适用范围:不活泼的金属,如Hg、Ag
2HgO 2Hg + O2 ↑
2Ag2O 4Ag + O2 ↑
凡草木烧之即尽,而丹砂烧之成水银,积变又还成丹砂。
HgS Hg + S
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
二、金属的冶炼
3、化学方法
热还原法
适用范围:中等活泼的金属,如Zn、Fe、Sn、Pb、Cu
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
常见还原剂:焦炭、CO、H2、活泼金属Al等
如:高炉炼铁
Fe2O3+3CO === 2Fe + 3CO2
高温
CuO+H2 === Cu + H2O
高温
CuO+ CO Cu + CO2
2CuO+ C 2Cu + CO2
二、金属的冶炼
3、化学方法
热还原法——铝热法
用两张圆形滤纸制成纸漏斗,在纸漏斗中倒入氧化铁粉末,再倒入铝粉,将两者混合均匀, 架上铁圈,下面放置盛沙的蒸发皿,把混合物放在纸漏斗中,上面加少量氯酸钾,并在混合物中间插一根打磨过的镁条, 点燃镁条,观察发生的现象。
二、金属的冶炼
3、化学方法
热还原法——铝热法
实验现象:
1、镁条剧烈燃烧,发出耀眼白光
2、漏斗内剧烈反应,放出大量的热,火星四射
3、纸漏斗的下部被烧穿,有红热熔融物落入沙中,冷却后变为黑色固体
实验原理:
点燃镁条,促使氯酸钾分解,释放出氧气,使镁条更剧烈燃烧,单位时间内放出更多热量,从而引发Al和Fe2O3发生反应。
引燃剂
助燃剂
还原剂
氧化剂
用 途:
野外焊接铁轨,冶炼高熔点,且活动性比铝差的金属,如: Cu、Fe、V、Cr、Mn等
2Al+Fe2O3 2Fe+Al2O3
二、金属的冶炼
4、化学方法
电解法
适用范围:活泼金属,如K Ga Na Mg Al
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
MgCl2 (熔融) === Mg + Cl2 ↑
电解
2Al2O3 (熔融) === 4Al + 3O2 ↑
电解
冰晶石
2NaCl (熔融) === 2Na + Cl2 ↑
电解
助熔剂,可以降低氧化铝的熔化所需的温度
注意点:
①条件是“熔融”
②必须是离子化合物,共价化合物熔融不导电,所以不能用氯化铝AlCl3进行冶炼。
二、金属的冶炼
5、化学方法
其他特殊冶炼方法
同一种金属可能有不同的冶炼方法,可根据原料、生产设备、金属的用途等来确定,如Cu可采用热还原法、湿法冶炼、火法炼铜。
(1)湿法冶金:利用溶液中发生的化学反应,对原料中的金属进行分离和提取的方法,如湿法炼铜:
Fe+CuSO4 = FeSO4 + Cu
(2)火法炼铜:
Cu2S+O2 === 2Cu + SO2
高温
在汉代许多著作里有记载“石胆能化铁为铜”,晋葛洪《抱朴子内篇·黄白》中也有“以曾青涂铁,铁赤色如铜”的记载。
二、金属的冶炼
为什么要合理开发和利用金属矿物资源?
原 因:
措 施:
资源有限且分布不均;
金属的冶炼消耗许多能量;
金属冶炼造成环境污染;
金属腐蚀造成大量损失
提高金属矿物的利用率;
使用其他材料代替金属材料;
加强废旧金属的回收和再利用;
开发环保高效的金属冶炼方法;
防止金属的腐蚀
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
热还原法
富集法
热分解法
电解法
2.下列反应中,可通过置换反应得到铁的是( )
A.铝粉末和氧化铁粉末混合并加热至高温反应
B.一氧化碳通过炽热的氧化铁
C. 溶液加锌粉
D. 溶液中加金属钠
1.下列金属中,工业上常采用热还原法冶炼的是( )
A.Al B.Fe C.Hg D.Ag
B
A
3.“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景在《本草经集注》中提到“钢铁是杂炼生鍒作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约0.1%)混合加热,生铁熔化灌入熟铁,再锻打成钢,下列说法错误的是( )
A.钢是以铁为主的含碳合金
B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比纯铁高
D.冶炼铁的原料之一赤铁矿的主要成分为Fe2O3,俗称铁红
C
4.化学兴趣小组用如图所示装置制备铁,下列说法正确的是( )
A. KClO3作为引燃剂,也可用Na2O代替
B.仪器a可以用装有蒸馏水的烧杯代替
C.工业上常利用铝热反应来冶炼熔点较高的钒、铬、锰
D.常温下,反应后a中的金属可以用浓硝酸洗涤干净
C
金属矿物的开发利用
不同金属的冶炼方法
为什么铝元素在地壳中含量比铜铁元素多得多,为什么却到大约两百年前才开始广泛使用,远在铜器铁器时代之后呢?
金属的使用时间
Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
约200年前
约3000年前铁器时代
约5000年前青铜时代
约10000年前
金属在自然界中的存在状态和金属的活泼性。
金属越活泼,冶炼时所需条件要求越高,在人类历史上出现相对晚一些。
金属越不活泼,冶炼的方法越简单,人们使用的时间越早,所以有青铜、铁器等时代的发展历程。
如图表示金属活动性顺序表中金、铜、铁和铝元素被人类大规模开发利用的大致年限。
这些金属在历史上出现的时间和哪些因素有关呢?
一、金属元素在自然界的存在形式
· 自然界的金属单质
金Au
银Ag
铜Cu
陨铁Fe
除了金、铂等极少数金属,绝大多数金属元素以化合物的形式存在于自然界。
一、金属元素在自然界的存在形式
· 自然界的金属化合物
蓝铜矿Cu2(OH)2CO3
黄铜矿CuFeS2
黄铁矿FeS2
铝土矿Al2O3
那么,如何从金属矿石中得到我们想要的金属呢?
将金属从其化合物中还原出来的过程,工业上称之为金属的冶炼
得电子,被还原
Mn+(化合态) M(游离态)
+ne-
二、金属的冶炼
根据金属存在形式和活泼性的不同,其冶炼方法不同。金属活泼性不同,将其由化合态还原为游离态的难易程度不同,工业上则采用不同的冶炼方法进行冶炼。
定义:
二、金属的冶炼
1、物理方法
富集法
适用范围:很不活泼的金属,如Au、Pt
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
淘金,指淘金者们打捞起河里或湖里的淤泥后,在淘盘将淤泥洗涤,以便找出淤泥里的天然金沙。
《浪淘沙》-刘禹锡
千淘万漉虽辛苦,吹尽狂沙始到金。
美人首饰侯王印,尽是沙中浪底来。
淘金原理:金的密度比沙大
二、金属的冶炼
2、化学方法
热分解法
适用范围:不活泼的金属,如Hg、Ag
2HgO 2Hg + O2 ↑
2Ag2O 4Ag + O2 ↑
凡草木烧之即尽,而丹砂烧之成水银,积变又还成丹砂。
HgS Hg + S
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
二、金属的冶炼
3、化学方法
热还原法
适用范围:中等活泼的金属,如Zn、Fe、Sn、Pb、Cu
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
常见还原剂:焦炭、CO、H2、活泼金属Al等
如:高炉炼铁
Fe2O3+3CO === 2Fe + 3CO2
高温
CuO+H2 === Cu + H2O
高温
CuO+ CO Cu + CO2
2CuO+ C 2Cu + CO2
二、金属的冶炼
3、化学方法
热还原法——铝热法
用两张圆形滤纸制成纸漏斗,在纸漏斗中倒入氧化铁粉末,再倒入铝粉,将两者混合均匀, 架上铁圈,下面放置盛沙的蒸发皿,把混合物放在纸漏斗中,上面加少量氯酸钾,并在混合物中间插一根打磨过的镁条, 点燃镁条,观察发生的现象。
二、金属的冶炼
3、化学方法
热还原法——铝热法
实验现象:
1、镁条剧烈燃烧,发出耀眼白光
2、漏斗内剧烈反应,放出大量的热,火星四射
3、纸漏斗的下部被烧穿,有红热熔融物落入沙中,冷却后变为黑色固体
实验原理:
点燃镁条,促使氯酸钾分解,释放出氧气,使镁条更剧烈燃烧,单位时间内放出更多热量,从而引发Al和Fe2O3发生反应。
引燃剂
助燃剂
还原剂
氧化剂
用 途:
野外焊接铁轨,冶炼高熔点,且活动性比铝差的金属,如: Cu、Fe、V、Cr、Mn等
2Al+Fe2O3 2Fe+Al2O3
二、金属的冶炼
4、化学方法
电解法
适用范围:活泼金属,如K Ga Na Mg Al
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
MgCl2 (熔融) === Mg + Cl2 ↑
电解
2Al2O3 (熔融) === 4Al + 3O2 ↑
电解
冰晶石
2NaCl (熔融) === 2Na + Cl2 ↑
电解
助熔剂,可以降低氧化铝的熔化所需的温度
注意点:
①条件是“熔融”
②必须是离子化合物,共价化合物熔融不导电,所以不能用氯化铝AlCl3进行冶炼。
二、金属的冶炼
5、化学方法
其他特殊冶炼方法
同一种金属可能有不同的冶炼方法,可根据原料、生产设备、金属的用途等来确定,如Cu可采用热还原法、湿法冶炼、火法炼铜。
(1)湿法冶金:利用溶液中发生的化学反应,对原料中的金属进行分离和提取的方法,如湿法炼铜:
Fe+CuSO4 = FeSO4 + Cu
(2)火法炼铜:
Cu2S+O2 === 2Cu + SO2
高温
在汉代许多著作里有记载“石胆能化铁为铜”,晋葛洪《抱朴子内篇·黄白》中也有“以曾青涂铁,铁赤色如铜”的记载。
二、金属的冶炼
为什么要合理开发和利用金属矿物资源?
原 因:
措 施:
资源有限且分布不均;
金属的冶炼消耗许多能量;
金属冶炼造成环境污染;
金属腐蚀造成大量损失
提高金属矿物的利用率;
使用其他材料代替金属材料;
加强废旧金属的回收和再利用;
开发环保高效的金属冶炼方法;
防止金属的腐蚀
K Ga Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au
热还原法
富集法
热分解法
电解法
2.下列反应中,可通过置换反应得到铁的是( )
A.铝粉末和氧化铁粉末混合并加热至高温反应
B.一氧化碳通过炽热的氧化铁
C. 溶液加锌粉
D. 溶液中加金属钠
1.下列金属中,工业上常采用热还原法冶炼的是( )
A.Al B.Fe C.Hg D.Ag
B
A
3.“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景在《本草经集注》中提到“钢铁是杂炼生鍒作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约0.1%)混合加热,生铁熔化灌入熟铁,再锻打成钢,下列说法错误的是( )
A.钢是以铁为主的含碳合金
B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比纯铁高
D.冶炼铁的原料之一赤铁矿的主要成分为Fe2O3,俗称铁红
C
4.化学兴趣小组用如图所示装置制备铁,下列说法正确的是( )
A. KClO3作为引燃剂,也可用Na2O代替
B.仪器a可以用装有蒸馏水的烧杯代替
C.工业上常利用铝热反应来冶炼熔点较高的钒、铬、锰
D.常温下,反应后a中的金属可以用浓硝酸洗涤干净
C
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
