第一节 原子的构成课时2 原子中的电子课件(共23张PPT内嵌视频)
文档属性
| 名称 | 第一节 原子的构成课时2 原子中的电子课件(共23张PPT内嵌视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-01 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
第一节 原子的构成
课时2 原子中的电子
学习目标
1.认识核外电子的排布特点,会根据原子结构示意图判断原子的化学性质。
2.了解离子的形成过程,会识别常见粒子的结构示意图。
情景导入
原子核外的电子是如何运动的?
一、原子中的电子
(1)高速运动
(2)无规则运动
(3)分层运动
普通氢原子核外只有一个电子,这一电子围绕氢的原子核在核外的“巨大”空间里高速运动。在具有多个电子的原子中,电子是如何运动的呢?
通常情况下,氢原
子电子云示意图
学习探究
1.核外电子的分层排布
(2)电子层:科学家们将电子经常出现的区域称为电子层。离核最近的称为第一电子层,依次有第二、三、四、五、六、七电子层,离核最远的又称为___________。
(1)电子在原子核外是_________的,能量低的电子在离核较近的区域运动,能量高的电子在离核较远的区域运动。通常把电子在离核远近不同的区域运动称为电子的分层排布。
分层运动
最外电子层
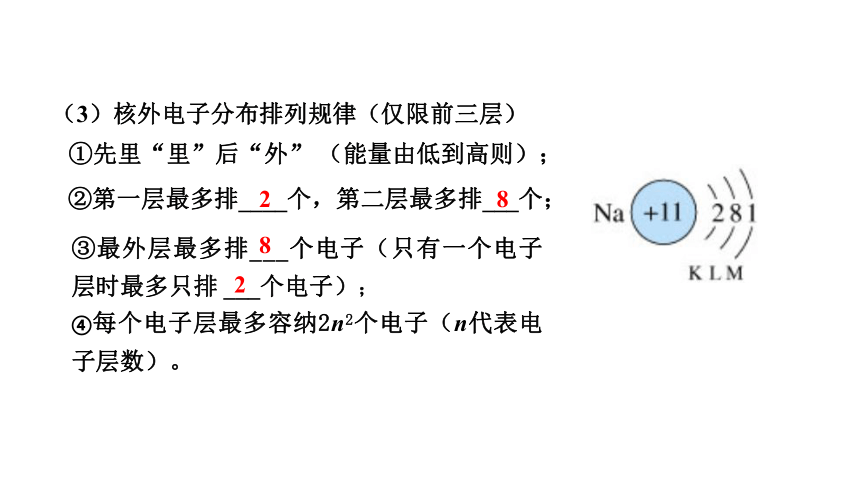
(3)核外电子分布排列规律(仅限前三层)
①先里“里”后“外” (能量由低到高则);
②第一层最多排____个,第二层最多排___个;
③最外层最多排___个电子(只有一个电子层时最多只排 ___个电子);
④每个电子层最多容纳2n2个电子(n代表电子层数)。
2
8
8
2
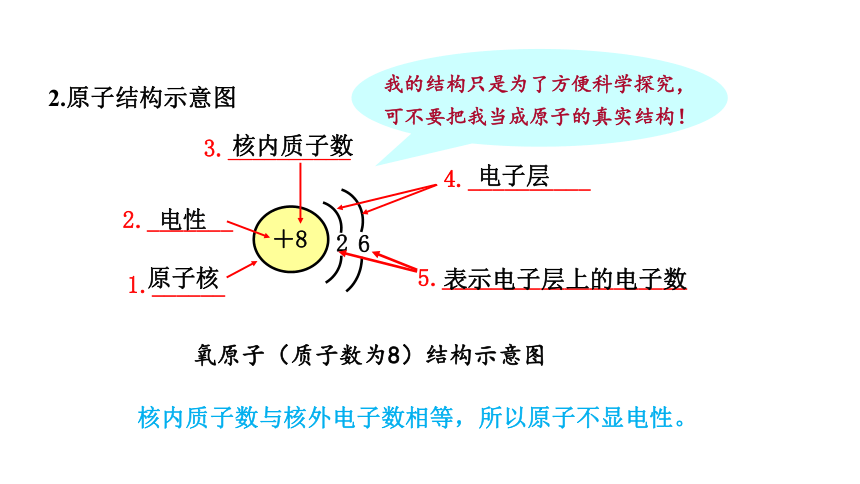
2.原子结构示意图
+8
2
6
氧原子(质子数为8)结构示意图
核内质子数与核外电子数相等,所以原子不显电性。
3.__________
4.__________
5.____________________
1.______
原子核
核内质子数
电子层
表示电子层上的电子数
我的结构只是为了方便科学探究,
可不要把我当成原子的真实结构!
2._______
电性
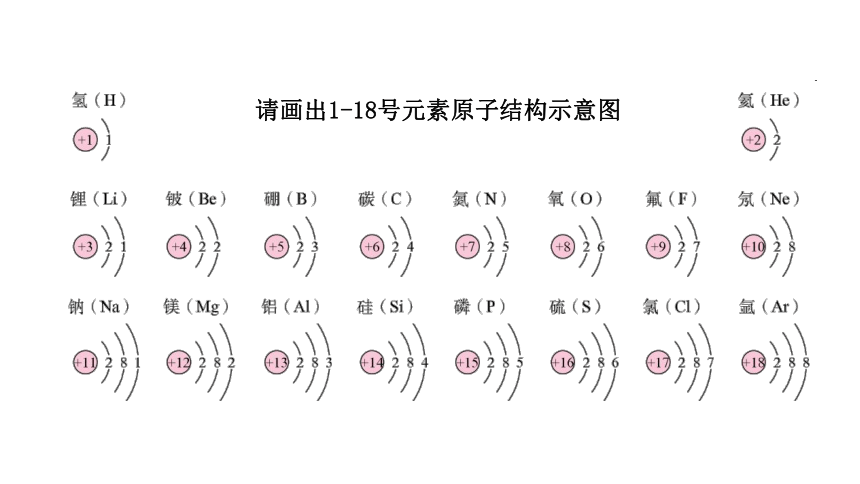
请画出1-18号元素原子结构示意图
元素的化学性质与原子核外电子的排布,特别是最外层电子数有密切关系。
3.元素的性质与原子最外层电子数的关系
原子的分类 最外层电子数 得失电子趋势 化学性质
稀有气体原子 8 个(氦是2个) ____________ ______________________
金属原子 一般小于4 __________ _______ ______________________
非金属原子 一般不少于4 __________
不易得失电子
易失去最外
层电子
易得电子
难发生化
学反应
容易发生
化学反应
(1)稀有气体一般不易与其他物质发生化学反应,原因是它们的原子最外层有8个(氦是2个)电子,这样的结构被认为是稳定结构。
(2)金属原子的最外层电子数一般小于4,在化学反应中易失去最外层电子,从而达到稳定结构。
(3)非金属原子的最外层电子数一般大于4,在化学反应中易得到电子,使最外层达到稳定结构。
4.原子的稳定结构
1.最外层电子数为8的结构是稳定结构,但达到稳定结构的原子最外层电子数不一定是8,如氦原子最外层电子数为2,也是稳定结构。
2.原子的化学性质与最外层电子数关系密切,但是最外层电子数相同的原子化学性质不一定相似,如氦与镁;化学性质相似的原子最外层电子数也不一定相同,如氦与氖。
例2 下列粒子的结构示意图,表示具有稳定结构的原子的是( )
例1 某原子结构示意图为 ,它的核电荷数和最外层电子数分别是( )
A.6和8 B.8 和6 C.8和2 D.6和2
B
解析:C的最外层电子数是8,具有稳定结构。
C
解析:钠原子的核外第一层有2个电子,A错误;钠原子的最外电子层有1个电子,在化学反应中容易失去这1个电子,B正确;钠原子核内质子数为11,中子数无法从原子结构示意图中获得,C错误;钠原子的核外有3层电子,D错误。
B
例3 如图为钠的原子结构示意图,从图中可获得的信息是( )
A.钠原子的核外第一层有1个电子
B.钠原子在化学反应中容易失去1个电子
C.钠原子核内的质子数为11,中子数为0
D.钠原子的核外有2层电子
B
B
根据原子的结构分析,氯化钠是怎样形成的?
情景导入
Na(钠原子)
8
+11
1
2
8
+17
7
2
Cl(氯原子)
钠 + 氯气 氯化钠
点燃
Na(钠原子)
NaCl
8
+11
1
2
8
+17
7
2
Cl(氯原子)
8
+17
8
2
8
+11
2
Na+
失一个电子
得一个电子
Cl-
1.离子
构成物质的一种基本粒子,如氯化钠等由离子构成。
二、离子
2.离子的形成
阳离子(带正电荷) 原子 阴离子(带负电荷)
失去电子 得到电子
3.离子的书写
2Mg2+
表示每个镁离子带2个单位的正电荷
表示2个镁离子
先写出元素符号,再在右上角标明该离子带的电荷数,注意“+”“-”紧跟在数字后面。
4.原子和离子的比较
项目 原 子 离 子
概念 化学变化中的最小粒子 带电荷的原子或原子团
电性 不显电性 带电
数量关系 核内质子数= 核外电子数 阳离子:核内质子数> 核外电子数
阴离子:核内质子数< 核外电子数
转化关系 都是构成物质的一种粒子
失电子
阴离子
得电子
原子
失电子
阳离子
得电子
5.分子、原子、离子及物质之间的联系
原
子
阴、阳离子
分子
物
质
构成
构成
直接构成
得失电子
构成
解析:铜由铜原子构成,二氧化碳由二氧化碳分子构成,氯化钠由钠离子和氯离子构成,金刚石由碳原子构成,故选C。
例1 下列物质由离子构成的是( )
A.铜 B.二氧化碳
C.氯化钠 D.金刚石
C
解析:①是氦原子,②是镁原子,③是镁离子,④是氖原子;②在反应中容易失电子;①③④都达到了相对稳定结构。
例2 如图所示是几种粒子的结构示意图,有关说法正确的是( )
A.①和②两种粒子的化学性质相似
B.③和④最外层电子数都是8,达到相对稳定结构,都是稀有气体的原子
C.粒子②在化学反应中容易失去电子
D.①②③④都达到了相对稳定结构
C
课堂小结
原子核外电子的排布
呈现形式
电子层
归纳
排布规律
金属原子
非金属原子
稀有气体原子
表示方法
原子结构示意图
决定因素
最外层电子数
离子
形成
得失电子
原子
定义
分类
表示方法
紧密联系
构成
物质
随 堂 测试
2. 某阳离子A3+的核外有23个电子,核内有30个中子,则该离子对应原子的核电荷数和相对原子质量分别为 ( )
A.23,53 B.26,30 C.26,56 D.23,46
C
1.下列结构示意图表示的微粒中,最易失去电子的是 ( )
A
3.某元素原子结构示意图如图,请回答:
(1)该原子核电荷数为______。
(2)图中x=______。
(3)该原子属于___________元素原子(填“金属”或“非金属”)。
(4)该原子在化学反应中容易_______(填“得”或“失”)电子。
4.下列是粒子的结构示意图,回答问题:
(1)B粒子核内有_______个质子。
(2)其中阳离子是______(填序号)。
(3)A、B、C、D四个粒子都具有
__________________________结构。
得
非金属
10
6
8
C
相对稳定
第一节 原子的构成
课时2 原子中的电子
学习目标
1.认识核外电子的排布特点,会根据原子结构示意图判断原子的化学性质。
2.了解离子的形成过程,会识别常见粒子的结构示意图。
情景导入
原子核外的电子是如何运动的?
一、原子中的电子
(1)高速运动
(2)无规则运动
(3)分层运动
普通氢原子核外只有一个电子,这一电子围绕氢的原子核在核外的“巨大”空间里高速运动。在具有多个电子的原子中,电子是如何运动的呢?
通常情况下,氢原
子电子云示意图
学习探究
1.核外电子的分层排布
(2)电子层:科学家们将电子经常出现的区域称为电子层。离核最近的称为第一电子层,依次有第二、三、四、五、六、七电子层,离核最远的又称为___________。
(1)电子在原子核外是_________的,能量低的电子在离核较近的区域运动,能量高的电子在离核较远的区域运动。通常把电子在离核远近不同的区域运动称为电子的分层排布。
分层运动
最外电子层
(3)核外电子分布排列规律(仅限前三层)
①先里“里”后“外” (能量由低到高则);
②第一层最多排____个,第二层最多排___个;
③最外层最多排___个电子(只有一个电子层时最多只排 ___个电子);
④每个电子层最多容纳2n2个电子(n代表电子层数)。
2
8
8
2
2.原子结构示意图
+8
2
6
氧原子(质子数为8)结构示意图
核内质子数与核外电子数相等,所以原子不显电性。
3.__________
4.__________
5.____________________
1.______
原子核
核内质子数
电子层
表示电子层上的电子数
我的结构只是为了方便科学探究,
可不要把我当成原子的真实结构!
2._______
电性
请画出1-18号元素原子结构示意图
元素的化学性质与原子核外电子的排布,特别是最外层电子数有密切关系。
3.元素的性质与原子最外层电子数的关系
原子的分类 最外层电子数 得失电子趋势 化学性质
稀有气体原子 8 个(氦是2个) ____________ ______________________
金属原子 一般小于4 __________ _______ ______________________
非金属原子 一般不少于4 __________
不易得失电子
易失去最外
层电子
易得电子
难发生化
学反应
容易发生
化学反应
(1)稀有气体一般不易与其他物质发生化学反应,原因是它们的原子最外层有8个(氦是2个)电子,这样的结构被认为是稳定结构。
(2)金属原子的最外层电子数一般小于4,在化学反应中易失去最外层电子,从而达到稳定结构。
(3)非金属原子的最外层电子数一般大于4,在化学反应中易得到电子,使最外层达到稳定结构。
4.原子的稳定结构
1.最外层电子数为8的结构是稳定结构,但达到稳定结构的原子最外层电子数不一定是8,如氦原子最外层电子数为2,也是稳定结构。
2.原子的化学性质与最外层电子数关系密切,但是最外层电子数相同的原子化学性质不一定相似,如氦与镁;化学性质相似的原子最外层电子数也不一定相同,如氦与氖。
例2 下列粒子的结构示意图,表示具有稳定结构的原子的是( )
例1 某原子结构示意图为 ,它的核电荷数和最外层电子数分别是( )
A.6和8 B.8 和6 C.8和2 D.6和2
B
解析:C的最外层电子数是8,具有稳定结构。
C
解析:钠原子的核外第一层有2个电子,A错误;钠原子的最外电子层有1个电子,在化学反应中容易失去这1个电子,B正确;钠原子核内质子数为11,中子数无法从原子结构示意图中获得,C错误;钠原子的核外有3层电子,D错误。
B
例3 如图为钠的原子结构示意图,从图中可获得的信息是( )
A.钠原子的核外第一层有1个电子
B.钠原子在化学反应中容易失去1个电子
C.钠原子核内的质子数为11,中子数为0
D.钠原子的核外有2层电子
B
B
根据原子的结构分析,氯化钠是怎样形成的?
情景导入
Na(钠原子)
8
+11
1
2
8
+17
7
2
Cl(氯原子)
钠 + 氯气 氯化钠
点燃
Na(钠原子)
NaCl
8
+11
1
2
8
+17
7
2
Cl(氯原子)
8
+17
8
2
8
+11
2
Na+
失一个电子
得一个电子
Cl-
1.离子
构成物质的一种基本粒子,如氯化钠等由离子构成。
二、离子
2.离子的形成
阳离子(带正电荷) 原子 阴离子(带负电荷)
失去电子 得到电子
3.离子的书写
2Mg2+
表示每个镁离子带2个单位的正电荷
表示2个镁离子
先写出元素符号,再在右上角标明该离子带的电荷数,注意“+”“-”紧跟在数字后面。
4.原子和离子的比较
项目 原 子 离 子
概念 化学变化中的最小粒子 带电荷的原子或原子团
电性 不显电性 带电
数量关系 核内质子数= 核外电子数 阳离子:核内质子数> 核外电子数
阴离子:核内质子数< 核外电子数
转化关系 都是构成物质的一种粒子
失电子
阴离子
得电子
原子
失电子
阳离子
得电子
5.分子、原子、离子及物质之间的联系
原
子
阴、阳离子
分子
物
质
构成
构成
直接构成
得失电子
构成
解析:铜由铜原子构成,二氧化碳由二氧化碳分子构成,氯化钠由钠离子和氯离子构成,金刚石由碳原子构成,故选C。
例1 下列物质由离子构成的是( )
A.铜 B.二氧化碳
C.氯化钠 D.金刚石
C
解析:①是氦原子,②是镁原子,③是镁离子,④是氖原子;②在反应中容易失电子;①③④都达到了相对稳定结构。
例2 如图所示是几种粒子的结构示意图,有关说法正确的是( )
A.①和②两种粒子的化学性质相似
B.③和④最外层电子数都是8,达到相对稳定结构,都是稀有气体的原子
C.粒子②在化学反应中容易失去电子
D.①②③④都达到了相对稳定结构
C
课堂小结
原子核外电子的排布
呈现形式
电子层
归纳
排布规律
金属原子
非金属原子
稀有气体原子
表示方法
原子结构示意图
决定因素
最外层电子数
离子
形成
得失电子
原子
定义
分类
表示方法
紧密联系
构成
物质
随 堂 测试
2. 某阳离子A3+的核外有23个电子,核内有30个中子,则该离子对应原子的核电荷数和相对原子质量分别为 ( )
A.23,53 B.26,30 C.26,56 D.23,46
C
1.下列结构示意图表示的微粒中,最易失去电子的是 ( )
A
3.某元素原子结构示意图如图,请回答:
(1)该原子核电荷数为______。
(2)图中x=______。
(3)该原子属于___________元素原子(填“金属”或“非金属”)。
(4)该原子在化学反应中容易_______(填“得”或“失”)电子。
4.下列是粒子的结构示意图,回答问题:
(1)B粒子核内有_______个质子。
(2)其中阳离子是______(填序号)。
(3)A、B、C、D四个粒子都具有
__________________________结构。
得
非金属
10
6
8
C
相对稳定
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
