山西省忻州市2023-2024学年高一下学期5月月考试题 化学(含答案)
文档属性
| 名称 | 山西省忻州市2023-2024学年高一下学期5月月考试题 化学(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 905.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-04 00:00:00 | ||
图片预览


文档简介
高一化学试题
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、隆位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容;人教版必修第二册第五章至第七章。
5.可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Cu 64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.鹊桥二号中继星已完成在轨对通测试,可为探月工程四期及后续国内外月球探测任务提供中继通信服务,下列说法正确的是
A.卫星上使用的太阳能电池的主要成分为
B.月壤中含有,和属于同种核素
C.长征八号遥三运载火箭使用的聚甲基丙烯酰亚胺(PMI)为高分子
D.长征八号运载火箭以液氢、液氧为推进剂,液氢燃烧时化学能全部转化为热能
2.下列化学用语表述正确的是
A.羧基的结构: B.果糖的分子式:
C.乙烷的空间填充模型; D.乙酸的结构式:
3.化学反应速率是用来表示化学反应过程进行快慢的物理量,下列措施能减慢反应速率的是
选项 反应 措施
A 铁片与稀硫酸反应制取 将铁片换成铁屑
B 大理石与稀盐酸反应制取 加入NaCl溶液
C 熔液分解制备 添加少量
D 密闭容器中与合成 压缩容器体积
4.设为阿伏加德罗常数的值,下列说法中正确的是
A.11.2L 中含有0.5个氧原子
B.17g —OH所含电子数为10
C.1L 18浓硫酸与足量铜粉充分反应,转移的电子数为18
D.常温常压下,11g乙烯和17g丙烯的混合气体中所含原子总数为6
5.某化学兴趣小组在阴暗的地方用如图所示装置探究与的反应,灯泡接通电源后,开始实验。下到说法错误的是
A.软管内会发生取代反应,生成物有5种
B.透明软管内气体颜色会逐新变浅,透明软管的体积会缩小直至完全凹瘪
C.软管内会有油状液滴产生
D.充分反应后,打开,导管口可能会有白雾出现
6.夏县西瓜是全国农产品地理标志。下列说法正确的是
A.西瓜富含葡萄糖,葡萄糖和果糖互为同系物
B.西瓜中含有的瓜氨酸()属于天然高分子化合物
C.西瓜中含有的乙二醇()能被催化氧化为乙二醛()
D.西瓜藤中含有的纤维素属于多糖,与淀粉互为同分异构体
7.劳动是创造物质财富和精神财富的过程,下列劳动项目与所描述的化学知识没有关联的是
选项 劳动项目 化学知识
A 将生石膏点在豆浆中制作豆腐 生石膏受热会失去大部分结晶水而变成熟石膏
B 利用酒精给教室消毒 75%的乙醇溶液具有杀菌的功能
C 利用食醋除水垢 乙酸的酸性比碳酸强
D 用溶液刻蚀覆铜版制作印刷电路板 的氧化性比强
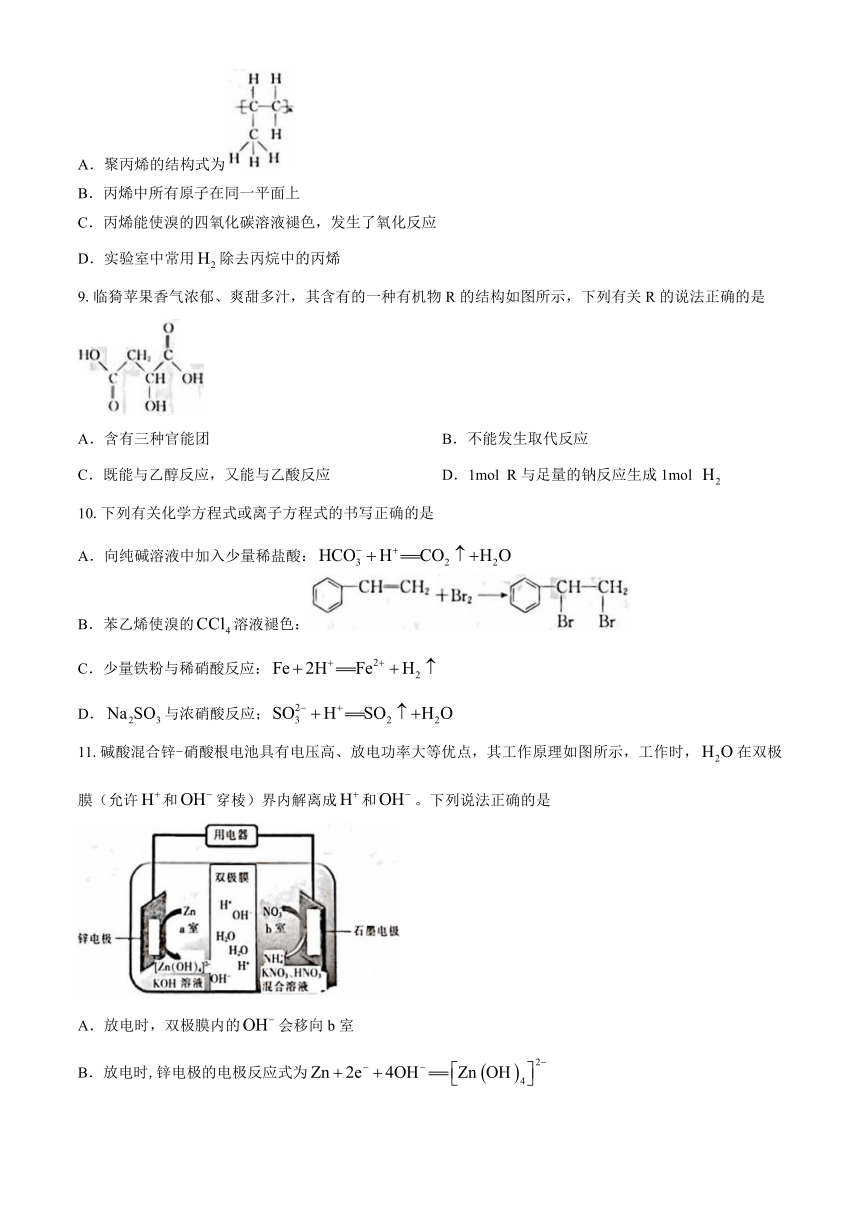
8.聚丙烯可用于生产空调室外机罩壳、遮光板等长期在户外使用的塑料部件,下列说法正确的是
A.聚丙烯的结构式为
B.丙烯中所有原子在同一平面上
C.丙烯能使溴的四氧化碳溶液褪色,发生了氧化反应
D.实验室中常用除去丙烷中的丙烯
9.临猗苹果香气浓郁、爽甜多汁,其含有的一种有机物R的结构如图所示,下列有关R的说法正确的是
A.含有三种官能团 B.不能发生取代反应
C.既能与乙醇反应,又能与乙酸反应 D.1mol R与足量的钠反应生成1mol
10.下列有关化学方程式或离子方程式的书写正确的是
A.向纯碱溶液中加入少量稀盐酸:
B.苯乙烯使溴的溶液褪色:
C.少量铁粉与稀硝酸反应:
D.与浓硝酸反应;
11.碱酸混合锌-硝酸根电池具有电压高、放电功率大等优点,其工作原理如图所示,工作时,在双极膜(允许和穿棱)界内解离成和。下列说法正确的是
A.放电时,双极膜内的会移向b室
B.放电时,锌电极的电极反应式为
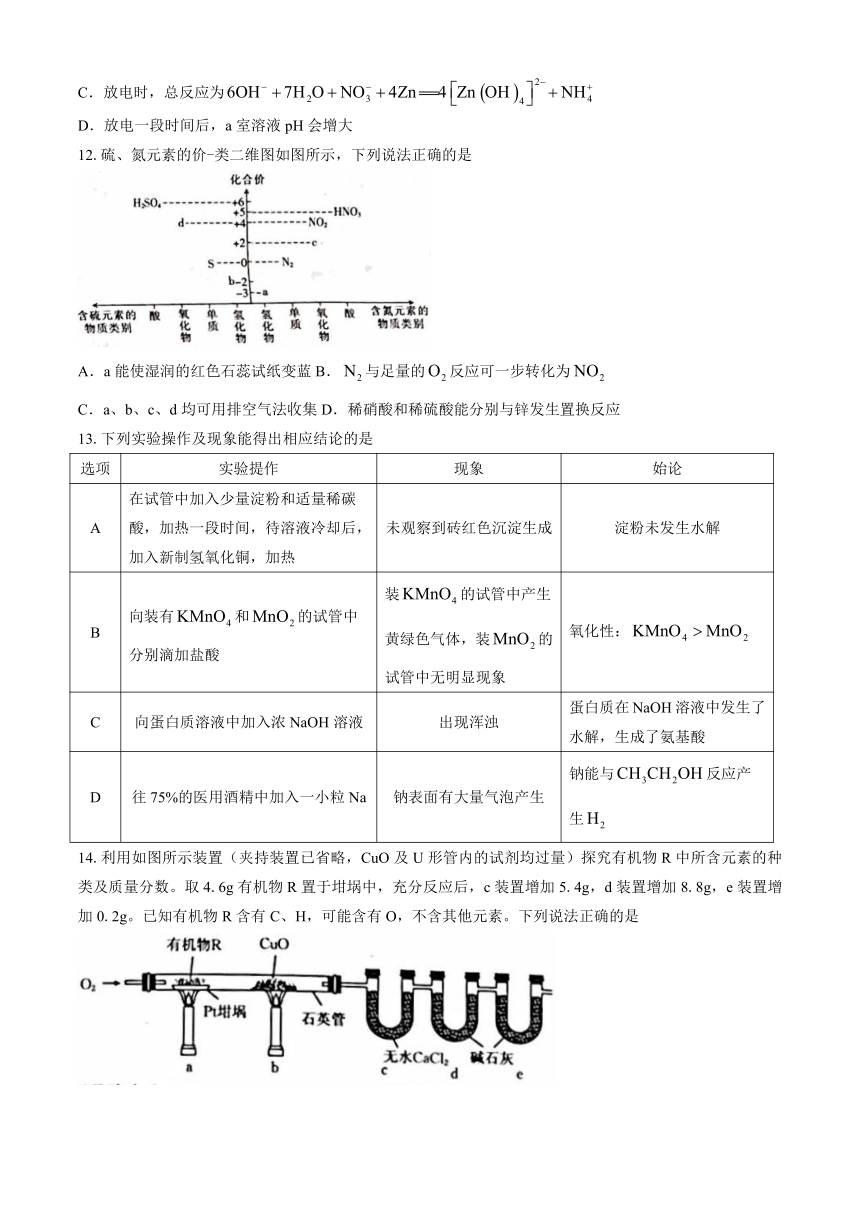
C.放电时,总反应为
D.放电一段时间后,a室溶液pH会增大
12.硫、氮元素的价-类二维图如图所示,下列说法正确的是
A.a能使湿润的红色石蕊试纸变蓝B.与足量的反应可一步转化为
C.a、b、c、d均可用排空气法收集D.稀硝酸和稀硫酸能分别与锌发生置换反应
13.下列实验操作及现象能得出相应结论的是
选项 实验提作 现象 始论
A 在试管中加入少量淀粉和适量稀碳酸,加热一段时间,待溶液冷却后,加入新制氢氧化铜,加热 未观察到砖红色沉淀生成 淀粉未发生水解
B 向装有和的试管中分别滴加盐酸 装的试管中产生黄绿色气体,装的试管中无明显现象 氧化性:
C 向蛋白质溶液中加入浓NaOH溶液 出现浑浊 蛋白质在NaOH溶液中发生了水解,生成了氨基酸
D 往75%的医用酒精中加入一小粒Na 钠表面有大量气泡产生 钠能与反应产生
14.利用如图所示装置(夹持装置已省略,CuO及U形管内的试剂均过量)探究有机物R中所含元素的种类及质量分数。取4.6g有机物R置于坩埚中,充分反应后,c装置增加5.4g,d装置增加8.8g,e装置增加0.2g。已知有机物R含有C、H,可能含有O,不含其他元素。下列说法正确的是
A.CuO的作用是除去多余的,防止其干扰后续气体的吸收
B.d中试剂可以用浓硫酸代替
C.若缺少装置e,则得出的C的质量分数会偏小
D.有机物R的分子式为
二、非选择题:本题共4小题,共58分。
15.(14分)
利用废旧磷酸铁锂电池正极材料(主要成分为、、石墨粉和铝箔)制备的一种流程如图所示,请回答下列问题:
已知:在水中的溶解度很小,溶解度随温度的升高而降低;、不溶于冷水,能溶于硫酸。
(1)为了提高“碱溶”速率,可以采取的措施有 ;“碱溶”时铝箔发生反应的离子方程式为 。
(2)“操作1”和“操作2”需要使用的主要成分为无机非金属材料的仪器有烧杯、 ;滤渣2和滤渣3的主要成分分别为 、 。
(3)磷酸铁锂电池放电时的反应为,放电时,正极的电极反应式为 ;若放电时电路中转移1mol电子,则电池负极质量减少 g。
(4)粗品可以用 (填标号)洗涤;检验是否洗涤干净的操作及现象为
。
A.热水 B.冷水 C.稀硫酸 D.氯化锂溶液
16.(15分)
为了加深对乙醇主要性质的认识,某兴趣小组围绕乙醇的性质进行如下实验。回答下列问题:
Ⅰ.按如图所示装置(加热与夹持装置已省略)进行乙醇的催化氧化实验。
(1)丁处盛装碱石灰的装置名称为 ,戊处导管未伸入液面下的原因是
。
(2)实验开始后,间歇性地通入氧气,乙中铜丝会红黑交替且丙处白色固体变蓝,则乙处乙醇生成乙醛的总反应的化学方程式为 。
Ⅱ.按如图所示装置制备乙酸乙酯。
(3)实验过程中需要小心加热,原因是 ;导管a的作用为 。
(4)反应生成乙酸乙酯的化学方程式为 ;饱和溶液的作用是除去挥发出的乙酸、 ;实验结束后,往收集到乙酸乙酯的试管中小心加入紫色石蕊试液0.5mL,这时石蕊试液将存在于饱和碳酸钠溶液层与乙酸乙酯层之间。静置,最有可能出现的现象为 (填标号)。
A.中间层为紫色,其他层均为无色 B.石蕊层为三色层,由上而下是红、紫、蓝
C.石蕊层为双色层,上层为紫色,下层为红色 D.石蕊层为三色层,由上而下是蓝、紫、红
17.(14分)
已知断裂1mol化学键使气态分子离解成气态原子所吸收的能量如表所示,
化学键 C=O(CO中的碳氧键) H-H C-H C-O H—O C=O
吸收能量/kJ 1072 436 413.5 351 463 803
(1)与在催化剂作用下能发生如图所示转化,该反应的化学方程式为
,该反应为 热反应。
(2)T℃时,、在一体积为2L的恒容密闭容器中发生反应生成(g)和R(g),反应过程中,各物质的物质的量随时间的变化如图所示(R与的变化曲线重叠)。
①R的分子式为 ;0~5min内,用表示的该反应的反应速率为 ;平衡时,R(g)的体积分数为 %。
②下列选项不能判断该反应达到平衡状态的是 (填标号)。
A.密闭容器中的体积分数不变
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中混合气体的平均相对分子质量不变
E.断裂6mol H-H键的同时生成2mol (g)
(3)科学家团队找到了一种方法,可以利用电化学原理吸收,实现碳中和,其原理如图所示。电池工作时,Na发生了 (填“氧化”或“还原”)反应,电池的正极的电极反应
。
18.(15分)
正丁酸乙酯(G)是我国规定允许使用的食用香料,常用于调制苹果、香蕉、菠萝等果香型食用香精和威士忌酒香精,以有机物A为原料制备正丁酸乙酯(G)的一种合成路线如图所示,有机物A的产量可以用来衡量一个国家石油化学工业的发展水平。回答下列问题:
(1)A的名称为 ,E中官能团的名称为 。
(2)A→B反应的化学方程式为 ,反应类型为 ;F→G反应的反应类型为 。
(3)E可以发生加聚反应生成高分子化合物H,H的结构简式为 。
(4)G的同分异构体有多种,其中能与饱和溶液反应产生的有 种,其中分子中含有3个甲基的结构简式为 (任写一种)。
高一化学试题参考答案
1.C 2.D 3.B 4.D 5.B 6.C 7.A 8.A 9.C 10.B 11.C
12.A 13.B 14.D
15.
(1)搅拌(或其他合理答案,1分);
(2)漏斗、玻璃棒;石墨粉;
(3);7
(4)A;取最后一次洗涤液,加入盐酸酸化的溶液,若无明显现象,则证明已经洗涤干净,反之则没有
16.
(1)球形干燥管(或干燥管,1分);防止发生倒吸
(2)
(3)适当加快反应速率的同时减少乙醇、乙酸的挥发;导气、冷凝
(4);吸收乙醇、降低乙酸乙酯的溶解度;B
17.
(1);吸
(2)①;0.24;12.5 ②CE
(3)氧化;
18.
(1)乙烯;碳碳双键、羧基
(2)(写H2O同样给分,2分);加成反应;取代反应或酯化反应
(3)
(4)8;(答案合理即可,2分)
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、隆位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容;人教版必修第二册第五章至第七章。
5.可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Cu 64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.鹊桥二号中继星已完成在轨对通测试,可为探月工程四期及后续国内外月球探测任务提供中继通信服务,下列说法正确的是
A.卫星上使用的太阳能电池的主要成分为
B.月壤中含有,和属于同种核素
C.长征八号遥三运载火箭使用的聚甲基丙烯酰亚胺(PMI)为高分子
D.长征八号运载火箭以液氢、液氧为推进剂,液氢燃烧时化学能全部转化为热能
2.下列化学用语表述正确的是
A.羧基的结构: B.果糖的分子式:
C.乙烷的空间填充模型; D.乙酸的结构式:
3.化学反应速率是用来表示化学反应过程进行快慢的物理量,下列措施能减慢反应速率的是
选项 反应 措施
A 铁片与稀硫酸反应制取 将铁片换成铁屑
B 大理石与稀盐酸反应制取 加入NaCl溶液
C 熔液分解制备 添加少量
D 密闭容器中与合成 压缩容器体积
4.设为阿伏加德罗常数的值,下列说法中正确的是
A.11.2L 中含有0.5个氧原子
B.17g —OH所含电子数为10
C.1L 18浓硫酸与足量铜粉充分反应,转移的电子数为18
D.常温常压下,11g乙烯和17g丙烯的混合气体中所含原子总数为6
5.某化学兴趣小组在阴暗的地方用如图所示装置探究与的反应,灯泡接通电源后,开始实验。下到说法错误的是
A.软管内会发生取代反应,生成物有5种
B.透明软管内气体颜色会逐新变浅,透明软管的体积会缩小直至完全凹瘪
C.软管内会有油状液滴产生
D.充分反应后,打开,导管口可能会有白雾出现
6.夏县西瓜是全国农产品地理标志。下列说法正确的是
A.西瓜富含葡萄糖,葡萄糖和果糖互为同系物
B.西瓜中含有的瓜氨酸()属于天然高分子化合物
C.西瓜中含有的乙二醇()能被催化氧化为乙二醛()
D.西瓜藤中含有的纤维素属于多糖,与淀粉互为同分异构体
7.劳动是创造物质财富和精神财富的过程,下列劳动项目与所描述的化学知识没有关联的是
选项 劳动项目 化学知识
A 将生石膏点在豆浆中制作豆腐 生石膏受热会失去大部分结晶水而变成熟石膏
B 利用酒精给教室消毒 75%的乙醇溶液具有杀菌的功能
C 利用食醋除水垢 乙酸的酸性比碳酸强
D 用溶液刻蚀覆铜版制作印刷电路板 的氧化性比强
8.聚丙烯可用于生产空调室外机罩壳、遮光板等长期在户外使用的塑料部件,下列说法正确的是
A.聚丙烯的结构式为
B.丙烯中所有原子在同一平面上
C.丙烯能使溴的四氧化碳溶液褪色,发生了氧化反应
D.实验室中常用除去丙烷中的丙烯
9.临猗苹果香气浓郁、爽甜多汁,其含有的一种有机物R的结构如图所示,下列有关R的说法正确的是
A.含有三种官能团 B.不能发生取代反应
C.既能与乙醇反应,又能与乙酸反应 D.1mol R与足量的钠反应生成1mol
10.下列有关化学方程式或离子方程式的书写正确的是
A.向纯碱溶液中加入少量稀盐酸:
B.苯乙烯使溴的溶液褪色:
C.少量铁粉与稀硝酸反应:
D.与浓硝酸反应;
11.碱酸混合锌-硝酸根电池具有电压高、放电功率大等优点,其工作原理如图所示,工作时,在双极膜(允许和穿棱)界内解离成和。下列说法正确的是
A.放电时,双极膜内的会移向b室
B.放电时,锌电极的电极反应式为
C.放电时,总反应为
D.放电一段时间后,a室溶液pH会增大
12.硫、氮元素的价-类二维图如图所示,下列说法正确的是
A.a能使湿润的红色石蕊试纸变蓝B.与足量的反应可一步转化为
C.a、b、c、d均可用排空气法收集D.稀硝酸和稀硫酸能分别与锌发生置换反应
13.下列实验操作及现象能得出相应结论的是
选项 实验提作 现象 始论
A 在试管中加入少量淀粉和适量稀碳酸,加热一段时间,待溶液冷却后,加入新制氢氧化铜,加热 未观察到砖红色沉淀生成 淀粉未发生水解
B 向装有和的试管中分别滴加盐酸 装的试管中产生黄绿色气体,装的试管中无明显现象 氧化性:
C 向蛋白质溶液中加入浓NaOH溶液 出现浑浊 蛋白质在NaOH溶液中发生了水解,生成了氨基酸
D 往75%的医用酒精中加入一小粒Na 钠表面有大量气泡产生 钠能与反应产生
14.利用如图所示装置(夹持装置已省略,CuO及U形管内的试剂均过量)探究有机物R中所含元素的种类及质量分数。取4.6g有机物R置于坩埚中,充分反应后,c装置增加5.4g,d装置增加8.8g,e装置增加0.2g。已知有机物R含有C、H,可能含有O,不含其他元素。下列说法正确的是
A.CuO的作用是除去多余的,防止其干扰后续气体的吸收
B.d中试剂可以用浓硫酸代替
C.若缺少装置e,则得出的C的质量分数会偏小
D.有机物R的分子式为
二、非选择题:本题共4小题,共58分。
15.(14分)
利用废旧磷酸铁锂电池正极材料(主要成分为、、石墨粉和铝箔)制备的一种流程如图所示,请回答下列问题:
已知:在水中的溶解度很小,溶解度随温度的升高而降低;、不溶于冷水,能溶于硫酸。
(1)为了提高“碱溶”速率,可以采取的措施有 ;“碱溶”时铝箔发生反应的离子方程式为 。
(2)“操作1”和“操作2”需要使用的主要成分为无机非金属材料的仪器有烧杯、 ;滤渣2和滤渣3的主要成分分别为 、 。
(3)磷酸铁锂电池放电时的反应为,放电时,正极的电极反应式为 ;若放电时电路中转移1mol电子,则电池负极质量减少 g。
(4)粗品可以用 (填标号)洗涤;检验是否洗涤干净的操作及现象为
。
A.热水 B.冷水 C.稀硫酸 D.氯化锂溶液
16.(15分)
为了加深对乙醇主要性质的认识,某兴趣小组围绕乙醇的性质进行如下实验。回答下列问题:
Ⅰ.按如图所示装置(加热与夹持装置已省略)进行乙醇的催化氧化实验。
(1)丁处盛装碱石灰的装置名称为 ,戊处导管未伸入液面下的原因是
。
(2)实验开始后,间歇性地通入氧气,乙中铜丝会红黑交替且丙处白色固体变蓝,则乙处乙醇生成乙醛的总反应的化学方程式为 。
Ⅱ.按如图所示装置制备乙酸乙酯。
(3)实验过程中需要小心加热,原因是 ;导管a的作用为 。
(4)反应生成乙酸乙酯的化学方程式为 ;饱和溶液的作用是除去挥发出的乙酸、 ;实验结束后,往收集到乙酸乙酯的试管中小心加入紫色石蕊试液0.5mL,这时石蕊试液将存在于饱和碳酸钠溶液层与乙酸乙酯层之间。静置,最有可能出现的现象为 (填标号)。
A.中间层为紫色,其他层均为无色 B.石蕊层为三色层,由上而下是红、紫、蓝
C.石蕊层为双色层,上层为紫色,下层为红色 D.石蕊层为三色层,由上而下是蓝、紫、红
17.(14分)
已知断裂1mol化学键使气态分子离解成气态原子所吸收的能量如表所示,
化学键 C=O(CO中的碳氧键) H-H C-H C-O H—O C=O
吸收能量/kJ 1072 436 413.5 351 463 803
(1)与在催化剂作用下能发生如图所示转化,该反应的化学方程式为
,该反应为 热反应。
(2)T℃时,、在一体积为2L的恒容密闭容器中发生反应生成(g)和R(g),反应过程中,各物质的物质的量随时间的变化如图所示(R与的变化曲线重叠)。
①R的分子式为 ;0~5min内,用表示的该反应的反应速率为 ;平衡时,R(g)的体积分数为 %。
②下列选项不能判断该反应达到平衡状态的是 (填标号)。
A.密闭容器中的体积分数不变
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中混合气体的平均相对分子质量不变
E.断裂6mol H-H键的同时生成2mol (g)
(3)科学家团队找到了一种方法,可以利用电化学原理吸收,实现碳中和,其原理如图所示。电池工作时,Na发生了 (填“氧化”或“还原”)反应,电池的正极的电极反应
。
18.(15分)
正丁酸乙酯(G)是我国规定允许使用的食用香料,常用于调制苹果、香蕉、菠萝等果香型食用香精和威士忌酒香精,以有机物A为原料制备正丁酸乙酯(G)的一种合成路线如图所示,有机物A的产量可以用来衡量一个国家石油化学工业的发展水平。回答下列问题:
(1)A的名称为 ,E中官能团的名称为 。
(2)A→B反应的化学方程式为 ,反应类型为 ;F→G反应的反应类型为 。
(3)E可以发生加聚反应生成高分子化合物H,H的结构简式为 。
(4)G的同分异构体有多种,其中能与饱和溶液反应产生的有 种,其中分子中含有3个甲基的结构简式为 (任写一种)。
高一化学试题参考答案
1.C 2.D 3.B 4.D 5.B 6.C 7.A 8.A 9.C 10.B 11.C
12.A 13.B 14.D
15.
(1)搅拌(或其他合理答案,1分);
(2)漏斗、玻璃棒;石墨粉;
(3);7
(4)A;取最后一次洗涤液,加入盐酸酸化的溶液,若无明显现象,则证明已经洗涤干净,反之则没有
16.
(1)球形干燥管(或干燥管,1分);防止发生倒吸
(2)
(3)适当加快反应速率的同时减少乙醇、乙酸的挥发;导气、冷凝
(4);吸收乙醇、降低乙酸乙酯的溶解度;B
17.
(1);吸
(2)①;0.24;12.5 ②CE
(3)氧化;
18.
(1)乙烯;碳碳双键、羧基
(2)(写H2O同样给分,2分);加成反应;取代反应或酯化反应
(3)
(4)8;(答案合理即可,2分)
同课章节目录
