第二章第3节 第3课时分子结构与物质的性质教案 高中化学人教版(2019)选择性必修二
文档属性
| 名称 | 第二章第3节 第3课时分子结构与物质的性质教案 高中化学人教版(2019)选择性必修二 |

|
|
| 格式 | docx | ||
| 文件大小 | 433.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-10 00:00:00 | ||
图片预览

文档简介
分子结构与物质的性质
第3课时
教学目标
1. 初步认识分子的手性,了解手性分子在药物研究中的应用。
2. 能判断简单分子是否存在手性异构体。
3. 整合分子空间结构、化学键极性、分子极性,分子间作用力、氢键等概念,综合运用解决物质性质问题。
教学重难点
手性分子的概念及判断。
教学过程
一、新课导入
分子是有空间结构的,对于复杂的分子,可以形成多种空间结构。
在学习烯烃时,我们知道不同的取代基团在碳碳双键双侧分布不同时,会产生同分异构现象,如下面的顺反异构:
那是否还存其他类型的立体异构呢?即原子连接顺序相同,但是由于原子在空间的排布不同而造成的异构现象。
二、讲授新课
三、分子的手性
【模型搭建】
任务1. 以小组为单位动手搭建两个CH2ClBr模型,通过旋转模型,看这两个模型是否可以完全重合?
经过实践,我们发现任意两个模型总能完全重合。因此CH2ClBr有且仅有一种空间结构,它没有同分异构体。
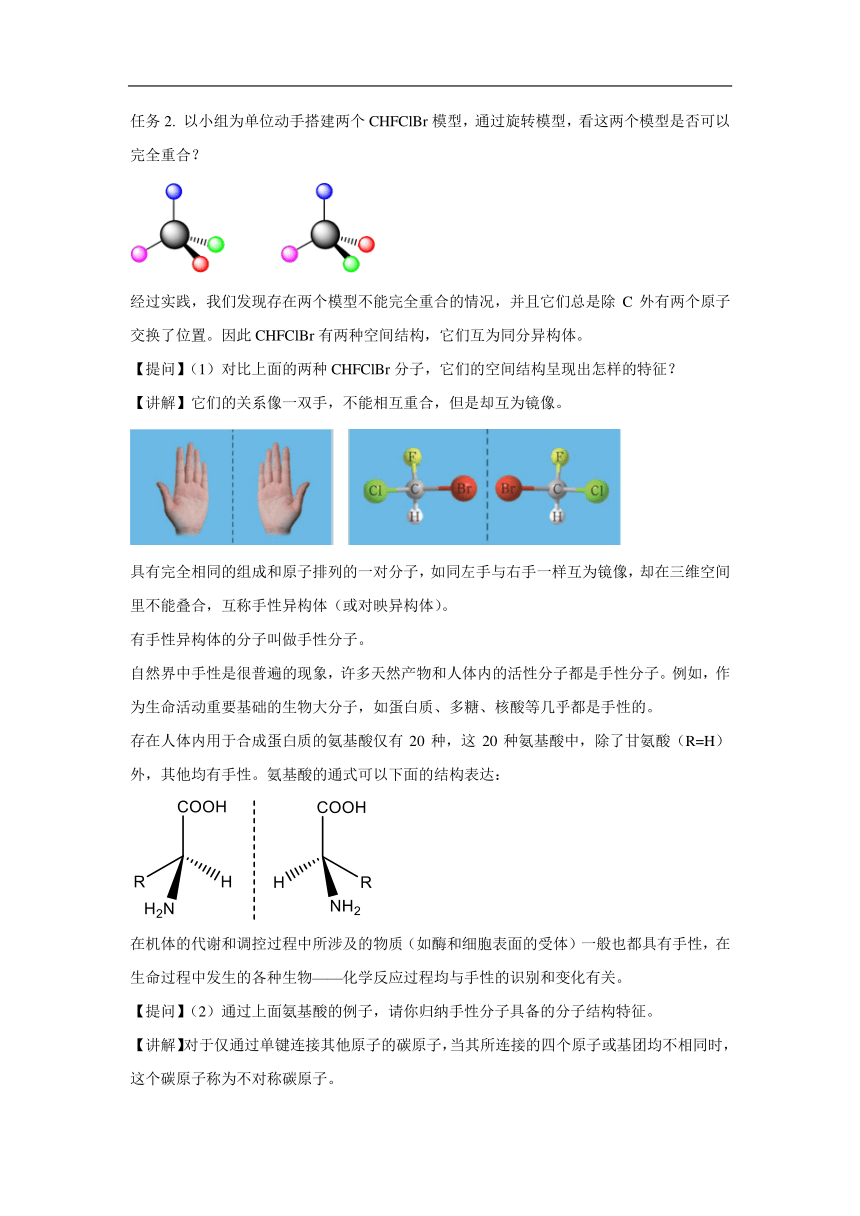
任务2. 以小组为单位动手搭建两个CHFClBr模型,通过旋转模型,看这两个模型是否可以完全重合?
经过实践,我们发现存在两个模型不能完全重合的情况,并且它们总是除C外有两个原子交换了位置。因此CHFClBr有两种空间结构,它们互为同分异构体。
【提问】(1)对比上面的两种CHFClBr分子,它们的空间结构呈现出怎样的特征?
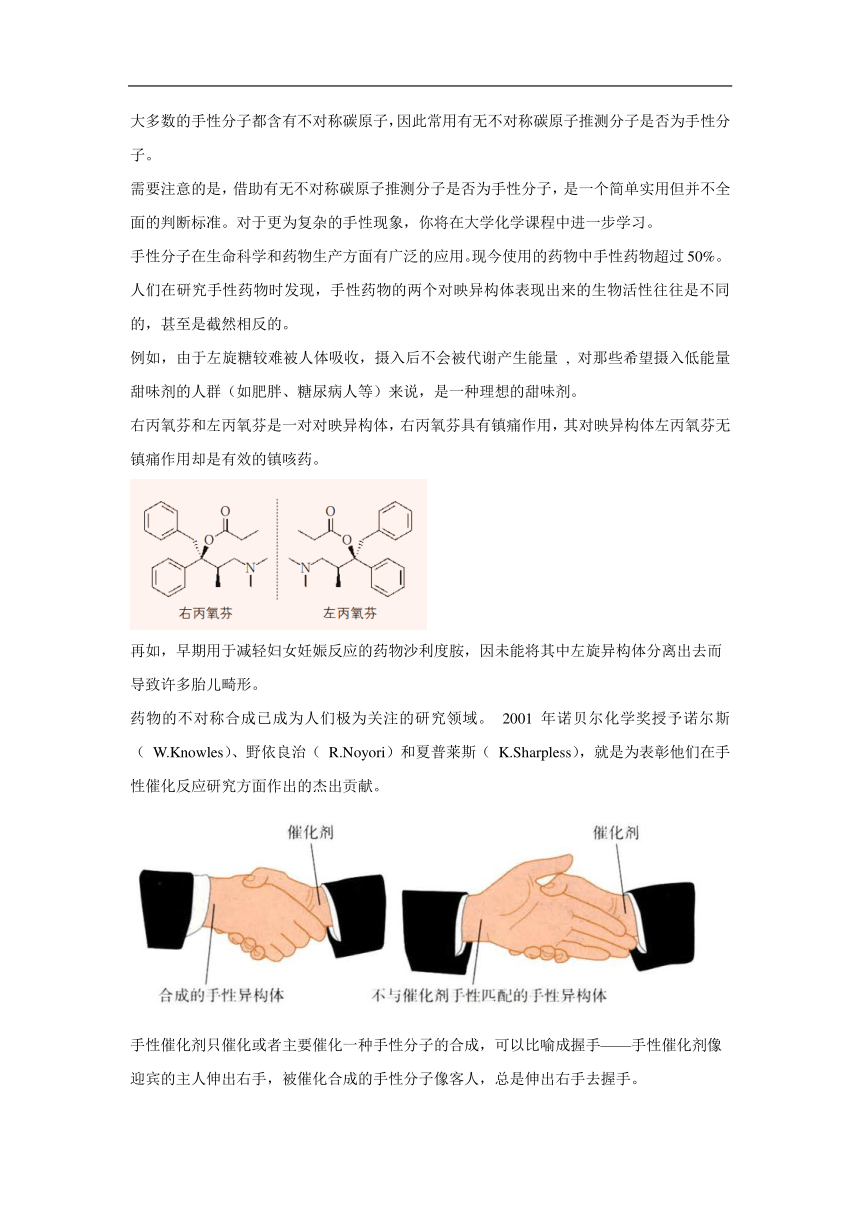
【讲解】它们的关系像一双手,不能相互重合,但是却互为镜像。
具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜像,却在三维空间里不能叠合,互称手性异构体(或对映异构体)。
有手性异构体的分子叫做手性分子。
自然界中手性是很普遍的现象,许多天然产物和人体内的活性分子都是手性分子。例如,作为生命活动重要基础的生物大分子,如蛋白质、多糖、核酸等几乎都是手性的。
存在人体内用于合成蛋白质的氨基酸仅有20种,这20种氨基酸中,除了甘氨酸(R=H)外,其他均有手性。氨基酸的通式可以下面的结构表达:
在机体的代谢和调控过程中所涉及的物质(如酶和细胞表面的受体)一般也都具有手性,在生命过程中发生的各种生物——化学反应过程均与手性的识别和变化有关。
【提问】(2)通过上面氨基酸的例子,请你归纳手性分子具备的分子结构特征。
【讲解】对于仅通过单键连接其他原子的碳原子,当其所连接的四个原子或基团均不相同时,这个碳原子称为不对称碳原子。
大多数的手性分子都含有不对称碳原子,因此常用有无不对称碳原子推测分子是否为手性分子。
需要注意的是,借助有无不对称碳原子推测分子是否为手性分子,是一个简单实用但并不全面的判断标准。对于更为复杂的手性现象,你将在大学化学课程中进一步学习。
手性分子在生命科学和药物生产方面有广泛的应用。现今使用的药物中手性药物超过50%。人们在研究手性药物时发现,手性药物的两个对映异构体表现出来的生物活性往往是不同的,甚至是截然相反的。
例如,由于左旋糖较难被人体吸收,摄入后不会被代谢产生能量 , 对那些希望摄入低能量甜味剂的人群(如肥胖、糖尿病人等)来说,是一种理想的甜味剂。
右丙氧芬和左丙氧芬是一对对映异构体,右丙氧芬具有镇痛作用,其对映异构体左丙氧芬无镇痛作用却是有效的镇咳药。
再如,早期用于减轻妇女妊娠反应的药物沙利度胺,因未能将其中左旋异构体分离出去而导致许多胎儿畸形。
药物的不对称合成已成为人们极为关注的研究领域。 2001 年诺贝尔化学奖授予诺尔斯( W.Knowles)、野依良治( R.Noyori)和夏普莱斯( K.Sharpless),就是为表彰他们在手性催化反应研究方面作出的杰出贡献。
手性催化剂只催化或者主要催化一种手性分子的合成,可以比喻成握手——手性催化剂像迎宾的主人伸出右手,被催化合成的手性分子像客人,总是伸出右手去握手。
三、课堂小结
1. 手性是自然界普遍存在的现象,对于生命有重要的意义。
2. 通过深入研究手性,人类可以选择合适的手性催化剂合成手性异构体中的某一种,这种技术在药物生产、生命科学中具有广泛的应用。
3. 碳原子所连接的四个原子或基团均不相同时,这个碳原子称为不对称碳原子。大多数的手性分子都含有不对称碳原子,因此常用有无不对称碳原子推测分子是否为手性分子。
四、分子空间结构与物质性质整合提升
【典型例题】
例1. 下列共价键①H-H、②H-F、③H-O、④N-H、⑤P-H中,将键的极性由小到大排序 ① < ⑤ < ④ < ③ < ②。
解析 键的极性源自于共用电子的两原子吸引电子能力不同,能力差别越大,键的极性越大。在一个H固定后,另一原子的电负性越强,键的极性越大。电负性的变化规律:同周期自左向右增大,同主族自上而下减小,由此可知电负性P < N < O < F,键的极性与此顺序一致。
例2. 下列分子为极性分子的是 ③ ④ 。
①CH4 ②BeCl2 ③NH3 ④H2S ⑤CO2 ⑥BCl3
解析 判断多原子分子极性的步骤:
1. 依据VSEPR模型预测判断分子的空间结构;
2. 确定共价键极性的向量方向;
3. 将所有向量求和,依据向量和是否为零对分子极性做出判断。
①为正四面体,②为直线形,③为三角锥形,④为V形,⑤为直线形,⑥为平面三角形。共价键极性向量求和后不为0的是三角锥形和V形。
例3. 下列说法正确的是:( A )
A. 分子构成的固态物质中一定存在分子间作用力,不一定存在共价键
B. 水加热到很高的温度都难以分解与氢键有关
C. CH4、SiH4、GeH4、SnH4的熔点随着相对分子质量的增大而降低
D. HF、HCl、HBr、HI的熔沸点随着相对分子质量的增大而升高
解析 A项,分子间作用是普遍存在于分子间的,稀有气体是单原子分子,固态的He、Ne等中不存在共价键。B项,水的稳定性主要是因为O-H键键能大,氢键只影响熔沸点;C项,组成、结构相似的分子,相对分子量越大,范德华力越大,熔沸点越高。D项,HF分子间能形成氢键,熔沸点明显升高。
例4. 碘单质在水中溶解度很小,但在CCl4中溶解度很大,这是因为( D )
A. CCl4与I2相对分子质量相差较小,而H2O与I2相对分子质量相差较大
B. CCl4和I2都是直线形分子,而H2O不是直线形分子
C. CCl4和I2都不含氢元素,而H2O中含有氢元素
D. CCl4和I2都是非极性分子,而H2O是极性分子
解析 CCl4是正四面体形的分子,为非极性分子,H2O是V形分子,为极性分子。依据相似相溶规律,非极性溶质在非极性溶剂中溶解度更大。I2是非极性分子,故其在CCl4溶解度更大。溶解度与是否含有氢元素、分子量差值等因素无关。
四、课堂练习
1. 试根据分子中羟基(-OH)的极性大小,判断下列酸的酸性最强的是
已知:下列分子中除羟基外,其他O都只直接与Cl原子形成共价键
A. HClO B. HClO2 C. HClO3 D.HClO4
答案 D
解析 Cl与O共用电子时,因O的电负性大于Cl,电子对偏向O,这种键的极性会沿着σ键传递到羟基的O-H键,使得O-H键极性进一步增大,H+更容易被电离出。故除羟基外,与Cl相连的O的数量越多,这种效应叠加的越强,酸的酸性越强。
2. 在极性分子中,正电荷中心与负电荷中心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正电荷中心的电量(q)有关,一般用偶极矩μ来衡量,计算表达式为μ = d · q。试回答以下问题:
(1)HCl、CS2、H2S、SO2四种分子中,μ = 0的是_______________
(2)实验测得,μ(PF3) = 1.03、μ(BCl3) = 0。由此可知PF3分子的空间结构是___________,BCl3分子的空间结构是_______________。
(3)治癌药Pt(NH3)2Cl2具有平面四边形分子结构。其中,Pt处在四边形中心,NH3和Cl分别处在四边形的四个角上。已知该化合物有两种异构体,淡黄色者μ = 0,棕黄色者μ > 0。在下列横线处画出两种结构的异构体的结构图。
淡黄色________________ 棕黄色___________________
答案 (1)CS2 (2)三角锥 平面三角形
(3)淡黄色________________ 棕黄色___________________
解析 (1)根据计算表达式μ = d · q,因正电中心的电量q必为一个不为0的数,故当μ = 0时可推知d = 0,即正负电荷中心的距离为0,二者重合,这样的分子是非极性分子。故μ=0等价于分子为非极性分子。
CS2是直线形的非极性分子。其他3种均为极性分子。
(2)根据偶极矩数据可知,PF3是极性分子,BCl3是非极性分子。四原子分子是三角锥形或平面三角形。平面三角形高度对称,共价键极性矢量和为0,为非极性分子。三角锥形共价键极性矢量和不为0,为极性分子。
(3)淡黄色的分子是非极性分子。在平面四边形中,若相同的两个基团处于中心原子的对位,如Cl-Pt-Cl的键角为180°时,Pt-Cl共价键极性的矢量恰好抵消。当 Cl、NH3交替排列时两种基团的矢量各自抵消,分子为非极性分子。
3. 推测下列分子在水中溶解度最大的是
A. NH3 B. CO C. H2 D. 苯
答案 A
解析 H2和苯是非极性分子,CO和NH3是极性分子,水是极性溶剂。根据相似相溶规律,CO和NH3的溶解度大于H2和苯。
又因为NH3能与H2O形成很强的氢键,大大增加了它在水中的溶解度。
4. 下面的分子经过某种转化后,仍存在手性异构体,满足该条件的反应是( )
A. 将-CHO还原为-CH2OH
B. 将-CH2OH替换为-CH2Cl
C. 将-CH2OOCCH3水解为-CH2OH
D. 将-CHO氧化为-COOH
答案 B
解析 碳原子所连接的四个原子或基团均不相同时,这个碳原子称为不对称碳原子。这里运用判据:大多数的手性分子都含有不对称碳原子。发生A、C、D的转化后,中间的碳原子就连接了两个相同的基团,从而“丧失手性”
5. 关于氢键的说法正确的是
A. 每一个水分子内含有两个氢键
B. 冰、水中都存在氢键
C. 分子间形成的氢键使物质的熔点和沸点降低
D. 邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点高
答案 B
解析 A项,水分子只能形成分子间氢键,无法形成分子内氢键;B项,固态和液态时,水分子间距离都较小,能彼此靠近形成氢键;C项,分子间形成的氢键后,在物质熔化或汽化时,需要更多能量克服分子间的这种相互作用,故氢键使熔沸点升高。邻羟基苯甲醛形成分子内氢键,对羟基苯甲醛形成分子间氢键,故对羟基苯甲醛的沸点更高。
第3课时
教学目标
1. 初步认识分子的手性,了解手性分子在药物研究中的应用。
2. 能判断简单分子是否存在手性异构体。
3. 整合分子空间结构、化学键极性、分子极性,分子间作用力、氢键等概念,综合运用解决物质性质问题。
教学重难点
手性分子的概念及判断。
教学过程
一、新课导入
分子是有空间结构的,对于复杂的分子,可以形成多种空间结构。
在学习烯烃时,我们知道不同的取代基团在碳碳双键双侧分布不同时,会产生同分异构现象,如下面的顺反异构:
那是否还存其他类型的立体异构呢?即原子连接顺序相同,但是由于原子在空间的排布不同而造成的异构现象。
二、讲授新课
三、分子的手性
【模型搭建】
任务1. 以小组为单位动手搭建两个CH2ClBr模型,通过旋转模型,看这两个模型是否可以完全重合?
经过实践,我们发现任意两个模型总能完全重合。因此CH2ClBr有且仅有一种空间结构,它没有同分异构体。
任务2. 以小组为单位动手搭建两个CHFClBr模型,通过旋转模型,看这两个模型是否可以完全重合?
经过实践,我们发现存在两个模型不能完全重合的情况,并且它们总是除C外有两个原子交换了位置。因此CHFClBr有两种空间结构,它们互为同分异构体。
【提问】(1)对比上面的两种CHFClBr分子,它们的空间结构呈现出怎样的特征?
【讲解】它们的关系像一双手,不能相互重合,但是却互为镜像。
具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜像,却在三维空间里不能叠合,互称手性异构体(或对映异构体)。
有手性异构体的分子叫做手性分子。
自然界中手性是很普遍的现象,许多天然产物和人体内的活性分子都是手性分子。例如,作为生命活动重要基础的生物大分子,如蛋白质、多糖、核酸等几乎都是手性的。
存在人体内用于合成蛋白质的氨基酸仅有20种,这20种氨基酸中,除了甘氨酸(R=H)外,其他均有手性。氨基酸的通式可以下面的结构表达:
在机体的代谢和调控过程中所涉及的物质(如酶和细胞表面的受体)一般也都具有手性,在生命过程中发生的各种生物——化学反应过程均与手性的识别和变化有关。
【提问】(2)通过上面氨基酸的例子,请你归纳手性分子具备的分子结构特征。
【讲解】对于仅通过单键连接其他原子的碳原子,当其所连接的四个原子或基团均不相同时,这个碳原子称为不对称碳原子。
大多数的手性分子都含有不对称碳原子,因此常用有无不对称碳原子推测分子是否为手性分子。
需要注意的是,借助有无不对称碳原子推测分子是否为手性分子,是一个简单实用但并不全面的判断标准。对于更为复杂的手性现象,你将在大学化学课程中进一步学习。
手性分子在生命科学和药物生产方面有广泛的应用。现今使用的药物中手性药物超过50%。人们在研究手性药物时发现,手性药物的两个对映异构体表现出来的生物活性往往是不同的,甚至是截然相反的。
例如,由于左旋糖较难被人体吸收,摄入后不会被代谢产生能量 , 对那些希望摄入低能量甜味剂的人群(如肥胖、糖尿病人等)来说,是一种理想的甜味剂。
右丙氧芬和左丙氧芬是一对对映异构体,右丙氧芬具有镇痛作用,其对映异构体左丙氧芬无镇痛作用却是有效的镇咳药。
再如,早期用于减轻妇女妊娠反应的药物沙利度胺,因未能将其中左旋异构体分离出去而导致许多胎儿畸形。
药物的不对称合成已成为人们极为关注的研究领域。 2001 年诺贝尔化学奖授予诺尔斯( W.Knowles)、野依良治( R.Noyori)和夏普莱斯( K.Sharpless),就是为表彰他们在手性催化反应研究方面作出的杰出贡献。
手性催化剂只催化或者主要催化一种手性分子的合成,可以比喻成握手——手性催化剂像迎宾的主人伸出右手,被催化合成的手性分子像客人,总是伸出右手去握手。
三、课堂小结
1. 手性是自然界普遍存在的现象,对于生命有重要的意义。
2. 通过深入研究手性,人类可以选择合适的手性催化剂合成手性异构体中的某一种,这种技术在药物生产、生命科学中具有广泛的应用。
3. 碳原子所连接的四个原子或基团均不相同时,这个碳原子称为不对称碳原子。大多数的手性分子都含有不对称碳原子,因此常用有无不对称碳原子推测分子是否为手性分子。
四、分子空间结构与物质性质整合提升
【典型例题】
例1. 下列共价键①H-H、②H-F、③H-O、④N-H、⑤P-H中,将键的极性由小到大排序 ① < ⑤ < ④ < ③ < ②。
解析 键的极性源自于共用电子的两原子吸引电子能力不同,能力差别越大,键的极性越大。在一个H固定后,另一原子的电负性越强,键的极性越大。电负性的变化规律:同周期自左向右增大,同主族自上而下减小,由此可知电负性P < N < O < F,键的极性与此顺序一致。
例2. 下列分子为极性分子的是 ③ ④ 。
①CH4 ②BeCl2 ③NH3 ④H2S ⑤CO2 ⑥BCl3
解析 判断多原子分子极性的步骤:
1. 依据VSEPR模型预测判断分子的空间结构;
2. 确定共价键极性的向量方向;
3. 将所有向量求和,依据向量和是否为零对分子极性做出判断。
①为正四面体,②为直线形,③为三角锥形,④为V形,⑤为直线形,⑥为平面三角形。共价键极性向量求和后不为0的是三角锥形和V形。
例3. 下列说法正确的是:( A )
A. 分子构成的固态物质中一定存在分子间作用力,不一定存在共价键
B. 水加热到很高的温度都难以分解与氢键有关
C. CH4、SiH4、GeH4、SnH4的熔点随着相对分子质量的增大而降低
D. HF、HCl、HBr、HI的熔沸点随着相对分子质量的增大而升高
解析 A项,分子间作用是普遍存在于分子间的,稀有气体是单原子分子,固态的He、Ne等中不存在共价键。B项,水的稳定性主要是因为O-H键键能大,氢键只影响熔沸点;C项,组成、结构相似的分子,相对分子量越大,范德华力越大,熔沸点越高。D项,HF分子间能形成氢键,熔沸点明显升高。
例4. 碘单质在水中溶解度很小,但在CCl4中溶解度很大,这是因为( D )
A. CCl4与I2相对分子质量相差较小,而H2O与I2相对分子质量相差较大
B. CCl4和I2都是直线形分子,而H2O不是直线形分子
C. CCl4和I2都不含氢元素,而H2O中含有氢元素
D. CCl4和I2都是非极性分子,而H2O是极性分子
解析 CCl4是正四面体形的分子,为非极性分子,H2O是V形分子,为极性分子。依据相似相溶规律,非极性溶质在非极性溶剂中溶解度更大。I2是非极性分子,故其在CCl4溶解度更大。溶解度与是否含有氢元素、分子量差值等因素无关。
四、课堂练习
1. 试根据分子中羟基(-OH)的极性大小,判断下列酸的酸性最强的是
已知:下列分子中除羟基外,其他O都只直接与Cl原子形成共价键
A. HClO B. HClO2 C. HClO3 D.HClO4
答案 D
解析 Cl与O共用电子时,因O的电负性大于Cl,电子对偏向O,这种键的极性会沿着σ键传递到羟基的O-H键,使得O-H键极性进一步增大,H+更容易被电离出。故除羟基外,与Cl相连的O的数量越多,这种效应叠加的越强,酸的酸性越强。
2. 在极性分子中,正电荷中心与负电荷中心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正电荷中心的电量(q)有关,一般用偶极矩μ来衡量,计算表达式为μ = d · q。试回答以下问题:
(1)HCl、CS2、H2S、SO2四种分子中,μ = 0的是_______________
(2)实验测得,μ(PF3) = 1.03、μ(BCl3) = 0。由此可知PF3分子的空间结构是___________,BCl3分子的空间结构是_______________。
(3)治癌药Pt(NH3)2Cl2具有平面四边形分子结构。其中,Pt处在四边形中心,NH3和Cl分别处在四边形的四个角上。已知该化合物有两种异构体,淡黄色者μ = 0,棕黄色者μ > 0。在下列横线处画出两种结构的异构体的结构图。
淡黄色________________ 棕黄色___________________
答案 (1)CS2 (2)三角锥 平面三角形
(3)淡黄色________________ 棕黄色___________________
解析 (1)根据计算表达式μ = d · q,因正电中心的电量q必为一个不为0的数,故当μ = 0时可推知d = 0,即正负电荷中心的距离为0,二者重合,这样的分子是非极性分子。故μ=0等价于分子为非极性分子。
CS2是直线形的非极性分子。其他3种均为极性分子。
(2)根据偶极矩数据可知,PF3是极性分子,BCl3是非极性分子。四原子分子是三角锥形或平面三角形。平面三角形高度对称,共价键极性矢量和为0,为非极性分子。三角锥形共价键极性矢量和不为0,为极性分子。
(3)淡黄色的分子是非极性分子。在平面四边形中,若相同的两个基团处于中心原子的对位,如Cl-Pt-Cl的键角为180°时,Pt-Cl共价键极性的矢量恰好抵消。当 Cl、NH3交替排列时两种基团的矢量各自抵消,分子为非极性分子。
3. 推测下列分子在水中溶解度最大的是
A. NH3 B. CO C. H2 D. 苯
答案 A
解析 H2和苯是非极性分子,CO和NH3是极性分子,水是极性溶剂。根据相似相溶规律,CO和NH3的溶解度大于H2和苯。
又因为NH3能与H2O形成很强的氢键,大大增加了它在水中的溶解度。
4. 下面的分子经过某种转化后,仍存在手性异构体,满足该条件的反应是( )
A. 将-CHO还原为-CH2OH
B. 将-CH2OH替换为-CH2Cl
C. 将-CH2OOCCH3水解为-CH2OH
D. 将-CHO氧化为-COOH
答案 B
解析 碳原子所连接的四个原子或基团均不相同时,这个碳原子称为不对称碳原子。这里运用判据:大多数的手性分子都含有不对称碳原子。发生A、C、D的转化后,中间的碳原子就连接了两个相同的基团,从而“丧失手性”
5. 关于氢键的说法正确的是
A. 每一个水分子内含有两个氢键
B. 冰、水中都存在氢键
C. 分子间形成的氢键使物质的熔点和沸点降低
D. 邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点高
答案 B
解析 A项,水分子只能形成分子间氢键,无法形成分子内氢键;B项,固态和液态时,水分子间距离都较小,能彼此靠近形成氢键;C项,分子间形成的氢键后,在物质熔化或汽化时,需要更多能量克服分子间的这种相互作用,故氢键使熔沸点升高。邻羟基苯甲醛形成分子内氢键,对羟基苯甲醛形成分子间氢键,故对羟基苯甲醛的沸点更高。
