2.3 构成物质的微粒(4)---原子和离子
文档属性
| 名称 | 2.3 构成物质的微粒(4)---原子和离子 |

|
|
| 格式 | zip | ||
| 文件大小 | 360.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-12-15 00:00:00 | ||
图片预览

文档简介
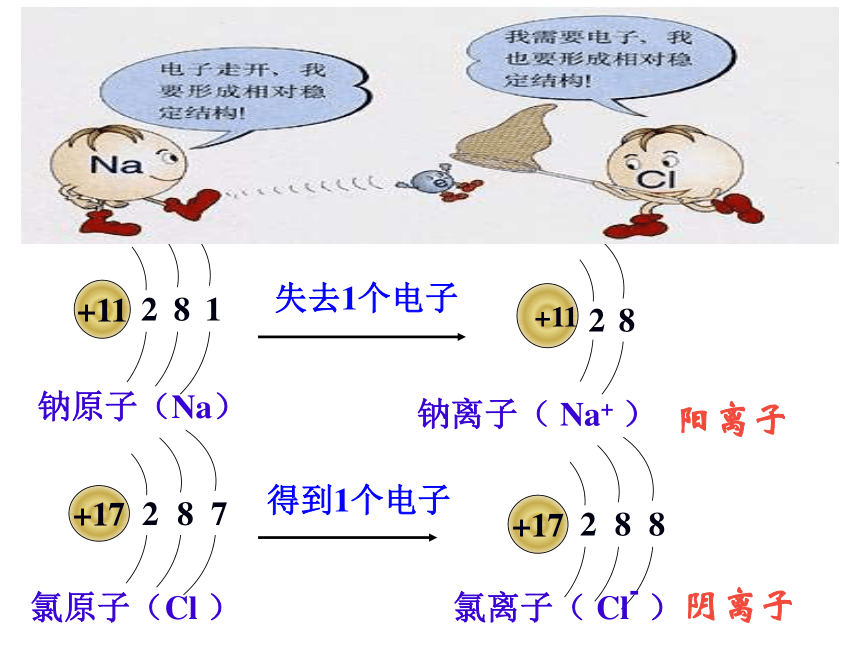
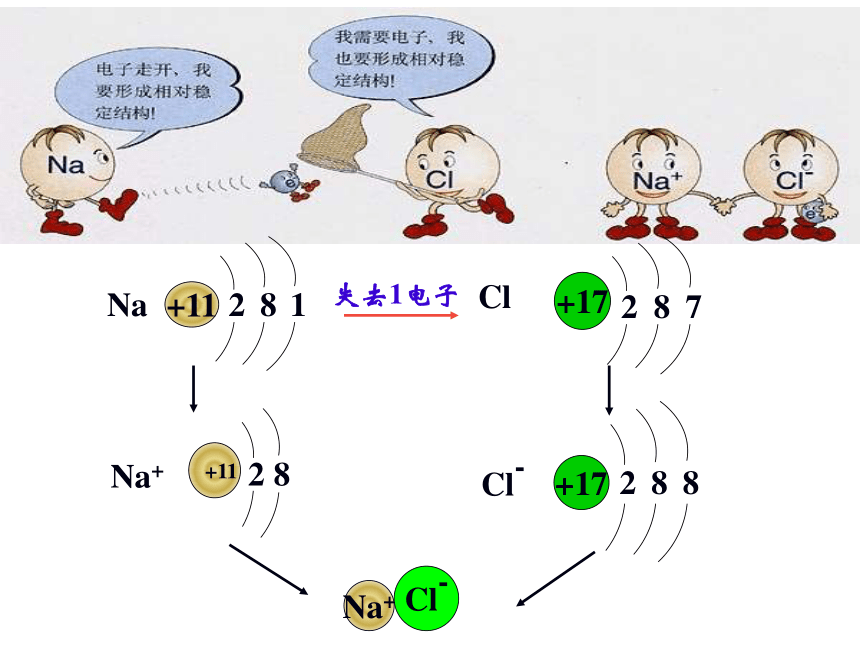
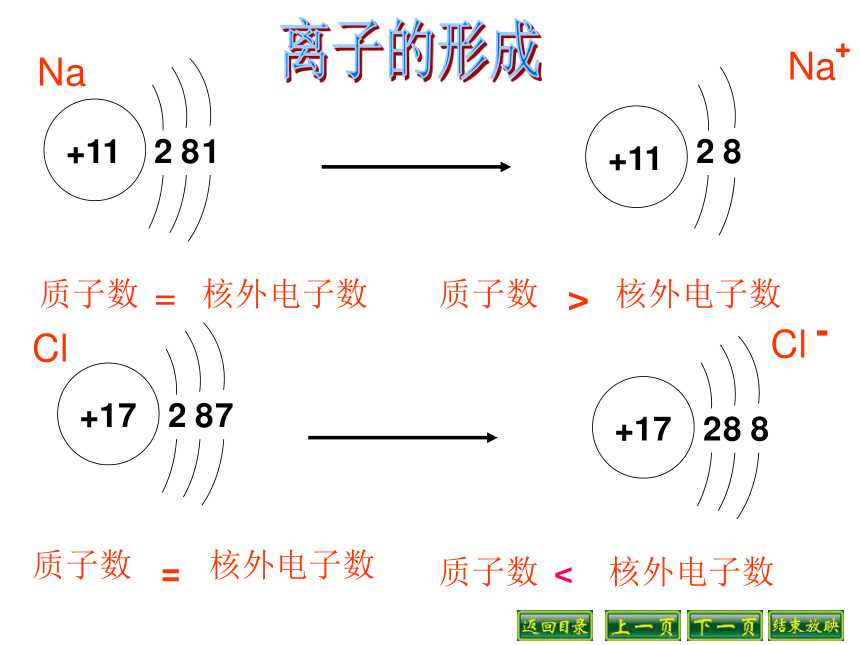
课件9张PPT。四、离子怎样形成钠原子(Na)钠离子( Na+ )氯原子(Cl )氯离子( Cl- )阳离子阴离子失去1电子+11281+1128质子数核外电子数=质子数核外电子数>+17287+17288NaCl质子数核外电子数=质子数
核外电子数<离子的形成离子的形成原子阴离子( - )阳离子( + )1、概念:带电的原子或原子团,如S2-、SO42-。
离子带的电荷数等于该原子(或原子团)
失去或得到电子的数目。离 子:带电荷的原子或原子团
阳离子:带正电荷的原子或原子团
阴离子:带负电荷的原子或原子团举例Als离子归纳总结SO42-离子化合物:由阴、阳离子相互作用而形成的化合物常见的离子化合物有:注意由金属元素和非金属元素形成的化合物一般都是离子化合物1.原子和阴、阳离子之间是怎样相互转化的?2.原子与离子之间有什么区别和联系?
失电子得电子得电子失电子阴离子阳离子 原子 讨论综合应用3、将①分子②原子③质子④中子⑤电子等粒子用序号分别填入下列适当空格中:
(1)构成物质的基本粒子是________
(2)构成原子的基本粒子是_______
(3)显电中性(不带电)的粒子是_________
(4)带正电的粒子是______
(5)化学变化中种类一定改变的粒子是______,决定原子种类的粒子是 。
(6)原子中数目一定相等的粒子是________
①②③④⑤①②④③①③⑤ ③
核外电子数<离子的形成离子的形成原子阴离子( - )阳离子( + )1、概念:带电的原子或原子团,如S2-、SO42-。
离子带的电荷数等于该原子(或原子团)
失去或得到电子的数目。离 子:带电荷的原子或原子团
阳离子:带正电荷的原子或原子团
阴离子:带负电荷的原子或原子团举例Als离子归纳总结SO42-离子化合物:由阴、阳离子相互作用而形成的化合物常见的离子化合物有:注意由金属元素和非金属元素形成的化合物一般都是离子化合物1.原子和阴、阳离子之间是怎样相互转化的?2.原子与离子之间有什么区别和联系?
失电子得电子得电子失电子阴离子阳离子 原子 讨论综合应用3、将①分子②原子③质子④中子⑤电子等粒子用序号分别填入下列适当空格中:
(1)构成物质的基本粒子是________
(2)构成原子的基本粒子是_______
(3)显电中性(不带电)的粒子是_________
(4)带正电的粒子是______
(5)化学变化中种类一定改变的粒子是______,决定原子种类的粒子是 。
(6)原子中数目一定相等的粒子是________
①②③④⑤①②④③①③⑤ ③
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
