第五章 化工生产中的重要非金属元素 复习课件(共20张PPT)
文档属性
| 名称 | 第五章 化工生产中的重要非金属元素 复习课件(共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-12 00:00:00 | ||
图片预览





文档简介
(共20张PPT)
第五章 化工生产中的重要非金属元素 复习
单击此处添加副标题
学习目标
1.能从物质类别和化合价的角度研究物质的性质和转化。
2.通过对烟气脱硫、脱硝的思考,形成研究物质转化的一般思路,使所学知识系统化、结构化。
3.知道在工业生产中除了要关注反应能否发生,还需要对反应条件进行调控。
4.能体会物质转化在工业生产中的重要价值,能认识到化学对社会进步的价值,提升科学态度和社会责任感的核心素养。
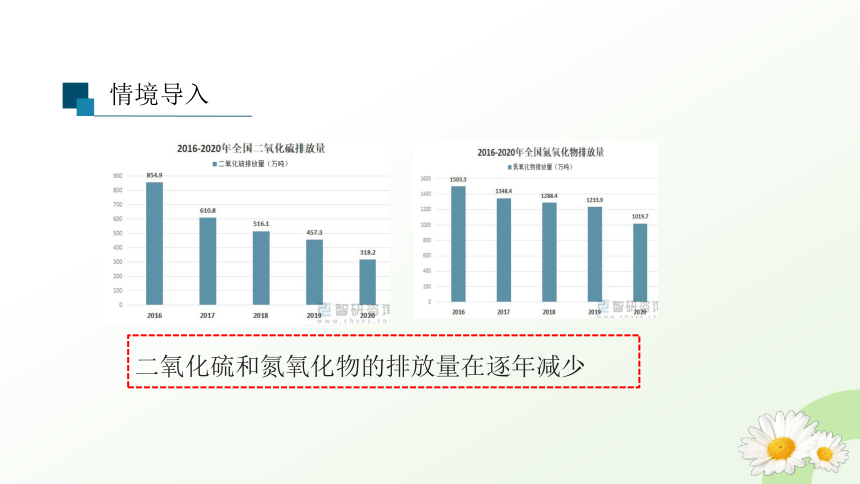
情境导入
2018.10
2022.10
情境导入
二氧化硫和氮氧化物的排放量在逐年减少
工业烟气如何进行脱硫和脱硝?
烟气脱硫脱硝是指脱去烟气中的SO2和NOx
【任务一】构建模型:明确研究物质性质和转化的基本思路
化合价
特性
物质类别
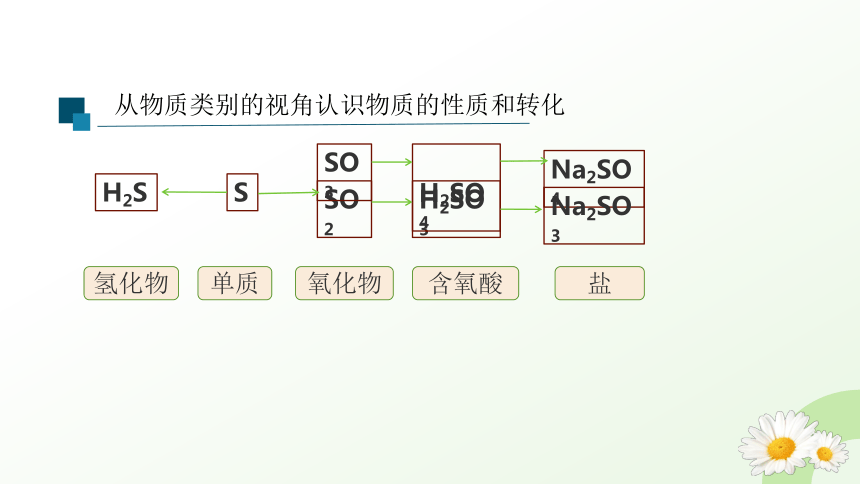
从物质类别的视角认识物质的性质和转化
氢化物
氧化物
单质
含氧酸
盐
H2S
S
SO2
SO3
H2SO3
H2SO4
Na2SO4
Na2SO3
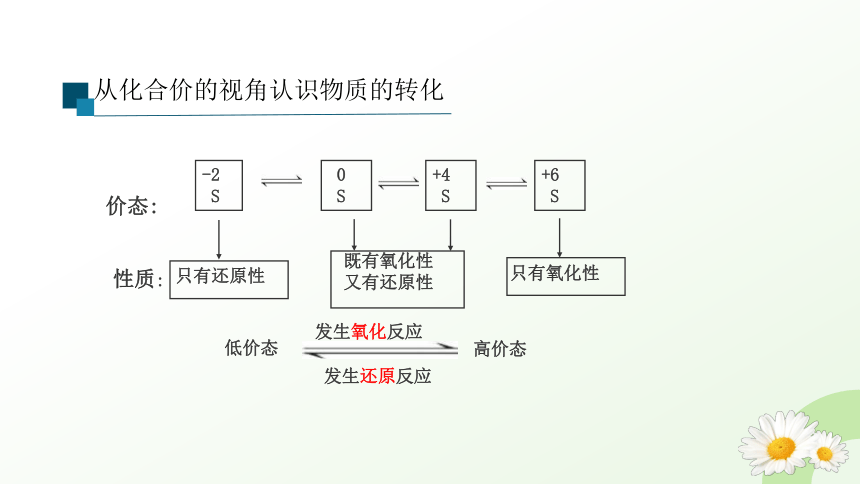
从化合价的视角认识物质的转化
发生氧化反应
价态:
性质:
只有还原性
既有氧化性
又有还原性
只有氧化性
低价态
高价态
-2
S
0
S
+4
S
+6
S
发生还原反应
+6
+4
0
-2
化合价
类别
氢化物
单质
氧化物
酸
盐
H2S
S
SO2
SO3
H2SO3
H2SO4
SO42-
SO32-
FeS
Na2S、NaHS
FeS2
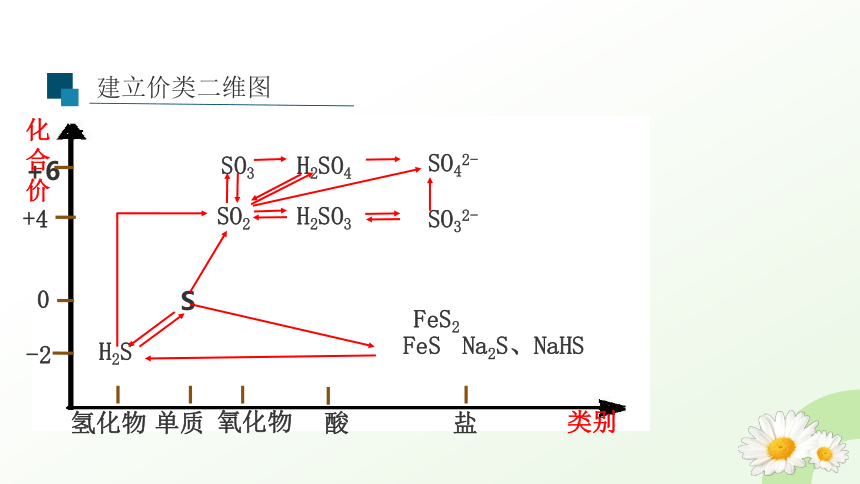
建立价类二维图
+6
+4
0
-2
化合价
类别
氢化物
单质
氧化物
酸
盐
H2S
S
SO2
SO3
H2SO3
H2SO4
SO42-
SO32-
FeS
Na2S、NaHS
FeS2
【任务二】应用模型讨论脱除二氧化硫的方法
酸碱转化
类维
氧化还原
价维
【任务二】应用模型讨论脱除二氧化硫的方法
方案1:类维: CaO+SO2 CaSO3
价维:2CaSO3+O2===2CaSO4
方案2:类维: 2NH3+SO2 + H2O===(NH4)2SO3,
价维:2(NH4)2SO3+O2===2(NH4)2SO4
方案4: 价维:SO2+H2O2===H2SO4
方案3:类维:2NaOH+SO2===Na2SO3+H2O
Na2CO3+SO2===Na2SO3+CO2
Na2SO3+SO2+H2O===2NaHSO3
【任务二】应用模型讨论脱除二氧化硫的方法
化合价
0
+2
+4
-3
NH3
N2
NO
NO2
HNO2
HNO3
NaNO2
NaNO3
稀、浓
NH4Cl
+5
+3
N2O5
NH3·H2O
盐
氧化物
类别
氢化物
碱
单质
酸
(类维)
氧化还原
价维
╳
【任务三】应用模型讨论脱除NOx的方法
方案1 :(价维)
NO2+NO+2NaOH===2NaNO2+H2O
2NO2+2NaOH===NaNO3+NaNO2+H2O
方案2:(价维)
8NH3+6NO2 7N2+12H2O
4NH3+6NO 5N2+6H2O
【任务三】应用模型讨论脱除NOx的方法
【任务四】工业生产中条件的选择
石灰石—石膏烟气脱硫是工业传统的脱硫技术,是除去SO2的一种常用方法。其过程如图1:
烟气脱硫效率与pH有关
【任务四】工业生产中条件的选择
煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在不同温度下,NaClO2溶液脱硫、脱硝的反应中SO2和NO的平衡分压pc如图所示。
温度越高,SO2和NO的平衡分压pc越高,脱硫脱硝效率越低
【任务四】工业生产中条件的选择
煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。
NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果,Ca(ClO)2的优点是能生成硫酸钙沉淀,促进反应向右进行,SO2的转化率提高
【思路梳理】
物质转化
反应条件
价类二维
温度、压强、pH、浓度
成本、对设备的要求
科学思维
工程思维
绿色化学
原子利用率高、物质循环使用、环保
反应、速率、产率
【任务五】课堂练习
煤燃烧排放的烟气含有SO2和NOx,是大气的重要污染源之一。用Ca(ClO)2溶液对烟气[n(SO2)∶n(NO)=3∶2]同时脱硫脱硝(分别生成SO42-、NO3-),得到NO、SO2脱除率如图所示,请思考:
1、脱除NO的反应
2、SO2脱除率高于NO的原因
2NO+3ClO-+H2O===2H++3Cl-+2NO3-
SO2在水中的溶解度大于NO在水中的溶解度
3、随着脱除反应的进行,吸收剂溶液的pH怎么变化?
吸收剂的pH逐渐减小,因为根据反应原理生成大量H+
【课后作业】
1、小组合作:查阅资料,找出几种工业脱硫脱硝的方法,并从反应原理和反应条件两方面评价方案的合理性。
2、完成作业练习中的题目。
第五章 化工生产中的重要非金属元素 复习
单击此处添加副标题
学习目标
1.能从物质类别和化合价的角度研究物质的性质和转化。
2.通过对烟气脱硫、脱硝的思考,形成研究物质转化的一般思路,使所学知识系统化、结构化。
3.知道在工业生产中除了要关注反应能否发生,还需要对反应条件进行调控。
4.能体会物质转化在工业生产中的重要价值,能认识到化学对社会进步的价值,提升科学态度和社会责任感的核心素养。
情境导入
2018.10
2022.10
情境导入
二氧化硫和氮氧化物的排放量在逐年减少
工业烟气如何进行脱硫和脱硝?
烟气脱硫脱硝是指脱去烟气中的SO2和NOx
【任务一】构建模型:明确研究物质性质和转化的基本思路
化合价
特性
物质类别
从物质类别的视角认识物质的性质和转化
氢化物
氧化物
单质
含氧酸
盐
H2S
S
SO2
SO3
H2SO3
H2SO4
Na2SO4
Na2SO3
从化合价的视角认识物质的转化
发生氧化反应
价态:
性质:
只有还原性
既有氧化性
又有还原性
只有氧化性
低价态
高价态
-2
S
0
S
+4
S
+6
S
发生还原反应
+6
+4
0
-2
化合价
类别
氢化物
单质
氧化物
酸
盐
H2S
S
SO2
SO3
H2SO3
H2SO4
SO42-
SO32-
FeS
Na2S、NaHS
FeS2
建立价类二维图
+6
+4
0
-2
化合价
类别
氢化物
单质
氧化物
酸
盐
H2S
S
SO2
SO3
H2SO3
H2SO4
SO42-
SO32-
FeS
Na2S、NaHS
FeS2
【任务二】应用模型讨论脱除二氧化硫的方法
酸碱转化
类维
氧化还原
价维
【任务二】应用模型讨论脱除二氧化硫的方法
方案1:类维: CaO+SO2 CaSO3
价维:2CaSO3+O2===2CaSO4
方案2:类维: 2NH3+SO2 + H2O===(NH4)2SO3,
价维:2(NH4)2SO3+O2===2(NH4)2SO4
方案4: 价维:SO2+H2O2===H2SO4
方案3:类维:2NaOH+SO2===Na2SO3+H2O
Na2CO3+SO2===Na2SO3+CO2
Na2SO3+SO2+H2O===2NaHSO3
【任务二】应用模型讨论脱除二氧化硫的方法
化合价
0
+2
+4
-3
NH3
N2
NO
NO2
HNO2
HNO3
NaNO2
NaNO3
稀、浓
NH4Cl
+5
+3
N2O5
NH3·H2O
盐
氧化物
类别
氢化物
碱
单质
酸
(类维)
氧化还原
价维
╳
【任务三】应用模型讨论脱除NOx的方法
方案1 :(价维)
NO2+NO+2NaOH===2NaNO2+H2O
2NO2+2NaOH===NaNO3+NaNO2+H2O
方案2:(价维)
8NH3+6NO2 7N2+12H2O
4NH3+6NO 5N2+6H2O
【任务三】应用模型讨论脱除NOx的方法
【任务四】工业生产中条件的选择
石灰石—石膏烟气脱硫是工业传统的脱硫技术,是除去SO2的一种常用方法。其过程如图1:
烟气脱硫效率与pH有关
【任务四】工业生产中条件的选择
煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在不同温度下,NaClO2溶液脱硫、脱硝的反应中SO2和NO的平衡分压pc如图所示。
温度越高,SO2和NO的平衡分压pc越高,脱硫脱硝效率越低
【任务四】工业生产中条件的选择
煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。
NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果,Ca(ClO)2的优点是能生成硫酸钙沉淀,促进反应向右进行,SO2的转化率提高
【思路梳理】
物质转化
反应条件
价类二维
温度、压强、pH、浓度
成本、对设备的要求
科学思维
工程思维
绿色化学
原子利用率高、物质循环使用、环保
反应、速率、产率
【任务五】课堂练习
煤燃烧排放的烟气含有SO2和NOx,是大气的重要污染源之一。用Ca(ClO)2溶液对烟气[n(SO2)∶n(NO)=3∶2]同时脱硫脱硝(分别生成SO42-、NO3-),得到NO、SO2脱除率如图所示,请思考:
1、脱除NO的反应
2、SO2脱除率高于NO的原因
2NO+3ClO-+H2O===2H++3Cl-+2NO3-
SO2在水中的溶解度大于NO在水中的溶解度
3、随着脱除反应的进行,吸收剂溶液的pH怎么变化?
吸收剂的pH逐渐减小,因为根据反应原理生成大量H+
【课后作业】
1、小组合作:查阅资料,找出几种工业脱硫脱硝的方法,并从反应原理和反应条件两方面评价方案的合理性。
2、完成作业练习中的题目。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
