化学人教版(2019)必修第二册7.2乙烯与有机高分子材料(共164张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.2乙烯与有机高分子材料(共164张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-16 00:00:00 | ||
图片预览







文档简介
(共164张PPT)
乙烯与有机高分子材料
化学2 第七章 第2节
碳碳双键键能大还是碳碳单键键能大?键长呢?
③碳碳双键键能大于碳碳单键,键长则小于碳碳单键
乙烯分子的空间构型是怎样的?
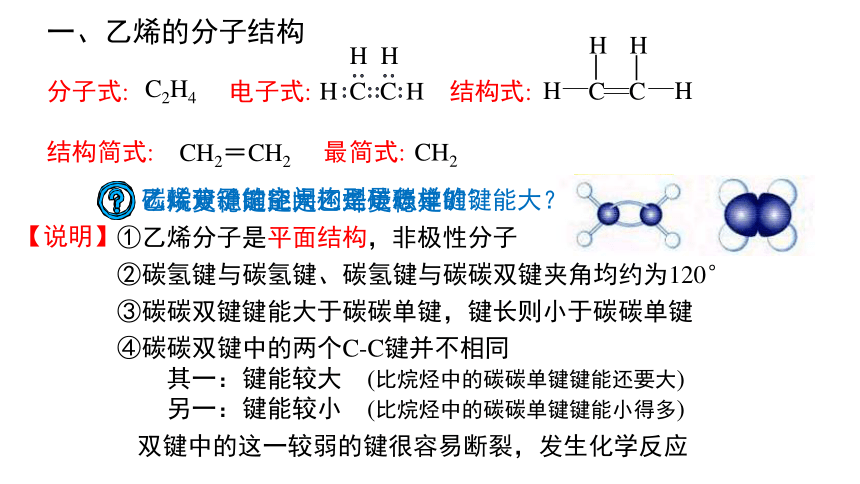
一、乙烯的分子结构
分子式: 电子式: 结构式:
结构简式: 最简式:
C
—
—
C
—
—
|
|
H
H
H
H
C
C
H
H
H
H
①乙烯分子是平面结构,非极性分子
②碳氢键与碳氢键、碳氢键与碳碳双键夹角均约为120°
④碳碳双键中的两个C-C键并不相同
其一:键能较大 (比烷烃中的碳碳单键键能还要大)
另一:键能较小 (比烷烃中的碳碳单键键能小得多)
乙烷更稳定还是乙烯更稳定?
双键中的这一较弱的键很容易断裂,发生化学反应
【说明】
C2H4
CH2=CH2
CH2
(2)乙烯是一种无色无味,易溶于水的气体( )
(1)乙烯的结构简式可书写为CH2CH2( )
判断正误
×
提示 乙烯分子中含有>C=C<,在书写时,官能团>C=C<不能省略,应为CH2=CH2。
×
提示 乙烯是一种稍有气味,难溶于水的气体。
(3)乙烯的充填模型为 ( )
(4)乙烯分子中所有原子共平面,可推断丙稀(CH2=CH—CH3)所有原子也共平面( )
(5)乙烯分子中的价键没有全部被氢原子“饱和”,因此乙烯属于不饱和烃( )
√
×
×
返回
三、乙烯的化学性质
1、氧化反应
为什么甲烷在空气中燃烧时无烟而乙烯有烟?
① C2H4能被KMnO4(H+)氧化
高锰酸钾溶液的紫色退去
——鉴别甲烷与乙烯
② 火焰明亮,伴有黑烟
C2H4 + 3O2 2CO2 + 2H2O
点燃
乙烯中碳的质量分数较高 ,燃烧时碳没有充分燃烧,因而产生黑烟——微小碳粒
烷烃通常状态下是稳定的,那么乙烯呢?
可否用于除去甲烷中的乙烯?
二、乙烯的物理性质
无色、稍有气味、气体,密度略小于空气,难溶于水
Br
—
C
|
C
—
—
|
|
H
H
H
H
+
Br
|
|
|
Br
C
┅
—
C
—
—
|
|
H
H
H
H
+
Br
┅
|
—
C
—
|
H
H
Cl
H
+
—
H
Cl
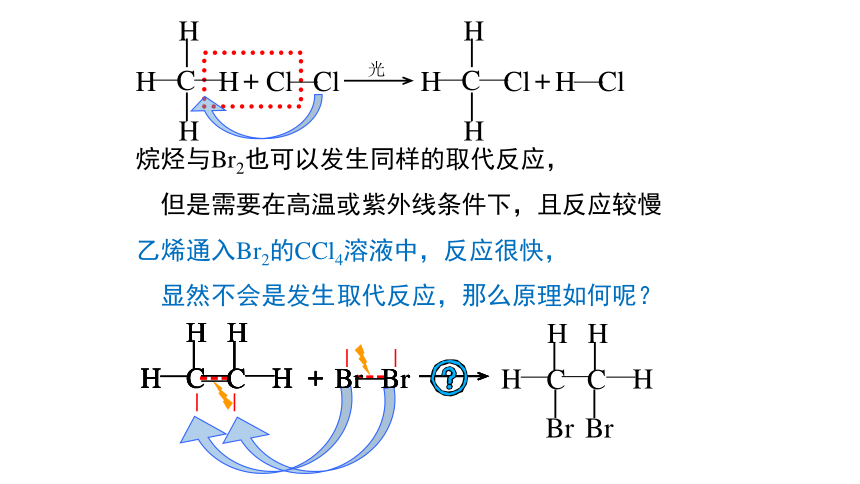
烷烃与Br2也可以发生同样的取代反应,
但是需要在高温或紫外线条件下,且反应较慢
|
—
C
—
|
H
H
H
H
+
—
Cl
Cl
光
C
—
C
—
—
|
|
H
H
H
H
|
|
Br
Br
C
—
—
C
—
—
|
|
H
H
H
H
—
Br
Br
+
乙烯通入Br2的CCl4溶液中,反应很快,
显然不会是发生取代反应,那么原理如何呢?
邬
C
—
—
C
—
—
|
|
H
H
H
H
+
—
Br
Br
【说明】
C2H4与Cl2、H2、HCl、H2O等众多物质均能发生加成反应
C
—
C
—
—
|
|
H
H
H
H
|
|
H
Cl
C
—
—
C
—
—
|
|
H
H
H
H
—
H
Cl
+
催化剂
C
—
C
—
—
|
|
H
H
H
H
|
|
H
OH
C
—
—
C
—
—
|
|
H
H
H
H
—
H
OH
+
催化剂
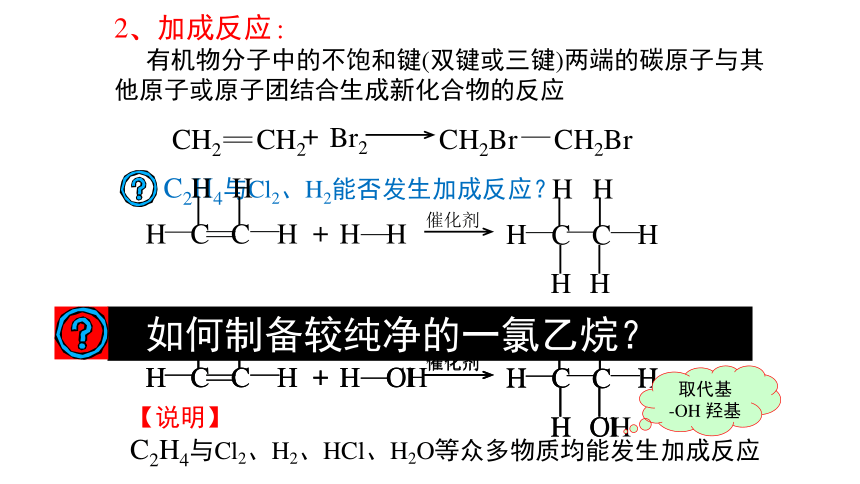
2、加成反应:
有机物分子中的不饱和键(双键或三键)两端的碳原子与其他原子或原子团结合生成新化合物的反应
Br2
+
CH2
CH2
—
—
CH2Br
CH2Br
—
C2H4与Cl2、H2能否发生加成反应?
C2H4与H2O能否发生加成反应?
C
—
C
—
—
|
|
H
H
H
H
|
|
H
H
C
—
—
C
—
—
|
|
H
H
H
H
—
H
H
+
催化剂
如何制备较纯净的一氯乙烷?
取代基
-OH 羟基
C
-
-
H
H
-
-
H
H
C
=
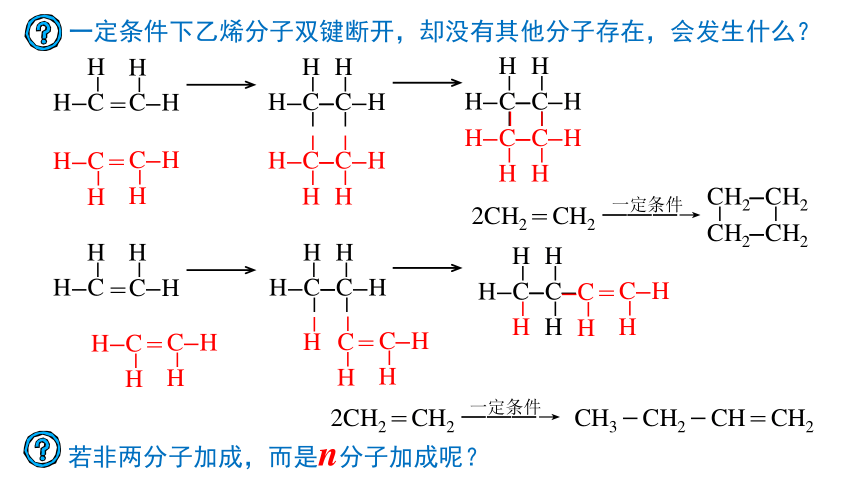
一定条件下乙烯分子双键断开,却没有其他分子存在,会发生什么?
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
H
H
-
-
H
H
C
=
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
H
H
-
-
H
H
C
=
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
H
H
H
-
-
H
C
-
=
C
-
-
H
H
-
-
H
H
C
=
C
-
-
-
-
H
H
C
-
-
-
-
H
H
H
C
-
-
H
H
-
-
H
C
=
若非两分子加成,而是n分子加成呢?
2CH2=CH2 ———→
-
CH2
-
-
CH2
-
CH2
-
CH2
-
一定条件
2CH2=CH2 ———→ CH3-CH2-CH=CH2
一定条件
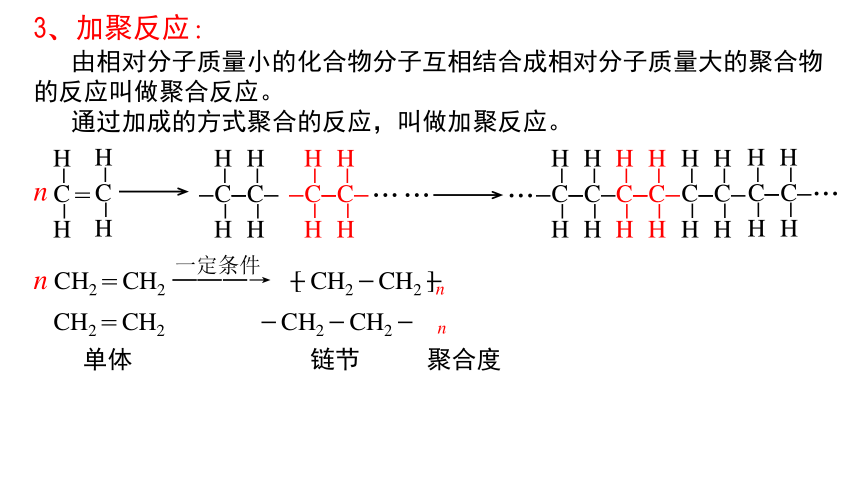
3、加聚反应:
由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反应。
通过加成的方式聚合的反应,叫做加聚反应。
C
-
-
H
H
-
-
H
H
C
=
n
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
……
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
H
H
…
…
[ ]
n CH2=CH2 ———→ -CH2-CH2-
一定条件
n
CH2=CH2
单体
-CH2-CH2-
链节
n
聚合度
三、乙烯的用途
乙烯是石油化学工业最重要的基础原料!
乙烯工业的发展水平是衡量一个国家石油化工水平的重要标志之一!
乙烯主要用于制造塑料、合成纤维、有机溶剂等。
乙烯可用于果实催熟(生果多果酸、丹宁)。
乙烯与生长素、赤霉素、细胞分裂素、 脱落酸一样,均为植物激素。
乙烯作用: 能使植物停止生长、变矮、落叶、落果;促进菠萝开花;刺激橡胶树和漆树吐胶泌液,增加产量;对黄瓜、甜瓜这些雌雄异花同株的植物,还可以改变花的性别,使雄花变为雌花。
乙烯作用极大,几乎所有植物的器官中都有,但含量极低。
(1)乙烯和乙烷都为碳氢化合物,因此性质相同( )
(2)乙烯的化学性质比乙烷活泼( )
(3)乙烯能使酸性KMnO4溶液和溴水褪色,反应原理相同( )
(4)酸性KMnO4既可以验证乙烷和乙烯,还可以除去乙烷中混有的乙烯
( )
判断正误
×
×
提示 乙烯使酸性KMnO4溶液褪色发生的是氧化反应,乙烯使溴水褪色发生的是加成反应。
√
×
(5)乙烯聚合生成聚乙烯,本质是每个乙烯分子中的碳碳双键的一个键断裂,相互结合生成聚乙烯,因此也称为加聚反应( )
(6)燃烧等质量的乙烯和聚乙烯耗氧量相同( )
提示 乙烯和聚乙烯的最简式相同。
(7)乙烷中混有乙烯,可通过与H2在一定条件下反应,使乙烯转化为乙烷
( )
提示 C2H4和H2反应可能使气体中又混有氢气。
×
√
√
分子式 C2H6 C2H4
结构式
碳碳键类别 碳碳单键 碳碳双键
原子相对位置 C、H不全在一个平面内 6个原子都在同一平面内
燃烧 2C2H6+7O2—→4CO2+6H2O C2H4+3O2—→2CO2+2H2O
特征反应 C2H6+Cl2—→C2H5Cl+HCl CH2=CH2+Br2—→CH2BrCH2Br
与高锰酸钾 酸性溶液 不反应 因发生氧化反应而使其褪色
乙烷与乙烯的分子结构和化学性质对比
解析 A项,乙烯和氢气加成反应生成CH3CH3,正确;
B项,CH3CHCl2不能通过乙烯的加成反应制得,错误;
C项,CH2==CH2和H2O加成可生成CH3CH2OH,正确;
D项,CH2==CH2可以和HBr加成生成CH3CH2Br,正确。
1.下列物质中,可以通过乙烯的加成反应得到的是______(填字母)。
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
深度思考
ACD
2.体育比赛中当运动员肌肉挫伤或扭伤时,队医常用药剂氯乙烷(CH3CH2Cl)
(沸点为12.27 ℃)对受伤部位进行局部冷却麻醉处理,工业上制取氯乙烷有两种方案:
a.CH3CH3+Cl2 CH3CH2Cl+HCl
b.CH2==CH2+HCl CH3—CH2Cl
你认为制备氯乙烷的最好方案为_____(填“a”或“b”),并说出选择该方案及不选择另一方案的理由:___________________________________
__________________________________________________________________________________________________________________________________________________________________。
b
a方案中CH3CH3和Cl2在光照条件下发生取代反应,反应产物中除CH3CH2Cl和HCl外,还有很多副产物,产物不纯,产率低;b方案中CH2==CH2和HCl在一定条件下发生加成反应,产物中只有CH3CH2Cl,产品纯度高、产率高
解析 CH3CH3和Cl2发生取代反应,生成的产物中除CH3CH2Cl外,还有很多副产物,CH2==CH2和HCl加成只产生CH3CH2Cl,故选择b方案。
3.运输水果时,为了吸收水果产生的乙烯,防止水果早熟腐烂,常将浸泡有_________溶液的硅藻土放置在盛放水果的容器中。
解析 KMnO4溶液可以吸收乙烯,同时产生CO2气体,故可以防止水果早熟腐烂。
高锰酸钾
返回
解析 乙烯分子中碳原子间形成的是双键,有两对共用电子对,A项错误;
碳原子的半径应比氢原子的大,B项错误;
乙烯的结构简式为CH2==CH2,D项错误。
1.(2020·黑龙江阿城区第一中学高一检测)对乙烯的结构,下列说法正确的是
A.乙烯的电子式为 B.乙烯的球棍模型为
C.乙烯分子在空间上呈平面结构 D.乙烯的结构简式为CH2CH2
1
2
3
5
随堂演练 知识落实
4
√
6
解析 分子中的碳氢原子个数比只能说明烃的组成,不能说明其结构特点;燃烧产物的物质的量相等和被酸性KMnO4溶液氧化,不能说明乙烯分子中含有一个碳碳双键;1 mol乙烯只能与1 mol溴单质加成,说明乙烯分子中含有一个碳碳双键。
2.(2019·自贡高一检测)能证明乙烯分子中含有一个碳碳双键的事实是
A.乙烯分子中碳、氢原子的个数比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色
1
2
3
5
4
√
6
3.(2020·郑州柘城第二高级中学检测)下列各反应不属于加成反应的是
A.CH2==CH2+H—OH CH3—CH2—OH
B.CH3CH==CH2+Br2―→CH3CHBrCH2Br
C. +H2 CH3—CH2—OH
D.CH3—CH3+2Cl2 CH2Cl—CH2Cl+2HCl
√
1
2
3
5
4
解析 D项中反应为取代反应。
6
4.(2019·武汉高一期中)①②是两种常见烃的球棍模型,则下列叙述正确的是
A.都能在空气中燃烧
B.都能使酸性高锰酸钾溶液褪色
C.都能发生加成反应
D.等质量的①②完全燃烧时,产生CO2的量相同
√
1
2
3
5
4
6
解析 由题图可知,①为乙烷,②为乙烯。乙烷不能使酸性高锰酸钾溶液褪色,而乙烯能,B项错误;
乙烷不能发生加成反应,而乙烯能,C项错误;
乙烷和乙烯的摩尔质量不同,等质量时二者的物质的量不同,产生CO2的量也不同,D项错误。
1
2
3
5
4
6
解析 1 mol CH2==CH2与HCl完全加成生成1 mol CH3CH2Cl,1 mol CH3CH2Cl中含5 mol H,故彻底取代需消耗5 mol Cl2,D项正确。
5.(2020·北京市第九中学月考)1 mol乙烯与HCl完全加成后再被Cl2彻底取代,则消耗氯气的物质的量是
A.2 mol B.2.5 mol C.4 mol D.5 mol
1
2
3
5
4
√
6
解析 乙烯和溴发生加成反应生成CH2BrCH2Br,甲烷不反应,因此用溴水除去CH2==CH2,然后通过浓H2SO4干燥,故B项满足,
乙烯可以被酸性KMnO4氧化最后生成CO2,因此,甲烷中会混有新杂质CO2,故C项错误。
6.(2020·安徽东至县第一中学高一月考)甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶
A.澄清石灰水,浓H2SO4 B.溴水,浓H2SO4
C.酸性高锰酸钾溶液,浓H2SO4 D.浓H2SO4,酸性高锰酸钾溶液
1
2
3
5
4
√
返回
6
1.现有a、b、c三种碳氢化合物,其球棍模型如图
下列有关说法错误的是
A.分子中所有原子共平面的只有b
B.a和c分子结构相似,互为同系物
C.b分子的结构简式为
D.b分子中含有 ,c分子中所有的共价键都为单键
课时对点练
题组一 乙烯的组成及结构
√
对点训练
解析 因为a、b、c三种分子都为碳氢化合物,由三种物质的球棍模型,可知a为甲烷,b为乙烯,c为乙烷,据碳原子成键特点,CH4和CH3CH3分子应为以碳为中心的四面体结构,乙烯分子中六个原子共平面,其结构简式为CH2==CH2,故C错误。
1
2
3
4
5
6
7
8
9
2.(2020·西藏林芝市第二高级中学月考)由乙烯推测丙烯(CH2==CHCH3)的结构或性质,以下关于丙烯的说法不正确的是
A.分子中3个碳原子不在同一直线上
B.与HCl在一定条件下加成只得到一种产物
C.最多有7个原子在同一平面上
D.在空气中燃烧时火焰明亮并伴有黑烟
√
1
2
3
4
5
6
7
8
9
解析 CH2==CHCH3与HCl在一定条件下加成可以得到 、
两种产物。
1
2
3
4
5
6
7
8
9
3.(2019·衡阳高一期末)氯乙烷是一种沸点较低(沸点为12.27 ℃),极易挥发的无色液体,常作为运动员肌肉挫伤或扭伤的冷冻麻醉剂,下列有关氯乙烷的制法,最好的是
A.乙烷与氯气发生取代反应 B.乙烯与氯气发生加成反应
C.乙烷与氯化氢混合 D.乙烯与氯化氢发生加成反应
√
1
2
3
4
5
6
7
8
9
题组二 乙烯的性质与用途
解析 乙烷与氯气发生取代反应生成多种氯代烃的混合物;乙烯与氯气发生加成反应生成1,2-二氯乙烷(CH2ClCH2Cl);乙烷与氯化氢不反应;乙烯与氯化氢发生加成反应生成氯乙烷。
4.(2019·江苏兴化一中高一下期末)既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的试剂是
A.溴水 B.氧气
C.酸性高锰酸钾溶液 D.氢气
1
2
3
4
5
6
7
8
9
√
1
2
3
4
5
6
7
8
9
解析 乙烷与溴水不反应,而乙烯与溴水发生加成反应生成1,2-二溴乙烷,使溴水褪色,所以可以鉴别二者,也可以除去乙烷中混有的乙烯杂质,A正确;
乙烯与酸性高锰酸钾溶液反应,使溶液褪色,而乙烷与酸性高锰酸钾溶液不反应,故可以鉴别二者,但由于乙烯被酸性高锰酸钾溶液氧化生成CO2气体,引入新杂质,故不能用于除去乙烷中混有的乙烯杂质,C错误;
乙烯与氢气在一定条件下发生反应,但反应现象不明显,不能用于鉴别二者,D错误。
5.(2020·贵州岑巩一中高一检测)如图表示球棍模型,小球表示原子序数小于10的原子,短线表示化学键,每个原子都到达稳定结构。下列有关说法正确的是
A.M分子的所有原子共面
B.0.1 mol·L-1的N溶液中H+的物质的量浓度为0.1 mol·L-1
C.L存在同分异构体
D.L能使酸性KMnO4溶液褪色
√
1
2
3
4
5
6
7
8
9
解析 小球表示原子序数小于10的原子,短线表示化学键,每个原子都达到稳定结构,由图可知,发生CH2==CH2+HF―→CH3CH2F。M为乙烯,含碳碳双键,为平面结构,M分子的所有原子共面,故A正确;
N为HF,为弱酸,不完全电离,因此0.1 mol·L-1的N溶液中H+的物质的量浓度小于0.1 mol·L-1,故B错误;
由乙烷中6个H相同可知,L为CH3CH2F,只有一种结构,不存在同分异构体,故C错误。
1
2
3
4
5
6
7
8
9
1
2
3
4
5
6
7
8
9
6.(2020·甘肃兰州一中月考)下列说法中错误的是
A.乙烯与Br2的加成,乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳
双键有关
B.用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.相同物质的量的乙烯和甲烷完全燃烧消耗的氧气的量相同
D.利用燃烧的方法可以鉴别乙烯和甲烷
√
题组三 加成反应概念理解及判断
1
2
3
4
5
6
7
8
9
解析 乙烯中含 ,能发生加成反应和氧化反应,双键断裂,A正确;
乙烯能与溴的四氯化碳溶液或酸性KMnO4溶液反应,使溶液褪色,而乙烷不能,故能鉴别,B正确;
乙烯和甲烷的分子式不同,1 mol乙烯需要耗氧3 mol,1 mol CH4耗氧为2 mol,
故两者完全燃烧耗氧量不相同,C错误;
乙烯比甲烷的含碳量高,燃烧时甲烷产生淡蓝色火焰,乙烯燃烧时火焰明亮并伴有黑烟,现象不同,能鉴别,D正确。
7.(2020·天津外国语大学附属中学高一期末)降冰片二烯在紫外线照射下可以发生下列转化。
下列说法错误的是
A.降冰片二烯与四环烷互为同分异构体
B.降冰片二烯能使酸性高锰酸钾溶液褪色
C.四环烷的一氯代物超过三种(不考虑立体异构)
D.降冰片二烯分子中位于同一平面的碳原子不超过4个
1
2
3
4
5
6
7
8
9
√
综合强化
解析 降冰片二烯与四环烷分子式相同,
结构不同,因此二者互为同分异构体,A
正确;
降冰片二烯分子中含有碳碳双键,因此能使酸性高锰酸钾溶液褪色,B正确;
四环烷含有三种化学环境不同的H原子,因此其一氯代物有三种,C错误;
根据乙烯分子是平面分子,与碳碳双键连接的C原子在碳碳双键所在的平面上,可知降冰片二烯分子中位于同一平面的碳原子最多为4个,D正确。
1
2
3
4
5
6
7
8
9
8.(2020·山东招远第一中学高一检测)将CH4和C2H4的混合气体15 g通入盛有足量溴水的容器中,溴水的质量增加了7 g,则混合气体中CH4和C2H4的体积之比为
A.1∶2 B.2∶1 C.3∶2 D.2∶3
1
2
3
4
5
6
7
8
9
√
解析 甲烷不能与溴水反应,乙烯可与Br2发生加成反应,因此,溴水质量增加是因为吸收了乙烯,故乙烯物质的量为 =0.25 mol,则
甲烷物质的量为 =0.5 mol,相同条件下气体体积之比等于其物质的量之比,即CH4与C2H4体积之比为2∶1。
解析 乙烯含有碳碳双键,能够与溴发生加成反应而使溴水褪色,反应方程式为CH2==CH2+Br2―→CH2Br—CH2Br。
9.(2019·山西太原一中期末)乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙烯
的原理和乙烯的主要
化学性质,实验装置
如图所示。
(1)用化学方程式解释
B装置中的实验现象:
_______________________________。
1
2
3
4
5
6
7
8
9
CH2==CH2+Br2―→CH2Br—CH2Br
解析 乙烯具有还原性,能够与酸性高锰酸钾溶液发生氧化还原反应而使酸性高锰酸钾溶液褪色。
(2)C装置中的现象是_________________________,其发生反应的类型是_____________。
1
2
3
4
5
6
7
8
9
酸性高锰酸钾溶液褪色
氧化还原反应
解析 乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙溶液反应生成碳酸钙沉淀,溶液变浑浊。
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置____(填字母)中的实验现象可判断该资料是否真实。
1
2
3
4
5
6
7
8
9
D
(4)通过上述实验探究可知,检验甲烷和乙烯的方法是______(填字母,下同);除去甲烷中乙烯的方法是____。
A.将气体通入水中
B.将气体通过装溴水的洗气瓶
C.将气体通过装酸性高锰酸钾
溶液的洗气瓶
D.将气体通入氢氧化钠溶液中
1
2
3
4
5
6
7
8
9
BC
B
解析 A项,甲烷、乙烯均不溶
于水,且常温下与水都不反应,
不能用于鉴别和除杂;
B项,乙烯中含有 ,能
与溴水发生加成反应生成1,2-二溴乙烷液体,甲烷不与溴水反应,所以可用溴水除去甲烷中混有的乙烯,也可以鉴别甲烷与乙烯;
C项,甲烷与高锰酸钾溶液不反应,乙烯能够与高锰酸钾溶液反应而使其褪色,可以鉴别甲烷与乙烯;但是乙烯被氧化生成二氧化碳气体,故不能用于除去甲烷中混有的乙烯杂质;
1
2
3
4
5
6
7
8
9
D项,甲烷、乙烯都不溶于氢氧化钠溶液,不能用来鉴别和除杂。综上所述,可用来鉴别的是B、C项,可用来除杂的是B项。
1
2
3
4
5
6
7
8
9
返回
四、烯烃
通式
单烯烃:CnH2n
结构
含有碳碳双键(>C=C<)
分类
单烯烃、二烯烃、环烯烃……
化学性质
⑴氧化反应
能使KMnO4酸性溶液和溴水[Br2(H2O)]褪色
⑵加成反应
能使溴的四氯化碳溶液[Br2(CCl4)]褪色
火焰明亮,伴有黑烟
CH3-CH=CH2 + Br2 ——→ CH3-CHBr-CH2Br
CH3-CH=CH-CH3+ HBr ——→CH3-CH2-CHBr-CH3
CH3-CH=CH2+ HBr ——→
CH3-CH-CH3
-
Br
CH3-CH2-CH2Br
马氏规则Markovnikov's rule锦上添花
⑶加聚反应
nCH3-CH=CH2——→
CH3-CH=CH-CH3
CH2=CH-CH=CH2
-CH-CH2-
[
]n
CH3
-
CnH2n+ O2 ——→ n CO2+ n H2O
点燃
⑷取代反应
CH2=CH-CH3 + Cl2 ——→ CH2=CH-CH2Cl + HCl
500℃
n
-CH2-CH=CH-CH2-
[
]n
———→
一定条件
分子式:
电子式:
结构式:
结构简式:
最简式:
空间构型:
球棍模型:
空间充填模型:
五、炔烃 乙炔
通式
单炔烃:CnH2n-2
结构
含有碳碳双键(-C≡C-)
分类
单炔烃、二炔烃、环炔烃…
C
C
H
H
H-C≡C-H
HC≡CH
CH≡CH
CH
C2H2
直线形
CH2=CH-C≡C-CH3分子中最多有几个原子共平面?几个原子共直线?
炔烃的化学性质
⑴氧化反应
能使KMnO4酸性溶液和溴水[Br2(H2O)]褪色
⑵加成反应
能使溴的四氯化碳溶液[Br2(CCl4)]褪色
CnH2n-2+ O2 → nCO2 + (n-1)H2O
火焰明亮,浓烈黑烟
CH≡CH + Br2
CHBr=CHBr
CHBr=CHBr + Br2
CHBr2-CHBr2
CH≡CH + HBr
CH2=CHBr
⑶加聚反应
n CH≡CH
-CH=CH-
[
]n
CH2=CHBr + HBr
CH3-CHBr2
CH2Br-CH2Br
聚氯乙烯-PVC (Polyvinyl chloride)是世界上产量最大用途最广的通用塑料,如何制备?涉及什么反应类型?
-CH-CH2-
[
]n
Cl
-
CH≡CH + HCl
CH2=CHCl
n CH2=CHCl
[ CH2-CHCl ]n
-
-
分子式:
结构式:
结构简式:
空间构型:
球棍模型:
空间充填模型:
六、芳香烃 苯
通式
苯的同系物:CnH2n-6
结构
含有苯环
分类
苯的同系物、多环芳烃
C6H6
平面结构
苯分子的结构特点
C构成平面正六边形,12个原子共面,
C、H原子所处环境完全相同,
碳原子间是一种介于碳碳单键
和碳碳双键之间的特殊共价键
什么事实可以证明苯不是
单双键交替出现的结构?
苯的物理性质
无色、有特殊气味、液体,密度比水小,难溶于水,是一种重要溶剂。m.p. 5.5℃,b.p. 80.1℃,易挥发。
⑴氧化反应
不能使酸性KMnO4溶液和溴水褪色
2C6H6+15O2 → 12CO2+6H2O
火焰明亮 浓烈黑烟
⑵取代反应
HO-NO2
+ H2O
+ HNO3 ——→
浓硫酸
50~60℃
浓硫酸:
催化剂、吸水剂
苯的硝化
苯的溴代
+ HBr
+ Br2 ——→
FeBr3
+ H2O
+ H2SO4 ——→
△
苯的磺化
HO-SO3H
⑶加成反应
不能使溴水[Br2(H2O)]褪色,但能使溴水层褪色——萃取
+ 3H2 ———→
催化剂
加热加压
“666”有机氯杀虫剂20th 50s广泛使用,现已禁用。它可由苯与氯气在一定
条件下反应得到,分子式为C6H6Cl6,该反应属于哪种反应类型?
苯的化学性质
1.烃的概念
仅含___和___两种元素的有机化合物称为碳氢化合物,也称为烃。
2.烃的分类
(1)依据:烃分子中碳原子间_________的不同及________的不同。
一、烃
碳
氢
成键方式
碳骨架
(2)分类
CH2==CH2
—C≡C—
烃 甲烷 乙烯 乙炔
电子式 _________ _____________ ____________
化学键 ______ _____和 ____________________ _____和_________
分子结构特点 _________ _____ _____
3.常见烃的分子结构
C—H
H—C
H—C
—C≡C—
正四面体
平面
直线
(2)甲烷、乙烯和乙炔分子中都只含有碳和氢两元素,故它们是同系物
( )
(1)一种有机物完全燃烧,产物只有CO2和H2O,则该有机物一定属于烃
( )
判断正误
×
提示 该有机物中可能含氧元素,如CH3CH2OH不是烃。
×
提示 三者的结构不同,甲烷分子中全部为单键,乙烯分子中含有碳碳双键,乙炔分子中含有碳碳三键,而且分子组成上也不相差一个或若干个CH2原子团,故不为同系物。
(4)属于烃的有机化合物分子中的氢原子数一定为偶数个( )
提示 和 分子中都不含有苯环( ),不属于芳香烃。
(5) 和 都属于芳香烃( )
(3)乙烯的分子式为C2H4,故分子组成为C6H12的烃一定属于烯烃( )
√
×
提示 分子组成为C6H12的烃,可能是烯烃,也可能属于环烷烃,如环己烷。
提示 根据碳原子的4价键理论,烃分子中的氢原子一定为偶数。
×
(6)苯的分子式为C6H6,结构简式为 ,分子高度不饱和,故苯分子中
一定含有碳碳双键,属于烯烃( )
×
提示 苯分子中含有 ,结构简式 是一种习惯写法,分子中不含
有 ,属于芳香烃。
A B C D
①球棍模型 ②能和Cl2在光照条件下生成多种氯代物 ①能使溴水褪色 ②标准状况下,气体密度为1.25 g·L-1 ①既不能使溴水褪色,也不能使酸性KMnO4溶液褪色 ②平面结构 ③球棍模型 ①能使溴水褪色
②1 mol能和2 mol H2加成
③充填模型
1.如表是A、B、C、D四种烃的有关信息。
深度思考
(1)烃A的电子式:______________,烃B分子的空间结构为__________,烃D的结构式为______________,空间结构为________。
(2)四种烃中,和甲烷互为同系物的是________(填结构简式,下同),完全燃烧,生成CO2和H2O的物质的量之比为1∶1的是__________。
(3)写出烃B和H2O在一定条件下反应的化学方程式:_________________
______________________。
平面结构
H—C≡C—H
直线形
CH3CH3
CH2==CH2
CH2==CH2+H2O
(4)已知B和D具有相似的化学性质,试写出烃D和Br2按物质的量之比为
1∶1反应的化学方程式:__________________________,将烃D通入酸性KMnO4溶液的现象是____________________。
CH≡CH+Br2―→
紫红色褪去(或变浅)
(5)下列有关烃C的说法正确的是________。
A.烃C的分子式为C6H6,属于不饱和烃
B.从烃C的组成上看,分子结构应该存在碳碳双键,故应属于烯烃
C.烃C分子中的12个原子都在同一平面内
D.烃C分子中的化学键应当比较特殊,化学键不同于一般的碳碳单键和
碳碳双键
E.1 mol C分子和H2在一定条件下反应,最多需要3 mol H2
ACDE
解析 根据信息及四种烃的结构,可推断烃A为乙烷(CH3CH3),烃B为乙
烯(CH2==CH2),烃C为苯( ),烃D为乙炔(CH≡CH)。乙烷为饱和
烷烃,和甲烷互为同系物;乙烯、乙炔和苯为不饱和烃,其中乙烯和乙炔性质相似,可以发生加成反应和氧化反应,故乙炔和Br2按1∶1加成反应的方程式为CH≡CH+Br2―→ ,乙炔通入酸性高锰酸钾溶液
中紫红色褪去;苯分子的化学式为C6H6,根据信息和碳原子的四价键关系,分子中不存在一般的碳碳单键和双键,而是一种特殊的共价键。
解析 根据乙炔、乙烯和甲烷的结构,有机物M的分子结构为 ,
则最多有4个原子共直线,因为单键可以旋转,甲基上3个H原子中,可以有一个H原子旋进面内,因此最多有9个原子共面,故选C。
2.已知乙烯分子为平面结构,C2H2为直线结构。则有机物M(CH≡C—CH==CH—CH3)分子中,共直线和共平面的原子数最多分别为
A.6、11 B.5、10 C.4、9 D.4、11
√
返回
七、有机高分子材料
天然有机高分子材料:
合成有机高分子材料:
棉花、羊毛、天然橡胶……
塑料、合成纤维、合成橡胶、黏合剂、涂料……
七、有机高分子材料
⑴
二、有机高分子材料
1.有机高分子材料的分类
有机高分子材料
_____有机高分子材料:如棉花、羊毛、天然橡胶
_____有机高分子材料:如_____、__________、
_________、黏合剂、涂料等
天然
合成
塑料
合成纤维
合成橡胶
2.有机高分子材料
(1)塑料
①组成
提高塑性:______
防止老化:______
增强材料
着色剂
主要成分:_________
添加剂
合成树脂
增塑剂
防老剂
②性能:强度___、密度___、_______、易加工等。
高
小
耐腐蚀
名称 结构简式 用途
聚乙烯 可制成食品包装袋等
聚氯乙烯 可制成电线的绝缘层、管道等
聚苯乙烯 可制成泡沫包装材料、绝缘材料等
③常见塑料及用途
聚四氟乙烯 可制成实验仪器、化工用品等
聚丙烯 可制成管道、包装材料等
有机玻璃(聚甲 基丙烯酸甲酯) 可制成飞机和车辆的风挡、光学仪器等
脲醛塑料(电玉) 可制成电器开关、插座等
(2)橡胶
①橡胶是一类具有高弹性的高分子材料,是制造汽车、飞机轮胎和各种密封材料所必需的原料。天然橡胶的主要成分是____________,结构简式为 ,其单体为 ;天然橡
胶分子中含有 ,易发生_____反应和_____反应。
聚异戊二烯
加成
氧化
②橡胶的分类
③性能:具有高弹性、绝缘性、气密性、耐油、耐高温或耐低温等性能。
④用途:制造汽车、飞机轮胎;各种密封材料。
(3)纤维
①纤维的分类
动物纤维——羊毛、蚕丝等
植物纤维——棉花、麻等
____
纤维
纤维
____
纤维
_____纤维——黏胶纤维、大豆蛋白纤维等
____纤维
(六大纶)
____(聚丙烯纤维)
____(聚氯乙烯纤维)
____(聚丙烯腈纤维)
____(聚对苯二甲酸乙二酯纤维)
__________(聚酰胺纤维)
天然
再生
化学
合成
丙纶
氯纶
腈纶
涤纶
锦纶、芳纶
②合成纤维性能:强度___、弹性___、耐磨、耐化学腐蚀,不易虫蛀等。
③主要用途:制_____、绳索、渔网等,广泛应用于工农业领域。
高
好
衣料
(1)通常所说的三大合成材料是塑料、合成纤维和合成橡胶( )
(2)塑料包装袋都可以包装食品( )
(3)有机高分子材料是一类结构非常复杂的有机物( )
提示 有机高分子材料虽然相对分子质量很大,但一般结构简单,是由很多重复的链节构成。
(4)真丝、塑料和涤纶都是合成高分子材料( )
提示 真丝是天然高分子材料,塑料和涤纶是合成高分子材料。
判断正误
×
×
√
×
(5)纯净的聚乙烯塑料为纯净物( )
提示 有机高分子材料是由很多重复的链节构成,聚合度n不同,故为混合物,不为纯净物。
(6)乙烯和聚乙烯都能使溴的CCl4溶液褪色( )
提示 聚乙烯结构为 ,链节中不存在碳碳双键,不能使溴的CCl4溶液褪色。
(7)天然橡胶硫化的过程没有发生化学变化( )
提示 橡胶硫化是线型高分子链之间通过硫原子形成化学键,产生交联,形成网状结构,发生的是化学变化。
×
×
×
(8)以石油、煤、天然气为原料可以生产某些有机高分子材料( )
提示 以石油、天然气和煤为原料制成有机高分子单体,再聚合生成塑料、合成纤维等有机高分子材料。
√
解析 高聚物 的链节为 ,单体为CH2==CH
—CN。
1.腈纶又名“人造羊毛”,其结构简式为 ,按要求回答问题。
(1)“人造羊毛”的链节为_____________,单体为_______________。
深度思考
CH2==CH—CN
(2)实验测得“人造羊毛”的相对分子质量(平均值)为32 800,则该高聚物的聚合度n为_____。
619
解析 高聚物的链节的化学式为C3H3N,式量为53,链节的个数也就是
聚合度n,故n=
(3)工业上以乙炔和HCN为原料合成腈纶,合成路线如下:
写出有关的化学方程式并注明反应类型:
①_______________________________________________;
②_______________________________________________。
。
nCH2==CH—CN ,加聚反应
CH≡CH CH==CH2—CN
解析 根据反应流程,CH≡CH和HCN先发生加成反应生成CH2==CHCN,再发生加聚反应生成聚丙烯腈,故化学方程式为①CH≡CH+HCN
CH2==CH—CN;
②nCH2==CH—CN 。
2.ABS树脂( )是一种强度高、韧性
好、易于加工成型的热塑型高分子材料。用于制备仪表、电气、电器、机械等各种零件。
(1)ABS树脂的链节为____________________________________。
(2)合成ABS树脂的单体为_________________、_____________________、
________________。
CH2==CH—CN
CH2==CH—CH==CH2
CH2==CH—C6H5
加聚反应单体的判断方法
方法总结
方法一:弯箭头法(一边赶法),去掉[ ]和n,将链节中的一个键从左向右折叠,单变双,双变单,遇到碳超过4价,则断开。
如维通橡胶 ―→
―→CH2==CF2和CF2==CF—CF3。
方法二:单变双,双变单,超过四价则断开。
如:丁苯橡胶
―→
―→CH2==CH—CH==CH2和 。
返回
解析 烃是分子中只有碳和氢元素的有机物,A错误;
含苯环的碳氢化合物才属于芳香烃,C错误;
乙烯和乙炔分子结构不同,不为同系物,D错误。
1.下列有关烃的说法正确的是
A.烃分子中除了含碳和氢之外,还可能含其他元素
B.根据烃分子中碳原子间成键方式不同,可把烃分为饱和烃与不饱和烃
C.分子中含有苯环的有机物就是芳香烃
D.乙烯和乙炔分子中都含有不饱和键,故它们互为同系物
1
2
3
5
随堂演练 知识落实
4
√
6
2.(2020·江苏苏州中学高一月考)下列有机分子中,所有原子不可能在同一平面内的是
A.CH2==CHCl B.CH3CH2CH3
C. D.CF2==CF2
1
2
3
5
4
√
6
解析 CH2==CHCl和CF2==CF2可看作CH2==CH2分子中的H原子被Cl或F原子代替后的产物,因乙烯为平面结构,故A和D中所有原子共面;
因苯环中6个碳和6个H原子共平面,HC≡CH中4个原子共直线,故C项所有原子共面;
丙烷分子中碳原子为饱和结构,空间结构为四面体结构,故丙烷分子中所有原子不可能共面。
1
2
3
5
4
6
3.(2019·山西平遥祝中学高一期末)下列对烃的分类不正确的是
A.CH4、CH2==CH2、CH2==CHCH==CH2均属于饱和烃
B.CH3CH2CH3、CH3CH==CH2、CH3CH==CHCH2CH==CH2均属于链状烃
C.CH3CH3、 、C18H38均属于饱和烃
D. 、 、 均属于芳香烃
√
1
2
3
5
4
6
解析 CH2==CH2、CH2==CHCH==CH2分子中含有碳碳双键,属于不饱和烃,A项错误;
链状烃指的是分子中无环状结构的烃,B项正确;
CH3CH3、 、C18H38三种分子中每个C原子均达到饱和状态,属于饱和烃,C项正确;
含苯环的烃属于芳香烃,D项正确。
1
2
3
5
4
6
4.人们在日常生活中大量使用各种高分子材料,下列说法中正确的是
A.天然橡胶易溶于水
B.羊毛是合成高分子化合物
C.聚乙烯塑料是天然高分子材料
D.聚氯乙烯塑料会造成“白色污染”
√
1
2
3
5
4
6
解析 聚氯乙烯塑料在自然界中难以降解会造成“白色污染”,天然橡胶、羊毛和聚乙烯塑料都是高分子材料,难溶于水,羊毛是天然的,而聚乙烯塑料是合成的高分子材料。综上所述,D项正确。
5.(2020·哈尔滨第二中学高一检测)下列说法正确的是
A.乙烯通过聚合反应可得到高分子材料
B.聚丙烯的结构单元是—CH2—CH2—CH2—
C.碳纤维属于合成有机高分子化合物
D.聚乙烯塑料的老化是因为发生了加成反应
1
2
3
5
4
√
6
解析 乙烯加聚得到的聚乙烯是高分子材料,A正确;
聚丙烯是丙烯发生加成聚合反应生成的,结构单元是 ,B
错误;
碳纤维是一种含碳量在95%以上的新型无机非金属材料,C错误;
聚乙烯分子中不含有碳碳双键,不能发生加成反应,D错误。
1
2
3
5
4
6
6.橡胶树是热带植物,在我国海南已有大面积种植。从橡胶树的胶乳中可提取天然橡胶,天然橡胶的成分是聚异戊二烯,其结构为
。
试回答下列问题:
天然橡胶加入适当硫进行硫化后,其结构由_____变成_____,天然橡胶的单体是一种无色液体,将该无色液体加入溴水中,溴水_____(填“能”或“不能”)褪色。
1
2
3
5
4
6
线型
网状
能
解析 天然橡胶中加入硫,使线型的高分子链之间通过硫原子形成化学键,产生交联,形成网状结构,天然橡胶的单体为 ,
分子中含有不饱和双键,可以和Br2加成,因此能使溴水褪色。
1
2
3
5
4
返回
6
1.(2019·南京高一检测)科学家对探测器发回的数据进行了分析,发现土卫六的大气层中含有95%的氮气,剩余的气体为甲烷和其他碳氢化合物。下列关于碳氢化合物的叙述正确的是
A.碳氢化合物的通式为CnH2n+2
B.燃烧产物为二氧化碳和水的化合物一定是碳氢化合物
C.有些烷烃在光照下不能与氯气发生取代反应
D.碳氢化合物分子的相对分子质量一定是偶数
课时对点练
1
2
3
4
5
6
7
8
9
题组一 常见烃的结构、性质及分类
√
对点训练
10
解析 CnH2n+2是链状烷烃的通式,而不是所有碳氢化合物的通式,A错误;
燃烧产物为CO2和H2O的化合物不一定为碳氢化合物,有可能含有氧元素,B错误;
烷烃都能在光照下与Cl2发生取代反应,C错误;
因为碳的原子量为偶数且成的价键为4个,结合的氢原子一定为偶数,因此碳氢化合物的相对分子量一定为偶数,D正确。
1
2
3
4
5
6
7
8
9
10
解析 H2CO3属于无机物,A错;
属于有机酸,含有氧元素,所以不为烃,B正确;
CH2==CH—CH3和CH≡CH分别属于烯烃和炔烃,都为烃,故C、D错误。
2.(2020·湖南茶陵三中月考)下列有机物中,属于有机物,但不属于烃的是
A.H2CO3 B.
C.CH2==CH—CH3 D.CH≡CH
√
1
2
3
4
5
6
7
8
9
10
3.(2019·黑龙江伊春第二中学期末)下列属于烯烃的是
A.CH3CH2CH3 B.CH2==CHCH3
C.CH2==CHCH2Cl D.CH2==CHCOOH
√
1
2
3
4
5
6
7
8
9
解析 CH3CH2CH3属于烷烃,CH2==CHCH2Cl含有氯元素,不为烃,CH2==CHCOOH含有氧元素,也不为烃,CH2==CH—CH3为丙烯,属于烯烃。
10
4.(2019·广东湛江一中月考)丙烯是合成聚丙烯塑料的化工原料,反应的方程式为nCH2==CH—CH3―→ ,下列有关说法错误的是
A.丙烯通过加聚反应合成聚丙烯
B.丙烯和聚丙烯均能使酸性高锰酸钾溶液褪色
C.丙烯为纯净物,聚丙烯为混合物
D.聚丙烯的平均相对分子质量为42n(n为聚合度)
1
2
3
4
5
6
7
8
9
√
题组二 常见的有机高分子材料
10
1
2
3
4
5
6
7
8
9
解析 丙烯通过加聚反应生成聚丙烯, 中的n不确定,因
此聚丙烯为混合物,其平均相对分子质量为42n。故A、C、D正确;
在聚丙烯的链中,不存在 ,故不能使酸性KMnO4溶液褪色,B错误。
10
5.(2019·深圳科学高中期中)橡胶属于重要的工业原料,它是一种有机高分子化合物,具有良好的弹性,但强度较差。为了增加某些橡胶制品的强度,加工时往往需要进行硫化处理,即使橡胶原料与硫黄在一定条件下反应。橡胶制品硫化程度越高,强度越大,同时弹性越差。下列橡胶制品中,加工时硫化程度较高的是
A.医用橡胶手套 B.皮鞋胶底
C.自行车内胎 D.橡皮筋
√
1
2
3
4
5
6
7
8
9
10
解析 根据橡胶制品硫化程度越高,强度越大,弹性越差的特点,可知皮鞋胶底应当强度大,弹性较橡胶手套、自行车内胎及橡皮筋要差,故皮鞋胶底的硫化程度较高。
1
2
3
4
5
6
7
8
9
10
1
2
3
4
5
6
7
8
9
6.(2020·山西太原一中高一检测)聚氯乙烯塑料在工农业生产中广泛应用,其结构简式为 ,它是由CH≡CH、HCl两种小分子经过系列
反应形成的,由聚氯乙烯分析合成过程中发生的反应类型有
①取代反应 ②加成反应 ③加聚反应 ④氧化反应
A.①③ B.②③ C.①②③ D.①③④
√
10
1
2
3
4
5
6
7
8
9
解析 由聚氯乙烯的结构简式可知,其单体为 ,据题给原料,
应由CH≡CH和HCl加成反应制得,因此制聚氯乙烯的过程应
有加成反应和加聚反应。
10
7.(2019·山东师范大学附中高一期末)桥环烃是指由两个碳环共用两个或两个以上碳原子的一类环烃,二环[1,1,0]丁烷( )是最简单一种桥环烃。下列关于该化合物的说法错误的是
A.与CH2==CHCH==CH2互为同分异构体
B.二氯代物共有4种
C.所含碳碳键不只是单键
D.每个碳原子均处于与其直接相连的原子构成的四面体内部
1
2
3
4
5
6
7
8
9
√
综合强化
10
解析 由二环[1,1,0]丁烷的结构简式可知其分子式为C4H6,它与CH2==CHCH==CH2互为同分异构体,A项正确;
二环[1,1,0]丁烷的二氯代物中,两个氯原子取代同一个碳原子上的氢原子的结构有1种,两个氯原子取代不同碳原子上的氢原子的结构有3种,共有4种,B项正确;
二环[1,1,0]丁烷分子中的碳碳键均是单键,C项错误;
二环[1,1,0]丁烷分子中,每个碳原子均形成4个单键,类似于甲烷分子中的碳原子,处于与其直接相连的原子构成的四面体内部,D项正确。
1
2
3
4
5
6
7
8
9
10
8.(2019·上海大学附属中学期中)丁腈橡胶( )
具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是
①CH2==CH—CH==CH2 ②CH3—C≡C—CH3 ③CH2==CH—CN
④CH3—CH==CHCN ⑤CH3—CH==CH2 ⑥CH3—CH==CH—CH3
A.①③ B.③⑥ C.②③ D.④⑤
1
2
3
4
5
6
7
8
9
√
10
解析 高聚物属于加聚产物,链节主链上存在碳碳双键结构,有6个碳原子,单体为两种。按如图所示断开
然后打开双键中的1个C—C,将半键闭合就得到高聚物单体:CH2==CH
—CH==CH2和CH2==CH—CN,故选A。
1
2
3
4
5
6
7
8
9
10
解析 CH≡CH和HCN加成生成CH2==CHCN,CH2==CHCN经过加聚反应生成聚丙烯腈。
9.(2020·甘肃陇南市一中高一检测)(1)写出以CH≡CH、HCN为原料制备聚丙烯腈(“人造羊毛”)的过程中所发生的反应类型___________________。
1
2
3
4
5
6
7
8
9
加成反应、加聚反应
10
(2)PVC(聚氯乙烯)和PE(聚乙烯)都是常用的塑料,它们的单体分别为____________和___________。
(3)PE(聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。辨别PE和PVC有三种方法,一是闻气味法:具有刺激性气味的是_________;二是测密度法:密度大的应是__________;三是燃烧法:PE的单体和PVC的单体在足量空气中燃烧的实验现象的明显区别是____
_______________________________________________________。
1
2
3
4
5
6
7
8
9
CH2==CHCl
CH2==CH2
聚氯乙烯
聚氯乙烯
聚乙烯更易燃烧,聚氯乙烯燃烧有白雾(HCl的小液滴)生成
10
解析 具有刺激性气味的是聚氯乙烯;聚氯乙烯中含有相对原子质量相对较大的氯原子,其密度比聚乙烯大;聚氯乙烯不易燃烧,燃烧时产生HCl,有白雾(含有HCl的小液滴)生成。
1
2
3
4
5
6
7
8
9
10
解析 PVDC的单体为CH2==CCl2,该单体的同分异构体为CHCl==CHCl。
(4)PVDC( )是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品等的包装。写出合成PVDC的单体的同分异构体的结构简式:_____________。
1
2
3
4
5
6
7
8
9
CHCl==CHCl
10
10.(2019·日照高一检测)聚四氟乙烯的耐热性和化学稳定性都超过其他塑料,甚至在“王水”中也不发生变化,故号称“塑料王”,在工业上有着广泛的用途。
(1)按照下列所示的合成路线,试在方框中填入合适的化合物的结构简式:
1
2
3
4
5
6
7
8
9
氯仿
二氟一氯甲烷
四氟乙烯
聚四氟乙烯
D
CHCl3
CHClF2
CF2==CF2
10
(2)写出下列化学方程式:
B→C:______________________________。
C→D:________________________________。
(3)聚四氟乙烯的链节为______________,单体为__________,四氟乙烯生成聚四氟乙烯的反应类型为_________。
1
2
3
4
5
6
7
8
9
—CF2—CF2—
加聚反应
CF2==CF2
解析 根据信息,氯仿为三氯甲烷(CHCl3),找出反应物与生成物之间的关系,写出化学方程式。
返回
10
1.(2020·吉林延边二中检测)设NA为阿伏加德罗常数,下列说法正确的是
A.22.4 L CH4分子中含有10NA个电子
B.16 g CH4分子中含有4NA个C—H
C.等体积的CH4和NH3所含氢原子数之比为4∶3
D.等质量的CH4和HF所含共价键数目之比为4∶1
17
一、常见烃的成键特点与结构
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
√
17
解析 A、C两项均未说明气体所处状况,故无法计算;
D项,等质量的CH4和HF所含有共价键数目之比为
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
2.(2019·河北沧州一中高一月考)下列有关乙烯的说法中错误的是
A.乙烯分子的双键中有一个键较易断裂
B.乙烯分子中所有原子都在同一个平面上,且碳氢键之间的键角约为120°
C.乙烯的化学性质较甲烷活泼
D.乙烯和环己烷( )的分子组成符合通式CnH2n,因此它们互为同系物
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 乙烯分子中含有碳碳双键,其中一个键容易断裂,故乙烯化学性质比乙烷活泼,容易发生加成反应和氧化反应,A、C正确;
乙烯分子是平面结构,所有原子都在同一个平面上,且碳氢键之间的键角约为120°,B正确;
乙烯与环己烷的结构不相似,不是同类物质,不互为同系物,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
3.(2020·江西九江一中高一检测)某直链烷烃分子中有18个氢原子,它的分子式为
A.C8H18 B.C9H18 C.C10H18 D.C11H18
√
解析 直链烷烃的分子通式为CnH2n+2,由题意得2n+2=18,解得n=8,该直链烷烃的分子式是C8H18。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
4.(2019·河南信阳高级中学月考)已知某有机物含有4个C,每个碳原子都以键长相等的三条单键连接3个C,且整个结构中所有碳碳键之间的夹角都为60°,则下列说法不正确的是
A.该有机物不存在
B.该有机物的分子式为C4H4
C.该有机物的空间结构为正四面体
D.该有机物的一氯代物仅有1种
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 该有机物结构为 ,A错误,C正确;
据题给信息,推知该有机物分子式为C4H4,分子完全对称,只有一种位置的H原子,因此一氯代物仅有1种,B、D正确。
5.(2019·青海湟川中学检测)已知某种气态化石燃料中含有碳和氢两种元素。为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
实验前 实验后
干燥剂和U形管的总质量 101.1 g 102.9 g
石灰水和广口瓶的总质量 312.0 g 314.2 g
解析 生成水的质量为102.9 g-101.1 g=1.8 g,生成正盐即CaCO3的质
量为
根据实验数据求:
(1)实验完毕后,生成物中水的质量为_____g。假设广口瓶里生成一种正盐,其质量为____g。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1.8
5
(2)生成的水中氢元素的质量为_____g。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
0.2
(3)生成的CO2中碳元素的质量为_____g。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
0.6
(4)气态化石燃料中碳元素与氢元素的质量比为________,该烃的分子式为______。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
3∶1
CH4
解析 碳元素与氢元素的质量比为0.6 g∶0.2 g=3∶1,由此可求出碳和氢的原子个数之比为 ,根据碳原子的成键特点,该烃为CH4。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
二、同系物与同分异构体性质及判断
6.(2019·江西奉新一中高一期中)有A、B两种烃,碳元素的质量分数相同,下列关于A和B的叙述中正确的是
A.A和B一定是同分异构体
B.A和B不可能是同系物
C.燃烧等质量的A和B,消耗氧气的量一定相等
D.A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 因烃中只有碳、氢两种元素,碳元素的质量分数相同,所以氢元素的质量分数也相同,最简式相同,因此燃烧相同质量的两种物质,消耗氧气的量一定相等,C正确;
最简式相同的烃,可能是同分异构体,如丙烯与环丙烷,也可能不是,比如乙炔和苯,A错误;
最简式相同的烃,可能是同系物,如乙烯与丙烯,B错误;
若为同分异构体,则A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等;若为同系物,则A和B各1 mol完全燃烧后生成的二氧化碳的质量一定不相等,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
7.(2020·甘肃陇南一中检测)C5H12有3种不同的结构,甲:CH3(CH2)3CH3,乙:CH3CH(CH3)CH2CH3,丙:C(CH3)4,下列相关叙述正确的是
A.甲、乙、丙属同系物,均可与氯气、溴蒸气发生取代反应
B.C5H12表示一种纯净物
C.甲、乙、丙中,丙的沸点最低
D.乙有3种不同沸点的一氯取代物
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 甲、乙、丙的结构不同,分子式相同,互为同分异构体,A错误;
C5H12有3种同分异构体,所以不能表示纯净物,B错误;
烷烃的同分异构体中,支链越多,沸点越低,丙分子中支链最多,所以沸点最低,C正确;
乙分子中有4种位置的氢原子,即: ,故一氯代物
有4种,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
8.(2020·广西师大附属中高一期中)有以下结构的三种烃分子,下列有关说法错误的是
A.1 mol甲分子内含有10 mol共价键
B.由乙分子构成的物质不能使溴的四氯化碳溶液褪色
C.丙分子的二氯取代产物只有3种
D.三种分子内成键方式相同,而且最简式相同,故互为同系物
√
解析 1 mol甲分子中含有6 mol碳碳单键和4 mol碳氢键,A正确;
乙分子中不存在不饱和的 或“—C≡C—”,不能使溴的四氯化
碳溶液褪色,B正确;
丙分子有取代基位于棱边、面对角线、体对角线三种位置关系的二氯代物,C正确;
甲、乙、丙三种分子的分子式分别为C4H4、C6H6和C8H8,最简式相同,但分子组成上不是相差若干个CH2原子团,故不互为同系物,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
9.(2019·安徽黄山屯溪第一中学月考)a、b、c的分子式均为C8H8,其结构如下所示,下列说法错误的是
A.a的同分异构体可与苯互为同系物
B.c苯环上的一氯代物有3种
C.b能与溴水发生加成反应
D.c中所有原子可以处于同一平面
√
解析 a的同分异构体分子式为C8H8,苯的分子式为C6H6,分子组成上不相差若干个CH2原子团,故a的同分异构体和苯不互为同系物,A错误;
c分子苯环上有三种位置的H原子,故苯环上的一氯代物有3种,B正确;
b分子中含有 ,故可以和Br2发生加成反应,C正确;
苯环和 都是平面结构,且单键可以旋转,故C分子中所有原子可以共平面,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
三、常见烃的性质及应用
10.(2019·山东济宁二中高一期中)甲烷是天然气的主要成分,是一种高效、低耗、污染小的清洁能源。下列有关甲烷的说法正确的是
①甲烷是一种正四面体结构的分子
②甲烷与氯气按物质的量之比为1∶1发生取代反应时,生成物只有CH3Cl和HCl
③0.5 mol CH4完全燃烧时消耗1 mol O2
④1 mol CH4全部生成CCl4,最多消耗2 mol Cl2
A.①② B.③④ C.①③ D.②④
√
解析 ①甲烷是一种正四面体结构的分子,正确;
②甲烷与氯气按物质的量之比为1∶1发生取代反应时,生成物不是只有CH3Cl和HCl,还含有CH2Cl2、CHCl3、CCl4,错误;
③1 mol CH4完全燃烧时,消耗2 mol O2,则0.5 mol CH4完全燃烧时消耗
1 mol O2,正确;
④根据取代反应的特点,1 mol CH4全部生成CCl4,最多消耗4 mol Cl2,错误。综上分析, 答案选C。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
11.(2019·四川成都外国语学校高一月考)柠檬烯具有良好的镇咳、祛痰、抑菌作用,其结构如图所示。下列关于柠檬烯的说法正确的是
A.1 mol柠檬烯只能与1 mol Br2发生加成反应
B.能发生取代反应、加成反应和氧化反应
C.属于乙烯的同系物
D.不能使酸性高锰酸钾溶液褪色
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 A项,1 mol柠檬烯能与2 mol Br2发生加成反应,错误;
B项,柠檬烯能与气态卤素单质在光照条件下发生取代反应,分子中含有碳碳双键,能与H2发生加成反应,也可以被O2、酸性KMnO4溶液氧化,正确;
C项,一个柠檬烯分子中有两个碳碳双键,且分子中含有环状结构,与乙烯的结构不相同,故其不属于乙烯的同系物,错误;
D项,柠檬烯分子中含有碳碳双键,能使酸性高锰酸钾溶液褪色,错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
12.(2019·河北邢台一中高一第一次月考)已知1 mol链烃CxHy可以发生如下系列转化:
(无机试剂是足量的)
下列说法错误的是
A.x=5、n(Cl2)=11 mol
B.用酸性高锰酸钾溶液可以区分CxHy和Q
C.上述转化过程中依次发生了加成反应和取代反应
D.CxCl12可能的结构有三种
√
解析 CxHy可与HCl发生加成反应,则含有不饱和键,消耗HCl的物质的量为1 mol,则1个CxHy分子中含有1个碳碳双键,生成的Q为氯代烷烃,分子式为CxHy+1Cl,Q与氯气在光照条件下发生取代反应生成CxCl12,CxCl12中不含不饱和键,则x=5,y=10,消耗氯气的物质的量为11 mol,A正确;
C5H10中含有碳碳双键,能使酸性高锰酸钾溶液褪色,C5H11Cl不能使酸性高锰酸钾溶液褪色,可以区分,B正确;
C5H10与HCl发生加成反应,C5H11Cl与氯气发生取代反应,C正确;
新戊烷不存在对应烯烃,则符合题中转化关系的C5Cl12可能的结构只有两种,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
13.(2019·济南高一检测)石油是工业的血液,与我们的生产、生活息息相关,乙烯的产量通常用来
衡量一个国家的石油化工
水平。根据右面转化关系
回答下列问题:
(1)乙烯的结构简式为__________。
CH2==CH2
解析 乙烯为平面四边形结构,官能团为碳碳双键,结构简式为CH2==CH2。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
(2)写出乙烯和水反应生成B的反应③的化学方程式(注明条件):_________
_______________________,反应类型为__________。写出反应⑥的化学
方程式(注明条件):_________________________________。
CH2==CH2
加成反应
解析 乙烯和水发生反应生成乙醇,化学方程式为CH2==CH2+H2O
CH3CH2OH,该反应为加成反应,反应⑥为乙烷与氯气在光照条件下发生取代反应生成氯乙烷,反应方程式为CH3CH3+Cl2
CH3CH2Cl+HCl。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 氯乙烷可通过乙烯与氯化氢发生加成反应和乙烷与氯气发生取代反应制得,最好的方法是加成反应④,因为乙烷与氯气反应将得到多种氯代物的混合物,产物不纯。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
(3)物质C的沸点为12.27 ℃,常用于局部冷冻麻醉应急处理。物质C可通过反应④和反应⑥制得,其中
最好的方法是反应____(填“④”
或“⑥”),理由为_________
__________________________
_________________。
④
乙烷与氯气反应将得到多种氯代物的混合物,产物不纯
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
四、有机高分子材料及其应用
14.(2020·广西玉林高级中学高一检测)下列说法不正确的是
A.高分子材料的原料一般具有价廉、易得、适用于大规模生产的特点,
且来自含量较少的自然资源
B.棉花、羊毛和天然橡胶是有机高分子材料
C.合成高分子材料包括塑料、合成纤维、合成橡胶、黏合剂、涂料等
D.三大合成材料为塑料、合成纤维、合成橡胶
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 高分子材料的原料一般来自含量丰富的自然资源,故A错误;
棉花、羊毛和天然橡胶是天然有机高分子材料,故B正确;
合成高分子材料包括塑料、合成纤维、合成橡胶、黏合剂、涂料等,故C正确;
三大合成材料为塑料、合成纤维、合成橡胶,故D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
15.(2020·安徽阜阳一中高一检测)聚苯乙烯是日常生活中用途非常广泛的一种塑料,下列说法不正确的是
A.其单体为 ,经过加聚反应制得
B.链节为
C.平均相对分子质量为104n(n为聚合度)
D.是一种难降解的塑料,会造成环境污染
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 聚苯乙烯是由 经过加聚反应生成,单体为 ,
链节为 ,故A正确,B错误;
聚苯乙烯链节的相对分子质量为104,故聚苯乙烯的平均相对分子质量104n(n为聚合度),C正确;
聚苯乙烯是一种难降解的塑料,会导致环境污染,故D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
16.(2019·江苏海安高级中学期中)加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯。用如图所示装置探究废旧塑料的再利用。下列叙述不正确的是
A.聚丙烯塑料和丙烯都能使溴的四
氯化碳溶液褪色
B.装置乙的试管可收集到液态烃,
主要成分为苯和甲苯
C.装置丙内发生的反应为加成反应
D.最后收集到的气体是优良的燃料
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 聚丙烯塑料结构中无“ ”,不能使溴的四氯化碳溶液褪
色,A错误;
产物中的 和 沸点
较高,经液化可被收集,B正确;
乙烯、丙烯在丙装置中和Br2发生加成反应而被吸收,C正确;
最后气体为H2和CH4,是优良的燃料,D正确。
17.(2019·山东泰山一中高一检测)某高分子化合物结构如下:
其单体可能是
①CH2==CH—CN ②CH2==CH2
③CH2==CH—CH==CH2 ④
⑤ ⑥CH2==CH—CH2—CH3
A.①③⑤ B.②③⑤ C.①②⑥ D.①③④
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
√
解析 根据“见双键,四个碳;无双键,两个碳”划线断开,则该聚合物按照如下断键方式断裂: ,
断键后将半键闭合,即将单双键互换,得到的单体为CH2==CHCN、
CH2==CH—CH==CH2和 ,则A项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
17
18.(2020·江苏省江一中学高一检测)现有①甲烷、②乙烯、③丙烯、④苯、⑤苯乙烯5种烃,请用序号或按题中要求作答:
(1)分子中所有原子一定都共平面的是______。
②④
解析 乙烯、苯分子中所有原子均处于同一平面上,丙烯中存在甲基,甲基上的原子为四面体构型,故丙烯分子中所有原子不可能在一个平面内,苯乙烯中苯环和乙烯基团之间的单键可以旋转,故苯乙烯分子中所有原子不一定在同一平面内。
解析 完全燃烧后生成CO2和H2O的物质的量之比为1∶1,则有机物分子中C、H原子个数比为1∶2,CH2==CH2、CH3CH==CH2均符合上述要求。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
17
(2)相同质量的上述烃完全燃烧耗氧量最高的是__________,其电子式为
__________。
①
解析 相同质量的烃中,甲烷的含氢量最高,因此耗氧量最大。
(3)完全燃烧后生成的CO2和水的物质的量之比为1∶1的化合物是______。
②③
解析 苯乙烯在一定条件下发生加聚反应,化学方程式为n
。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
17
(4)⑤在一定条件下反应生成高分子材料的化学方程式:______________
_________________________,反应类型为__________。
加聚反应
3、 式量为128的烃可能为:
式量为30的有机物可能为:
式量为44的有机物可能为:
式量为46的有机物可能为:
式量为60的有机物可能为:
ω(C)=40%的有机物可能为:
C3H8、CH3CHO、环氧乙烷
C2H6、HCHO
C9H20、C10H8
C2H5OH、CH3OCH3、HCOOH
C3H7OH(2种)、CH3OCH2CH3、
CH3COOH、HCOOCH3、HOCH2CHO、
CO(NH2)2
五、乙烯的制法
工业制法:从石油化学工业产生的气体中分离得到。
实验室制法?
C
—
—
C
—
—
|
|
H
H
H
H
+ H2O
浓H2SO4
C
—
C
—
—
|
|
H
H
H
H
|
|
H
OH
实验室制法:
↑
170℃
消去反应:有机化合物在一定条件下,一个分子脱去一个小分子 (如:H2O,HBr等) ,而生成不饱和 (含双键或三键)化合物的反应。
应选用什么装置制取乙烯呢?与哪种制气装置相似?
1、应选用什么装置制取乙烯呢?与哪种制气装置相似?
监控反应温度;温度计水银球应在液面以下,不触瓶底。
液体(+固体)加热制取气体;与制氯气装置相似。
2、为何使用温度计?温度计水银球应在 什么位置?
3、这样的气体发生装置(液体加热)还差一样重要的实验用品——碎瓷片!
你知道有何必要,作何用途吗?
沸石:防止暴沸
(暴沸:液体受热沸腾时剧烈跳动)
碎瓷片
邬
邬
7、根据实验现象,联系已学知识,推测所得乙烯气体中可能包括哪些气体?如何除去杂质?
浓硫酸量多是 为避免过度稀释,反应不充分。
先撤导管后灭灯。
4、乙醇与浓硫酸以体积比1∶3混合,为什么浓硫酸要多些?实验完毕,是先撤酒精灯,还是先撤导管?
浓硫酸作 脱水剂 和 催化剂。
5、浓硫酸在反应中的作用?
乙烯是无色、稍有气味的气体,难溶于水,密度略小于空气(S.P.T. 1.25 g/L)。
6、能否用排气法收集乙烯?乙烯有哪些物理性质?
C2H4、H2O、CO2、SO2……
8、乙醇脱水制乙烯 为啥控温一百七?
C
—
—
C
—
—
|
|
H
H
H
H
+ H2O
浓H2SO4
C
—
C
—
—
|
|
H
H
H
H
|
|
H
O-H
↑
170℃
C
—
C
—
—
|
|
H
H
H
H
|
|
H
O-H
+
C
—
C
—
—
|
|
H
H
H
H
|
|
H-O
H
-OH 羟基上的H原子也容易脱去
浓H2SO4
140℃
+ H2O
C
—
C
—
—
|
|
H
H
H
|
|
H
H
C
—
C
—
—
|
|
H
H
O
H
|
|
H
H
分子内脱水
分子间脱水
CH3CH2OCH2CH3
乙醚
思考:什么事实证明了甲烷不是
平面十字结构而是正四面体结构?
思考:什么事实证明了苯不是
单双键交替出现的结构?
乙烯与有机高分子材料
化学2 第七章 第2节
碳碳双键键能大还是碳碳单键键能大?键长呢?
③碳碳双键键能大于碳碳单键,键长则小于碳碳单键
乙烯分子的空间构型是怎样的?
一、乙烯的分子结构
分子式: 电子式: 结构式:
结构简式: 最简式:
C
—
—
C
—
—
|
|
H
H
H
H
C
C
H
H
H
H
①乙烯分子是平面结构,非极性分子
②碳氢键与碳氢键、碳氢键与碳碳双键夹角均约为120°
④碳碳双键中的两个C-C键并不相同
其一:键能较大 (比烷烃中的碳碳单键键能还要大)
另一:键能较小 (比烷烃中的碳碳单键键能小得多)
乙烷更稳定还是乙烯更稳定?
双键中的这一较弱的键很容易断裂,发生化学反应
【说明】
C2H4
CH2=CH2
CH2
(2)乙烯是一种无色无味,易溶于水的气体( )
(1)乙烯的结构简式可书写为CH2CH2( )
判断正误
×
提示 乙烯分子中含有>C=C<,在书写时,官能团>C=C<不能省略,应为CH2=CH2。
×
提示 乙烯是一种稍有气味,难溶于水的气体。
(3)乙烯的充填模型为 ( )
(4)乙烯分子中所有原子共平面,可推断丙稀(CH2=CH—CH3)所有原子也共平面( )
(5)乙烯分子中的价键没有全部被氢原子“饱和”,因此乙烯属于不饱和烃( )
√
×
×
返回
三、乙烯的化学性质
1、氧化反应
为什么甲烷在空气中燃烧时无烟而乙烯有烟?
① C2H4能被KMnO4(H+)氧化
高锰酸钾溶液的紫色退去
——鉴别甲烷与乙烯
② 火焰明亮,伴有黑烟
C2H4 + 3O2 2CO2 + 2H2O
点燃
乙烯中碳的质量分数较高 ,燃烧时碳没有充分燃烧,因而产生黑烟——微小碳粒
烷烃通常状态下是稳定的,那么乙烯呢?
可否用于除去甲烷中的乙烯?
二、乙烯的物理性质
无色、稍有气味、气体,密度略小于空气,难溶于水
Br
—
C
|
C
—
—
|
|
H
H
H
H
+
Br
|
|
|
Br
C
┅
—
C
—
—
|
|
H
H
H
H
+
Br
┅
|
—
C
—
|
H
H
Cl
H
+
—
H
Cl
烷烃与Br2也可以发生同样的取代反应,
但是需要在高温或紫外线条件下,且反应较慢
|
—
C
—
|
H
H
H
H
+
—
Cl
Cl
光
C
—
C
—
—
|
|
H
H
H
H
|
|
Br
Br
C
—
—
C
—
—
|
|
H
H
H
H
—
Br
Br
+
乙烯通入Br2的CCl4溶液中,反应很快,
显然不会是发生取代反应,那么原理如何呢?
邬
C
—
—
C
—
—
|
|
H
H
H
H
+
—
Br
Br
【说明】
C2H4与Cl2、H2、HCl、H2O等众多物质均能发生加成反应
C
—
C
—
—
|
|
H
H
H
H
|
|
H
Cl
C
—
—
C
—
—
|
|
H
H
H
H
—
H
Cl
+
催化剂
C
—
C
—
—
|
|
H
H
H
H
|
|
H
OH
C
—
—
C
—
—
|
|
H
H
H
H
—
H
OH
+
催化剂
2、加成反应:
有机物分子中的不饱和键(双键或三键)两端的碳原子与其他原子或原子团结合生成新化合物的反应
Br2
+
CH2
CH2
—
—
CH2Br
CH2Br
—
C2H4与Cl2、H2能否发生加成反应?
C2H4与H2O能否发生加成反应?
C
—
C
—
—
|
|
H
H
H
H
|
|
H
H
C
—
—
C
—
—
|
|
H
H
H
H
—
H
H
+
催化剂
如何制备较纯净的一氯乙烷?
取代基
-OH 羟基
C
-
-
H
H
-
-
H
H
C
=
一定条件下乙烯分子双键断开,却没有其他分子存在,会发生什么?
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
H
H
-
-
H
H
C
=
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
H
H
-
-
H
H
C
=
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
H
H
H
-
-
H
C
-
=
C
-
-
H
H
-
-
H
H
C
=
C
-
-
-
-
H
H
C
-
-
-
-
H
H
H
C
-
-
H
H
-
-
H
C
=
若非两分子加成,而是n分子加成呢?
2CH2=CH2 ———→
-
CH2
-
-
CH2
-
CH2
-
CH2
-
一定条件
2CH2=CH2 ———→ CH3-CH2-CH=CH2
一定条件
3、加聚反应:
由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反应。
通过加成的方式聚合的反应,叫做加聚反应。
C
-
-
H
H
-
-
H
H
C
=
n
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
……
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
H
H
C
-
-
-
-
H
H
C
-
-
-
H
H
…
…
[ ]
n CH2=CH2 ———→ -CH2-CH2-
一定条件
n
CH2=CH2
单体
-CH2-CH2-
链节
n
聚合度
三、乙烯的用途
乙烯是石油化学工业最重要的基础原料!
乙烯工业的发展水平是衡量一个国家石油化工水平的重要标志之一!
乙烯主要用于制造塑料、合成纤维、有机溶剂等。
乙烯可用于果实催熟(生果多果酸、丹宁)。
乙烯与生长素、赤霉素、细胞分裂素、 脱落酸一样,均为植物激素。
乙烯作用: 能使植物停止生长、变矮、落叶、落果;促进菠萝开花;刺激橡胶树和漆树吐胶泌液,增加产量;对黄瓜、甜瓜这些雌雄异花同株的植物,还可以改变花的性别,使雄花变为雌花。
乙烯作用极大,几乎所有植物的器官中都有,但含量极低。
(1)乙烯和乙烷都为碳氢化合物,因此性质相同( )
(2)乙烯的化学性质比乙烷活泼( )
(3)乙烯能使酸性KMnO4溶液和溴水褪色,反应原理相同( )
(4)酸性KMnO4既可以验证乙烷和乙烯,还可以除去乙烷中混有的乙烯
( )
判断正误
×
×
提示 乙烯使酸性KMnO4溶液褪色发生的是氧化反应,乙烯使溴水褪色发生的是加成反应。
√
×
(5)乙烯聚合生成聚乙烯,本质是每个乙烯分子中的碳碳双键的一个键断裂,相互结合生成聚乙烯,因此也称为加聚反应( )
(6)燃烧等质量的乙烯和聚乙烯耗氧量相同( )
提示 乙烯和聚乙烯的最简式相同。
(7)乙烷中混有乙烯,可通过与H2在一定条件下反应,使乙烯转化为乙烷
( )
提示 C2H4和H2反应可能使气体中又混有氢气。
×
√
√
分子式 C2H6 C2H4
结构式
碳碳键类别 碳碳单键 碳碳双键
原子相对位置 C、H不全在一个平面内 6个原子都在同一平面内
燃烧 2C2H6+7O2—→4CO2+6H2O C2H4+3O2—→2CO2+2H2O
特征反应 C2H6+Cl2—→C2H5Cl+HCl CH2=CH2+Br2—→CH2BrCH2Br
与高锰酸钾 酸性溶液 不反应 因发生氧化反应而使其褪色
乙烷与乙烯的分子结构和化学性质对比
解析 A项,乙烯和氢气加成反应生成CH3CH3,正确;
B项,CH3CHCl2不能通过乙烯的加成反应制得,错误;
C项,CH2==CH2和H2O加成可生成CH3CH2OH,正确;
D项,CH2==CH2可以和HBr加成生成CH3CH2Br,正确。
1.下列物质中,可以通过乙烯的加成反应得到的是______(填字母)。
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
深度思考
ACD
2.体育比赛中当运动员肌肉挫伤或扭伤时,队医常用药剂氯乙烷(CH3CH2Cl)
(沸点为12.27 ℃)对受伤部位进行局部冷却麻醉处理,工业上制取氯乙烷有两种方案:
a.CH3CH3+Cl2 CH3CH2Cl+HCl
b.CH2==CH2+HCl CH3—CH2Cl
你认为制备氯乙烷的最好方案为_____(填“a”或“b”),并说出选择该方案及不选择另一方案的理由:___________________________________
__________________________________________________________________________________________________________________________________________________________________。
b
a方案中CH3CH3和Cl2在光照条件下发生取代反应,反应产物中除CH3CH2Cl和HCl外,还有很多副产物,产物不纯,产率低;b方案中CH2==CH2和HCl在一定条件下发生加成反应,产物中只有CH3CH2Cl,产品纯度高、产率高
解析 CH3CH3和Cl2发生取代反应,生成的产物中除CH3CH2Cl外,还有很多副产物,CH2==CH2和HCl加成只产生CH3CH2Cl,故选择b方案。
3.运输水果时,为了吸收水果产生的乙烯,防止水果早熟腐烂,常将浸泡有_________溶液的硅藻土放置在盛放水果的容器中。
解析 KMnO4溶液可以吸收乙烯,同时产生CO2气体,故可以防止水果早熟腐烂。
高锰酸钾
返回
解析 乙烯分子中碳原子间形成的是双键,有两对共用电子对,A项错误;
碳原子的半径应比氢原子的大,B项错误;
乙烯的结构简式为CH2==CH2,D项错误。
1.(2020·黑龙江阿城区第一中学高一检测)对乙烯的结构,下列说法正确的是
A.乙烯的电子式为 B.乙烯的球棍模型为
C.乙烯分子在空间上呈平面结构 D.乙烯的结构简式为CH2CH2
1
2
3
5
随堂演练 知识落实
4
√
6
解析 分子中的碳氢原子个数比只能说明烃的组成,不能说明其结构特点;燃烧产物的物质的量相等和被酸性KMnO4溶液氧化,不能说明乙烯分子中含有一个碳碳双键;1 mol乙烯只能与1 mol溴单质加成,说明乙烯分子中含有一个碳碳双键。
2.(2019·自贡高一检测)能证明乙烯分子中含有一个碳碳双键的事实是
A.乙烯分子中碳、氢原子的个数比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色
1
2
3
5
4
√
6
3.(2020·郑州柘城第二高级中学检测)下列各反应不属于加成反应的是
A.CH2==CH2+H—OH CH3—CH2—OH
B.CH3CH==CH2+Br2―→CH3CHBrCH2Br
C. +H2 CH3—CH2—OH
D.CH3—CH3+2Cl2 CH2Cl—CH2Cl+2HCl
√
1
2
3
5
4
解析 D项中反应为取代反应。
6
4.(2019·武汉高一期中)①②是两种常见烃的球棍模型,则下列叙述正确的是
A.都能在空气中燃烧
B.都能使酸性高锰酸钾溶液褪色
C.都能发生加成反应
D.等质量的①②完全燃烧时,产生CO2的量相同
√
1
2
3
5
4
6
解析 由题图可知,①为乙烷,②为乙烯。乙烷不能使酸性高锰酸钾溶液褪色,而乙烯能,B项错误;
乙烷不能发生加成反应,而乙烯能,C项错误;
乙烷和乙烯的摩尔质量不同,等质量时二者的物质的量不同,产生CO2的量也不同,D项错误。
1
2
3
5
4
6
解析 1 mol CH2==CH2与HCl完全加成生成1 mol CH3CH2Cl,1 mol CH3CH2Cl中含5 mol H,故彻底取代需消耗5 mol Cl2,D项正确。
5.(2020·北京市第九中学月考)1 mol乙烯与HCl完全加成后再被Cl2彻底取代,则消耗氯气的物质的量是
A.2 mol B.2.5 mol C.4 mol D.5 mol
1
2
3
5
4
√
6
解析 乙烯和溴发生加成反应生成CH2BrCH2Br,甲烷不反应,因此用溴水除去CH2==CH2,然后通过浓H2SO4干燥,故B项满足,
乙烯可以被酸性KMnO4氧化最后生成CO2,因此,甲烷中会混有新杂质CO2,故C项错误。
6.(2020·安徽东至县第一中学高一月考)甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶
A.澄清石灰水,浓H2SO4 B.溴水,浓H2SO4
C.酸性高锰酸钾溶液,浓H2SO4 D.浓H2SO4,酸性高锰酸钾溶液
1
2
3
5
4
√
返回
6
1.现有a、b、c三种碳氢化合物,其球棍模型如图
下列有关说法错误的是
A.分子中所有原子共平面的只有b
B.a和c分子结构相似,互为同系物
C.b分子的结构简式为
D.b分子中含有 ,c分子中所有的共价键都为单键
课时对点练
题组一 乙烯的组成及结构
√
对点训练
解析 因为a、b、c三种分子都为碳氢化合物,由三种物质的球棍模型,可知a为甲烷,b为乙烯,c为乙烷,据碳原子成键特点,CH4和CH3CH3分子应为以碳为中心的四面体结构,乙烯分子中六个原子共平面,其结构简式为CH2==CH2,故C错误。
1
2
3
4
5
6
7
8
9
2.(2020·西藏林芝市第二高级中学月考)由乙烯推测丙烯(CH2==CHCH3)的结构或性质,以下关于丙烯的说法不正确的是
A.分子中3个碳原子不在同一直线上
B.与HCl在一定条件下加成只得到一种产物
C.最多有7个原子在同一平面上
D.在空气中燃烧时火焰明亮并伴有黑烟
√
1
2
3
4
5
6
7
8
9
解析 CH2==CHCH3与HCl在一定条件下加成可以得到 、
两种产物。
1
2
3
4
5
6
7
8
9
3.(2019·衡阳高一期末)氯乙烷是一种沸点较低(沸点为12.27 ℃),极易挥发的无色液体,常作为运动员肌肉挫伤或扭伤的冷冻麻醉剂,下列有关氯乙烷的制法,最好的是
A.乙烷与氯气发生取代反应 B.乙烯与氯气发生加成反应
C.乙烷与氯化氢混合 D.乙烯与氯化氢发生加成反应
√
1
2
3
4
5
6
7
8
9
题组二 乙烯的性质与用途
解析 乙烷与氯气发生取代反应生成多种氯代烃的混合物;乙烯与氯气发生加成反应生成1,2-二氯乙烷(CH2ClCH2Cl);乙烷与氯化氢不反应;乙烯与氯化氢发生加成反应生成氯乙烷。
4.(2019·江苏兴化一中高一下期末)既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的试剂是
A.溴水 B.氧气
C.酸性高锰酸钾溶液 D.氢气
1
2
3
4
5
6
7
8
9
√
1
2
3
4
5
6
7
8
9
解析 乙烷与溴水不反应,而乙烯与溴水发生加成反应生成1,2-二溴乙烷,使溴水褪色,所以可以鉴别二者,也可以除去乙烷中混有的乙烯杂质,A正确;
乙烯与酸性高锰酸钾溶液反应,使溶液褪色,而乙烷与酸性高锰酸钾溶液不反应,故可以鉴别二者,但由于乙烯被酸性高锰酸钾溶液氧化生成CO2气体,引入新杂质,故不能用于除去乙烷中混有的乙烯杂质,C错误;
乙烯与氢气在一定条件下发生反应,但反应现象不明显,不能用于鉴别二者,D错误。
5.(2020·贵州岑巩一中高一检测)如图表示球棍模型,小球表示原子序数小于10的原子,短线表示化学键,每个原子都到达稳定结构。下列有关说法正确的是
A.M分子的所有原子共面
B.0.1 mol·L-1的N溶液中H+的物质的量浓度为0.1 mol·L-1
C.L存在同分异构体
D.L能使酸性KMnO4溶液褪色
√
1
2
3
4
5
6
7
8
9
解析 小球表示原子序数小于10的原子,短线表示化学键,每个原子都达到稳定结构,由图可知,发生CH2==CH2+HF―→CH3CH2F。M为乙烯,含碳碳双键,为平面结构,M分子的所有原子共面,故A正确;
N为HF,为弱酸,不完全电离,因此0.1 mol·L-1的N溶液中H+的物质的量浓度小于0.1 mol·L-1,故B错误;
由乙烷中6个H相同可知,L为CH3CH2F,只有一种结构,不存在同分异构体,故C错误。
1
2
3
4
5
6
7
8
9
1
2
3
4
5
6
7
8
9
6.(2020·甘肃兰州一中月考)下列说法中错误的是
A.乙烯与Br2的加成,乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳
双键有关
B.用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.相同物质的量的乙烯和甲烷完全燃烧消耗的氧气的量相同
D.利用燃烧的方法可以鉴别乙烯和甲烷
√
题组三 加成反应概念理解及判断
1
2
3
4
5
6
7
8
9
解析 乙烯中含 ,能发生加成反应和氧化反应,双键断裂,A正确;
乙烯能与溴的四氯化碳溶液或酸性KMnO4溶液反应,使溶液褪色,而乙烷不能,故能鉴别,B正确;
乙烯和甲烷的分子式不同,1 mol乙烯需要耗氧3 mol,1 mol CH4耗氧为2 mol,
故两者完全燃烧耗氧量不相同,C错误;
乙烯比甲烷的含碳量高,燃烧时甲烷产生淡蓝色火焰,乙烯燃烧时火焰明亮并伴有黑烟,现象不同,能鉴别,D正确。
7.(2020·天津外国语大学附属中学高一期末)降冰片二烯在紫外线照射下可以发生下列转化。
下列说法错误的是
A.降冰片二烯与四环烷互为同分异构体
B.降冰片二烯能使酸性高锰酸钾溶液褪色
C.四环烷的一氯代物超过三种(不考虑立体异构)
D.降冰片二烯分子中位于同一平面的碳原子不超过4个
1
2
3
4
5
6
7
8
9
√
综合强化
解析 降冰片二烯与四环烷分子式相同,
结构不同,因此二者互为同分异构体,A
正确;
降冰片二烯分子中含有碳碳双键,因此能使酸性高锰酸钾溶液褪色,B正确;
四环烷含有三种化学环境不同的H原子,因此其一氯代物有三种,C错误;
根据乙烯分子是平面分子,与碳碳双键连接的C原子在碳碳双键所在的平面上,可知降冰片二烯分子中位于同一平面的碳原子最多为4个,D正确。
1
2
3
4
5
6
7
8
9
8.(2020·山东招远第一中学高一检测)将CH4和C2H4的混合气体15 g通入盛有足量溴水的容器中,溴水的质量增加了7 g,则混合气体中CH4和C2H4的体积之比为
A.1∶2 B.2∶1 C.3∶2 D.2∶3
1
2
3
4
5
6
7
8
9
√
解析 甲烷不能与溴水反应,乙烯可与Br2发生加成反应,因此,溴水质量增加是因为吸收了乙烯,故乙烯物质的量为 =0.25 mol,则
甲烷物质的量为 =0.5 mol,相同条件下气体体积之比等于其物质的量之比,即CH4与C2H4体积之比为2∶1。
解析 乙烯含有碳碳双键,能够与溴发生加成反应而使溴水褪色,反应方程式为CH2==CH2+Br2―→CH2Br—CH2Br。
9.(2019·山西太原一中期末)乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙烯
的原理和乙烯的主要
化学性质,实验装置
如图所示。
(1)用化学方程式解释
B装置中的实验现象:
_______________________________。
1
2
3
4
5
6
7
8
9
CH2==CH2+Br2―→CH2Br—CH2Br
解析 乙烯具有还原性,能够与酸性高锰酸钾溶液发生氧化还原反应而使酸性高锰酸钾溶液褪色。
(2)C装置中的现象是_________________________,其发生反应的类型是_____________。
1
2
3
4
5
6
7
8
9
酸性高锰酸钾溶液褪色
氧化还原反应
解析 乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙溶液反应生成碳酸钙沉淀,溶液变浑浊。
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置____(填字母)中的实验现象可判断该资料是否真实。
1
2
3
4
5
6
7
8
9
D
(4)通过上述实验探究可知,检验甲烷和乙烯的方法是______(填字母,下同);除去甲烷中乙烯的方法是____。
A.将气体通入水中
B.将气体通过装溴水的洗气瓶
C.将气体通过装酸性高锰酸钾
溶液的洗气瓶
D.将气体通入氢氧化钠溶液中
1
2
3
4
5
6
7
8
9
BC
B
解析 A项,甲烷、乙烯均不溶
于水,且常温下与水都不反应,
不能用于鉴别和除杂;
B项,乙烯中含有 ,能
与溴水发生加成反应生成1,2-二溴乙烷液体,甲烷不与溴水反应,所以可用溴水除去甲烷中混有的乙烯,也可以鉴别甲烷与乙烯;
C项,甲烷与高锰酸钾溶液不反应,乙烯能够与高锰酸钾溶液反应而使其褪色,可以鉴别甲烷与乙烯;但是乙烯被氧化生成二氧化碳气体,故不能用于除去甲烷中混有的乙烯杂质;
1
2
3
4
5
6
7
8
9
D项,甲烷、乙烯都不溶于氢氧化钠溶液,不能用来鉴别和除杂。综上所述,可用来鉴别的是B、C项,可用来除杂的是B项。
1
2
3
4
5
6
7
8
9
返回
四、烯烃
通式
单烯烃:CnH2n
结构
含有碳碳双键(>C=C<)
分类
单烯烃、二烯烃、环烯烃……
化学性质
⑴氧化反应
能使KMnO4酸性溶液和溴水[Br2(H2O)]褪色
⑵加成反应
能使溴的四氯化碳溶液[Br2(CCl4)]褪色
火焰明亮,伴有黑烟
CH3-CH=CH2 + Br2 ——→ CH3-CHBr-CH2Br
CH3-CH=CH-CH3+ HBr ——→CH3-CH2-CHBr-CH3
CH3-CH=CH2+ HBr ——→
CH3-CH-CH3
-
Br
CH3-CH2-CH2Br
马氏规则Markovnikov's rule锦上添花
⑶加聚反应
nCH3-CH=CH2——→
CH3-CH=CH-CH3
CH2=CH-CH=CH2
-CH-CH2-
[
]n
CH3
-
CnH2n+ O2 ——→ n CO2+ n H2O
点燃
⑷取代反应
CH2=CH-CH3 + Cl2 ——→ CH2=CH-CH2Cl + HCl
500℃
n
-CH2-CH=CH-CH2-
[
]n
———→
一定条件
分子式:
电子式:
结构式:
结构简式:
最简式:
空间构型:
球棍模型:
空间充填模型:
五、炔烃 乙炔
通式
单炔烃:CnH2n-2
结构
含有碳碳双键(-C≡C-)
分类
单炔烃、二炔烃、环炔烃…
C
C
H
H
H-C≡C-H
HC≡CH
CH≡CH
CH
C2H2
直线形
CH2=CH-C≡C-CH3分子中最多有几个原子共平面?几个原子共直线?
炔烃的化学性质
⑴氧化反应
能使KMnO4酸性溶液和溴水[Br2(H2O)]褪色
⑵加成反应
能使溴的四氯化碳溶液[Br2(CCl4)]褪色
CnH2n-2+ O2 → nCO2 + (n-1)H2O
火焰明亮,浓烈黑烟
CH≡CH + Br2
CHBr=CHBr
CHBr=CHBr + Br2
CHBr2-CHBr2
CH≡CH + HBr
CH2=CHBr
⑶加聚反应
n CH≡CH
-CH=CH-
[
]n
CH2=CHBr + HBr
CH3-CHBr2
CH2Br-CH2Br
聚氯乙烯-PVC (Polyvinyl chloride)是世界上产量最大用途最广的通用塑料,如何制备?涉及什么反应类型?
-CH-CH2-
[
]n
Cl
-
CH≡CH + HCl
CH2=CHCl
n CH2=CHCl
[ CH2-CHCl ]n
-
-
分子式:
结构式:
结构简式:
空间构型:
球棍模型:
空间充填模型:
六、芳香烃 苯
通式
苯的同系物:CnH2n-6
结构
含有苯环
分类
苯的同系物、多环芳烃
C6H6
平面结构
苯分子的结构特点
C构成平面正六边形,12个原子共面,
C、H原子所处环境完全相同,
碳原子间是一种介于碳碳单键
和碳碳双键之间的特殊共价键
什么事实可以证明苯不是
单双键交替出现的结构?
苯的物理性质
无色、有特殊气味、液体,密度比水小,难溶于水,是一种重要溶剂。m.p. 5.5℃,b.p. 80.1℃,易挥发。
⑴氧化反应
不能使酸性KMnO4溶液和溴水褪色
2C6H6+15O2 → 12CO2+6H2O
火焰明亮 浓烈黑烟
⑵取代反应
HO-NO2
+ H2O
+ HNO3 ——→
浓硫酸
50~60℃
浓硫酸:
催化剂、吸水剂
苯的硝化
苯的溴代
+ HBr
+ Br2 ——→
FeBr3
+ H2O
+ H2SO4 ——→
△
苯的磺化
HO-SO3H
⑶加成反应
不能使溴水[Br2(H2O)]褪色,但能使溴水层褪色——萃取
+ 3H2 ———→
催化剂
加热加压
“666”有机氯杀虫剂20th 50s广泛使用,现已禁用。它可由苯与氯气在一定
条件下反应得到,分子式为C6H6Cl6,该反应属于哪种反应类型?
苯的化学性质
1.烃的概念
仅含___和___两种元素的有机化合物称为碳氢化合物,也称为烃。
2.烃的分类
(1)依据:烃分子中碳原子间_________的不同及________的不同。
一、烃
碳
氢
成键方式
碳骨架
(2)分类
CH2==CH2
—C≡C—
烃 甲烷 乙烯 乙炔
电子式 _________ _____________ ____________
化学键 ______ _____和 ____________________ _____和_________
分子结构特点 _________ _____ _____
3.常见烃的分子结构
C—H
H—C
H—C
—C≡C—
正四面体
平面
直线
(2)甲烷、乙烯和乙炔分子中都只含有碳和氢两元素,故它们是同系物
( )
(1)一种有机物完全燃烧,产物只有CO2和H2O,则该有机物一定属于烃
( )
判断正误
×
提示 该有机物中可能含氧元素,如CH3CH2OH不是烃。
×
提示 三者的结构不同,甲烷分子中全部为单键,乙烯分子中含有碳碳双键,乙炔分子中含有碳碳三键,而且分子组成上也不相差一个或若干个CH2原子团,故不为同系物。
(4)属于烃的有机化合物分子中的氢原子数一定为偶数个( )
提示 和 分子中都不含有苯环( ),不属于芳香烃。
(5) 和 都属于芳香烃( )
(3)乙烯的分子式为C2H4,故分子组成为C6H12的烃一定属于烯烃( )
√
×
提示 分子组成为C6H12的烃,可能是烯烃,也可能属于环烷烃,如环己烷。
提示 根据碳原子的4价键理论,烃分子中的氢原子一定为偶数。
×
(6)苯的分子式为C6H6,结构简式为 ,分子高度不饱和,故苯分子中
一定含有碳碳双键,属于烯烃( )
×
提示 苯分子中含有 ,结构简式 是一种习惯写法,分子中不含
有 ,属于芳香烃。
A B C D
①球棍模型 ②能和Cl2在光照条件下生成多种氯代物 ①能使溴水褪色 ②标准状况下,气体密度为1.25 g·L-1 ①既不能使溴水褪色,也不能使酸性KMnO4溶液褪色 ②平面结构 ③球棍模型 ①能使溴水褪色
②1 mol能和2 mol H2加成
③充填模型
1.如表是A、B、C、D四种烃的有关信息。
深度思考
(1)烃A的电子式:______________,烃B分子的空间结构为__________,烃D的结构式为______________,空间结构为________。
(2)四种烃中,和甲烷互为同系物的是________(填结构简式,下同),完全燃烧,生成CO2和H2O的物质的量之比为1∶1的是__________。
(3)写出烃B和H2O在一定条件下反应的化学方程式:_________________
______________________。
平面结构
H—C≡C—H
直线形
CH3CH3
CH2==CH2
CH2==CH2+H2O
(4)已知B和D具有相似的化学性质,试写出烃D和Br2按物质的量之比为
1∶1反应的化学方程式:__________________________,将烃D通入酸性KMnO4溶液的现象是____________________。
CH≡CH+Br2―→
紫红色褪去(或变浅)
(5)下列有关烃C的说法正确的是________。
A.烃C的分子式为C6H6,属于不饱和烃
B.从烃C的组成上看,分子结构应该存在碳碳双键,故应属于烯烃
C.烃C分子中的12个原子都在同一平面内
D.烃C分子中的化学键应当比较特殊,化学键不同于一般的碳碳单键和
碳碳双键
E.1 mol C分子和H2在一定条件下反应,最多需要3 mol H2
ACDE
解析 根据信息及四种烃的结构,可推断烃A为乙烷(CH3CH3),烃B为乙
烯(CH2==CH2),烃C为苯( ),烃D为乙炔(CH≡CH)。乙烷为饱和
烷烃,和甲烷互为同系物;乙烯、乙炔和苯为不饱和烃,其中乙烯和乙炔性质相似,可以发生加成反应和氧化反应,故乙炔和Br2按1∶1加成反应的方程式为CH≡CH+Br2―→ ,乙炔通入酸性高锰酸钾溶液
中紫红色褪去;苯分子的化学式为C6H6,根据信息和碳原子的四价键关系,分子中不存在一般的碳碳单键和双键,而是一种特殊的共价键。
解析 根据乙炔、乙烯和甲烷的结构,有机物M的分子结构为 ,
则最多有4个原子共直线,因为单键可以旋转,甲基上3个H原子中,可以有一个H原子旋进面内,因此最多有9个原子共面,故选C。
2.已知乙烯分子为平面结构,C2H2为直线结构。则有机物M(CH≡C—CH==CH—CH3)分子中,共直线和共平面的原子数最多分别为
A.6、11 B.5、10 C.4、9 D.4、11
√
返回
七、有机高分子材料
天然有机高分子材料:
合成有机高分子材料:
棉花、羊毛、天然橡胶……
塑料、合成纤维、合成橡胶、黏合剂、涂料……
七、有机高分子材料
⑴
二、有机高分子材料
1.有机高分子材料的分类
有机高分子材料
_____有机高分子材料:如棉花、羊毛、天然橡胶
_____有机高分子材料:如_____、__________、
_________、黏合剂、涂料等
天然
合成
塑料
合成纤维
合成橡胶
2.有机高分子材料
(1)塑料
①组成
提高塑性:______
防止老化:______
增强材料
着色剂
主要成分:_________
添加剂
合成树脂
增塑剂
防老剂
②性能:强度___、密度___、_______、易加工等。
高
小
耐腐蚀
名称 结构简式 用途
聚乙烯 可制成食品包装袋等
聚氯乙烯 可制成电线的绝缘层、管道等
聚苯乙烯 可制成泡沫包装材料、绝缘材料等
③常见塑料及用途
聚四氟乙烯 可制成实验仪器、化工用品等
聚丙烯 可制成管道、包装材料等
有机玻璃(聚甲 基丙烯酸甲酯) 可制成飞机和车辆的风挡、光学仪器等
脲醛塑料(电玉) 可制成电器开关、插座等
(2)橡胶
①橡胶是一类具有高弹性的高分子材料,是制造汽车、飞机轮胎和各种密封材料所必需的原料。天然橡胶的主要成分是____________,结构简式为 ,其单体为 ;天然橡
胶分子中含有 ,易发生_____反应和_____反应。
聚异戊二烯
加成
氧化
②橡胶的分类
③性能:具有高弹性、绝缘性、气密性、耐油、耐高温或耐低温等性能。
④用途:制造汽车、飞机轮胎;各种密封材料。
(3)纤维
①纤维的分类
动物纤维——羊毛、蚕丝等
植物纤维——棉花、麻等
____
纤维
纤维
____
纤维
_____纤维——黏胶纤维、大豆蛋白纤维等
____纤维
(六大纶)
____(聚丙烯纤维)
____(聚氯乙烯纤维)
____(聚丙烯腈纤维)
____(聚对苯二甲酸乙二酯纤维)
__________(聚酰胺纤维)
天然
再生
化学
合成
丙纶
氯纶
腈纶
涤纶
锦纶、芳纶
②合成纤维性能:强度___、弹性___、耐磨、耐化学腐蚀,不易虫蛀等。
③主要用途:制_____、绳索、渔网等,广泛应用于工农业领域。
高
好
衣料
(1)通常所说的三大合成材料是塑料、合成纤维和合成橡胶( )
(2)塑料包装袋都可以包装食品( )
(3)有机高分子材料是一类结构非常复杂的有机物( )
提示 有机高分子材料虽然相对分子质量很大,但一般结构简单,是由很多重复的链节构成。
(4)真丝、塑料和涤纶都是合成高分子材料( )
提示 真丝是天然高分子材料,塑料和涤纶是合成高分子材料。
判断正误
×
×
√
×
(5)纯净的聚乙烯塑料为纯净物( )
提示 有机高分子材料是由很多重复的链节构成,聚合度n不同,故为混合物,不为纯净物。
(6)乙烯和聚乙烯都能使溴的CCl4溶液褪色( )
提示 聚乙烯结构为 ,链节中不存在碳碳双键,不能使溴的CCl4溶液褪色。
(7)天然橡胶硫化的过程没有发生化学变化( )
提示 橡胶硫化是线型高分子链之间通过硫原子形成化学键,产生交联,形成网状结构,发生的是化学变化。
×
×
×
(8)以石油、煤、天然气为原料可以生产某些有机高分子材料( )
提示 以石油、天然气和煤为原料制成有机高分子单体,再聚合生成塑料、合成纤维等有机高分子材料。
√
解析 高聚物 的链节为 ,单体为CH2==CH
—CN。
1.腈纶又名“人造羊毛”,其结构简式为 ,按要求回答问题。
(1)“人造羊毛”的链节为_____________,单体为_______________。
深度思考
CH2==CH—CN
(2)实验测得“人造羊毛”的相对分子质量(平均值)为32 800,则该高聚物的聚合度n为_____。
619
解析 高聚物的链节的化学式为C3H3N,式量为53,链节的个数也就是
聚合度n,故n=
(3)工业上以乙炔和HCN为原料合成腈纶,合成路线如下:
写出有关的化学方程式并注明反应类型:
①_______________________________________________;
②_______________________________________________。
。
nCH2==CH—CN ,加聚反应
CH≡CH CH==CH2—CN
解析 根据反应流程,CH≡CH和HCN先发生加成反应生成CH2==CHCN,再发生加聚反应生成聚丙烯腈,故化学方程式为①CH≡CH+HCN
CH2==CH—CN;
②nCH2==CH—CN 。
2.ABS树脂( )是一种强度高、韧性
好、易于加工成型的热塑型高分子材料。用于制备仪表、电气、电器、机械等各种零件。
(1)ABS树脂的链节为____________________________________。
(2)合成ABS树脂的单体为_________________、_____________________、
________________。
CH2==CH—CN
CH2==CH—CH==CH2
CH2==CH—C6H5
加聚反应单体的判断方法
方法总结
方法一:弯箭头法(一边赶法),去掉[ ]和n,将链节中的一个键从左向右折叠,单变双,双变单,遇到碳超过4价,则断开。
如维通橡胶 ―→
―→CH2==CF2和CF2==CF—CF3。
方法二:单变双,双变单,超过四价则断开。
如:丁苯橡胶
―→
―→CH2==CH—CH==CH2和 。
返回
解析 烃是分子中只有碳和氢元素的有机物,A错误;
含苯环的碳氢化合物才属于芳香烃,C错误;
乙烯和乙炔分子结构不同,不为同系物,D错误。
1.下列有关烃的说法正确的是
A.烃分子中除了含碳和氢之外,还可能含其他元素
B.根据烃分子中碳原子间成键方式不同,可把烃分为饱和烃与不饱和烃
C.分子中含有苯环的有机物就是芳香烃
D.乙烯和乙炔分子中都含有不饱和键,故它们互为同系物
1
2
3
5
随堂演练 知识落实
4
√
6
2.(2020·江苏苏州中学高一月考)下列有机分子中,所有原子不可能在同一平面内的是
A.CH2==CHCl B.CH3CH2CH3
C. D.CF2==CF2
1
2
3
5
4
√
6
解析 CH2==CHCl和CF2==CF2可看作CH2==CH2分子中的H原子被Cl或F原子代替后的产物,因乙烯为平面结构,故A和D中所有原子共面;
因苯环中6个碳和6个H原子共平面,HC≡CH中4个原子共直线,故C项所有原子共面;
丙烷分子中碳原子为饱和结构,空间结构为四面体结构,故丙烷分子中所有原子不可能共面。
1
2
3
5
4
6
3.(2019·山西平遥祝中学高一期末)下列对烃的分类不正确的是
A.CH4、CH2==CH2、CH2==CHCH==CH2均属于饱和烃
B.CH3CH2CH3、CH3CH==CH2、CH3CH==CHCH2CH==CH2均属于链状烃
C.CH3CH3、 、C18H38均属于饱和烃
D. 、 、 均属于芳香烃
√
1
2
3
5
4
6
解析 CH2==CH2、CH2==CHCH==CH2分子中含有碳碳双键,属于不饱和烃,A项错误;
链状烃指的是分子中无环状结构的烃,B项正确;
CH3CH3、 、C18H38三种分子中每个C原子均达到饱和状态,属于饱和烃,C项正确;
含苯环的烃属于芳香烃,D项正确。
1
2
3
5
4
6
4.人们在日常生活中大量使用各种高分子材料,下列说法中正确的是
A.天然橡胶易溶于水
B.羊毛是合成高分子化合物
C.聚乙烯塑料是天然高分子材料
D.聚氯乙烯塑料会造成“白色污染”
√
1
2
3
5
4
6
解析 聚氯乙烯塑料在自然界中难以降解会造成“白色污染”,天然橡胶、羊毛和聚乙烯塑料都是高分子材料,难溶于水,羊毛是天然的,而聚乙烯塑料是合成的高分子材料。综上所述,D项正确。
5.(2020·哈尔滨第二中学高一检测)下列说法正确的是
A.乙烯通过聚合反应可得到高分子材料
B.聚丙烯的结构单元是—CH2—CH2—CH2—
C.碳纤维属于合成有机高分子化合物
D.聚乙烯塑料的老化是因为发生了加成反应
1
2
3
5
4
√
6
解析 乙烯加聚得到的聚乙烯是高分子材料,A正确;
聚丙烯是丙烯发生加成聚合反应生成的,结构单元是 ,B
错误;
碳纤维是一种含碳量在95%以上的新型无机非金属材料,C错误;
聚乙烯分子中不含有碳碳双键,不能发生加成反应,D错误。
1
2
3
5
4
6
6.橡胶树是热带植物,在我国海南已有大面积种植。从橡胶树的胶乳中可提取天然橡胶,天然橡胶的成分是聚异戊二烯,其结构为
。
试回答下列问题:
天然橡胶加入适当硫进行硫化后,其结构由_____变成_____,天然橡胶的单体是一种无色液体,将该无色液体加入溴水中,溴水_____(填“能”或“不能”)褪色。
1
2
3
5
4
6
线型
网状
能
解析 天然橡胶中加入硫,使线型的高分子链之间通过硫原子形成化学键,产生交联,形成网状结构,天然橡胶的单体为 ,
分子中含有不饱和双键,可以和Br2加成,因此能使溴水褪色。
1
2
3
5
4
返回
6
1.(2019·南京高一检测)科学家对探测器发回的数据进行了分析,发现土卫六的大气层中含有95%的氮气,剩余的气体为甲烷和其他碳氢化合物。下列关于碳氢化合物的叙述正确的是
A.碳氢化合物的通式为CnH2n+2
B.燃烧产物为二氧化碳和水的化合物一定是碳氢化合物
C.有些烷烃在光照下不能与氯气发生取代反应
D.碳氢化合物分子的相对分子质量一定是偶数
课时对点练
1
2
3
4
5
6
7
8
9
题组一 常见烃的结构、性质及分类
√
对点训练
10
解析 CnH2n+2是链状烷烃的通式,而不是所有碳氢化合物的通式,A错误;
燃烧产物为CO2和H2O的化合物不一定为碳氢化合物,有可能含有氧元素,B错误;
烷烃都能在光照下与Cl2发生取代反应,C错误;
因为碳的原子量为偶数且成的价键为4个,结合的氢原子一定为偶数,因此碳氢化合物的相对分子量一定为偶数,D正确。
1
2
3
4
5
6
7
8
9
10
解析 H2CO3属于无机物,A错;
属于有机酸,含有氧元素,所以不为烃,B正确;
CH2==CH—CH3和CH≡CH分别属于烯烃和炔烃,都为烃,故C、D错误。
2.(2020·湖南茶陵三中月考)下列有机物中,属于有机物,但不属于烃的是
A.H2CO3 B.
C.CH2==CH—CH3 D.CH≡CH
√
1
2
3
4
5
6
7
8
9
10
3.(2019·黑龙江伊春第二中学期末)下列属于烯烃的是
A.CH3CH2CH3 B.CH2==CHCH3
C.CH2==CHCH2Cl D.CH2==CHCOOH
√
1
2
3
4
5
6
7
8
9
解析 CH3CH2CH3属于烷烃,CH2==CHCH2Cl含有氯元素,不为烃,CH2==CHCOOH含有氧元素,也不为烃,CH2==CH—CH3为丙烯,属于烯烃。
10
4.(2019·广东湛江一中月考)丙烯是合成聚丙烯塑料的化工原料,反应的方程式为nCH2==CH—CH3―→ ,下列有关说法错误的是
A.丙烯通过加聚反应合成聚丙烯
B.丙烯和聚丙烯均能使酸性高锰酸钾溶液褪色
C.丙烯为纯净物,聚丙烯为混合物
D.聚丙烯的平均相对分子质量为42n(n为聚合度)
1
2
3
4
5
6
7
8
9
√
题组二 常见的有机高分子材料
10
1
2
3
4
5
6
7
8
9
解析 丙烯通过加聚反应生成聚丙烯, 中的n不确定,因
此聚丙烯为混合物,其平均相对分子质量为42n。故A、C、D正确;
在聚丙烯的链中,不存在 ,故不能使酸性KMnO4溶液褪色,B错误。
10
5.(2019·深圳科学高中期中)橡胶属于重要的工业原料,它是一种有机高分子化合物,具有良好的弹性,但强度较差。为了增加某些橡胶制品的强度,加工时往往需要进行硫化处理,即使橡胶原料与硫黄在一定条件下反应。橡胶制品硫化程度越高,强度越大,同时弹性越差。下列橡胶制品中,加工时硫化程度较高的是
A.医用橡胶手套 B.皮鞋胶底
C.自行车内胎 D.橡皮筋
√
1
2
3
4
5
6
7
8
9
10
解析 根据橡胶制品硫化程度越高,强度越大,弹性越差的特点,可知皮鞋胶底应当强度大,弹性较橡胶手套、自行车内胎及橡皮筋要差,故皮鞋胶底的硫化程度较高。
1
2
3
4
5
6
7
8
9
10
1
2
3
4
5
6
7
8
9
6.(2020·山西太原一中高一检测)聚氯乙烯塑料在工农业生产中广泛应用,其结构简式为 ,它是由CH≡CH、HCl两种小分子经过系列
反应形成的,由聚氯乙烯分析合成过程中发生的反应类型有
①取代反应 ②加成反应 ③加聚反应 ④氧化反应
A.①③ B.②③ C.①②③ D.①③④
√
10
1
2
3
4
5
6
7
8
9
解析 由聚氯乙烯的结构简式可知,其单体为 ,据题给原料,
应由CH≡CH和HCl加成反应制得,因此制聚氯乙烯的过程应
有加成反应和加聚反应。
10
7.(2019·山东师范大学附中高一期末)桥环烃是指由两个碳环共用两个或两个以上碳原子的一类环烃,二环[1,1,0]丁烷( )是最简单一种桥环烃。下列关于该化合物的说法错误的是
A.与CH2==CHCH==CH2互为同分异构体
B.二氯代物共有4种
C.所含碳碳键不只是单键
D.每个碳原子均处于与其直接相连的原子构成的四面体内部
1
2
3
4
5
6
7
8
9
√
综合强化
10
解析 由二环[1,1,0]丁烷的结构简式可知其分子式为C4H6,它与CH2==CHCH==CH2互为同分异构体,A项正确;
二环[1,1,0]丁烷的二氯代物中,两个氯原子取代同一个碳原子上的氢原子的结构有1种,两个氯原子取代不同碳原子上的氢原子的结构有3种,共有4种,B项正确;
二环[1,1,0]丁烷分子中的碳碳键均是单键,C项错误;
二环[1,1,0]丁烷分子中,每个碳原子均形成4个单键,类似于甲烷分子中的碳原子,处于与其直接相连的原子构成的四面体内部,D项正确。
1
2
3
4
5
6
7
8
9
10
8.(2019·上海大学附属中学期中)丁腈橡胶( )
具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是
①CH2==CH—CH==CH2 ②CH3—C≡C—CH3 ③CH2==CH—CN
④CH3—CH==CHCN ⑤CH3—CH==CH2 ⑥CH3—CH==CH—CH3
A.①③ B.③⑥ C.②③ D.④⑤
1
2
3
4
5
6
7
8
9
√
10
解析 高聚物属于加聚产物,链节主链上存在碳碳双键结构,有6个碳原子,单体为两种。按如图所示断开
然后打开双键中的1个C—C,将半键闭合就得到高聚物单体:CH2==CH
—CH==CH2和CH2==CH—CN,故选A。
1
2
3
4
5
6
7
8
9
10
解析 CH≡CH和HCN加成生成CH2==CHCN,CH2==CHCN经过加聚反应生成聚丙烯腈。
9.(2020·甘肃陇南市一中高一检测)(1)写出以CH≡CH、HCN为原料制备聚丙烯腈(“人造羊毛”)的过程中所发生的反应类型___________________。
1
2
3
4
5
6
7
8
9
加成反应、加聚反应
10
(2)PVC(聚氯乙烯)和PE(聚乙烯)都是常用的塑料,它们的单体分别为____________和___________。
(3)PE(聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。辨别PE和PVC有三种方法,一是闻气味法:具有刺激性气味的是_________;二是测密度法:密度大的应是__________;三是燃烧法:PE的单体和PVC的单体在足量空气中燃烧的实验现象的明显区别是____
_______________________________________________________。
1
2
3
4
5
6
7
8
9
CH2==CHCl
CH2==CH2
聚氯乙烯
聚氯乙烯
聚乙烯更易燃烧,聚氯乙烯燃烧有白雾(HCl的小液滴)生成
10
解析 具有刺激性气味的是聚氯乙烯;聚氯乙烯中含有相对原子质量相对较大的氯原子,其密度比聚乙烯大;聚氯乙烯不易燃烧,燃烧时产生HCl,有白雾(含有HCl的小液滴)生成。
1
2
3
4
5
6
7
8
9
10
解析 PVDC的单体为CH2==CCl2,该单体的同分异构体为CHCl==CHCl。
(4)PVDC( )是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品等的包装。写出合成PVDC的单体的同分异构体的结构简式:_____________。
1
2
3
4
5
6
7
8
9
CHCl==CHCl
10
10.(2019·日照高一检测)聚四氟乙烯的耐热性和化学稳定性都超过其他塑料,甚至在“王水”中也不发生变化,故号称“塑料王”,在工业上有着广泛的用途。
(1)按照下列所示的合成路线,试在方框中填入合适的化合物的结构简式:
1
2
3
4
5
6
7
8
9
氯仿
二氟一氯甲烷
四氟乙烯
聚四氟乙烯
D
CHCl3
CHClF2
CF2==CF2
10
(2)写出下列化学方程式:
B→C:______________________________。
C→D:________________________________。
(3)聚四氟乙烯的链节为______________,单体为__________,四氟乙烯生成聚四氟乙烯的反应类型为_________。
1
2
3
4
5
6
7
8
9
—CF2—CF2—
加聚反应
CF2==CF2
解析 根据信息,氯仿为三氯甲烷(CHCl3),找出反应物与生成物之间的关系,写出化学方程式。
返回
10
1.(2020·吉林延边二中检测)设NA为阿伏加德罗常数,下列说法正确的是
A.22.4 L CH4分子中含有10NA个电子
B.16 g CH4分子中含有4NA个C—H
C.等体积的CH4和NH3所含氢原子数之比为4∶3
D.等质量的CH4和HF所含共价键数目之比为4∶1
17
一、常见烃的成键特点与结构
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
√
17
解析 A、C两项均未说明气体所处状况,故无法计算;
D项,等质量的CH4和HF所含有共价键数目之比为
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
2.(2019·河北沧州一中高一月考)下列有关乙烯的说法中错误的是
A.乙烯分子的双键中有一个键较易断裂
B.乙烯分子中所有原子都在同一个平面上,且碳氢键之间的键角约为120°
C.乙烯的化学性质较甲烷活泼
D.乙烯和环己烷( )的分子组成符合通式CnH2n,因此它们互为同系物
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 乙烯分子中含有碳碳双键,其中一个键容易断裂,故乙烯化学性质比乙烷活泼,容易发生加成反应和氧化反应,A、C正确;
乙烯分子是平面结构,所有原子都在同一个平面上,且碳氢键之间的键角约为120°,B正确;
乙烯与环己烷的结构不相似,不是同类物质,不互为同系物,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
3.(2020·江西九江一中高一检测)某直链烷烃分子中有18个氢原子,它的分子式为
A.C8H18 B.C9H18 C.C10H18 D.C11H18
√
解析 直链烷烃的分子通式为CnH2n+2,由题意得2n+2=18,解得n=8,该直链烷烃的分子式是C8H18。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
4.(2019·河南信阳高级中学月考)已知某有机物含有4个C,每个碳原子都以键长相等的三条单键连接3个C,且整个结构中所有碳碳键之间的夹角都为60°,则下列说法不正确的是
A.该有机物不存在
B.该有机物的分子式为C4H4
C.该有机物的空间结构为正四面体
D.该有机物的一氯代物仅有1种
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 该有机物结构为 ,A错误,C正确;
据题给信息,推知该有机物分子式为C4H4,分子完全对称,只有一种位置的H原子,因此一氯代物仅有1种,B、D正确。
5.(2019·青海湟川中学检测)已知某种气态化石燃料中含有碳和氢两种元素。为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
实验前 实验后
干燥剂和U形管的总质量 101.1 g 102.9 g
石灰水和广口瓶的总质量 312.0 g 314.2 g
解析 生成水的质量为102.9 g-101.1 g=1.8 g,生成正盐即CaCO3的质
量为
根据实验数据求:
(1)实验完毕后,生成物中水的质量为_____g。假设广口瓶里生成一种正盐,其质量为____g。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1.8
5
(2)生成的水中氢元素的质量为_____g。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
0.2
(3)生成的CO2中碳元素的质量为_____g。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
0.6
(4)气态化石燃料中碳元素与氢元素的质量比为________,该烃的分子式为______。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
3∶1
CH4
解析 碳元素与氢元素的质量比为0.6 g∶0.2 g=3∶1,由此可求出碳和氢的原子个数之比为 ,根据碳原子的成键特点,该烃为CH4。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
二、同系物与同分异构体性质及判断
6.(2019·江西奉新一中高一期中)有A、B两种烃,碳元素的质量分数相同,下列关于A和B的叙述中正确的是
A.A和B一定是同分异构体
B.A和B不可能是同系物
C.燃烧等质量的A和B,消耗氧气的量一定相等
D.A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 因烃中只有碳、氢两种元素,碳元素的质量分数相同,所以氢元素的质量分数也相同,最简式相同,因此燃烧相同质量的两种物质,消耗氧气的量一定相等,C正确;
最简式相同的烃,可能是同分异构体,如丙烯与环丙烷,也可能不是,比如乙炔和苯,A错误;
最简式相同的烃,可能是同系物,如乙烯与丙烯,B错误;
若为同分异构体,则A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等;若为同系物,则A和B各1 mol完全燃烧后生成的二氧化碳的质量一定不相等,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
7.(2020·甘肃陇南一中检测)C5H12有3种不同的结构,甲:CH3(CH2)3CH3,乙:CH3CH(CH3)CH2CH3,丙:C(CH3)4,下列相关叙述正确的是
A.甲、乙、丙属同系物,均可与氯气、溴蒸气发生取代反应
B.C5H12表示一种纯净物
C.甲、乙、丙中,丙的沸点最低
D.乙有3种不同沸点的一氯取代物
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 甲、乙、丙的结构不同,分子式相同,互为同分异构体,A错误;
C5H12有3种同分异构体,所以不能表示纯净物,B错误;
烷烃的同分异构体中,支链越多,沸点越低,丙分子中支链最多,所以沸点最低,C正确;
乙分子中有4种位置的氢原子,即: ,故一氯代物
有4种,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
8.(2020·广西师大附属中高一期中)有以下结构的三种烃分子,下列有关说法错误的是
A.1 mol甲分子内含有10 mol共价键
B.由乙分子构成的物质不能使溴的四氯化碳溶液褪色
C.丙分子的二氯取代产物只有3种
D.三种分子内成键方式相同,而且最简式相同,故互为同系物
√
解析 1 mol甲分子中含有6 mol碳碳单键和4 mol碳氢键,A正确;
乙分子中不存在不饱和的 或“—C≡C—”,不能使溴的四氯化
碳溶液褪色,B正确;
丙分子有取代基位于棱边、面对角线、体对角线三种位置关系的二氯代物,C正确;
甲、乙、丙三种分子的分子式分别为C4H4、C6H6和C8H8,最简式相同,但分子组成上不是相差若干个CH2原子团,故不互为同系物,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
9.(2019·安徽黄山屯溪第一中学月考)a、b、c的分子式均为C8H8,其结构如下所示,下列说法错误的是
A.a的同分异构体可与苯互为同系物
B.c苯环上的一氯代物有3种
C.b能与溴水发生加成反应
D.c中所有原子可以处于同一平面
√
解析 a的同分异构体分子式为C8H8,苯的分子式为C6H6,分子组成上不相差若干个CH2原子团,故a的同分异构体和苯不互为同系物,A错误;
c分子苯环上有三种位置的H原子,故苯环上的一氯代物有3种,B正确;
b分子中含有 ,故可以和Br2发生加成反应,C正确;
苯环和 都是平面结构,且单键可以旋转,故C分子中所有原子可以共平面,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
三、常见烃的性质及应用
10.(2019·山东济宁二中高一期中)甲烷是天然气的主要成分,是一种高效、低耗、污染小的清洁能源。下列有关甲烷的说法正确的是
①甲烷是一种正四面体结构的分子
②甲烷与氯气按物质的量之比为1∶1发生取代反应时,生成物只有CH3Cl和HCl
③0.5 mol CH4完全燃烧时消耗1 mol O2
④1 mol CH4全部生成CCl4,最多消耗2 mol Cl2
A.①② B.③④ C.①③ D.②④
√
解析 ①甲烷是一种正四面体结构的分子,正确;
②甲烷与氯气按物质的量之比为1∶1发生取代反应时,生成物不是只有CH3Cl和HCl,还含有CH2Cl2、CHCl3、CCl4,错误;
③1 mol CH4完全燃烧时,消耗2 mol O2,则0.5 mol CH4完全燃烧时消耗
1 mol O2,正确;
④根据取代反应的特点,1 mol CH4全部生成CCl4,最多消耗4 mol Cl2,错误。综上分析, 答案选C。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
11.(2019·四川成都外国语学校高一月考)柠檬烯具有良好的镇咳、祛痰、抑菌作用,其结构如图所示。下列关于柠檬烯的说法正确的是
A.1 mol柠檬烯只能与1 mol Br2发生加成反应
B.能发生取代反应、加成反应和氧化反应
C.属于乙烯的同系物
D.不能使酸性高锰酸钾溶液褪色
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 A项,1 mol柠檬烯能与2 mol Br2发生加成反应,错误;
B项,柠檬烯能与气态卤素单质在光照条件下发生取代反应,分子中含有碳碳双键,能与H2发生加成反应,也可以被O2、酸性KMnO4溶液氧化,正确;
C项,一个柠檬烯分子中有两个碳碳双键,且分子中含有环状结构,与乙烯的结构不相同,故其不属于乙烯的同系物,错误;
D项,柠檬烯分子中含有碳碳双键,能使酸性高锰酸钾溶液褪色,错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
12.(2019·河北邢台一中高一第一次月考)已知1 mol链烃CxHy可以发生如下系列转化:
(无机试剂是足量的)
下列说法错误的是
A.x=5、n(Cl2)=11 mol
B.用酸性高锰酸钾溶液可以区分CxHy和Q
C.上述转化过程中依次发生了加成反应和取代反应
D.CxCl12可能的结构有三种
√
解析 CxHy可与HCl发生加成反应,则含有不饱和键,消耗HCl的物质的量为1 mol,则1个CxHy分子中含有1个碳碳双键,生成的Q为氯代烷烃,分子式为CxHy+1Cl,Q与氯气在光照条件下发生取代反应生成CxCl12,CxCl12中不含不饱和键,则x=5,y=10,消耗氯气的物质的量为11 mol,A正确;
C5H10中含有碳碳双键,能使酸性高锰酸钾溶液褪色,C5H11Cl不能使酸性高锰酸钾溶液褪色,可以区分,B正确;
C5H10与HCl发生加成反应,C5H11Cl与氯气发生取代反应,C正确;
新戊烷不存在对应烯烃,则符合题中转化关系的C5Cl12可能的结构只有两种,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
13.(2019·济南高一检测)石油是工业的血液,与我们的生产、生活息息相关,乙烯的产量通常用来
衡量一个国家的石油化工
水平。根据右面转化关系
回答下列问题:
(1)乙烯的结构简式为__________。
CH2==CH2
解析 乙烯为平面四边形结构,官能团为碳碳双键,结构简式为CH2==CH2。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
(2)写出乙烯和水反应生成B的反应③的化学方程式(注明条件):_________
_______________________,反应类型为__________。写出反应⑥的化学
方程式(注明条件):_________________________________。
CH2==CH2
加成反应
解析 乙烯和水发生反应生成乙醇,化学方程式为CH2==CH2+H2O
CH3CH2OH,该反应为加成反应,反应⑥为乙烷与氯气在光照条件下发生取代反应生成氯乙烷,反应方程式为CH3CH3+Cl2
CH3CH2Cl+HCl。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 氯乙烷可通过乙烯与氯化氢发生加成反应和乙烷与氯气发生取代反应制得,最好的方法是加成反应④,因为乙烷与氯气反应将得到多种氯代物的混合物,产物不纯。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
(3)物质C的沸点为12.27 ℃,常用于局部冷冻麻醉应急处理。物质C可通过反应④和反应⑥制得,其中
最好的方法是反应____(填“④”
或“⑥”),理由为_________
__________________________
_________________。
④
乙烷与氯气反应将得到多种氯代物的混合物,产物不纯
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
四、有机高分子材料及其应用
14.(2020·广西玉林高级中学高一检测)下列说法不正确的是
A.高分子材料的原料一般具有价廉、易得、适用于大规模生产的特点,
且来自含量较少的自然资源
B.棉花、羊毛和天然橡胶是有机高分子材料
C.合成高分子材料包括塑料、合成纤维、合成橡胶、黏合剂、涂料等
D.三大合成材料为塑料、合成纤维、合成橡胶
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 高分子材料的原料一般来自含量丰富的自然资源,故A错误;
棉花、羊毛和天然橡胶是天然有机高分子材料,故B正确;
合成高分子材料包括塑料、合成纤维、合成橡胶、黏合剂、涂料等,故C正确;
三大合成材料为塑料、合成纤维、合成橡胶,故D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
15.(2020·安徽阜阳一中高一检测)聚苯乙烯是日常生活中用途非常广泛的一种塑料,下列说法不正确的是
A.其单体为 ,经过加聚反应制得
B.链节为
C.平均相对分子质量为104n(n为聚合度)
D.是一种难降解的塑料,会造成环境污染
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 聚苯乙烯是由 经过加聚反应生成,单体为 ,
链节为 ,故A正确,B错误;
聚苯乙烯链节的相对分子质量为104,故聚苯乙烯的平均相对分子质量104n(n为聚合度),C正确;
聚苯乙烯是一种难降解的塑料,会导致环境污染,故D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
16.(2019·江苏海安高级中学期中)加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯。用如图所示装置探究废旧塑料的再利用。下列叙述不正确的是
A.聚丙烯塑料和丙烯都能使溴的四
氯化碳溶液褪色
B.装置乙的试管可收集到液态烃,
主要成分为苯和甲苯
C.装置丙内发生的反应为加成反应
D.最后收集到的气体是优良的燃料
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
解析 聚丙烯塑料结构中无“ ”,不能使溴的四氯化碳溶液褪
色,A错误;
产物中的 和 沸点
较高,经液化可被收集,B正确;
乙烯、丙烯在丙装置中和Br2发生加成反应而被吸收,C正确;
最后气体为H2和CH4,是优良的燃料,D正确。
17.(2019·山东泰山一中高一检测)某高分子化合物结构如下:
其单体可能是
①CH2==CH—CN ②CH2==CH2
③CH2==CH—CH==CH2 ④
⑤ ⑥CH2==CH—CH2—CH3
A.①③⑤ B.②③⑤ C.①②⑥ D.①③④
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
√
解析 根据“见双键,四个碳;无双键,两个碳”划线断开,则该聚合物按照如下断键方式断裂: ,
断键后将半键闭合,即将单双键互换,得到的单体为CH2==CHCN、
CH2==CH—CH==CH2和 ,则A项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
17
18.(2020·江苏省江一中学高一检测)现有①甲烷、②乙烯、③丙烯、④苯、⑤苯乙烯5种烃,请用序号或按题中要求作答:
(1)分子中所有原子一定都共平面的是______。
②④
解析 乙烯、苯分子中所有原子均处于同一平面上,丙烯中存在甲基,甲基上的原子为四面体构型,故丙烯分子中所有原子不可能在一个平面内,苯乙烯中苯环和乙烯基团之间的单键可以旋转,故苯乙烯分子中所有原子不一定在同一平面内。
解析 完全燃烧后生成CO2和H2O的物质的量之比为1∶1,则有机物分子中C、H原子个数比为1∶2,CH2==CH2、CH3CH==CH2均符合上述要求。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
17
(2)相同质量的上述烃完全燃烧耗氧量最高的是__________,其电子式为
__________。
①
解析 相同质量的烃中,甲烷的含氢量最高,因此耗氧量最大。
(3)完全燃烧后生成的CO2和水的物质的量之比为1∶1的化合物是______。
②③
解析 苯乙烯在一定条件下发生加聚反应,化学方程式为n
。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
18
17
(4)⑤在一定条件下反应生成高分子材料的化学方程式:______________
_________________________,反应类型为__________。
加聚反应
3、 式量为128的烃可能为:
式量为30的有机物可能为:
式量为44的有机物可能为:
式量为46的有机物可能为:
式量为60的有机物可能为:
ω(C)=40%的有机物可能为:
C3H8、CH3CHO、环氧乙烷
C2H6、HCHO
C9H20、C10H8
C2H5OH、CH3OCH3、HCOOH
C3H7OH(2种)、CH3OCH2CH3、
CH3COOH、HCOOCH3、HOCH2CHO、
CO(NH2)2
五、乙烯的制法
工业制法:从石油化学工业产生的气体中分离得到。
实验室制法?
C
—
—
C
—
—
|
|
H
H
H
H
+ H2O
浓H2SO4
C
—
C
—
—
|
|
H
H
H
H
|
|
H
OH
实验室制法:
↑
170℃
消去反应:有机化合物在一定条件下,一个分子脱去一个小分子 (如:H2O,HBr等) ,而生成不饱和 (含双键或三键)化合物的反应。
应选用什么装置制取乙烯呢?与哪种制气装置相似?
1、应选用什么装置制取乙烯呢?与哪种制气装置相似?
监控反应温度;温度计水银球应在液面以下,不触瓶底。
液体(+固体)加热制取气体;与制氯气装置相似。
2、为何使用温度计?温度计水银球应在 什么位置?
3、这样的气体发生装置(液体加热)还差一样重要的实验用品——碎瓷片!
你知道有何必要,作何用途吗?
沸石:防止暴沸
(暴沸:液体受热沸腾时剧烈跳动)
碎瓷片
邬
邬
7、根据实验现象,联系已学知识,推测所得乙烯气体中可能包括哪些气体?如何除去杂质?
浓硫酸量多是 为避免过度稀释,反应不充分。
先撤导管后灭灯。
4、乙醇与浓硫酸以体积比1∶3混合,为什么浓硫酸要多些?实验完毕,是先撤酒精灯,还是先撤导管?
浓硫酸作 脱水剂 和 催化剂。
5、浓硫酸在反应中的作用?
乙烯是无色、稍有气味的气体,难溶于水,密度略小于空气(S.P.T. 1.25 g/L)。
6、能否用排气法收集乙烯?乙烯有哪些物理性质?
C2H4、H2O、CO2、SO2……
8、乙醇脱水制乙烯 为啥控温一百七?
C
—
—
C
—
—
|
|
H
H
H
H
+ H2O
浓H2SO4
C
—
C
—
—
|
|
H
H
H
H
|
|
H
O-H
↑
170℃
C
—
C
—
—
|
|
H
H
H
H
|
|
H
O-H
+
C
—
C
—
—
|
|
H
H
H
H
|
|
H-O
H
-OH 羟基上的H原子也容易脱去
浓H2SO4
140℃
+ H2O
C
—
C
—
—
|
|
H
H
H
|
|
H
H
C
—
C
—
—
|
|
H
H
O
H
|
|
H
H
分子内脱水
分子间脱水
CH3CH2OCH2CH3
乙醚
思考:什么事实证明了甲烷不是
平面十字结构而是正四面体结构?
思考:什么事实证明了苯不是
单双键交替出现的结构?
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
