1.1 物质的分类及转化 课后练习(含解析) 化学人教版(2019)必修第一册
文档属性
| 名称 | 1.1 物质的分类及转化 课后练习(含解析) 化学人教版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 382.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-17 00:00:00 | ||
图片预览




文档简介
1.1 物质的分类及转化 课后练习
2023-2024学年高一上学期化学人教版(2019)必修第一册
一、单选题
1.胶体在自然界普遍存在,下列事实与胶体无关的是( )
A.将某些胶态金属氧化物分散于玻璃中制成有色玻璃
B.光线透过树叶间的缝隙射入密林中时,会看到一道道光柱
C.将纳米二氧化硅颗粒(直径)均匀分散到树脂中形成的分散系
D.植物油与水混合,充分振荡后可形成油水混合物
2.下列叙述正确的是( )
A.物质按照组成可以分为单质和化合物
B.氢氧化铁胶体带正电荷,土壤胶体带负电荷
C.无机化合物主要包括:酸、碱、盐和氧化物
D.按照树状分类法可将化学反应分为:氧化还原反应和离子反应
3.科学家发现了一种纯碳新材料“碳纳米泡沫”,每个碳纳米泡沫含有约4000个碳原子,直径约6~9nm,则这种“碳纳米泡沫”分散到空气中属于( )
A.溶液 B.悬浊液 C.乳浊液 D.胶体
4.分类法是学习和研究化学的一种常用的科学方法,下列正确的是( )
A.、、都是碱性氧化物
B.只含一种元素的物质一定是纯净物
C.与均含相同的元素氢,故也可以称为酸
D.液氯、均属于纯净物
5.下列关于分散系的说法错误的是( )
A.直径为1.3×10-9 m的“钴钛菁”分子在水中形成的分散系属于胶体
B.向沸水中滴加适量饱和FeCl3溶液,能形成带电的胶体
C.向氢氧化铁胶体中滴加稀硫酸,先产生沉淀,后沉淀溶解
D.利用丁达尔效应可区分溶液与胶体
6.下列属于碱性氧化物的是( )
A.CO2 B.Na2O2 C.SiO2 D.CaO
7.胶体与溶液的本质差异在于( )
A.是否稳定 B.是否有颜色
C.是否透明 D.粒子直径大小
8.在沸水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。下列说法正确的是( )
A.用激光笔照射该液体,会出现丁达尔效应
B.将液体静置片刻,会出现沉淀现象
C.所得分散系中分散质的粒子直径大于100 nm
D.用滤纸可实现该分散系中分散剂与分散质的分离
9.下列分散系不能产生“丁达尔效应”的是( )
A.墨水 B.硫酸钠溶液
C.氢氧化铁胶体 D.淀粉溶液
10.下列物质的分类正确的是( )
混合物 纯净物 酸性氧化物 碱 盐
A 空气 Fe(OH)3胶体 CO2 石灰水 KAl(SO4)2
B 豆浆 Cu SO3 烧碱 NaHCO3
C 稀硫酸 石墨 CO 氨气 CuSO4·5H2O
D 冰水混合物 生石灰 Cl2O7 纯碱 Cu2(OH)2CO3
A.A B.B
C.C D.D
11.能产生“丁达尔效应”的是( )
A.饱和食盐水 B.Fe(OH)3胶体 C.盐酸 D.硫酸铜溶液
12.下列物质中,不属于盐类的是( )
A.KOH B.MgCl2 C.KNO3 D.NaHCO3
13.X、Y、Z、W各代表一种物质,若X+Y=Z+W,则X和Y的反应不可能是( )
A.盐和盐的反应 B.酸与碱的反应
C.碱性氧化物和水的反应 D.酸性氧化物和碱的反应
14.以下有关垃圾分类说法正确的是( )
A.茶叶果皮属于厨余垃圾,可通过转化变为有机氮肥
B.废旧玻璃属于可回收垃圾,其主要成分为新型无机非金属材料
C.食品包装塑料袋属于其他垃圾,其主要成分聚氯乙烯为有机高分子化合物
D.医疗废弃物属于有害垃圾,经过处理、消毒后可加工成儿童玩具
15.一些装有化学物质的容器上常贴有危险化学品的标志。下列标志中,应贴在装有乙醇的容器上的是( )
A. B.
C. D.
16.下列有关叙述、对应的方程式、所属基本反应类型都正确的是( )
A.葡萄糖在人体内氧化氧化反应
B.拉瓦锡研究空气成分分解反应
C.生石灰作干燥剂化合反应
D.三氧化硫与氢氧化钠溶液反应复分解反应
17.按照物质的树状分类和交叉分类,硫酸应属于( )
①酸 ②能导电的纯净物 ③含氧酸 ④混合物 ⑤化合物 ⑥二元酸
A.①②③④ B.①③⑤⑥ C.①②③⑤⑥ D.②③⑤⑥
18.下列物质归类正确的是( )
A.硝酸盐:芒硝、硝石 B.碱:烧碱、纯碱
C.硫酸盐:胆矾、明矾 D.混合物:液氨、漂白粉
19.当光束通过下列物质时,不会出现丁达尔效应的是
A.冰水混合物 B.云 C.雾 D.Fe(OH)3胶体
20.下列物质不能通过化合反应直接制得的是( )
A.Fe(OH)3 B.FeCl2 C.CuS D.FeCl3
二、综合题
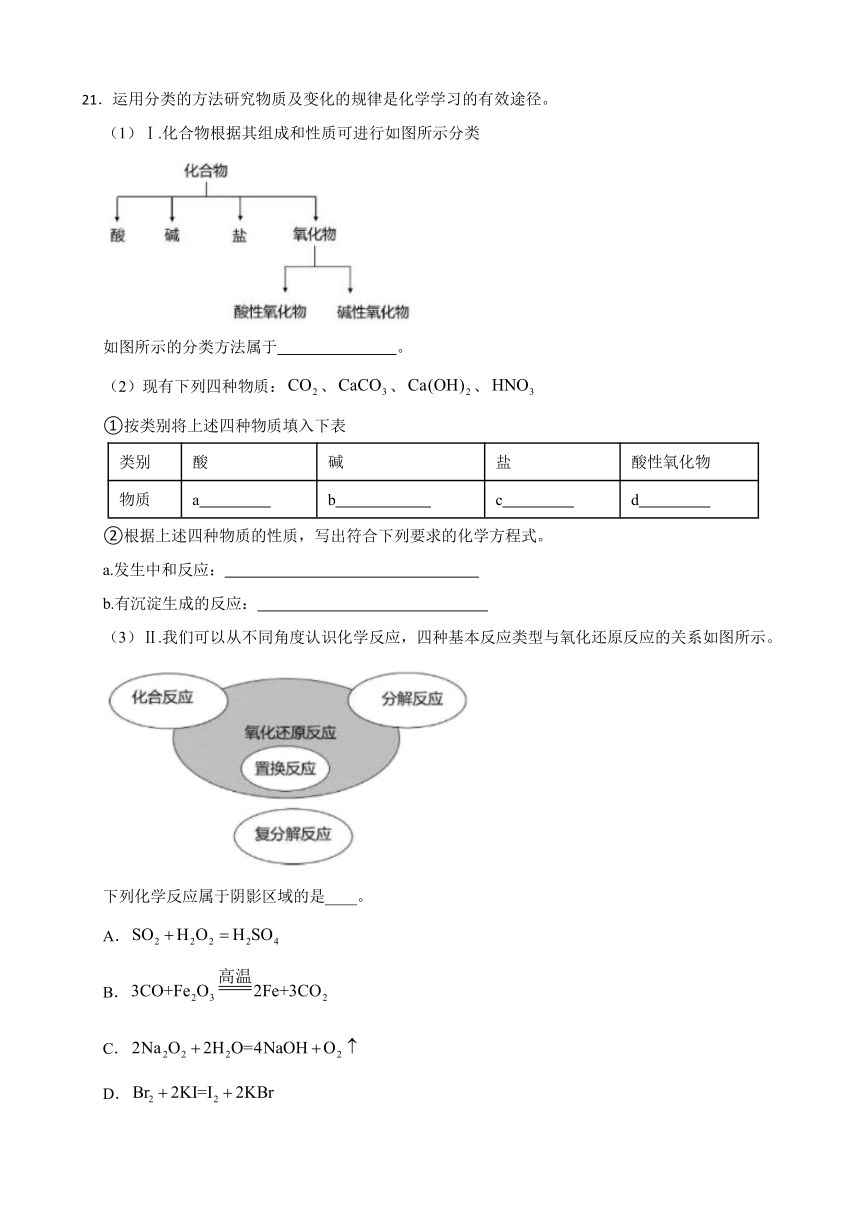
21.运用分类的方法研究物质及变化的规律是化学学习的有效途径。
(1)Ⅰ.化合物根据其组成和性质可进行如图所示分类
如图所示的分类方法属于 。
(2)现有下列四种物质:、、、
①按类别将上述四种物质填入下表
类别 酸 碱 盐 酸性氧化物
物质 a b c d
②根据上述四种物质的性质,写出符合下列要求的化学方程式。
a.发生中和反应:
b.有沉淀生成的反应:
(3)Ⅱ.我们可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示。
下列化学反应属于阴影区域的是____。
A.
B.
C.
D.
E.
22.运用树状分类法对下列9种物质进行分类,然后按要求回答问题:
(1)进行分类(将各物质序号填入相应方框中),并在相应空格处作答 。
(2)氢氧化铁胶体和氯化铁溶液从外观上很难进行区分,你认为可通过什么实验来区分? (简要说明实验方法和判断依据)。
(3)写出上述10种物质中的强酸强碱混合,发生中和反应的化学方程式: 。
23.某化学小组制备氢氧化铁胶体:洁净的小烧杯盛适量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol·L-1氯化铁溶液,至液体呈透明的红褐色。回答下列问题:
(1)氢氧化铁胶体中微粒直径的范围是 。
(2)检验胶体制备成功的操作是 。
(3)实验中手不慎被玻璃割破,可用氯化铁溶液应急止血,主要原因是 (填序号)。
①氯化铁溶液具有杀菌消毒的作用
②氯化铁溶液能使血液胶体凝固
③氯化铁溶液能产生氢氧化铁沉淀堵住伤口
④氯化铁溶液能使血液发生化学变化
(4)制备胶体的化学方程式为 。如果将1molFeCl3全部制成胶体,胶粒数目 NA(选填“大于”“等于”“小于”)。
24.现有下列10种物质:①H2O、②空气、③Mg、④CaO、⑤H2SO4、⑥Ca(OH)2、⑦CuSO4·5H2O、⑧碘酒、⑨C2H5OH和⑩NaHCO3。其中,
(1)属于混合物的是 (填序号,下同);
(2)属于氧化物的是 ;
(3)属于酸的是 ;
(4)属于碱的是 ;
(5)属于盐的是 ;
(6)属于有机物的是 。
25.将少量饱和FeCl3溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
(1)将丙继续加热煮沸至液体呈红褐色,反应的化学方程式为 。
(2)如何用最简单的方法判断丙中是否成功制备出胶体 。
(3)向经过检验后的丙中逐滴加入盐酸,会出现一系列变化:
①先出现和乙中相同的现象,原因是 ;
②随后发生变化得到和甲相同的溶液,此反应的离子方程式为 。
答案解析部分
1.【答案】D
【解析】【解答】A.有色玻璃是固溶胶,A不符合题意;
B.光线透过树叶间的缝隙射入密林中时,会看到一道道光柱是丁达尔效应,B不符合题意;
C.纳米二氧化硅颗粒(直径1 100nm)均匀分散到树脂中形成的分散系属于胶体,C不符合题意;
D.植物油与水混合,充分振荡后可形成油水混合物属于乳浊液,D符合题意;
故答案为:D。
【分析】分散质粒子直径位于1~100nm之间的分散系为胶体,胶体能产生丁达尔效应。
2.【答案】C
【解析】【解答】A、按照组成,可将物质分为纯净物和混合物,按照物质的组成元素,可将纯净物分为单质和化合物,故A错误;
B、胶体不带电,带电的为胶体微粒,故B错误;
C、无机物通常分为酸、碱、盐和氧化物等,故C正确;
D、氧化还原反应与离子反应是交叉关系,按树状分类应为氧化还原反应和非氧化还原反应,故D错误;
故答案为:C。
【分析】A、物质按照组成可以分为纯净物和混合物;
B、胶体不带电;
C、无机化合物包括酸、碱、盐等;
D、氧化还原反应与离子反应是交叉关系。
3.【答案】D
【解析】【解答】每个碳纳米泡沫含有约4000个碳原子,直径约6~9nm,则“碳纳米泡沫”分散到空气形成胶体分散系,故选D;
故答案为:D。
【分析】分散质粒子直径介于1~100nm之间的分散系为胶体。
4.【答案】D
【解析】【解答】A.碱性氧化物和酸反应只生成盐和水,和酸反应还生成氧气,属于过氧化物,A不符合题意;
B.同种元素可能形成不同的单质,如金刚石、石墨只含碳元素,二者在一起是混合物,B不符合题意;
C.酸是电离出的阳离子只有氢离子的化合物,属于酸式盐,C不符合题意;
D.液氯、均属于纯净物,D符合题意;
故答案为:D。
【分析】A、碱性氧化物和酸反应只生成盐和水;
B、纯净物的特点是只有一种分子;
C、酸的特点是电离的阳离子只有氢离子;
D、液氯和五水合硫酸铜都是纯净物。
5.【答案】B
【解析】【解答】A.胶体中分散质粒子直径为1~100nm,直径为1.3×10-9 m的“钴钛菁”分子在水中形成的分散系属于胶体,故A不符合题意;
B.胶体不带电,胶粒带电,向沸水中滴加适量饱和FeCl3溶液,能形胶粒带正电荷的胶体,故B符合题意;
C.氢氧化铁胶体中加入硫酸发生聚沉,氢氧化铁与硫酸反应生成硫酸铁溶液,所以先产生沉淀,后沉淀溶解,故C不符合题意;
D.胶体能产生丁达尔效应,溶液不能,所以利用丁达尔效应可区分溶液与胶体,故D不符合题意。
【分析】A.根据胶体粒子的直径进行判断;
B.胶体本身不带电;
C.氢氧化铁胶体中加入电解质发生聚沉,氢氧化铁沉淀与过量盐酸反应又会溶解;
D.胶体具有丁达尔效应,而溶液没有丁达尔效应。
6.【答案】D
【解析】【解答】A. CO2与NaOH反应产生Na2CO3和H2O,所以CO2属于酸性氧化物,A不符合题意;
B. Na2O2与HCl反应产生NaCl、H2O和O2,所以Na2O2不是碱性氧化物,B不符合题意;
C. SiO2与NaOH反应产生Na2SiO3和H2O,所以SiO2是酸性氧化物,C不符合题意;
D. CaO和HCl反应产生CaCl2和H2O,所以CaO是碱性氧化物,D符合题意;
故答案为:D。
【分析】和碱反应生成盐和水的氧化物是酸性氧化物,和酸反应生成盐和水的氧化物是碱性氧化物。
7.【答案】D
【解析】【解答】胶体与溶液的本质区别是微粒直径大小,微粒直径在1nm-100nm之间的分散系为胶体,小于1nm的分散系为溶液,
故答案为:D
【分析】溶液、胶体和浊液的划分就是根据分散质离子直径大小的原则。
8.【答案】A
【解析】【解答】A.制取得到液体是Fe(OH)3胶体,会产生丁达尔效应,因此用激光笔照射该液体,能够产生一条光亮的通路,A符合题意;
B.制取得到的Fe(OH)3胶体是一种介稳体系,将其静置,不会出现沉淀现象,B不符合题意;
C.制取得到的是Fe(OH)3胶体,分散质微粒直径在1-100 nm之间,C不符合题意;
D.胶体微粒及离子都可通过滤纸,因此不能用滤纸可实现该分散系中分散剂与分散质的分离,D不符合题意;
故答案为:A。
【分析】 在沸水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至溶液呈红褐色 ,得到Fe(OH)3胶体,胶体粒子是大量氢氧化铁的聚集体,根据胶体的性质解答该题。
9.【答案】B
【解析】【解答】A. 墨水属于胶体,能产生“丁达尔效应”,A不符合题意;
B. 硫酸钠溶液属于溶液,不能产生“丁达尔效应”,B符合题意;
C. 氢氧化铁胶体,产生“丁达尔效应”,C不符合题意;
D. 淀粉溶液属于胶体,产生“丁达尔效应”,D不符合题意;
故答案为:B。
【分析】有丁达尔效应的产生说明是胶体,找出不是胶体的即可
10.【答案】B
【解析】【解答】A.Fe(OH)3胶体中含有多种物质,属于混合物,A不符合题意;
B.各物质的分类正确,B符合题意;
C.CO不能与碱反应生成盐和水,故CO不是酸性氧化物,氨气无法电离产生OH-,故氨气也不是碱,C不符合题意;
D.冰水混合物的成分为水,只含有一种物质,为纯净物,纯碱为Na2CO3,属于盐,D不符合题意;
故答案为:B
【分析】此题是对物质分类的考查,结合混合物、纯净物、酸性氧化物、碱和盐的相关概念进行分析即可。
11.【答案】B
【解析】【解答】A.饱和食盐水属于溶液,不具有丁达尔效应,故A不符合题意;
B.Fe(OH)3胶体属于胶体,能发生丁达尔效应,故B符合题意;
C.盐酸属于溶液,不具有丁达尔效应,故C不符合题意;
D.硫酸铜溶液属于溶液,不具有丁达尔效应,故D不符合题意;
故答案为:B。
【分析】具有丁达尔效应的是胶体,结合选项找出即可
12.【答案】A
【解析】【解答】A.KOH电离出的阴离子全部是OH-,则KOH是碱,不属于盐,故A符合题意;
B.MgCl2是由金属镁离子和盐酸根组成的化合物,属于盐酸盐,故B不符合题意;
C.KNO3是由金属钾离子和硝酸根组成的化合物,属于硝酸盐,故C不符合题意;
D.NaHCO3是由钠离子和碳酸氢根离子构成的化合物,属于盐,故D不符合题意;
故答案为:A。
【分析】盐是由金属离子(或铵根离子)和酸根离子组成的化合物,据此进行分析判断。
13.【答案】C
【解析】【解答】A.盐和盐反应会产生两种新盐,反应物、生成物都是两种,A不符合题意;
B.酸与碱反应产生盐和水,反应物、生成物都是两种,B不符合题意;
C.碱性氧化物和水反应产生碱,反应物是两种,生成物只有一种,C符合题意;
D.酸性氧化物和碱反应产生盐和水,反应物、生成物都是两种,D不符合题意;
故答案为:C。
【分析】依据化学方程式反应物和产物的个数确定反应类型。
14.【答案】A
【解析】【解答】A. 茶叶果皮属于厨余垃圾,主要成分为有机物、可通过转化变为有机氮肥,A符合题意;
B. 废旧玻璃属于可回收垃圾,其主要成分为硅酸盐,不属于新型无机非金属材料,B不符合题意;
C. 聚氯乙烯不可用于食品包装,食品包装塑料袋主要成分为聚乙烯、属于有机高分子化合物,C不符合题意;
D. 医疗废弃物属于有害垃圾,应由指定专业机构回收处理、不可加工成儿童玩具,D不符合题意;
故答案为:A。
【分析】A.氮肥主要是含有氮元素
B.废旧玻璃是传统的无机非金属材料
C.聚氯乙烯有毒一般用于垃圾袋
D.儿童玩具的原材料必须是无毒的
15.【答案】B
【解析】【解答】乙醇是可燃性液体,易燃烧,因此应贴在装有乙醇的容器上的是易燃液体的标识。
故答案为:B。
【分析】依据物质的性质确定标识。
16.【答案】C
【解析】【解答】A.氧化反应不是基本反应类型,A不符合题意;
B.方程式没有配平,B不符合题意;
C.生石灰与水反应生成氢氧化钙,属于化合反应,C符合题意;
D.三氧化硫与氢氧化钠溶液的反应不属于复分解反应类型,D不符合题意;
故答案为:C。
【分析】基本反应类型包括:分解反应、化合反应、复分解反应和置换反应。
17.【答案】B
【解析】【解答】硫酸应属于⑤化合物,也属于①酸,还属于③含氧酸,也属于⑥二元酸,故答案:B符合题意;
故答案为:B。
【分析】硫酸电离的阳离子只有氢离子,溶液中有自由移动的阴阳离子,含有氧元素,电离出2个自由移动的阴离子。
18.【答案】C
【解析】【解答】A.硝石主要成分是KNO3,属于硝酸盐,而芒硝是Na2SO4 10H2O的俗名,属于硫酸盐,故A不符合题意;
B.烧碱是NaOH的俗名,属于碱,但纯碱是Na2CO3属于盐,故B不符合题意;
C.胆矾是CuSO4 5H2O,明矾是KAl(SO4)2 12H2O,都属于硫酸盐,故C符合题意;
D.漂白粉的主要成分是氯化钙和次氯酸钙,属于混合物,而液氨是液态的氨,为纯净物,故D不符合题意;
故答案为:C。
【分析】A.硝酸盐主要含有硝酸根,但是芒硝不含硝酸根不是硝酸盐
B.碱是在水溶液中电离出的阴离子全部是氢和氧根离子,但是纯碱不是碱
C.硫酸盐是含有硫酸根的盐,胆矾和明矾具有硫酸根
D.混合物是含有多种物质,但是液氨是单质只含有一种物质,漂白粉是混合物
19.【答案】A
【解析】【解答】A.冰水混合物不属于胶体,A符合题意;
B.云属于气溶胶,B不符合题意;
C.雾属于气溶胶,C不符合题意;
D.Fe(OH)3胶体属于液溶胶,D不符合题意;
故答案为:A
【分析】A.冰水混合物不属于胶体,不出现丁达尔效应;
B.云属于气溶胶,产生丁达尔效应;
C.雾属于气溶胶,产生丁达尔效应;
D.Fe(OH)3胶体属于液溶胶,产生丁达尔效应。
20.【答案】C
【解析】【解答】A. 氢氧化亚铁、氧气和水发生化合反应生成Fe(OH)3,A不符合题意;
B. 铁和氯化铁溶液发生化合反应生成FeCl2,B不符合题意;
C. CuS不能通化合反应直接制得,C符合题意;
D. 铁和氯气发生化合反应生成FeCl3,D不符合题意,
故答案为:C。
【分析】化合反应指的是多种单质或化合物生成一种化合物的反应。
21.【答案】(1)树状分类法
(2);;;;;CaCO3↓+H2O
(3)B;C
【解析】【解答】(1)由题干信息可知,该分类方法是按照层次,一层一层来分,则为树状分类法,故答案为:树状分类法;
(2)①酸是指在水溶液中电离出的阳离子全部是H+的化合物,故HNO3属于酸,碱是指在水溶液中电离出的阴离子全部是OH-的化合物,故Ca(OH)2属于碱,盐是指由金属阳离子或铵根离子和酸根离子构成的化合物,故CaCO3属于盐,酸性氧化物是指能与碱反应生成盐和水的氧化物,故CO2属于酸性氧化物,故答案为:HNO3;Ca(OH)2;CaCO3;CO2;
②a.发生中和反应即酸碱中和,故反应方程式为:,故答案为:;
b.有沉淀生成的反应即CO2通入澄清石灰水,反应方程式为:CaCO3↓+H2O,故答案为:CaCO3↓+H2O;
(3)图中阴影部分所示的反应为属于氧化还原反应但不属于四大基础反应类型的反应。
A:化合反应+氧化还原反应,A不合题意;
B:仅氧化还原反应,B正确;
C:仅氧化还原反应,C正确;
D:置换反应+氧化还原反应,D不合题意;
E:分解反应+非氧化还原反应,E不合题意;
综上,故答案为:BC。
【分析】(1)该分类方法是按照层次,一层一层来分,为树状分类法;
(2)①酸:电离出的阳离子全部是氢离子的化合物,碱:电离出的阴离子全部为氢氧根的化合物,盐:由金属阳离子(或铵根离子)和酸根阴离子组成的化合物,酸性氧化物:能和碱反应只生产盐和水的氧化物;
②酸与碱发生中和反应生成盐和水;二氧化碳通入澄清石灰水变浑浊;
(3)阴影区域的反应类型是属于氧化还原反应,但不属于四种反应类型的反应。
22.【答案】(1)③、④、⑥、⑦、⑨;②、⑩;电解质;非电解质;④、⑥、⑦、⑨;③
(2)分别取样做丁达尔实验,出现丁达尔效应的是氢氧化铁胶体
(3)2HNO3+Ca(OH)2=Ca(NO3)2+2H2O
【解析】【解答】(1)由一种元素组成的纯净物是单质,如②、⑩,由不同种元素组成的纯净物是化合物,如:③、④、⑥、⑦、⑨;根据化合物在水溶液和熔融态下是否导电将化合物分为:电解质和非电解质;在水溶液或熔融状态下能导电的化合物是电解质,如④、⑥、⑦、⑨,在水溶液和熔融状态下均不导电的化合物是非电解质,如③;
(2)氢氧化铁胶体具有丁达尔效应,而溶液不具备该性质,可以做丁达尔实验来区分,即分别取样做丁达尔实验,出现丁达尔效应的是氢氧化铁胶体;
(3)上述10种物质中硝酸是强酸,氢氧化钙是强碱,混合后,发生中和反应生成盐和水,化学方程式为2HNO3+Ca(OH)2=Ca(NO3)2+2H2O。
【分析】(1)根据化合物、单质、电解质、非电解质定义进行分类即可;
(2)胶体具有丁达尔效应,可以用来区分溶液与胶体;
(3)熟悉常见的强酸与强碱。
23.【答案】(1)1~100nm
(2)用一束光照射,观察到一条光亮的通路
(3)②
(4)FeCl3+3H2O Fe(OH)3(胶体)+3HCl;小于
【解析】【解答】(1)氢氧化铁胶体是胶体分散系中的一种,胶体粒子直径大小在1nm~100nm;
故答案是:1nm~100nm;(2)胶体区别于溶液的关键在于:溶液粒子直径小于1nm,胶体粒子直径大小在1nm~100nm,即溶液不产生丁达尔效应,而氢氧化铁胶体能产生丁达尔效应;用一束光线照射氢氧化铁胶体,能产生一条光亮的通路;
故答案是:用一束光线照射,能产生一条光亮的通路;(3)血液属于胶体,氯化铁溶液属于电解质溶液,加入电解质溶液(FeCl3溶液)可使胶粒聚沉,血液凝聚达到止血效果;
故答案为:②;(4)把饱和氯化铁溶液滴入沸水中继续加热煮沸,得到红褐色的液体为氢氧化铁胶体,制备胶体的化学方程式为:FeCl3+3H2O Fe(OH)3(胶体)+3HCl;由于胶体是大量粒子的集合体,因此如果将1molFeCl3全部制成胶体,胶粒数目小于NA;
故答案是:FeCl3+3H2O Fe(OH)3(胶体)+3HCl;小于。
【分析】(1)胶体离子的分散质离子直径在1~100nm 之间;
(2)可以用丁达尔原理来验证是否制备胶体成功;
(3)胶体在遇到电解质之后会发生聚沉现象;
(4)胶体是大量粒子的集合体,因此如果将1molFeCl3全部制成胶体,胶粒数目小于NA。
24.【答案】(1)②⑧
(2)①④
(3)⑤
(4)⑥
(5)⑦⑩
(6)⑨
【解析】【解答】根据物质的组成和概念判断物质的分类:②空气、⑧碘酒、 氨水由两种或两种以上不同物质组成的物质组成,为混合物;①H2O、④CaO由两种元素组成且其中一种是氧元素,属于氧化物;⑤H2SO4电离出的阳离子全部是氢离子,属于酸;⑥Ca(OH)2电离产生的阴离子全部为氢氧根离子的化合物;⑦CuSO4 5H2O ⑩NaHCO3、 纯碱在溶液中电离出的阳离子为金属离子,阴离子为酸根离子,属于盐;⑨C2H5OH 是含碳化合物,属于有机物;故属于混合物的是②⑧ ;属于氧化物的是①④;属于酸的是⑤;属于碱的是⑥;属于盐的是⑦⑩ ;属于有机物的是⑨。
【分析】混合物由两种或两种以上不同物质组成的物质;酸是指在电离时产生的阳离子全部是氢离子的化合物;碱是电离产生的阴离子全部为氢氧根离子的化合物;氧化物是由两种元素组成的且有一种是氧元素的化合物;盐是由金属离子和酸根离子组成的化合物;有机物是绝大多数含碳化合物;以此解答该题。
25.【答案】(1)FeCl3+3H2O=Fe(OH)3(胶体)+3HCl
(2)利用丁达尔效应,用一束光照射所得的液体,从侧面观察是否有—条光亮的“通路”出现
(3)Fe(OH)3胶体遇电解质聚沉;Fe(OH)3+3H+=Fe3++3H2O
【解析】【解答】(1)实验室制备氢氧化铁胶体的方法是:加热烧杯中的水至沸腾,向沸水滴加几滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色,即停止加热,反应的化学方程式为:FeCl3+3H2O Fe(OH)3(胶体)+3HCl,因此,本题正确答案是:FeCl3+3H2O Fe(OH)3(胶体)+3HCl;
(2)利用丁达尔效应,鉴别胶体和溶液,因此利用丁达尔效应可判断胶体是否制备成功,操作为:用一束光照射所得的液体,从侧面观察是否有—条光亮的“通路”出现;因此,本题正确答案是:利用丁达尔效应,用一束光照射所得的液体,从侧面观察是否有—条光亮的“通路”出现;
(3)电解质溶液能引起胶体的聚沉,先产生红褐色沉淀,氢氧化铁和盐酸发生反应生成氯化铁和水,随后沉淀溶解,反应的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O;因此,本题正确答案是:Fe(OH)3胶体遇电解质聚沉;Fe(OH)3+3H+=Fe3++3H2O。
【分析】(1)液体呈现红褐色,是由于Fe(OH)3的产生,据此写出反应的化学方程式;
(2)根据胶体的丁达尔效应进行分析;
(3)①加入电解质溶液,胶体会发生聚沉;
②加入盐酸后,溶液中的H+能与Fe(OH)3反应,使得沉淀溶解,据此写出离子方程式;
2023-2024学年高一上学期化学人教版(2019)必修第一册
一、单选题
1.胶体在自然界普遍存在,下列事实与胶体无关的是( )
A.将某些胶态金属氧化物分散于玻璃中制成有色玻璃
B.光线透过树叶间的缝隙射入密林中时,会看到一道道光柱
C.将纳米二氧化硅颗粒(直径)均匀分散到树脂中形成的分散系
D.植物油与水混合,充分振荡后可形成油水混合物
2.下列叙述正确的是( )
A.物质按照组成可以分为单质和化合物
B.氢氧化铁胶体带正电荷,土壤胶体带负电荷
C.无机化合物主要包括:酸、碱、盐和氧化物
D.按照树状分类法可将化学反应分为:氧化还原反应和离子反应
3.科学家发现了一种纯碳新材料“碳纳米泡沫”,每个碳纳米泡沫含有约4000个碳原子,直径约6~9nm,则这种“碳纳米泡沫”分散到空气中属于( )
A.溶液 B.悬浊液 C.乳浊液 D.胶体
4.分类法是学习和研究化学的一种常用的科学方法,下列正确的是( )
A.、、都是碱性氧化物
B.只含一种元素的物质一定是纯净物
C.与均含相同的元素氢,故也可以称为酸
D.液氯、均属于纯净物
5.下列关于分散系的说法错误的是( )
A.直径为1.3×10-9 m的“钴钛菁”分子在水中形成的分散系属于胶体
B.向沸水中滴加适量饱和FeCl3溶液,能形成带电的胶体
C.向氢氧化铁胶体中滴加稀硫酸,先产生沉淀,后沉淀溶解
D.利用丁达尔效应可区分溶液与胶体
6.下列属于碱性氧化物的是( )
A.CO2 B.Na2O2 C.SiO2 D.CaO
7.胶体与溶液的本质差异在于( )
A.是否稳定 B.是否有颜色
C.是否透明 D.粒子直径大小
8.在沸水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。下列说法正确的是( )
A.用激光笔照射该液体,会出现丁达尔效应
B.将液体静置片刻,会出现沉淀现象
C.所得分散系中分散质的粒子直径大于100 nm
D.用滤纸可实现该分散系中分散剂与分散质的分离
9.下列分散系不能产生“丁达尔效应”的是( )
A.墨水 B.硫酸钠溶液
C.氢氧化铁胶体 D.淀粉溶液
10.下列物质的分类正确的是( )
混合物 纯净物 酸性氧化物 碱 盐
A 空气 Fe(OH)3胶体 CO2 石灰水 KAl(SO4)2
B 豆浆 Cu SO3 烧碱 NaHCO3
C 稀硫酸 石墨 CO 氨气 CuSO4·5H2O
D 冰水混合物 生石灰 Cl2O7 纯碱 Cu2(OH)2CO3
A.A B.B
C.C D.D
11.能产生“丁达尔效应”的是( )
A.饱和食盐水 B.Fe(OH)3胶体 C.盐酸 D.硫酸铜溶液
12.下列物质中,不属于盐类的是( )
A.KOH B.MgCl2 C.KNO3 D.NaHCO3
13.X、Y、Z、W各代表一种物质,若X+Y=Z+W,则X和Y的反应不可能是( )
A.盐和盐的反应 B.酸与碱的反应
C.碱性氧化物和水的反应 D.酸性氧化物和碱的反应
14.以下有关垃圾分类说法正确的是( )
A.茶叶果皮属于厨余垃圾,可通过转化变为有机氮肥
B.废旧玻璃属于可回收垃圾,其主要成分为新型无机非金属材料
C.食品包装塑料袋属于其他垃圾,其主要成分聚氯乙烯为有机高分子化合物
D.医疗废弃物属于有害垃圾,经过处理、消毒后可加工成儿童玩具
15.一些装有化学物质的容器上常贴有危险化学品的标志。下列标志中,应贴在装有乙醇的容器上的是( )
A. B.
C. D.
16.下列有关叙述、对应的方程式、所属基本反应类型都正确的是( )
A.葡萄糖在人体内氧化氧化反应
B.拉瓦锡研究空气成分分解反应
C.生石灰作干燥剂化合反应
D.三氧化硫与氢氧化钠溶液反应复分解反应
17.按照物质的树状分类和交叉分类,硫酸应属于( )
①酸 ②能导电的纯净物 ③含氧酸 ④混合物 ⑤化合物 ⑥二元酸
A.①②③④ B.①③⑤⑥ C.①②③⑤⑥ D.②③⑤⑥
18.下列物质归类正确的是( )
A.硝酸盐:芒硝、硝石 B.碱:烧碱、纯碱
C.硫酸盐:胆矾、明矾 D.混合物:液氨、漂白粉
19.当光束通过下列物质时,不会出现丁达尔效应的是
A.冰水混合物 B.云 C.雾 D.Fe(OH)3胶体
20.下列物质不能通过化合反应直接制得的是( )
A.Fe(OH)3 B.FeCl2 C.CuS D.FeCl3
二、综合题
21.运用分类的方法研究物质及变化的规律是化学学习的有效途径。
(1)Ⅰ.化合物根据其组成和性质可进行如图所示分类
如图所示的分类方法属于 。
(2)现有下列四种物质:、、、
①按类别将上述四种物质填入下表
类别 酸 碱 盐 酸性氧化物
物质 a b c d
②根据上述四种物质的性质,写出符合下列要求的化学方程式。
a.发生中和反应:
b.有沉淀生成的反应:
(3)Ⅱ.我们可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示。
下列化学反应属于阴影区域的是____。
A.
B.
C.
D.
E.
22.运用树状分类法对下列9种物质进行分类,然后按要求回答问题:
(1)进行分类(将各物质序号填入相应方框中),并在相应空格处作答 。
(2)氢氧化铁胶体和氯化铁溶液从外观上很难进行区分,你认为可通过什么实验来区分? (简要说明实验方法和判断依据)。
(3)写出上述10种物质中的强酸强碱混合,发生中和反应的化学方程式: 。
23.某化学小组制备氢氧化铁胶体:洁净的小烧杯盛适量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol·L-1氯化铁溶液,至液体呈透明的红褐色。回答下列问题:
(1)氢氧化铁胶体中微粒直径的范围是 。
(2)检验胶体制备成功的操作是 。
(3)实验中手不慎被玻璃割破,可用氯化铁溶液应急止血,主要原因是 (填序号)。
①氯化铁溶液具有杀菌消毒的作用
②氯化铁溶液能使血液胶体凝固
③氯化铁溶液能产生氢氧化铁沉淀堵住伤口
④氯化铁溶液能使血液发生化学变化
(4)制备胶体的化学方程式为 。如果将1molFeCl3全部制成胶体,胶粒数目 NA(选填“大于”“等于”“小于”)。
24.现有下列10种物质:①H2O、②空气、③Mg、④CaO、⑤H2SO4、⑥Ca(OH)2、⑦CuSO4·5H2O、⑧碘酒、⑨C2H5OH和⑩NaHCO3。其中,
(1)属于混合物的是 (填序号,下同);
(2)属于氧化物的是 ;
(3)属于酸的是 ;
(4)属于碱的是 ;
(5)属于盐的是 ;
(6)属于有机物的是 。
25.将少量饱和FeCl3溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
(1)将丙继续加热煮沸至液体呈红褐色,反应的化学方程式为 。
(2)如何用最简单的方法判断丙中是否成功制备出胶体 。
(3)向经过检验后的丙中逐滴加入盐酸,会出现一系列变化:
①先出现和乙中相同的现象,原因是 ;
②随后发生变化得到和甲相同的溶液,此反应的离子方程式为 。
答案解析部分
1.【答案】D
【解析】【解答】A.有色玻璃是固溶胶,A不符合题意;
B.光线透过树叶间的缝隙射入密林中时,会看到一道道光柱是丁达尔效应,B不符合题意;
C.纳米二氧化硅颗粒(直径1 100nm)均匀分散到树脂中形成的分散系属于胶体,C不符合题意;
D.植物油与水混合,充分振荡后可形成油水混合物属于乳浊液,D符合题意;
故答案为:D。
【分析】分散质粒子直径位于1~100nm之间的分散系为胶体,胶体能产生丁达尔效应。
2.【答案】C
【解析】【解答】A、按照组成,可将物质分为纯净物和混合物,按照物质的组成元素,可将纯净物分为单质和化合物,故A错误;
B、胶体不带电,带电的为胶体微粒,故B错误;
C、无机物通常分为酸、碱、盐和氧化物等,故C正确;
D、氧化还原反应与离子反应是交叉关系,按树状分类应为氧化还原反应和非氧化还原反应,故D错误;
故答案为:C。
【分析】A、物质按照组成可以分为纯净物和混合物;
B、胶体不带电;
C、无机化合物包括酸、碱、盐等;
D、氧化还原反应与离子反应是交叉关系。
3.【答案】D
【解析】【解答】每个碳纳米泡沫含有约4000个碳原子,直径约6~9nm,则“碳纳米泡沫”分散到空气形成胶体分散系,故选D;
故答案为:D。
【分析】分散质粒子直径介于1~100nm之间的分散系为胶体。
4.【答案】D
【解析】【解答】A.碱性氧化物和酸反应只生成盐和水,和酸反应还生成氧气,属于过氧化物,A不符合题意;
B.同种元素可能形成不同的单质,如金刚石、石墨只含碳元素,二者在一起是混合物,B不符合题意;
C.酸是电离出的阳离子只有氢离子的化合物,属于酸式盐,C不符合题意;
D.液氯、均属于纯净物,D符合题意;
故答案为:D。
【分析】A、碱性氧化物和酸反应只生成盐和水;
B、纯净物的特点是只有一种分子;
C、酸的特点是电离的阳离子只有氢离子;
D、液氯和五水合硫酸铜都是纯净物。
5.【答案】B
【解析】【解答】A.胶体中分散质粒子直径为1~100nm,直径为1.3×10-9 m的“钴钛菁”分子在水中形成的分散系属于胶体,故A不符合题意;
B.胶体不带电,胶粒带电,向沸水中滴加适量饱和FeCl3溶液,能形胶粒带正电荷的胶体,故B符合题意;
C.氢氧化铁胶体中加入硫酸发生聚沉,氢氧化铁与硫酸反应生成硫酸铁溶液,所以先产生沉淀,后沉淀溶解,故C不符合题意;
D.胶体能产生丁达尔效应,溶液不能,所以利用丁达尔效应可区分溶液与胶体,故D不符合题意。
【分析】A.根据胶体粒子的直径进行判断;
B.胶体本身不带电;
C.氢氧化铁胶体中加入电解质发生聚沉,氢氧化铁沉淀与过量盐酸反应又会溶解;
D.胶体具有丁达尔效应,而溶液没有丁达尔效应。
6.【答案】D
【解析】【解答】A. CO2与NaOH反应产生Na2CO3和H2O,所以CO2属于酸性氧化物,A不符合题意;
B. Na2O2与HCl反应产生NaCl、H2O和O2,所以Na2O2不是碱性氧化物,B不符合题意;
C. SiO2与NaOH反应产生Na2SiO3和H2O,所以SiO2是酸性氧化物,C不符合题意;
D. CaO和HCl反应产生CaCl2和H2O,所以CaO是碱性氧化物,D符合题意;
故答案为:D。
【分析】和碱反应生成盐和水的氧化物是酸性氧化物,和酸反应生成盐和水的氧化物是碱性氧化物。
7.【答案】D
【解析】【解答】胶体与溶液的本质区别是微粒直径大小,微粒直径在1nm-100nm之间的分散系为胶体,小于1nm的分散系为溶液,
故答案为:D
【分析】溶液、胶体和浊液的划分就是根据分散质离子直径大小的原则。
8.【答案】A
【解析】【解答】A.制取得到液体是Fe(OH)3胶体,会产生丁达尔效应,因此用激光笔照射该液体,能够产生一条光亮的通路,A符合题意;
B.制取得到的Fe(OH)3胶体是一种介稳体系,将其静置,不会出现沉淀现象,B不符合题意;
C.制取得到的是Fe(OH)3胶体,分散质微粒直径在1-100 nm之间,C不符合题意;
D.胶体微粒及离子都可通过滤纸,因此不能用滤纸可实现该分散系中分散剂与分散质的分离,D不符合题意;
故答案为:A。
【分析】 在沸水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至溶液呈红褐色 ,得到Fe(OH)3胶体,胶体粒子是大量氢氧化铁的聚集体,根据胶体的性质解答该题。
9.【答案】B
【解析】【解答】A. 墨水属于胶体,能产生“丁达尔效应”,A不符合题意;
B. 硫酸钠溶液属于溶液,不能产生“丁达尔效应”,B符合题意;
C. 氢氧化铁胶体,产生“丁达尔效应”,C不符合题意;
D. 淀粉溶液属于胶体,产生“丁达尔效应”,D不符合题意;
故答案为:B。
【分析】有丁达尔效应的产生说明是胶体,找出不是胶体的即可
10.【答案】B
【解析】【解答】A.Fe(OH)3胶体中含有多种物质,属于混合物,A不符合题意;
B.各物质的分类正确,B符合题意;
C.CO不能与碱反应生成盐和水,故CO不是酸性氧化物,氨气无法电离产生OH-,故氨气也不是碱,C不符合题意;
D.冰水混合物的成分为水,只含有一种物质,为纯净物,纯碱为Na2CO3,属于盐,D不符合题意;
故答案为:B
【分析】此题是对物质分类的考查,结合混合物、纯净物、酸性氧化物、碱和盐的相关概念进行分析即可。
11.【答案】B
【解析】【解答】A.饱和食盐水属于溶液,不具有丁达尔效应,故A不符合题意;
B.Fe(OH)3胶体属于胶体,能发生丁达尔效应,故B符合题意;
C.盐酸属于溶液,不具有丁达尔效应,故C不符合题意;
D.硫酸铜溶液属于溶液,不具有丁达尔效应,故D不符合题意;
故答案为:B。
【分析】具有丁达尔效应的是胶体,结合选项找出即可
12.【答案】A
【解析】【解答】A.KOH电离出的阴离子全部是OH-,则KOH是碱,不属于盐,故A符合题意;
B.MgCl2是由金属镁离子和盐酸根组成的化合物,属于盐酸盐,故B不符合题意;
C.KNO3是由金属钾离子和硝酸根组成的化合物,属于硝酸盐,故C不符合题意;
D.NaHCO3是由钠离子和碳酸氢根离子构成的化合物,属于盐,故D不符合题意;
故答案为:A。
【分析】盐是由金属离子(或铵根离子)和酸根离子组成的化合物,据此进行分析判断。
13.【答案】C
【解析】【解答】A.盐和盐反应会产生两种新盐,反应物、生成物都是两种,A不符合题意;
B.酸与碱反应产生盐和水,反应物、生成物都是两种,B不符合题意;
C.碱性氧化物和水反应产生碱,反应物是两种,生成物只有一种,C符合题意;
D.酸性氧化物和碱反应产生盐和水,反应物、生成物都是两种,D不符合题意;
故答案为:C。
【分析】依据化学方程式反应物和产物的个数确定反应类型。
14.【答案】A
【解析】【解答】A. 茶叶果皮属于厨余垃圾,主要成分为有机物、可通过转化变为有机氮肥,A符合题意;
B. 废旧玻璃属于可回收垃圾,其主要成分为硅酸盐,不属于新型无机非金属材料,B不符合题意;
C. 聚氯乙烯不可用于食品包装,食品包装塑料袋主要成分为聚乙烯、属于有机高分子化合物,C不符合题意;
D. 医疗废弃物属于有害垃圾,应由指定专业机构回收处理、不可加工成儿童玩具,D不符合题意;
故答案为:A。
【分析】A.氮肥主要是含有氮元素
B.废旧玻璃是传统的无机非金属材料
C.聚氯乙烯有毒一般用于垃圾袋
D.儿童玩具的原材料必须是无毒的
15.【答案】B
【解析】【解答】乙醇是可燃性液体,易燃烧,因此应贴在装有乙醇的容器上的是易燃液体的标识。
故答案为:B。
【分析】依据物质的性质确定标识。
16.【答案】C
【解析】【解答】A.氧化反应不是基本反应类型,A不符合题意;
B.方程式没有配平,B不符合题意;
C.生石灰与水反应生成氢氧化钙,属于化合反应,C符合题意;
D.三氧化硫与氢氧化钠溶液的反应不属于复分解反应类型,D不符合题意;
故答案为:C。
【分析】基本反应类型包括:分解反应、化合反应、复分解反应和置换反应。
17.【答案】B
【解析】【解答】硫酸应属于⑤化合物,也属于①酸,还属于③含氧酸,也属于⑥二元酸,故答案:B符合题意;
故答案为:B。
【分析】硫酸电离的阳离子只有氢离子,溶液中有自由移动的阴阳离子,含有氧元素,电离出2个自由移动的阴离子。
18.【答案】C
【解析】【解答】A.硝石主要成分是KNO3,属于硝酸盐,而芒硝是Na2SO4 10H2O的俗名,属于硫酸盐,故A不符合题意;
B.烧碱是NaOH的俗名,属于碱,但纯碱是Na2CO3属于盐,故B不符合题意;
C.胆矾是CuSO4 5H2O,明矾是KAl(SO4)2 12H2O,都属于硫酸盐,故C符合题意;
D.漂白粉的主要成分是氯化钙和次氯酸钙,属于混合物,而液氨是液态的氨,为纯净物,故D不符合题意;
故答案为:C。
【分析】A.硝酸盐主要含有硝酸根,但是芒硝不含硝酸根不是硝酸盐
B.碱是在水溶液中电离出的阴离子全部是氢和氧根离子,但是纯碱不是碱
C.硫酸盐是含有硫酸根的盐,胆矾和明矾具有硫酸根
D.混合物是含有多种物质,但是液氨是单质只含有一种物质,漂白粉是混合物
19.【答案】A
【解析】【解答】A.冰水混合物不属于胶体,A符合题意;
B.云属于气溶胶,B不符合题意;
C.雾属于气溶胶,C不符合题意;
D.Fe(OH)3胶体属于液溶胶,D不符合题意;
故答案为:A
【分析】A.冰水混合物不属于胶体,不出现丁达尔效应;
B.云属于气溶胶,产生丁达尔效应;
C.雾属于气溶胶,产生丁达尔效应;
D.Fe(OH)3胶体属于液溶胶,产生丁达尔效应。
20.【答案】C
【解析】【解答】A. 氢氧化亚铁、氧气和水发生化合反应生成Fe(OH)3,A不符合题意;
B. 铁和氯化铁溶液发生化合反应生成FeCl2,B不符合题意;
C. CuS不能通化合反应直接制得,C符合题意;
D. 铁和氯气发生化合反应生成FeCl3,D不符合题意,
故答案为:C。
【分析】化合反应指的是多种单质或化合物生成一种化合物的反应。
21.【答案】(1)树状分类法
(2);;;;;CaCO3↓+H2O
(3)B;C
【解析】【解答】(1)由题干信息可知,该分类方法是按照层次,一层一层来分,则为树状分类法,故答案为:树状分类法;
(2)①酸是指在水溶液中电离出的阳离子全部是H+的化合物,故HNO3属于酸,碱是指在水溶液中电离出的阴离子全部是OH-的化合物,故Ca(OH)2属于碱,盐是指由金属阳离子或铵根离子和酸根离子构成的化合物,故CaCO3属于盐,酸性氧化物是指能与碱反应生成盐和水的氧化物,故CO2属于酸性氧化物,故答案为:HNO3;Ca(OH)2;CaCO3;CO2;
②a.发生中和反应即酸碱中和,故反应方程式为:,故答案为:;
b.有沉淀生成的反应即CO2通入澄清石灰水,反应方程式为:CaCO3↓+H2O,故答案为:CaCO3↓+H2O;
(3)图中阴影部分所示的反应为属于氧化还原反应但不属于四大基础反应类型的反应。
A:化合反应+氧化还原反应,A不合题意;
B:仅氧化还原反应,B正确;
C:仅氧化还原反应,C正确;
D:置换反应+氧化还原反应,D不合题意;
E:分解反应+非氧化还原反应,E不合题意;
综上,故答案为:BC。
【分析】(1)该分类方法是按照层次,一层一层来分,为树状分类法;
(2)①酸:电离出的阳离子全部是氢离子的化合物,碱:电离出的阴离子全部为氢氧根的化合物,盐:由金属阳离子(或铵根离子)和酸根阴离子组成的化合物,酸性氧化物:能和碱反应只生产盐和水的氧化物;
②酸与碱发生中和反应生成盐和水;二氧化碳通入澄清石灰水变浑浊;
(3)阴影区域的反应类型是属于氧化还原反应,但不属于四种反应类型的反应。
22.【答案】(1)③、④、⑥、⑦、⑨;②、⑩;电解质;非电解质;④、⑥、⑦、⑨;③
(2)分别取样做丁达尔实验,出现丁达尔效应的是氢氧化铁胶体
(3)2HNO3+Ca(OH)2=Ca(NO3)2+2H2O
【解析】【解答】(1)由一种元素组成的纯净物是单质,如②、⑩,由不同种元素组成的纯净物是化合物,如:③、④、⑥、⑦、⑨;根据化合物在水溶液和熔融态下是否导电将化合物分为:电解质和非电解质;在水溶液或熔融状态下能导电的化合物是电解质,如④、⑥、⑦、⑨,在水溶液和熔融状态下均不导电的化合物是非电解质,如③;
(2)氢氧化铁胶体具有丁达尔效应,而溶液不具备该性质,可以做丁达尔实验来区分,即分别取样做丁达尔实验,出现丁达尔效应的是氢氧化铁胶体;
(3)上述10种物质中硝酸是强酸,氢氧化钙是强碱,混合后,发生中和反应生成盐和水,化学方程式为2HNO3+Ca(OH)2=Ca(NO3)2+2H2O。
【分析】(1)根据化合物、单质、电解质、非电解质定义进行分类即可;
(2)胶体具有丁达尔效应,可以用来区分溶液与胶体;
(3)熟悉常见的强酸与强碱。
23.【答案】(1)1~100nm
(2)用一束光照射,观察到一条光亮的通路
(3)②
(4)FeCl3+3H2O Fe(OH)3(胶体)+3HCl;小于
【解析】【解答】(1)氢氧化铁胶体是胶体分散系中的一种,胶体粒子直径大小在1nm~100nm;
故答案是:1nm~100nm;(2)胶体区别于溶液的关键在于:溶液粒子直径小于1nm,胶体粒子直径大小在1nm~100nm,即溶液不产生丁达尔效应,而氢氧化铁胶体能产生丁达尔效应;用一束光线照射氢氧化铁胶体,能产生一条光亮的通路;
故答案是:用一束光线照射,能产生一条光亮的通路;(3)血液属于胶体,氯化铁溶液属于电解质溶液,加入电解质溶液(FeCl3溶液)可使胶粒聚沉,血液凝聚达到止血效果;
故答案为:②;(4)把饱和氯化铁溶液滴入沸水中继续加热煮沸,得到红褐色的液体为氢氧化铁胶体,制备胶体的化学方程式为:FeCl3+3H2O Fe(OH)3(胶体)+3HCl;由于胶体是大量粒子的集合体,因此如果将1molFeCl3全部制成胶体,胶粒数目小于NA;
故答案是:FeCl3+3H2O Fe(OH)3(胶体)+3HCl;小于。
【分析】(1)胶体离子的分散质离子直径在1~100nm 之间;
(2)可以用丁达尔原理来验证是否制备胶体成功;
(3)胶体在遇到电解质之后会发生聚沉现象;
(4)胶体是大量粒子的集合体,因此如果将1molFeCl3全部制成胶体,胶粒数目小于NA。
24.【答案】(1)②⑧
(2)①④
(3)⑤
(4)⑥
(5)⑦⑩
(6)⑨
【解析】【解答】根据物质的组成和概念判断物质的分类:②空气、⑧碘酒、 氨水由两种或两种以上不同物质组成的物质组成,为混合物;①H2O、④CaO由两种元素组成且其中一种是氧元素,属于氧化物;⑤H2SO4电离出的阳离子全部是氢离子,属于酸;⑥Ca(OH)2电离产生的阴离子全部为氢氧根离子的化合物;⑦CuSO4 5H2O ⑩NaHCO3、 纯碱在溶液中电离出的阳离子为金属离子,阴离子为酸根离子,属于盐;⑨C2H5OH 是含碳化合物,属于有机物;故属于混合物的是②⑧ ;属于氧化物的是①④;属于酸的是⑤;属于碱的是⑥;属于盐的是⑦⑩ ;属于有机物的是⑨。
【分析】混合物由两种或两种以上不同物质组成的物质;酸是指在电离时产生的阳离子全部是氢离子的化合物;碱是电离产生的阴离子全部为氢氧根离子的化合物;氧化物是由两种元素组成的且有一种是氧元素的化合物;盐是由金属离子和酸根离子组成的化合物;有机物是绝大多数含碳化合物;以此解答该题。
25.【答案】(1)FeCl3+3H2O=Fe(OH)3(胶体)+3HCl
(2)利用丁达尔效应,用一束光照射所得的液体,从侧面观察是否有—条光亮的“通路”出现
(3)Fe(OH)3胶体遇电解质聚沉;Fe(OH)3+3H+=Fe3++3H2O
【解析】【解答】(1)实验室制备氢氧化铁胶体的方法是:加热烧杯中的水至沸腾,向沸水滴加几滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色,即停止加热,反应的化学方程式为:FeCl3+3H2O Fe(OH)3(胶体)+3HCl,因此,本题正确答案是:FeCl3+3H2O Fe(OH)3(胶体)+3HCl;
(2)利用丁达尔效应,鉴别胶体和溶液,因此利用丁达尔效应可判断胶体是否制备成功,操作为:用一束光照射所得的液体,从侧面观察是否有—条光亮的“通路”出现;因此,本题正确答案是:利用丁达尔效应,用一束光照射所得的液体,从侧面观察是否有—条光亮的“通路”出现;
(3)电解质溶液能引起胶体的聚沉,先产生红褐色沉淀,氢氧化铁和盐酸发生反应生成氯化铁和水,随后沉淀溶解,反应的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O;因此,本题正确答案是:Fe(OH)3胶体遇电解质聚沉;Fe(OH)3+3H+=Fe3++3H2O。
【分析】(1)液体呈现红褐色,是由于Fe(OH)3的产生,据此写出反应的化学方程式;
(2)根据胶体的丁达尔效应进行分析;
(3)①加入电解质溶液,胶体会发生聚沉;
②加入盐酸后,溶液中的H+能与Fe(OH)3反应,使得沉淀溶解,据此写出离子方程式;
