【高效课堂】人教A版(2019)高中化学必修2--7.2.2烃(教学课件)
文档属性
| 名称 | 【高效课堂】人教A版(2019)高中化学必修2--7.2.2烃(教学课件) |

|
|
| 格式 | pptx | ||
| 文件大小 | 58.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-19 00:00:00 | ||
图片预览






文档简介
(共36张PPT)
第七章
第二节 乙烯与有机高分子材料
第二课时 烃
新人教版 化学 必修第二册
目录
01
02
烃的燃烧规律
烃
03
烃中原子共线、共面
01
一、烃
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
仅含 和 两种元素的有机化合物称为碳氢化合物,也称为烃。
碳
氢
烷烃:只含 和 两种元素,分子中的碳原子之间都以 结合,碳原子的剩余价键均与 结合,使碳原子的化合价都达到“ ”,这样的一类有机化合物称为 ,也称为烷烃。
碳
氢
单键
氢原子
饱和
饱和烃
烯烃:烃分子中含有碳碳双键的烃称为烯烃。
炔烃:烃分子中含有碳碳三键的烃称为炔烃。
芳香烃:烃分子中含有苯环的烃称为芳香烃。
1.烃的概念
2.烷烃、烯烃、炔烃、芳香烃
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
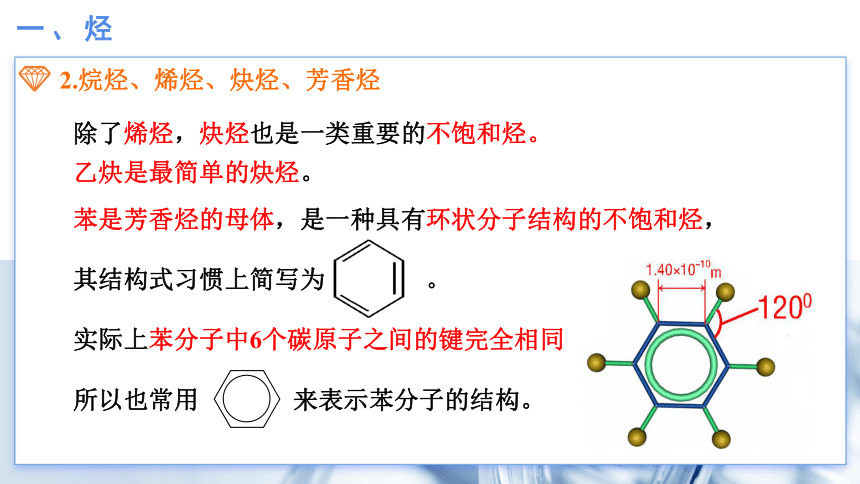
除了烯烃,炔烃也是一类重要的不饱和烃。
乙炔是最简单的炔烃。
苯是芳香烃的母体,是一种具有环状分子结构的不饱和烃,
其结构式习惯上简写为 。
实际上苯分子中6个碳原子之间的键完全相同
所以也常用 来表示苯分子的结构。
2.烷烃、烯烃、炔烃、芳香烃
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
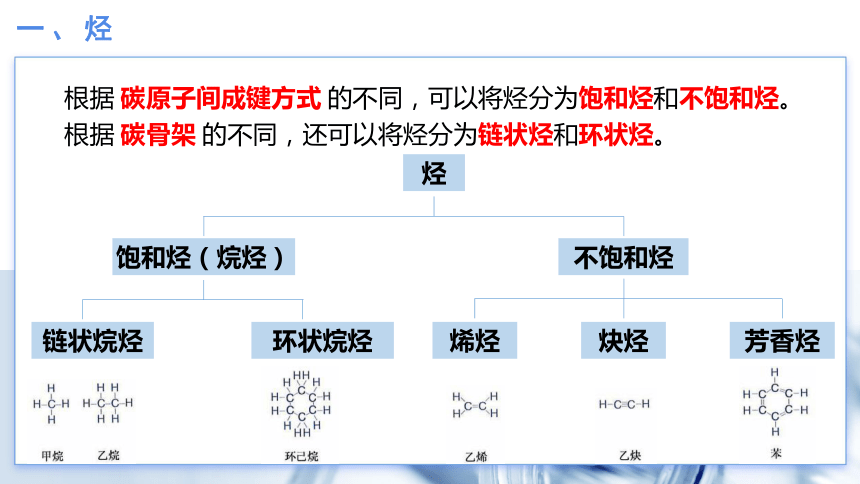
根据 碳骨架 的不同,还可以将烃分为链状烃和环状烃。
烃
饱和烃(烷烃)
不饱和烃
链状烷烃
环状烷烃
烯烃
炔烃
芳香烃
根据 碳原子间成键方式 的不同,可以将烃分为饱和烃和不饱和烃。
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
烃的分子结构
【目的】
以甲烷、乙烯和乙炔为例,借助模型认识烃的分子结构。
【活动】
(1) 根据碳原子的成键规律和甲烷、乙烯、乙炔的结构式,写出三者的电子式,并讨论其分子中有哪些类型的化学键。
(2) 结合以上分析,使用分子结构模型(或橡皮泥、黏土、泡沫塑料、牙签等代用品)搭建甲烷、乙烯和乙炔分子的球棍模型。展示并描述三者的分子结构特点。
活动探究
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
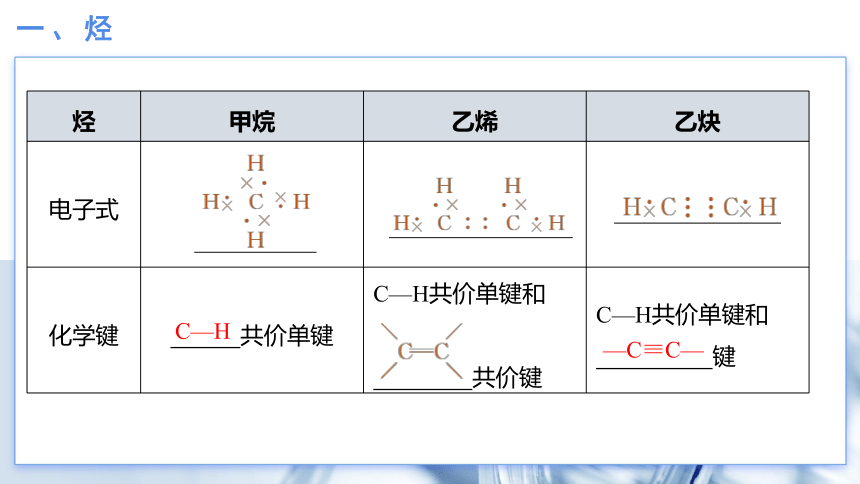
烃 甲烷 乙烯 乙炔
电子式
化学键 共价单键 C—H共价单键和 共价键 C—H共价单键和
键
C—H
—C≡C—
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
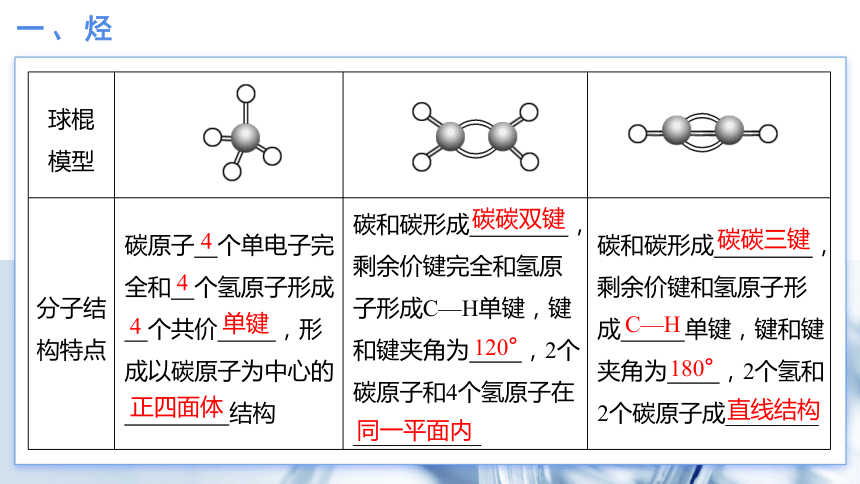
球棍 模型
分子结 构特点 碳原子 个单电子完全和 个氢原子形成 个共价 ,形成以碳原子为中心的 结构 碳和碳形成 ,剩余价键完全和氢原子形成C—H单键,键和键夹角为 ,2个碳原子和4个氢原子在 ___________ 碳和碳形成 ,剩余价键和氢原子形成 单键,键和键夹角为 ,2个氢和2个碳原子成________
4
4
4
单键
正四面体
碳碳双键
120°
同一平面内
碳碳三键
C—H
180°
直线结构
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
(1) 比较CH4、CH2==CH2的化学性质,并分析其化学性质与二者结构的关系?
物质 甲烷 乙烯
与Br2 反应 Br2试剂 ________ ___________________
反应条件 _____
反应类型 _____ _____
氧化 反应 和O2燃烧 燃烧,火焰 呈 色 燃烧,火焰_______________
酸性KMnO4溶液 _______ ____________________
Br2蒸气
溴水或溴的CCl4溶液
光照
取代
加成
淡蓝
明亮、伴有黑烟
不反应
酸性KMnO4溶液褪色
思考与讨论
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
性质和结构关系 CH4分子中的碳原子为 结构,所成的键为 ,性质 ,主要发生 反应 CH2==CH2分子中的碳原子为___
结构,所成的键为 ,其中一个键容易断裂,性质活泼,主要发生 、 反应
饱和
单键
稳定
取代
不
饱和
碳碳双键
加成反应
氧化
(1) 比较CH4、CH2==CH2的化学性质,并分析其化学性质与二者结构的关系?
(2) 乙炔是甲烷或乙烯的同系物吗?为什么?
不是,同系物要求结构组成相似,甲烷、乙烯、乙炔的结构不同。
思考与讨论
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
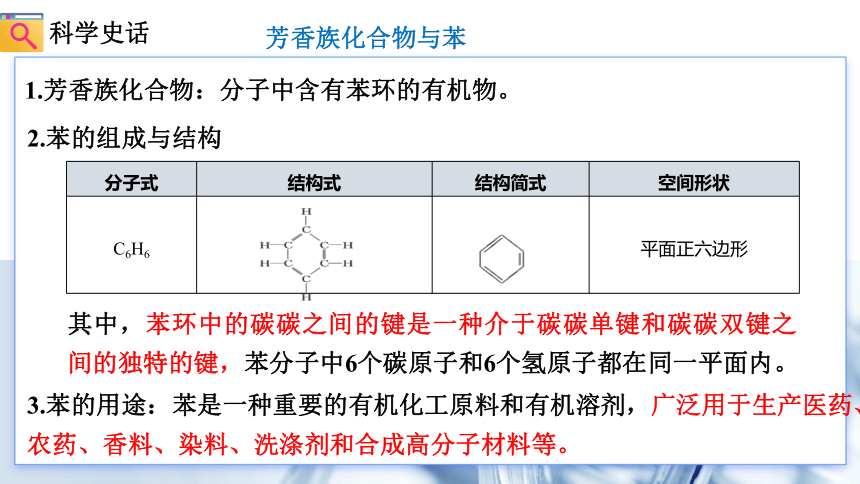
1.芳香族化合物:分子中含有苯环的有机物。
分子式 结构式 结构简式 空间形状
C6H6 平面正六边形
3.苯的用途:苯是一种重要的有机化工原料和有机溶剂,广泛用于生产医药、农药、香料、染料、洗涤剂和合成高分子材料等。
芳香族化合物与苯
科学史话
其中,苯环中的碳碳之间的键是一种介于碳碳单键和碳碳双键之间的独特的键,苯分子中6个碳原子和6个氢原子都在同一平面内。
2.苯的组成与结构
01
二、烃的燃烧规律
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
烃燃烧时,火焰的明亮程度以及是否有黑烟与含碳量有关。
1.烃燃烧的现象
烃中碳元素的质量分数越大
燃烧时火焰越明亮
黑烟越浓
https://i耗氧量多少取决于mg2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
x+y/4
x
y/4
2.等物质的量的烃(CxHy)完全燃烧规律
耗氧量多少取决于:
生成CO2的量的多少取决于:
生成水的量的多少取决于:
等物质的量的烃
(CxHy)完全燃烧
②C ~ O2 ~ CO2,4H ~ O2 ~ 2H2O
12 g 1 mol 4 g 1 mol
二、烃的燃烧规律
3.等质量的烃(CxHy)完全燃烧规律
等质量的烃(CxHy)完全燃烧
越大,耗氧量越多
越小,耗氧量越小
C ~ O2 ~ CO2, 4H ~ O2 ~ 2H2O
12 g 1 mol 4 g 1 mol
下列有机混合物不论以何种比例混合,只要总质量一定时,充分燃烧后产生的H2O的量为定值的是( )
A.CH4、C2H6 B.C2H6、C3H6 C.C3H6O3、C6H12O6 D.C3H4、C3H6
下列有机混合物不论以何种比例混合,只要总质量一定时,充分燃烧后产生的H2O的量为定值的是( )
A.CH4、C2H6 B.C2H6、C3H6 C.C3H6O3、C6H12O6 D.C3H4、C3H6
【答案】C【答案】C
二、烃的燃烧规律
B
等质量的下列烃完全燃烧,消耗O2最多的是( )
A.C3H6
B.C2H6
C.C6H6
D.C3H8
越大,耗氧量越多
https://img2.baidm/it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
4.气态烃燃烧时气体体积的变化
若温度大于100 ℃,即H2O为气态
ΔV=V前-V后
则ΔV=
当y<4时,ΔV>0,即反应后气体体积减小
当y=4时,ΔV=0,即反应后气体体积不变
当y>4时,ΔV>0,即反应后气体体积增大
https://img2.baidm/it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
4.气态烃燃烧时气体体积的变化
ΔV=V前-V后
则ΔV=
若温度小于100 ℃,即H2O为液态
反应后气体体积始终减小
且减少量与氢原子数有关
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
120℃时1体积某气态烃和4体积O2混合,完全燃烧后恢复到原来的温度和压强时,体积不变,该分子式中所含的碳原子数不可能是( )
A.1
B.2
C.3
D.7
D
y=4
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
标准状况下,某两种气态烃组成的混合气体4.48 L完全燃烧后,得到8.96 L二氧化碳(体积已折算成标准状况)和7.2 g水。则这两种气态烃可能是
A.CH4和C3H8
B.CH4和C3H4
C.C2H4和C3H4
D.C2H4和C2H6
0.2 mol
0.4 mol
0.4 mol
平均 C2H4
B
01
三、烃中原子共线、共面
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
三、烃中原子共线、共面
—C≡C—
1.典型空间结构
甲烷型
乙烯型
乙炔型
苯型
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
三、烃中原子共线、共面
1.典型空间结构
甲烷型
甲烷中最多____个原子共平面
乙烷中最多____个原子共平面
丁烷中所有碳原子______可以在同一平面
正四面体→凡是碳原子与4个原子形成4个共价键时,其空间结构都是四面体形,5个原子中最多有3个原子共平面。
可以
3
4
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
三、烃中原子共线、共面
1.典型空间结构
乙烯型
平面结构→
与碳碳双键直接相连的4个原子与2个碳原子共平面
乙烯中______个原子共平面
丙烯中最多_____个原子共平面
丁二烯中最多_____个原子共平面
10
6
7
平面结构→位于苯环上的12个原子共平面,位于对角线位置上的4个原子共直线。
三、烃中原子共线、共面
—C≡C—
1.典型空间结构
乙炔型
直线结构→
与碳碳三键直接相连的2个原子与2个碳原子共直线。
乙炔中____个原子共线?
丙炔中最多____个原子共线?
丙炔中最多____个原子共面?
4
4
5
平面结构→位于苯环上的12个原子共平面,位于对角线位置上的4个原子共直线。
三、烃中原子共线、共面
1.典型空间结构
平面结构→
位于苯环上的12个原子共平面,
位于对角线位置上的4个原子共直线。
苯型
苯中____个原子共平面,最多____个原子共线
甲苯中最多____个原子共平面
苯乙烯中最多_____个原子共平面
12
13
16
4
课堂检测
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
D.P—P键的键能为 kJ/mol
课堂检测
A
1.下列烃①C4H10、②C4H8、③C7H8、④C6H12分别完全燃烧,耗氧量分析不正确的是( )
A.等物质的量时耗氧量最少的是①
B.等物质的量时③和④的耗氧量相等
C.等质量时耗氧量最大的是①
D.等质量时②和④的耗氧量相等
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
2.两种气态烃以任意比例混合,在105 ℃时1 L该混合烃与10 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍为11 L。下列各组混合烃中符合此条件的是( )
A.C2H4、C2H6 B.CH4、C3H8
C.C2H6、C3H6 D.CH4、C3H4
D.P—P键的键能为 kJ/mol
课堂检测
D
2.两种气态烃以任意比例混合,在105 ℃时1 L该混合烃与10 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍为11 L。下列各组混合烃中符合此条件的是( )
A.C2H4、C2H6 B.CH4、C3H8
C.C2H6、C3H6 D.CH4、C3H4
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
D.P—P键的键能为 kJ/mol
课堂检测
C
3.两种气态烃的混合物6.72 L(标准状况),完全燃烧生成0.48 mol CO2和10.8 g H2O,则该混合烃中( )
A.一定不存在乙烯 B.一定不存在甲烷
C.一定存在甲烷 D.一定存在乙烯
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
D.P—P键的键能为 kJ/mol
课堂检测
C
4.已知乙烯分子为平面结构,C2H2为直线结构。则有机物M(CH≡C—CH===CH—CH3)分子中,共直线和共平面的原子数最多分别为( )
A.6、11 B.5、10
C.4、9 D.4、11
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
D.P—P键的键能为 kJ/mol
课堂检测
B
5.下列关于乙烯结构与性质的叙述中,错误的是( )
A.乙烯分子中6个原子在同一平面内
B.乙烯与酸性KMnO4溶液发生加成反应使其褪色
C.乙烯与溴的四氯化碳溶液发生加成反应
D.乙烯分子的一氯代物只有一种结构
课堂总结
课堂总结
01
02
03
烃
烃的燃烧规律
烃分子中原子共线、共面
THANKS
THANKS
感谢观看
第七章
第二节 乙烯与有机高分子材料
第二课时 烃
新人教版 化学 必修第二册
目录
01
02
烃的燃烧规律
烃
03
烃中原子共线、共面
01
一、烃
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
仅含 和 两种元素的有机化合物称为碳氢化合物,也称为烃。
碳
氢
烷烃:只含 和 两种元素,分子中的碳原子之间都以 结合,碳原子的剩余价键均与 结合,使碳原子的化合价都达到“ ”,这样的一类有机化合物称为 ,也称为烷烃。
碳
氢
单键
氢原子
饱和
饱和烃
烯烃:烃分子中含有碳碳双键的烃称为烯烃。
炔烃:烃分子中含有碳碳三键的烃称为炔烃。
芳香烃:烃分子中含有苯环的烃称为芳香烃。
1.烃的概念
2.烷烃、烯烃、炔烃、芳香烃
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
除了烯烃,炔烃也是一类重要的不饱和烃。
乙炔是最简单的炔烃。
苯是芳香烃的母体,是一种具有环状分子结构的不饱和烃,
其结构式习惯上简写为 。
实际上苯分子中6个碳原子之间的键完全相同
所以也常用 来表示苯分子的结构。
2.烷烃、烯烃、炔烃、芳香烃
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
根据 碳骨架 的不同,还可以将烃分为链状烃和环状烃。
烃
饱和烃(烷烃)
不饱和烃
链状烷烃
环状烷烃
烯烃
炔烃
芳香烃
根据 碳原子间成键方式 的不同,可以将烃分为饱和烃和不饱和烃。
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
烃的分子结构
【目的】
以甲烷、乙烯和乙炔为例,借助模型认识烃的分子结构。
【活动】
(1) 根据碳原子的成键规律和甲烷、乙烯、乙炔的结构式,写出三者的电子式,并讨论其分子中有哪些类型的化学键。
(2) 结合以上分析,使用分子结构模型(或橡皮泥、黏土、泡沫塑料、牙签等代用品)搭建甲烷、乙烯和乙炔分子的球棍模型。展示并描述三者的分子结构特点。
活动探究
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
烃 甲烷 乙烯 乙炔
电子式
化学键 共价单键 C—H共价单键和 共价键 C—H共价单键和
键
C—H
—C≡C—
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
一、烃
球棍 模型
分子结 构特点 碳原子 个单电子完全和 个氢原子形成 个共价 ,形成以碳原子为中心的 结构 碳和碳形成 ,剩余价键完全和氢原子形成C—H单键,键和键夹角为 ,2个碳原子和4个氢原子在 ___________ 碳和碳形成 ,剩余价键和氢原子形成 单键,键和键夹角为 ,2个氢和2个碳原子成________
4
4
4
单键
正四面体
碳碳双键
120°
同一平面内
碳碳三键
C—H
180°
直线结构
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
(1) 比较CH4、CH2==CH2的化学性质,并分析其化学性质与二者结构的关系?
物质 甲烷 乙烯
与Br2 反应 Br2试剂 ________ ___________________
反应条件 _____
反应类型 _____ _____
氧化 反应 和O2燃烧 燃烧,火焰 呈 色 燃烧,火焰_______________
酸性KMnO4溶液 _______ ____________________
Br2蒸气
溴水或溴的CCl4溶液
光照
取代
加成
淡蓝
明亮、伴有黑烟
不反应
酸性KMnO4溶液褪色
思考与讨论
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
性质和结构关系 CH4分子中的碳原子为 结构,所成的键为 ,性质 ,主要发生 反应 CH2==CH2分子中的碳原子为___
结构,所成的键为 ,其中一个键容易断裂,性质活泼,主要发生 、 反应
饱和
单键
稳定
取代
不
饱和
碳碳双键
加成反应
氧化
(1) 比较CH4、CH2==CH2的化学性质,并分析其化学性质与二者结构的关系?
(2) 乙炔是甲烷或乙烯的同系物吗?为什么?
不是,同系物要求结构组成相似,甲烷、乙烯、乙炔的结构不同。
思考与讨论
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
1.芳香族化合物:分子中含有苯环的有机物。
分子式 结构式 结构简式 空间形状
C6H6 平面正六边形
3.苯的用途:苯是一种重要的有机化工原料和有机溶剂,广泛用于生产医药、农药、香料、染料、洗涤剂和合成高分子材料等。
芳香族化合物与苯
科学史话
其中,苯环中的碳碳之间的键是一种介于碳碳单键和碳碳双键之间的独特的键,苯分子中6个碳原子和6个氢原子都在同一平面内。
2.苯的组成与结构
01
二、烃的燃烧规律
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
烃燃烧时,火焰的明亮程度以及是否有黑烟与含碳量有关。
1.烃燃烧的现象
烃中碳元素的质量分数越大
燃烧时火焰越明亮
黑烟越浓
https://i耗氧量多少取决于mg2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
x+y/4
x
y/4
2.等物质的量的烃(CxHy)完全燃烧规律
耗氧量多少取决于:
生成CO2的量的多少取决于:
生成水的量的多少取决于:
等物质的量的烃
(CxHy)完全燃烧
②C ~ O2 ~ CO2,4H ~ O2 ~ 2H2O
12 g 1 mol 4 g 1 mol
二、烃的燃烧规律
3.等质量的烃(CxHy)完全燃烧规律
等质量的烃(CxHy)完全燃烧
越大,耗氧量越多
越小,耗氧量越小
C ~ O2 ~ CO2, 4H ~ O2 ~ 2H2O
12 g 1 mol 4 g 1 mol
下列有机混合物不论以何种比例混合,只要总质量一定时,充分燃烧后产生的H2O的量为定值的是( )
A.CH4、C2H6 B.C2H6、C3H6 C.C3H6O3、C6H12O6 D.C3H4、C3H6
下列有机混合物不论以何种比例混合,只要总质量一定时,充分燃烧后产生的H2O的量为定值的是( )
A.CH4、C2H6 B.C2H6、C3H6 C.C3H6O3、C6H12O6 D.C3H4、C3H6
【答案】C【答案】C
二、烃的燃烧规律
B
等质量的下列烃完全燃烧,消耗O2最多的是( )
A.C3H6
B.C2H6
C.C6H6
D.C3H8
越大,耗氧量越多
https://img2.baidm/it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
4.气态烃燃烧时气体体积的变化
若温度大于100 ℃,即H2O为气态
ΔV=V前-V后
则ΔV=
当y<4时,ΔV>0,即反应后气体体积减小
当y=4时,ΔV=0,即反应后气体体积不变
当y>4时,ΔV>0,即反应后气体体积增大
https://img2.baidm/it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
4.气态烃燃烧时气体体积的变化
ΔV=V前-V后
则ΔV=
若温度小于100 ℃,即H2O为液态
反应后气体体积始终减小
且减少量与氢原子数有关
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
120℃时1体积某气态烃和4体积O2混合,完全燃烧后恢复到原来的温度和压强时,体积不变,该分子式中所含的碳原子数不可能是( )
A.1
B.2
C.3
D.7
D
y=4
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
二、烃的燃烧规律
标准状况下,某两种气态烃组成的混合气体4.48 L完全燃烧后,得到8.96 L二氧化碳(体积已折算成标准状况)和7.2 g水。则这两种气态烃可能是
A.CH4和C3H8
B.CH4和C3H4
C.C2H4和C3H4
D.C2H4和C2H6
0.2 mol
0.4 mol
0.4 mol
平均 C2H4
B
01
三、烃中原子共线、共面
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
三、烃中原子共线、共面
—C≡C—
1.典型空间结构
甲烷型
乙烯型
乙炔型
苯型
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
三、烃中原子共线、共面
1.典型空间结构
甲烷型
甲烷中最多____个原子共平面
乙烷中最多____个原子共平面
丁烷中所有碳原子______可以在同一平面
正四面体→凡是碳原子与4个原子形成4个共价键时,其空间结构都是四面体形,5个原子中最多有3个原子共平面。
可以
3
4
https://img2./it/u=4137884964,1688312958&fm=253&fmt=auto&app=138&f=JPEG w=500&h=507
三、烃中原子共线、共面
1.典型空间结构
乙烯型
平面结构→
与碳碳双键直接相连的4个原子与2个碳原子共平面
乙烯中______个原子共平面
丙烯中最多_____个原子共平面
丁二烯中最多_____个原子共平面
10
6
7
平面结构→位于苯环上的12个原子共平面,位于对角线位置上的4个原子共直线。
三、烃中原子共线、共面
—C≡C—
1.典型空间结构
乙炔型
直线结构→
与碳碳三键直接相连的2个原子与2个碳原子共直线。
乙炔中____个原子共线?
丙炔中最多____个原子共线?
丙炔中最多____个原子共面?
4
4
5
平面结构→位于苯环上的12个原子共平面,位于对角线位置上的4个原子共直线。
三、烃中原子共线、共面
1.典型空间结构
平面结构→
位于苯环上的12个原子共平面,
位于对角线位置上的4个原子共直线。
苯型
苯中____个原子共平面,最多____个原子共线
甲苯中最多____个原子共平面
苯乙烯中最多_____个原子共平面
12
13
16
4
课堂检测
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
D.P—P键的键能为 kJ/mol
课堂检测
A
1.下列烃①C4H10、②C4H8、③C7H8、④C6H12分别完全燃烧,耗氧量分析不正确的是( )
A.等物质的量时耗氧量最少的是①
B.等物质的量时③和④的耗氧量相等
C.等质量时耗氧量最大的是①
D.等质量时②和④的耗氧量相等
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
2.两种气态烃以任意比例混合,在105 ℃时1 L该混合烃与10 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍为11 L。下列各组混合烃中符合此条件的是( )
A.C2H4、C2H6 B.CH4、C3H8
C.C2H6、C3H6 D.CH4、C3H4
D.P—P键的键能为 kJ/mol
课堂检测
D
2.两种气态烃以任意比例混合,在105 ℃时1 L该混合烃与10 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍为11 L。下列各组混合烃中符合此条件的是( )
A.C2H4、C2H6 B.CH4、C3H8
C.C2H6、C3H6 D.CH4、C3H4
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
D.P—P键的键能为 kJ/mol
课堂检测
C
3.两种气态烃的混合物6.72 L(标准状况),完全燃烧生成0.48 mol CO2和10.8 g H2O,则该混合烃中( )
A.一定不存在乙烯 B.一定不存在甲烷
C.一定存在甲烷 D.一定存在乙烯
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
D.P—P键的键能为 kJ/mol
课堂检测
C
4.已知乙烯分子为平面结构,C2H2为直线结构。则有机物M(CH≡C—CH===CH—CH3)分子中,共直线和共平面的原子数最多分别为( )
A.6、11 B.5、10
C.4、9 D.4、11
内容内容内容
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ/mol,PCl3中P—Cl键的键能为1.2c kJ/mol。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为 kJ/mol
D.P—P键的键能为 kJ/mol
课堂检测
B
5.下列关于乙烯结构与性质的叙述中,错误的是( )
A.乙烯分子中6个原子在同一平面内
B.乙烯与酸性KMnO4溶液发生加成反应使其褪色
C.乙烯与溴的四氯化碳溶液发生加成反应
D.乙烯分子的一氯代物只有一种结构
课堂总结
课堂总结
01
02
03
烃
烃的燃烧规律
烃分子中原子共线、共面
THANKS
THANKS
感谢观看
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
