2025鲁教版高中化学必修第一册同步练习题--专题强化练2 物质的量浓度的有关计算(含解析)
文档属性
| 名称 | 2025鲁教版高中化学必修第一册同步练习题--专题强化练2 物质的量浓度的有关计算(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 329.9KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-19 00:00:00 | ||
图片预览

文档简介
中小学教育资源及组卷应用平台
2025鲁教版高中化学必修第一册
第1章 认识化学科学
专题强化练2 物质的量浓度的有关计算
1.(2024河南南阳期末联考)某溶液中含有Na+、Mg2+、S、Cl-,其中c(Na+)∶c(Mg2+)∶c(Cl-)=3∶5∶5,若Na+的物质的量浓度为3 mol·L-1,则S的物质的量浓度为( )
A.2 mol·L-1 B.3 mol·L-1
C.4 mol·L-1 D.8 mol·L-1
2.(2024山东省实验中学月考)下列叙述正确的是 ( )
A.将8.4 g NaHCO3晶体溶于100 mL水中,制得1 mol·L-1 NaHCO3溶液
B.将25 g无水CuSO4溶于水制成100 mL溶液,其浓度为1 mol·L-1
C.将w g a%的NaCl饱和溶液蒸发掉0.5w g水,得到2a%的NaCl溶液
D.将1体积c1 mol·L-1的硫酸用水稀释至5体积,所得溶液的浓度为0.2c1 mol·L-1
3.(2024河北石家庄阶段练习)V mL Al2(SO4)3溶液中含有Al3+ a g,取V mL溶液稀释至4V mL,则稀释后溶液中S的物质的量浓度是( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
4.(2024山东莱西一中月考)某同学购买了一瓶84消毒液,部分包装说明如下:
净含量:500 mL
密度:1.19 g/cm3
有效成分:NaClO
使用方法:稀释至100倍(体积比)后使用
注意事项:密封保存,易吸收空气中的CO2
变质
溶质质量分数:25%
根据以上信息和相关知识判断,下列说法不正确的是( )
A.该84消毒液的物质的量浓度约为4.0 mol·L-1
B.欲用NaClO固体配制480 mL该浓度消毒液,需要称量的NaClO固体质量为145.75 g
C.取100 mL该84消毒液稀释至100倍,稀释后的溶液中c(Na+)约为0.04 mol·L-1
D.要使一瓶该84消毒液完全变质生成NaHCO3,需要吸收标准状况下44.8 L CO2
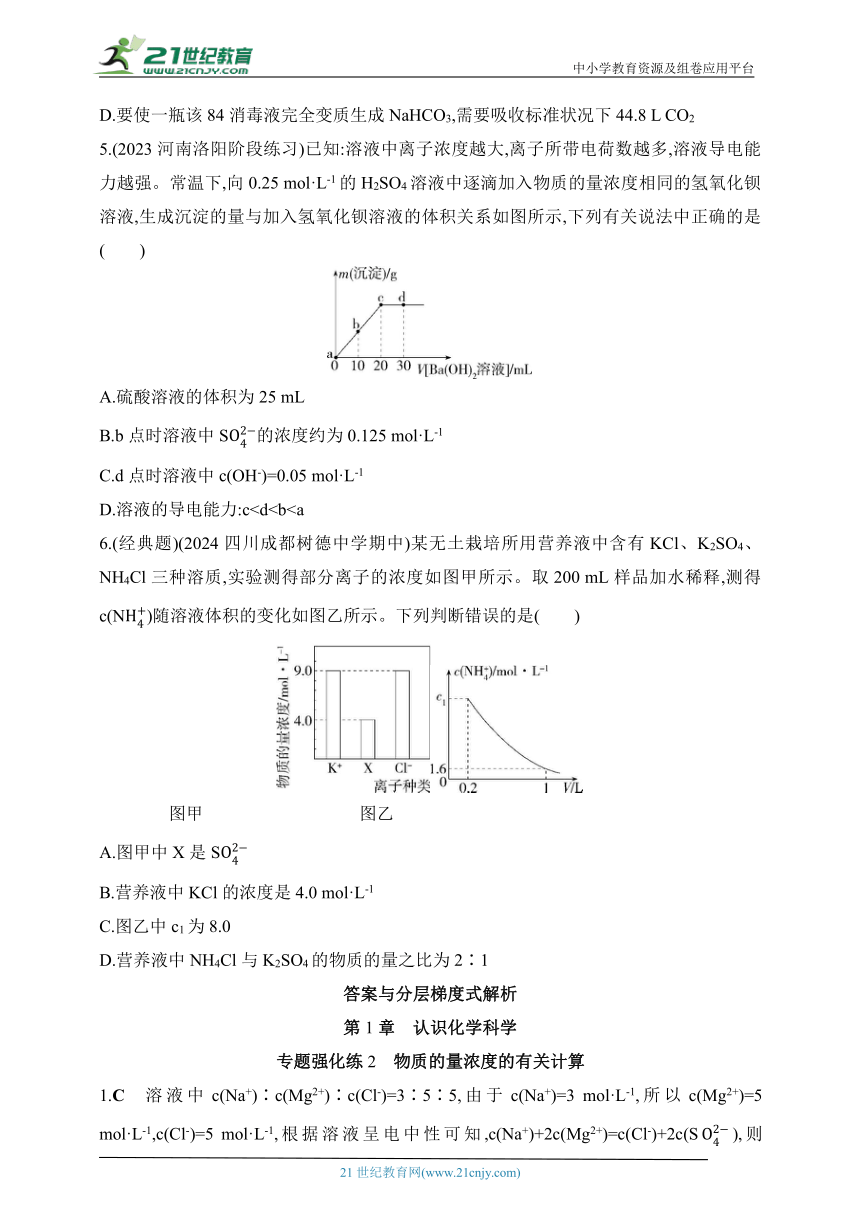
5.(2023河南洛阳阶段练习)已知:溶液中离子浓度越大,离子所带电荷数越多,溶液导电能力越强。常温下,向0.25 mol·L-1的H2SO4溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,下列有关说法中正确的是( )
A.硫酸溶液的体积为25 mL
B.b点时溶液中S的浓度约为0.125 mol·L-1
C.d点时溶液中c(OH-)=0.05 mol·L-1
D.溶液的导电能力:c6.(经典题)(2024四川成都树德中学期中)某无土栽培所用营养液中含有KCl、K2SO4、NH4Cl三种溶质,实验测得部分离子的浓度如图甲所示。取200 mL样品加水稀释,测得c(N)随溶液体积的变化如图乙所示。下列判断错误的是( )
图甲 图乙
A.图甲中X是S
B.营养液中KCl的浓度是4.0 mol·L-1
C.图乙中c1为8.0
D.营养液中NH4Cl与K2SO4的物质的量之比为2∶1
答案与分层梯度式解析
第1章 认识化学科学
专题强化练2 物质的量浓度的有关计算
1.C 溶液中c(Na+)∶c(Mg2+)∶c(Cl-)=3∶5∶5,由于c(Na+)=3 mol·L-1,所以c(Mg2+)=5 mol·L-1,c(Cl-)=5 mol·L-1,根据溶液呈电中性可知,c(Na+)+2c(Mg2+)=c(Cl-)+2c(S),则c(S)=4 mol·L-1,故选C。
名师点睛 根据溶液呈电中性计算溶液中的离子浓度时,一定要注意离子所带的电荷数。
2.D 8.4 g碳酸氢钠溶于100 mL水,得到的溶液的体积不是0.1 L,碳酸氢钠的浓度不等于1 mol·L-1,A错误;25 g无水硫酸铜的物质的量为0.156 25 mol,溶于水制成100 mL溶液,其浓度大于1 mol·L-1,B错误;将w g a%的NaCl饱和溶液蒸发掉0.5w g水,随着水蒸发,NaCl结晶析出,最终仍得到a%的NaCl饱和溶液,C错误;1体积c1 mol·L-1的硫酸用水稀释至5体积,稀释后浓度变为原来的1/5,即0.2c1 mol·L-1,D正确。
3.C V mL Al2(SO4)3溶液中Al3+的质量为a g,Al3+的物质的量为a mol,则Sa mol×a mol,所以稀释至4V mL后S mol·L-1。
4.B 该84消毒液的物质的量浓度为 mol·L-1≈4.0 mol·L-1,A正确;欲用NaClO固体配制480 mL 该浓度消毒液,应选用500 mL容量瓶,需要称量的NaClO固体质量为4 mol·L-1×0.5 L×74.5 g·mol-1=149.0 g,B不正确;该84消毒液的物质的量浓度约为4.0 mol·L-1,取100 mL该84消毒液稀释至100倍,稀释后溶液中c(Na+)约为0.04 mol·L-1,C正确;一瓶该84消毒液中NaClO的物质的量为2 mol,使一瓶该84消毒液完全变质生成NaHCO3,需要吸收2 mol CO2,标准状况下的体积为44.8 L,D正确。
5.D 硫酸和氢氧化钡反应的化学方程式为H2SO4+Ba(OH)2 BaSO4↓+2H2O,二者完全反应时消耗的物质的量相等,因为c(H2SO4)=c[Ba(OH)2],所以消耗两溶液的体积相等,均为20 mL,A错误;b点时溶液中S沉淀一半,溶液体积约变为原来的1.5倍,S≈0.083 mol·L-1,B错误;d点时Ba(OH)2过量,c(OH-)= mol·L-1=0.1 mol·L-1,C错误;根据已知信息可知,溶液的导电能力主要取决于离子浓度和离子所带电荷数目,a点为H2SO4溶液,浓度为0.25 mol·L-1,b点H2SO4反应了一半,浓度约为0.083 mol·L-1,c点H2SO4与Ba(OH)2恰好完全反应,溶液导电能力最弱,b点时溶液中溶质为H2SO4,d点时溶液中溶质为Ba(OH)2,二者物质的量均为0.25 mol·L-1×10×10-3 L=2.5×10-3 mol,但d点时溶液体积大,离子浓度小,导电能力较弱,则溶液的导电能力:c6.B 由图乙可知,铵根离子的起始浓度为c1 mol·L-1,根据稀释前后溶质的物质的量不变可得c1 mol·L-1×0.2 L=1.6 mol·L-1×1 L,解得c1=8.0,所以图甲中的X是S,故A、C正确;营养液中含有KCl、K2SO4、NH4Cl三种溶质,只有KCl、NH4Cl中含有氯离子,由氯离子的总物质的量浓度为9.0 mol·L-1,铵根离子的物质的量浓度为8.0 mol·L-1,可知氯化钾的物质的量浓度为9.0 mol·L-1-8.0 mol·L-1=1.0 mol·L-1,故B错误;NH4Cl的物质的量浓度为8.0 mol·L-1,K2SO4的物质的量浓度为4.0 mol·L-1,同一溶液中,两物质的物质的量浓度之比等于物质的量之比,所以营养液中NH4Cl与K2SO4的物质的量之比为2∶1,故D正确。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025鲁教版高中化学必修第一册
第1章 认识化学科学
专题强化练2 物质的量浓度的有关计算
1.(2024河南南阳期末联考)某溶液中含有Na+、Mg2+、S、Cl-,其中c(Na+)∶c(Mg2+)∶c(Cl-)=3∶5∶5,若Na+的物质的量浓度为3 mol·L-1,则S的物质的量浓度为( )
A.2 mol·L-1 B.3 mol·L-1
C.4 mol·L-1 D.8 mol·L-1
2.(2024山东省实验中学月考)下列叙述正确的是 ( )
A.将8.4 g NaHCO3晶体溶于100 mL水中,制得1 mol·L-1 NaHCO3溶液
B.将25 g无水CuSO4溶于水制成100 mL溶液,其浓度为1 mol·L-1
C.将w g a%的NaCl饱和溶液蒸发掉0.5w g水,得到2a%的NaCl溶液
D.将1体积c1 mol·L-1的硫酸用水稀释至5体积,所得溶液的浓度为0.2c1 mol·L-1
3.(2024河北石家庄阶段练习)V mL Al2(SO4)3溶液中含有Al3+ a g,取V mL溶液稀释至4V mL,则稀释后溶液中S的物质的量浓度是( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
4.(2024山东莱西一中月考)某同学购买了一瓶84消毒液,部分包装说明如下:
净含量:500 mL
密度:1.19 g/cm3
有效成分:NaClO
使用方法:稀释至100倍(体积比)后使用
注意事项:密封保存,易吸收空气中的CO2
变质
溶质质量分数:25%
根据以上信息和相关知识判断,下列说法不正确的是( )
A.该84消毒液的物质的量浓度约为4.0 mol·L-1
B.欲用NaClO固体配制480 mL该浓度消毒液,需要称量的NaClO固体质量为145.75 g
C.取100 mL该84消毒液稀释至100倍,稀释后的溶液中c(Na+)约为0.04 mol·L-1
D.要使一瓶该84消毒液完全变质生成NaHCO3,需要吸收标准状况下44.8 L CO2
5.(2023河南洛阳阶段练习)已知:溶液中离子浓度越大,离子所带电荷数越多,溶液导电能力越强。常温下,向0.25 mol·L-1的H2SO4溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,下列有关说法中正确的是( )
A.硫酸溶液的体积为25 mL
B.b点时溶液中S的浓度约为0.125 mol·L-1
C.d点时溶液中c(OH-)=0.05 mol·L-1
D.溶液的导电能力:c
图甲 图乙
A.图甲中X是S
B.营养液中KCl的浓度是4.0 mol·L-1
C.图乙中c1为8.0
D.营养液中NH4Cl与K2SO4的物质的量之比为2∶1
答案与分层梯度式解析
第1章 认识化学科学
专题强化练2 物质的量浓度的有关计算
1.C 溶液中c(Na+)∶c(Mg2+)∶c(Cl-)=3∶5∶5,由于c(Na+)=3 mol·L-1,所以c(Mg2+)=5 mol·L-1,c(Cl-)=5 mol·L-1,根据溶液呈电中性可知,c(Na+)+2c(Mg2+)=c(Cl-)+2c(S),则c(S)=4 mol·L-1,故选C。
名师点睛 根据溶液呈电中性计算溶液中的离子浓度时,一定要注意离子所带的电荷数。
2.D 8.4 g碳酸氢钠溶于100 mL水,得到的溶液的体积不是0.1 L,碳酸氢钠的浓度不等于1 mol·L-1,A错误;25 g无水硫酸铜的物质的量为0.156 25 mol,溶于水制成100 mL溶液,其浓度大于1 mol·L-1,B错误;将w g a%的NaCl饱和溶液蒸发掉0.5w g水,随着水蒸发,NaCl结晶析出,最终仍得到a%的NaCl饱和溶液,C错误;1体积c1 mol·L-1的硫酸用水稀释至5体积,稀释后浓度变为原来的1/5,即0.2c1 mol·L-1,D正确。
3.C V mL Al2(SO4)3溶液中Al3+的质量为a g,Al3+的物质的量为a mol,则Sa mol×a mol,所以稀释至4V mL后S mol·L-1。
4.B 该84消毒液的物质的量浓度为 mol·L-1≈4.0 mol·L-1,A正确;欲用NaClO固体配制480 mL 该浓度消毒液,应选用500 mL容量瓶,需要称量的NaClO固体质量为4 mol·L-1×0.5 L×74.5 g·mol-1=149.0 g,B不正确;该84消毒液的物质的量浓度约为4.0 mol·L-1,取100 mL该84消毒液稀释至100倍,稀释后溶液中c(Na+)约为0.04 mol·L-1,C正确;一瓶该84消毒液中NaClO的物质的量为2 mol,使一瓶该84消毒液完全变质生成NaHCO3,需要吸收2 mol CO2,标准状况下的体积为44.8 L,D正确。
5.D 硫酸和氢氧化钡反应的化学方程式为H2SO4+Ba(OH)2 BaSO4↓+2H2O,二者完全反应时消耗的物质的量相等,因为c(H2SO4)=c[Ba(OH)2],所以消耗两溶液的体积相等,均为20 mL,A错误;b点时溶液中S沉淀一半,溶液体积约变为原来的1.5倍,S≈0.083 mol·L-1,B错误;d点时Ba(OH)2过量,c(OH-)= mol·L-1=0.1 mol·L-1,C错误;根据已知信息可知,溶液的导电能力主要取决于离子浓度和离子所带电荷数目,a点为H2SO4溶液,浓度为0.25 mol·L-1,b点H2SO4反应了一半,浓度约为0.083 mol·L-1,c点H2SO4与Ba(OH)2恰好完全反应,溶液导电能力最弱,b点时溶液中溶质为H2SO4,d点时溶液中溶质为Ba(OH)2,二者物质的量均为0.25 mol·L-1×10×10-3 L=2.5×10-3 mol,但d点时溶液体积大,离子浓度小,导电能力较弱,则溶液的导电能力:c
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
