2024年安徽省芜湖市繁昌区第三中学自主招生模拟考化学试题(图片版,无答案)
文档属性
| 名称 | 2024年安徽省芜湖市繁昌区第三中学自主招生模拟考化学试题(图片版,无答案) |
|
|
| 格式 | |||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-18 00:00:00 | ||
图片预览


文档简介
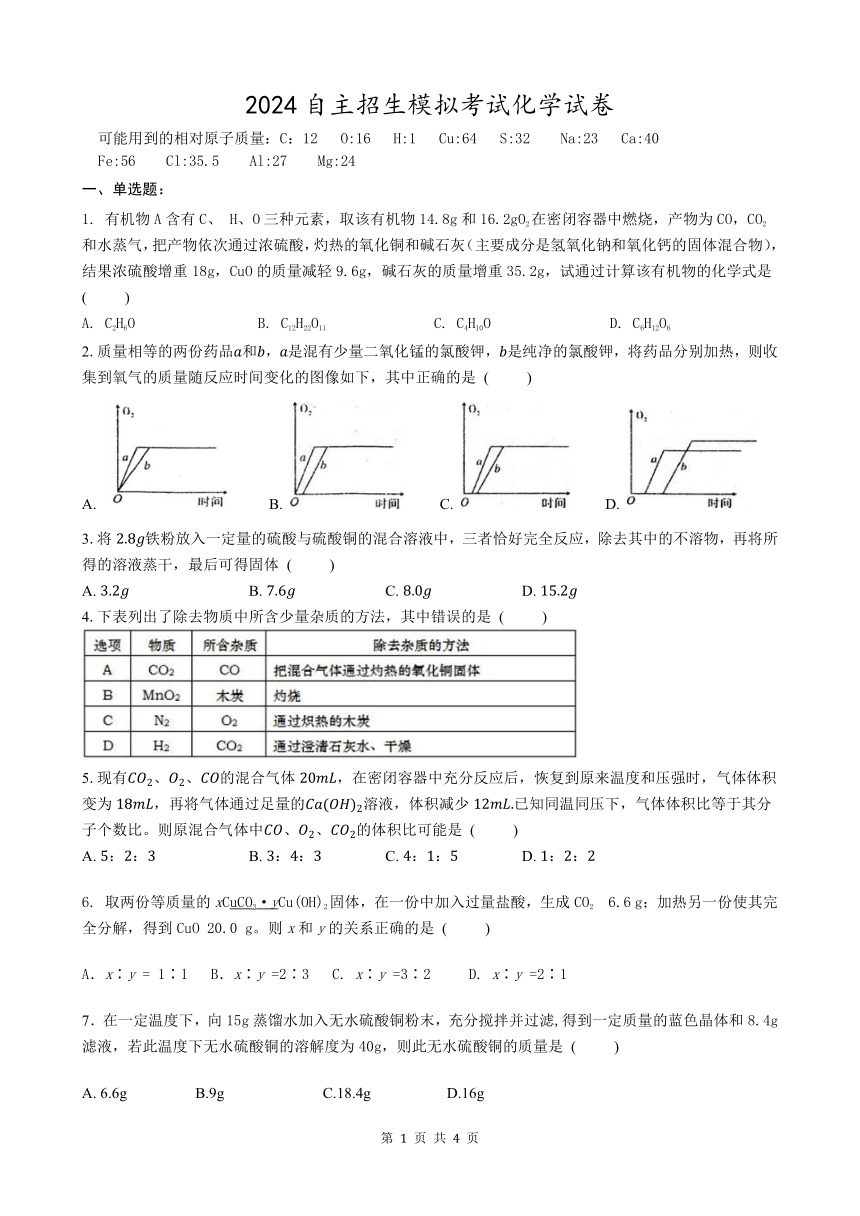
2024 自主招生模拟考试化学试卷
可能用到的相对原子质量:C:12 O:16 H:1 Cu:64 S:32 Na:23 Ca:40
Fe:56 Cl:35.5 Al:27 Mg:24
一、单选题:
1. 有机物 A 含有 C、 H、O三种元素,取该有机物 14.8g 和 16.2gO2在密闭容器中燃烧,产物为 CO,CO2
和水蒸气,把产物依次通过浓硫酸,灼热的氧化铜和碱石灰(主要成分是氢氧化钠和氧化钙的固体混合物),
结果浓硫酸增重 18g,CuO 的质量减轻 9.6g,碱石灰的质量增重 35.2g,试通过计算该有机物的化学式是
( )
A. C2H6O B. C12H22O11 C. C4H10O D. C6H12O6
2.质量相等的两份药品 和 , 是混有少量二氧化锰的氯酸钾, 是纯净的氯酸钾,将药品分别加热,则收
集到氧气的质量随反应时间变化的图像如下,其中正确的是 ( )
A. B. C. D.
3.将 2.8 铁粉放入一定量的硫酸与硫酸铜的混合溶液中,三者恰好完全反应,除去其中的不溶物,再将所
得的溶液蒸干,最后可得固体 ( )
A. 3.2 B. 7.6 C. 8.0 D. 15.2
4.下表列出了除去物质中所含少量杂质的方法,其中错误的是 ( )
5.现有 2、 2、 的混合气体 20 ,在密闭容器中充分反应后,恢复到原来温度和压强时,气体体积
变为 18 ,再将气体通过足量的 ( )2溶液,体积减少 12 .已知同温同压下,气体体积比等于其分
子个数比。则原混合气体中 、 2、 2的体积比可能是 ( )
A. 5:2:3 B. 3:4:3 C. 4:1:5 D. 1:2:2
6. 取两份等质量的 xCuCO3·yCu(OH)2固体,在一份中加入过量盐酸,生成 CO2 6.6 g;加热另一份使其完
全分解,得到 CuO 20.0 g。则 x和 y的关系正确的是 ( )
A.x∶y = 1∶1 B.x∶y =2∶3 C. x∶y =3∶2 D. x∶y =2∶1
7.在一定温度下,向 15g 蒸馏水加入无水硫酸铜粉末,充分搅拌并过滤,得到一定质量的蓝色晶体和 8.4g
滤液,若此温度下无水硫酸铜的溶解度为 40g,则此无水硫酸铜的质量是 ( )
A. 6.6g B.9g C.18.4g D.16g
第 1 页 共 4 页
{#{QQABKQIEggioAJBAAAhCAwXgCkOQkBECCQgOgAAMoAAAABNABCA=}#}
8. t℃时,加热烧杯中的石灰水,发现溶液变浑浊,测得此时溶液的 pH>7。关于溶液变浑浊的原因,同
学们有两种观点:①Ca(OH)2 的溶解度随温度升高而减小;②Ca(OH)2 与空气中的 CO2 反应。他们设计以
下方案进行探究,其中没有意义的是 ( )
A. 将装有浊液的烧杯,用冷水冷却,恢复至 t℃,观察浑浊是否消失
B. 取适量浊液,过滤,往滤渣中加入盐酸,观察是否有气泡产生
C. 取适量浊液,过滤,往滤液中加入 Na2CO3 溶液,观察是否有沉淀生成
D. 其他条件不变,隔绝空气,再做一个加热石灰水的对比实验
二.非选择题
9.下图是初中化学常见物质间的转化关系。 、 是组成元素相同的两种气体, 、 都是黑色固体, 是生
活中常用的调味剂、防腐剂,(部分反应条件和产物略去)。
(1)写出反应①的化学方程式
(2)反应④中 F和 R的最佳质量比为
(3)图中反应的基本类型有
10.神舟十一号与天宫二号的成功对接增强了国人的民族自信,推动了相关领域的研究。
(1)合金材料的研发
①合金的很多性能与组成它们的纯金属不同,如图中能表示锡铅合金的是 (填序号“ ”、
“ ”或“ ”)
②镁合金被誉为“21世纪绿色金属结构材料”。 17 12是一种特殊的镁合金。该合金是一种储氢材料,
完全吸氢后得到 2和 ,“储氢过程”属于 (填“物理”或“化学”)变化。
(2)合成材料的改良
碱式碳酸铝镁[ [ ] ( 3) ]是一种新型塑料阻燃剂,其中 、 、 、 的代数关系式:
2 + 3 = 。
(3) 2的绿色利用
目前空间站处理 2的一种方法是在催化剂作用下,利用 2使 2转化为 4并得到生活用水。该反应的化
学方程式为 。
11.兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关探究。
(提出问题)它们溶液的酸碱性及与酸反应时溶液的 pH如何变化?
(1)(实验探究 1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝
汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
第 2 页 共 4 页
{#{QQABKQIEggioAJBAAAhCAwXgCkOQkBECCQgOgAAMoAAAABNABCA=}#}
液体名称 蒸馏水 碳酸氢钠溶液 碳酸钠溶液 氢氧化钠溶液
紫甘蓝汁液显示的颜色 蓝紫色 蓝色 绿色 黄色
查阅资料:
pH 7.5~9 10~11.9 12~14
紫甘蓝汁液显示的颜色 蓝色 绿色 黄色
(得出结论 1)三种溶液的碱性由强到弱的顺序为 。
(2)(实验探究 2)甲同学在烧杯溶液中加入约 5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶
液由无色变为 色。乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的
盐酸,得到 pH变化与时间的关系如图 1所示.
a点的意义为
(3)(得出结论 2)从微观角度分析,该反应的实质是 。
(4)(实验探究 3)向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的
盐酸,得列 pH变化与时间的关系如图 2、图 3所示。
(交流与反思)b点的溶质为 (写化学式),将图 2和图 3的阴影部分进行叠加,发
现两者基本重合,c点的溶质 (写化学式)
(5)(得出结论 3)通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表
示: 、 。
12.已知某种治疗胃病药品的主要成份是铝碳酸镁片,化学式为 ( )16 3·4 2 ,假设药品中的其
它成份受热不分解、不溶于水且不与稀硫酸反应。某研究性学习小组设计了如下实验探究铝碳酸镁片的组
成。 查阅资料:
①氯化钙是一种白色粒状物,吸湿性极强,暴露于空气中极易潮解;
②碱石灰是 与 的固体混合物。
第 3 页 共 4 页
{#{QQABKQIEggioAJBAAAhCAwXgCkOQkBECCQgOgAAMoAAAABNABCA=}#}
【实验一】取 该药片,研成粉末放入硬质玻璃管中,加热。
(1)铝碳酸镁片加热分解的产物为 2 3、 、 2和水,若要测定生成的 2和水的质量,装置 和 中
盛放的药品应选择: _____、 ______。(填序号)
①浓硫酸 ②碱石灰 ③氯化钙 ④纯碱
(2)实验开始前关闭弹簧夹_____(填 或 ),打开另一个弹簧夹,先通入一段时间空气,装置 中盛放的是
碱石灰,它的作用是______________。
(3)一段时间后,打开和关闭相应的弹簧夹,点燃酒精灯加热,充分反应后,停止加热,继续通入一段时间
空气,目的是______________________。
【实验二】另取 该药片,加入 100 9.8%的稀硫酸,充分反应后滤去不溶物,得到含有 4和
2( 4)3等溶质的滤液,向滤液中逐渐加入足量的稀 溶液,产生沉淀的质量与加入溶液中 的
质量的关系如图。
已知:
4 + 2 = ( )2 ↓+ 2 4
2( 4)3 + 6 = 2 ( )3 ↓+ 3 2 4
( )3 + = 2 + 2 2
( )2不溶于 , 2可溶于水。
(4)图中当加入溶液中 的质量为 0.80 时仍没有沉淀,说明滤液中含有______。当加入溶液中
的质量到 时,生成的沉淀成分为____g________、____g________, =_____ 。
(5)试确定铝碳酸镁的化学式为_________。
13.实验室有一变质的氢氧化钠样品(样品中只含 Na2CO3杂质,且成分均匀),为测量样品中 Na2CO3的质量
分数,某同学称取 10g 氢氧化钠样品放入烧杯中,加入 40g 水完全溶解,将 150g 盐酸平均分 6 份依次加
人烧杯中(烧杯的质量为 50g),每次充分反应后都用电子天平进行称量(假设产生的气体完全逸出),
实验数据如表所示,图乙表示产生气休的质量与加人稀盐酸质量的关系。
实验次数 1 2 3 4 5 6
加入稀盐
酸的质量 25 25 25 25 25 25
/g
电子天平
125 150 175 199.7 223.9 248.9
的示数/g
(1)分析表格数据和图乙,判断 n 的值为_____。
(2)计算氢氧化钠样品中 Na2CO3的质量分数为多少?
(3)通过实验加计算,该同学发现:加稀盐酸,若氢氧化钠溶液不变质,不会产生二氧化碳:氢氧化钠
变质的量越多,产生的二氧化碳越多:氢氧化钠完全变质,产生的二氧化碳最多,于是该同学推测:样品
中氢氧化钠变质的量越多,完全反应所需的稀盐酸的质量越大。请判断该同学的推测是否正确并说明理由。
第 4 页 共 4 页
{#{QQABKQIEggioAJBAAAhCAwXgCkOQkBECCQgOgAAMoAAAABNABCA=}#}
可能用到的相对原子质量:C:12 O:16 H:1 Cu:64 S:32 Na:23 Ca:40
Fe:56 Cl:35.5 Al:27 Mg:24
一、单选题:
1. 有机物 A 含有 C、 H、O三种元素,取该有机物 14.8g 和 16.2gO2在密闭容器中燃烧,产物为 CO,CO2
和水蒸气,把产物依次通过浓硫酸,灼热的氧化铜和碱石灰(主要成分是氢氧化钠和氧化钙的固体混合物),
结果浓硫酸增重 18g,CuO 的质量减轻 9.6g,碱石灰的质量增重 35.2g,试通过计算该有机物的化学式是
( )
A. C2H6O B. C12H22O11 C. C4H10O D. C6H12O6
2.质量相等的两份药品 和 , 是混有少量二氧化锰的氯酸钾, 是纯净的氯酸钾,将药品分别加热,则收
集到氧气的质量随反应时间变化的图像如下,其中正确的是 ( )
A. B. C. D.
3.将 2.8 铁粉放入一定量的硫酸与硫酸铜的混合溶液中,三者恰好完全反应,除去其中的不溶物,再将所
得的溶液蒸干,最后可得固体 ( )
A. 3.2 B. 7.6 C. 8.0 D. 15.2
4.下表列出了除去物质中所含少量杂质的方法,其中错误的是 ( )
5.现有 2、 2、 的混合气体 20 ,在密闭容器中充分反应后,恢复到原来温度和压强时,气体体积
变为 18 ,再将气体通过足量的 ( )2溶液,体积减少 12 .已知同温同压下,气体体积比等于其分
子个数比。则原混合气体中 、 2、 2的体积比可能是 ( )
A. 5:2:3 B. 3:4:3 C. 4:1:5 D. 1:2:2
6. 取两份等质量的 xCuCO3·yCu(OH)2固体,在一份中加入过量盐酸,生成 CO2 6.6 g;加热另一份使其完
全分解,得到 CuO 20.0 g。则 x和 y的关系正确的是 ( )
A.x∶y = 1∶1 B.x∶y =2∶3 C. x∶y =3∶2 D. x∶y =2∶1
7.在一定温度下,向 15g 蒸馏水加入无水硫酸铜粉末,充分搅拌并过滤,得到一定质量的蓝色晶体和 8.4g
滤液,若此温度下无水硫酸铜的溶解度为 40g,则此无水硫酸铜的质量是 ( )
A. 6.6g B.9g C.18.4g D.16g
第 1 页 共 4 页
{#{QQABKQIEggioAJBAAAhCAwXgCkOQkBECCQgOgAAMoAAAABNABCA=}#}
8. t℃时,加热烧杯中的石灰水,发现溶液变浑浊,测得此时溶液的 pH>7。关于溶液变浑浊的原因,同
学们有两种观点:①Ca(OH)2 的溶解度随温度升高而减小;②Ca(OH)2 与空气中的 CO2 反应。他们设计以
下方案进行探究,其中没有意义的是 ( )
A. 将装有浊液的烧杯,用冷水冷却,恢复至 t℃,观察浑浊是否消失
B. 取适量浊液,过滤,往滤渣中加入盐酸,观察是否有气泡产生
C. 取适量浊液,过滤,往滤液中加入 Na2CO3 溶液,观察是否有沉淀生成
D. 其他条件不变,隔绝空气,再做一个加热石灰水的对比实验
二.非选择题
9.下图是初中化学常见物质间的转化关系。 、 是组成元素相同的两种气体, 、 都是黑色固体, 是生
活中常用的调味剂、防腐剂,(部分反应条件和产物略去)。
(1)写出反应①的化学方程式
(2)反应④中 F和 R的最佳质量比为
(3)图中反应的基本类型有
10.神舟十一号与天宫二号的成功对接增强了国人的民族自信,推动了相关领域的研究。
(1)合金材料的研发
①合金的很多性能与组成它们的纯金属不同,如图中能表示锡铅合金的是 (填序号“ ”、
“ ”或“ ”)
②镁合金被誉为“21世纪绿色金属结构材料”。 17 12是一种特殊的镁合金。该合金是一种储氢材料,
完全吸氢后得到 2和 ,“储氢过程”属于 (填“物理”或“化学”)变化。
(2)合成材料的改良
碱式碳酸铝镁[ [ ] ( 3) ]是一种新型塑料阻燃剂,其中 、 、 、 的代数关系式:
2 + 3 = 。
(3) 2的绿色利用
目前空间站处理 2的一种方法是在催化剂作用下,利用 2使 2转化为 4并得到生活用水。该反应的化
学方程式为 。
11.兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关探究。
(提出问题)它们溶液的酸碱性及与酸反应时溶液的 pH如何变化?
(1)(实验探究 1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝
汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
第 2 页 共 4 页
{#{QQABKQIEggioAJBAAAhCAwXgCkOQkBECCQgOgAAMoAAAABNABCA=}#}
液体名称 蒸馏水 碳酸氢钠溶液 碳酸钠溶液 氢氧化钠溶液
紫甘蓝汁液显示的颜色 蓝紫色 蓝色 绿色 黄色
查阅资料:
pH 7.5~9 10~11.9 12~14
紫甘蓝汁液显示的颜色 蓝色 绿色 黄色
(得出结论 1)三种溶液的碱性由强到弱的顺序为 。
(2)(实验探究 2)甲同学在烧杯溶液中加入约 5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶
液由无色变为 色。乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的
盐酸,得到 pH变化与时间的关系如图 1所示.
a点的意义为
(3)(得出结论 2)从微观角度分析,该反应的实质是 。
(4)(实验探究 3)向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的
盐酸,得列 pH变化与时间的关系如图 2、图 3所示。
(交流与反思)b点的溶质为 (写化学式),将图 2和图 3的阴影部分进行叠加,发
现两者基本重合,c点的溶质 (写化学式)
(5)(得出结论 3)通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表
示: 、 。
12.已知某种治疗胃病药品的主要成份是铝碳酸镁片,化学式为 ( )16 3·4 2 ,假设药品中的其
它成份受热不分解、不溶于水且不与稀硫酸反应。某研究性学习小组设计了如下实验探究铝碳酸镁片的组
成。 查阅资料:
①氯化钙是一种白色粒状物,吸湿性极强,暴露于空气中极易潮解;
②碱石灰是 与 的固体混合物。
第 3 页 共 4 页
{#{QQABKQIEggioAJBAAAhCAwXgCkOQkBECCQgOgAAMoAAAABNABCA=}#}
【实验一】取 该药片,研成粉末放入硬质玻璃管中,加热。
(1)铝碳酸镁片加热分解的产物为 2 3、 、 2和水,若要测定生成的 2和水的质量,装置 和 中
盛放的药品应选择: _____、 ______。(填序号)
①浓硫酸 ②碱石灰 ③氯化钙 ④纯碱
(2)实验开始前关闭弹簧夹_____(填 或 ),打开另一个弹簧夹,先通入一段时间空气,装置 中盛放的是
碱石灰,它的作用是______________。
(3)一段时间后,打开和关闭相应的弹簧夹,点燃酒精灯加热,充分反应后,停止加热,继续通入一段时间
空气,目的是______________________。
【实验二】另取 该药片,加入 100 9.8%的稀硫酸,充分反应后滤去不溶物,得到含有 4和
2( 4)3等溶质的滤液,向滤液中逐渐加入足量的稀 溶液,产生沉淀的质量与加入溶液中 的
质量的关系如图。
已知:
4 + 2 = ( )2 ↓+ 2 4
2( 4)3 + 6 = 2 ( )3 ↓+ 3 2 4
( )3 + = 2 + 2 2
( )2不溶于 , 2可溶于水。
(4)图中当加入溶液中 的质量为 0.80 时仍没有沉淀,说明滤液中含有______。当加入溶液中
的质量到 时,生成的沉淀成分为____g________、____g________, =_____ 。
(5)试确定铝碳酸镁的化学式为_________。
13.实验室有一变质的氢氧化钠样品(样品中只含 Na2CO3杂质,且成分均匀),为测量样品中 Na2CO3的质量
分数,某同学称取 10g 氢氧化钠样品放入烧杯中,加入 40g 水完全溶解,将 150g 盐酸平均分 6 份依次加
人烧杯中(烧杯的质量为 50g),每次充分反应后都用电子天平进行称量(假设产生的气体完全逸出),
实验数据如表所示,图乙表示产生气休的质量与加人稀盐酸质量的关系。
实验次数 1 2 3 4 5 6
加入稀盐
酸的质量 25 25 25 25 25 25
/g
电子天平
125 150 175 199.7 223.9 248.9
的示数/g
(1)分析表格数据和图乙,判断 n 的值为_____。
(2)计算氢氧化钠样品中 Na2CO3的质量分数为多少?
(3)通过实验加计算,该同学发现:加稀盐酸,若氢氧化钠溶液不变质,不会产生二氧化碳:氢氧化钠
变质的量越多,产生的二氧化碳越多:氢氧化钠完全变质,产生的二氧化碳最多,于是该同学推测:样品
中氢氧化钠变质的量越多,完全反应所需的稀盐酸的质量越大。请判断该同学的推测是否正确并说明理由。
第 4 页 共 4 页
{#{QQABKQIEggioAJBAAAhCAwXgCkOQkBECCQgOgAAMoAAAABNABCA=}#}
同课章节目录
