7.3 乙醇与乙酸课件(共94张ppt)人教版(2019)必修第二册
文档属性
| 名称 | 7.3 乙醇与乙酸课件(共94张ppt)人教版(2019)必修第二册 |  | |
| 格式 | pptx | ||
| 文件大小 | 95.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-20 19:28:25 | ||
图片预览











文档简介
(共94张PPT)
第七章
有机化合物
第三节
乙醇与乙酸
中国有历史悠久的酒文化!你能想到那些关于酒的诗句吗??
劝君更尽一杯酒,西出阳关无故人。
葡萄美酒夜光杯,欲饮琵琶马上催。
醉酒当歌,人生几何?
兰陵美酒夜光杯,欲饮琵琶马上催
白日放歌须纵酒,青春作伴好还乡。
绿蚁新醅酒,红泥小火炉。
人们很早就知道用粮食或水果发酵生产酒和醋。酒中含有的乙醇和醋中含有的乙酸是两种常见的有机化合物。
一
乙醇
早在几千年前,人类就掌握了发酵法酿酒的技术。
各种酒类都含有浓度不等的乙醇,故乙醇俗称酒精。
乙醇的物理性质
颜色状态:无色透明的液体
气味:特殊的香味
密度:比水小,200C时的密度是0.7893g/cm3
挥发性:沸点78℃,易挥发
溶解性:乙醇是一种重要的有机溶剂,能够溶解多种有机物和无机物,并能与水以任意比例互溶。
工业制备无水乙醇:加生石灰(CaO)蒸馏
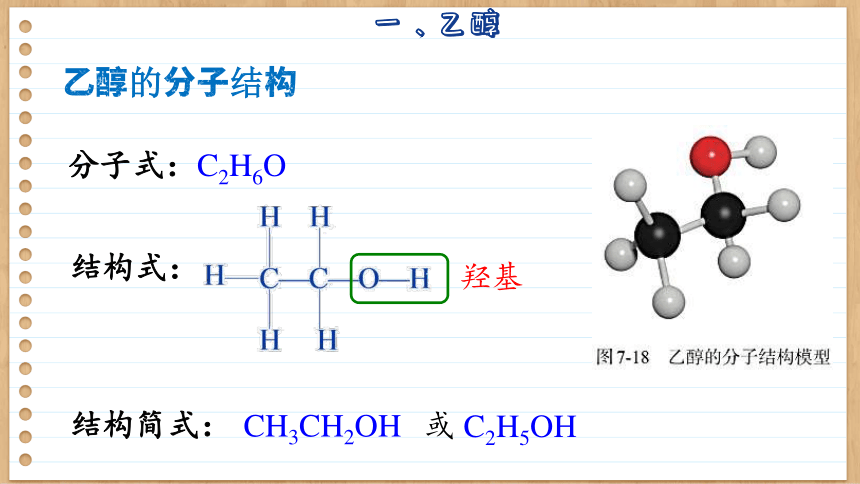
乙醇的分子结构
分子式:C2H6O
结构式:
结构简式:
CH3CH2OH
或 C2H5OH
羟基
我们把 ─OH 原子团叫做羟基。乙醇可以看成是乙烷分子中的一个氢原子被羟基取代后的产物。我们把烃类物质侧链中的氢原子被羟基取代而成的化合物,叫做醇。
像这样,烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物成为烃的衍生物。比如前面学习的一氯甲烷、二氯甲烷、1,2─二溴乙烷都属于烃的衍生物。烃的衍生物和烃具有不同的性质。
1 . 乙醇与钠反应
【实验 7-4】
在盛有少量无水乙醇的试管中,加入一小块新切的用滤纸吸干表面煤油的钠,在试管口迅速塞上带尖嘴导管的橡胶塞。
用小试管收集气体并检验其纯度,然后点燃(如图7─19),再将干燥的小烧杯罩在火焰上,待烧杯壁上出现液滴后,迅速倒转烧杯,向其中加入少量澄清石灰水,观察现象,并与前面做过的水与钠反应的实验现象进行比较。
实验现象:钠与乙醇反应,沉入乙醇底部,仍为块状,没有声音,放出气泡,反应缓慢;产生的气体可在空气中安静地燃烧,烧壁上有水滴生成,烧杯中加入澄清的石灰水不变浑浊。说明产生的气体是H2
乙醇和钠的反应
与烷烃不同,乙醇由于分子中羟基的存在,可以与钠发生反应。在该反应中,钠置换了释基中的氢,生成了氢气和乙醇钠。
2CH3CH2OH +2Na → 2CH3CH2ONa +H2↑
乙醇钠
注意 ①断O-H键,发生置换反应、取代反应
②氢原子活泼性:酸>水>醇
③此反应可检验─OH的存在,用来计算分子中─OH的数目 (2个—OH产生1个H2,故物质的量之比为2∶1)
O—H 键断开
H H
| |
H— C — C — O —H
|
H
钠与水、与乙醇反应的现象比较
钠与水
钠是否浮在液面上
钠的形状是否变化
有无声音
有无气泡
剧烈程度
反应方程式
2Na+2H2O=2NaOH+H2↑
浮在水面
剧烈
有气泡产生
熔化
发出嘶嘶声
钠与乙醇
钠是否浮在液面上
钠的形状是否变化
有无声音
有无气泡
剧烈程度
反应方程式
有气泡产生
没有声音
不熔化
沉入底部
缓慢
2CH3CH2OH+2Na → 2CH3CH2ONa+H2↑
想一想:实验现象说明了什么问题
(1) 钠浮在水面上,而沉在乙醇中
(3) 钠与乙醇的反应速率比钠与水的反应速率慢,说明羟基上的H原子与水分子中H原子的活泼性:
(2) 乙醇与钠反应的性质是由它的什么决定的
[说明]
(1) 水的密度>钠的密度>乙醇的密度
(2) 羟基决定乙醇能和钠反应生成氢气
(3) 羟基中的H原子的活泼性:醇<水
官能团决定有机物的性质,连接官能团的其它部分对性质也有所影响。
官能团
乙醇和乙烷性质的不同,从分子结构分析,是因为取代氢原子的羟基对乙醇性质产生了影响。
像这样决定有机化合物特性的原子或原子团叫做官能团。
羟基是醇类物质的官能团,碳碳双键和碳碳三键分别是烯烃和炔烃的官能团。
常见官能团碳碳双键 C═C、碳碳三键 C≡C、羟基─OH、羧基 ─COOH、醛基 ─CHO、─Cl (卤素原子)等。
有机化学反应主要发生在官能团上,官能团对有机物的性质起决定作用。
提示
烃分子失去1个氢原子后所剩余的部分叫做烃基,可以用一R来表示。如 ─CH3叫甲基,─CH2CH3;叫乙基。烃的衍生物分子一般可以看成是烃基和官能团相互结合组成的。例如,乙醇分子可以看成是由乙基和轻基组成的:CH3CH2─┊─OH。
2. 氧化反应
乙醇在空气中燃烧时生成二氧化碳和水,同时放出大量的热。
2CO2 + 3H2O
C2H5OH + 3O2
点燃
现象:产生淡蓝色火焰,同时放出大量热。
在一定条件下,乙醇还能被氧化为其他产物。
酒精燃料飞机
酒精火锅
【实验 7-5】
向试管中加入少量乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼烧后插入乙醇,反复几次。注意观察反应现象,小心地闻试管中液体产生的气味。
a. 铜丝红色→黑色→红色反复变化
[实验现象]
b. 在试管口可以闻到刺激性气味
[思考] 铜丝在此实验中起什么作用?
催化剂
乙醇在加热和有催化剂 (如铜或银)存在等条件下可以被空气中的氧气氧化为乙醛 (CH3CHO)。
化学反应的方程式为:
(乙醇具有还原性)
2 CH3CH2OH +O2 2CH3CHO + 2H2O
Cu / Ag
乙醇
断键机理:
2CH3─C─O─H + O2 2CH3─C─H+2H2O
│
H
H
│
Cu / Ag
O
║
醇催化氧化的条件:羟基碳原子上必须有氢
反应历程
2 Cu+O2 ═══ 2CuO
CH3CH2OH + CuO Cu + CH3CHO + H2O
H H
| |
H— C — C══O
|
H 乙醛
CH3CHO结构中的 —CHO基团叫醛基,醛基由一个碳原子、一个氢原子及一个双键氧原子组成。
H H
| |
2R—C—O—H+O═O 2R—C══O+2H2O
|
H
醇催化氧化机理
醇发生催化氧化时去掉2个H原子。连接-OH官能团的碳原子上必须有H,才能发生催化氧化。
醛
Cu
△
乙醇被氧化为乙酸
乙醛的官能团是醛基( ─ C ─ H,或写作 ─ CHO),在适当条件下乙醛可以被氧气进一步氧化,生成乙醇(CH3COOH).
O
║
2CH3CH2OH + O2 2CH3CHO + 2H2O
Cu / Ag
乙醇被氧化为乙醛
乙醛接着可以被氧化为乙酸
2CH3CHO + O2 2CH3COOH
催化剂
也能被强氧化剂直接氧化为乙酸
乙醇还可以与酸性高酸钾溶液或酸性重铬酸钾(K2Cr2O7) 溶液反应,被氧化成乙酸。
CH3CH2OH CH3COOH
酸性高锰酸钾溶液
酸性重铬酸钾溶液
橙红 K2Cr2O7 溶液把乙醇氧化为乙酸,发生颜色变化
2K2Cr2O7 + 3CH3CH2OH +8H2SO4
2Cr2(SO4)3 +3CH3─C─OH+2K2SO4+11H2O
橙红色
蓝绿色
O║
K2Cr2O7
Cr2(SO4)3
(橙红色)
(蓝绿色)
乙醇
交警常用此原理检测司机是否酒后驾车。
乙醇发生反应的断键原理
乙醇分子中不同的化学键如图:
发生不同化学反应时乙醇的断键位置
(1)与活泼金属反应键________断裂
(2) CH3CH2OH 燃烧键________断裂
(3) 在Cu或Ag催化下和O2反应键________断裂
H
C
O
H
H
H
H
C
H
①
③
②
④
①
①③
全部
乙醇的用途
乙醇可用作燃料,还是重要的有机化工原料和溶剂用于生产医药、香料、化妆品、涂料等。医疗上常用75% (体积分数)的乙醇溶液作消毒剂。
消毒剂(75%的乙醇溶液)体积分数
医药
可以做燃料,提供能量
燃料
化工原料
饮料
可以做溶剂,提取多种有机物、无机物
工业
资料卡片~~~~~~~~~~~~~~~~~~~~~~~~~~~
酒类产品标签中的酒精度是指乙醇的体积分数,白酒一般在25%~68%,啤酒一般在3%~5%。乙醇进入人体后,会在肝中通过酶的催化作用被氧化为乙醛和乙酸,最终被氧化为二氧化碳和水。过量饮酒会加重肝负担,血液中较高浓度的乙醇和乙醛也会对人体产生毒害作用。
随堂练习
1.下列有关乙醇的物理性质的应用中不正确的是 ( )。
A.熟语“酒香不怕巷子深”是由于乙醇容易挥发
B.用乙醇提取中药的有效成分是由于乙醇能够溶解很多种有机物和无机物
C.酒厂可以勾兑各种浓度的酒是由于乙醇能够以任意比溶解于水
D.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
D
2、下列物质可使酸性高锰酸钾溶液褪色, 不能使溴水褪色的是( )
A、甲烷 B、乙烯 C、乙醇 D、乙烷
C
3. 比较乙烷和乙醇的结构,下列说法错误的是( )。
A. 两个分子中碳原子都以单键相连
B. 乙醇可以看成是乙烷分子中的一个氢原子被羟基取代后的产物
C. 分子里都含有6个相同的氢原子
D. 乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
C
4、能用来检验酒精中是否含有水的试剂是 ( )。
A、 CuSO4·5H2O B、CuSO4
C、 浓硫酸 D、金属钠
B
5. 将等质量的铜片放在酒精灯上加热后,分别插入下列溶液中,放置片刻,铜片质量增加的是( )。
A. 硝酸 B. 无水乙醇
C. 石灰水 D. 盐酸
C
二
乙酸
传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。
烧菜时放了一些,味道特别鲜美,便贮藏着
作为“调味酱”。故醋在古代又叫“苦酒”。
醋的来历?
食醋是生活中常见的调味品,其中含有3%~ 5%的乙酸,所以乙酸又被称为醋酸。
乙酸的物理性质
乙酸是有强烈刺激性气味的无色液体。
当温度低于熔点时,乙酸可凝结成类似冰的晶体所以纯净的乙酸又叫冰醋酸。
乙酸易溶于水和乙醇。
数据
乙酸
熔点:16.6 ℃
沸点:118 ℃
密度:1.05 g/cm3
(1) 乙酸的分子式:
(2) 结构式:
(3) 结构简式:
分子组成与结构
C2H4O2
CH3COOH
官能团为羧基
CH3 —C—OH
O
羧基可以表示为—COOH 或者
—C—OH
O
CH3 —C—OH
O
(4) 乙酸结构分析
甲基 和 羧基
受 C══O 的影响,氢氧键更易断
当氢氧键断裂时,容易解离出氢离子,使乙酸具有酸性。
1 . 酸性
乙酸的化学性质 (主要由羧基决定)
可以电离:CH3COOH CH3COO-+H+
使紫色石蕊试液变红。
乙酸是一种重要的有机酸,具有酸性 (弱酸性)。
可以和碱反应:
NaOH+CH3COOH ══ CH3COONa+H2O
可以和金属反应:
Mg+2CH3COOH ══ (CH3COO)2Mg+H2↑
Cu(OH)2+2CH3COOH ══ (CH3COO)2Cu+2H2O
思考与讨论
(1) 食醋可以清除水壶中的少量水垢 (主要成分是碳酸钙),这是利用了乙酸的什么性质 请写出相关反应的化学方程式。
CaCO3+2CH3COOH══ (CH3COO)2Ca+CO2↑+H2O
(除水垢)
CaCO3+2CH3COOH══2CH3COO─+Ca2++CO2↑+H2O
(2) 如何比较乙酸、碳酸、盐酸的酸性强弱?请查阅资料,与同学讨论,根据生活经验设计实验方案。
CaCO3+2CH3COOH ══ (CH3COO)2Ca+CO2↑+H2O
(除水垢)
HCl+CH3COONa ══ CH3COOH+NaCl
酸性: HCl>CH3COOH > H2CO3
以上2个反应能够进行,根据强酸制弱酸的原理
2. 酯化反应
在一支试管中加入3ml乙醇,然后边振荡试管边慢慢加入2ml浓硫酸和2ml乙酸,再加入几片碎瓷片。连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和Na2CO3溶液的液面上(如图7-22),观察现象。
【实验 7-6】
【实验现象】
饱和碳酸钠溶液的液面上有透明的油状液体,并可闻到香味。
先加乙醇 3mL
再加浓硫酸 2mL
再加乙酸 2mL
饱和的Na2CO3溶液收集
碎瓷片的作用是防止暴沸。
实验药品及其用量
实验的药品加入顺序
注意
乙醇和乙酸乙醋是常用的化工原料和有机溶剂。它们在储存时应置于密闭容器,存放在阴凉通风处,并与氧化剂、易燃物等分开存放,注意远离火种和热源。
在反应过程中,右侧试管内液体的上层有无色透明的油状液体产生,并可以闻到香味,这种有香味的液体是乙酸乙酯。
该反应的化学方程式为:
① 浓硫酸的作用?
② 饱和Na2CO3溶液的作用?
催化剂、吸水剂
中和乙酸
溶解乙酸乙酯中乙醇
降低乙酸乙酯在水中的溶解度
浓硫酸和饱和 Na2CO3 溶液的作用
③ 为什么导管不插入饱和Na2CO3溶液中?
防止受热不匀发生倒吸
酯化反应定义:酸跟醇起作用,生成酯和水的反应
实质:酸脱羟基、醇去氢(羟基上的)
酯化反应属于取代反应
酯化反应反应机理
CH3─C─OH+H─O─C2H5 CH3─C─O─C2H5+H2O
浓H2SO4
△
O
║
O
║
为了提高酯化反应的速率,一般需要加热,并加入浓硫酸等催化剂。
酯化反应是可逆反应,乙酸乙酯会与水发生水解反应生成乙酸和乙醇。
CH3COOH+HOC2H5 CH3COOC2H5+H2O
浓H2SO4
△
乙酸乙酯是酯类物质中的一种,其官能团是酯基 ( ,或写作─COOR)。
─C─O─R
O
║
很多鲜花和水果的香味都来自酯,如草莓中含有乙酸乙酯和乙酸异戊酯,苹果中含有戊酸戊酯。
这些分子中碳原子数较少、相对分子质量较小的低级酯具有一定的挥发性,有芳否气味,可用作饮料、糖果、化妆品中的香料和有机溶剂。
三
官能团与有机化合物的分类
通过对乙烯、乙醇和乙酸性质的学习,我们认识到官能团对有机物的性质具有决定作用,含有相同官能团的有机物在性质上具有相似之处。
因此我们可以根据有机物分子中所含官能团的不同,从结构和性质上对数量庞大的有机物进行分类 (如表7-2 )。
表7-2 常见的有机化合物类别、官能团和代表物
方法导引~~~~~~~~~~~~~~~~~~~~~~~~~~~
认识有机化合物的一般思路
认识一种有机物,可先从结构入手,分析其碳骨架和官能团,了解它所属的有机物类别;再结合这类有机物的一般性质推测该有机物可能具有的性质,并通过实验进行验证:在此基础上进一步了解该有机物的用途。
另外,还可以根据有机物发生的化学反应,了解其在有机物转化 (有机合成)中的作用。与认识无机物类似,认识有机物也体现了“结构决定性质”的观念各类有机物在结构和性质上具有的明显规律性,有助于我们更好地认识有机物。
乙酸的用途
随堂练习
1. 关于乙酸的下列说法中不正确的是 ( )
A. 乙酸易溶于水和乙醇
B. 无水乙酸又称冰醋酸,它是纯净物
C. 乙酸是一种重要的有机酸,是有刺激性气味的液体
D. 乙酸分子里有四个氢原子,所以不是一元酸
D
2、炒菜时,又加酒又加醋,可使菜变得香味可口,原因是( )。
A.有盐类物质生成 B.有酸类物质生成
C.有醇类物质生成 D.有酯类物质生成
D
3. 除去乙酸乙酯中含有的乙酸,最好的处理和操作是( )。
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
C
4.下列关于乙酸性质的叙述中,错误的是( )。
A. 乙酸的酸性比碳酸强,所以它可以与碳酸盐反应,产生CO2气体
B. 乙酸能与醇类物质发生酯化反应
C. 乙酸分子中含有碳氧双键,所以它能使溴水褪色
D. 乙酸在温度低于16.6℃时,就凝结成冰状晶体
C
5. 下列关于醋酸性质的叙述错误的是 ( )。
A. 醋酸是一种有强烈刺激性气味的无色液体
B. 冰醋酸是无水乙酸,不是乙酸的水溶液
C. 醋酸能跟碳酸钠溶液发生反应产生CO2
D. 在发生酯化反应时,醋酸分子中羟基中的氢原子跟醇分子中的羟基结合成水
D
6. 某有机物的结构为 它最不可能具有的性质是( )。
A. 能与金属钠反应放出H2
B. 既能与C2H5OH发生酯化反应也能与CH3COOH发生酯化反应
C. 能发生加聚反应
D. 水溶液能使紫色石蕊试纸变红
CH2─COOH
|
OH
C
练习与应用
1. 从结构上看,烃的衍生物是____________分子中的_______________被______________________所取代的产物。含有相同官能团的有机物在性质上___________,因此我们可以根据有机物分子中________________的不同对有机物进行分类。
烃
氢原子
其他原子或原子团
相似
官能团的种类
2. 乙醇和乙酸都是烃的衍生物,其分子中的官能团分别是__________和__________。乙醇可以发生________反应生成乙醛,乙醛的官能团是_________。乙醇和乙酸在_________________条件下可以发生________反应生成乙酸乙醋,乙酸乙酷的官能团是__________。
羟基
羧基
氧化
醛基
浓硫酸、加热
酯化
酯基
3. 下列说法中正确的是 ( )。
A. 乙醇分子中有─OH基团,所以乙醇溶于水后溶液显碱性
B. 乙醇与钠反应可以产生氢气,所以乙醇溶于水后溶液显酸性
C. 乙醇在空气中燃烧生成二氧化碳和水,说明乙醇分子中含有C、H、O三种元素
D. 乙醇轻基中的氢原子比乙烷中的氢原子活泼
D
4.下列物质中不能用来鉴别乙醇和乙酸的是 ( )。
A.铁粉 B.溴水
C.碳酸钠溶液 D.紫色石蕊溶液
B
5. 46 g 某无色液体与足量钠完全反应,得到11.2L氢气 (标准状况),该物质可能是( )。
A. CH3COOH B. H2O
C. CH3COOC2H5 D. C2H5OH
D
6. 请描述下列物质与水混合并静置后的现象,结合该物质的性质进行解释。
①溴水 ② CH3CH2OH ③ CH3COOH
④ CCl4 ⑤ CH3COOC2H5 ⑥ C6H14
①溴水:分层,因澳是非极性分子,水是极性分子,两者互不相溶出现分层现象;
② CH3CH2OH:两者互,无明显现象,因CH3CH2OH与水分子间存在氢键;
③ CH3COOH:两者互溶,无明显现象,因CH3COOH与水分子间存在氢键;
④ CCl4:分层,因四氯化碳是非极性分子,水是极性分子,两者互不相溶;
⑤ CH3COOC2H5:分层,因酷不溶于水,密度小于水;
⑥ C6H14:分层,因烃不溶于水,密度小于水,油层在上层。
7. 30 g乙酸与46 g乙醇在一定条件下发生酷化反应,如果实际产率为68%,则可得到的乙酸乙酷的质量是多少
解:乙酸与乙醇发生醋化反应的化学方程式为:
CH3COOH+C2H5OH CH3COOC2H5+H2O
浓H2SO4
△
30g乙酸物质的量为 ═ 0.5mol,
46g乙醇物质的量为 ═ 1mol,
由此可46g/mol知反应中乙醇过量,根据乙酸物质的量计算生成乙酸乙酷的理论质量为:
0.5mol×88g/mol=44g,
实际产率为68%,则可得到乙酸乙醋的质量为:
44g×68%=29.92 g。
8. 写出下列物质间转化的化学方程式,并注明反应条件,分析转化过程中官能团与有机物类别的变化。
①
②
③
① CH2═CH2+H2O ────→ CH3CH2OH,
官能团碳碳双键转化为醇羟基,物质类别是烯烃转化为醇;
催化剂
①
②
③
② 2C2H5OH+O2 ───→ 2CH3CHO+2H2O,
官能团醇羟基转化为醛基,物质类别是醇转化为醛;
Cu
△
①
②
③
③ 2C2H5OH+C2H5OH CH3COOCH2CH3+H2O,
官能团醇羟基和羧基转化为酯基,醇与羧酸反应转化为酯。
浓H2SO4
△
9. 人们常说“酒是陈的香”,而有的酒在存放过程中却会变酸。请查阅资料,结合本节所学内容对上述现象进行解释。
有的酒在存放过程中,由于微生物的作用,少量的醇氧化成有机酸,酸与醇会发生酯化反应生成酯类物质,而酯类物质往往具有香味。
本课结束
This lesson is over
THANKS!
第七章
有机化合物
第三节
乙醇与乙酸
中国有历史悠久的酒文化!你能想到那些关于酒的诗句吗??
劝君更尽一杯酒,西出阳关无故人。
葡萄美酒夜光杯,欲饮琵琶马上催。
醉酒当歌,人生几何?
兰陵美酒夜光杯,欲饮琵琶马上催
白日放歌须纵酒,青春作伴好还乡。
绿蚁新醅酒,红泥小火炉。
人们很早就知道用粮食或水果发酵生产酒和醋。酒中含有的乙醇和醋中含有的乙酸是两种常见的有机化合物。
一
乙醇
早在几千年前,人类就掌握了发酵法酿酒的技术。
各种酒类都含有浓度不等的乙醇,故乙醇俗称酒精。
乙醇的物理性质
颜色状态:无色透明的液体
气味:特殊的香味
密度:比水小,200C时的密度是0.7893g/cm3
挥发性:沸点78℃,易挥发
溶解性:乙醇是一种重要的有机溶剂,能够溶解多种有机物和无机物,并能与水以任意比例互溶。
工业制备无水乙醇:加生石灰(CaO)蒸馏
乙醇的分子结构
分子式:C2H6O
结构式:
结构简式:
CH3CH2OH
或 C2H5OH
羟基
我们把 ─OH 原子团叫做羟基。乙醇可以看成是乙烷分子中的一个氢原子被羟基取代后的产物。我们把烃类物质侧链中的氢原子被羟基取代而成的化合物,叫做醇。
像这样,烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物成为烃的衍生物。比如前面学习的一氯甲烷、二氯甲烷、1,2─二溴乙烷都属于烃的衍生物。烃的衍生物和烃具有不同的性质。
1 . 乙醇与钠反应
【实验 7-4】
在盛有少量无水乙醇的试管中,加入一小块新切的用滤纸吸干表面煤油的钠,在试管口迅速塞上带尖嘴导管的橡胶塞。
用小试管收集气体并检验其纯度,然后点燃(如图7─19),再将干燥的小烧杯罩在火焰上,待烧杯壁上出现液滴后,迅速倒转烧杯,向其中加入少量澄清石灰水,观察现象,并与前面做过的水与钠反应的实验现象进行比较。
实验现象:钠与乙醇反应,沉入乙醇底部,仍为块状,没有声音,放出气泡,反应缓慢;产生的气体可在空气中安静地燃烧,烧壁上有水滴生成,烧杯中加入澄清的石灰水不变浑浊。说明产生的气体是H2
乙醇和钠的反应
与烷烃不同,乙醇由于分子中羟基的存在,可以与钠发生反应。在该反应中,钠置换了释基中的氢,生成了氢气和乙醇钠。
2CH3CH2OH +2Na → 2CH3CH2ONa +H2↑
乙醇钠
注意 ①断O-H键,发生置换反应、取代反应
②氢原子活泼性:酸>水>醇
③此反应可检验─OH的存在,用来计算分子中─OH的数目 (2个—OH产生1个H2,故物质的量之比为2∶1)
O—H 键断开
H H
| |
H— C — C — O —H
|
H
钠与水、与乙醇反应的现象比较
钠与水
钠是否浮在液面上
钠的形状是否变化
有无声音
有无气泡
剧烈程度
反应方程式
2Na+2H2O=2NaOH+H2↑
浮在水面
剧烈
有气泡产生
熔化
发出嘶嘶声
钠与乙醇
钠是否浮在液面上
钠的形状是否变化
有无声音
有无气泡
剧烈程度
反应方程式
有气泡产生
没有声音
不熔化
沉入底部
缓慢
2CH3CH2OH+2Na → 2CH3CH2ONa+H2↑
想一想:实验现象说明了什么问题
(1) 钠浮在水面上,而沉在乙醇中
(3) 钠与乙醇的反应速率比钠与水的反应速率慢,说明羟基上的H原子与水分子中H原子的活泼性:
(2) 乙醇与钠反应的性质是由它的什么决定的
[说明]
(1) 水的密度>钠的密度>乙醇的密度
(2) 羟基决定乙醇能和钠反应生成氢气
(3) 羟基中的H原子的活泼性:醇<水
官能团决定有机物的性质,连接官能团的其它部分对性质也有所影响。
官能团
乙醇和乙烷性质的不同,从分子结构分析,是因为取代氢原子的羟基对乙醇性质产生了影响。
像这样决定有机化合物特性的原子或原子团叫做官能团。
羟基是醇类物质的官能团,碳碳双键和碳碳三键分别是烯烃和炔烃的官能团。
常见官能团碳碳双键 C═C、碳碳三键 C≡C、羟基─OH、羧基 ─COOH、醛基 ─CHO、─Cl (卤素原子)等。
有机化学反应主要发生在官能团上,官能团对有机物的性质起决定作用。
提示
烃分子失去1个氢原子后所剩余的部分叫做烃基,可以用一R来表示。如 ─CH3叫甲基,─CH2CH3;叫乙基。烃的衍生物分子一般可以看成是烃基和官能团相互结合组成的。例如,乙醇分子可以看成是由乙基和轻基组成的:CH3CH2─┊─OH。
2. 氧化反应
乙醇在空气中燃烧时生成二氧化碳和水,同时放出大量的热。
2CO2 + 3H2O
C2H5OH + 3O2
点燃
现象:产生淡蓝色火焰,同时放出大量热。
在一定条件下,乙醇还能被氧化为其他产物。
酒精燃料飞机
酒精火锅
【实验 7-5】
向试管中加入少量乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼烧后插入乙醇,反复几次。注意观察反应现象,小心地闻试管中液体产生的气味。
a. 铜丝红色→黑色→红色反复变化
[实验现象]
b. 在试管口可以闻到刺激性气味
[思考] 铜丝在此实验中起什么作用?
催化剂
乙醇在加热和有催化剂 (如铜或银)存在等条件下可以被空气中的氧气氧化为乙醛 (CH3CHO)。
化学反应的方程式为:
(乙醇具有还原性)
2 CH3CH2OH +O2 2CH3CHO + 2H2O
Cu / Ag
乙醇
断键机理:
2CH3─C─O─H + O2 2CH3─C─H+2H2O
│
H
H
│
Cu / Ag
O
║
醇催化氧化的条件:羟基碳原子上必须有氢
反应历程
2 Cu+O2 ═══ 2CuO
CH3CH2OH + CuO Cu + CH3CHO + H2O
H H
| |
H— C — C══O
|
H 乙醛
CH3CHO结构中的 —CHO基团叫醛基,醛基由一个碳原子、一个氢原子及一个双键氧原子组成。
H H
| |
2R—C—O—H+O═O 2R—C══O+2H2O
|
H
醇催化氧化机理
醇发生催化氧化时去掉2个H原子。连接-OH官能团的碳原子上必须有H,才能发生催化氧化。
醛
Cu
△
乙醇被氧化为乙酸
乙醛的官能团是醛基( ─ C ─ H,或写作 ─ CHO),在适当条件下乙醛可以被氧气进一步氧化,生成乙醇(CH3COOH).
O
║
2CH3CH2OH + O2 2CH3CHO + 2H2O
Cu / Ag
乙醇被氧化为乙醛
乙醛接着可以被氧化为乙酸
2CH3CHO + O2 2CH3COOH
催化剂
也能被强氧化剂直接氧化为乙酸
乙醇还可以与酸性高酸钾溶液或酸性重铬酸钾(K2Cr2O7) 溶液反应,被氧化成乙酸。
CH3CH2OH CH3COOH
酸性高锰酸钾溶液
酸性重铬酸钾溶液
橙红 K2Cr2O7 溶液把乙醇氧化为乙酸,发生颜色变化
2K2Cr2O7 + 3CH3CH2OH +8H2SO4
2Cr2(SO4)3 +3CH3─C─OH+2K2SO4+11H2O
橙红色
蓝绿色
O║
K2Cr2O7
Cr2(SO4)3
(橙红色)
(蓝绿色)
乙醇
交警常用此原理检测司机是否酒后驾车。
乙醇发生反应的断键原理
乙醇分子中不同的化学键如图:
发生不同化学反应时乙醇的断键位置
(1)与活泼金属反应键________断裂
(2) CH3CH2OH 燃烧键________断裂
(3) 在Cu或Ag催化下和O2反应键________断裂
H
C
O
H
H
H
H
C
H
①
③
②
④
①
①③
全部
乙醇的用途
乙醇可用作燃料,还是重要的有机化工原料和溶剂用于生产医药、香料、化妆品、涂料等。医疗上常用75% (体积分数)的乙醇溶液作消毒剂。
消毒剂(75%的乙醇溶液)体积分数
医药
可以做燃料,提供能量
燃料
化工原料
饮料
可以做溶剂,提取多种有机物、无机物
工业
资料卡片~~~~~~~~~~~~~~~~~~~~~~~~~~~
酒类产品标签中的酒精度是指乙醇的体积分数,白酒一般在25%~68%,啤酒一般在3%~5%。乙醇进入人体后,会在肝中通过酶的催化作用被氧化为乙醛和乙酸,最终被氧化为二氧化碳和水。过量饮酒会加重肝负担,血液中较高浓度的乙醇和乙醛也会对人体产生毒害作用。
随堂练习
1.下列有关乙醇的物理性质的应用中不正确的是 ( )。
A.熟语“酒香不怕巷子深”是由于乙醇容易挥发
B.用乙醇提取中药的有效成分是由于乙醇能够溶解很多种有机物和无机物
C.酒厂可以勾兑各种浓度的酒是由于乙醇能够以任意比溶解于水
D.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
D
2、下列物质可使酸性高锰酸钾溶液褪色, 不能使溴水褪色的是( )
A、甲烷 B、乙烯 C、乙醇 D、乙烷
C
3. 比较乙烷和乙醇的结构,下列说法错误的是( )。
A. 两个分子中碳原子都以单键相连
B. 乙醇可以看成是乙烷分子中的一个氢原子被羟基取代后的产物
C. 分子里都含有6个相同的氢原子
D. 乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
C
4、能用来检验酒精中是否含有水的试剂是 ( )。
A、 CuSO4·5H2O B、CuSO4
C、 浓硫酸 D、金属钠
B
5. 将等质量的铜片放在酒精灯上加热后,分别插入下列溶液中,放置片刻,铜片质量增加的是( )。
A. 硝酸 B. 无水乙醇
C. 石灰水 D. 盐酸
C
二
乙酸
传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。
烧菜时放了一些,味道特别鲜美,便贮藏着
作为“调味酱”。故醋在古代又叫“苦酒”。
醋的来历?
食醋是生活中常见的调味品,其中含有3%~ 5%的乙酸,所以乙酸又被称为醋酸。
乙酸的物理性质
乙酸是有强烈刺激性气味的无色液体。
当温度低于熔点时,乙酸可凝结成类似冰的晶体所以纯净的乙酸又叫冰醋酸。
乙酸易溶于水和乙醇。
数据
乙酸
熔点:16.6 ℃
沸点:118 ℃
密度:1.05 g/cm3
(1) 乙酸的分子式:
(2) 结构式:
(3) 结构简式:
分子组成与结构
C2H4O2
CH3COOH
官能团为羧基
CH3 —C—OH
O
羧基可以表示为—COOH 或者
—C—OH
O
CH3 —C—OH
O
(4) 乙酸结构分析
甲基 和 羧基
受 C══O 的影响,氢氧键更易断
当氢氧键断裂时,容易解离出氢离子,使乙酸具有酸性。
1 . 酸性
乙酸的化学性质 (主要由羧基决定)
可以电离:CH3COOH CH3COO-+H+
使紫色石蕊试液变红。
乙酸是一种重要的有机酸,具有酸性 (弱酸性)。
可以和碱反应:
NaOH+CH3COOH ══ CH3COONa+H2O
可以和金属反应:
Mg+2CH3COOH ══ (CH3COO)2Mg+H2↑
Cu(OH)2+2CH3COOH ══ (CH3COO)2Cu+2H2O
思考与讨论
(1) 食醋可以清除水壶中的少量水垢 (主要成分是碳酸钙),这是利用了乙酸的什么性质 请写出相关反应的化学方程式。
CaCO3+2CH3COOH══ (CH3COO)2Ca+CO2↑+H2O
(除水垢)
CaCO3+2CH3COOH══2CH3COO─+Ca2++CO2↑+H2O
(2) 如何比较乙酸、碳酸、盐酸的酸性强弱?请查阅资料,与同学讨论,根据生活经验设计实验方案。
CaCO3+2CH3COOH ══ (CH3COO)2Ca+CO2↑+H2O
(除水垢)
HCl+CH3COONa ══ CH3COOH+NaCl
酸性: HCl>CH3COOH > H2CO3
以上2个反应能够进行,根据强酸制弱酸的原理
2. 酯化反应
在一支试管中加入3ml乙醇,然后边振荡试管边慢慢加入2ml浓硫酸和2ml乙酸,再加入几片碎瓷片。连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和Na2CO3溶液的液面上(如图7-22),观察现象。
【实验 7-6】
【实验现象】
饱和碳酸钠溶液的液面上有透明的油状液体,并可闻到香味。
先加乙醇 3mL
再加浓硫酸 2mL
再加乙酸 2mL
饱和的Na2CO3溶液收集
碎瓷片的作用是防止暴沸。
实验药品及其用量
实验的药品加入顺序
注意
乙醇和乙酸乙醋是常用的化工原料和有机溶剂。它们在储存时应置于密闭容器,存放在阴凉通风处,并与氧化剂、易燃物等分开存放,注意远离火种和热源。
在反应过程中,右侧试管内液体的上层有无色透明的油状液体产生,并可以闻到香味,这种有香味的液体是乙酸乙酯。
该反应的化学方程式为:
① 浓硫酸的作用?
② 饱和Na2CO3溶液的作用?
催化剂、吸水剂
中和乙酸
溶解乙酸乙酯中乙醇
降低乙酸乙酯在水中的溶解度
浓硫酸和饱和 Na2CO3 溶液的作用
③ 为什么导管不插入饱和Na2CO3溶液中?
防止受热不匀发生倒吸
酯化反应定义:酸跟醇起作用,生成酯和水的反应
实质:酸脱羟基、醇去氢(羟基上的)
酯化反应属于取代反应
酯化反应反应机理
CH3─C─OH+H─O─C2H5 CH3─C─O─C2H5+H2O
浓H2SO4
△
O
║
O
║
为了提高酯化反应的速率,一般需要加热,并加入浓硫酸等催化剂。
酯化反应是可逆反应,乙酸乙酯会与水发生水解反应生成乙酸和乙醇。
CH3COOH+HOC2H5 CH3COOC2H5+H2O
浓H2SO4
△
乙酸乙酯是酯类物质中的一种,其官能团是酯基 ( ,或写作─COOR)。
─C─O─R
O
║
很多鲜花和水果的香味都来自酯,如草莓中含有乙酸乙酯和乙酸异戊酯,苹果中含有戊酸戊酯。
这些分子中碳原子数较少、相对分子质量较小的低级酯具有一定的挥发性,有芳否气味,可用作饮料、糖果、化妆品中的香料和有机溶剂。
三
官能团与有机化合物的分类
通过对乙烯、乙醇和乙酸性质的学习,我们认识到官能团对有机物的性质具有决定作用,含有相同官能团的有机物在性质上具有相似之处。
因此我们可以根据有机物分子中所含官能团的不同,从结构和性质上对数量庞大的有机物进行分类 (如表7-2 )。
表7-2 常见的有机化合物类别、官能团和代表物
方法导引~~~~~~~~~~~~~~~~~~~~~~~~~~~
认识有机化合物的一般思路
认识一种有机物,可先从结构入手,分析其碳骨架和官能团,了解它所属的有机物类别;再结合这类有机物的一般性质推测该有机物可能具有的性质,并通过实验进行验证:在此基础上进一步了解该有机物的用途。
另外,还可以根据有机物发生的化学反应,了解其在有机物转化 (有机合成)中的作用。与认识无机物类似,认识有机物也体现了“结构决定性质”的观念各类有机物在结构和性质上具有的明显规律性,有助于我们更好地认识有机物。
乙酸的用途
随堂练习
1. 关于乙酸的下列说法中不正确的是 ( )
A. 乙酸易溶于水和乙醇
B. 无水乙酸又称冰醋酸,它是纯净物
C. 乙酸是一种重要的有机酸,是有刺激性气味的液体
D. 乙酸分子里有四个氢原子,所以不是一元酸
D
2、炒菜时,又加酒又加醋,可使菜变得香味可口,原因是( )。
A.有盐类物质生成 B.有酸类物质生成
C.有醇类物质生成 D.有酯类物质生成
D
3. 除去乙酸乙酯中含有的乙酸,最好的处理和操作是( )。
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
C
4.下列关于乙酸性质的叙述中,错误的是( )。
A. 乙酸的酸性比碳酸强,所以它可以与碳酸盐反应,产生CO2气体
B. 乙酸能与醇类物质发生酯化反应
C. 乙酸分子中含有碳氧双键,所以它能使溴水褪色
D. 乙酸在温度低于16.6℃时,就凝结成冰状晶体
C
5. 下列关于醋酸性质的叙述错误的是 ( )。
A. 醋酸是一种有强烈刺激性气味的无色液体
B. 冰醋酸是无水乙酸,不是乙酸的水溶液
C. 醋酸能跟碳酸钠溶液发生反应产生CO2
D. 在发生酯化反应时,醋酸分子中羟基中的氢原子跟醇分子中的羟基结合成水
D
6. 某有机物的结构为 它最不可能具有的性质是( )。
A. 能与金属钠反应放出H2
B. 既能与C2H5OH发生酯化反应也能与CH3COOH发生酯化反应
C. 能发生加聚反应
D. 水溶液能使紫色石蕊试纸变红
CH2─COOH
|
OH
C
练习与应用
1. 从结构上看,烃的衍生物是____________分子中的_______________被______________________所取代的产物。含有相同官能团的有机物在性质上___________,因此我们可以根据有机物分子中________________的不同对有机物进行分类。
烃
氢原子
其他原子或原子团
相似
官能团的种类
2. 乙醇和乙酸都是烃的衍生物,其分子中的官能团分别是__________和__________。乙醇可以发生________反应生成乙醛,乙醛的官能团是_________。乙醇和乙酸在_________________条件下可以发生________反应生成乙酸乙醋,乙酸乙酷的官能团是__________。
羟基
羧基
氧化
醛基
浓硫酸、加热
酯化
酯基
3. 下列说法中正确的是 ( )。
A. 乙醇分子中有─OH基团,所以乙醇溶于水后溶液显碱性
B. 乙醇与钠反应可以产生氢气,所以乙醇溶于水后溶液显酸性
C. 乙醇在空气中燃烧生成二氧化碳和水,说明乙醇分子中含有C、H、O三种元素
D. 乙醇轻基中的氢原子比乙烷中的氢原子活泼
D
4.下列物质中不能用来鉴别乙醇和乙酸的是 ( )。
A.铁粉 B.溴水
C.碳酸钠溶液 D.紫色石蕊溶液
B
5. 46 g 某无色液体与足量钠完全反应,得到11.2L氢气 (标准状况),该物质可能是( )。
A. CH3COOH B. H2O
C. CH3COOC2H5 D. C2H5OH
D
6. 请描述下列物质与水混合并静置后的现象,结合该物质的性质进行解释。
①溴水 ② CH3CH2OH ③ CH3COOH
④ CCl4 ⑤ CH3COOC2H5 ⑥ C6H14
①溴水:分层,因澳是非极性分子,水是极性分子,两者互不相溶出现分层现象;
② CH3CH2OH:两者互,无明显现象,因CH3CH2OH与水分子间存在氢键;
③ CH3COOH:两者互溶,无明显现象,因CH3COOH与水分子间存在氢键;
④ CCl4:分层,因四氯化碳是非极性分子,水是极性分子,两者互不相溶;
⑤ CH3COOC2H5:分层,因酷不溶于水,密度小于水;
⑥ C6H14:分层,因烃不溶于水,密度小于水,油层在上层。
7. 30 g乙酸与46 g乙醇在一定条件下发生酷化反应,如果实际产率为68%,则可得到的乙酸乙酷的质量是多少
解:乙酸与乙醇发生醋化反应的化学方程式为:
CH3COOH+C2H5OH CH3COOC2H5+H2O
浓H2SO4
△
30g乙酸物质的量为 ═ 0.5mol,
46g乙醇物质的量为 ═ 1mol,
由此可46g/mol知反应中乙醇过量,根据乙酸物质的量计算生成乙酸乙酷的理论质量为:
0.5mol×88g/mol=44g,
实际产率为68%,则可得到乙酸乙醋的质量为:
44g×68%=29.92 g。
8. 写出下列物质间转化的化学方程式,并注明反应条件,分析转化过程中官能团与有机物类别的变化。
①
②
③
① CH2═CH2+H2O ────→ CH3CH2OH,
官能团碳碳双键转化为醇羟基,物质类别是烯烃转化为醇;
催化剂
①
②
③
② 2C2H5OH+O2 ───→ 2CH3CHO+2H2O,
官能团醇羟基转化为醛基,物质类别是醇转化为醛;
Cu
△
①
②
③
③ 2C2H5OH+C2H5OH CH3COOCH2CH3+H2O,
官能团醇羟基和羧基转化为酯基,醇与羧酸反应转化为酯。
浓H2SO4
△
9. 人们常说“酒是陈的香”,而有的酒在存放过程中却会变酸。请查阅资料,结合本节所学内容对上述现象进行解释。
有的酒在存放过程中,由于微生物的作用,少量的醇氧化成有机酸,酸与醇会发生酯化反应生成酯类物质,而酯类物质往往具有香味。
本课结束
This lesson is over
THANKS!
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
