3.1.3 水的电离平衡 课件(共14张PPT)
文档属性
| 名称 | 3.1.3 水的电离平衡 课件(共14张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 437.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-23 00:00:00 | ||
图片预览






文档简介
(共14张PPT)
选 择 性 必 修 一
学
化
J
S
第一单元 弱电解质的电离平衡
3 水的电离平衡
水是生活中最常见也是最为重要的化合物。水是优良的溶剂,能溶解很多化合物。在水分子的作用下,自然界里存在的许多物质被溶解了,也就有了不同水质的水。其中有些物质在水中分散后能与其他物质接触发生化学反应,生成新的物质。不知你是否想过,作为溶剂的水,自身又有什么特征呢?
温故知新
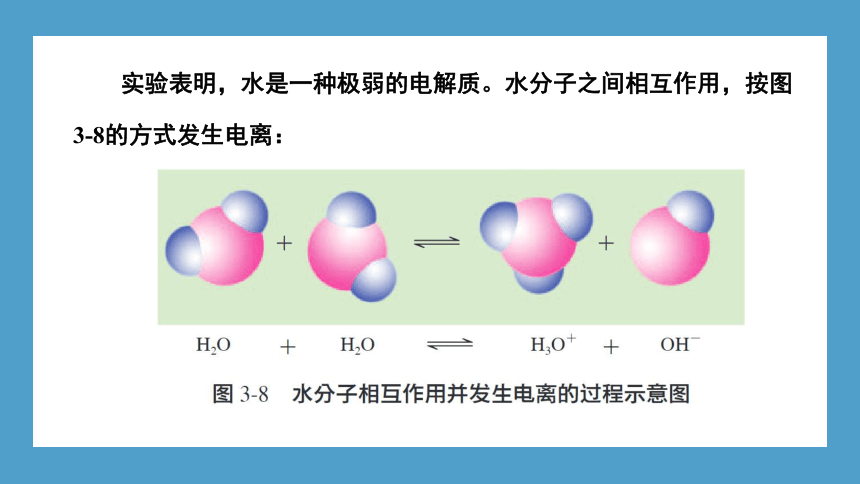
实验表明,水是一种极弱的电解质。水分子之间相互作用,按图3-8的方式发生电离:
水的电离方程式可简写为:
水的电离平衡常数可表示为:
在一定温度下,纯水和稀溶液中c(H2O)可视为一定值,因此有:
Kw称为水的离子积常数,简称水的离子积。实验测得,在25 °C时,Kw为1.0×10-14。水的离子积不仅适用于纯水,也适用于稀的电解质水溶液。
已知在25 °C时,水的离子积常数Kw=1.0×10-14;在50 °C时,Kw=5.5×10-14;在75 °C时,Kw=2.0×10-13;而在100 °C时 , Kw =5 . 6 × 1 0 - 1 3 。 常温下,水电离过程的焓变 H=57 kJ·mol-1,且近似认为该焓变不随温度发生变化。请你与同学讨论,不同温度下Kw值出现差异的原因。
交流讨论
我们知道,H+ 和 OH- 之间发生中和反应,伴随着放热。由此可知,水的电离过程是吸热的。根据化学平衡移动原理,升高温度会促使水的电离平衡向电离的方向移动,水的离子积常数也随之增大。
进一步研究表明,弱电解质的电离是一个吸热过程,因此,升高温度会促使电离平衡向电离的方向移动,电离平衡常数也随之增大。
已知在25 °C时,Kw=1.0×10-14;100 °C时,Kw=5.6×10-13。
若在100 °C时某溶液的c(H+)=1.0×10-7 mol·L-1,则该溶液呈酸性、中性还是碱性?请说明判断的依据。
学以致用
B
课堂训练
C
D
A
水的电离是吸热过程,温度低时,电离程度小,c(H+)、c(OH-)小
C
看
观
谢
谢
选 择 性 必 修 一
学
化
J
S
第一单元 弱电解质的电离平衡
3 水的电离平衡
水是生活中最常见也是最为重要的化合物。水是优良的溶剂,能溶解很多化合物。在水分子的作用下,自然界里存在的许多物质被溶解了,也就有了不同水质的水。其中有些物质在水中分散后能与其他物质接触发生化学反应,生成新的物质。不知你是否想过,作为溶剂的水,自身又有什么特征呢?
温故知新
实验表明,水是一种极弱的电解质。水分子之间相互作用,按图3-8的方式发生电离:
水的电离方程式可简写为:
水的电离平衡常数可表示为:
在一定温度下,纯水和稀溶液中c(H2O)可视为一定值,因此有:
Kw称为水的离子积常数,简称水的离子积。实验测得,在25 °C时,Kw为1.0×10-14。水的离子积不仅适用于纯水,也适用于稀的电解质水溶液。
已知在25 °C时,水的离子积常数Kw=1.0×10-14;在50 °C时,Kw=5.5×10-14;在75 °C时,Kw=2.0×10-13;而在100 °C时 , Kw =5 . 6 × 1 0 - 1 3 。 常温下,水电离过程的焓变 H=57 kJ·mol-1,且近似认为该焓变不随温度发生变化。请你与同学讨论,不同温度下Kw值出现差异的原因。
交流讨论
我们知道,H+ 和 OH- 之间发生中和反应,伴随着放热。由此可知,水的电离过程是吸热的。根据化学平衡移动原理,升高温度会促使水的电离平衡向电离的方向移动,水的离子积常数也随之增大。
进一步研究表明,弱电解质的电离是一个吸热过程,因此,升高温度会促使电离平衡向电离的方向移动,电离平衡常数也随之增大。
已知在25 °C时,Kw=1.0×10-14;100 °C时,Kw=5.6×10-13。
若在100 °C时某溶液的c(H+)=1.0×10-7 mol·L-1,则该溶液呈酸性、中性还是碱性?请说明判断的依据。
学以致用
B
课堂训练
C
D
A
水的电离是吸热过程,温度低时,电离程度小,c(H+)、c(OH-)小
C
看
观
谢
谢
