【高效课堂】人教A版(2019)高中化学必修2--6.2.1化学反应速率(教学课件)
文档属性
| 名称 | 【高效课堂】人教A版(2019)高中化学必修2--6.2.1化学反应速率(教学课件) |

|
|
| 格式 | pptx | ||
| 文件大小 | 68.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-21 00:00:00 | ||
图片预览











文档简介
(共30张PPT)
第六章
第二节 化学反应的速率和限度
第一课时 化学反应的速率
新人教版 化学 必修第二册
目录
01
02
化学反应速率
的影响因素
化学反应的速率
快慢差别很大的化学反应
爆炸
铁桥生锈
快慢差别很大的化学反应
牛奶变质
溶洞形成
01
一、化学反应的速率
内容内容内容
一、化学反应的速率
chemical reaction rate
快慢
1.含义
化学反应速率是用来描述化学反应______的物理量。
反应物浓度的减少量
生成物浓度的增加量
通常用单位时间内__________________或__________________来表示。
2.表示方法
均取正值
一、化学反应的速率
chemical reaction rate
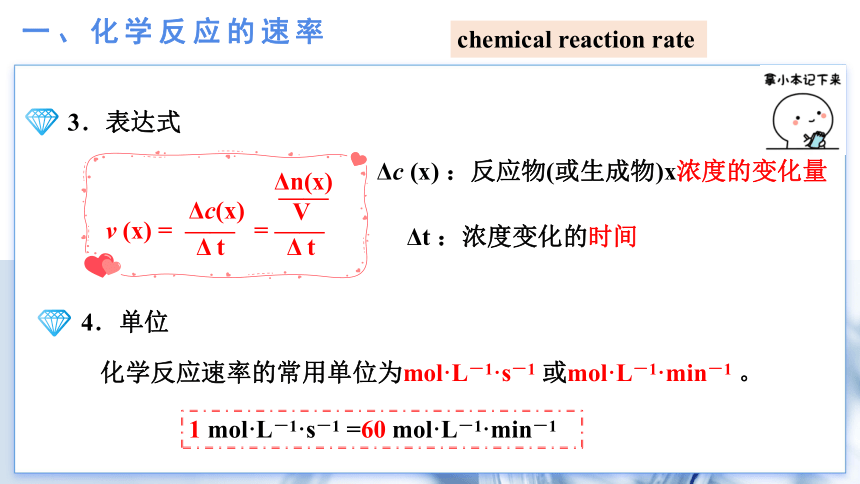
3.表达式
Δt :浓度变化的时间
Δc (x) :反应物(或生成物)x浓度的变化量
4.单位
化学反应速率的常用单位为mol·L-1·s-1 或mol·L-1·min-1 。
v (x) = —— = ——
Δc(x)
Δ t
Δ t
Δn(x)
V
——
1 mol·L-1·s-1 =60 mol·L-1·min-1
内容内容内容
一、化学反应的速率
chemical reaction rate
例
向4L容器中充入0.7moL SO2和0.4moL O2,在一定条件下反应,
4s末测得容器内剩余SO2 是0.3moL,求4s内SO2反应速率?
【解】υ (SO2) =
△n(SO2 )
V△t
=
(0.7 – 0.3) mol
4L×4s
= 0.025 mol/(L·s)
化学反应速率实际上是指某一段时间内化学反应的平均速率,而不是某一时刻的瞬时速率。
微提醒
内容内容内容
一、化学反应的速率
chemical reaction rate
例
v(O2)=0.0025 mol/(L·s)
v(NH3)=0.002 mol/(L·s)
v(NO)=0.002 mol/(L·s)
反应4NH3+5O2 = 4NO+6H2O 在5L的密闭容器中进行,
30秒后,NO的物质的量增加了0.3mol,此反应的平均反应速率为多少?分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示
同一反应的速率可用不同物质来表示,其数值可能不同,
但表示的意义相同,所以需要指明具体物质,如v(NO)
微提醒
不用固体或纯液体表示化学反应速率。
内容内容内容
一、化学反应的速率
chemical reaction rate
例
v(O2)=0.0025 mol/(L·s)
v(NH3)=0.002 mol/(L·s)
v(NO)=0.002 mol/(L·s)
反应4NH3+5O2 = 4NO+6H2O 在5L的密闭容器中进行,
30秒后,NO的物质的量增加了0.3mol,此反应的平均反应速率为多少?分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示
v(NO):v(O2):v(NH3)=
4:5:4
微提醒
化学反应速率之比=物质的量浓度的变化量之比
=物质的量的变化量之比=化学计量数之比。
内容内容内容
一、化学反应的速率
chemical reaction rate
微点拨
同一反应用不同的物质来表示速率,需要指明具体物质,如v(NO)。
化学反应速率指平均速率,不是瞬时速率。
不用固体或纯液体表示化学反应速率。
同一化学反应: aA+bB = cC+dD,
有v(A)︰v(B)︰v(C)︰v(D)=a︰b︰c︰d
化学反应速率之比=化学计量数之比
内容内容内容
一、化学反应的速率
chemical reaction rate
5.化学反应速率大小的比较方法
②换算成同一物质表示的反应速率,再比较数值的大小
归一法
①看单位是否统一,若不统一,换算成相同的单位
通过两幅图能判断出马和狗水跑的快吗?
内容内容内容
一、化学反应的速率
chemical reaction rate
则该反应速率的快慢顺序为:_____________________
【例】反应 A + 3B = 2C + 2D 在四种不同条件下的反应速率为:
(1)v(A)=0.3mol/(L·s )
(2) v(B)=0.6mol/(L·s)
(3) v(C)=0.4mol/(L·min)
(4) v(D)=0.45mol/(L·s)
(1)>(4)>(2)>(3)
v(C)=0.6mol/(L·s)
v(C)=0.4mol/(L·s)
v(C)=0.4/60 =0.0067mol/(L·s)
v(C)=0.45mol/(L·s)
01
二、化学反应速率的影响因素
二、化学反应速率的影响因素
1.探究催化剂对化学反应速率的影响
实验操作
实验现象
实验结论
②产生气泡的速率大于①
FeCl3能加快H2O2分解的反应速率
探究实验
影响化学反应速率的因素
2.探究温度对化学反应速率的影响
实验操作
试管中均为2~3 mL相同浓度的滴有FeCl3溶液的H2O2溶液
实验现象
实验结论
溶液中产生气泡速率的相对大小为①<②
其他条件不变时,温度升高,化学反应速率加快
②
探究实验
影响化学反应速率的因素
3.探究浓度对化学反应速率的影响
实验操作
实验现象
实验结论
装有1mol/L盐酸的试管中产生气泡快
增大反应物浓度能使反应速率加快
大理石碎块
0.1mol/L
盐酸
大理石碎块
1mol/L
盐酸
二、化学反应速率的影响因素
不同的化学反应,具有不同的反应速率,这说明化学反应速率的大小主要取决于 。
反应物本身的性质
1.内因
钠与水反应
镁与水反应
二、化学反应速率的影响因素
2.外因
浓度
增大反应物浓度
加快化学反应速率
减小反应物浓度
减慢化学反应速率
温度
升高温度
加快化学反应速率
降低温度
减慢化学反应速率
催化剂
多数情况下,使用催化剂能够加快化学反应速率
二、化学反应速率的影响因素
2.外因
压强
有气体参加的反应,改变压强对反应速率的影响实质是改变体积使反应物的浓度改变导致的。
(1)恒温时
体积缩小压强增大
浓度增大
反应速率加快
二、化学反应速率的影响因素
2.外因
压强
(2)恒容时
①充入气体反应物
浓度增大
反应速率加快
②充入惰性气体
总压强增大,各物质的浓度不变,反应速率不变
(注:此处惰性气体指不参加反应的气体)
(3)恒压时
充入惰性气体
体积增大
各反应物浓度减小
反应速率减慢
二、化学反应速率的影响因素
固体反应物表面积
在其他条件相同时,增大固体反应物的表面积,化学反应速率加快;减小固体反应物的表面积,化学反应速率减慢
形成原电池,使用合适的溶剂等也能影响化学反应的速率
其他
课堂检测
内容内容内容
10.下列反应属于放热反应的是
A.煅烧石灰石制生石灰 B.煤的气化制水煤气
课堂检测
B
1.将4 mol A和2 mol B在2 L的密闭容器中混合,并在一定条件下发生如下反应:2A(s)+B(g)=2C(g),反应2 s后测得C的浓度为0.6 mol·L-1。下列说法正确的是( )
A.用物质A表示2 s内的平均反应速率为0.3 mol·L-1·s-1
B.用物质B表示2 s内的平均反应速率为0.6 mol·L-1·s-1
C.2 s时v(C)=0.3 mol·L-1·s-1
D.2 s时物质B的浓度为0.7 mol·L-1
内容内容内容
10.下列反应属于放热反应的是
A.煅烧石灰石制生石灰 B.煤的气化制水煤气
课堂检测
D
2.在2A(g)+3B(g)===2C(g)+D(g)反应中,表示反应速率最快的是( )
A.v(A)=0.5 mol·L-1·min-1
B.v(B)=0.6 mol·L-1·min-1
C.v(C)=0.35 mol·L-1·min-1
D.v(D)=0.4 mol·L-1·min-1
内容内容内容
10.下列反应属于放热反应的是
A.煅烧石灰石制生石灰 B.煤的气化制水煤气
课堂检测
C
3.在2 L容积不变的容器中,发生N2(g)+3H2(g)? ?2NH3(g)的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol·L-1·s-1,则10 s时容器中N2的物质的量是( )
A.1.6 mol B.2.8 mol
C.3.2 mol D.3.6 mol
内容内容内容
10.下列反应属于放热反应的是
A.煅烧石灰石制生石灰 B.煤的气化制水煤气
课堂检测
C
4.用锌粒与2 mol·L-1的稀硫酸混合制备氢气时,若向其中分别再加入少量等体积的下列物质:①KCl溶液、②4 mol·L-1盐酸、③CuCl2溶液、④4 mol·L-1 CH3COONa溶液,则加入后反应生成氢气速率的大小顺序是( )
A.②>③>④>①
B.③>①>②>④
C.③>②>①>④
D.①>④>③>②
课堂总结
课堂总结
01
02
03
04
化学反应速率
化学反应速率
大小的比较方法
化学反应速率计算
化学反应影响因素
THANKS
THANKS
感谢观看
第六章
第二节 化学反应的速率和限度
第一课时 化学反应的速率
新人教版 化学 必修第二册
目录
01
02
化学反应速率
的影响因素
化学反应的速率
快慢差别很大的化学反应
爆炸
铁桥生锈
快慢差别很大的化学反应
牛奶变质
溶洞形成
01
一、化学反应的速率
内容内容内容
一、化学反应的速率
chemical reaction rate
快慢
1.含义
化学反应速率是用来描述化学反应______的物理量。
反应物浓度的减少量
生成物浓度的增加量
通常用单位时间内__________________或__________________来表示。
2.表示方法
均取正值
一、化学反应的速率
chemical reaction rate
3.表达式
Δt :浓度变化的时间
Δc (x) :反应物(或生成物)x浓度的变化量
4.单位
化学反应速率的常用单位为mol·L-1·s-1 或mol·L-1·min-1 。
v (x) = —— = ——
Δc(x)
Δ t
Δ t
Δn(x)
V
——
1 mol·L-1·s-1 =60 mol·L-1·min-1
内容内容内容
一、化学反应的速率
chemical reaction rate
例
向4L容器中充入0.7moL SO2和0.4moL O2,在一定条件下反应,
4s末测得容器内剩余SO2 是0.3moL,求4s内SO2反应速率?
【解】υ (SO2) =
△n(SO2 )
V△t
=
(0.7 – 0.3) mol
4L×4s
= 0.025 mol/(L·s)
化学反应速率实际上是指某一段时间内化学反应的平均速率,而不是某一时刻的瞬时速率。
微提醒
内容内容内容
一、化学反应的速率
chemical reaction rate
例
v(O2)=0.0025 mol/(L·s)
v(NH3)=0.002 mol/(L·s)
v(NO)=0.002 mol/(L·s)
反应4NH3+5O2 = 4NO+6H2O 在5L的密闭容器中进行,
30秒后,NO的物质的量增加了0.3mol,此反应的平均反应速率为多少?分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示
同一反应的速率可用不同物质来表示,其数值可能不同,
但表示的意义相同,所以需要指明具体物质,如v(NO)
微提醒
不用固体或纯液体表示化学反应速率。
内容内容内容
一、化学反应的速率
chemical reaction rate
例
v(O2)=0.0025 mol/(L·s)
v(NH3)=0.002 mol/(L·s)
v(NO)=0.002 mol/(L·s)
反应4NH3+5O2 = 4NO+6H2O 在5L的密闭容器中进行,
30秒后,NO的物质的量增加了0.3mol,此反应的平均反应速率为多少?分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示
v(NO):v(O2):v(NH3)=
4:5:4
微提醒
化学反应速率之比=物质的量浓度的变化量之比
=物质的量的变化量之比=化学计量数之比。
内容内容内容
一、化学反应的速率
chemical reaction rate
微点拨
同一反应用不同的物质来表示速率,需要指明具体物质,如v(NO)。
化学反应速率指平均速率,不是瞬时速率。
不用固体或纯液体表示化学反应速率。
同一化学反应: aA+bB = cC+dD,
有v(A)︰v(B)︰v(C)︰v(D)=a︰b︰c︰d
化学反应速率之比=化学计量数之比
内容内容内容
一、化学反应的速率
chemical reaction rate
5.化学反应速率大小的比较方法
②换算成同一物质表示的反应速率,再比较数值的大小
归一法
①看单位是否统一,若不统一,换算成相同的单位
通过两幅图能判断出马和狗水跑的快吗?
内容内容内容
一、化学反应的速率
chemical reaction rate
则该反应速率的快慢顺序为:_____________________
【例】反应 A + 3B = 2C + 2D 在四种不同条件下的反应速率为:
(1)v(A)=0.3mol/(L·s )
(2) v(B)=0.6mol/(L·s)
(3) v(C)=0.4mol/(L·min)
(4) v(D)=0.45mol/(L·s)
(1)>(4)>(2)>(3)
v(C)=0.6mol/(L·s)
v(C)=0.4mol/(L·s)
v(C)=0.4/60 =0.0067mol/(L·s)
v(C)=0.45mol/(L·s)
01
二、化学反应速率的影响因素
二、化学反应速率的影响因素
1.探究催化剂对化学反应速率的影响
实验操作
实验现象
实验结论
②产生气泡的速率大于①
FeCl3能加快H2O2分解的反应速率
探究实验
影响化学反应速率的因素
2.探究温度对化学反应速率的影响
实验操作
试管中均为2~3 mL相同浓度的滴有FeCl3溶液的H2O2溶液
实验现象
实验结论
溶液中产生气泡速率的相对大小为①<②
其他条件不变时,温度升高,化学反应速率加快
②
探究实验
影响化学反应速率的因素
3.探究浓度对化学反应速率的影响
实验操作
实验现象
实验结论
装有1mol/L盐酸的试管中产生气泡快
增大反应物浓度能使反应速率加快
大理石碎块
0.1mol/L
盐酸
大理石碎块
1mol/L
盐酸
二、化学反应速率的影响因素
不同的化学反应,具有不同的反应速率,这说明化学反应速率的大小主要取决于 。
反应物本身的性质
1.内因
钠与水反应
镁与水反应
二、化学反应速率的影响因素
2.外因
浓度
增大反应物浓度
加快化学反应速率
减小反应物浓度
减慢化学反应速率
温度
升高温度
加快化学反应速率
降低温度
减慢化学反应速率
催化剂
多数情况下,使用催化剂能够加快化学反应速率
二、化学反应速率的影响因素
2.外因
压强
有气体参加的反应,改变压强对反应速率的影响实质是改变体积使反应物的浓度改变导致的。
(1)恒温时
体积缩小压强增大
浓度增大
反应速率加快
二、化学反应速率的影响因素
2.外因
压强
(2)恒容时
①充入气体反应物
浓度增大
反应速率加快
②充入惰性气体
总压强增大,各物质的浓度不变,反应速率不变
(注:此处惰性气体指不参加反应的气体)
(3)恒压时
充入惰性气体
体积增大
各反应物浓度减小
反应速率减慢
二、化学反应速率的影响因素
固体反应物表面积
在其他条件相同时,增大固体反应物的表面积,化学反应速率加快;减小固体反应物的表面积,化学反应速率减慢
形成原电池,使用合适的溶剂等也能影响化学反应的速率
其他
课堂检测
内容内容内容
10.下列反应属于放热反应的是
A.煅烧石灰石制生石灰 B.煤的气化制水煤气
课堂检测
B
1.将4 mol A和2 mol B在2 L的密闭容器中混合,并在一定条件下发生如下反应:2A(s)+B(g)=2C(g),反应2 s后测得C的浓度为0.6 mol·L-1。下列说法正确的是( )
A.用物质A表示2 s内的平均反应速率为0.3 mol·L-1·s-1
B.用物质B表示2 s内的平均反应速率为0.6 mol·L-1·s-1
C.2 s时v(C)=0.3 mol·L-1·s-1
D.2 s时物质B的浓度为0.7 mol·L-1
内容内容内容
10.下列反应属于放热反应的是
A.煅烧石灰石制生石灰 B.煤的气化制水煤气
课堂检测
D
2.在2A(g)+3B(g)===2C(g)+D(g)反应中,表示反应速率最快的是( )
A.v(A)=0.5 mol·L-1·min-1
B.v(B)=0.6 mol·L-1·min-1
C.v(C)=0.35 mol·L-1·min-1
D.v(D)=0.4 mol·L-1·min-1
内容内容内容
10.下列反应属于放热反应的是
A.煅烧石灰石制生石灰 B.煤的气化制水煤气
课堂检测
C
3.在2 L容积不变的容器中,发生N2(g)+3H2(g)? ?2NH3(g)的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol·L-1·s-1,则10 s时容器中N2的物质的量是( )
A.1.6 mol B.2.8 mol
C.3.2 mol D.3.6 mol
内容内容内容
10.下列反应属于放热反应的是
A.煅烧石灰石制生石灰 B.煤的气化制水煤气
课堂检测
C
4.用锌粒与2 mol·L-1的稀硫酸混合制备氢气时,若向其中分别再加入少量等体积的下列物质:①KCl溶液、②4 mol·L-1盐酸、③CuCl2溶液、④4 mol·L-1 CH3COONa溶液,则加入后反应生成氢气速率的大小顺序是( )
A.②>③>④>①
B.③>①>②>④
C.③>②>①>④
D.①>④>③>②
课堂总结
课堂总结
01
02
03
04
化学反应速率
化学反应速率
大小的比较方法
化学反应速率计算
化学反应影响因素
THANKS
THANKS
感谢观看
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
