河南省九师联盟2023-2024学年高一下学期6月质量检测试题 化学(含解析)
文档属性
| 名称 | 河南省九师联盟2023-2024学年高一下学期6月质量检测试题 化学(含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 604.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-23 00:00:00 | ||
图片预览





文档简介
九师联盟2023~2024学年高一教学质量检测
化 学
可能用到的相对原子质量:
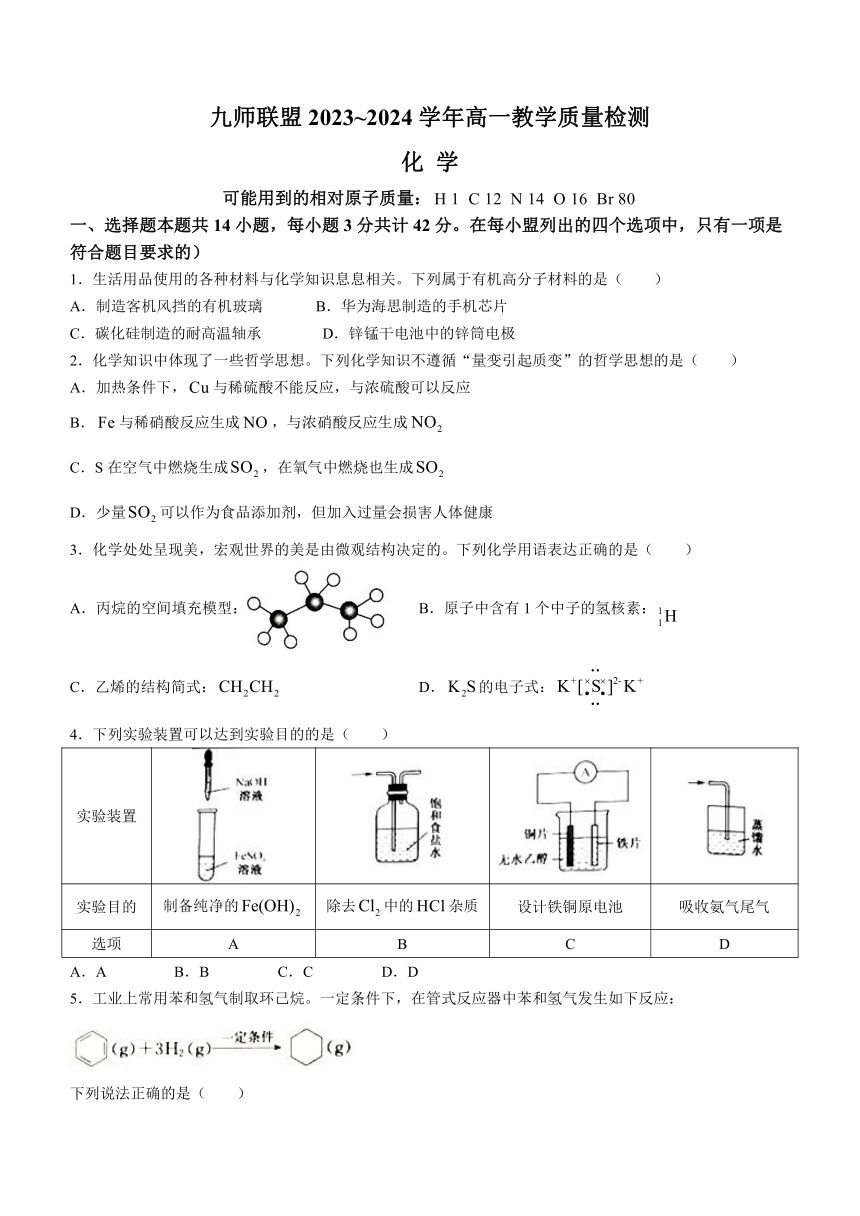
一、选择题本题共14小题,每小题3分共计42分。在每小盟列出的四个选项中,只有一项是符合题目要求的)
1.生活用品使用的各种材料与化学知识息息相关。下列属于有机高分子材料的是( )
A.制造客机风挡的有机玻璃 B.华为海思制造的手机芯片
C.碳化硅制造的耐高温轴承 D.锌锰干电池中的锌筒电极
2.化学知识中体现了一些哲学思想。下列化学知识不遵循“量变引起质变”的哲学思想的是( )
A.加热条件下,与稀硫酸不能反应,与浓硫酸可以反应
B.与稀硝酸反应生成,与浓硝酸反应生成
C.S在空气中燃烧生成,在氧气中燃烧也生成
D.少量可以作为食品添加剂,但加入过量会损害人体健康
3.化学处处呈现美,宏观世界的美是由微观结构决定的。下列化学用语表达正确的是( )
A.丙烷的空间填充模型: B.原子中含有1个中子的氢核素:
C.乙烯的结构简式: D.的电子式:
4.下列实验装置可以达到实验目的的是( )
实验装置
实验目的 制备纯净的 除去中的杂质 设计铁铜原电池 吸收氨气尾气
选项 A B C D
A.A B.B C.C D.D
5.工业上常用苯和氢气制取环己烷。一定条件下,在管式反应器中苯和氢气发生如下反应:
下列说法正确的是( )
A.该反应属于取代反应 B.苯中含有碳碳双键,可以发生加聚反应
C.环己烷的分子式为 D.苯分子中所有原子均在同一平面内
6.天然气制氢气是工业制氢气的主要方法之一。在一定温度下,向恒容密闭的催化反应器中充入和,发生反应。下列说法正确的是( )
A.反应过程中一定存在
B.反应过程中有键断裂的同时一定有键断裂
C.当时,可以判断反应已经达到平衡状态
D.当时,可以判断反应已经达到平衡状态
7.我国传统饮食文化中包含丰富的化学知识。下列说法中错误的是( )
A.“柴米油盐酱醋茶”所代表物质中的主要成分均是有机物
B.“青梅煮酒”是因为酒中的乙醇可以溶解青梅中含有香味的有机物
C.食用油可以看作是高级脂肪酸与甘油形成的酯类化合物
D.煎蛋时,蛋清变为白色固体是因为蛋白质发生了变性
8.下图是工业生产中除去电石渣浆(含在反应中提供碱性环境)中的并制取硫酸盐的一种工艺流程。下列说法正确的是( )
A.碱性条件下,氧化性:
B.过程I发生反应的离子方程式为
C.利用上述流程处理,理论上需要消耗(标准状况)
D.制得硫酸盐中的硫酸钙可以用于制作石膏绷带
9.在适当条件下,正丁烷(g)可以转化为异丁烷(g),转化过程中能量变化关系如图所示。下列说法中错误的是( )
A.该反应是放热反应
B.正丁烷和异丁烷互为同分异构体
C.适当降低反应温度可以加快放热反应进行的速率
D.等质量的正丁烷(g)和异丁烷(g)完全燃烧放出的热量:正丁烷>异丁烷
10.在指定条件下,下列选项所示的含氮物质间转化不能一步实现的是( )
A. B.
C. D.
11.阿托酸甲酯能用于治疗肠道疾病,它可由阿托酸经过下列反应合成:
下列说法错误的是( )
A.阿托酸可以使溴的四氯化碳溶液褪色
B.该反应有生成
C.阿托酸和阿托酸甲酯分子中均只含有一种官能团
D.可以使用饱和溶液鉴别阿托酸和阿托酸甲酯
12.X、Y、Z、W是原子序数依次增大的短周期主族元素。只有Y、Z、W三种元素位于同一周期,Y是形成有机物必不可少的元素,W的一种氢化物为常用消毒剂。下列说法中错误的是( )
A.原子半径: B.Y的氢化物常温下均为气态
C.最简单气态氢化物的热稳定性: D.分子中含有极性键和非极性键
13.根据下列实验操作和现象得出的实验结论正确的是( )
选项 实验操作和现象 实验结论
A 向淀粉溶液中加入适量稀硫酸,静置一段时间后,加入刚配制好的银氨溶液,水浴加热后没有固体生成,再滴加几滴碘水,溶液变为蓝色 淀粉未发生水解
B 向某溶液中加入盐酸酸化的溶液,有白色固体生成 该溶液中一定含有
C 将通入溶液中,无明显现象,再向溶液中通入气体X,产生白色沉淀 气体X一定具有强氧化性
D 用洁净的铂丝蘸取某溶液后,放在酒精灯上灼烧,焰色为黄色 该溶液中一定含有钠元素
A.A B.B C.C D.D
14.一种衍生的。共掺杂微状作为正极和作为负极的水系锌离子电池工作原理如图所示。已知:在金属活动性顺序表中,锰、锌、钴的活动性依次减弱。下列叙述正确的是( )
A.电势:a电极B.放电时,电流由b极经外电路流向a极
C.若用溶液替代溶液,该电池仍然正常工作
D.负极电极反应式为
二、非选择题(本题共4小题,共58分)
15.(14分)为响应党的二十大重要精神,将经济建设与环境保护的工作合二为一,黄铁矿(主要成分是,还有少量等杂质)冶铁时产生的大量废气在工业上进一步回收利用的工艺流程如下图:
回答下列问题:
(1)“煅烧”时,将空气从黄铁矿底部通入的目的是______________________;写出该反应生成的化学方程式:______________________。
(2)“高炉炼铁”时,加入石灰石的作用是与反应生成硅酸盐从而形成炉渣,用氧化物的形式()可以表示为______________________。
(3)“氧化1”得到的气体中仍然混有、,且延长反应时间气体中、的含量不变,原因是_________________________________;“吸收”时,要用浓硫酸吸收而不是用,主要原因是_________________________________。
(4)在“吸收塔”中,和吸收发生反应的离子方程式为_________________________________;“氧化2”得到理论上需要通入___________(假设该状态下的摩尔体积为,用含的式子表示)。
16.(15分)一种高分子功能材料W的合成路线如下图所示:
回答下列问题:
(1)有机物A~W中属于烃的是___________(填字母)。
(2)有机物E的分子式为,其结构简式为______________________。
(3)写出E→F反应的化学方程式:_________________________________。
(4)有机物G中的官能团名称为___________;某兴趣小组将铜丝在酒精灯上灼烧变黑后,快速伸入取样后的有机物G中,可以观察到的现象是_________________________________,且试管中的液体有刺激性气味:产生刺激性气味的原因是_________________________________。
(5)有机物G转化为高分子化合物W的过程可以看作G分子与G分子不断发生酯化反应的过程,2个G分子在浓硫酸、加热的条件下脱去1个分子形成的酯为___________(填结构简式)。
(6)下列说法正确的是___________(填序号)。
①A与C含有官能团的种类和数目完全相同,A与C互为同系物
②D的同分异构体中,含有苯环且与D官能团相同的有3种
③高分子化合物W不宜与强酸或者强碱长时间接触
④有机物B既可以使酸性高锰酸钾溶液褪色又可以使溴的四氯化碳溶液褪色
17.(14分)利用还原可以有效缓解大气污染。实验室研究烟气(含、、等)脱硝的实验装置如下图:
回答下列问题:
(1)装置A为制备氨气的发生装置,可选择下列装置。
①若选浓氨水,加热制备少量氨气,应选择装置___________(填序号)。
②若选择装置Ⅱ,则选择的药品是___________(填名称)。
③若选择氯化铵、熟石灰制备氨气,则选择的装置是___________(填序号);写出该反应的化学方程式:______________________。
(2)装置D中溶液可以吸收未除尽的尾气,与、反应生成的离子方程式为_________________________________。
(3)若烟气中含有少量,会生成堵塞催化剂孔道。写出该反应的化学方程式:_________________________________。
(4)将烟气中的体积分数检测后,再经过装置C气体检测测得的转化率随反应温度变化的曲线如图所示。
温度高于时,的转化率经降低为负值,其可能原因是______________________。
18.(15分)、的资源化利用是当今化学研究的热点之一。回答下列问题:
(1)由和转化为高附加值产品的催化反应历程如图所示:
①该历程总反应的化学方程式为_________________________________。
②a→b时,___________(填“放出”或“吸收”)能量并形成了C-C键,加入催化剂时反应速率___________(填“增大”“减小”或“不变”)。
(2)可充电电池结构如图所示,实现了再利用。研究发现正极电极产物有熔融碳酸盐和碳,则负极为___________(填“a”或“b”,下同)极。放电时,该电池中K向___________极移动。
(3)某温度下,将和分别充入和的两个刚性容器中,发生反应:,实验测得的体积分数随时间变化如图所示:
①反应进行到b点时,反应速率___________。
②a点处,的平衡转化率__________。
③下列说法中可以判断反应已经达到平衡状态的是___________(填字母)。
A.容器中气体的平均相对分子质量不变 B.容器中的体积分数不变
C.容器中压强不变 D.容器中气体的密度不变
九师联盟2023~2024学年高一教学质量检测·化学
参考答案、提示及评分细则
1.A 有机玻璃属于有机高分子材料,A项正确;手机芯片是高纯硅,和碳化硅同样属于无机非金属材料,B、C两项错误;锌筒电极属于金属材料,D项错误。
2.C 不论氧气是否过量,S与反应均生成,C项不符合题意。
3.D 丙烷的结构简式为,C的原子半径大于H,其球棍模型为,A项错误;原子中含有1个中子的氢核素:,B项错误;结构简式不能省略碳碳双键,C项错误;为离子化合物,的电子式为,D项正确。
4.B 制备纯净的必须隔绝,A项错误;用饱和食盐水吸收气体且不吸收,B项正确;缺少电解质溶液,C项错误;氨气必须防倒吸,D项错误。
5.D 该反应属于加成反应,A项错误;苯中不含碳碳双键,B项错误;环己烷的分子式为,C项错误;苯分子中所有原子均在同一平面内,D项正确。
6.B 反应过程中一定存在,A项错误;反应过程中有键断裂的同时一定有键断裂,B项正确;当时,可以判断反应已经达到平衡状态,C项错误;物质的量关系不能作为判断平衡状态的标准,D项错误。
7.A 盐的主要成分是,不是有机物,A项错误;乙醇可以溶解有机物,B项正确;油可以看作是高级脂肪酸和甘油形成的酯,C项正确;高温可以使蛋白质变性,D项正确。
8.D 根据过程I可以判断,碱性条件下,氧化性:,A项错误;碱性条件下不应该加配平电荷,B项错误;该流程将最终转化为,失去的电子最终都是由得到,因此理论上需要消耗(标准状况),C项错误;制得硫酸盐中的硫酸钙可以用于制作石膏绷带,D项正确。
9.C 根据能量变化判断该反应是放热反应,A项正确;正丁烷和异丁烷互为同分异构体,B项正确;降低温度可以促进放热反应进行,但是反应速率会变慢,C项错误;完全燃烧时正丁烷(g)放出的热量比异丁烷(g)更多,D项正确。
10.C ,A项不符合题意;,B项不符合题意;,C项符合题意;,D项不符合题意。
11.C 阿托酸中含有碳碳双键,可以使溴的四氯化碳溶液褪色,A项正确;该反应是酯化反应,还有生成,B项正确;阿托酸中含有碳碳双键和羧基,阿托酸甲酯中含有碳碳双键和酯基,C项错误;羧基具有酸性,可以与溶液反应生成气体,而酯基不能,D项正确。
12.B 由题干信息可知,X、Y、Z、W依次为H、C、N、O。原子半径:,A项正确;当C原子个数大于4时,其氢化物常温下太多不再是气态,B项错误;最简单气态氢化物的热稳定性:,C项正确;分子中既含有极性键,又含有非极性键,D项正确。
13.D 银镜反应检验葡萄糖必须先调节溶液H至碱性,A项错误;该溶液中还可能含有,B项错误;气体X还可以是氨气,生成白色沉淀为,C项错误;钠元素的焰色为黄色,D项正确。
14.D 依题意,a电极为正极,b电极为负极,正极电势高于负极电势,A项错误;电池放电时,电流由正极经外电路流向负极,B项错误;根据金属活动性顺序知,锌不能与硫酸锰反应,若用硫酸锰溶液替代硫酸钴溶液,电池反应不能自发进行,即使发生金属腐蚀也不能持续产生电流,无法正常工作,C项错误;a极电极反应式为,b极电极反应式为,D项正确。
15.(1)使黄铁矿与空气充分接触,加快反应速率,提高原料利用率;,
(2)
(3)与的反应是可逆反应,且反应已达到平衡状态;极易溶于水且与水发生剧烈反应,生成硫酸酸雾,吸收效率低
(4);(或,每空2分)
16.(1)B(1分)
(2)(2分)
(3)(2分)
(4)羟基、羧基;铜丝由黑色变为红色;有机物G中的羟基被氧化,产生了醛类物质(各2分)
(5)(2分)
(6)②③④(2分,少选得1分)
17.(1)①I ②生石灰(或氢氧化钠)、浓氨水 ③Ⅲ:
(2)
(3)
(4)在温度高于时与反应,生成氮氧化物的量大于脱硝去除的量(每空2分)
18.(1)①(2分,将“”写为“”也正确)
②放出;增大(各2分)
(2)a;b(各1分)
(3)①(2分) ②37.5(3分) ③ABC(2分)
化 学
可能用到的相对原子质量:
一、选择题本题共14小题,每小题3分共计42分。在每小盟列出的四个选项中,只有一项是符合题目要求的)
1.生活用品使用的各种材料与化学知识息息相关。下列属于有机高分子材料的是( )
A.制造客机风挡的有机玻璃 B.华为海思制造的手机芯片
C.碳化硅制造的耐高温轴承 D.锌锰干电池中的锌筒电极
2.化学知识中体现了一些哲学思想。下列化学知识不遵循“量变引起质变”的哲学思想的是( )
A.加热条件下,与稀硫酸不能反应,与浓硫酸可以反应
B.与稀硝酸反应生成,与浓硝酸反应生成
C.S在空气中燃烧生成,在氧气中燃烧也生成
D.少量可以作为食品添加剂,但加入过量会损害人体健康
3.化学处处呈现美,宏观世界的美是由微观结构决定的。下列化学用语表达正确的是( )
A.丙烷的空间填充模型: B.原子中含有1个中子的氢核素:
C.乙烯的结构简式: D.的电子式:
4.下列实验装置可以达到实验目的的是( )
实验装置
实验目的 制备纯净的 除去中的杂质 设计铁铜原电池 吸收氨气尾气
选项 A B C D
A.A B.B C.C D.D
5.工业上常用苯和氢气制取环己烷。一定条件下,在管式反应器中苯和氢气发生如下反应:
下列说法正确的是( )
A.该反应属于取代反应 B.苯中含有碳碳双键,可以发生加聚反应
C.环己烷的分子式为 D.苯分子中所有原子均在同一平面内
6.天然气制氢气是工业制氢气的主要方法之一。在一定温度下,向恒容密闭的催化反应器中充入和,发生反应。下列说法正确的是( )
A.反应过程中一定存在
B.反应过程中有键断裂的同时一定有键断裂
C.当时,可以判断反应已经达到平衡状态
D.当时,可以判断反应已经达到平衡状态
7.我国传统饮食文化中包含丰富的化学知识。下列说法中错误的是( )
A.“柴米油盐酱醋茶”所代表物质中的主要成分均是有机物
B.“青梅煮酒”是因为酒中的乙醇可以溶解青梅中含有香味的有机物
C.食用油可以看作是高级脂肪酸与甘油形成的酯类化合物
D.煎蛋时,蛋清变为白色固体是因为蛋白质发生了变性
8.下图是工业生产中除去电石渣浆(含在反应中提供碱性环境)中的并制取硫酸盐的一种工艺流程。下列说法正确的是( )
A.碱性条件下,氧化性:
B.过程I发生反应的离子方程式为
C.利用上述流程处理,理论上需要消耗(标准状况)
D.制得硫酸盐中的硫酸钙可以用于制作石膏绷带
9.在适当条件下,正丁烷(g)可以转化为异丁烷(g),转化过程中能量变化关系如图所示。下列说法中错误的是( )
A.该反应是放热反应
B.正丁烷和异丁烷互为同分异构体
C.适当降低反应温度可以加快放热反应进行的速率
D.等质量的正丁烷(g)和异丁烷(g)完全燃烧放出的热量:正丁烷>异丁烷
10.在指定条件下,下列选项所示的含氮物质间转化不能一步实现的是( )
A. B.
C. D.
11.阿托酸甲酯能用于治疗肠道疾病,它可由阿托酸经过下列反应合成:
下列说法错误的是( )
A.阿托酸可以使溴的四氯化碳溶液褪色
B.该反应有生成
C.阿托酸和阿托酸甲酯分子中均只含有一种官能团
D.可以使用饱和溶液鉴别阿托酸和阿托酸甲酯
12.X、Y、Z、W是原子序数依次增大的短周期主族元素。只有Y、Z、W三种元素位于同一周期,Y是形成有机物必不可少的元素,W的一种氢化物为常用消毒剂。下列说法中错误的是( )
A.原子半径: B.Y的氢化物常温下均为气态
C.最简单气态氢化物的热稳定性: D.分子中含有极性键和非极性键
13.根据下列实验操作和现象得出的实验结论正确的是( )
选项 实验操作和现象 实验结论
A 向淀粉溶液中加入适量稀硫酸,静置一段时间后,加入刚配制好的银氨溶液,水浴加热后没有固体生成,再滴加几滴碘水,溶液变为蓝色 淀粉未发生水解
B 向某溶液中加入盐酸酸化的溶液,有白色固体生成 该溶液中一定含有
C 将通入溶液中,无明显现象,再向溶液中通入气体X,产生白色沉淀 气体X一定具有强氧化性
D 用洁净的铂丝蘸取某溶液后,放在酒精灯上灼烧,焰色为黄色 该溶液中一定含有钠元素
A.A B.B C.C D.D
14.一种衍生的。共掺杂微状作为正极和作为负极的水系锌离子电池工作原理如图所示。已知:在金属活动性顺序表中,锰、锌、钴的活动性依次减弱。下列叙述正确的是( )
A.电势:a电极
C.若用溶液替代溶液,该电池仍然正常工作
D.负极电极反应式为
二、非选择题(本题共4小题,共58分)
15.(14分)为响应党的二十大重要精神,将经济建设与环境保护的工作合二为一,黄铁矿(主要成分是,还有少量等杂质)冶铁时产生的大量废气在工业上进一步回收利用的工艺流程如下图:
回答下列问题:
(1)“煅烧”时,将空气从黄铁矿底部通入的目的是______________________;写出该反应生成的化学方程式:______________________。
(2)“高炉炼铁”时,加入石灰石的作用是与反应生成硅酸盐从而形成炉渣,用氧化物的形式()可以表示为______________________。
(3)“氧化1”得到的气体中仍然混有、,且延长反应时间气体中、的含量不变,原因是_________________________________;“吸收”时,要用浓硫酸吸收而不是用,主要原因是_________________________________。
(4)在“吸收塔”中,和吸收发生反应的离子方程式为_________________________________;“氧化2”得到理论上需要通入___________(假设该状态下的摩尔体积为,用含的式子表示)。
16.(15分)一种高分子功能材料W的合成路线如下图所示:
回答下列问题:
(1)有机物A~W中属于烃的是___________(填字母)。
(2)有机物E的分子式为,其结构简式为______________________。
(3)写出E→F反应的化学方程式:_________________________________。
(4)有机物G中的官能团名称为___________;某兴趣小组将铜丝在酒精灯上灼烧变黑后,快速伸入取样后的有机物G中,可以观察到的现象是_________________________________,且试管中的液体有刺激性气味:产生刺激性气味的原因是_________________________________。
(5)有机物G转化为高分子化合物W的过程可以看作G分子与G分子不断发生酯化反应的过程,2个G分子在浓硫酸、加热的条件下脱去1个分子形成的酯为___________(填结构简式)。
(6)下列说法正确的是___________(填序号)。
①A与C含有官能团的种类和数目完全相同,A与C互为同系物
②D的同分异构体中,含有苯环且与D官能团相同的有3种
③高分子化合物W不宜与强酸或者强碱长时间接触
④有机物B既可以使酸性高锰酸钾溶液褪色又可以使溴的四氯化碳溶液褪色
17.(14分)利用还原可以有效缓解大气污染。实验室研究烟气(含、、等)脱硝的实验装置如下图:
回答下列问题:
(1)装置A为制备氨气的发生装置,可选择下列装置。
①若选浓氨水,加热制备少量氨气,应选择装置___________(填序号)。
②若选择装置Ⅱ,则选择的药品是___________(填名称)。
③若选择氯化铵、熟石灰制备氨气,则选择的装置是___________(填序号);写出该反应的化学方程式:______________________。
(2)装置D中溶液可以吸收未除尽的尾气,与、反应生成的离子方程式为_________________________________。
(3)若烟气中含有少量,会生成堵塞催化剂孔道。写出该反应的化学方程式:_________________________________。
(4)将烟气中的体积分数检测后,再经过装置C气体检测测得的转化率随反应温度变化的曲线如图所示。
温度高于时,的转化率经降低为负值,其可能原因是______________________。
18.(15分)、的资源化利用是当今化学研究的热点之一。回答下列问题:
(1)由和转化为高附加值产品的催化反应历程如图所示:
①该历程总反应的化学方程式为_________________________________。
②a→b时,___________(填“放出”或“吸收”)能量并形成了C-C键,加入催化剂时反应速率___________(填“增大”“减小”或“不变”)。
(2)可充电电池结构如图所示,实现了再利用。研究发现正极电极产物有熔融碳酸盐和碳,则负极为___________(填“a”或“b”,下同)极。放电时,该电池中K向___________极移动。
(3)某温度下,将和分别充入和的两个刚性容器中,发生反应:,实验测得的体积分数随时间变化如图所示:
①反应进行到b点时,反应速率___________。
②a点处,的平衡转化率__________。
③下列说法中可以判断反应已经达到平衡状态的是___________(填字母)。
A.容器中气体的平均相对分子质量不变 B.容器中的体积分数不变
C.容器中压强不变 D.容器中气体的密度不变
九师联盟2023~2024学年高一教学质量检测·化学
参考答案、提示及评分细则
1.A 有机玻璃属于有机高分子材料,A项正确;手机芯片是高纯硅,和碳化硅同样属于无机非金属材料,B、C两项错误;锌筒电极属于金属材料,D项错误。
2.C 不论氧气是否过量,S与反应均生成,C项不符合题意。
3.D 丙烷的结构简式为,C的原子半径大于H,其球棍模型为,A项错误;原子中含有1个中子的氢核素:,B项错误;结构简式不能省略碳碳双键,C项错误;为离子化合物,的电子式为,D项正确。
4.B 制备纯净的必须隔绝,A项错误;用饱和食盐水吸收气体且不吸收,B项正确;缺少电解质溶液,C项错误;氨气必须防倒吸,D项错误。
5.D 该反应属于加成反应,A项错误;苯中不含碳碳双键,B项错误;环己烷的分子式为,C项错误;苯分子中所有原子均在同一平面内,D项正确。
6.B 反应过程中一定存在,A项错误;反应过程中有键断裂的同时一定有键断裂,B项正确;当时,可以判断反应已经达到平衡状态,C项错误;物质的量关系不能作为判断平衡状态的标准,D项错误。
7.A 盐的主要成分是,不是有机物,A项错误;乙醇可以溶解有机物,B项正确;油可以看作是高级脂肪酸和甘油形成的酯,C项正确;高温可以使蛋白质变性,D项正确。
8.D 根据过程I可以判断,碱性条件下,氧化性:,A项错误;碱性条件下不应该加配平电荷,B项错误;该流程将最终转化为,失去的电子最终都是由得到,因此理论上需要消耗(标准状况),C项错误;制得硫酸盐中的硫酸钙可以用于制作石膏绷带,D项正确。
9.C 根据能量变化判断该反应是放热反应,A项正确;正丁烷和异丁烷互为同分异构体,B项正确;降低温度可以促进放热反应进行,但是反应速率会变慢,C项错误;完全燃烧时正丁烷(g)放出的热量比异丁烷(g)更多,D项正确。
10.C ,A项不符合题意;,B项不符合题意;,C项符合题意;,D项不符合题意。
11.C 阿托酸中含有碳碳双键,可以使溴的四氯化碳溶液褪色,A项正确;该反应是酯化反应,还有生成,B项正确;阿托酸中含有碳碳双键和羧基,阿托酸甲酯中含有碳碳双键和酯基,C项错误;羧基具有酸性,可以与溶液反应生成气体,而酯基不能,D项正确。
12.B 由题干信息可知,X、Y、Z、W依次为H、C、N、O。原子半径:,A项正确;当C原子个数大于4时,其氢化物常温下太多不再是气态,B项错误;最简单气态氢化物的热稳定性:,C项正确;分子中既含有极性键,又含有非极性键,D项正确。
13.D 银镜反应检验葡萄糖必须先调节溶液H至碱性,A项错误;该溶液中还可能含有,B项错误;气体X还可以是氨气,生成白色沉淀为,C项错误;钠元素的焰色为黄色,D项正确。
14.D 依题意,a电极为正极,b电极为负极,正极电势高于负极电势,A项错误;电池放电时,电流由正极经外电路流向负极,B项错误;根据金属活动性顺序知,锌不能与硫酸锰反应,若用硫酸锰溶液替代硫酸钴溶液,电池反应不能自发进行,即使发生金属腐蚀也不能持续产生电流,无法正常工作,C项错误;a极电极反应式为,b极电极反应式为,D项正确。
15.(1)使黄铁矿与空气充分接触,加快反应速率,提高原料利用率;,
(2)
(3)与的反应是可逆反应,且反应已达到平衡状态;极易溶于水且与水发生剧烈反应,生成硫酸酸雾,吸收效率低
(4);(或,每空2分)
16.(1)B(1分)
(2)(2分)
(3)(2分)
(4)羟基、羧基;铜丝由黑色变为红色;有机物G中的羟基被氧化,产生了醛类物质(各2分)
(5)(2分)
(6)②③④(2分,少选得1分)
17.(1)①I ②生石灰(或氢氧化钠)、浓氨水 ③Ⅲ:
(2)
(3)
(4)在温度高于时与反应,生成氮氧化物的量大于脱硝去除的量(每空2分)
18.(1)①(2分,将“”写为“”也正确)
②放出;增大(各2分)
(2)a;b(各1分)
(3)①(2分) ②37.5(3分) ③ABC(2分)
同课章节目录
