专题24金属的电化学腐蚀与防护--2025年高三化学一轮复习【专题专练】(含解析)
文档属性
| 名称 | 专题24金属的电化学腐蚀与防护--2025年高三化学一轮复习【专题专练】(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-27 09:31:38 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
专题24金属的电化学腐蚀与防护--2025年高三化学一轮复习【专题专练】(含解析)
1.下列事实中涉及的反应与氧化还原无关的是
A.用溶液吸收
B.利用铜与浓硫酸加热反应制取
C.乙醇使紫色酸性溶液褪色
D.在船体上镶嵌锌块,可以减缓船体被海水腐蚀
2.化学与生产、生活、社会密切相关。下列有关说法正确的是
A.制白砂糖时用活性炭脱色属于化学变化
B.杭州亚运会使用的运动场地防滑涂层——石墨烯属于有机高分子材料
C.港珠澳大桥使用高性能富锌底漆防腐,依据的是外加电流的保护法
D.北京冬奥会采用氢能源汽车代替燃油车,有利于“碳达峰”、“碳中和”战略的实施
3.在西汉刘安组织编撰的《淮南万毕术》中,有“曾青得铁则化为铜”的记载。下列说法错误的是
A.这个反应是湿法冶金的基础,冶金过程中金属元素都发生还原反应
B.铁表面镀锌可以增强其抗腐蚀性
C.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
D.还原铁粉可以在食品包装袋内做脱氧剂
4.劳动是人生存发展的必要技能,下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 制作豆腐:将少量石石膏投入大豆研磨过滤后的溶液中 蛋白质发生聚沉而凝固
B 家庭自制肥皂:食用油和食用碱在一定条件混合 油脂在碱性条件下水解
C 餐具保存:擦干已洗净铁锅表面的水,以防生锈 防止潮湿环境下发生化学腐蚀
D 泳池消毒:用漂粉精作游泳池的消毒剂 漂粉精有强氧化性,可用于杀菌
A.A B.B C.C D.D
5.2024年5月8日,我国第三艘航空母舰福建舰顺利完成首次海试。舰体表面需要采取有效的防锈措施,下列防锈措施中不形成表面钝化膜的是
A.发蓝处理 B.阳极氧化 C.表面渗镀 D.喷涂油漆
6.“挖掘文物价值,讲好中国故事。”下列文物在潮湿空气中易发生电化学腐蚀的是
A.先锋煲(陶) B.曜变天目碗(瓷)
C.铁足大铜鼎 D.六棱柱形水晶穿珠
A.A B.B C.C D.D
7.下列对文中加点内容所做说明错误的是
A.帘外芭蕉惹骤雨,门环惹铜绿——金属的吸氧腐蚀
B.蒸熟谷粒酒中潜,廿日珍存变为酸——葡萄糖的水解
C.玉梅雪柳千家闹,火树银花十里开——焰色试验
D.白胎烧就彩虹来,五色成窑画作开——颜料的氧化还原反应
8.化学与生产、生活、社会密切相关。下列有关说法中正确的是
A.使用乙醇汽油可以减少汽车尾气中氮氧化物的排放
B.实施海底封存,需要将进行液化,液化过程中的共价键被破坏
C.“深海一号”母船海水浸泡区的铝基可保障船体不易腐蚀
D.飞船操纵杆的材料碳纤维与石墨烯互为同素异形体
9.下列离子方程式正确的是
A.用硫化钠溶液除去废水中的汞离子:
B.与水反应:
C.钢铁发生吸氧腐蚀,正极反应:
D.向溶液中加入少量:
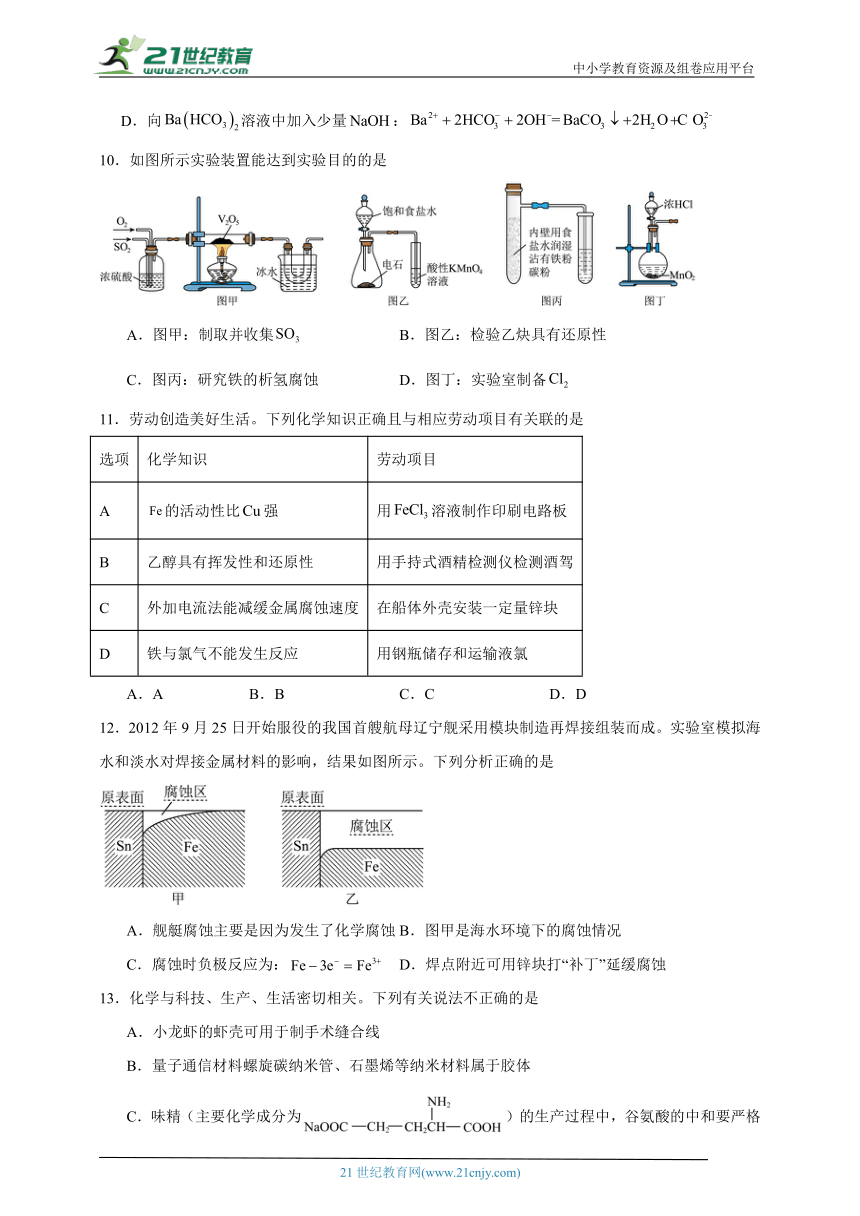
10.如图所示实验装置能达到实验目的的是
A.图甲:制取并收集 B.图乙:检验乙炔具有还原性
C.图丙:研究铁的析氢腐蚀 D.图丁:实验室制备
11.劳动创造美好生活。下列化学知识正确且与相应劳动项目有关联的是
选项 化学知识 劳动项目
A 的活动性比强 用溶液制作印刷电路板
B 乙醇具有挥发性和还原性 用手持式酒精检测仪检测酒驾
C 外加电流法能减缓金属腐蚀速度 在船体外壳安装一定量锌块
D 铁与氯气不能发生反应 用钢瓶储存和运输液氯
A.A B.B C.C D.D
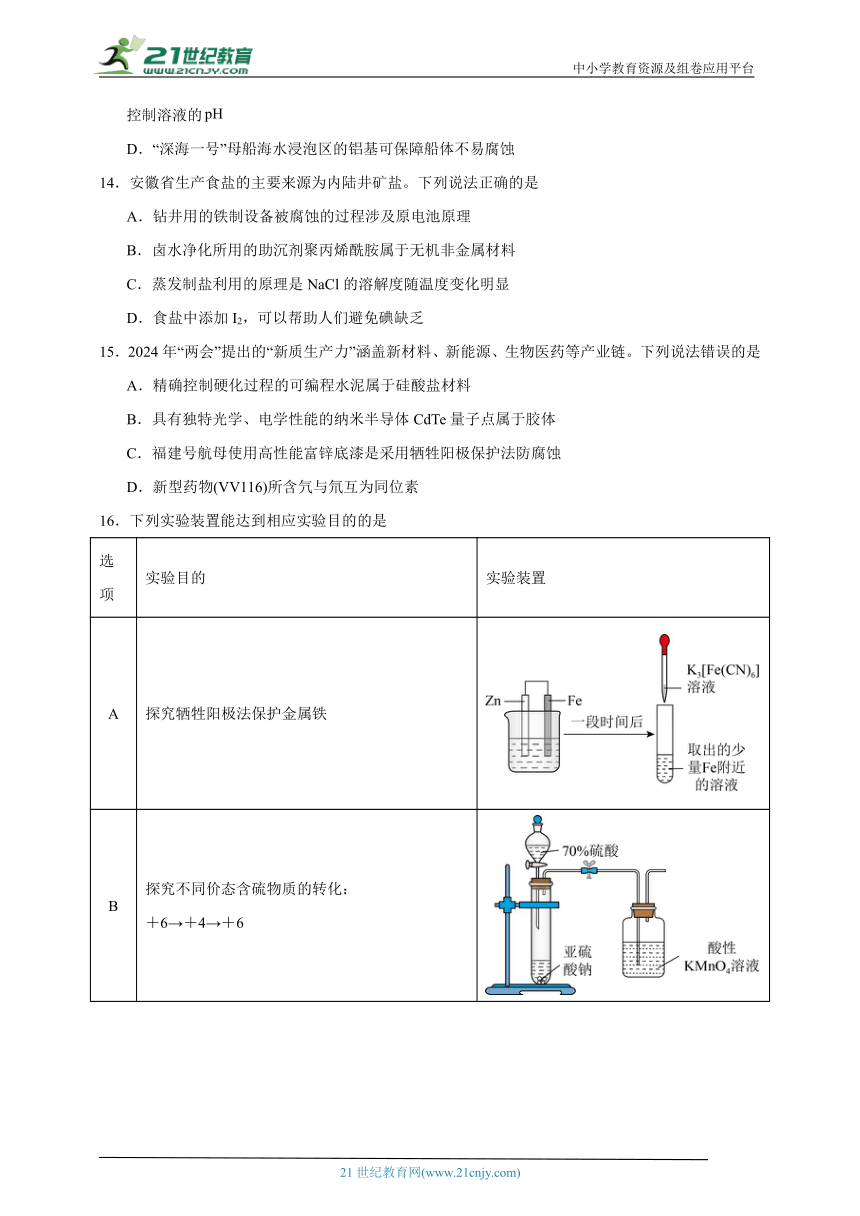
12.2012年9月25日开始服役的我国首艘航母辽宁舰采用模块制造再焊接组装而成。实验室模拟海水和淡水对焊接金属材料的影响,结果如图所示。下列分析正确的是
A.舰艇腐蚀主要是因为发生了化学腐蚀 B.图甲是海水环境下的腐蚀情况
C.腐蚀时负极反应为: D.焊点附近可用锌块打“补丁”延缓腐蚀
13.化学与科技、生产、生活密切相关。下列有关说法不正确的是
A.小龙虾的虾壳可用于制手术缝合线
B.量子通信材料螺旋碳纳米管、石墨烯等纳米材料属于胶体
C.味精(主要化学成分为)的生产过程中,谷氨酸的中和要严格控制溶液的
D.“深海一号”母船海水浸泡区的铝基可保障船体不易腐蚀
14.安徽省生产食盐的主要来源为内陆井矿盐。下列说法正确的是
A.钻井用的铁制设备被腐蚀的过程涉及原电池原理
B.卤水净化所用的助沉剂聚丙烯酰胺属于无机非金属材料
C.蒸发制盐利用的原理是NaCl的溶解度随温度变化明显
D.食盐中添加I2,可以帮助人们避免碘缺乏
15.2024年“两会”提出的“新质生产力”涵盖新材料、新能源、生物医药等产业链。下列说法错误的是
A.精确控制硬化过程的可编程水泥属于硅酸盐材料
B.具有独特光学、电学性能的纳米半导体CdTe量子点属于胶体
C.福建号航母使用高性能富锌底漆是采用牺牲阳极保护法防腐蚀
D.新型药物(VV116)所含氕与氘互为同位素
16.下列实验装置能达到相应实验目的的是
选项 实验目的 实验装置
A 探究牺牲阳极法保护金属铁
B 探究不同价态含硫物质的转化: +6→+4→+6
C 探究、对与反应速率的影响
D 探究用标准酸性溶液测定葡萄酒中的含量
A.A B.B C.C D.D
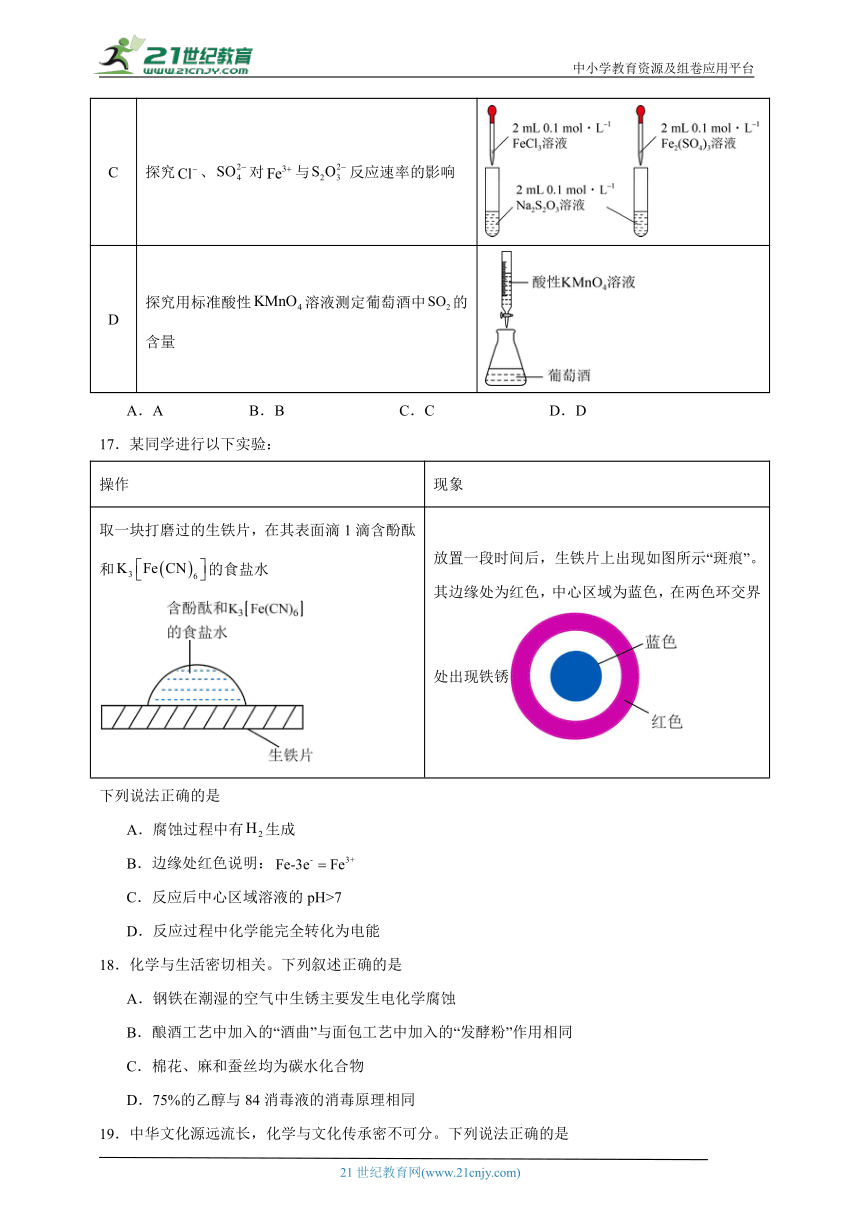
17.某同学进行以下实验:
操作 现象
取一块打磨过的生铁片,在其表面滴1滴含酚酞和的食盐水 放置一段时间后,生铁片上出现如图所示“斑痕”。其边缘处为红色,中心区域为蓝色,在两色环交界处出现铁锈
下列说法正确的是
A.腐蚀过程中有生成
B.边缘处红色说明:
C.反应后中心区域溶液的pH>7
D.反应过程中化学能完全转化为电能
18.化学与生活密切相关。下列叙述正确的是
A.钢铁在潮湿的空气中生锈主要发生电化学腐蚀
B.酿酒工艺中加入的“酒曲”与面包工艺中加入的“发酵粉”作用相同
C.棉花、麻和蚕丝均为碳水化合物
D.75%的乙醇与84消毒液的消毒原理相同
19.中华文化源远流长,化学与文化传承密不可分。下列说法正确的是
A.清朱耷芦雁轴纸本的主要成分是淀粉,淀粉为高分子化合物
B.四千余年前用谷物酿造出酒和醋,酿造过程中只发生水解反应
C.《本草纲目》“烧酒”条目写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”叙述了“蒸馏”技术在古代酿酒工艺中的应用
D.广汉三星堆出土的青铜面具呈红棕色斑迹,是由于铜发生了吸氧腐蚀
20.下列实验装置或操作不能达到实验目的的是
A B
检验否沉淀完全 提纯含有少量氯化钠和泥沙的苯甲酸
C D
牺牲阳极法保护铁 易溶于水且溶液呈碱性
A.A B.B C.C D.D
21.秦始皇陵是我国历史上规模最大的帝王陵墓,秦始皇陵兵马俑被誉为“世界第八大奇迹”,考古发现并出土了大量竹简、兵马俑、钱币、石甲胄等珍贵文物,下列说法错误的是
A.竹简密封保存,并充以氮气,可延缓其降解
B.陶制兵马俑的烧制过程涉及化学变化
C.铜制钱币比铁制钱币的耐腐蚀性更强
D.石甲胄的主要成分为合金
22.化学学科有独特的符号表达。下列叙述正确的是
A.将Cl2通入冷的石灰乳中制备漂白粉的离子方程式:
B.牺牲阳极法保护钢铁的正极反应式:
C.工业上人工固氮的化学方程式:
D.CH4(g)燃烧热的热化学方程式:
23.对下列实验装置、操作或目的理解正确的是
A.不能制取NH3,因为收集方式有误 B.将浓硫酸加入到容量瓶中,再加水稀释,可得稀硫酸
C.不能保护铁件,会发生吸氧腐蚀加快铁件的损耗 D.可以收集NO,因为NO密度比空气小
A.A B.B C.C D.D
24.物质都有两面性。下列说法错误的是
A.稀甲醛溶液浸泡种子能消毒杀菌;浸泡蔬菜保鲜会危害人体健康
B.聚氯乙烯塑料可用于油炸食品包装;随意弃置会造成“白色污染”
C.亚硝酸钠抑制微生物生长、抗氧化,可用作食品添加剂;摄入过量会造成中毒
D.适当的碳含量可增加钢铁的硬度及耐磨性;过量的碳会导致钢铁腐蚀加剧
25.化学与科学、技术、社会、生活等密切相关。下列有关说法正确的是
A.用于清洗伤口、杀菌、消毒的医用酒精有强氧化性
B.在日常生活中, 造成钢铁腐蚀的主要原因是化学腐蚀
C.直馏汽油、裂化汽油、植物油均能使 的四氯化碳溶液褪色
D.可以用热的纯碱溶液来清洗油污
26.铁是现代社会应用最广泛的金属,下列关于铁及其化合物的说法正确的是
A.河道出海口的钢铁闸门往往镶嵌锌块,利用牺牲阴极保护法
B.四氧化三铁具有磁性,可用作录音磁带和电讯器材的原材料
C.保暖贴是利用铁粉与空气中氧气发生化学腐蚀而发热的原理
D.野外铁路抢修作业用高温下铁粉与氧化铝的反应来焊接铁轨
27.利用下列实验装置进行实验,操作正确且能达到实验目的的是
A.用装置甲蒸干溶液制无水晶体 B.用装置乙证明乙炔可使溴水褪色
C.用装置丙制备固体 D.用装置丁验证铁钉吸氧腐蚀
28.下列离子方程式书写不正确的是
A.向AlCl3溶液中滴加少量氨水产生白色沉淀:Al3++3OH-=Al(OH)3↓
B.铁钉在潮湿空气中生锈的负极反应:Fe-2e-=Fe2+
C.CuSO4溶液与闪锌矿(ZnS)反应生成铜蓝(CuS):Cu2+(aq)+ZnS(s)CuS(s)+Zn2+(aq)
D.向FeBr2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl-
29.青少年帮厨既可培养劳动习惯,也能将化学知识应用于实践。下列有关解释合理的是
A.清洗铁锅后及时擦干,能减缓铁锅因发生吸氧腐蚀而生锈
B.烹煮食物的后期加入食盐,能避免长时间受热而分解
C.将白糖熬制成焦糖汁,利用蔗糖高温下充分炭化为食物增色
D.制作面点时加入食用纯碱,利用中和发酵过程产生的酸
30.下图所示装置不能达到目的的是
A.用图甲装置制备乙酸乙酯
B.用图乙装置制备硫酸四氨合铜晶体
C.用图丙装置制备检验醛基用的
D.用图丁装置保护钢铁设备
参考答案:
1.A
【详解】A.溶液吸收生成碳酸钠和水,无元素化合价改变,与氧化还原无关,A符合题意;
B.生成二氧化硫,硫元素化合价改变,属于氧化还原反应,B不符合题意;
C.高锰酸钾具有强氧化性,和乙醇发生氧化还原反应而使得溶液褪色,C不符合题意;
D.锌比铁活泼,在船体上镶嵌锌块避免船体遭受腐蚀的原理是牺牲阳极法安装活泼金属做原电池负极,被保护的钢铁做正极,与氧化还原反应有关,D不符合题意;
故选A。
2.D
【详解】A.制白砂糖时用活性炭脱色为活性炭的吸附作用,属于物理变化,A错误;
B.石墨烯为碳单质,不属于有机高分子材,B错误;
C.港珠澳大桥使用高性能富锌底漆防腐,锌作负极保护铁,依据的是牺牲阳极法,C错误;
D.采用氢能源汽车代替燃油车,减少CO2的产生和排放,有利于“碳达峰、碳中和”,D正确;
故选D。
3.A
【详解】A.这个反应是湿法冶金的基础,冶金过程中铜元素化合价降低、硫酸铜发生还原反应,铁元素化合价升高、铁发生氧化反应,A错误;
B. 铁表面镀锌隔绝了空气和水分,可以增强金属的抗腐蚀性,即使镀层破损,锌可为原电池负极、利用牺牲阳极的阴极保护法保护作为正极的铁不被腐蚀,B正确;
C.明矾水解溶液呈酸性,能与铜锈的成分碱式碳酸铜反应使其溶解,但不与铜反应,则中国古代利用明矾溶液的酸性清除铜镜表面的铜锈,C正确;
D. 还原铁粉具有还原性、可以在食品包装袋内做脱氧剂,D正确;
答案选A。
4.C
【详解】A.大豆研磨过滤后的溶液中含有大量蛋白质,轻金属盐溶液可以使蛋白质胶体聚沉,故可以用于制作豆腐,故A不选;
B.食用油是多种高级脂肪酸甘油酯的混合物,食用碱的为碳酸钠,水解后溶液显碱性。高级脂肪酸甘油酯在碱的作用下发生水解生成高级脂肪酸钠和甘油,高级脂肪酸钠是肥皂的主要成分,故可以用食用油和食用碱在一定条件下混合制肥皂,故B不选;
C.擦干已洗净铁锅表面的水,可以防止潮湿环境下铁锅发生电化学腐蚀,不是化学腐蚀,故C选;
D.漂粉精的有效成分为次氯酸钙,次氯酸钙可以水解为有强氧化性的次氯酸,从而可以用于泳池消毒,故D不选;
故选C。
5.D
【详解】A.发蓝处理技术通常用于钢铁等黑色金属,通过在空气中加热或直接浸泡于浓氧化性溶液中来实现,可在金属表面形成一层极薄的氧化膜,这层氧化膜能有效防锈,A不符合题意;
B.阳极氧化是将待保护的金属与电源正极连接,在金属表面形成一层氧化膜的过程,B不符合题意;
C.表面渗镀是在高温下将气态、固态或熔化状态的欲渗镀的物质(金属或非金属元素)通过扩散作用从被渗镀的金属的表面渗入内部以形成表层合金镀层的一种表面处理的方法,C不符合题意;
D.喷涂油漆是将油漆涂在待保护的金属表面并没有在表面形成钝化膜,D符合题意;
故答案选D。
6.C
【详解】先锋煲、曜变天目碗、六棱柱形水晶穿珠的主要成分都是无机非金属材料,而铁足大铜鼎的主要成分是金属材料,所以铁足大铜鼎在潮湿空气中易发生电化学腐蚀被损耗,故选C。
7.B
【详解】A.铜的吸氧腐蚀生成铜绿的电极反应是一种常见的化学变化,它涉及到铜在氧气的存在下腐蚀生成铜绿的过程,A正确;
B.葡萄糖为单糖,不能水解,B错误;
C.火树银花十里开,描述的是烟花,烟花与焰色试验有关,C正确;
D.白胎烧就彩虹来,颜料在灼烧下发生氧化还原反应,产生颜色变化,D正确;
故选B。
8.C
【详解】A.高温下空气中的氮气和氧气反应生成NO,NO与氧气反应生成,则乙醇汽油的使用不能减少汽车尾气中氮氧化物的排放,A错误;
B.二氧化碳是分子晶体,所以二氧化碳液化时,只改变分子间的作用力,不破坏分子内的共价键,B错误;
C.“深海一号”母船海水浸泡区的铝基作负极可以与船体形成原电池,利用“牺牲阳极的阴极保护法”可保障船体不易腐蚀,C正确;
D.碳纤维是一种复合材料,属于混合物,与石墨烯不互为同素异形体,D错误;
故选C。
9.C
【详解】A.用硫化钠溶液除去废水中的汞离子,离子方程式为Hg2++S2-=HgS↓,A错误;
B.Cl2与水反应生成的HClO为弱电解质,不能拆成离子的形式,离子方程式为Cl2+H2OCl-+H++HClO,B错误;
C.钢铁发生吸氧腐蚀,正极上氧气得电子结合水生成氢氧根离子,离子方程式正确,C正确;
D.向碳酸氢钡溶液中滴加少量NaOH,反应的离子方程式为Ba2+++OH-=BaCO3↓+H2O,D错误;
故答案选C。
10.A
【详解】A.二氧化硫催化氧化生成三氧化硫,冰水冷却三氧化硫,图中装置可制取并收集SO3,A正确;
B.生成的乙炔中混有硫化氢,均可被酸性高锰酸钾溶液氧化,紫色褪去,不能证明乙炔具有还原性,B错误;
C.食盐水为中性环境,铁发生的是吸氧腐蚀,C错误;
D.常温下浓盐酸与二氧化锰不反应,图中缺少酒精灯,D错误;
故答案为:A。
11.B
【详解】A.用溶液制作印刷电路板是因为铜和氯化铁反应得到氯化铜和氯化亚铁,与的活动性比强无关,故A错误;
B.喝酒后人呼出的气体中含有乙醇蒸汽,说明乙醇具有挥发性,酸性条件下乙醇还原重铬酸钾生成铬离子,橙红色变绿,故可用手持式酒精检测仪检测酒驾,说明乙醇具有还原性,二者有关联,故B正确;
C.船体外壳安装一定量锌块,是为了形成原电池,减缓船体腐蚀速度,是牺牲阳极的阴极保护法,外加电流法能减缓金属腐蚀速度,被保护的电极作阴极,是利用电解池原理,故C错误;
D.常温下铁与干燥的氯气不能发生反应,故用钢瓶储存和运输液氯,但在高温条件下,铁与氯气发生反应,故D错误;
故选B。
12.D
【分析】由图可知,该腐蚀过程是因为形成了原电池,Fe比Sn活泼,Fe作负极,电极反应式为Fe-2e-=Fe2+,Sn作正极被保护,电极反应式为O2+4e-+2H2O=4OH-,据此作答。
【详解】A.舰艇被腐蚀是因为形成了原电池,发生了电化学腐蚀,故A错误;
B.海水中含有电解质浓度大,腐蚀速度快,故乙为海水环境下的腐蚀情况,甲为淡水环境下的腐蚀情况,故B错误;
C.Sn作正极被保护,电极反应式为O2+4e-+2H2O=4OH-,Fe作负极,电极反应式为Fe-2e-=Fe2+,故C错误;
D.焊点附近用锌块打“补丁”,Zn比Fe活泼,Zn作负极,Fe作正极被保护,可延缓腐蚀,故D正确;
故选:D。
13.B
【详解】A.小龙虾的虾壳中含有壳聚糖,可用于制手术缝合线,故A正确;
B.螺旋碳纳米管、石墨烯等纳米材料不是胶体,纳米材料分散在其它分散剂中生成的分散系属于胶体,故B错误;
C.味精(主要化学成分为)的生产过程中,若不控制pH,羧基与氢氧根离子反应或或氨基与氢离子反应,所以谷氨酸的中和要严格控制溶液的,故C正确;
D.“深海一号”母船海水浸泡区的铝、铁构成原电池,铝为负极,为牺牲阳极的阴极保护法,铝基可保障船体不易腐蚀,故D正确;
选B。
14.A
【详解】A.钢铁中混有杂质碳,能与铁形成原电池的两个电极,遇到电解质溶液钢铁就能发生电化学腐蚀,铁制设备会发生电化学腐蚀,A正确;
B.聚丙烯酰胺属于有机高分子材料,B错误;
C.蒸发制盐利用的原理由于NaCl的溶解度随温度变化不明显,故采用蒸发结晶,而不是降温结晶,C错误;
D.I2易升华,且有一定的腐蚀性,故食盐中加KIO3避免碘缺乏,D错误;
故答案为:A。
15.B
【详解】A.水泥的主要成分为硅酸盐,属于传统无机非金属材料,故A正确;
B.纳米半导体CdTe量子点是纯净物,不属于胶体,故B错误;
C.由于锌比铁活泼,锌为负极被腐蚀,钢铁作为正极被保护,此依据是牺牲阳极法防腐,故C正确;
D.质子数相同,中子数不同的核素互为同位素,氕为与氘为互为同位素,故D正确;
故答案选B。
16.A
【详解】A.向锌铁原电池工作一段时间得到的溶液中滴入铁氰化钾溶液,没有蓝色沉淀生成说明锌做原电池的负极被损耗,铁做正极被保护,则题给装置能达到探究牺牲阳极法保护金属铁的实验目的,故A正确;
B.由图可知,亚硫酸钠固体与70%硫酸反应生成硫酸钠、二氧化硫和水,反应中没有元素发生化合价变化,则题给装置无法达到探究不同价态含硫物质的转化的实验目的,故B错误;
C.由图可知,等浓度的氯化铁溶液和硫酸铁溶液中铁离子浓度不同,由探究实验变量唯一化原则可知,题给装置无法达到探究、对与反应速率的影响的实验目的,故C错误;
D.葡萄酒中的乙醇也能与酸性高锰酸钾溶液发生氧化反应使溶液褪色,则题给装置无法达到探究用标准酸性溶液测定葡萄酒中的含量的实验目的,故D错误;
故选A。
17.C
【详解】A.取一块打磨过的生铁片,在其表面滴1滴含酚酞和的食盐水,铁皮发生吸氧腐蚀,没有生成,A错误;
B.铁片发生吸氧腐蚀,Fe电极方程式为:,边缘处红色得原因是二价铁被空气中的氧气氧化为三价铁,B错误;
C.铁片发生吸氧腐蚀,反应后中心区域溶液呈碱性,pH>7,C正确;
D.铁皮发生吸氧腐蚀得原理是原电池,但化学能不能完全转化为电能,D错误;
故选C。
18.A
【详解】A.钢铁在潮湿的空气中生锈,是原电池原理,主要发生电化学腐蚀,故A项正确;
B.酿酒工艺中加入的“酒曲”是催化剂,面包工艺中加入的“发酵粉”是反应物,故B项错误;
C.棉花、麻主要成分均为碳水化合物纤维素,蚕丝的主要成分是蛋白质,故C项错误;
D.75%的乙醇使蛋白质变性而消毒,84消毒液是用的强氧化性消毒,两者消毒原理不相同,故D项错误;
故本题选A。
19.C
【详解】A.纸本的主要成分是纤维素,为高分子化合物,故A错误;
B.乙醇氧化生成乙酸,所以酿造过程中不只发生水解反应,故B错误;
C.由信息可知,蒸令气上,则利用互溶混合物的沸点差异分离,则该法为蒸馏,故C正确;
D.铜发生吸氧腐蚀生成铜绿,红棕色斑迹是铁锈的颜色,故D错误;
故选:C。
20.B
【详解】A.沿烧杯壁向上清液中继续滴加1-2滴氯化钡,如果产生白色沉淀,说明没有沉淀完,故此方法可以检验否沉淀完全,故A正确;
B.提纯苯甲酸可以采用加热溶解,趁热过滤,过滤出泥沙,将滤液冷却结晶,过滤出苯甲酸,不能用分液操作提纯,故B错误;
C.锌铁形成原电池,锌作负极,铁作正极,铁电极两端变为红色,且没有蓝色沉淀,说明铁被保护了,故C正确;
D.形成喷泉实验,且溶液显红色,说明氨气易溶于水且溶液呈碱性,故D正确;
故答案为B。
21.D
【详解】A.氮气性质稳定,能够防止竹简被氧化,同时抑制细菌生长,故竹简密封保存,并充以氮气,可延缓其降解,A正确;
B.陶瓷发生过程中发生了复杂的物理化学变化,故陶制兵马俑的烧制过程涉及化学变化,B正确;
C.铜比铁更不活泼,故铜制钱币比铁制钱币的耐腐蚀性更强,C正确;
D.石甲胄的主要成分是青灰色岩溶性石灰石,故不为合金,而是无机盐属于无机非金属材料,D错误;
故答案为:D。
22.C
【详解】A.将Cl2通入冷的石灰乳中制备漂白粉的离子方程式:,A错误;
B.牺牲阳极法保护钢铁的正极反应式:,B错误;
C.工业上人工固氮的化学方程式:,C正确;
D.CH4(g)燃烧热的热化学方程式: ,D错误;
故选C。
23.C
【详解】A.实验室用氯化铵和氢氧化钙混合固体加热制取氨气,直接加热氯化铵不能制取氨气,原理错误,故A错误;
B.不能在容量瓶中进行浓溶液的稀释,故B错误;
C.该装置构成原电池,铁比石墨活泼,铁作负极,发生吸氧腐蚀加速铁的损耗,故C正确;
D.NO与氧气反应,因此不能用排空气法收集,故D错误;
故选:C。
24.B
【详解】A.甲醛能够使蛋白质发生变性而失去其生理活性,因此可以使用稀的甲醛溶液浸泡种子而起到消毒杀菌作用;但若使用甲醛水溶液浸泡蔬菜保鲜,甲醛会进入蔬菜中,从而危害人体健康,A正确;
B.聚氯乙烯塑料在高温下会产生游离的氯原子进入到食品中而危害人体健康,因此不能使用聚氯乙烯塑料来进行油炸食品包装,以免危害人体健康,B错误;
C.亚硝酸钠能够抑制微生物生长、抗氧化,因此可用作食品添加剂,但若摄入过量,会造成中毒,而影响人体人体健康,C正确;
D.钢铁是铁合金,主要杂质元素是碳元素,适当的碳含量可增加钢铁的硬度及耐磨性;但若碳过量,其中的铁、杂质碳与周围的水膜中的电解质会构成原电池,铁为原电池的负极,加快铁的腐蚀,因此容易导致钢铁腐蚀加剧,D正确;
故合理选项是B。
25.D
【详解】A.用于清洗伤口、杀菌、消毒的医用酒精能使蛋白变性,A错误;
B.在日常生活中,金属的腐蚀以电化学腐蚀为主,电化学腐蚀是造成钢铁腐蚀的主要原因,B错误;
C.直馏汽油无不饱和烃,不能使 的四氯化碳溶液褪色,C错误;
D.纯碱溶液显碱性,酯在碱性条件下发生水解,温度升高,水解反应为吸热反应,促进水解正向移动,D正确;
故选D。
26.B
【详解】A.钢铁闸门往往镶嵌锌块,锌块比较活泼失去电子,利用牺牲阳极保护法,故A错误;
B.四氧化三铁具有磁性,在磁性记录介质、磁性传感器等方面都有应用,可用作录音磁带和电讯器材的原材料,故B正确;
C.保暖贴中铁、碳构成原电池,铁是负极失电子发生氧化反应,利用电化学腐蚀提供热量,故C错误;
D.野外铁路抢修作业用高温下铝粉与氧化铁的反应来焊接铁轨,故D错误;
答案选B。
27.D
【详解】A.溶液蒸干过程中会彻底水解,生成氢氧化铜,甚至分解生成氧化铜,A错误;
B.电石与饱和食盐水产生的乙炔气体中含有等杂质,也能使溴水褪色,所以溴水褪色不一定是乙炔所导致,B错误;
C.二氧化碳与饱和食盐水不能生成碳酸氢钠,需要先溶入足量氨气,C错误;
D.根据氧气传感器测定氧气浓度,可以通过氧气浓度的变化来验证铁钉发生吸氧腐蚀,D正确;
故选D。
28.A
【详解】A.氨水为弱电解质,故向AlCl3溶液中滴加少量氨水产生白色沉淀:Al3++3NH3·H2O=Al(OH)3↓+3,A错误;
B.铁钉在潮湿空气中生锈时发生电化学腐蚀,铁为负极,碳为正极,负极反应式为:Fe-2e-=Fe2+,B正确;
C.CuSO4溶液与闪锌矿(ZnS)反应生成铜蓝(CuS)存在沉淀的转化,即ZnS转化为CuS,离子方程式为:Cu2+(aq)+ZnS(s)CuS(s)+Zn2+(aq),C正确;
D.已知Fe2+的还原性强于Br-,故向FeBr2溶液中通入少量Cl2的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,D正确;
故答案为:A。
29.A
【详解】A.铁发生吸氧腐蚀时,正极上O2得电子结合水生成氢氧根离子,清洗铁锅后及时擦干,除去了铁锅表面的水分,没有了电解质溶液,能减缓铁锅因发生吸氧腐蚀而生锈,A正确;
B.食盐中含有碘酸钾,碘酸钾受热不稳定易分解,因此烹煮食物时后期加入食盐,与NaCl无关,B错误;
C.焦糖的主要成分仍是糖类,同时还含有一些醛类、酮类等物质,蔗糖在高温下并未炭化,C错误;
D.食用纯碱主要成分为Na2CO3,制作面点时加入食用纯碱,利用了Na2CO3中和发酵过程产生的酸,D错误;
故答案选A。
30.B
【详解】A.饱和碳酸钠溶液可以起到中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度,A正确;
B.由于CCl4不溶于水,故向硫酸四氨合铜溶液中加入CCl4不能起到减弱水分子极性的作用,不能制得硫酸四氨合铜晶体,应该加入95%乙醇,可降低硫酸四氨合铜的溶解度,使其析出,B错误;
C.制备检验醛基用的,氢氧化钠溶液需过量,C正确;
D.将闸门与电源的负极相连,属于外加电源阴极保护法,D正确;
故答案选B。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
专题24金属的电化学腐蚀与防护--2025年高三化学一轮复习【专题专练】(含解析)
1.下列事实中涉及的反应与氧化还原无关的是
A.用溶液吸收
B.利用铜与浓硫酸加热反应制取
C.乙醇使紫色酸性溶液褪色
D.在船体上镶嵌锌块,可以减缓船体被海水腐蚀
2.化学与生产、生活、社会密切相关。下列有关说法正确的是
A.制白砂糖时用活性炭脱色属于化学变化
B.杭州亚运会使用的运动场地防滑涂层——石墨烯属于有机高分子材料
C.港珠澳大桥使用高性能富锌底漆防腐,依据的是外加电流的保护法
D.北京冬奥会采用氢能源汽车代替燃油车,有利于“碳达峰”、“碳中和”战略的实施
3.在西汉刘安组织编撰的《淮南万毕术》中,有“曾青得铁则化为铜”的记载。下列说法错误的是
A.这个反应是湿法冶金的基础,冶金过程中金属元素都发生还原反应
B.铁表面镀锌可以增强其抗腐蚀性
C.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
D.还原铁粉可以在食品包装袋内做脱氧剂
4.劳动是人生存发展的必要技能,下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 制作豆腐:将少量石石膏投入大豆研磨过滤后的溶液中 蛋白质发生聚沉而凝固
B 家庭自制肥皂:食用油和食用碱在一定条件混合 油脂在碱性条件下水解
C 餐具保存:擦干已洗净铁锅表面的水,以防生锈 防止潮湿环境下发生化学腐蚀
D 泳池消毒:用漂粉精作游泳池的消毒剂 漂粉精有强氧化性,可用于杀菌
A.A B.B C.C D.D
5.2024年5月8日,我国第三艘航空母舰福建舰顺利完成首次海试。舰体表面需要采取有效的防锈措施,下列防锈措施中不形成表面钝化膜的是
A.发蓝处理 B.阳极氧化 C.表面渗镀 D.喷涂油漆
6.“挖掘文物价值,讲好中国故事。”下列文物在潮湿空气中易发生电化学腐蚀的是
A.先锋煲(陶) B.曜变天目碗(瓷)
C.铁足大铜鼎 D.六棱柱形水晶穿珠
A.A B.B C.C D.D
7.下列对文中加点内容所做说明错误的是
A.帘外芭蕉惹骤雨,门环惹铜绿——金属的吸氧腐蚀
B.蒸熟谷粒酒中潜,廿日珍存变为酸——葡萄糖的水解
C.玉梅雪柳千家闹,火树银花十里开——焰色试验
D.白胎烧就彩虹来,五色成窑画作开——颜料的氧化还原反应
8.化学与生产、生活、社会密切相关。下列有关说法中正确的是
A.使用乙醇汽油可以减少汽车尾气中氮氧化物的排放
B.实施海底封存,需要将进行液化,液化过程中的共价键被破坏
C.“深海一号”母船海水浸泡区的铝基可保障船体不易腐蚀
D.飞船操纵杆的材料碳纤维与石墨烯互为同素异形体
9.下列离子方程式正确的是
A.用硫化钠溶液除去废水中的汞离子:
B.与水反应:
C.钢铁发生吸氧腐蚀,正极反应:
D.向溶液中加入少量:
10.如图所示实验装置能达到实验目的的是
A.图甲:制取并收集 B.图乙:检验乙炔具有还原性
C.图丙:研究铁的析氢腐蚀 D.图丁:实验室制备
11.劳动创造美好生活。下列化学知识正确且与相应劳动项目有关联的是
选项 化学知识 劳动项目
A 的活动性比强 用溶液制作印刷电路板
B 乙醇具有挥发性和还原性 用手持式酒精检测仪检测酒驾
C 外加电流法能减缓金属腐蚀速度 在船体外壳安装一定量锌块
D 铁与氯气不能发生反应 用钢瓶储存和运输液氯
A.A B.B C.C D.D
12.2012年9月25日开始服役的我国首艘航母辽宁舰采用模块制造再焊接组装而成。实验室模拟海水和淡水对焊接金属材料的影响,结果如图所示。下列分析正确的是
A.舰艇腐蚀主要是因为发生了化学腐蚀 B.图甲是海水环境下的腐蚀情况
C.腐蚀时负极反应为: D.焊点附近可用锌块打“补丁”延缓腐蚀
13.化学与科技、生产、生活密切相关。下列有关说法不正确的是
A.小龙虾的虾壳可用于制手术缝合线
B.量子通信材料螺旋碳纳米管、石墨烯等纳米材料属于胶体
C.味精(主要化学成分为)的生产过程中,谷氨酸的中和要严格控制溶液的
D.“深海一号”母船海水浸泡区的铝基可保障船体不易腐蚀
14.安徽省生产食盐的主要来源为内陆井矿盐。下列说法正确的是
A.钻井用的铁制设备被腐蚀的过程涉及原电池原理
B.卤水净化所用的助沉剂聚丙烯酰胺属于无机非金属材料
C.蒸发制盐利用的原理是NaCl的溶解度随温度变化明显
D.食盐中添加I2,可以帮助人们避免碘缺乏
15.2024年“两会”提出的“新质生产力”涵盖新材料、新能源、生物医药等产业链。下列说法错误的是
A.精确控制硬化过程的可编程水泥属于硅酸盐材料
B.具有独特光学、电学性能的纳米半导体CdTe量子点属于胶体
C.福建号航母使用高性能富锌底漆是采用牺牲阳极保护法防腐蚀
D.新型药物(VV116)所含氕与氘互为同位素
16.下列实验装置能达到相应实验目的的是
选项 实验目的 实验装置
A 探究牺牲阳极法保护金属铁
B 探究不同价态含硫物质的转化: +6→+4→+6
C 探究、对与反应速率的影响
D 探究用标准酸性溶液测定葡萄酒中的含量
A.A B.B C.C D.D
17.某同学进行以下实验:
操作 现象
取一块打磨过的生铁片,在其表面滴1滴含酚酞和的食盐水 放置一段时间后,生铁片上出现如图所示“斑痕”。其边缘处为红色,中心区域为蓝色,在两色环交界处出现铁锈
下列说法正确的是
A.腐蚀过程中有生成
B.边缘处红色说明:
C.反应后中心区域溶液的pH>7
D.反应过程中化学能完全转化为电能
18.化学与生活密切相关。下列叙述正确的是
A.钢铁在潮湿的空气中生锈主要发生电化学腐蚀
B.酿酒工艺中加入的“酒曲”与面包工艺中加入的“发酵粉”作用相同
C.棉花、麻和蚕丝均为碳水化合物
D.75%的乙醇与84消毒液的消毒原理相同
19.中华文化源远流长,化学与文化传承密不可分。下列说法正确的是
A.清朱耷芦雁轴纸本的主要成分是淀粉,淀粉为高分子化合物
B.四千余年前用谷物酿造出酒和醋,酿造过程中只发生水解反应
C.《本草纲目》“烧酒”条目写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”叙述了“蒸馏”技术在古代酿酒工艺中的应用
D.广汉三星堆出土的青铜面具呈红棕色斑迹,是由于铜发生了吸氧腐蚀
20.下列实验装置或操作不能达到实验目的的是
A B
检验否沉淀完全 提纯含有少量氯化钠和泥沙的苯甲酸
C D
牺牲阳极法保护铁 易溶于水且溶液呈碱性
A.A B.B C.C D.D
21.秦始皇陵是我国历史上规模最大的帝王陵墓,秦始皇陵兵马俑被誉为“世界第八大奇迹”,考古发现并出土了大量竹简、兵马俑、钱币、石甲胄等珍贵文物,下列说法错误的是
A.竹简密封保存,并充以氮气,可延缓其降解
B.陶制兵马俑的烧制过程涉及化学变化
C.铜制钱币比铁制钱币的耐腐蚀性更强
D.石甲胄的主要成分为合金
22.化学学科有独特的符号表达。下列叙述正确的是
A.将Cl2通入冷的石灰乳中制备漂白粉的离子方程式:
B.牺牲阳极法保护钢铁的正极反应式:
C.工业上人工固氮的化学方程式:
D.CH4(g)燃烧热的热化学方程式:
23.对下列实验装置、操作或目的理解正确的是
A.不能制取NH3,因为收集方式有误 B.将浓硫酸加入到容量瓶中,再加水稀释,可得稀硫酸
C.不能保护铁件,会发生吸氧腐蚀加快铁件的损耗 D.可以收集NO,因为NO密度比空气小
A.A B.B C.C D.D
24.物质都有两面性。下列说法错误的是
A.稀甲醛溶液浸泡种子能消毒杀菌;浸泡蔬菜保鲜会危害人体健康
B.聚氯乙烯塑料可用于油炸食品包装;随意弃置会造成“白色污染”
C.亚硝酸钠抑制微生物生长、抗氧化,可用作食品添加剂;摄入过量会造成中毒
D.适当的碳含量可增加钢铁的硬度及耐磨性;过量的碳会导致钢铁腐蚀加剧
25.化学与科学、技术、社会、生活等密切相关。下列有关说法正确的是
A.用于清洗伤口、杀菌、消毒的医用酒精有强氧化性
B.在日常生活中, 造成钢铁腐蚀的主要原因是化学腐蚀
C.直馏汽油、裂化汽油、植物油均能使 的四氯化碳溶液褪色
D.可以用热的纯碱溶液来清洗油污
26.铁是现代社会应用最广泛的金属,下列关于铁及其化合物的说法正确的是
A.河道出海口的钢铁闸门往往镶嵌锌块,利用牺牲阴极保护法
B.四氧化三铁具有磁性,可用作录音磁带和电讯器材的原材料
C.保暖贴是利用铁粉与空气中氧气发生化学腐蚀而发热的原理
D.野外铁路抢修作业用高温下铁粉与氧化铝的反应来焊接铁轨
27.利用下列实验装置进行实验,操作正确且能达到实验目的的是
A.用装置甲蒸干溶液制无水晶体 B.用装置乙证明乙炔可使溴水褪色
C.用装置丙制备固体 D.用装置丁验证铁钉吸氧腐蚀
28.下列离子方程式书写不正确的是
A.向AlCl3溶液中滴加少量氨水产生白色沉淀:Al3++3OH-=Al(OH)3↓
B.铁钉在潮湿空气中生锈的负极反应:Fe-2e-=Fe2+
C.CuSO4溶液与闪锌矿(ZnS)反应生成铜蓝(CuS):Cu2+(aq)+ZnS(s)CuS(s)+Zn2+(aq)
D.向FeBr2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl-
29.青少年帮厨既可培养劳动习惯,也能将化学知识应用于实践。下列有关解释合理的是
A.清洗铁锅后及时擦干,能减缓铁锅因发生吸氧腐蚀而生锈
B.烹煮食物的后期加入食盐,能避免长时间受热而分解
C.将白糖熬制成焦糖汁,利用蔗糖高温下充分炭化为食物增色
D.制作面点时加入食用纯碱,利用中和发酵过程产生的酸
30.下图所示装置不能达到目的的是
A.用图甲装置制备乙酸乙酯
B.用图乙装置制备硫酸四氨合铜晶体
C.用图丙装置制备检验醛基用的
D.用图丁装置保护钢铁设备
参考答案:
1.A
【详解】A.溶液吸收生成碳酸钠和水,无元素化合价改变,与氧化还原无关,A符合题意;
B.生成二氧化硫,硫元素化合价改变,属于氧化还原反应,B不符合题意;
C.高锰酸钾具有强氧化性,和乙醇发生氧化还原反应而使得溶液褪色,C不符合题意;
D.锌比铁活泼,在船体上镶嵌锌块避免船体遭受腐蚀的原理是牺牲阳极法安装活泼金属做原电池负极,被保护的钢铁做正极,与氧化还原反应有关,D不符合题意;
故选A。
2.D
【详解】A.制白砂糖时用活性炭脱色为活性炭的吸附作用,属于物理变化,A错误;
B.石墨烯为碳单质,不属于有机高分子材,B错误;
C.港珠澳大桥使用高性能富锌底漆防腐,锌作负极保护铁,依据的是牺牲阳极法,C错误;
D.采用氢能源汽车代替燃油车,减少CO2的产生和排放,有利于“碳达峰、碳中和”,D正确;
故选D。
3.A
【详解】A.这个反应是湿法冶金的基础,冶金过程中铜元素化合价降低、硫酸铜发生还原反应,铁元素化合价升高、铁发生氧化反应,A错误;
B. 铁表面镀锌隔绝了空气和水分,可以增强金属的抗腐蚀性,即使镀层破损,锌可为原电池负极、利用牺牲阳极的阴极保护法保护作为正极的铁不被腐蚀,B正确;
C.明矾水解溶液呈酸性,能与铜锈的成分碱式碳酸铜反应使其溶解,但不与铜反应,则中国古代利用明矾溶液的酸性清除铜镜表面的铜锈,C正确;
D. 还原铁粉具有还原性、可以在食品包装袋内做脱氧剂,D正确;
答案选A。
4.C
【详解】A.大豆研磨过滤后的溶液中含有大量蛋白质,轻金属盐溶液可以使蛋白质胶体聚沉,故可以用于制作豆腐,故A不选;
B.食用油是多种高级脂肪酸甘油酯的混合物,食用碱的为碳酸钠,水解后溶液显碱性。高级脂肪酸甘油酯在碱的作用下发生水解生成高级脂肪酸钠和甘油,高级脂肪酸钠是肥皂的主要成分,故可以用食用油和食用碱在一定条件下混合制肥皂,故B不选;
C.擦干已洗净铁锅表面的水,可以防止潮湿环境下铁锅发生电化学腐蚀,不是化学腐蚀,故C选;
D.漂粉精的有效成分为次氯酸钙,次氯酸钙可以水解为有强氧化性的次氯酸,从而可以用于泳池消毒,故D不选;
故选C。
5.D
【详解】A.发蓝处理技术通常用于钢铁等黑色金属,通过在空气中加热或直接浸泡于浓氧化性溶液中来实现,可在金属表面形成一层极薄的氧化膜,这层氧化膜能有效防锈,A不符合题意;
B.阳极氧化是将待保护的金属与电源正极连接,在金属表面形成一层氧化膜的过程,B不符合题意;
C.表面渗镀是在高温下将气态、固态或熔化状态的欲渗镀的物质(金属或非金属元素)通过扩散作用从被渗镀的金属的表面渗入内部以形成表层合金镀层的一种表面处理的方法,C不符合题意;
D.喷涂油漆是将油漆涂在待保护的金属表面并没有在表面形成钝化膜,D符合题意;
故答案选D。
6.C
【详解】先锋煲、曜变天目碗、六棱柱形水晶穿珠的主要成分都是无机非金属材料,而铁足大铜鼎的主要成分是金属材料,所以铁足大铜鼎在潮湿空气中易发生电化学腐蚀被损耗,故选C。
7.B
【详解】A.铜的吸氧腐蚀生成铜绿的电极反应是一种常见的化学变化,它涉及到铜在氧气的存在下腐蚀生成铜绿的过程,A正确;
B.葡萄糖为单糖,不能水解,B错误;
C.火树银花十里开,描述的是烟花,烟花与焰色试验有关,C正确;
D.白胎烧就彩虹来,颜料在灼烧下发生氧化还原反应,产生颜色变化,D正确;
故选B。
8.C
【详解】A.高温下空气中的氮气和氧气反应生成NO,NO与氧气反应生成,则乙醇汽油的使用不能减少汽车尾气中氮氧化物的排放,A错误;
B.二氧化碳是分子晶体,所以二氧化碳液化时,只改变分子间的作用力,不破坏分子内的共价键,B错误;
C.“深海一号”母船海水浸泡区的铝基作负极可以与船体形成原电池,利用“牺牲阳极的阴极保护法”可保障船体不易腐蚀,C正确;
D.碳纤维是一种复合材料,属于混合物,与石墨烯不互为同素异形体,D错误;
故选C。
9.C
【详解】A.用硫化钠溶液除去废水中的汞离子,离子方程式为Hg2++S2-=HgS↓,A错误;
B.Cl2与水反应生成的HClO为弱电解质,不能拆成离子的形式,离子方程式为Cl2+H2OCl-+H++HClO,B错误;
C.钢铁发生吸氧腐蚀,正极上氧气得电子结合水生成氢氧根离子,离子方程式正确,C正确;
D.向碳酸氢钡溶液中滴加少量NaOH,反应的离子方程式为Ba2+++OH-=BaCO3↓+H2O,D错误;
故答案选C。
10.A
【详解】A.二氧化硫催化氧化生成三氧化硫,冰水冷却三氧化硫,图中装置可制取并收集SO3,A正确;
B.生成的乙炔中混有硫化氢,均可被酸性高锰酸钾溶液氧化,紫色褪去,不能证明乙炔具有还原性,B错误;
C.食盐水为中性环境,铁发生的是吸氧腐蚀,C错误;
D.常温下浓盐酸与二氧化锰不反应,图中缺少酒精灯,D错误;
故答案为:A。
11.B
【详解】A.用溶液制作印刷电路板是因为铜和氯化铁反应得到氯化铜和氯化亚铁,与的活动性比强无关,故A错误;
B.喝酒后人呼出的气体中含有乙醇蒸汽,说明乙醇具有挥发性,酸性条件下乙醇还原重铬酸钾生成铬离子,橙红色变绿,故可用手持式酒精检测仪检测酒驾,说明乙醇具有还原性,二者有关联,故B正确;
C.船体外壳安装一定量锌块,是为了形成原电池,减缓船体腐蚀速度,是牺牲阳极的阴极保护法,外加电流法能减缓金属腐蚀速度,被保护的电极作阴极,是利用电解池原理,故C错误;
D.常温下铁与干燥的氯气不能发生反应,故用钢瓶储存和运输液氯,但在高温条件下,铁与氯气发生反应,故D错误;
故选B。
12.D
【分析】由图可知,该腐蚀过程是因为形成了原电池,Fe比Sn活泼,Fe作负极,电极反应式为Fe-2e-=Fe2+,Sn作正极被保护,电极反应式为O2+4e-+2H2O=4OH-,据此作答。
【详解】A.舰艇被腐蚀是因为形成了原电池,发生了电化学腐蚀,故A错误;
B.海水中含有电解质浓度大,腐蚀速度快,故乙为海水环境下的腐蚀情况,甲为淡水环境下的腐蚀情况,故B错误;
C.Sn作正极被保护,电极反应式为O2+4e-+2H2O=4OH-,Fe作负极,电极反应式为Fe-2e-=Fe2+,故C错误;
D.焊点附近用锌块打“补丁”,Zn比Fe活泼,Zn作负极,Fe作正极被保护,可延缓腐蚀,故D正确;
故选:D。
13.B
【详解】A.小龙虾的虾壳中含有壳聚糖,可用于制手术缝合线,故A正确;
B.螺旋碳纳米管、石墨烯等纳米材料不是胶体,纳米材料分散在其它分散剂中生成的分散系属于胶体,故B错误;
C.味精(主要化学成分为)的生产过程中,若不控制pH,羧基与氢氧根离子反应或或氨基与氢离子反应,所以谷氨酸的中和要严格控制溶液的,故C正确;
D.“深海一号”母船海水浸泡区的铝、铁构成原电池,铝为负极,为牺牲阳极的阴极保护法,铝基可保障船体不易腐蚀,故D正确;
选B。
14.A
【详解】A.钢铁中混有杂质碳,能与铁形成原电池的两个电极,遇到电解质溶液钢铁就能发生电化学腐蚀,铁制设备会发生电化学腐蚀,A正确;
B.聚丙烯酰胺属于有机高分子材料,B错误;
C.蒸发制盐利用的原理由于NaCl的溶解度随温度变化不明显,故采用蒸发结晶,而不是降温结晶,C错误;
D.I2易升华,且有一定的腐蚀性,故食盐中加KIO3避免碘缺乏,D错误;
故答案为:A。
15.B
【详解】A.水泥的主要成分为硅酸盐,属于传统无机非金属材料,故A正确;
B.纳米半导体CdTe量子点是纯净物,不属于胶体,故B错误;
C.由于锌比铁活泼,锌为负极被腐蚀,钢铁作为正极被保护,此依据是牺牲阳极法防腐,故C正确;
D.质子数相同,中子数不同的核素互为同位素,氕为与氘为互为同位素,故D正确;
故答案选B。
16.A
【详解】A.向锌铁原电池工作一段时间得到的溶液中滴入铁氰化钾溶液,没有蓝色沉淀生成说明锌做原电池的负极被损耗,铁做正极被保护,则题给装置能达到探究牺牲阳极法保护金属铁的实验目的,故A正确;
B.由图可知,亚硫酸钠固体与70%硫酸反应生成硫酸钠、二氧化硫和水,反应中没有元素发生化合价变化,则题给装置无法达到探究不同价态含硫物质的转化的实验目的,故B错误;
C.由图可知,等浓度的氯化铁溶液和硫酸铁溶液中铁离子浓度不同,由探究实验变量唯一化原则可知,题给装置无法达到探究、对与反应速率的影响的实验目的,故C错误;
D.葡萄酒中的乙醇也能与酸性高锰酸钾溶液发生氧化反应使溶液褪色,则题给装置无法达到探究用标准酸性溶液测定葡萄酒中的含量的实验目的,故D错误;
故选A。
17.C
【详解】A.取一块打磨过的生铁片,在其表面滴1滴含酚酞和的食盐水,铁皮发生吸氧腐蚀,没有生成,A错误;
B.铁片发生吸氧腐蚀,Fe电极方程式为:,边缘处红色得原因是二价铁被空气中的氧气氧化为三价铁,B错误;
C.铁片发生吸氧腐蚀,反应后中心区域溶液呈碱性,pH>7,C正确;
D.铁皮发生吸氧腐蚀得原理是原电池,但化学能不能完全转化为电能,D错误;
故选C。
18.A
【详解】A.钢铁在潮湿的空气中生锈,是原电池原理,主要发生电化学腐蚀,故A项正确;
B.酿酒工艺中加入的“酒曲”是催化剂,面包工艺中加入的“发酵粉”是反应物,故B项错误;
C.棉花、麻主要成分均为碳水化合物纤维素,蚕丝的主要成分是蛋白质,故C项错误;
D.75%的乙醇使蛋白质变性而消毒,84消毒液是用的强氧化性消毒,两者消毒原理不相同,故D项错误;
故本题选A。
19.C
【详解】A.纸本的主要成分是纤维素,为高分子化合物,故A错误;
B.乙醇氧化生成乙酸,所以酿造过程中不只发生水解反应,故B错误;
C.由信息可知,蒸令气上,则利用互溶混合物的沸点差异分离,则该法为蒸馏,故C正确;
D.铜发生吸氧腐蚀生成铜绿,红棕色斑迹是铁锈的颜色,故D错误;
故选:C。
20.B
【详解】A.沿烧杯壁向上清液中继续滴加1-2滴氯化钡,如果产生白色沉淀,说明没有沉淀完,故此方法可以检验否沉淀完全,故A正确;
B.提纯苯甲酸可以采用加热溶解,趁热过滤,过滤出泥沙,将滤液冷却结晶,过滤出苯甲酸,不能用分液操作提纯,故B错误;
C.锌铁形成原电池,锌作负极,铁作正极,铁电极两端变为红色,且没有蓝色沉淀,说明铁被保护了,故C正确;
D.形成喷泉实验,且溶液显红色,说明氨气易溶于水且溶液呈碱性,故D正确;
故答案为B。
21.D
【详解】A.氮气性质稳定,能够防止竹简被氧化,同时抑制细菌生长,故竹简密封保存,并充以氮气,可延缓其降解,A正确;
B.陶瓷发生过程中发生了复杂的物理化学变化,故陶制兵马俑的烧制过程涉及化学变化,B正确;
C.铜比铁更不活泼,故铜制钱币比铁制钱币的耐腐蚀性更强,C正确;
D.石甲胄的主要成分是青灰色岩溶性石灰石,故不为合金,而是无机盐属于无机非金属材料,D错误;
故答案为:D。
22.C
【详解】A.将Cl2通入冷的石灰乳中制备漂白粉的离子方程式:,A错误;
B.牺牲阳极法保护钢铁的正极反应式:,B错误;
C.工业上人工固氮的化学方程式:,C正确;
D.CH4(g)燃烧热的热化学方程式: ,D错误;
故选C。
23.C
【详解】A.实验室用氯化铵和氢氧化钙混合固体加热制取氨气,直接加热氯化铵不能制取氨气,原理错误,故A错误;
B.不能在容量瓶中进行浓溶液的稀释,故B错误;
C.该装置构成原电池,铁比石墨活泼,铁作负极,发生吸氧腐蚀加速铁的损耗,故C正确;
D.NO与氧气反应,因此不能用排空气法收集,故D错误;
故选:C。
24.B
【详解】A.甲醛能够使蛋白质发生变性而失去其生理活性,因此可以使用稀的甲醛溶液浸泡种子而起到消毒杀菌作用;但若使用甲醛水溶液浸泡蔬菜保鲜,甲醛会进入蔬菜中,从而危害人体健康,A正确;
B.聚氯乙烯塑料在高温下会产生游离的氯原子进入到食品中而危害人体健康,因此不能使用聚氯乙烯塑料来进行油炸食品包装,以免危害人体健康,B错误;
C.亚硝酸钠能够抑制微生物生长、抗氧化,因此可用作食品添加剂,但若摄入过量,会造成中毒,而影响人体人体健康,C正确;
D.钢铁是铁合金,主要杂质元素是碳元素,适当的碳含量可增加钢铁的硬度及耐磨性;但若碳过量,其中的铁、杂质碳与周围的水膜中的电解质会构成原电池,铁为原电池的负极,加快铁的腐蚀,因此容易导致钢铁腐蚀加剧,D正确;
故合理选项是B。
25.D
【详解】A.用于清洗伤口、杀菌、消毒的医用酒精能使蛋白变性,A错误;
B.在日常生活中,金属的腐蚀以电化学腐蚀为主,电化学腐蚀是造成钢铁腐蚀的主要原因,B错误;
C.直馏汽油无不饱和烃,不能使 的四氯化碳溶液褪色,C错误;
D.纯碱溶液显碱性,酯在碱性条件下发生水解,温度升高,水解反应为吸热反应,促进水解正向移动,D正确;
故选D。
26.B
【详解】A.钢铁闸门往往镶嵌锌块,锌块比较活泼失去电子,利用牺牲阳极保护法,故A错误;
B.四氧化三铁具有磁性,在磁性记录介质、磁性传感器等方面都有应用,可用作录音磁带和电讯器材的原材料,故B正确;
C.保暖贴中铁、碳构成原电池,铁是负极失电子发生氧化反应,利用电化学腐蚀提供热量,故C错误;
D.野外铁路抢修作业用高温下铝粉与氧化铁的反应来焊接铁轨,故D错误;
答案选B。
27.D
【详解】A.溶液蒸干过程中会彻底水解,生成氢氧化铜,甚至分解生成氧化铜,A错误;
B.电石与饱和食盐水产生的乙炔气体中含有等杂质,也能使溴水褪色,所以溴水褪色不一定是乙炔所导致,B错误;
C.二氧化碳与饱和食盐水不能生成碳酸氢钠,需要先溶入足量氨气,C错误;
D.根据氧气传感器测定氧气浓度,可以通过氧气浓度的变化来验证铁钉发生吸氧腐蚀,D正确;
故选D。
28.A
【详解】A.氨水为弱电解质,故向AlCl3溶液中滴加少量氨水产生白色沉淀:Al3++3NH3·H2O=Al(OH)3↓+3,A错误;
B.铁钉在潮湿空气中生锈时发生电化学腐蚀,铁为负极,碳为正极,负极反应式为:Fe-2e-=Fe2+,B正确;
C.CuSO4溶液与闪锌矿(ZnS)反应生成铜蓝(CuS)存在沉淀的转化,即ZnS转化为CuS,离子方程式为:Cu2+(aq)+ZnS(s)CuS(s)+Zn2+(aq),C正确;
D.已知Fe2+的还原性强于Br-,故向FeBr2溶液中通入少量Cl2的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,D正确;
故答案为:A。
29.A
【详解】A.铁发生吸氧腐蚀时,正极上O2得电子结合水生成氢氧根离子,清洗铁锅后及时擦干,除去了铁锅表面的水分,没有了电解质溶液,能减缓铁锅因发生吸氧腐蚀而生锈,A正确;
B.食盐中含有碘酸钾,碘酸钾受热不稳定易分解,因此烹煮食物时后期加入食盐,与NaCl无关,B错误;
C.焦糖的主要成分仍是糖类,同时还含有一些醛类、酮类等物质,蔗糖在高温下并未炭化,C错误;
D.食用纯碱主要成分为Na2CO3,制作面点时加入食用纯碱,利用了Na2CO3中和发酵过程产生的酸,D错误;
故答案选A。
30.B
【详解】A.饱和碳酸钠溶液可以起到中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度,A正确;
B.由于CCl4不溶于水,故向硫酸四氨合铜溶液中加入CCl4不能起到减弱水分子极性的作用,不能制得硫酸四氨合铜晶体,应该加入95%乙醇,可降低硫酸四氨合铜的溶解度,使其析出,B错误;
C.制备检验醛基用的,氢氧化钠溶液需过量,C正确;
D.将闸门与电源的负极相连,属于外加电源阴极保护法,D正确;
故答案选B。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
