人教版九年级化学上册课件:5.1 质量守恒定律(共23张PPT)
文档属性
| 名称 | 人教版九年级化学上册课件:5.1 质量守恒定律(共23张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-12-21 17:55:15 | ||
图片预览




文档简介
课件23张PPT。课题1 质量守恒定律第五单元 化学方程式生日宴会中我们发现生日蜡烛会越烧越短。金属生锈后质量变大了。1、结合生活中遇到的现象,提出问题: 化学反应前后物质的质量有没有变化呢?
2、你的猜想是 (变大、变小、或不变);一、质量守恒定律3、设计实验,验证你的猜想。【方案二】铁丝与硫酸铜溶液反应前后质量的测定。【方案一】白磷燃烧前后的质量测定(1)实验原理:铁 + 硫酸铜 → 铜 + 硫酸亚铁
(2)实验目的:铁与硫酸铜反应前后的质量变化;
(3)实验的步骤:
①首先 ;
②然后,不动砝码和游码,取下烧杯,将铁丝的一端
放入到硫酸铜溶液中,过一会取出,观察现象;
③反应后 ;
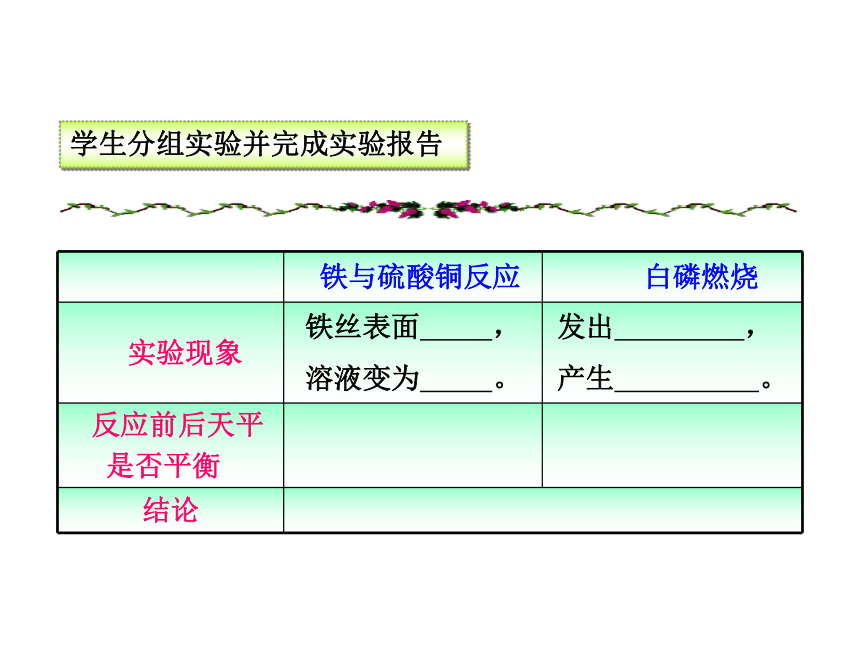
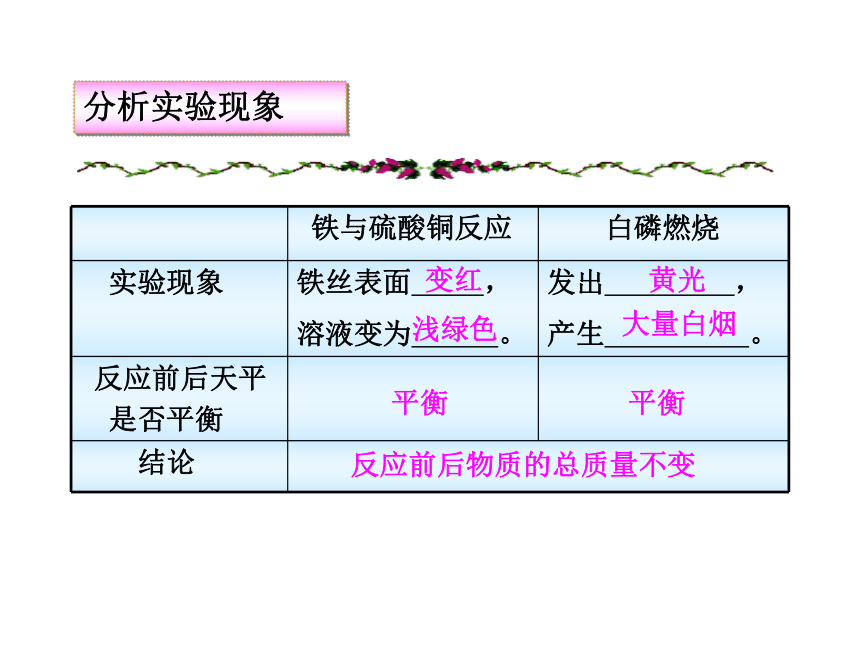
④实验完毕,整理实验仪器 (砝码回盒,游码回零)称量烧杯、硫酸铜、铁丝的质量再次放到天平上称量,看天平是否平衡【方案二】学生分组实验并完成实验报告平衡反应前后物质的总质量不变平衡黄光浅绿色大量白烟变红分析实验现象+ M 参加反应的
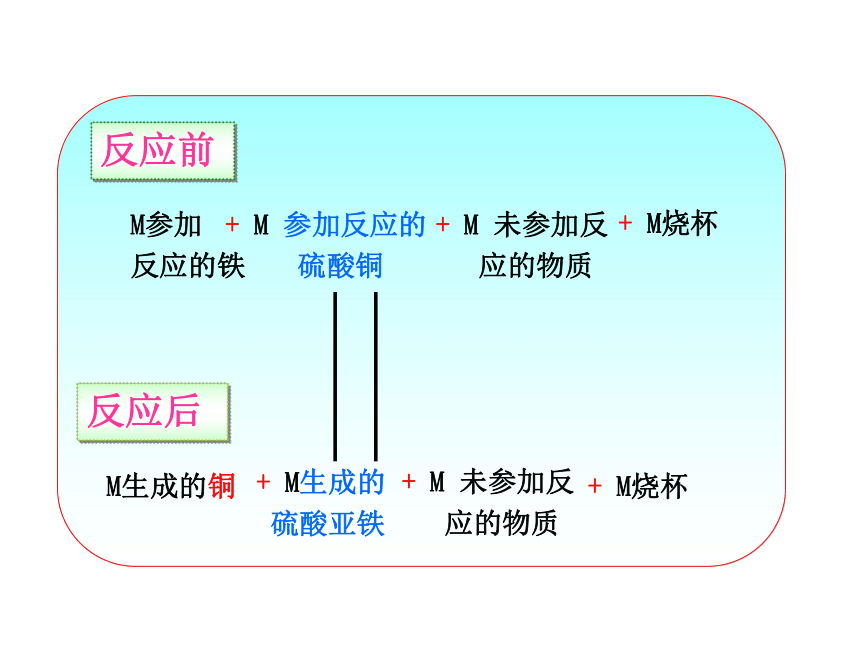
硫酸铜M生成的铜 M参加
反应的铁 + M生成的
硫酸亚铁 反应前+ M烧杯+ M 未参加反
应的物质+ M 未参加反
应的物质+ M烧杯反应后参加反应的
各物质的质
量总和生成的各物质的质量总和质量守恒定律:水通电分解的微观展示点击按钮播放视频化学变化的实质是:分子原子分解为新分子重组反应前后原子的种类、数目、质量没有改变。1、现有31g红磷与40g氧气恰好完全反应,则生成五氧化二磷的质量____g。2、6g的碳在充足的氧气中燃烧,生成二氧化碳22 g ,则有____g 氧气参加反应。7116比一比,看谁快1、碳酸钠与盐酸的反应
碳酸钠 + 盐酸 → 氯化钠
+水+二氧化碳
Na2CO3 + HCl → NaCl + H2O + CO2↑实验的现象: ;
天平指针的变化: ;产生大量气泡偏右自主探究2、镁条在空气中燃烧
镁 + 氧气 氧化镁
Mg + O2 MgO点燃实验的现象: ;氧化镁的质量比镁的 ;发出耀眼的白光大点燃应用质量守恒定律要注意:1、质量守恒定律适用于化学反应。
2、“总和”意味着把各种状态的反应物和生成物都计算在内。如沉淀、肉眼看不见的气体也应考虑。
3、参加化学反应的各物质的质量总和并不是各物质的任意质量之和,不参加反应的物质的质量不能计算在内。1、蜡烛在空气中燃烧,蜡烛的质量为什么会变小?2、铁生锈后,质量为什么会变大?解释日常生活中的一些现象3、木炭在空气中燃烧,木炭的质量为什么变小,该反应是否遵守质量守恒定律?1、定义:用化学式来表示化学反应的式子2、意义 ①表示反应物、生成物、反应条件 ②表示各物质之间的质量比12 32 44二、化学方程式本节课你有哪些收获?质量守恒定律内容:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和解释:反应前后原子的种类、数目、质量都没有改变自我诊断检测题C1、化学反应前后,肯定没有发生变化的是( )
①原子数目 ②分子数目 ③元素种类
④物质的总质量 ⑤物质的种类
A ① ④ B ① ③ ⑤
C ① ③ ④ D ① ② ③ ④ ⑤D2、红磷在密闭容器(含有空气)内燃烧,容器内有关的量随时间变化的关系的图像( )
A B C D 3、将25g氯酸钾和6g二氧化锰的混合物加热一段时间后,得到残余固体质量为22 g,则产生氧气____g。
4、煤的气化是提高煤的利用率,减少环境污染的有效措施。煤的气化过程中发生了化学反应 C + H2O = CO + X。请你写出X的化学式 。9H2Thank you!
2、你的猜想是 (变大、变小、或不变);一、质量守恒定律3、设计实验,验证你的猜想。【方案二】铁丝与硫酸铜溶液反应前后质量的测定。【方案一】白磷燃烧前后的质量测定(1)实验原理:铁 + 硫酸铜 → 铜 + 硫酸亚铁
(2)实验目的:铁与硫酸铜反应前后的质量变化;
(3)实验的步骤:
①首先 ;
②然后,不动砝码和游码,取下烧杯,将铁丝的一端
放入到硫酸铜溶液中,过一会取出,观察现象;
③反应后 ;
④实验完毕,整理实验仪器 (砝码回盒,游码回零)称量烧杯、硫酸铜、铁丝的质量再次放到天平上称量,看天平是否平衡【方案二】学生分组实验并完成实验报告平衡反应前后物质的总质量不变平衡黄光浅绿色大量白烟变红分析实验现象+ M 参加反应的
硫酸铜M生成的铜 M参加
反应的铁 + M生成的
硫酸亚铁 反应前+ M烧杯+ M 未参加反
应的物质+ M 未参加反
应的物质+ M烧杯反应后参加反应的
各物质的质
量总和生成的各物质的质量总和质量守恒定律:水通电分解的微观展示点击按钮播放视频化学变化的实质是:分子原子分解为新分子重组反应前后原子的种类、数目、质量没有改变。1、现有31g红磷与40g氧气恰好完全反应,则生成五氧化二磷的质量____g。2、6g的碳在充足的氧气中燃烧,生成二氧化碳22 g ,则有____g 氧气参加反应。7116比一比,看谁快1、碳酸钠与盐酸的反应
碳酸钠 + 盐酸 → 氯化钠
+水+二氧化碳
Na2CO3 + HCl → NaCl + H2O + CO2↑实验的现象: ;
天平指针的变化: ;产生大量气泡偏右自主探究2、镁条在空气中燃烧
镁 + 氧气 氧化镁
Mg + O2 MgO点燃实验的现象: ;氧化镁的质量比镁的 ;发出耀眼的白光大点燃应用质量守恒定律要注意:1、质量守恒定律适用于化学反应。
2、“总和”意味着把各种状态的反应物和生成物都计算在内。如沉淀、肉眼看不见的气体也应考虑。
3、参加化学反应的各物质的质量总和并不是各物质的任意质量之和,不参加反应的物质的质量不能计算在内。1、蜡烛在空气中燃烧,蜡烛的质量为什么会变小?2、铁生锈后,质量为什么会变大?解释日常生活中的一些现象3、木炭在空气中燃烧,木炭的质量为什么变小,该反应是否遵守质量守恒定律?1、定义:用化学式来表示化学反应的式子2、意义 ①表示反应物、生成物、反应条件 ②表示各物质之间的质量比12 32 44二、化学方程式本节课你有哪些收获?质量守恒定律内容:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和解释:反应前后原子的种类、数目、质量都没有改变自我诊断检测题C1、化学反应前后,肯定没有发生变化的是( )
①原子数目 ②分子数目 ③元素种类
④物质的总质量 ⑤物质的种类
A ① ④ B ① ③ ⑤
C ① ③ ④ D ① ② ③ ④ ⑤D2、红磷在密闭容器(含有空气)内燃烧,容器内有关的量随时间变化的关系的图像( )
A B C D 3、将25g氯酸钾和6g二氧化锰的混合物加热一段时间后,得到残余固体质量为22 g,则产生氧气____g。
4、煤的气化是提高煤的利用率,减少环境污染的有效措施。煤的气化过程中发生了化学反应 C + H2O = CO + X。请你写出X的化学式 。9H2Thank you!
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
