江苏省江阴市2023-2024学年高一下学期期末考试化学(选修)试题(含答案)
文档属性
| 名称 | 江苏省江阴市2023-2024学年高一下学期期末考试化学(选修)试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 649.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-06-30 00:00:00 | ||
图片预览




文档简介
江阴市2023-2024学年高一下学期期末考试
化学 2024.06
注意事项:
1.本试卷分单项选择题和非选择题两部分,共100分。考试时间75分钟。
2.答案全部写在答题卡上,写在试题纸上一律无效。
3.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32 Cl 35.5
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.化学与人类社会的可持续发展密切相关。下列说法正确的是( )
A.胃舒平[主要成分:]是一种抗酸药
B.利用海水制取镁单质涉及的所有反应均为非氧化还原反应
C.研发催化剂将氧化为甲醇是促进“碳中和”直接有效的措施
D.为了使婴儿对食品有浓厚兴趣,可以在婴儿食品中加入大量着色剂
2.下列化学用语表述正确的是( )
A.乙烯的最简式为: B.羟基的电子式为:
C.乙醇和乙醚互为同分异构体 D.乙酸和乙酸乙酯属于同系物
阅读下列材料,回答第3-6题。
硫及其化合物有着广泛的作用。硫元素具有多种化合价,在一定条件下能发生相互转化。合理应用和处理含硫化合物,在生产、生活中有着重要意义。
3.火法炼铜主要发生的反应为,下列说法不正确的是( )
A.中铜的化合价为+1 B.该反应为置换反应
C.仅是氧化产物 D.中子数为16的硫原子:
4.某同学设计以下实验装置制取少量并探究其性质,能达到实验目的的是( )
A.装置A中使用的硫酸溶液是10%的稀硫酸 B.装置B中溶液褪色,说明具有还原性
C.装置C中溶液红色褪去,说明具有漂白性 D.用装置D收集并吸收尾气中的
5.下列有关硫及其化合物的性质与用途具有对应关系的是( )
A.硫单质呈黄色,可用作橡胶硫化剂
B.溶液呈酸性,可用于除去废水中的
C.浓硫酸具有强氧化性,可用作酯化反应的催化剂
D.具有还原性,可用于处理自来水中残留的
6.在指定条件下,下列所示的物质间转化不能实现的是( )
A.工业制酸: B.火山喷发:
C.尾气吸收: D.酸雨侵蚀:
7.下列化学材料的有关说法不正确的是( )
A.太阳能电池板将太阳能转化为电能,电池板芯片的主要成分为
B.火星探测器的天线接收器外壳为钛合金,钛合金属于金属材料
C.国产大型飞机C919用到的氮化硅陶瓷是新型无机非金属材料
D.量子通信材料螺旋碳纳米管与石墨烯互为同素异形体
8.乙烯等低碳烯烃是重要的基础有机化工原料,如图是一种新型催化甲烷合成低碳烯烃的工艺流程。有关说法正确的是( )
A.的空间结构为平面正方形 B.该工艺流程中,HCl是催化剂
C.低碳烯烃也可通过石油分馏大量获得 D.上述工艺实现了原子利用率达到100%
9.二苯乙醇酮可作为药物和润湿剂的原料,结构简式如图。下列有关该物质说法正确的是( )
A.化学式为 B.能发生水解反应
C.所有碳原子可能处于同一平面 D.与足量氢气加成所得分子中含有4个手性碳原子
10.化学是以实验为基础的科学。下列实验方案正确且能达到实验目的的是( )
选项 实验方案 实验目的
A 向乙醇中加入一小粒金属钠,观察现象 乙醇中是否含有水
B 向乙酸和乙酸乙酯的混合物加入饱和溶液充分振荡后静置分液 除去乙酸乙酯中的乙酸
C 将溴乙烷、乙醇和氢氧化钠的混合物加热,产生的气体直接通入酸性溶液中,溶液褪色 溴乙烷发生了消去反应
D 取少量苯丙烯醛()于试管中,滴加酸性溶液,紫红色褪去 苯丙烯醛中含有碳碳双键
11.化合物C是一种重要的药物中间体,可由下列方法获得:
下列说法正确的是( )
A.A分子所含硝基和氨基中N的化合价相同 B.B分子苯环上的一氯代物有4种
C.C中的含氧官能团有硝基、酰胺键和碳氯键 D.A、B生成C的反应类型是取代反应
12.已知羟醛缩合反应的过程如下:
下列说法不正确的是( )
A.上述反应可看作先后经历加成、消去的过程
B.上述过程可能得到的副产物为
C.羟醛缩合反应是有机合成中增长碳链的一种常用方法
D.与丙醛发生羟醛缩合反应的产物为
13.叠氮化钠()不溶于乙醚,易溶于水,常用于汽车安全防护袋的气源。尿素法制备水合肼(,强还原性)并利用其进一步反应制取NaN3的流程如下:
下列说法不正确的是( )
A.中存在的化学键有离子键和非极性共价键
B.吸收塔中发生反应的离子方程式为
C.反应器1中加料方式为向含NaClO的吸收液中加入并缓慢加入尿素
D.反应器2中加入无水乙醚的作用是降低的溶解度,有利于晶体析出
二、非选择题:共4题,共61分。
14.(15分)烟气中的主要含氮污染物有、NO,烟气脱硝是指去除氮氧化物的过程,从而大大减少对环境的污染。
(1)碱液吸收脱硝法
用NaOH溶液吸收烟气,主要反应如下:
;
①下列措施一定能提高NaOH溶液吸收烟气中NO和效率的有______(填字母)。
A.降低通入烟气的速率 B.气、液逆流吸收烟气 C.水浴加热NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到晶体,该晶体中的主要杂质是______(填化学式);吸收后排放的尾气中含量较高的氮氧化物是______(填化学式)。
(2)络合脱硝法
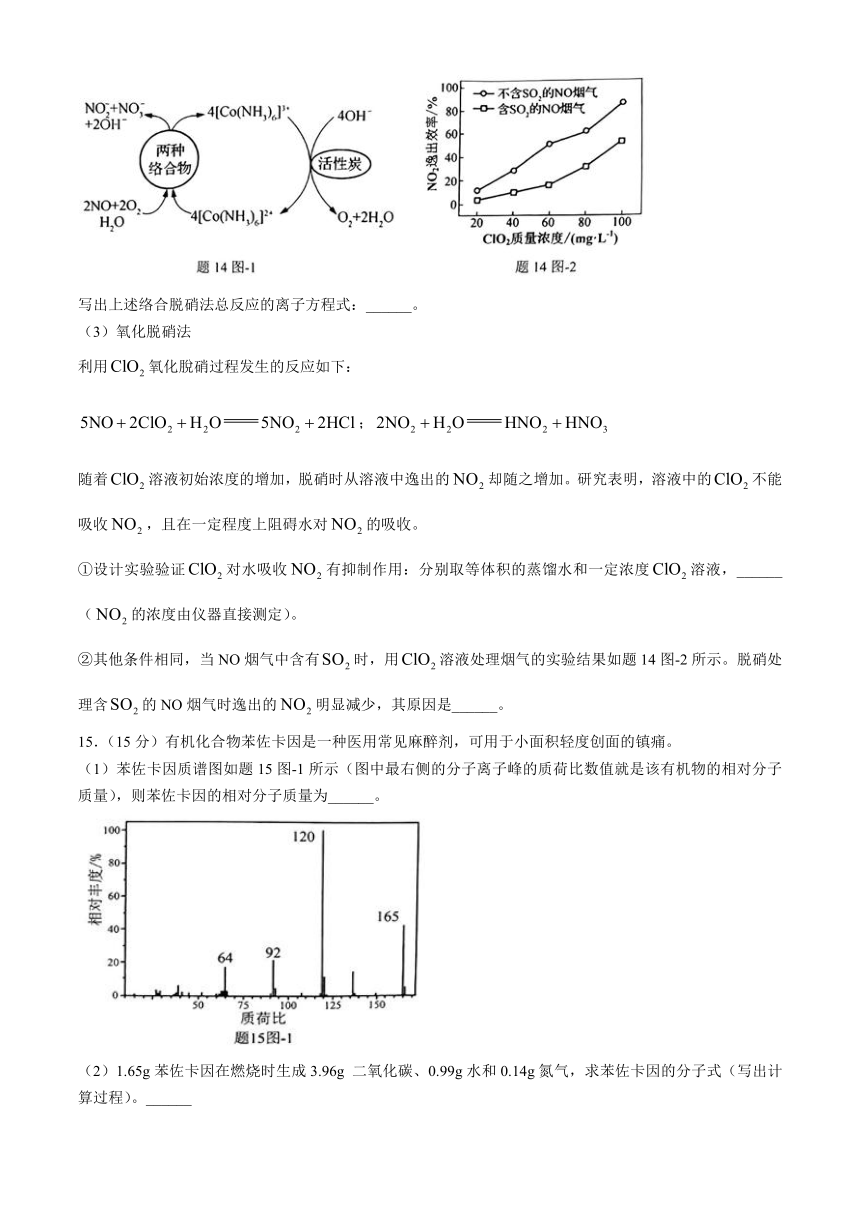
六氨合钴溶液中的能络合烟气中的NO和,形成的两种络合物在溶液中极易发生反应,实现NO的脱除。在吸收液中加入活性炭可有效催化的再生,维持溶液脱除NO的能力,原理如题14图-1所示。
写出上述络合脱硝法总反应的离子方程式:______。
(3)氧化脱硝法
利用氧化脫硝过程发生的反应如下:
;
随着溶液初始浓度的增加,脱硝时从溶液中逸出的却随之增加。研究表明,溶液中的不能吸收,且在一定程度上阻碍水对的吸收。
①设计实验验证对水吸收有抑制作用:分别取等体积的蒸馏水和一定浓度溶液,______(的浓度由仪器直接测定)。
②其他条件相同,当NO烟气中含有时,用溶液处理烟气的实验结果如题14图-2所示。脱硝处理含的NO烟气时逸出的明显减少,其原因是______。
15.(15分)有机化合物苯佐卡因是一种医用常见麻醉剂,可用于小面积轻度创面的镇痛。
(1)苯佐卡因质谱图如题15图-1所示(图中最右侧的分子离子峰的质荷比数值就是该有机物的相对分子质量),则苯佐卡因的相对分子质量为______。
(2)1.65g苯佐卡因在燃烧时生成3.96g 二氧化碳、0.99g水和0.14g氮气,求苯佐卡因的分子式(写出计算过程)。______
(3)苯佐卡因的红外光谱如题15图-2所示,且该物质的核磁共振氢谱有5个峰,其面积之比为3∶2∶2∶2∶2,则该物质的结构简式为______。
(4)写出苯佐卡因与氢氧化钠溶液在加热条件下发生反应的化学方程式______。
(5)苯佐卡因的一种芳香族同分异构体,具有三种不同化学环境的氢,满足条件的同分异构体的结构简式为______。
16.(16分)乙炔是重要的化工原料,一种药物中间体G合成路线如图所示:
(1)物质F所含的官能团名称______。
(2)物质D的结构简式为______。
(3)D与F反应时会生成副产物X,X与G互为同分异构体,X的结构简式为______。
(4)G的一种同分异构体同时满足下列条件,该同分异构体的结构简式为______。
①能使溶液发生显色反应
②1mol该物质与溴水反应,最多消耗2mol
③分子中含有4种不同化学环境的氢原子
(5)反应A→B机理示例如题16图-1所示。
①请按示例在答题卡题16图-2中标出反应A→E过程中分子中一个C原子和一个O原子所带电荷,并用箭头表示反应连接方式(原子所带负电荷用标注,原子所带正电荷用标注,箭头由带负电荷原子指向带正电荷原子)。
②已知:
下列流程中产物Y的结构简式为______。
17.(15分)化合物G是新型抗肿瘤药物,其合成路线如下:
已知:表示
(1)分子中处于同一平面上的原子个数最多为______。
(2)D→E的反应类型为______。
(3)F→G转化过程中还生成G的一种同分异构体M,M的结构简式为______。
(4)请写出同时符合下列条件的的一种同分异构体的结构简式:______。
①核磁共振氢谱显示有4组峰;
②能发生银镜反应,且酸性条件下水解产物之一能与溶液发生显色反应。
(5)已知:①(易被氧化)
②(在酸性条件下极易水解)
写出以和苯酚为原料制备的合成路线流程图(无机试剂、有机溶剂及原流程图中的试剂任用,合成路线流程图示例见本题题干)。
江阴市2023-2024学年高一下学期期末考试化学参考答案 2024.06
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.A 2.B 3.C 4.B 5.D 6.D 7.A 8.B 9.C 10.B 11.D 12.D 13.C
二、非选择题:共4题,共61分。
14.(15分)(1)①B(2分) ②(2分) NO(2分)
(2)(3分)
(3)①在相同时间内以相同的流速向两份溶液中通入,比较逸出的浓度,若通过蒸馏水逸出的浓度较小,则说明对的吸收有抑制作用(3分)
②溶液中的部分与发生反应,溶液中剩余的浓度减小。减弱了对水吸收的阻碍作用,逸出的明显减少(3分)
15.(15分)(1)165(1分)
(2) (1分)
(1分)
(1分)
(1分)
苯佐卡因分子式为(1分)
(3)(3分)
(4)(3分)
(5)或(3分)
16.(16分)(1)碳碳三键、酯基(2分)
(2)(2分)
(3)(3分)
(4)(3分)
(5)①(3分) ②(3分)
17.(15分)(1)13(2分)
(2)取代反应(2分)
(3)(3分)
(4)或(3分)
(5)(5分)
化学 2024.06
注意事项:
1.本试卷分单项选择题和非选择题两部分,共100分。考试时间75分钟。
2.答案全部写在答题卡上,写在试题纸上一律无效。
3.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32 Cl 35.5
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.化学与人类社会的可持续发展密切相关。下列说法正确的是( )
A.胃舒平[主要成分:]是一种抗酸药
B.利用海水制取镁单质涉及的所有反应均为非氧化还原反应
C.研发催化剂将氧化为甲醇是促进“碳中和”直接有效的措施
D.为了使婴儿对食品有浓厚兴趣,可以在婴儿食品中加入大量着色剂
2.下列化学用语表述正确的是( )
A.乙烯的最简式为: B.羟基的电子式为:
C.乙醇和乙醚互为同分异构体 D.乙酸和乙酸乙酯属于同系物
阅读下列材料,回答第3-6题。
硫及其化合物有着广泛的作用。硫元素具有多种化合价,在一定条件下能发生相互转化。合理应用和处理含硫化合物,在生产、生活中有着重要意义。
3.火法炼铜主要发生的反应为,下列说法不正确的是( )
A.中铜的化合价为+1 B.该反应为置换反应
C.仅是氧化产物 D.中子数为16的硫原子:
4.某同学设计以下实验装置制取少量并探究其性质,能达到实验目的的是( )
A.装置A中使用的硫酸溶液是10%的稀硫酸 B.装置B中溶液褪色,说明具有还原性
C.装置C中溶液红色褪去,说明具有漂白性 D.用装置D收集并吸收尾气中的
5.下列有关硫及其化合物的性质与用途具有对应关系的是( )
A.硫单质呈黄色,可用作橡胶硫化剂
B.溶液呈酸性,可用于除去废水中的
C.浓硫酸具有强氧化性,可用作酯化反应的催化剂
D.具有还原性,可用于处理自来水中残留的
6.在指定条件下,下列所示的物质间转化不能实现的是( )
A.工业制酸: B.火山喷发:
C.尾气吸收: D.酸雨侵蚀:
7.下列化学材料的有关说法不正确的是( )
A.太阳能电池板将太阳能转化为电能,电池板芯片的主要成分为
B.火星探测器的天线接收器外壳为钛合金,钛合金属于金属材料
C.国产大型飞机C919用到的氮化硅陶瓷是新型无机非金属材料
D.量子通信材料螺旋碳纳米管与石墨烯互为同素异形体
8.乙烯等低碳烯烃是重要的基础有机化工原料,如图是一种新型催化甲烷合成低碳烯烃的工艺流程。有关说法正确的是( )
A.的空间结构为平面正方形 B.该工艺流程中,HCl是催化剂
C.低碳烯烃也可通过石油分馏大量获得 D.上述工艺实现了原子利用率达到100%
9.二苯乙醇酮可作为药物和润湿剂的原料,结构简式如图。下列有关该物质说法正确的是( )
A.化学式为 B.能发生水解反应
C.所有碳原子可能处于同一平面 D.与足量氢气加成所得分子中含有4个手性碳原子
10.化学是以实验为基础的科学。下列实验方案正确且能达到实验目的的是( )
选项 实验方案 实验目的
A 向乙醇中加入一小粒金属钠,观察现象 乙醇中是否含有水
B 向乙酸和乙酸乙酯的混合物加入饱和溶液充分振荡后静置分液 除去乙酸乙酯中的乙酸
C 将溴乙烷、乙醇和氢氧化钠的混合物加热,产生的气体直接通入酸性溶液中,溶液褪色 溴乙烷发生了消去反应
D 取少量苯丙烯醛()于试管中,滴加酸性溶液,紫红色褪去 苯丙烯醛中含有碳碳双键
11.化合物C是一种重要的药物中间体,可由下列方法获得:
下列说法正确的是( )
A.A分子所含硝基和氨基中N的化合价相同 B.B分子苯环上的一氯代物有4种
C.C中的含氧官能团有硝基、酰胺键和碳氯键 D.A、B生成C的反应类型是取代反应
12.已知羟醛缩合反应的过程如下:
下列说法不正确的是( )
A.上述反应可看作先后经历加成、消去的过程
B.上述过程可能得到的副产物为
C.羟醛缩合反应是有机合成中增长碳链的一种常用方法
D.与丙醛发生羟醛缩合反应的产物为
13.叠氮化钠()不溶于乙醚,易溶于水,常用于汽车安全防护袋的气源。尿素法制备水合肼(,强还原性)并利用其进一步反应制取NaN3的流程如下:
下列说法不正确的是( )
A.中存在的化学键有离子键和非极性共价键
B.吸收塔中发生反应的离子方程式为
C.反应器1中加料方式为向含NaClO的吸收液中加入并缓慢加入尿素
D.反应器2中加入无水乙醚的作用是降低的溶解度,有利于晶体析出
二、非选择题:共4题,共61分。
14.(15分)烟气中的主要含氮污染物有、NO,烟气脱硝是指去除氮氧化物的过程,从而大大减少对环境的污染。
(1)碱液吸收脱硝法
用NaOH溶液吸收烟气,主要反应如下:
;
①下列措施一定能提高NaOH溶液吸收烟气中NO和效率的有______(填字母)。
A.降低通入烟气的速率 B.气、液逆流吸收烟气 C.水浴加热NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到晶体,该晶体中的主要杂质是______(填化学式);吸收后排放的尾气中含量较高的氮氧化物是______(填化学式)。
(2)络合脱硝法
六氨合钴溶液中的能络合烟气中的NO和,形成的两种络合物在溶液中极易发生反应,实现NO的脱除。在吸收液中加入活性炭可有效催化的再生,维持溶液脱除NO的能力,原理如题14图-1所示。
写出上述络合脱硝法总反应的离子方程式:______。
(3)氧化脱硝法
利用氧化脫硝过程发生的反应如下:
;
随着溶液初始浓度的增加,脱硝时从溶液中逸出的却随之增加。研究表明,溶液中的不能吸收,且在一定程度上阻碍水对的吸收。
①设计实验验证对水吸收有抑制作用:分别取等体积的蒸馏水和一定浓度溶液,______(的浓度由仪器直接测定)。
②其他条件相同,当NO烟气中含有时,用溶液处理烟气的实验结果如题14图-2所示。脱硝处理含的NO烟气时逸出的明显减少,其原因是______。
15.(15分)有机化合物苯佐卡因是一种医用常见麻醉剂,可用于小面积轻度创面的镇痛。
(1)苯佐卡因质谱图如题15图-1所示(图中最右侧的分子离子峰的质荷比数值就是该有机物的相对分子质量),则苯佐卡因的相对分子质量为______。
(2)1.65g苯佐卡因在燃烧时生成3.96g 二氧化碳、0.99g水和0.14g氮气,求苯佐卡因的分子式(写出计算过程)。______
(3)苯佐卡因的红外光谱如题15图-2所示,且该物质的核磁共振氢谱有5个峰,其面积之比为3∶2∶2∶2∶2,则该物质的结构简式为______。
(4)写出苯佐卡因与氢氧化钠溶液在加热条件下发生反应的化学方程式______。
(5)苯佐卡因的一种芳香族同分异构体,具有三种不同化学环境的氢,满足条件的同分异构体的结构简式为______。
16.(16分)乙炔是重要的化工原料,一种药物中间体G合成路线如图所示:
(1)物质F所含的官能团名称______。
(2)物质D的结构简式为______。
(3)D与F反应时会生成副产物X,X与G互为同分异构体,X的结构简式为______。
(4)G的一种同分异构体同时满足下列条件,该同分异构体的结构简式为______。
①能使溶液发生显色反应
②1mol该物质与溴水反应,最多消耗2mol
③分子中含有4种不同化学环境的氢原子
(5)反应A→B机理示例如题16图-1所示。
①请按示例在答题卡题16图-2中标出反应A→E过程中分子中一个C原子和一个O原子所带电荷,并用箭头表示反应连接方式(原子所带负电荷用标注,原子所带正电荷用标注,箭头由带负电荷原子指向带正电荷原子)。
②已知:
下列流程中产物Y的结构简式为______。
17.(15分)化合物G是新型抗肿瘤药物,其合成路线如下:
已知:表示
(1)分子中处于同一平面上的原子个数最多为______。
(2)D→E的反应类型为______。
(3)F→G转化过程中还生成G的一种同分异构体M,M的结构简式为______。
(4)请写出同时符合下列条件的的一种同分异构体的结构简式:______。
①核磁共振氢谱显示有4组峰;
②能发生银镜反应,且酸性条件下水解产物之一能与溶液发生显色反应。
(5)已知:①(易被氧化)
②(在酸性条件下极易水解)
写出以和苯酚为原料制备的合成路线流程图(无机试剂、有机溶剂及原流程图中的试剂任用,合成路线流程图示例见本题题干)。
江阴市2023-2024学年高一下学期期末考试化学参考答案 2024.06
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.A 2.B 3.C 4.B 5.D 6.D 7.A 8.B 9.C 10.B 11.D 12.D 13.C
二、非选择题:共4题,共61分。
14.(15分)(1)①B(2分) ②(2分) NO(2分)
(2)(3分)
(3)①在相同时间内以相同的流速向两份溶液中通入,比较逸出的浓度,若通过蒸馏水逸出的浓度较小,则说明对的吸收有抑制作用(3分)
②溶液中的部分与发生反应,溶液中剩余的浓度减小。减弱了对水吸收的阻碍作用,逸出的明显减少(3分)
15.(15分)(1)165(1分)
(2) (1分)
(1分)
(1分)
(1分)
苯佐卡因分子式为(1分)
(3)(3分)
(4)(3分)
(5)或(3分)
16.(16分)(1)碳碳三键、酯基(2分)
(2)(2分)
(3)(3分)
(4)(3分)
(5)①(3分) ②(3分)
17.(15分)(1)13(2分)
(2)取代反应(2分)
(3)(3分)
(4)或(3分)
(5)(5分)
同课章节目录
