江西省景德镇市2023-2024学年高一下学期6月期末考试化学试题(含答案)
文档属性
| 名称 | 江西省景德镇市2023-2024学年高一下学期6月期末考试化学试题(含答案) | 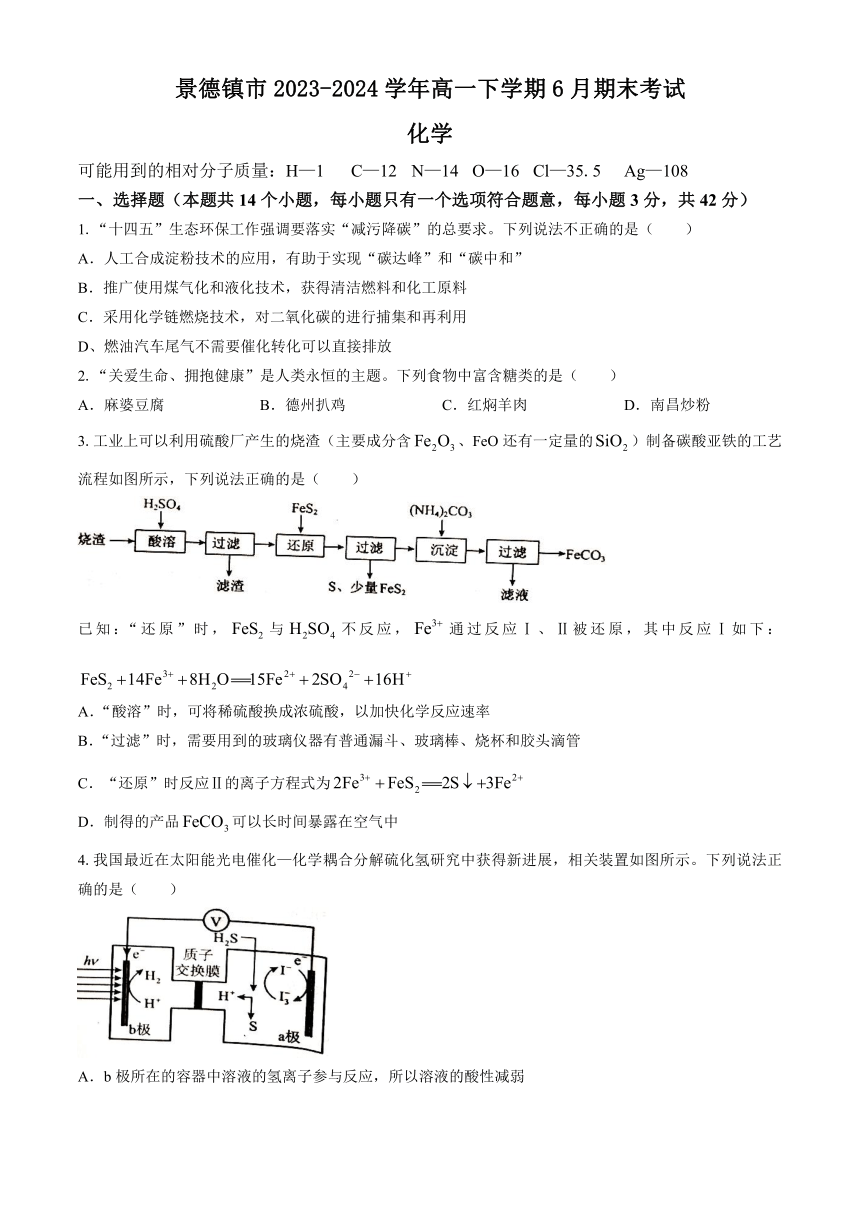 | |
| 格式 | docx | ||
| 文件大小 | 811.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-01 08:15:12 | ||
图片预览




文档简介
景德镇市2023-2024学年高一下学期6月期末考试
化学
可能用到的相对分子质量:H—1 C—12 N—14 O—16 Cl—35.5 Ag—108
一、选择题(本题共14个小题,每小题只有一个选项符合题意,每小题3分,共42分)
1.“十四五”生态环保工作强调要落实“减污降碳”的总要求。下列说法不正确的是( )
A.人工合成淀粉技术的应用,有助于实现“碳达峰”和“碳中和”
B.推广使用煤气化和液化技术,获得清洁燃料和化工原料
C.采用化学链燃烧技术,对二氧化碳的进行捕集和再利用
D、燃油汽车尾气不需要催化转化可以直接排放
2.“关爱生命、拥抱健康”是人类永恒的主题。下列食物中富含糖类的是( )
A.麻婆豆腐 B.德州扒鸡 C.红焖羊肉 D.南昌炒粉
3.工业上可以利用硫酸厂产生的烧渣(主要成分含、FeO还有一定量的)制备碳酸亚铁的工艺流程如图所示,下列说法正确的是( )
已知:“还原”时,与不反应,通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:
A.“酸溶”时,可将稀硫酸换成浓硫酸,以加快化学反应速率
B.“过滤”时,需要用到的玻璃仪器有普通漏斗、玻璃棒、烧杯和胶头滴管
C.“还原”时反应Ⅱ的离子方程式为
D.制得的产品可以长时间暴露在空气中
4.我国最近在太阳能光电催化—化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是( )
A.b极所在的容器中溶液的氢离子参与反应,所以溶液的酸性减弱
B.该装置总反应为
C.a极上发生的电极反应为
D.a极区需不断补充含和的溶液
5.有机物a、b、c的结构如图。下列说法正确的是( )
A.a的一氯代物有3种 B.b是的单体
C.c的二氯代物有4种 D.a、b、c互为同分异构体
6.某化学兴趣小组用如图所示装置探究与的反应,将该装置置于阳光下照射,开始实验。下列说法错误的是( )
A.软管内会发生取代反应,生成物可能有5种
B.充分反应后,打开,导管口可能会有白雾出现
C.软管内会有油状液滴产生
D.透明软管内气体颜色会逐渐变浅,透明软管的体积会缩小直至完全凹瘪
7.我们知道,任何化学反应过程中一定有物质变化,同时伴随着能量变化。下图横坐标表示反应过程,纵坐标表示能量,关于下图的说法不正确的是( )
A.1mol固态碘与1mol氢气化合生成2mol HI气体时,需要吸收5kJ的能量
B.2mol HI气体分解生成1mol碘蒸气与1mol氢气时需要吸收12kJ的能量
C.1mol固态碘变为1mol碘蒸气时需要吸收17kJ的能量
D.碘蒸气与氢气生成HI气体的反应是吸热反应
8.海洋是一座巨大的化学资源宝库,如图是从海水中提取若干种化学物质的流程图,则下列说法正确的是( )
A.除去粗盐中的、、,依次加入足量的NaOH、、溶液
B.用贝壳为原料生产石灰乳,可用于①中沉淀
C.②中包含制取溶液、无水及热还原法冶炼Mg几个阶段
D.③④⑤中溴元素均被氧化
9.下列关于热化学反应的描述正确的是( )
A.由C(石墨)=C(金刚石) 可知,石墨能量更高,燃烧热更大
B.已知 ,则在一定条件下将4mol 和2mol 置于一密闭容器中充分反应,放出的热量等于392kJ
C.在稀溶液中: ,若将含1mol 的醋酸溶液与含1mol 的氨水溶液混合,放出的热量小于57.3kJ
D.中和热测定实验中可用金属材质的环形搅拌棒代替环形玻璃搅拌棒
10.下列有机实验操作正确的是( )
A.鸡蛋白溶液中,加入醋酸铅溶液有沉淀析出,加入水后沉淀不溶解
B.制乙酸乙酯:大试管中加入浓硫酸,然后慢慢加入无水乙醇和乙酸
C.检验蔗糖在酸催化下的水解产物:向水解液中加入少量新制备的,再水浴加热观察现象
D.制备纯净的氯乙烷:等物质的量的氯气与乙烷在光照条件下反应
11.下列叙述中,正确的有几个( )
①烷烃中除甲烷外,很多都能使酸性溶液的紫色褪去
②甲烷中存在少量的乙烯可以通过高锰酸钾溶液除去,使甲烷中无杂质
③氯仿没有同分异构体可证明甲烷是正四面体结构
④乙烷在光照条件下与氯气发生取代反应可能生成的有机物共9种
⑤苯属于芳香烃
⑥煤的干馏、石油的分馏及催化裂化都属于化学变化
⑦乙酸乙酯的碱性水解叫做皂化反应
A.4个 B.3个 C.2个 D.1个
12.柠檬酸的结构简式如图,下列说法正确的是( )
A.1mol柠檬酸可与4mol NaOH发生中和反应
B.柠檬酸中能发生酯化反应的官能团有2种
C.1mol柠檬酸与反应生成3mol
D.柠檬酸与在Cu作催化剂、加热的条件下,能发生催化氧化反应
13.已知 ,
,
若使23g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )kJ
A. B.
C. D.
14.阿司匹林是一种重要的药物,化学名称为乙酰水杨酸(),水杨酸()和乙酸酐()在一定的条件下发生取代反应可制得乙酰水杨酸及物质X,下列说法正确的是( )
B.乙酰水杨酸的分子式为
A.水杨酸含有三种官能团
C.物质X为
D.标准状况下,1mol水杨酸和金属钠完全反应能产生11.2L氢气
二、非选择题(本题共4小题,共58分)
15.(14分)
Ⅰ.现有下列几种有机物:① ② ③ ④癸烷 ⑤
⑥ ⑦ ⑧丙烷。请根据上述物质按要求回答下列问题。
(1)与密度(同温同压下)相同的烷烃的为 (填序号)。
(2)与③互为同分异构体的是 (填序号)。
(3)有机物②与在Cu作催化剂、加热的条件下反应的化学方程式为
。
(4)在120℃、Pa条件下,某种气态烃与足量的,完全反应后,测得反应前后气体的体积没有发生改变,则该烃是 (填序号)。
Ⅱ.写出下列热化学方程式
(5)已知:0.4mol液态肼()与足量的液态双氧水反应,生成氮气和水蒸气,并放出256.6kJ的热量,反应的热化学方程式为 。
(6)已知充分燃烧a g乙炔()气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,乙炔燃烧的热化学方程式为 。
(7)在一定条件下与反应生成,已知拆开1mol H—H键、1mol N—H键、1mol N≡N键分别需要的能量是436kJ、391kJ、945.7kJ,则与反应生成的热化学方程式为:
。
16.(16分)
工业上1,2-二氯乙烷()是重要的有机生产原料,不溶于水,易溶于有机溶剂。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置图如下:
回答下列问题
(1)仪器A的名称是 ,其中发生反应的离子方程为 。
(2)装置丁中多孔球泡的作用是 。
(3)写出丁装置中发生反应的化学方程式 。
(4)己装置中水的作用是 。
(5)实验时应先在丁装置中预先加入少量1,2二氯乙烷液体,作用是 。
a.溶解和乙烯 b.作催化剂 c.促进气体反应物间的接触
(6)制得的1,2-二氯乙烷中溶解有、乙烯,可适当加热将气体逐出,逐出的气体可依次通过NaOH溶液、 以达到尾气处理的目的。
(7)产品纯度的测定:量取5.0mL逐出和乙烯后的产品,产品密度为1.2,加足量稀NaOH溶液,加热充分反应:。所得溶液先用稀硝酸中和至酸性,然后加入1.000的标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为 %。
17.(14分)
某气态烃A与的相对密度为14,其产量可以用来衡量一个国家的石油化工发展水平。以该化合物为原料合成化合物G、E和I的流程如下:
已知:
Ⅰ.芳香族化合物F为C、H、O化合物,其相对分子质量为166,环上的一氯代物有一种,1mol F与足量溶液反应能生成2mol ,F与B反应生成G。
Ⅱ.H为二元醇,其蒸气密度折算成标准状况为2.77g/L,H与足量D反应生成I。
(1)A的电子式为 ,C的官能团的名称为 。
(2)F的分子式为 。
(3)若G的分子式为,写出反应⑤的化学方程式 ,反应类型为 。
(4)某学生用新制的检验C的官能团,取1mol/L 溶液和1mol/L NaOH方各1mL,在一支洁净的试管内混合后,向其中又加入0.5mL 40%的C,加热后无红色沉出现。该同学实验失败的原因可能是 。(选填序号)
①加入的C过多 ②加入的C太少
③加入溶液的量过多 ④加入溶液的量不够
(5)H的同系物J的相对分子质量比H大14,已知同一个碳原子上不能连接两个羟基,则J的所有可能结构简式为 (不考虑立体异构)。
18.(14分)
浩瀚的海洋里蕴藏着丰富的化学资源,从海带中提取碘单质的工艺流程如图。回答下列问题:
(1)在实验室进行于海带的灼烧操作时,是将海带放入 (填仪器名称)中,用酒精灯充分加热灰化。
(2)浸取液中碘主要以存在,写出①发生反应的离子方程式 ,实验步骤①后若检验溶液中碘单质的存在,具体方法是 。
(3)已知步骤②中加入浓NaOH溶液发生反应后得到的氧化产物为,写出该步骤的化学方程式 ,步骤③反应中氧化剂与还原剂物质的量之比为 。
(4)操作c的名称为 。
(5)已知:,氯气既可以氧化,也可以氧化。往200mL 溶液中通入8.96L(标准状况),反应完成后,溶液中有被氧化,则原溶液的物质的量浓度为 。
景德镇市2023-2024学年高一下学期6月期末考试
化学答案
1 2 3 4 5 6 7
D D C B A D D
8 9 10 11 12 13 14
B C A C B C C
15.【答案】(1)⑧
(2)⑦
(3)
(4)①
(5)
(6)
(7)
16.【答案】
(1)圆底烧瓶
(2)增大气体与液体的接触面积,使反应物反应更充分
(3)
(4)除去乙醇
(5)ac
(6)溴水或溴的四氯化碳溶液
(7)82.5%
17.【答案】
(1) 醛基
(2)C8H6O4
(3)
酯化反应或取代反应
(4)③
(5)HO-CH2-CHOH-CH3、HO-CH2-CH2-CH2-OH
18.【答案】
(1)坩埚
(2)2I-+H2O2+2H+=I2+2H2O
取氧化后的溶液少量于试管中,滴加淀粉溶液,若溶液变蓝证明含碘
(3)3I2+6NaOH=5NaI+NaIO3+3H2O 1∶5
(4)过滤
(5)1.6
化学
可能用到的相对分子质量:H—1 C—12 N—14 O—16 Cl—35.5 Ag—108
一、选择题(本题共14个小题,每小题只有一个选项符合题意,每小题3分,共42分)
1.“十四五”生态环保工作强调要落实“减污降碳”的总要求。下列说法不正确的是( )
A.人工合成淀粉技术的应用,有助于实现“碳达峰”和“碳中和”
B.推广使用煤气化和液化技术,获得清洁燃料和化工原料
C.采用化学链燃烧技术,对二氧化碳的进行捕集和再利用
D、燃油汽车尾气不需要催化转化可以直接排放
2.“关爱生命、拥抱健康”是人类永恒的主题。下列食物中富含糖类的是( )
A.麻婆豆腐 B.德州扒鸡 C.红焖羊肉 D.南昌炒粉
3.工业上可以利用硫酸厂产生的烧渣(主要成分含、FeO还有一定量的)制备碳酸亚铁的工艺流程如图所示,下列说法正确的是( )
已知:“还原”时,与不反应,通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:
A.“酸溶”时,可将稀硫酸换成浓硫酸,以加快化学反应速率
B.“过滤”时,需要用到的玻璃仪器有普通漏斗、玻璃棒、烧杯和胶头滴管
C.“还原”时反应Ⅱ的离子方程式为
D.制得的产品可以长时间暴露在空气中
4.我国最近在太阳能光电催化—化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是( )
A.b极所在的容器中溶液的氢离子参与反应,所以溶液的酸性减弱
B.该装置总反应为
C.a极上发生的电极反应为
D.a极区需不断补充含和的溶液
5.有机物a、b、c的结构如图。下列说法正确的是( )
A.a的一氯代物有3种 B.b是的单体
C.c的二氯代物有4种 D.a、b、c互为同分异构体
6.某化学兴趣小组用如图所示装置探究与的反应,将该装置置于阳光下照射,开始实验。下列说法错误的是( )
A.软管内会发生取代反应,生成物可能有5种
B.充分反应后,打开,导管口可能会有白雾出现
C.软管内会有油状液滴产生
D.透明软管内气体颜色会逐渐变浅,透明软管的体积会缩小直至完全凹瘪
7.我们知道,任何化学反应过程中一定有物质变化,同时伴随着能量变化。下图横坐标表示反应过程,纵坐标表示能量,关于下图的说法不正确的是( )
A.1mol固态碘与1mol氢气化合生成2mol HI气体时,需要吸收5kJ的能量
B.2mol HI气体分解生成1mol碘蒸气与1mol氢气时需要吸收12kJ的能量
C.1mol固态碘变为1mol碘蒸气时需要吸收17kJ的能量
D.碘蒸气与氢气生成HI气体的反应是吸热反应
8.海洋是一座巨大的化学资源宝库,如图是从海水中提取若干种化学物质的流程图,则下列说法正确的是( )
A.除去粗盐中的、、,依次加入足量的NaOH、、溶液
B.用贝壳为原料生产石灰乳,可用于①中沉淀
C.②中包含制取溶液、无水及热还原法冶炼Mg几个阶段
D.③④⑤中溴元素均被氧化
9.下列关于热化学反应的描述正确的是( )
A.由C(石墨)=C(金刚石) 可知,石墨能量更高,燃烧热更大
B.已知 ,则在一定条件下将4mol 和2mol 置于一密闭容器中充分反应,放出的热量等于392kJ
C.在稀溶液中: ,若将含1mol 的醋酸溶液与含1mol 的氨水溶液混合,放出的热量小于57.3kJ
D.中和热测定实验中可用金属材质的环形搅拌棒代替环形玻璃搅拌棒
10.下列有机实验操作正确的是( )
A.鸡蛋白溶液中,加入醋酸铅溶液有沉淀析出,加入水后沉淀不溶解
B.制乙酸乙酯:大试管中加入浓硫酸,然后慢慢加入无水乙醇和乙酸
C.检验蔗糖在酸催化下的水解产物:向水解液中加入少量新制备的,再水浴加热观察现象
D.制备纯净的氯乙烷:等物质的量的氯气与乙烷在光照条件下反应
11.下列叙述中,正确的有几个( )
①烷烃中除甲烷外,很多都能使酸性溶液的紫色褪去
②甲烷中存在少量的乙烯可以通过高锰酸钾溶液除去,使甲烷中无杂质
③氯仿没有同分异构体可证明甲烷是正四面体结构
④乙烷在光照条件下与氯气发生取代反应可能生成的有机物共9种
⑤苯属于芳香烃
⑥煤的干馏、石油的分馏及催化裂化都属于化学变化
⑦乙酸乙酯的碱性水解叫做皂化反应
A.4个 B.3个 C.2个 D.1个
12.柠檬酸的结构简式如图,下列说法正确的是( )
A.1mol柠檬酸可与4mol NaOH发生中和反应
B.柠檬酸中能发生酯化反应的官能团有2种
C.1mol柠檬酸与反应生成3mol
D.柠檬酸与在Cu作催化剂、加热的条件下,能发生催化氧化反应
13.已知 ,
,
若使23g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )kJ
A. B.
C. D.
14.阿司匹林是一种重要的药物,化学名称为乙酰水杨酸(),水杨酸()和乙酸酐()在一定的条件下发生取代反应可制得乙酰水杨酸及物质X,下列说法正确的是( )
B.乙酰水杨酸的分子式为
A.水杨酸含有三种官能团
C.物质X为
D.标准状况下,1mol水杨酸和金属钠完全反应能产生11.2L氢气
二、非选择题(本题共4小题,共58分)
15.(14分)
Ⅰ.现有下列几种有机物:① ② ③ ④癸烷 ⑤
⑥ ⑦ ⑧丙烷。请根据上述物质按要求回答下列问题。
(1)与密度(同温同压下)相同的烷烃的为 (填序号)。
(2)与③互为同分异构体的是 (填序号)。
(3)有机物②与在Cu作催化剂、加热的条件下反应的化学方程式为
。
(4)在120℃、Pa条件下,某种气态烃与足量的,完全反应后,测得反应前后气体的体积没有发生改变,则该烃是 (填序号)。
Ⅱ.写出下列热化学方程式
(5)已知:0.4mol液态肼()与足量的液态双氧水反应,生成氮气和水蒸气,并放出256.6kJ的热量,反应的热化学方程式为 。
(6)已知充分燃烧a g乙炔()气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,乙炔燃烧的热化学方程式为 。
(7)在一定条件下与反应生成,已知拆开1mol H—H键、1mol N—H键、1mol N≡N键分别需要的能量是436kJ、391kJ、945.7kJ,则与反应生成的热化学方程式为:
。
16.(16分)
工业上1,2-二氯乙烷()是重要的有机生产原料,不溶于水,易溶于有机溶剂。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置图如下:
回答下列问题
(1)仪器A的名称是 ,其中发生反应的离子方程为 。
(2)装置丁中多孔球泡的作用是 。
(3)写出丁装置中发生反应的化学方程式 。
(4)己装置中水的作用是 。
(5)实验时应先在丁装置中预先加入少量1,2二氯乙烷液体,作用是 。
a.溶解和乙烯 b.作催化剂 c.促进气体反应物间的接触
(6)制得的1,2-二氯乙烷中溶解有、乙烯,可适当加热将气体逐出,逐出的气体可依次通过NaOH溶液、 以达到尾气处理的目的。
(7)产品纯度的测定:量取5.0mL逐出和乙烯后的产品,产品密度为1.2,加足量稀NaOH溶液,加热充分反应:。所得溶液先用稀硝酸中和至酸性,然后加入1.000的标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为 %。
17.(14分)
某气态烃A与的相对密度为14,其产量可以用来衡量一个国家的石油化工发展水平。以该化合物为原料合成化合物G、E和I的流程如下:
已知:
Ⅰ.芳香族化合物F为C、H、O化合物,其相对分子质量为166,环上的一氯代物有一种,1mol F与足量溶液反应能生成2mol ,F与B反应生成G。
Ⅱ.H为二元醇,其蒸气密度折算成标准状况为2.77g/L,H与足量D反应生成I。
(1)A的电子式为 ,C的官能团的名称为 。
(2)F的分子式为 。
(3)若G的分子式为,写出反应⑤的化学方程式 ,反应类型为 。
(4)某学生用新制的检验C的官能团,取1mol/L 溶液和1mol/L NaOH方各1mL,在一支洁净的试管内混合后,向其中又加入0.5mL 40%的C,加热后无红色沉出现。该同学实验失败的原因可能是 。(选填序号)
①加入的C过多 ②加入的C太少
③加入溶液的量过多 ④加入溶液的量不够
(5)H的同系物J的相对分子质量比H大14,已知同一个碳原子上不能连接两个羟基,则J的所有可能结构简式为 (不考虑立体异构)。
18.(14分)
浩瀚的海洋里蕴藏着丰富的化学资源,从海带中提取碘单质的工艺流程如图。回答下列问题:
(1)在实验室进行于海带的灼烧操作时,是将海带放入 (填仪器名称)中,用酒精灯充分加热灰化。
(2)浸取液中碘主要以存在,写出①发生反应的离子方程式 ,实验步骤①后若检验溶液中碘单质的存在,具体方法是 。
(3)已知步骤②中加入浓NaOH溶液发生反应后得到的氧化产物为,写出该步骤的化学方程式 ,步骤③反应中氧化剂与还原剂物质的量之比为 。
(4)操作c的名称为 。
(5)已知:,氯气既可以氧化,也可以氧化。往200mL 溶液中通入8.96L(标准状况),反应完成后,溶液中有被氧化,则原溶液的物质的量浓度为 。
景德镇市2023-2024学年高一下学期6月期末考试
化学答案
1 2 3 4 5 6 7
D D C B A D D
8 9 10 11 12 13 14
B C A C B C C
15.【答案】(1)⑧
(2)⑦
(3)
(4)①
(5)
(6)
(7)
16.【答案】
(1)圆底烧瓶
(2)增大气体与液体的接触面积,使反应物反应更充分
(3)
(4)除去乙醇
(5)ac
(6)溴水或溴的四氯化碳溶液
(7)82.5%
17.【答案】
(1) 醛基
(2)C8H6O4
(3)
酯化反应或取代反应
(4)③
(5)HO-CH2-CHOH-CH3、HO-CH2-CH2-CH2-OH
18.【答案】
(1)坩埚
(2)2I-+H2O2+2H+=I2+2H2O
取氧化后的溶液少量于试管中,滴加淀粉溶液,若溶液变蓝证明含碘
(3)3I2+6NaOH=5NaI+NaIO3+3H2O 1∶5
(4)过滤
(5)1.6
同课章节目录
