江西省上进联考2023-2024学年高一下学期期末调研检测化学试题(含解析)
文档属性
| 名称 | 江西省上进联考2023-2024学年高一下学期期末调研检测化学试题(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-04 08:36:33 | ||
图片预览

文档简介
江西省上进联考2023-2024学年高一下学期期末调研检测
化学试卷
试卷共6页,18小题,满分100分。考试用时75分钟。
注意事项:
1.考查范围:必修第二册。
2.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡指定位置上。
3.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考生必须保持答题卡的整洁。考试结束后,请将答题卡交回。
可能用到的相对原子质量:H-1 C-12
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是最符合题目要求的。
1.江西有很多珍贵的非物质文化遗产,下列非物质文化遗产涉及的物品的主要成分不属于无机物的是( )
A.婺源歙砚 B.景德镇瓷器 C.新干剪纸 D.南丰泥炉
2.下列化学用语表示正确的是( )
A.一氯甲烷的电子式: B.聚丙烯的结构简式:
C.乙酸的结构式: D.乙烷的球棍模型:
3.下列叙述中不涉及氧化还原反应的是( )
A.酸雨的形成
B.豆科植物根瘤菌固氮
C.锌和稀硫酸反应时加入少量硫酸铜溶液能加快产生氢气的速率
D.胃酸过多病人服用氢氧化铝作为抗酸药
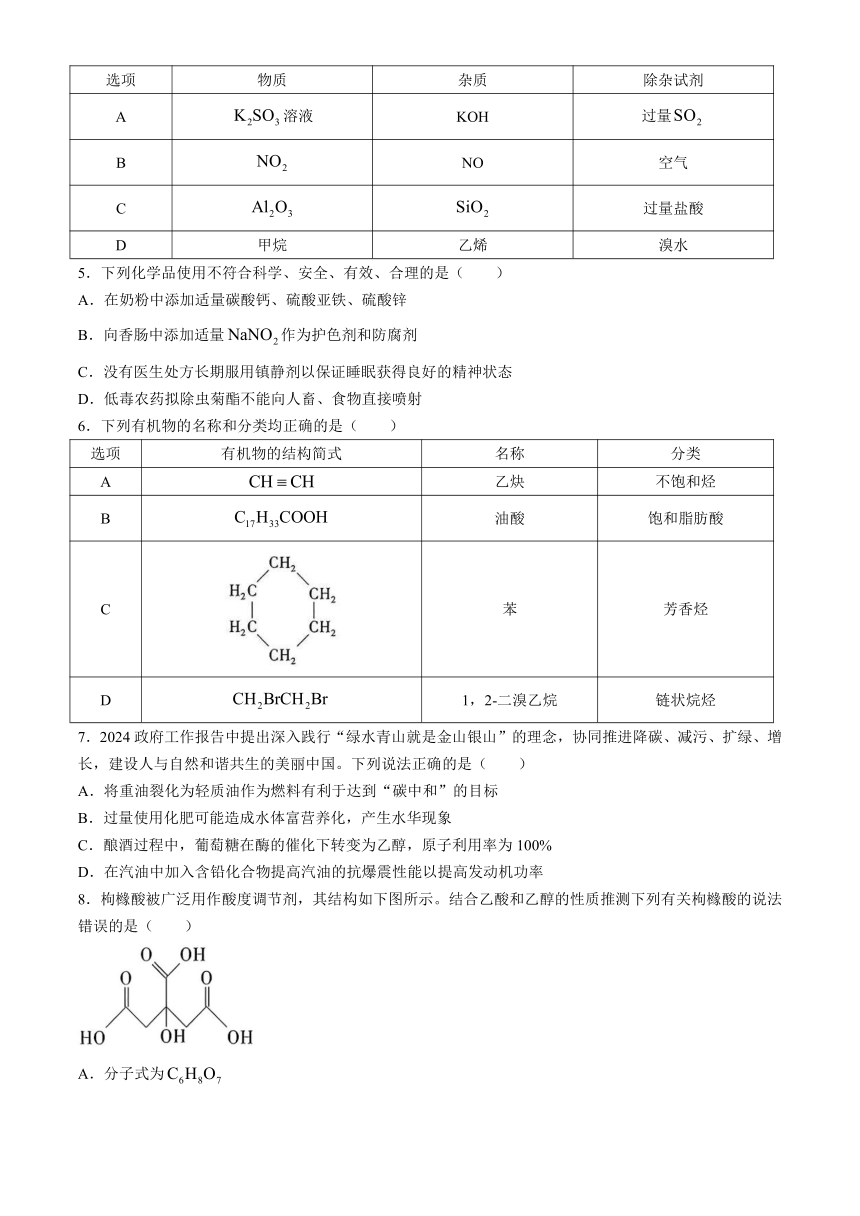
4.为除去下列物质中的杂质,除杂试剂选择合理的是( )
选项 物质 杂质 除杂试剂
A 溶液 KOH 过量
B NO 空气
C 过量盐酸
D 甲烷 乙烯 溴水
5.下列化学品使用不符合科学、安全、有效、合理的是( )
A.在奶粉中添加适量碳酸钙、硫酸亚铁、硫酸锌
B.向香肠中添加适量作为护色剂和防腐剂
C.没有医生处方长期服用镇静剂以保证睡眠获得良好的精神状态
D.低毒农药拟除虫菊酯不能向人畜、食物直接喷射
6.下列有机物的名称和分类均正确的是( )
选项 有机物的结构简式 名称 分类
A 乙炔 不饱和烃
B 油酸 饱和脂肪酸
C 苯 芳香烃
D 1,2-二溴乙烷 链状烷烃
7.2024政府工作报告中提出深入践行“绿水青山就是金山银山”的理念,协同推进降碳、减污、扩绿、增长,建设人与自然和谐共生的美丽中国。下列说法正确的是( )
A.将重油裂化为轻质油作为燃料有利于达到“碳中和”的目标
B.过量使用化肥可能造成水体富营养化,产生水华现象
C.酿酒过程中,葡萄糖在酶的催化下转变为乙醇,原子利用率为100%
D.在汽油中加入含铅化合物提高汽油的抗爆震性能以提高发动机功率
8.枸橼酸被广泛用作酸度调节剂,其结构如下图所示。结合乙酸和乙醇的性质推测下列有关枸橼酸的说法错误的是( )
A.分子式为
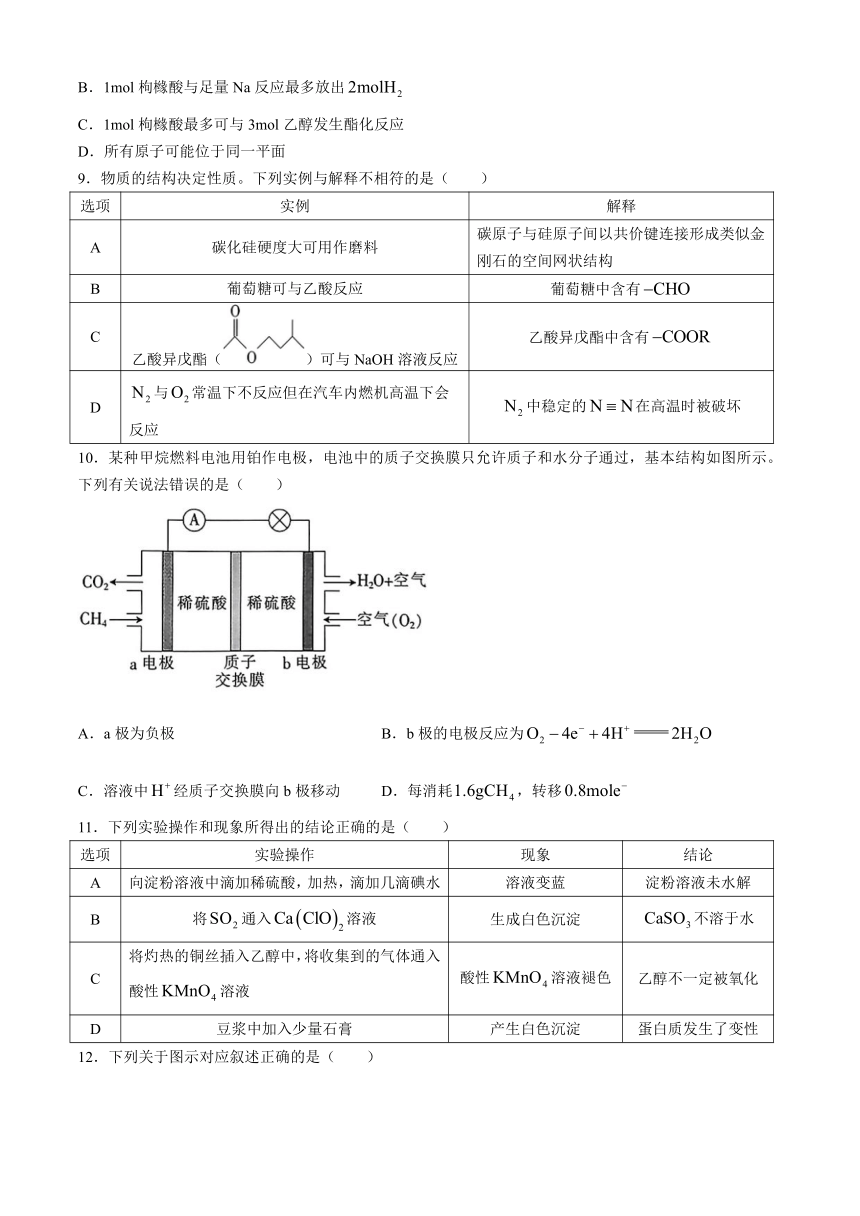
B.1mol枸橼酸与足量Na反应最多放出
C.1mol枸橼酸最多可与3mol乙醇发生酯化反应
D.所有原子可能位于同一平面
9.物质的结构决定性质。下列实例与解释不相符的是( )
选项 实例 解释
A 碳化硅硬度大可用作磨料 碳原子与硅原子间以共价键连接形成类似金刚石的空间网状结构
B 葡萄糖可与乙酸反应 葡萄糖中含有
C 乙酸异戊酯()可与NaOH溶液反应 乙酸异戊酯中含有
D 与常温下不反应但在汽车内燃机高温下会反应 中稳定的在高温时被破坏
10.某种甲烷燃料电池用铂作电极,电池中的质子交换膜只允许质子和水分子通过,基本结构如图所示。下列有关说法错误的是( )
A.a极为负极 B.b极的电极反应为
C.溶液中经质子交换膜向b极移动 D.每消耗,转移
11.下列实验操作和现象所得出的结论正确的是( )
选项 实验操作 现象 结论
A 向淀粉溶液中滴加稀硫酸,加热,滴加几滴碘水 溶液变蓝 淀粉溶液未水解
B 将通入溶液 生成白色沉淀 不溶于水
C 将灼热的铜丝插入乙醇中,将收集到的气体通入酸性溶液 酸性溶液褪色 乙醇不一定被氧化
D 豆浆中加入少量石膏 产生白色沉淀 蛋白质发生了变性
12.下列关于图示对应叙述正确的是( )
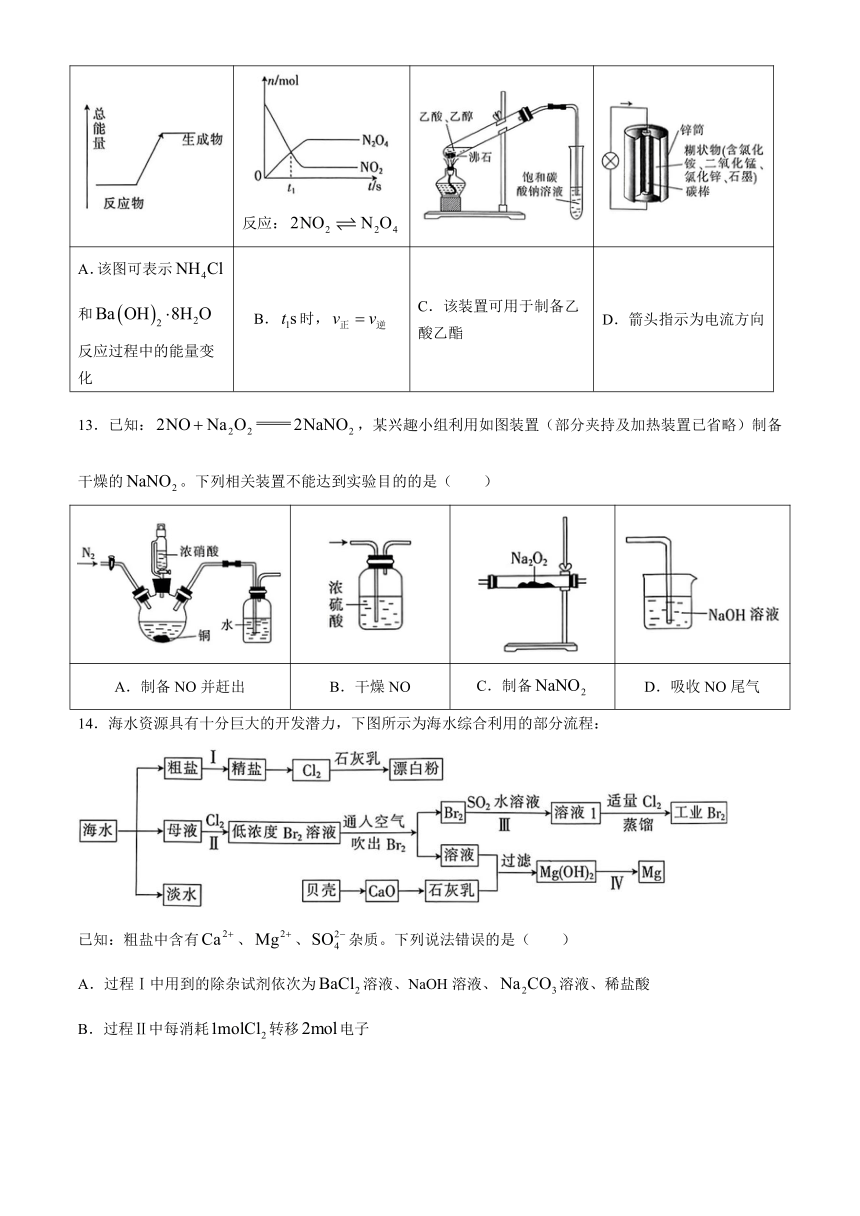
反应:
A.该图可表示和反应过程中的能量变化 B.时, C.该装置可用于制备乙酸乙酯 D.箭头指示为电流方向
13.已知:,某兴趣小组利用如图装置(部分夹持及加热装置已省略)制备干燥的。下列相关装置不能达到实验目的的是( )
A.制备NO并赶出 B.干燥NO C.制备 D.吸收NO尾气
14.海水资源具有十分巨大的开发潜力,下图所示为海水综合利用的部分流程:
已知:粗盐中含有、、杂质。下列说法错误的是( )
A.过程Ⅰ中用到的除杂试剂依次为溶液、NaOH溶液、溶液、稀盐酸
B.过程Ⅱ中每消耗转移电子
C.过程Ⅱ的离子方程式为
D.过程Ⅳ可将先转化为,再电解熔融得到Mg
二、非选择题:本题共4小题,共58分。
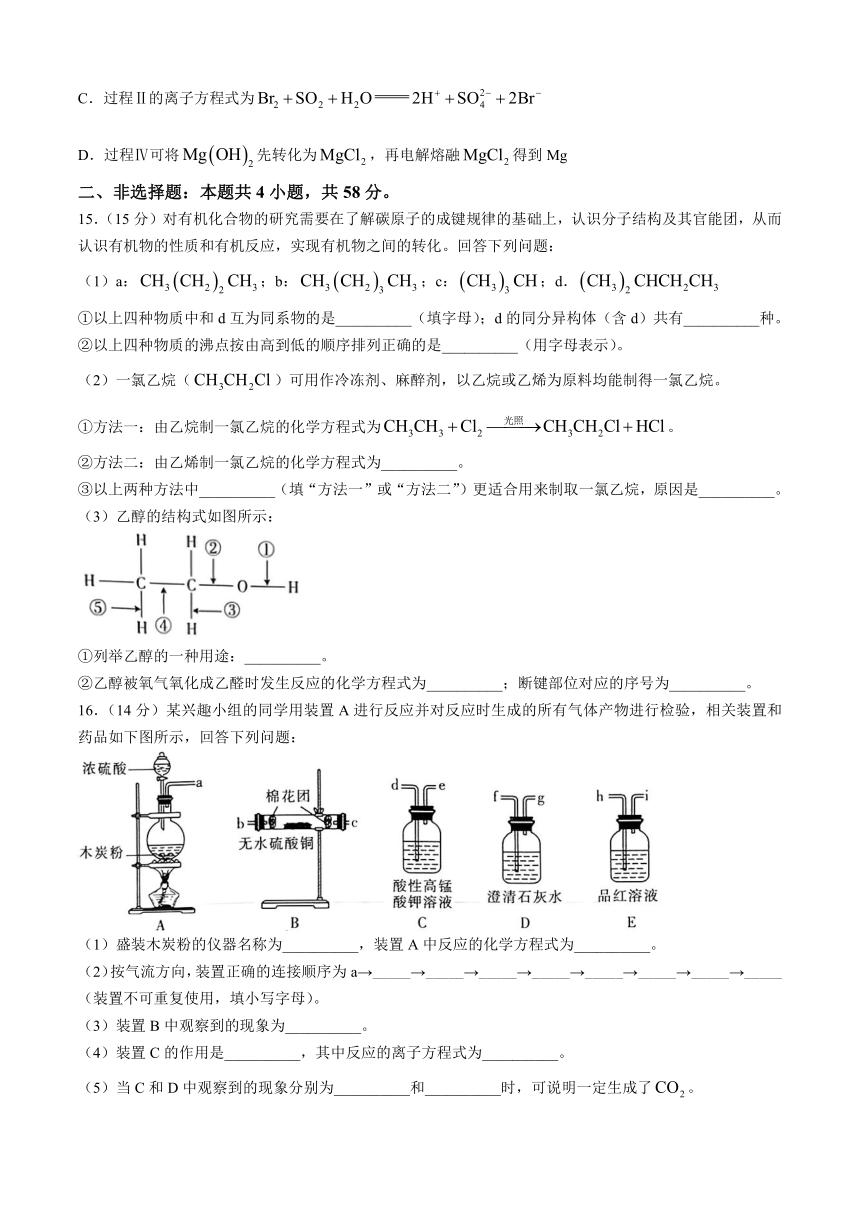
15.(15分)对有机化合物的研究需要在了解碳原子的成键规律的基础上,认识分子结构及其官能团,从而认识有机物的性质和有机反应,实现有机物之间的转化。回答下列问题:
(1)a:;b:;c:;d.
①以上四种物质中和d互为同系物的是__________(填字母);d的同分异构体(含d)共有__________种。
②以上四种物质的沸点按由高到低的顺序排列正确的是__________(用字母表示)。
(2)一氯乙烷()可用作冷冻剂、麻醉剂,以乙烷或乙烯为原料均能制得一氯乙烷。
①方法一:由乙烷制一氯乙烷的化学方程式为。
②方法二:由乙烯制一氯乙烷的化学方程式为__________。
③以上两种方法中__________(填“方法一”或“方法二”)更适合用来制取一氯乙烷,原因是__________。
(3)乙醇的结构式如图所示:
①列举乙醇的一种用途:__________。
②乙醇被氧气氧化成乙醛时发生反应的化学方程式为__________;断键部位对应的序号为__________。
16.(14分)某兴趣小组的同学用装置A进行反应并对反应时生成的所有气体产物进行检验,相关装置和药品如下图所示,回答下列问题:
(1)盛装木炭粉的仪器名称为__________,装置A中反应的化学方程式为__________。
(2)按气流方向,装置正确的连接顺序为a→_____→_____→_____→_____→_____→_____→_____→_____(装置不可重复使用,填小写字母)。
(3)装置B中观察到的现象为__________。
(4)装置C的作用是__________,其中反应的离子方程式为__________。
(5)当C和D中观察到的现象分别为__________和__________时,可说明一定生成了。
17.(15分)一种工业制硝酸的流程如下图所示,已知氨的沸点为-33.33 ℃,熔点为-77.7℃。
回答下列问题:
(1)“氧化1”的化学方程式为__________,“操作X”具体为__________。
(2)“吸收”时通入空气的目的是__________。
(3)用催化还原法处理硝酸工厂的尾气的化学方程式为。一定温度下,向体积为2L的恒容密闭容器中充入和使其浓度均为,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示。
①曲线B表示__________(填物质的化学式)的物质的量随时间的变化关系。
②在5min内的化学反应速率为__________。
③5min末时,的平衡转化率为__________(保留3位有效数字)。
④c点处,__________(填“>”“<”或“=”,下同);若保持其他条件不变,更换高效催化剂,c点对应横轴的坐标__________5。
18.(14分)聚甲基丙烯酸甲酯(H)具有高透明度,低价格,易于机械加工等优点,是平常经常使用的玻璃替代材料。一种合成路线如下图所示:
回答下列问题:
(1)反应①中X的化学式为__________,①过程中还可能会产生另一种物质M,M的结构简式为__________。
(2)反应③的反应类型为__________。
(3)E中官能团的名称为__________。
(4)反应⑥的化学方程式为__________,反应类型为__________。
(5)H的结构简式为__________。
高一化学参考答案
1.【答案】C
【解析】歙砚的主要矿物成分为绢云母、石英、黄铁矿、磁黄铁矿、褐铁矿、炭质等,A项不符合题意;高岭土是陶瓷工业最重要的原材料,B项不符合题意;剪纸的主要成分为纤维素,C项符合题意;南丰泥炉为江西省南丰县生产的传统陶器日用品,系选用优质泥料,经精制烧炼而成,D项不符合题意。
2.【答案】C
【解析】一氯甲烷的电子式中原子周围应有8个电子,A项错误;聚丙烯的结构简式为,B项错误;乙酸的结构式为,C项正确;为乙烷的空间填充模型,D项错误。
3.【答案】D
【解析】酸雨形成过程中,、被氧化成、,A项涉及氧化还原反应;豆科植物根瘤菌固氮指将空气中游离态的氮转化为含氮化合物的过程,B项涉及氧化还原反应;锌与置换出来的铜、稀硫酸形成原电池反应,化学反应速率加快,C项涉及氧化还原反应;氢氧化铝与盐酸的反应无元素化合价变化,D项不涉及氧化还原反应。
4.【答案】D
【解析】过量通入溶液中可得到溶液,物质被反应,A项错误;空气中含有多种气体,会引入新杂质,B项错误;与过量盐酸发生反应生成,还需再加入过量氨水,过滤、洗涤、灼烧,得到,C项错误;乙烯可与溴水中的溴单质反应生成油状物质,且甲烷与溴水不反应,D项正确。
5.【答案】C
【解析】可在奶粉中添加适量碳酸钙、硫酸亚铁、硫酸锌作为营养强化剂,A项正确;可以用作为护色剂和防腐剂,但由于有一定毒性,必须注意不能过量,B项正确;没有医生处方镇静剂和安眠药不能长期服用,C项错误;低毒农药拟除虫菊酯不能向人畜、食物直接喷射,防止中毒,D项正确。
6.【答案】A
【解析】乙炔含有碳碳三键属于炔烃,属于不饱和烃,A项正确;油酸是不饱和脂肪酸,B项错误;环己烷的名称错误且属于环状烷烃、不属于芳香烃,C项错误;1,2-二溴乙烷不只含碳、氢元素,不属于烃,D项错误。
7.【答案】B
【解析】将重油裂化为轻质油并不能减少二氧化碳的排放量,达不到碳中和的目的,A项错误;过量使用化肥,化肥可能随雨水流入江河湖泊,造成水体富营养化,产生水华现象,B项正确;葡萄糖在酶的催化下生成乙醇和,原子利用率达不到100%,C项错误;在汽油中加入含铅化合物会造成环境重金属污染,D项错误。
8.【答案】D
【解析】由结构可知,枸橼酸的分子式为,A项正确;1mol枸橼酸中含有3mol羧基和1mol羟基,均可与Na反应,反应最多放出,B项正确;1mol枸橼酸中含有3mol羧基,最多可与3mol乙醇发生酯化反应,C项正确;枸橼酸中含有饱和碳原子,以饱和碳原子为中心连接的四个原子形成四面体结构,枸橼酸中的所有原子不可能位于同一平面上,D项错误。
9.【答案】B
【解析】碳化硅中碳原子与硅原子间以共价键连接形成类似金刚石的空间网状结构,硬度很大,可用作磨料,A项不符合题意;葡萄糖中含有,可与乙酸反应,B项符合题意;乙酸异戊酯()因含有(酯基)可与溶液发生水解反应,C项不符合题意;中含有的稳定的在高温时被破坏,与反应生成NO,D项不符合题意。
10.【答案】B
【解析】电池总反应方程式为,是还原剂,是氧化剂,则装置中极为负极,极为正极,A项正确;极的电极反应式为,极的电极反应式为,B项错误;极为正极,经质子交换膜向极移动,C项正确;每消耗(0.1mol),消耗,转移,D项正确。
11.【答案】C
【解析】溶液变蓝说明有淀粉存在,可能淀粉未水解完全,A项错误;将氧化,白色沉淀为,B项错误;挥发的乙醇和反应生成的乙醛均能使酸性溶液褪色,则不能验证乙醇一定被氧化,C项正确;豆浆中加入少量石膏,使豆浆中的蛋白质聚沉,D项错误。
12.【答案】A
【解析】与的反应为吸热反应,与图示相符,A项正确;时,只能说明,并不能说明,B项错误;制备乙酸乙酯时,还需要浓硫酸作催化剂,且导管不能插入溶液中,C项错误;箭头指示为电子流动方向,D项错误。
13.【答案】D
【解析】铜和浓硝酸反应生成,通过水后转化为NO,A项正确;NO不与浓硫酸反应,可用浓硫酸作为干燥剂,B项正确;硬质玻璃管可作为制备的反应器,C项正确;NO不与碱溶液反应,不能用碱溶液吸收,可用酸性溶液吸收;D项错误。
14.【答案】C
【解析】依次加入溶液、NaOH溶液、溶液、稀盐酸除去、、杂质,并且不引入新杂质,A项正确;过程Ⅱ中反应的离子方程式为,每消耗转移电子,B项正确;过程Ⅲ的离子方程式为,C项错误;过程Ⅳ可将转化为,再电解熔融得到,D项正确。
15.【答案】(1)①ac(2分,写对1个得1分,多选或错选不得分) 3(2分);②bdac(或,2分)
(2)②(2分,反应物或生成物写错、未配平不得分,漏写反应条件扣1分,反应条件写“一定条件”也得分)
③方法二(1分) 副产物较少,产物较为纯净(1分,合理即可)
(3)①燃料、有机化工原料、有机溶剂或消毒剂(答一条即可,1分)
②(2分,反应物或生成物写错、未配平不得分,漏写反应条件扣1分,条件写“催化剂”也得分) ①和③(2分)
【解析】(1)①同系物是指结构相似、分子组成相差若干个“”原子团的有机化合物,和互为同系物的是、。d的同分异构体(含d)共有3种:,,;②烷烃的沸点随着分子中碳原子数的增加逐渐升高;碳原子数相同的烃,支链越多,熔、沸点越低;a、c中碳原子都是4个,a无支链,c中有支链,沸点:;b、d中碳原子数都是5,b无支链,d中有支链,沸点:;b、d中碳原子数为5,比a、c中碳原子数都多,则沸点较高,故沸点由高到低的排列顺序是bdac。
(2)②在催化剂、加热条件下,乙烯与发生加成反应生成氯乙烷,反应的化学方程式为,反应类型为加成反应;③用乙烷与氯气制备氯乙烷时,副产物较多,目标物质不纯净,而乙烯与的加成反应,只生成氯乙烷,则更适合用来制取一氯乙烷的为方法二。
(3)①乙醇可作为燃料、有机化工原料、有机溶剂和消毒剂等;②乙醇被氧气氧化成乙醛时发生反应的化学方程式为;断键部位对应的序号为①和③。
16.【答案】(1)圆底烧瓶(1分) (2分,反应物或生成物写错、未配平不得分,漏写反应条件或气体符号不扣分)
(2)(2分)
(3)白色粉末变为蓝色(2分)
(4)吸收(除去)(1分,合理即可) (2分,反应物或生成物写错、未配平不得分)
(5)紫色未全部褪去(2分,合理即可) 澄清石灰水变浑浊(2分,合理即可)
【解析】(1)盛装木炭粉的仪器名称为圆底烧瓶,装置中反应的化学方程式为。
(2)无水硫酸铜、品红溶液、酸性高锰酸钾溶液、澄清石灰水四种试剂分别用于检验水、检验、吸收、检验。考虑到气体检验时的相互干扰,应先用无水硫酸铜检验水、再用品红溶液检验、再用酸性高锰酸钾溶液吸收、然后用澄清石灰水检验,按气流方向,装置正确的连接顺序为。
(3)装置B用于检验水,观察到的现象为白色粉末变为蓝色。
(4)装置C的作用是吸收(除去),其中反应的化学方程式为,离子方程式为。
(5)当C中的紫色未全部褪去,说明溶液过量,被全部吸收,D中现象为澄清石灰水吸收变浑浊,可说明一定生成了。
17.【答案】(1)(2分,反应物或生成物写错、未配平不得分,漏写反应条件不扣分)液化或冷却至(或-34)℃(1分)
(2)使充分被水吸收,减少氮氧化物(有毒气体)的排放(2分,合理即可)
(3)①(2分) ②(2分) ③(2分) ④=(2分) <(2分)
【解析】(1)“氧化1”的化学方程式为,“操作X”为冷却至-33.33℃,分离出未反应的液氨,可应用于流程中的汽化工序,再次进行氧化。
(2)“吸收”时通入空气的目的是使充分被水吸收,减少氮氧化物(有毒气体)的排放。
(3)①5min内,A物质的物质的量的变化量为0.2mol,B物质的物质的量的变化量为0.4mol,所以A和B在该反应中的化学计量数之比为,因此A为,B为;②在5min内的平均反应速率为;③5min末时,达到平衡,的物质的量变化量为0.2mol,则的物质的量变化量为,可知的平衡转化率为;④c点处,已达到该条件下该反应的限度,为化学平衡状态,正、逆反应速率相等,故即为化学平衡状态,若保持其他条件不变,更换高效催化剂,反应速率加快,达到平衡所用时间变短,c点对应横轴的坐标小于5。
18.【答案】(1)(2分) (2分)
(2)加成反应(2分)
(3)羟基、羧基(2分,写对1个得1分)
(4)(2分,反应物或生成物写错、未配平不得分,漏写反应条件扣1分) 取代反应或酯化反应(2分)
(5)(2分)
【解析】(1)反应①为丙烯()和水发生加成反应生成,故的化学式为,丙烯与水发生加成反应还可能生成。
(2)对比反应物和产物可知反应③中碳氧双键断裂,与HCN发生加成反应。
(3)中官能团的名称为羟基和羧基。
(4)模仿乙酸和乙醇的反应写出反应⑥的化学方程式为,反应类型为取代反应或酯化反应。
(5)反应⑦为加成聚合反应,的结构简式为。
化学试卷
试卷共6页,18小题,满分100分。考试用时75分钟。
注意事项:
1.考查范围:必修第二册。
2.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡指定位置上。
3.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考生必须保持答题卡的整洁。考试结束后,请将答题卡交回。
可能用到的相对原子质量:H-1 C-12
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是最符合题目要求的。
1.江西有很多珍贵的非物质文化遗产,下列非物质文化遗产涉及的物品的主要成分不属于无机物的是( )
A.婺源歙砚 B.景德镇瓷器 C.新干剪纸 D.南丰泥炉
2.下列化学用语表示正确的是( )
A.一氯甲烷的电子式: B.聚丙烯的结构简式:
C.乙酸的结构式: D.乙烷的球棍模型:
3.下列叙述中不涉及氧化还原反应的是( )
A.酸雨的形成
B.豆科植物根瘤菌固氮
C.锌和稀硫酸反应时加入少量硫酸铜溶液能加快产生氢气的速率
D.胃酸过多病人服用氢氧化铝作为抗酸药
4.为除去下列物质中的杂质,除杂试剂选择合理的是( )
选项 物质 杂质 除杂试剂
A 溶液 KOH 过量
B NO 空气
C 过量盐酸
D 甲烷 乙烯 溴水
5.下列化学品使用不符合科学、安全、有效、合理的是( )
A.在奶粉中添加适量碳酸钙、硫酸亚铁、硫酸锌
B.向香肠中添加适量作为护色剂和防腐剂
C.没有医生处方长期服用镇静剂以保证睡眠获得良好的精神状态
D.低毒农药拟除虫菊酯不能向人畜、食物直接喷射
6.下列有机物的名称和分类均正确的是( )
选项 有机物的结构简式 名称 分类
A 乙炔 不饱和烃
B 油酸 饱和脂肪酸
C 苯 芳香烃
D 1,2-二溴乙烷 链状烷烃
7.2024政府工作报告中提出深入践行“绿水青山就是金山银山”的理念,协同推进降碳、减污、扩绿、增长,建设人与自然和谐共生的美丽中国。下列说法正确的是( )
A.将重油裂化为轻质油作为燃料有利于达到“碳中和”的目标
B.过量使用化肥可能造成水体富营养化,产生水华现象
C.酿酒过程中,葡萄糖在酶的催化下转变为乙醇,原子利用率为100%
D.在汽油中加入含铅化合物提高汽油的抗爆震性能以提高发动机功率
8.枸橼酸被广泛用作酸度调节剂,其结构如下图所示。结合乙酸和乙醇的性质推测下列有关枸橼酸的说法错误的是( )
A.分子式为
B.1mol枸橼酸与足量Na反应最多放出
C.1mol枸橼酸最多可与3mol乙醇发生酯化反应
D.所有原子可能位于同一平面
9.物质的结构决定性质。下列实例与解释不相符的是( )
选项 实例 解释
A 碳化硅硬度大可用作磨料 碳原子与硅原子间以共价键连接形成类似金刚石的空间网状结构
B 葡萄糖可与乙酸反应 葡萄糖中含有
C 乙酸异戊酯()可与NaOH溶液反应 乙酸异戊酯中含有
D 与常温下不反应但在汽车内燃机高温下会反应 中稳定的在高温时被破坏
10.某种甲烷燃料电池用铂作电极,电池中的质子交换膜只允许质子和水分子通过,基本结构如图所示。下列有关说法错误的是( )
A.a极为负极 B.b极的电极反应为
C.溶液中经质子交换膜向b极移动 D.每消耗,转移
11.下列实验操作和现象所得出的结论正确的是( )
选项 实验操作 现象 结论
A 向淀粉溶液中滴加稀硫酸,加热,滴加几滴碘水 溶液变蓝 淀粉溶液未水解
B 将通入溶液 生成白色沉淀 不溶于水
C 将灼热的铜丝插入乙醇中,将收集到的气体通入酸性溶液 酸性溶液褪色 乙醇不一定被氧化
D 豆浆中加入少量石膏 产生白色沉淀 蛋白质发生了变性
12.下列关于图示对应叙述正确的是( )
反应:
A.该图可表示和反应过程中的能量变化 B.时, C.该装置可用于制备乙酸乙酯 D.箭头指示为电流方向
13.已知:,某兴趣小组利用如图装置(部分夹持及加热装置已省略)制备干燥的。下列相关装置不能达到实验目的的是( )
A.制备NO并赶出 B.干燥NO C.制备 D.吸收NO尾气
14.海水资源具有十分巨大的开发潜力,下图所示为海水综合利用的部分流程:
已知:粗盐中含有、、杂质。下列说法错误的是( )
A.过程Ⅰ中用到的除杂试剂依次为溶液、NaOH溶液、溶液、稀盐酸
B.过程Ⅱ中每消耗转移电子
C.过程Ⅱ的离子方程式为
D.过程Ⅳ可将先转化为,再电解熔融得到Mg
二、非选择题:本题共4小题,共58分。
15.(15分)对有机化合物的研究需要在了解碳原子的成键规律的基础上,认识分子结构及其官能团,从而认识有机物的性质和有机反应,实现有机物之间的转化。回答下列问题:
(1)a:;b:;c:;d.
①以上四种物质中和d互为同系物的是__________(填字母);d的同分异构体(含d)共有__________种。
②以上四种物质的沸点按由高到低的顺序排列正确的是__________(用字母表示)。
(2)一氯乙烷()可用作冷冻剂、麻醉剂,以乙烷或乙烯为原料均能制得一氯乙烷。
①方法一:由乙烷制一氯乙烷的化学方程式为。
②方法二:由乙烯制一氯乙烷的化学方程式为__________。
③以上两种方法中__________(填“方法一”或“方法二”)更适合用来制取一氯乙烷,原因是__________。
(3)乙醇的结构式如图所示:
①列举乙醇的一种用途:__________。
②乙醇被氧气氧化成乙醛时发生反应的化学方程式为__________;断键部位对应的序号为__________。
16.(14分)某兴趣小组的同学用装置A进行反应并对反应时生成的所有气体产物进行检验,相关装置和药品如下图所示,回答下列问题:
(1)盛装木炭粉的仪器名称为__________,装置A中反应的化学方程式为__________。
(2)按气流方向,装置正确的连接顺序为a→_____→_____→_____→_____→_____→_____→_____→_____(装置不可重复使用,填小写字母)。
(3)装置B中观察到的现象为__________。
(4)装置C的作用是__________,其中反应的离子方程式为__________。
(5)当C和D中观察到的现象分别为__________和__________时,可说明一定生成了。
17.(15分)一种工业制硝酸的流程如下图所示,已知氨的沸点为-33.33 ℃,熔点为-77.7℃。
回答下列问题:
(1)“氧化1”的化学方程式为__________,“操作X”具体为__________。
(2)“吸收”时通入空气的目的是__________。
(3)用催化还原法处理硝酸工厂的尾气的化学方程式为。一定温度下,向体积为2L的恒容密闭容器中充入和使其浓度均为,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示。
①曲线B表示__________(填物质的化学式)的物质的量随时间的变化关系。
②在5min内的化学反应速率为__________。
③5min末时,的平衡转化率为__________(保留3位有效数字)。
④c点处,__________(填“>”“<”或“=”,下同);若保持其他条件不变,更换高效催化剂,c点对应横轴的坐标__________5。
18.(14分)聚甲基丙烯酸甲酯(H)具有高透明度,低价格,易于机械加工等优点,是平常经常使用的玻璃替代材料。一种合成路线如下图所示:
回答下列问题:
(1)反应①中X的化学式为__________,①过程中还可能会产生另一种物质M,M的结构简式为__________。
(2)反应③的反应类型为__________。
(3)E中官能团的名称为__________。
(4)反应⑥的化学方程式为__________,反应类型为__________。
(5)H的结构简式为__________。
高一化学参考答案
1.【答案】C
【解析】歙砚的主要矿物成分为绢云母、石英、黄铁矿、磁黄铁矿、褐铁矿、炭质等,A项不符合题意;高岭土是陶瓷工业最重要的原材料,B项不符合题意;剪纸的主要成分为纤维素,C项符合题意;南丰泥炉为江西省南丰县生产的传统陶器日用品,系选用优质泥料,经精制烧炼而成,D项不符合题意。
2.【答案】C
【解析】一氯甲烷的电子式中原子周围应有8个电子,A项错误;聚丙烯的结构简式为,B项错误;乙酸的结构式为,C项正确;为乙烷的空间填充模型,D项错误。
3.【答案】D
【解析】酸雨形成过程中,、被氧化成、,A项涉及氧化还原反应;豆科植物根瘤菌固氮指将空气中游离态的氮转化为含氮化合物的过程,B项涉及氧化还原反应;锌与置换出来的铜、稀硫酸形成原电池反应,化学反应速率加快,C项涉及氧化还原反应;氢氧化铝与盐酸的反应无元素化合价变化,D项不涉及氧化还原反应。
4.【答案】D
【解析】过量通入溶液中可得到溶液,物质被反应,A项错误;空气中含有多种气体,会引入新杂质,B项错误;与过量盐酸发生反应生成,还需再加入过量氨水,过滤、洗涤、灼烧,得到,C项错误;乙烯可与溴水中的溴单质反应生成油状物质,且甲烷与溴水不反应,D项正确。
5.【答案】C
【解析】可在奶粉中添加适量碳酸钙、硫酸亚铁、硫酸锌作为营养强化剂,A项正确;可以用作为护色剂和防腐剂,但由于有一定毒性,必须注意不能过量,B项正确;没有医生处方镇静剂和安眠药不能长期服用,C项错误;低毒农药拟除虫菊酯不能向人畜、食物直接喷射,防止中毒,D项正确。
6.【答案】A
【解析】乙炔含有碳碳三键属于炔烃,属于不饱和烃,A项正确;油酸是不饱和脂肪酸,B项错误;环己烷的名称错误且属于环状烷烃、不属于芳香烃,C项错误;1,2-二溴乙烷不只含碳、氢元素,不属于烃,D项错误。
7.【答案】B
【解析】将重油裂化为轻质油并不能减少二氧化碳的排放量,达不到碳中和的目的,A项错误;过量使用化肥,化肥可能随雨水流入江河湖泊,造成水体富营养化,产生水华现象,B项正确;葡萄糖在酶的催化下生成乙醇和,原子利用率达不到100%,C项错误;在汽油中加入含铅化合物会造成环境重金属污染,D项错误。
8.【答案】D
【解析】由结构可知,枸橼酸的分子式为,A项正确;1mol枸橼酸中含有3mol羧基和1mol羟基,均可与Na反应,反应最多放出,B项正确;1mol枸橼酸中含有3mol羧基,最多可与3mol乙醇发生酯化反应,C项正确;枸橼酸中含有饱和碳原子,以饱和碳原子为中心连接的四个原子形成四面体结构,枸橼酸中的所有原子不可能位于同一平面上,D项错误。
9.【答案】B
【解析】碳化硅中碳原子与硅原子间以共价键连接形成类似金刚石的空间网状结构,硬度很大,可用作磨料,A项不符合题意;葡萄糖中含有,可与乙酸反应,B项符合题意;乙酸异戊酯()因含有(酯基)可与溶液发生水解反应,C项不符合题意;中含有的稳定的在高温时被破坏,与反应生成NO,D项不符合题意。
10.【答案】B
【解析】电池总反应方程式为,是还原剂,是氧化剂,则装置中极为负极,极为正极,A项正确;极的电极反应式为,极的电极反应式为,B项错误;极为正极,经质子交换膜向极移动,C项正确;每消耗(0.1mol),消耗,转移,D项正确。
11.【答案】C
【解析】溶液变蓝说明有淀粉存在,可能淀粉未水解完全,A项错误;将氧化,白色沉淀为,B项错误;挥发的乙醇和反应生成的乙醛均能使酸性溶液褪色,则不能验证乙醇一定被氧化,C项正确;豆浆中加入少量石膏,使豆浆中的蛋白质聚沉,D项错误。
12.【答案】A
【解析】与的反应为吸热反应,与图示相符,A项正确;时,只能说明,并不能说明,B项错误;制备乙酸乙酯时,还需要浓硫酸作催化剂,且导管不能插入溶液中,C项错误;箭头指示为电子流动方向,D项错误。
13.【答案】D
【解析】铜和浓硝酸反应生成,通过水后转化为NO,A项正确;NO不与浓硫酸反应,可用浓硫酸作为干燥剂,B项正确;硬质玻璃管可作为制备的反应器,C项正确;NO不与碱溶液反应,不能用碱溶液吸收,可用酸性溶液吸收;D项错误。
14.【答案】C
【解析】依次加入溶液、NaOH溶液、溶液、稀盐酸除去、、杂质,并且不引入新杂质,A项正确;过程Ⅱ中反应的离子方程式为,每消耗转移电子,B项正确;过程Ⅲ的离子方程式为,C项错误;过程Ⅳ可将转化为,再电解熔融得到,D项正确。
15.【答案】(1)①ac(2分,写对1个得1分,多选或错选不得分) 3(2分);②bdac(或,2分)
(2)②(2分,反应物或生成物写错、未配平不得分,漏写反应条件扣1分,反应条件写“一定条件”也得分)
③方法二(1分) 副产物较少,产物较为纯净(1分,合理即可)
(3)①燃料、有机化工原料、有机溶剂或消毒剂(答一条即可,1分)
②(2分,反应物或生成物写错、未配平不得分,漏写反应条件扣1分,条件写“催化剂”也得分) ①和③(2分)
【解析】(1)①同系物是指结构相似、分子组成相差若干个“”原子团的有机化合物,和互为同系物的是、。d的同分异构体(含d)共有3种:,,;②烷烃的沸点随着分子中碳原子数的增加逐渐升高;碳原子数相同的烃,支链越多,熔、沸点越低;a、c中碳原子都是4个,a无支链,c中有支链,沸点:;b、d中碳原子数都是5,b无支链,d中有支链,沸点:;b、d中碳原子数为5,比a、c中碳原子数都多,则沸点较高,故沸点由高到低的排列顺序是bdac。
(2)②在催化剂、加热条件下,乙烯与发生加成反应生成氯乙烷,反应的化学方程式为,反应类型为加成反应;③用乙烷与氯气制备氯乙烷时,副产物较多,目标物质不纯净,而乙烯与的加成反应,只生成氯乙烷,则更适合用来制取一氯乙烷的为方法二。
(3)①乙醇可作为燃料、有机化工原料、有机溶剂和消毒剂等;②乙醇被氧气氧化成乙醛时发生反应的化学方程式为;断键部位对应的序号为①和③。
16.【答案】(1)圆底烧瓶(1分) (2分,反应物或生成物写错、未配平不得分,漏写反应条件或气体符号不扣分)
(2)(2分)
(3)白色粉末变为蓝色(2分)
(4)吸收(除去)(1分,合理即可) (2分,反应物或生成物写错、未配平不得分)
(5)紫色未全部褪去(2分,合理即可) 澄清石灰水变浑浊(2分,合理即可)
【解析】(1)盛装木炭粉的仪器名称为圆底烧瓶,装置中反应的化学方程式为。
(2)无水硫酸铜、品红溶液、酸性高锰酸钾溶液、澄清石灰水四种试剂分别用于检验水、检验、吸收、检验。考虑到气体检验时的相互干扰,应先用无水硫酸铜检验水、再用品红溶液检验、再用酸性高锰酸钾溶液吸收、然后用澄清石灰水检验,按气流方向,装置正确的连接顺序为。
(3)装置B用于检验水,观察到的现象为白色粉末变为蓝色。
(4)装置C的作用是吸收(除去),其中反应的化学方程式为,离子方程式为。
(5)当C中的紫色未全部褪去,说明溶液过量,被全部吸收,D中现象为澄清石灰水吸收变浑浊,可说明一定生成了。
17.【答案】(1)(2分,反应物或生成物写错、未配平不得分,漏写反应条件不扣分)液化或冷却至(或-34)℃(1分)
(2)使充分被水吸收,减少氮氧化物(有毒气体)的排放(2分,合理即可)
(3)①(2分) ②(2分) ③(2分) ④=(2分) <(2分)
【解析】(1)“氧化1”的化学方程式为,“操作X”为冷却至-33.33℃,分离出未反应的液氨,可应用于流程中的汽化工序,再次进行氧化。
(2)“吸收”时通入空气的目的是使充分被水吸收,减少氮氧化物(有毒气体)的排放。
(3)①5min内,A物质的物质的量的变化量为0.2mol,B物质的物质的量的变化量为0.4mol,所以A和B在该反应中的化学计量数之比为,因此A为,B为;②在5min内的平均反应速率为;③5min末时,达到平衡,的物质的量变化量为0.2mol,则的物质的量变化量为,可知的平衡转化率为;④c点处,已达到该条件下该反应的限度,为化学平衡状态,正、逆反应速率相等,故即为化学平衡状态,若保持其他条件不变,更换高效催化剂,反应速率加快,达到平衡所用时间变短,c点对应横轴的坐标小于5。
18.【答案】(1)(2分) (2分)
(2)加成反应(2分)
(3)羟基、羧基(2分,写对1个得1分)
(4)(2分,反应物或生成物写错、未配平不得分,漏写反应条件扣1分) 取代反应或酯化反应(2分)
(5)(2分)
【解析】(1)反应①为丙烯()和水发生加成反应生成,故的化学式为,丙烯与水发生加成反应还可能生成。
(2)对比反应物和产物可知反应③中碳氧双键断裂,与HCN发生加成反应。
(3)中官能团的名称为羟基和羧基。
(4)模仿乙酸和乙醇的反应写出反应⑥的化学方程式为,反应类型为取代反应或酯化反应。
(5)反应⑦为加成聚合反应,的结构简式为。
同课章节目录
