广东省汕头市2023-2024学年高一下学期期末教学质量检测化学试题(PDF版无答案)
文档属性
| 名称 | 广东省汕头市2023-2024学年高一下学期期末教学质量检测化学试题(PDF版无答案) |

|
|
| 格式 | |||
| 文件大小 | 672.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-05 00:00:00 | ||
图片预览


文档简介
试卷类型:A
汕头市 2023~2024学年度普通高中教学质量监测
高 一 化 学
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,合计 6页,全卷共 100分。考试时间 60分钟。
注意事项:
1.答题前,考生在答题卡上务必用 0.5毫米的黑色墨水签字笔将自己的姓名、准考证
号填写清楚。
2.第Ⅰ卷共 16 小题,均为单选题,共 64 分。选出答案后,用 2B铅笔把答题卡上对
应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号。在试题卷上
作答无效。
3.第Ⅱ卷共 3小题,合计 36 分。请用直径 0.5 毫米的黑色墨水签字笔在答题卡上各
题的答题区域内作答,在试题卷上作答无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 Fe-56
第 I 卷(选择题 64 分)
一、单项选择题:(本题共 16 小题, 每小题 4 分,共 64 分。每小题给出的四个选项
中,只有一项符合题意。)
1.中华民族文化历史悠久,下列博物馆馆藏文物中,主要是由合金材料制成的是
A.朱克柔缂丝图 B.琉璃内画 C.陶埙 D.三足鼎
2.化学用语构建了化学基础知识体系,下列化学用语不正确的是
A.Ca(OH) 的电离方程式:Ca(OH) 2 2 Ca 2OH
B. 32S 与 342 S4互为同位素
C.乙炔的电子式
D.氟离子(F-)的结构示意图:
3.衣食住行皆化学,下列有关说法错误的
A.民以食为天,均衡膳食助健康,主食中的淀粉可水解为葡萄糖
B.建筑用到的水泥属于新型硅酸盐材料
C.京剧表演者所穿的丝绸戏服,主要成分为蛋白质
D.汽车轮胎用到的橡胶属于高分子材料
4.下列离子组能大量共存且溶液为无色的是
A.Cu 2+、K 、SO 2-4 、NO
3 2
3 B. Fe 、Ba 、Cl
、NO 3
C.Mg2 、K 、CO 2 、Cl 3 D.Na
、Al(OH) 4 、OH 、Cl
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 1 页(共 6 页)
{#{QQABRTYoApgxwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
5.邮票记载了我国发展历程,形象地呈现了人类与化学相互依存的关系,下列与邮票相
关的叙述中没有发生化学变化的是
A.建筑上用生石 B.炼钢厂将生铁 C.液态水转化为水蒸 D.用侯氏制碱法
灰制熟石灰 炼成钢 气形成了云海 生产纯碱
6.辛勤劳动才能创造美好生活。下列劳动项目与所涉及的化学知识不相符的是
选项 劳动项目 化学知识
A 社区服务:更换球场高压钠灯 钠单质具有强还原性
B 家务劳动:柠檬煮水除去水壶中的水垢 柠檬酸可溶解碳酸钙等沉淀
趣味实验:用铝粉和氢氧化钠溶液疏通厨 铝粉与 NaOH溶液反应放热并
C
卫管道 产生H2
D 学农活动:用厨余垃圾制肥料 厨余垃圾含N、P等元素
7.下列说法错误的是
A.观察 KCl的焰色应透过蓝色钴玻璃
B.将次氯酸钠消毒剂与酒精消毒液混合使用效果更佳
C.食品中添加适量亚硝酸钠,可起到抗氧化、防腐作用
D.在周期表中金属元素与非金属元素的分界处可以找到制备半导体材料的元素,如
硅、锗、镓
8.下列离子方程式中,正确的是
A.Na与 CuSO4溶液反应: 2Na+ Cu2+ = Cu+ 2Na+
B.氧化亚铁与稀盐酸反应: Fe+2H+=Fe3++H2O
C.CuSO4溶液与 Ba(OH)2溶液反应:Cu2++ 2OH = Cu(OH) 2
D.NaHCO3溶液与 NaOH溶液混合:HCO 3 OH
H2O CO
2
3
9.已知:2KMnO4 5H2C2O4 3H2SO4 2MnSO4 K 2SO4 10CO2 8H2O。某化学
小组欲探究H2C2O4溶液和酸性KMnO4溶液反应过程中浓度、温度对化学反应速率的
影响,进行了如下实验(忽略混合时溶液体积变化):
编 0.01mol L 1酸性 0.1mol L 1H2C2O4 水的体 反应温 反应时间
号 KMnO4溶液体积/mL 溶液体积/mL 积/mL 度/℃ /min
Ⅰ 2 2 0 20 2.1
Ⅱ V1 2 1 20 5.5
Ⅲ 2 2 0 50 0.5
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 2 页(共 6 页)
{#{QQABTRYoApxgwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
下列说法不.正.确.的是
A.V1 1
B.实验计时是从溶液混合开始,溶液紫红色刚好褪去时结束
C.设计实验Ⅰ、Ⅲ的目的是探究温度对反应速率的影响
D.实验Ⅲ中用酸性KMnO4溶液的浓度变化表示的反应速率v(KMnO4) 0.02mol L
1 min 1
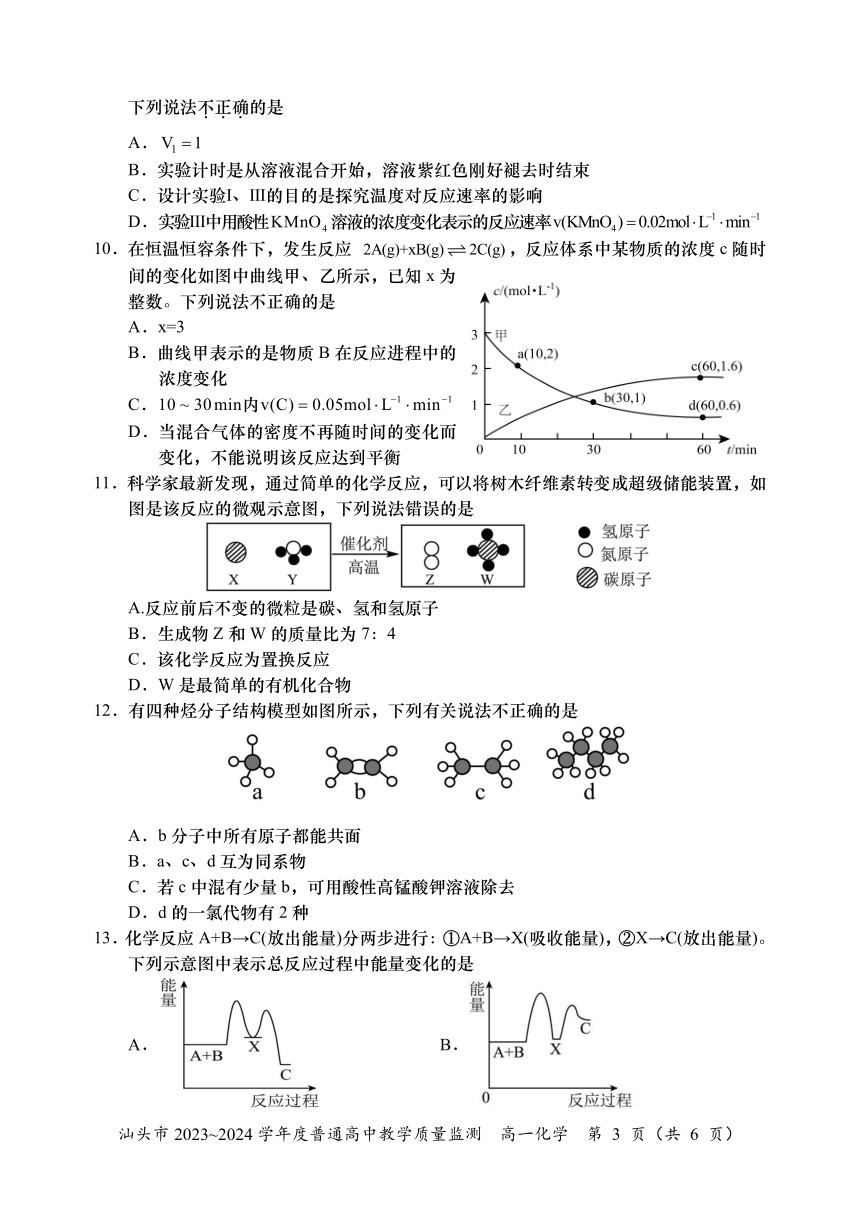
10.在恒温恒容条件下,发生反应 2A(g)+xB(g) 2C(g),反应体系中某物质的浓度 c随时
间的变化如图中曲线甲、乙所示,已知 x为
整数。下列说法不正确的是
A.x=3
B.曲线甲表示的是物质 B在反应进程中的
浓度变化
C.10 ~ 30min内v(C) 0.05mol L 1 min 1
D.当混合气体的密度不再随时间的变化而
变化,不能说明该反应达到平衡
11.科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如
图是该反应的微观示意图,下列说法错误的是
A.反应前后不变的微粒是碳、氢和氢原子
B.生成物 Z和W的质量比为 7:4
C.该化学反应为置换反应
D.W是最简单的有机化合物
12.有四种烃分子结构模型如图所示,下列有关说法不正确的是
A.b分子中所有原子都能共面
B.a、c、d互为同系物
C.若 c中混有少量 b,可用酸性高锰酸钾溶液除去
D.d的一氯代物有 2种
13.化学反应 A+B→C(放出能量)分两步进行:①A+B→X(吸收能量),②X→C(放出能量)。
下列示意图中表示总反应过程中能量变化的是
A. B.
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 3 页(共 6 页)
{#{QQABRTYoApgxwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
C. D.
14.NA代表阿伏伽德罗常数的值。下列说法正确的是
A.标准状态下,11.2LH2O分子中所含的 O原子数为 0.5NA
B.32gO3和O2的混合物中含有氧原子的数目为 2NA
C.1moL过氧化钠中阴离子数目为 2NA
D.0.5mol异丁烷分子中共价键的数目为13NA
15.下列实验操作、现象和得出的结论正确的是
实验操作 现象 结论
将固体样品加水溶解,滴入浓 NaOH溶液并 湿润的蓝色石
A 样品中含有NH
加热,试管口放一张湿润的蓝色石蕊试纸 蕊试纸变红 4
室温下,将铝片打磨后直接放入浓硫酸中,一 铝片表面未见紫 室温下铝和硫酸
B
段时间后取出并用水洗净,放入CuSO4溶液 红色固体生成 铜溶液不反应
将少量 Na2SO3样品溶于水,滴加过量稀硝酸C 有白色沉淀产生 说明Na2SO3已变质
后,再滴入BaCl2溶液
取 5mL0.1mol/LKI 溶液于试管中,加入
KI与 FeCl 的反应
D 1mL0.1mol/LFeCl3溶液,充分反应后滴入 5滴 溶液变血红色
3
有一定限度
10%KSCN溶液
16.流动电池是一种新型电池,其主要特点是可以通过电解质溶液的循环流动,在电池外部
调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。某种流动电池装置如图所
示,电池总反应为Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O。下列说法不正确的是
A.Cu为负极
B.该电池工作时 PbO2电极的电极反应式为:
PbO 4H SO 2 2e 2 4 =PbSO4 2H2O
C.电池工作一段时间后需要补充H2SO4
D.电子由 b极流出,经导线流向 a极
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 4 页(共 6 页)
{#{QQABTRYoApxgwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
第Ⅱ卷(非选择题 3小题,共 36分)
17.(12 分)
I.用下图装置可以制取氨气并探究其性质,按下列装置(部分夹持装置已略去)进行实验。
(1)图 1装置中生成NH3的化学方程式为 。
(2)用图 2探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。无水硫酸
铜的作用是 ;有同学认为需要在无水硫酸铜的后面再接一
个装有CaCl2固体的球形干燥管,这样做的目的是 。
(3)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是 (填字母)。
II.工业上制取硝酸铵的流程如图所示,请回答下列问题:
(4)设备 II中,每有 1molNO生成转移电子数目为 。
(5)设备 IV中的尾气主要为 NO。NH3催化还原氮氧化物(SCR技术是目前应用最
广泛的烟气氮氧化物脱除技术,反应原理下图所示:
SCR催化化反器中NH3还原 NO的程式为 。
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 5 页(共 6 页)
{#{QQABTRYoApgxwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
18.(12分)
高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多
种路线,其中主有甲、乙两种工艺流程示意图及主要反应如下:
(1)Si元素在元素周期表的位置是第 周期 族。
(2)SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程
式: 。
(3)关于硅及其相关化合物的叙述正确的是 。
A.自然界中不存在天然游离的硅单质
B.已知 C与 Si的最高正价都是正四价,由于CO2+H2O=H2CO3,用类比法得知
SiO2+H2O=H2SiO3
C.SiO2既能和 NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
D.硅元素在金属与非金属的分界线处,因此具有弱导电性,一般可用于作为半
导体材料
(4)流程乙中循环使用的物质除 Si、SiHCl3外,还有 。对比流程乙,
流程甲的缺点有 。(写出一条即可)
19.(12分)
化合物 G(丙酸异丙酯)可用作食品香料。现可通过下列转化制(部分反应条件略去):
(1)化合物 B中官能团的名称是 ,写出一定条件下 A→E的化学方程式
为 。
(2)化合物 C的结构简式 。
(3)E→F的反应类型为 。
(4)化合物 A在一定条件下可生成高分子聚丙烯,该反应的化学方程式
是 。
(5)下列关于化合物 B、D的说法不正确的是 。
a.均能和 NaOH反应 b.均溶于水
c.均能和O2在一定条件发生氧化反应 d.均能和NaHCO3反应放出CO2
(6)写出 D+F→G的化学方程式 。
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 6 页(共 6 页)
{#{QQABRTYoApgxwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
汕头市 2023~2024学年度普通高中教学质量监测
高 一 化 学
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,合计 6页,全卷共 100分。考试时间 60分钟。
注意事项:
1.答题前,考生在答题卡上务必用 0.5毫米的黑色墨水签字笔将自己的姓名、准考证
号填写清楚。
2.第Ⅰ卷共 16 小题,均为单选题,共 64 分。选出答案后,用 2B铅笔把答题卡上对
应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号。在试题卷上
作答无效。
3.第Ⅱ卷共 3小题,合计 36 分。请用直径 0.5 毫米的黑色墨水签字笔在答题卡上各
题的答题区域内作答,在试题卷上作答无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 Fe-56
第 I 卷(选择题 64 分)
一、单项选择题:(本题共 16 小题, 每小题 4 分,共 64 分。每小题给出的四个选项
中,只有一项符合题意。)
1.中华民族文化历史悠久,下列博物馆馆藏文物中,主要是由合金材料制成的是
A.朱克柔缂丝图 B.琉璃内画 C.陶埙 D.三足鼎
2.化学用语构建了化学基础知识体系,下列化学用语不正确的是
A.Ca(OH) 的电离方程式:Ca(OH) 2 2 Ca 2OH
B. 32S 与 342 S4互为同位素
C.乙炔的电子式
D.氟离子(F-)的结构示意图:
3.衣食住行皆化学,下列有关说法错误的
A.民以食为天,均衡膳食助健康,主食中的淀粉可水解为葡萄糖
B.建筑用到的水泥属于新型硅酸盐材料
C.京剧表演者所穿的丝绸戏服,主要成分为蛋白质
D.汽车轮胎用到的橡胶属于高分子材料
4.下列离子组能大量共存且溶液为无色的是
A.Cu 2+、K 、SO 2-4 、NO
3 2
3 B. Fe 、Ba 、Cl
、NO 3
C.Mg2 、K 、CO 2 、Cl 3 D.Na
、Al(OH) 4 、OH 、Cl
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 1 页(共 6 页)
{#{QQABRTYoApgxwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
5.邮票记载了我国发展历程,形象地呈现了人类与化学相互依存的关系,下列与邮票相
关的叙述中没有发生化学变化的是
A.建筑上用生石 B.炼钢厂将生铁 C.液态水转化为水蒸 D.用侯氏制碱法
灰制熟石灰 炼成钢 气形成了云海 生产纯碱
6.辛勤劳动才能创造美好生活。下列劳动项目与所涉及的化学知识不相符的是
选项 劳动项目 化学知识
A 社区服务:更换球场高压钠灯 钠单质具有强还原性
B 家务劳动:柠檬煮水除去水壶中的水垢 柠檬酸可溶解碳酸钙等沉淀
趣味实验:用铝粉和氢氧化钠溶液疏通厨 铝粉与 NaOH溶液反应放热并
C
卫管道 产生H2
D 学农活动:用厨余垃圾制肥料 厨余垃圾含N、P等元素
7.下列说法错误的是
A.观察 KCl的焰色应透过蓝色钴玻璃
B.将次氯酸钠消毒剂与酒精消毒液混合使用效果更佳
C.食品中添加适量亚硝酸钠,可起到抗氧化、防腐作用
D.在周期表中金属元素与非金属元素的分界处可以找到制备半导体材料的元素,如
硅、锗、镓
8.下列离子方程式中,正确的是
A.Na与 CuSO4溶液反应: 2Na+ Cu2+ = Cu+ 2Na+
B.氧化亚铁与稀盐酸反应: Fe+2H+=Fe3++H2O
C.CuSO4溶液与 Ba(OH)2溶液反应:Cu2++ 2OH = Cu(OH) 2
D.NaHCO3溶液与 NaOH溶液混合:HCO 3 OH
H2O CO
2
3
9.已知:2KMnO4 5H2C2O4 3H2SO4 2MnSO4 K 2SO4 10CO2 8H2O。某化学
小组欲探究H2C2O4溶液和酸性KMnO4溶液反应过程中浓度、温度对化学反应速率的
影响,进行了如下实验(忽略混合时溶液体积变化):
编 0.01mol L 1酸性 0.1mol L 1H2C2O4 水的体 反应温 反应时间
号 KMnO4溶液体积/mL 溶液体积/mL 积/mL 度/℃ /min
Ⅰ 2 2 0 20 2.1
Ⅱ V1 2 1 20 5.5
Ⅲ 2 2 0 50 0.5
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 2 页(共 6 页)
{#{QQABTRYoApxgwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
下列说法不.正.确.的是
A.V1 1
B.实验计时是从溶液混合开始,溶液紫红色刚好褪去时结束
C.设计实验Ⅰ、Ⅲ的目的是探究温度对反应速率的影响
D.实验Ⅲ中用酸性KMnO4溶液的浓度变化表示的反应速率v(KMnO4) 0.02mol L
1 min 1
10.在恒温恒容条件下,发生反应 2A(g)+xB(g) 2C(g),反应体系中某物质的浓度 c随时
间的变化如图中曲线甲、乙所示,已知 x为
整数。下列说法不正确的是
A.x=3
B.曲线甲表示的是物质 B在反应进程中的
浓度变化
C.10 ~ 30min内v(C) 0.05mol L 1 min 1
D.当混合气体的密度不再随时间的变化而
变化,不能说明该反应达到平衡
11.科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如
图是该反应的微观示意图,下列说法错误的是
A.反应前后不变的微粒是碳、氢和氢原子
B.生成物 Z和W的质量比为 7:4
C.该化学反应为置换反应
D.W是最简单的有机化合物
12.有四种烃分子结构模型如图所示,下列有关说法不正确的是
A.b分子中所有原子都能共面
B.a、c、d互为同系物
C.若 c中混有少量 b,可用酸性高锰酸钾溶液除去
D.d的一氯代物有 2种
13.化学反应 A+B→C(放出能量)分两步进行:①A+B→X(吸收能量),②X→C(放出能量)。
下列示意图中表示总反应过程中能量变化的是
A. B.
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 3 页(共 6 页)
{#{QQABRTYoApgxwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
C. D.
14.NA代表阿伏伽德罗常数的值。下列说法正确的是
A.标准状态下,11.2LH2O分子中所含的 O原子数为 0.5NA
B.32gO3和O2的混合物中含有氧原子的数目为 2NA
C.1moL过氧化钠中阴离子数目为 2NA
D.0.5mol异丁烷分子中共价键的数目为13NA
15.下列实验操作、现象和得出的结论正确的是
实验操作 现象 结论
将固体样品加水溶解,滴入浓 NaOH溶液并 湿润的蓝色石
A 样品中含有NH
加热,试管口放一张湿润的蓝色石蕊试纸 蕊试纸变红 4
室温下,将铝片打磨后直接放入浓硫酸中,一 铝片表面未见紫 室温下铝和硫酸
B
段时间后取出并用水洗净,放入CuSO4溶液 红色固体生成 铜溶液不反应
将少量 Na2SO3样品溶于水,滴加过量稀硝酸C 有白色沉淀产生 说明Na2SO3已变质
后,再滴入BaCl2溶液
取 5mL0.1mol/LKI 溶液于试管中,加入
KI与 FeCl 的反应
D 1mL0.1mol/LFeCl3溶液,充分反应后滴入 5滴 溶液变血红色
3
有一定限度
10%KSCN溶液
16.流动电池是一种新型电池,其主要特点是可以通过电解质溶液的循环流动,在电池外部
调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。某种流动电池装置如图所
示,电池总反应为Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O。下列说法不正确的是
A.Cu为负极
B.该电池工作时 PbO2电极的电极反应式为:
PbO 4H SO 2 2e 2 4 =PbSO4 2H2O
C.电池工作一段时间后需要补充H2SO4
D.电子由 b极流出,经导线流向 a极
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 4 页(共 6 页)
{#{QQABTRYoApxgwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
第Ⅱ卷(非选择题 3小题,共 36分)
17.(12 分)
I.用下图装置可以制取氨气并探究其性质,按下列装置(部分夹持装置已略去)进行实验。
(1)图 1装置中生成NH3的化学方程式为 。
(2)用图 2探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。无水硫酸
铜的作用是 ;有同学认为需要在无水硫酸铜的后面再接一
个装有CaCl2固体的球形干燥管,这样做的目的是 。
(3)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是 (填字母)。
II.工业上制取硝酸铵的流程如图所示,请回答下列问题:
(4)设备 II中,每有 1molNO生成转移电子数目为 。
(5)设备 IV中的尾气主要为 NO。NH3催化还原氮氧化物(SCR技术是目前应用最
广泛的烟气氮氧化物脱除技术,反应原理下图所示:
SCR催化化反器中NH3还原 NO的程式为 。
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 5 页(共 6 页)
{#{QQABTRYoApgxwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
18.(12分)
高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多
种路线,其中主有甲、乙两种工艺流程示意图及主要反应如下:
(1)Si元素在元素周期表的位置是第 周期 族。
(2)SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程
式: 。
(3)关于硅及其相关化合物的叙述正确的是 。
A.自然界中不存在天然游离的硅单质
B.已知 C与 Si的最高正价都是正四价,由于CO2+H2O=H2CO3,用类比法得知
SiO2+H2O=H2SiO3
C.SiO2既能和 NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
D.硅元素在金属与非金属的分界线处,因此具有弱导电性,一般可用于作为半
导体材料
(4)流程乙中循环使用的物质除 Si、SiHCl3外,还有 。对比流程乙,
流程甲的缺点有 。(写出一条即可)
19.(12分)
化合物 G(丙酸异丙酯)可用作食品香料。现可通过下列转化制(部分反应条件略去):
(1)化合物 B中官能团的名称是 ,写出一定条件下 A→E的化学方程式
为 。
(2)化合物 C的结构简式 。
(3)E→F的反应类型为 。
(4)化合物 A在一定条件下可生成高分子聚丙烯,该反应的化学方程式
是 。
(5)下列关于化合物 B、D的说法不正确的是 。
a.均能和 NaOH反应 b.均溶于水
c.均能和O2在一定条件发生氧化反应 d.均能和NaHCO3反应放出CO2
(6)写出 D+F→G的化学方程式 。
汕头市 2023~2024学年度普通高中教学质量监测 高一化学 第 6 页(共 6 页)
{#{QQABRTYoApgxwgiioYAgJIYAACAYh5C7QQQQWX6CACqQkJAGCQAJCcQggOOxVACFAIqMAoxAqwAJAFAIFAIFAA=B}#A}A=}#}
同课章节目录
