河南省驻马店市新蔡县第一高级中学2023-2024学年高二下学期7月月考化学试题(含答案)
文档属性
| 名称 | 河南省驻马店市新蔡县第一高级中学2023-2024学年高二下学期7月月考化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 808.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-05 00:00:00 | ||
图片预览



文档简介
新蔡县第一高级中学2023-2024学年高二下学期7月月考化学试题
可能用到的相对原子质量:H—1 C—12 N—14 O—16
一、选择题:本题共14小题,每小题3分,共42分)
1.下列说法正确的是
A. ,则完全破坏等质量的和中的化学键,需要的能量大
B.已知C(石墨,s)=C(金刚石,s),则金刚石比石墨稳定
C.在一定条件下,将和置于密闭容器中充分反应生成,放出热量79.2kJ,则该反应的热化学方程式
D.已知 ,中和热测定实验中将稀盐酸换成稀醋酸,生成1mol水时放出的热量小于57.3kJ
2.一定条件下,与反应合成的反应历程如图所示。已知其他条件不变时,反应物中的元素被质量数更大的同位素替换时,反应速率会变慢。说明:过渡态中“- -”表示化学键未完全断裂或形成。下列说法正确的是
A.反应历程中的两个反应均涉及氢原子的成键
B.相同条件下,与发生上述反应,则其过渡态的能量比高
C.该反应的
D.与发生上述反应,只能获得1种相对分子质量的有机产物
3.氢硫酸是一种弱酸(常温下,的、)。常温下用溶液吸收得X溶液。下列说法正确的是
A.X溶液中一定存在:
B.若X溶液中,则
C.当X溶液的时,溶液中存在:
D.能与发生反应:
4.为实现“碳中和”目标,实现循环利用,现利用双极膜电解含有的溶液,使转化成碳燃料,实现了的还原流动。电解池如图所示,双极膜中水电离的和在电场作用下可以向两极迁移。下列说法不正确的是
A.银网电极与电源负极相连
B.工作一段时间后,阳极区溶液pH不变
C.阴极电极反应为:
D.双极膜中有0.1mol 电离,则阳极附近理论上产生0.025mol
5.下列关于物质结构与性质的说法错误的是
A.空间结构为平面四边形
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.熔点:
D.沸点:,主要与是极性分子有关
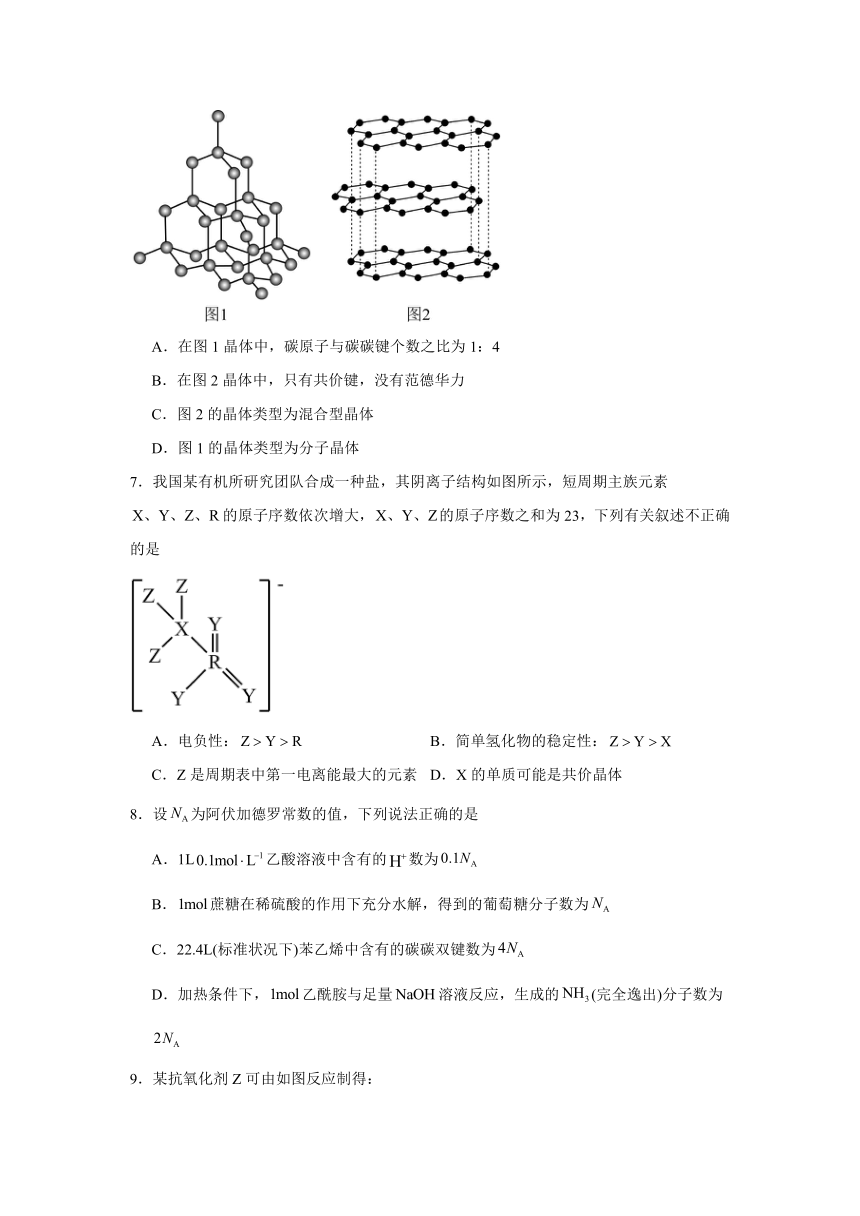
6.金刚石、石墨两种晶体的结构模型如图所示,下列说法正确的是
A.在图1晶体中,碳原子与碳碳键个数之比为1:4
B.在图2晶体中,只有共价键,没有范德华力
C.图2的晶体类型为混合型晶体
D.图1的晶体类型为分子晶体
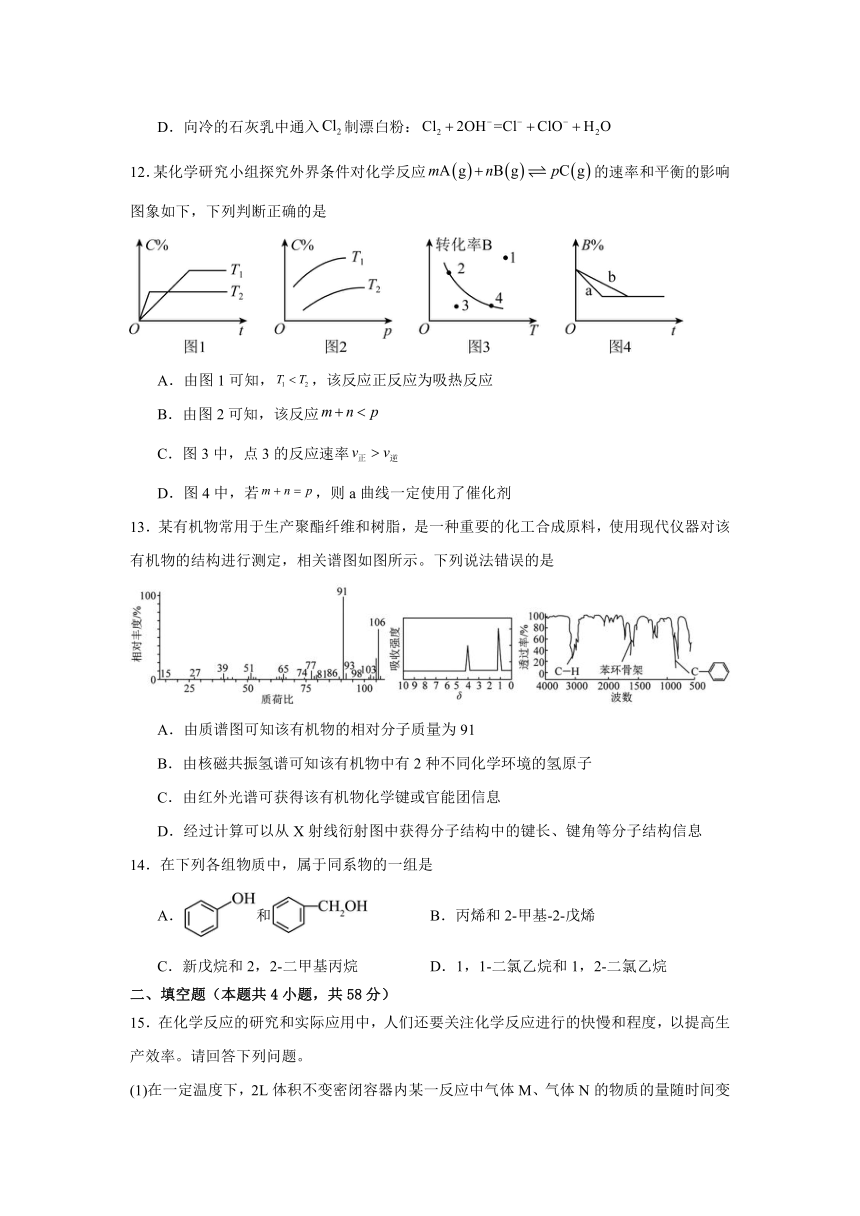
7.我国某有机所研究团队合成一种盐,其阴离子结构如图所示,短周期主族元素的原子序数依次增大,的原子序数之和为23,下列有关叙述不正确的是
A.电负性: B.简单氢化物的稳定性:
C.Z是周期表中第一电离能最大的元素 D.X的单质可能是共价晶体
8.设为阿伏加德罗常数的值,下列说法正确的是
A.1L乙酸溶液中含有的数为
B.蔗糖在稀硫酸的作用下充分水解,得到的葡萄糖分子数为
C.22.4L(标准状况下)苯乙烯中含有的碳碳双键数为
D.加热条件下,乙酰胺与足量溶液反应,生成的(完全逸出)分子数为
9.某抗氧化剂Z可由如图反应制得:
下列关于X、Y、Z的说法错误的是
A.Y中元素的电负性:O>C>H
B.X和Y均含有1个手性碳原子
C.X可以发生加聚反应,也可以发生缩聚反应
D.一定条件下,1mol Z与足量水溶液反应,最多消耗3mol
10.利用热再生氨电池可实现电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加入相同的电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室电极为正极
B.隔膜为阳离子交换膜
C.电池总反应为
D.扩散到乙室对电池电动势不产生影响
11.下列生产活动中对应的离子方程式书写正确的是
A.用溶液除去锅炉水垢中的:
B.用从酸化的海带灰浸出液中制取碘:
C.胶体的制备:
D.向冷的石灰乳中通入制漂白粉:
12.某化学研究小组探究外界条件对化学反应的速率和平衡的影响图象如下,下列判断正确的是
A.由图1可知,,该反应正反应为吸热反应
B.由图2可知,该反应
C.图3中,点3的反应速率
D.图4中,若,则a曲线一定使用了催化剂
13.某有机物常用于生产聚酯纤维和树脂,是一种重要的化工合成原料,使用现代仪器对该有机物的结构进行测定,相关谱图如图所示。下列说法错误的是
A.由质谱图可知该有机物的相对分子质量为91
B.由核磁共振氢谱可知该有机物中有2种不同化学环境的氢原子
C.由红外光谱可获得该有机物化学键或官能团信息
D.经过计算可以从X射线衍射图中获得分子结构中的键长、键角等分子结构信息
14.在下列各组物质中,属于同系物的一组是
A.和 B.丙烯和2-甲基-2-戊烯
C.新戊烷和2,2-二甲基丙烷 D.1,1-二氯乙烷和1,2-二氯乙烷
二、填空题(本题共4小题,共58分)
15.在化学反应的研究和实际应用中,人们还要关注化学反应进行的快慢和程度,以提高生产效率。请回答下列问题。
(1)在一定温度下,2L体积不变密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
①时刻,正、逆反应速率大小 (填“>”“=”或“<”)。
②若,计算反应开始至时刻用的浓度变化表示的平均反应速率为 。
③如果升高温度,则 (填“增大”“减小”或“不变”)。
(2)在密闭容器内,800℃时仅发生反应,体系中开始仅含有和随时间的变化如下表所示:
时间 0 1 2 3 4 5
0.020 0.010 0.007 0.006 0.006 0.006
①时,生成的物质的量为 ,在第时,的转化率为 。
②已知图中曲线分别代表浓度变化曲线,则无关曲线为 (填字母)。
③下列能说明该反应已达到平衡状态的是 (填字母)。
a.容器内压强不再变化 b.混合气体颜色不再改变
c.混合气体的平均相对分子质量不变 d.容器内密度保持不变
16.平衡思想是化学研究的一个重要观念,在电解质溶液中存在电离平衡、水解平衡、溶解平衡等多种平衡。
I.25℃时,三种弱酸的电离平衡常数如下:
弱酸 CH3COOH H2CO3 HClO
电离平衡常数 1.8×10-5 Ka1=4.2×10-7,Ka2=4.8×10-11 3.0×10-8
回答下列问题:
(1)碳酸二级电离平衡常数的表达式为Ka2= 。
(2)下列四种离子结合质子能力由大到小的顺序是 。
A.CO B.ClO- C.CH3COO- D.HCO
(3)下列反应不能发生的是___________。
A.CO+2CH3COOH=2CH3COO-+CO2↑+H2O
B.ClO-+CH3COOH=CH3COO-+HClO
C.CO+2HClO=CO2↑+H2O+2ClO-
D.2ClO-+CO2+H2O=CO+2HClO
Ⅱ.体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如下图所示。
(4)25 ℃时,pH为2的醋酸溶液中由水电离出的c(H+)= mol·L-1。
(5)用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________HX。
A.大于 B.等于 C.小于 D.无法比较
17.铜的配合物在自然界中广泛存在,请回答下列问题:
(1)硫酸铜溶液中存在多种微粒,硫酸铜溶液呈蓝色的原因是其中存在配离子 (填化学式),配体中提供孤电子对的原子是 (填元素符号)。
(2)同学甲设计如下制备铜的配合物的实验:
已知:铜离子的配位数通常为4。
①结合化学用语,用平衡移动原理解释试管c中浑浊液转变为深蓝色溶液的原因 。
②由上述实验可得出以下结论:
结论1:配合物的形成与 、 有关;
结论2:结合实验,试管b、c中深蓝色配离子的稳定性强弱顺序为: > (填化学式)。
③实验结束后,向c试管中加入乙醇,并用玻璃棒摩擦试管壁,析出深蓝色晶体[Cu(NH3)4]SO4·H2O,解释析出晶体的原因: 。
18.Ⅰ.经研究发现白蚁信息素有:A.;B.;家蚕的信息素C为:CH3(CH2)2CH=CH-CH=CH(CH2)8CH2.
(1)下列说法正确的是 (填字母)。
a.信息素A、B互为同系物 b.以上三种信息素均能发生加聚反应
c.信息素A、B互为同分异构体 d.家蚕信息素C中所有碳原子共直线
(2)白蚁信息素B与氢气加成产物的系统命名为 。
(3)写出信息素B与溴水反应的化学方程式 。
(4)烯烃D是信息素A的一种同分异构体,D与足量氢气加成得到烷烃E,E的一氯代物只有2种,则E的结构简式为 。
Ⅱ.A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如图所示:
(5)既能使FeCl3溶液显紫色又能和NaHCO3反应放出气体的是 (填字母)。
(6)1molB与足量溴水反应,最多消耗 mol溴。
(7)D的一种同分异构体F的结构简式为 ,写出F与足量NaOH溶液共热的化学反应方程式 。
参考答案:
D2.B3.B4.B5.D6.C7.C8.B9.B10.C
11.A 12.C 13.A 14.B
15.(1) > 0.01 增大
(2) 0.013 70% a abc
16.(1) (2)ABDC
(3)CD (4) (5)A
17.(1) [Cu(H2O)4]2+ O
(2) Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O 配体的种类 配体的浓度 [Cu(NH3)4]2+ [Cu(OH)4]2- [Cu(NH3)4]SO4·H2O在乙醇中的溶解度小于在水中的溶解度而结晶析出,因此会析出深蓝色晶体
18.(1)ab
(2)2,6-二甲基辛烷
(3)+
(4)
(5)D
(6)4
(7)+3NaOH+CH3COONa+2H2O
可能用到的相对原子质量:H—1 C—12 N—14 O—16
一、选择题:本题共14小题,每小题3分,共42分)
1.下列说法正确的是
A. ,则完全破坏等质量的和中的化学键,需要的能量大
B.已知C(石墨,s)=C(金刚石,s),则金刚石比石墨稳定
C.在一定条件下,将和置于密闭容器中充分反应生成,放出热量79.2kJ,则该反应的热化学方程式
D.已知 ,中和热测定实验中将稀盐酸换成稀醋酸,生成1mol水时放出的热量小于57.3kJ
2.一定条件下,与反应合成的反应历程如图所示。已知其他条件不变时,反应物中的元素被质量数更大的同位素替换时,反应速率会变慢。说明:过渡态中“- -”表示化学键未完全断裂或形成。下列说法正确的是
A.反应历程中的两个反应均涉及氢原子的成键
B.相同条件下,与发生上述反应,则其过渡态的能量比高
C.该反应的
D.与发生上述反应,只能获得1种相对分子质量的有机产物
3.氢硫酸是一种弱酸(常温下,的、)。常温下用溶液吸收得X溶液。下列说法正确的是
A.X溶液中一定存在:
B.若X溶液中,则
C.当X溶液的时,溶液中存在:
D.能与发生反应:
4.为实现“碳中和”目标,实现循环利用,现利用双极膜电解含有的溶液,使转化成碳燃料,实现了的还原流动。电解池如图所示,双极膜中水电离的和在电场作用下可以向两极迁移。下列说法不正确的是
A.银网电极与电源负极相连
B.工作一段时间后,阳极区溶液pH不变
C.阴极电极反应为:
D.双极膜中有0.1mol 电离,则阳极附近理论上产生0.025mol
5.下列关于物质结构与性质的说法错误的是
A.空间结构为平面四边形
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.熔点:
D.沸点:,主要与是极性分子有关
6.金刚石、石墨两种晶体的结构模型如图所示,下列说法正确的是
A.在图1晶体中,碳原子与碳碳键个数之比为1:4
B.在图2晶体中,只有共价键,没有范德华力
C.图2的晶体类型为混合型晶体
D.图1的晶体类型为分子晶体
7.我国某有机所研究团队合成一种盐,其阴离子结构如图所示,短周期主族元素的原子序数依次增大,的原子序数之和为23,下列有关叙述不正确的是
A.电负性: B.简单氢化物的稳定性:
C.Z是周期表中第一电离能最大的元素 D.X的单质可能是共价晶体
8.设为阿伏加德罗常数的值,下列说法正确的是
A.1L乙酸溶液中含有的数为
B.蔗糖在稀硫酸的作用下充分水解,得到的葡萄糖分子数为
C.22.4L(标准状况下)苯乙烯中含有的碳碳双键数为
D.加热条件下,乙酰胺与足量溶液反应,生成的(完全逸出)分子数为
9.某抗氧化剂Z可由如图反应制得:
下列关于X、Y、Z的说法错误的是
A.Y中元素的电负性:O>C>H
B.X和Y均含有1个手性碳原子
C.X可以发生加聚反应,也可以发生缩聚反应
D.一定条件下,1mol Z与足量水溶液反应,最多消耗3mol
10.利用热再生氨电池可实现电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加入相同的电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室电极为正极
B.隔膜为阳离子交换膜
C.电池总反应为
D.扩散到乙室对电池电动势不产生影响
11.下列生产活动中对应的离子方程式书写正确的是
A.用溶液除去锅炉水垢中的:
B.用从酸化的海带灰浸出液中制取碘:
C.胶体的制备:
D.向冷的石灰乳中通入制漂白粉:
12.某化学研究小组探究外界条件对化学反应的速率和平衡的影响图象如下,下列判断正确的是
A.由图1可知,,该反应正反应为吸热反应
B.由图2可知,该反应
C.图3中,点3的反应速率
D.图4中,若,则a曲线一定使用了催化剂
13.某有机物常用于生产聚酯纤维和树脂,是一种重要的化工合成原料,使用现代仪器对该有机物的结构进行测定,相关谱图如图所示。下列说法错误的是
A.由质谱图可知该有机物的相对分子质量为91
B.由核磁共振氢谱可知该有机物中有2种不同化学环境的氢原子
C.由红外光谱可获得该有机物化学键或官能团信息
D.经过计算可以从X射线衍射图中获得分子结构中的键长、键角等分子结构信息
14.在下列各组物质中,属于同系物的一组是
A.和 B.丙烯和2-甲基-2-戊烯
C.新戊烷和2,2-二甲基丙烷 D.1,1-二氯乙烷和1,2-二氯乙烷
二、填空题(本题共4小题,共58分)
15.在化学反应的研究和实际应用中,人们还要关注化学反应进行的快慢和程度,以提高生产效率。请回答下列问题。
(1)在一定温度下,2L体积不变密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
①时刻,正、逆反应速率大小 (填“>”“=”或“<”)。
②若,计算反应开始至时刻用的浓度变化表示的平均反应速率为 。
③如果升高温度,则 (填“增大”“减小”或“不变”)。
(2)在密闭容器内,800℃时仅发生反应,体系中开始仅含有和随时间的变化如下表所示:
时间 0 1 2 3 4 5
0.020 0.010 0.007 0.006 0.006 0.006
①时,生成的物质的量为 ,在第时,的转化率为 。
②已知图中曲线分别代表浓度变化曲线,则无关曲线为 (填字母)。
③下列能说明该反应已达到平衡状态的是 (填字母)。
a.容器内压强不再变化 b.混合气体颜色不再改变
c.混合气体的平均相对分子质量不变 d.容器内密度保持不变
16.平衡思想是化学研究的一个重要观念,在电解质溶液中存在电离平衡、水解平衡、溶解平衡等多种平衡。
I.25℃时,三种弱酸的电离平衡常数如下:
弱酸 CH3COOH H2CO3 HClO
电离平衡常数 1.8×10-5 Ka1=4.2×10-7,Ka2=4.8×10-11 3.0×10-8
回答下列问题:
(1)碳酸二级电离平衡常数的表达式为Ka2= 。
(2)下列四种离子结合质子能力由大到小的顺序是 。
A.CO B.ClO- C.CH3COO- D.HCO
(3)下列反应不能发生的是___________。
A.CO+2CH3COOH=2CH3COO-+CO2↑+H2O
B.ClO-+CH3COOH=CH3COO-+HClO
C.CO+2HClO=CO2↑+H2O+2ClO-
D.2ClO-+CO2+H2O=CO+2HClO
Ⅱ.体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如下图所示。
(4)25 ℃时,pH为2的醋酸溶液中由水电离出的c(H+)= mol·L-1。
(5)用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________HX。
A.大于 B.等于 C.小于 D.无法比较
17.铜的配合物在自然界中广泛存在,请回答下列问题:
(1)硫酸铜溶液中存在多种微粒,硫酸铜溶液呈蓝色的原因是其中存在配离子 (填化学式),配体中提供孤电子对的原子是 (填元素符号)。
(2)同学甲设计如下制备铜的配合物的实验:
已知:铜离子的配位数通常为4。
①结合化学用语,用平衡移动原理解释试管c中浑浊液转变为深蓝色溶液的原因 。
②由上述实验可得出以下结论:
结论1:配合物的形成与 、 有关;
结论2:结合实验,试管b、c中深蓝色配离子的稳定性强弱顺序为: > (填化学式)。
③实验结束后,向c试管中加入乙醇,并用玻璃棒摩擦试管壁,析出深蓝色晶体[Cu(NH3)4]SO4·H2O,解释析出晶体的原因: 。
18.Ⅰ.经研究发现白蚁信息素有:A.;B.;家蚕的信息素C为:CH3(CH2)2CH=CH-CH=CH(CH2)8CH2.
(1)下列说法正确的是 (填字母)。
a.信息素A、B互为同系物 b.以上三种信息素均能发生加聚反应
c.信息素A、B互为同分异构体 d.家蚕信息素C中所有碳原子共直线
(2)白蚁信息素B与氢气加成产物的系统命名为 。
(3)写出信息素B与溴水反应的化学方程式 。
(4)烯烃D是信息素A的一种同分异构体,D与足量氢气加成得到烷烃E,E的一氯代物只有2种,则E的结构简式为 。
Ⅱ.A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如图所示:
(5)既能使FeCl3溶液显紫色又能和NaHCO3反应放出气体的是 (填字母)。
(6)1molB与足量溴水反应,最多消耗 mol溴。
(7)D的一种同分异构体F的结构简式为 ,写出F与足量NaOH溶液共热的化学反应方程式 。
参考答案:
D2.B3.B4.B5.D6.C7.C8.B9.B10.C
11.A 12.C 13.A 14.B
15.(1) > 0.01 增大
(2) 0.013 70% a abc
16.(1) (2)ABDC
(3)CD (4) (5)A
17.(1) [Cu(H2O)4]2+ O
(2) Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O 配体的种类 配体的浓度 [Cu(NH3)4]2+ [Cu(OH)4]2- [Cu(NH3)4]SO4·H2O在乙醇中的溶解度小于在水中的溶解度而结晶析出,因此会析出深蓝色晶体
18.(1)ab
(2)2,6-二甲基辛烷
(3)+
(4)
(5)D
(6)4
(7)+3NaOH+CH3COONa+2H2O
同课章节目录
