【弯道超车】浙教版科学新初三新课预习八(金属化学性质)
文档属性
| 名称 | 【弯道超车】浙教版科学新初三新课预习八(金属化学性质) |

|
|
| 格式 | doc | ||
| 文件大小 | 445.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-07-09 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
新初三科学新课预习八(金属化学性质)
一、单选题
1.某废液中含有硝酸银和硝酸铜,为回收利用和减少污染,往废液中加入一定量的铁粉,充分反应后,过滤得到滤渣和滤液,向滤渣中加入少量稀盐酸,产生气泡,则下列判断正确的是( )
A.滤渣中一定含有银,可能含有铜
B.滤渣中一定含有银和铜,可能含有铁
C.滤液中一定含有硝酸亚铁,一定没有硝酸银和硝酸铜
D.滤液中一定含有硝酸亚铁,可能含有硝酸银和硝酸铜
2.将一定量的金属M加入到ZnCl2和CuCl2的混合溶液中,充分反应后过滤,得固体滤渣,滤液为无色,向滤渣中滴加稀硫酸气泡产生,下列有关金属M、Zn、Cu的金属活动性判断一定正确的是( )
A.M>Zn B.Zn>M C.M>Cu D.Cu>M
3.锰(Mn)和镍(Ni)是两种不常见的金属,为了比较锰、镍和铁的金属活动性,小明在老师的指导下进行了实验,结果如下表:
加金属锰 加金属铁 加金属镍
硝酸锰溶液 ▲ 有金属析出 无金属出现
则三种金属的活动性顺序为( )
A.Fe>Ni>Mn B.Mn>Fe>Ni C.Ni>Mn>Fe D.Fe>Mn>Ni
4.现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法正确的是( )
A.甲、乙、丙依次可能是Mg、Zn、Fe
B.金属活动性:甲>乙>丙
C.相对原子质量:乙>丙>甲
D.消耗硫酸的质量:甲>乙>丙
5.有A、B两种金属放入等质量且等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B
B.相对原子质量AC.与金属A反应的硫酸一定是过量的
D.与金属B反应的硫酸一定是过量的
6.在FeCl2和CuCl2的混合溶液中加入Zn粉,下列说法错误的是( )
A.若反应完成后Zn无剩余,溶液中若有CuCl2,则一定有FeCl2
B.若反应完成后Zn无剩余,溶液中若无CuCl2,则可能有FeCl2
C.若反应完成后Zn有剩余,则溶液中有ZnCl2,无CuCl2和FeCl2
D.若反应完成后Zn有剩余,则溶液中有ZnCl2,无CuCl2,可能有FeCl2
7.为探究X、Y、Z三种金属的活动性顺序,某科学兴趣小组进行了下列实验:
①向试管中加少量稀盐酸,插入X,产生气泡,溶液由无色变为浅绿色;②在(1)所得溶液中插入Y,无明显现象;③在①所得溶液中插入Z,溶液由浅绿色变为无色。三种金属的活动性顺序正确的是( )
A.Z>X>Y B.X>Y>Z C.Z>Y>X D.X>Z>Y
8.为比较Fe、Cu、Ag之间的活动性强弱,某同学在实验室分别准备用如下几组物质进行实验,你认为不可行的是( )
A.Fe、Ag、CuSO4溶液 B.Cu、Ag、FeSO4溶液
C.Fe、Cu、稀盐酸、AgNO3溶液 D.Cu、FeSO4溶液、AgNO3溶液
9.某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入少量的稀盐酸,无气泡产生,则下列有关说法中正确的是( )
A.滤出的固体中一定含有银,滤液可能含有硝酸亚铁
B.滤出的固体中一定含有银和铜,一定不含有铁
C.滤液中一定含有硝酸亚铁,一定没有硝酸银
D.滤出的固体中一定含有银,滤液中一定含有硝酸亚铁
10.在一定量AgNO3和Cu(NO3)3的混合溶液中加入铁粉,充分反应后,下列各图描述相关变化的曲线中,一定不正确的是( )
A. B.
C. D.
二、填空题
11.2018年,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。
(1)金属和金属材料在生产生活中有广泛的用途。请回答下列问题:
我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了新的突破。飞机外壳的主要材料是铝合金,“铝合金”属于 (填“金属材料”或“合成材料”)。
(2)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的是____(填序号)。
A.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C.ZnCl2溶液中加入足量铜粉后,再加入铁粉
(3)根据上述实验结论,下列措施中能有效防止金属锈蚀的是
①金属表面涂抹油漆②改变金属的内部结构③用湿布擦拭,保持金属表面清洁④在金属表面进行电镀⑤使金属表面形成致密的氧化物薄膜
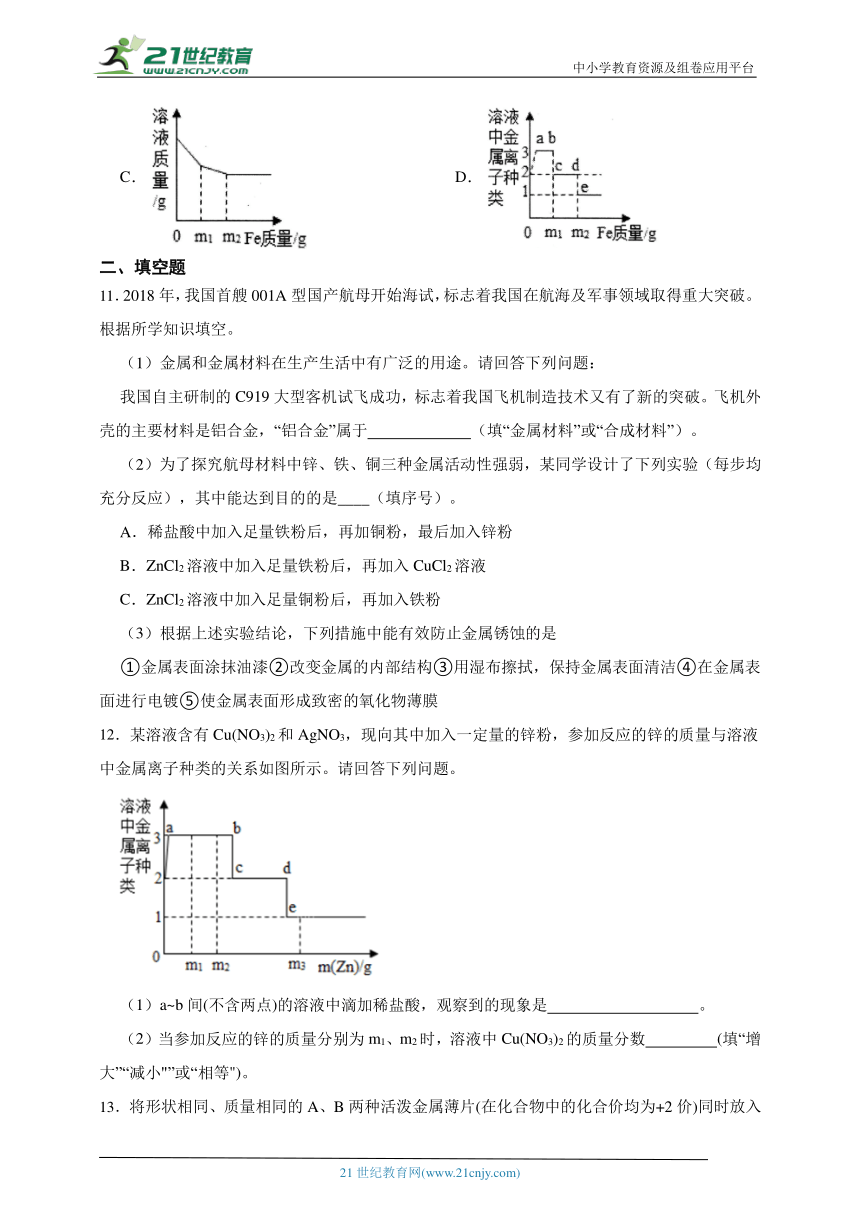
12.某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液中金属离子种类的关系如图所示。请回答下列问题。
(1)a~b间(不含两点)的溶液中滴加稀盐酸,观察到的现象是 。
(2)当参加反应的锌的质量分别为m1、m2时,溶液中Cu(NO3)2的质量分数 (填“增大”“减小"”或“相等")。
13.将形状相同、质量相同的A、B两种活泼金属薄片(在化合物中的化合价均为+2价)同时放入足量的盛放稀盐酸的烧杯中,产生H 的质量与反应时间的关系如图所示。
(1)A、B两种金属的活泼性比较强的是 ;(填“A”或“B”)
(2)A、B两种元素的相对原子质量比较大的是 ;(填“A”或“B”)
(3)如果A和B对应的金属有:①Mg和Fe②Zn和Fe③Zn和Cu,则A、B可能是 (填序号)。
14.有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42﹣、CO32﹣中的一种或几种,取此溶液做下列实验:
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。
试推断:
(1)溶液中一定含有的离子是 ;
(2)溶液中肯定不含有的离子是 ;
15.向一定质量的Mg(NO3)2和Cu(NO3)2混合溶液中加入a克锌粉和铁粉的混合物,充分反应后过滤,得到不饱和的滤液和滤渣,发现质量仍为a克。
(1)请写出其中一个化学反应方程式 。
(2)反应后的滤液中一定含有的溶质是 。
(3)往反应后的滤渣中加稀盐酸,无气泡产生,则滤渣中一定含有的物质是 。
16.从C、H、O、Fe中任意选取若干元素,组成下列物质(各写出一种物质的化学式)。
金属单质: ;非金属单质 ;金属氧化物: ;
非金属氧化物: ;有机物: ;酸: ;碱: 。
三、实验探究题
17.为探究锌、铁、铜、银的四种金属的活动性顺序,小科设计了如图所示的实验。
(1)运用控制变量法设计实验方案是科学研究的重要方法。在A、B、C三个实验中,需要控制的实验条件除了金属与稀硫酸的接触面积、稀硫酸的体积、温度以外还需要控制的条件是 。
(2)你认为从中选择四个实验即可验证锌、铁、铜、银的金属活动性顺序。这四个实验的组合是 。
18.图一、图二是某兴趣小组探究金属,酸的化学性质时所做的两组实验。实验结束后,将两组实验试管中的物质分别全部倒入甲、乙两个洁净的烧杯中,据图回答:
(1) 甲烧杯中的物质完全反应后,发现红色固体物质明显增多。下列说法正确的
是____。(多选)
A.试管②反应后的固体中一定不含铁
B.完全反应后,甲烧杯中的固体一定含有铁
C.完全反应后,甲烧杯的溶液中可能含有Cu2+
D.完全反应后,甲烧杯的溶液中一定含有Mg2+、Fe2+
(2)乙烧杯中的物质充分反应后,仅观察到有白色沉淀,无其他现象。则该白色沉淀
是 (写化学式)。
(3)将乙烧杯内的物质进行过滤,对所得滤液中溶质成分进行了如下探究:
实验操作 实验现象 实验结论
步骤1:取少量滤液于试管中,向其中滴加足量硝酸钡溶液 有白色沉淀生成 滤液中的溶质是
步骤2:静置,向上层清液中滴加无色酚酞溶液 溶液变红
四、解答题
19.现有一份质量为20g的金属混合物,已知该金属混合物由镁、铁和铜三种金属粉末混合而成。某课外兴趣小组为探究该金属混合物的组成,将250g稀硫酸分五次加到盛有该金属混合物的烧杯中,经测定得到如下数据:
次数 第1次 第2次 第3次 第4次 第5次
加入稀硫酸质量/g 50 50 50 50 50
剩余固体质量/g 17.6 15.2 11.2 a 2.8
(1)表格中a的值为 ;
(2)所用稀硫酸的溶质质量分数是 ;
(3)该金属混合物中铁的质量是多少?
20.小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供一瓶稀盐酸和相关的仪器。
(1)根据现有的条件,你认为能测出 中铜的质量分数。(填“Cu-Zn合金”、“Cu-Ag合金”或“两种合金”)
(2)为了测定该合金的组成,小华称取15克该合金粉末,在粉末中连续三次加入稀盐酸反应。每加一次盐酸,小华记录所得气体的质量,根据下表实验数据。(列式计算,结果精确到0.1%)
①求出加入稀盐酸的质量分数;②求出该合金中铜的质量分数。
第一次 第二次 第三次
连续加入盐酸的质量(g) 40 40 40
生成氢气的质量(g) 0.08 0.08 0.04
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】D
4.【答案】D
5.【答案】D
6.【答案】D
7.【答案】A
8.【答案】B
9.【答案】D
10.【答案】B
11.【答案】(1)金属材料
(2)A;B
(3)①②④⑤
12.【答案】(1)有白色沉淀产生
(2)增大
13.【答案】(1)A
(2)A
(3)②
14.【答案】(1)Mg2+、Al3+、SO42﹣
(2)Fe3+、Cu2+、H+、CO32﹣
15.【答案】(1)Zn+Cu(NO3)2=Zn(NO3)2+Cu或Fe+Cu(NO3)2=Fe(NO3)2+Cu
(2)硝酸镁、硝酸锌、硝酸亚铁
(3)铜
16.【答案】Fe;C;FeO;CO;CH4;H2CO3;Fe(OH)3
17.【答案】(1)稀硫酸的浓度
(2)ABCE 或 ABDE
18.【答案】(1)A;C;D
(2)BaCO3
(3)Na2CO3、NaOH、NaCl
19.【答案】(1)5.6
(2)19.6%
(3)设第3次反应中消耗的Mg的质量为x,消耗的Fe的质量为(4-x),
与Mg反应的硫酸溶质的质量为y1,与Fe反应的硫酸溶质的质量为y2。
Mg+H2SO4=MgSO4+H2↑ Fe+H2SO4=FeSO4+H2↑
24 98 56 98
x y1 (4-x) y2
y1=98x/24 y2=[98(4-x)]/56
98x/24+[98(4-x)]/56=9.8g
得x=1.2g
Mg的质量=2.4g+2.4g+1.2g=6g
Fe的质量=20g-6g-2.8g=11.2g
20.【答案】(1)Cu-Zn合金
(2)①解:设40g稀盐酸中HCl溶质质量为x.
Zn+2HCI=ZnCl2+H2↑
73 2
X 0.08g
x=2.92g
②解:设合金中锌的质量为y,生成氢气的总质量为:0.08g+0.08g+0.04g=0.2g
Zn+2HCl=ZnCl2+H2↑
65 2 mCu=15g-6.5g-8.5g
Y 0.2g
y=6.5g
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
新初三科学新课预习八(金属化学性质)
一、单选题
1.某废液中含有硝酸银和硝酸铜,为回收利用和减少污染,往废液中加入一定量的铁粉,充分反应后,过滤得到滤渣和滤液,向滤渣中加入少量稀盐酸,产生气泡,则下列判断正确的是( )
A.滤渣中一定含有银,可能含有铜
B.滤渣中一定含有银和铜,可能含有铁
C.滤液中一定含有硝酸亚铁,一定没有硝酸银和硝酸铜
D.滤液中一定含有硝酸亚铁,可能含有硝酸银和硝酸铜
2.将一定量的金属M加入到ZnCl2和CuCl2的混合溶液中,充分反应后过滤,得固体滤渣,滤液为无色,向滤渣中滴加稀硫酸气泡产生,下列有关金属M、Zn、Cu的金属活动性判断一定正确的是( )
A.M>Zn B.Zn>M C.M>Cu D.Cu>M
3.锰(Mn)和镍(Ni)是两种不常见的金属,为了比较锰、镍和铁的金属活动性,小明在老师的指导下进行了实验,结果如下表:
加金属锰 加金属铁 加金属镍
硝酸锰溶液 ▲ 有金属析出 无金属出现
则三种金属的活动性顺序为( )
A.Fe>Ni>Mn B.Mn>Fe>Ni C.Ni>Mn>Fe D.Fe>Mn>Ni
4.现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法正确的是( )
A.甲、乙、丙依次可能是Mg、Zn、Fe
B.金属活动性:甲>乙>丙
C.相对原子质量:乙>丙>甲
D.消耗硫酸的质量:甲>乙>丙
5.有A、B两种金属放入等质量且等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B
B.相对原子质量A
D.与金属B反应的硫酸一定是过量的
6.在FeCl2和CuCl2的混合溶液中加入Zn粉,下列说法错误的是( )
A.若反应完成后Zn无剩余,溶液中若有CuCl2,则一定有FeCl2
B.若反应完成后Zn无剩余,溶液中若无CuCl2,则可能有FeCl2
C.若反应完成后Zn有剩余,则溶液中有ZnCl2,无CuCl2和FeCl2
D.若反应完成后Zn有剩余,则溶液中有ZnCl2,无CuCl2,可能有FeCl2
7.为探究X、Y、Z三种金属的活动性顺序,某科学兴趣小组进行了下列实验:
①向试管中加少量稀盐酸,插入X,产生气泡,溶液由无色变为浅绿色;②在(1)所得溶液中插入Y,无明显现象;③在①所得溶液中插入Z,溶液由浅绿色变为无色。三种金属的活动性顺序正确的是( )
A.Z>X>Y B.X>Y>Z C.Z>Y>X D.X>Z>Y
8.为比较Fe、Cu、Ag之间的活动性强弱,某同学在实验室分别准备用如下几组物质进行实验,你认为不可行的是( )
A.Fe、Ag、CuSO4溶液 B.Cu、Ag、FeSO4溶液
C.Fe、Cu、稀盐酸、AgNO3溶液 D.Cu、FeSO4溶液、AgNO3溶液
9.某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入少量的稀盐酸,无气泡产生,则下列有关说法中正确的是( )
A.滤出的固体中一定含有银,滤液可能含有硝酸亚铁
B.滤出的固体中一定含有银和铜,一定不含有铁
C.滤液中一定含有硝酸亚铁,一定没有硝酸银
D.滤出的固体中一定含有银,滤液中一定含有硝酸亚铁
10.在一定量AgNO3和Cu(NO3)3的混合溶液中加入铁粉,充分反应后,下列各图描述相关变化的曲线中,一定不正确的是( )
A. B.
C. D.
二、填空题
11.2018年,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。
(1)金属和金属材料在生产生活中有广泛的用途。请回答下列问题:
我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了新的突破。飞机外壳的主要材料是铝合金,“铝合金”属于 (填“金属材料”或“合成材料”)。
(2)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的是____(填序号)。
A.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C.ZnCl2溶液中加入足量铜粉后,再加入铁粉
(3)根据上述实验结论,下列措施中能有效防止金属锈蚀的是
①金属表面涂抹油漆②改变金属的内部结构③用湿布擦拭,保持金属表面清洁④在金属表面进行电镀⑤使金属表面形成致密的氧化物薄膜
12.某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液中金属离子种类的关系如图所示。请回答下列问题。
(1)a~b间(不含两点)的溶液中滴加稀盐酸,观察到的现象是 。
(2)当参加反应的锌的质量分别为m1、m2时,溶液中Cu(NO3)2的质量分数 (填“增大”“减小"”或“相等")。
13.将形状相同、质量相同的A、B两种活泼金属薄片(在化合物中的化合价均为+2价)同时放入足量的盛放稀盐酸的烧杯中,产生H 的质量与反应时间的关系如图所示。
(1)A、B两种金属的活泼性比较强的是 ;(填“A”或“B”)
(2)A、B两种元素的相对原子质量比较大的是 ;(填“A”或“B”)
(3)如果A和B对应的金属有:①Mg和Fe②Zn和Fe③Zn和Cu,则A、B可能是 (填序号)。
14.有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42﹣、CO32﹣中的一种或几种,取此溶液做下列实验:
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。
试推断:
(1)溶液中一定含有的离子是 ;
(2)溶液中肯定不含有的离子是 ;
15.向一定质量的Mg(NO3)2和Cu(NO3)2混合溶液中加入a克锌粉和铁粉的混合物,充分反应后过滤,得到不饱和的滤液和滤渣,发现质量仍为a克。
(1)请写出其中一个化学反应方程式 。
(2)反应后的滤液中一定含有的溶质是 。
(3)往反应后的滤渣中加稀盐酸,无气泡产生,则滤渣中一定含有的物质是 。
16.从C、H、O、Fe中任意选取若干元素,组成下列物质(各写出一种物质的化学式)。
金属单质: ;非金属单质 ;金属氧化物: ;
非金属氧化物: ;有机物: ;酸: ;碱: 。
三、实验探究题
17.为探究锌、铁、铜、银的四种金属的活动性顺序,小科设计了如图所示的实验。
(1)运用控制变量法设计实验方案是科学研究的重要方法。在A、B、C三个实验中,需要控制的实验条件除了金属与稀硫酸的接触面积、稀硫酸的体积、温度以外还需要控制的条件是 。
(2)你认为从中选择四个实验即可验证锌、铁、铜、银的金属活动性顺序。这四个实验的组合是 。
18.图一、图二是某兴趣小组探究金属,酸的化学性质时所做的两组实验。实验结束后,将两组实验试管中的物质分别全部倒入甲、乙两个洁净的烧杯中,据图回答:
(1) 甲烧杯中的物质完全反应后,发现红色固体物质明显增多。下列说法正确的
是____。(多选)
A.试管②反应后的固体中一定不含铁
B.完全反应后,甲烧杯中的固体一定含有铁
C.完全反应后,甲烧杯的溶液中可能含有Cu2+
D.完全反应后,甲烧杯的溶液中一定含有Mg2+、Fe2+
(2)乙烧杯中的物质充分反应后,仅观察到有白色沉淀,无其他现象。则该白色沉淀
是 (写化学式)。
(3)将乙烧杯内的物质进行过滤,对所得滤液中溶质成分进行了如下探究:
实验操作 实验现象 实验结论
步骤1:取少量滤液于试管中,向其中滴加足量硝酸钡溶液 有白色沉淀生成 滤液中的溶质是
步骤2:静置,向上层清液中滴加无色酚酞溶液 溶液变红
四、解答题
19.现有一份质量为20g的金属混合物,已知该金属混合物由镁、铁和铜三种金属粉末混合而成。某课外兴趣小组为探究该金属混合物的组成,将250g稀硫酸分五次加到盛有该金属混合物的烧杯中,经测定得到如下数据:
次数 第1次 第2次 第3次 第4次 第5次
加入稀硫酸质量/g 50 50 50 50 50
剩余固体质量/g 17.6 15.2 11.2 a 2.8
(1)表格中a的值为 ;
(2)所用稀硫酸的溶质质量分数是 ;
(3)该金属混合物中铁的质量是多少?
20.小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供一瓶稀盐酸和相关的仪器。
(1)根据现有的条件,你认为能测出 中铜的质量分数。(填“Cu-Zn合金”、“Cu-Ag合金”或“两种合金”)
(2)为了测定该合金的组成,小华称取15克该合金粉末,在粉末中连续三次加入稀盐酸反应。每加一次盐酸,小华记录所得气体的质量,根据下表实验数据。(列式计算,结果精确到0.1%)
①求出加入稀盐酸的质量分数;②求出该合金中铜的质量分数。
第一次 第二次 第三次
连续加入盐酸的质量(g) 40 40 40
生成氢气的质量(g) 0.08 0.08 0.04
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】D
4.【答案】D
5.【答案】D
6.【答案】D
7.【答案】A
8.【答案】B
9.【答案】D
10.【答案】B
11.【答案】(1)金属材料
(2)A;B
(3)①②④⑤
12.【答案】(1)有白色沉淀产生
(2)增大
13.【答案】(1)A
(2)A
(3)②
14.【答案】(1)Mg2+、Al3+、SO42﹣
(2)Fe3+、Cu2+、H+、CO32﹣
15.【答案】(1)Zn+Cu(NO3)2=Zn(NO3)2+Cu或Fe+Cu(NO3)2=Fe(NO3)2+Cu
(2)硝酸镁、硝酸锌、硝酸亚铁
(3)铜
16.【答案】Fe;C;FeO;CO;CH4;H2CO3;Fe(OH)3
17.【答案】(1)稀硫酸的浓度
(2)ABCE 或 ABDE
18.【答案】(1)A;C;D
(2)BaCO3
(3)Na2CO3、NaOH、NaCl
19.【答案】(1)5.6
(2)19.6%
(3)设第3次反应中消耗的Mg的质量为x,消耗的Fe的质量为(4-x),
与Mg反应的硫酸溶质的质量为y1,与Fe反应的硫酸溶质的质量为y2。
Mg+H2SO4=MgSO4+H2↑ Fe+H2SO4=FeSO4+H2↑
24 98 56 98
x y1 (4-x) y2
y1=98x/24 y2=[98(4-x)]/56
98x/24+[98(4-x)]/56=9.8g
得x=1.2g
Mg的质量=2.4g+2.4g+1.2g=6g
Fe的质量=20g-6g-2.8g=11.2g
20.【答案】(1)Cu-Zn合金
(2)①解:设40g稀盐酸中HCl溶质质量为x.
Zn+2HCI=ZnCl2+H2↑
73 2
X 0.08g
x=2.92g
②解:设合金中锌的质量为y,生成氢气的总质量为:0.08g+0.08g+0.04g=0.2g
Zn+2HCl=ZnCl2+H2↑
65 2 mCu=15g-6.5g-8.5g
Y 0.2g
y=6.5g
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
